Лекция 9.pptx-1230972591.pptx
- Количество слайдов: 32
 Лекция № 9 Первое начало термодинамики. 1. 2. 3. 4. 5. Внутренняя энергия. Макроскопическая работа. Теплота. Первое начало. Теплоемкость идеального газа. Теорема Майера. 6. Закон о равномерном распределении энергии по степеням свободы. 7. Теплоемкости одноатомных и многоатомных газов. 8. Адиабатический процесс.
Лекция № 9 Первое начало термодинамики. 1. 2. 3. 4. 5. Внутренняя энергия. Макроскопическая работа. Теплота. Первое начало. Теплоемкость идеального газа. Теорема Майера. 6. Закон о равномерном распределении энергии по степеням свободы. 7. Теплоемкости одноатомных и многоатомных газов. 8. Адиабатический процесс.
 Внутренняя энергия . Важной характеристикой термодинамической системы является ее внутренняя энергия: энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов, ядер и т. д. ) + энергия взаимодействия этих частиц. Из этого определения следует, что к внутренней энергии не относятся кинетическая энергия движения системы как целого и потенциальная энергия системы во внешних полях.
Внутренняя энергия . Важной характеристикой термодинамической системы является ее внутренняя энергия: энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов, ядер и т. д. ) + энергия взаимодействия этих частиц. Из этого определения следует, что к внутренней энергии не относятся кинетическая энергия движения системы как целого и потенциальная энергия системы во внешних полях.
 Внутренняя энергия – функция состояния, т. е. в каждом состоянии система обладает вполне определенной внутренней энергией (она не зависит от того, как система пришла в данное состояние) и при переходе системы из одного состояния в другое изменение внутренней энергии определяется только разностью значений внутренней энергии этих состояний и не зависит от процесса (от пути перехода). И так, в каждом состоянии система обладает определенным значением внутренней энергии: , а ее изменение можно вычислить:
Внутренняя энергия – функция состояния, т. е. в каждом состоянии система обладает вполне определенной внутренней энергией (она не зависит от того, как система пришла в данное состояние) и при переходе системы из одного состояния в другое изменение внутренней энергии определяется только разностью значений внутренней энергии этих состояний и не зависит от процесса (от пути перехода). И так, в каждом состоянии система обладает определенным значением внутренней энергии: , а ее изменение можно вычислить:
 Малое изменение внутренней энергии математически записывается как полный дифференциал. Тогда в круговом процессе, когда система возвращается в первоначальное состояние, изменение внутренней энергии равно нулю: Внутренняя энергия определяется с точностью до определенной аддитивной постоянной: одно из состояний можно принять за нулевое (U = 0).
Малое изменение внутренней энергии математически записывается как полный дифференциал. Тогда в круговом процессе, когда система возвращается в первоначальное состояние, изменение внутренней энергии равно нулю: Внутренняя энергия определяется с точностью до определенной аддитивной постоянной: одно из состояний можно принять за нулевое (U = 0).
 Под внутренней энергией идеального газа подразумевают энергию теплового хаотического движения молекул, так как взаимодействие между молекулами не учитывается. Внутренняя энергия газа, содержащего N молекул: где - средняя кинетическая энергия молекулы, ; Для одноатомного газа - число молей. и Для газа с более сложными молекулами - число степеней ; свободы
Под внутренней энергией идеального газа подразумевают энергию теплового хаотического движения молекул, так как взаимодействие между молекулами не учитывается. Внутренняя энергия газа, содержащего N молекул: где - средняя кинетическая энергия молекулы, ; Для одноатомного газа - число молей. и Для газа с более сложными молекулами - число степеней ; свободы
 Макроскопическая работа А. Рассмотрим газ, находящийся под поршнем в цилиндрическом сосуде. Если газ, расширяясь, передвигает поршень на бесконечно малое расстояние , то он производит над ним элементарную работу где Таким образом, - площадь поршня, - изменение объема.
Макроскопическая работа А. Рассмотрим газ, находящийся под поршнем в цилиндрическом сосуде. Если газ, расширяясь, передвигает поршень на бесконечно малое расстояние , то он производит над ним элементарную работу где Таким образом, - площадь поршня, - изменение объема.
 Полную работу , совершаемую газом при изменении его объема от до находим интегрированием формулы для элементарной работы: Результат интегрирования определяется характером зависимости между давлением и объемом газа. Произведенную при том или ином процессе работу можно изобразить графически с помощью кривой в координатах.
Полную работу , совершаемую газом при изменении его объема от до находим интегрированием формулы для элементарной работы: Результат интегрирования определяется характером зависимости между давлением и объемом газа. Произведенную при том или ином процессе работу можно изобразить графически с помощью кривой в координатах.
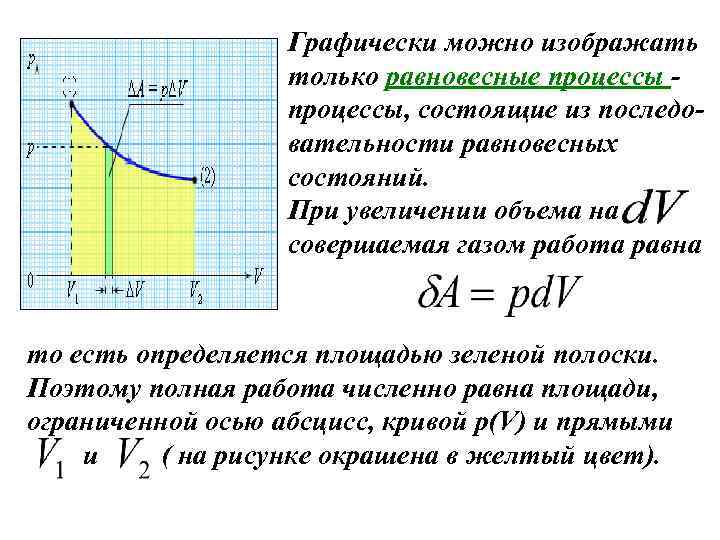 Графически можно изображать только равновесные процессы, состоящие из последовательности равновесных состояний. При увеличении объема на совершаемая газом работа равна то есть определяется площадью зеленой полоски. Поэтому полная работа численно равна площади, ограниченной осью абсцисс, кривой p(V) и прямыми и ( на рисунке окрашена в желтый цвет).
Графически можно изображать только равновесные процессы, состоящие из последовательности равновесных состояний. При увеличении объема на совершаемая газом работа равна то есть определяется площадью зеленой полоски. Поэтому полная работа численно равна площади, ограниченной осью абсцисс, кривой p(V) и прямыми и ( на рисунке окрашена в желтый цвет).
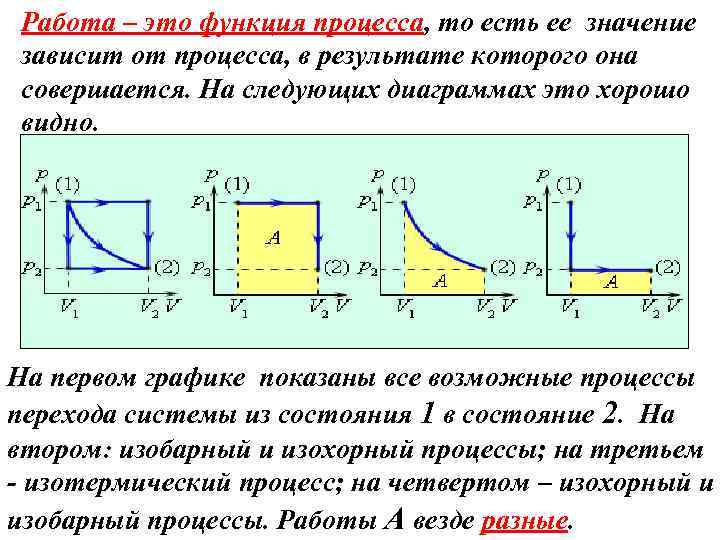 Работа – это функция процесса, то есть ее значение зависит от процесса, в результате которого она совершается. На следующих диаграммах это хорошо видно. На первом графике показаны все возможные процессы перехода системы из состояния 1 в состояние 2. На втором: изобарный и изохорный процессы; на третьем - изотермический процесс; на четвертом – изохорный и изобарный процессы. Работы А везде разные.
Работа – это функция процесса, то есть ее значение зависит от процесса, в результате которого она совершается. На следующих диаграммах это хорошо видно. На первом графике показаны все возможные процессы перехода системы из состояния 1 в состояние 2. На втором: изобарный и изохорный процессы; на третьем - изотермический процесс; на четвертом – изохорный и изобарный процессы. Работы А везде разные.
 В качестве примера рассчитаем работу газа в изотермическом процессе. По определению Из уравнения М-К:
В качестве примера рассчитаем работу газа в изотермическом процессе. По определению Из уравнения М-К:
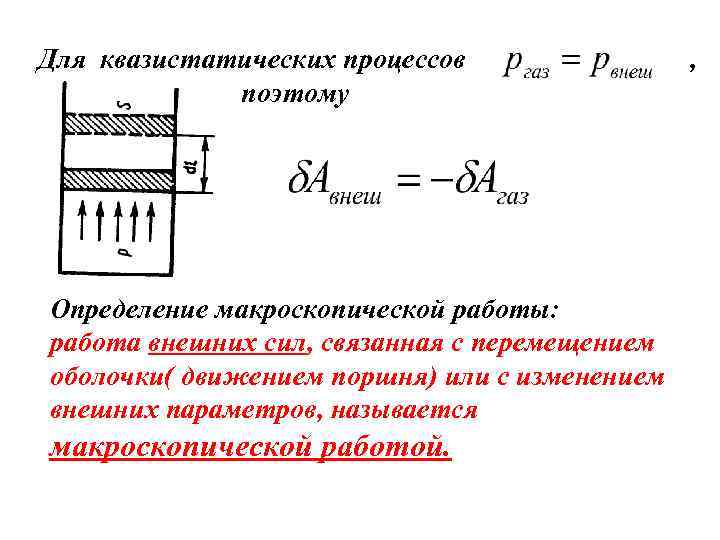 Для квазистатических процессов поэтому Определение макроскопической работы: работа внешних сил, связанная с перемещением оболочки( движением поршня) или с изменением внешних параметров, называется макроскопической работой. ,
Для квазистатических процессов поэтому Определение макроскопической работы: работа внешних сил, связанная с перемещением оболочки( движением поршня) или с изменением внешних параметров, называется макроскопической работой. ,
 Теплота. Количество теплоты Q. Изменение внутренней энергии возможно за счет : 1) работы внешних сил и 2) перехода внутренней энергии от более нагретого тела к менее нагретому. Процесс обмена внутренними энергиями соприкасающихся тел, не сопровождающийся совершением макроскопической работы, называется теплообменом. Энергия, переданная в результате теплообмена, называется количеством теплоты или просто теплотой.
Теплота. Количество теплоты Q. Изменение внутренней энергии возможно за счет : 1) работы внешних сил и 2) перехода внутренней энергии от более нагретого тела к менее нагретому. Процесс обмена внутренними энергиями соприкасающихся тел, не сопровождающийся совершением макроскопической работы, называется теплообменом. Энергия, переданная в результате теплообмена, называется количеством теплоты или просто теплотой.
 Процесс передачи энергии происходит в результате столкновений молекул более нагретого тела с молекулами менее нагретого – то есть в результате микроскопической работы. Теплота Q является функцией процесса, то есть ее изменение зависит от процесса, в котором это происходит. Единица измерения в системе СИ - [Q] = Дж. Менее распространенной в настоящее время единицей измерения теплоты является калория. Связь калории с джоулем называется механическим эквивалентом теплоты: 1 кал = 4, 18 Дж
Процесс передачи энергии происходит в результате столкновений молекул более нагретого тела с молекулами менее нагретого – то есть в результате микроскопической работы. Теплота Q является функцией процесса, то есть ее изменение зависит от процесса, в котором это происходит. Единица измерения в системе СИ - [Q] = Дж. Менее распространенной в настоящее время единицей измерения теплоты является калория. Связь калории с джоулем называется механическим эквивалентом теплоты: 1 кал = 4, 18 Дж
 Первое начало термодинамики представляет собой закон сохранения энергии применительно к тепловым процессам. Изменение внутренней энергии термодинамической системы возможно в результате сообщения ей теплоты и совершения внешней работы: Это одна из формулировок первого начала.
Первое начало термодинамики представляет собой закон сохранения энергии применительно к тепловым процессам. Изменение внутренней энергии термодинамической системы возможно в результате сообщения ей теплоты и совершения внешней работы: Это одна из формулировок первого начала.
 Используя, , получим: Тогда окончательно: Количество тепла, сообщенное системе, идет на приращение внутренней энергии термодинамической системы и на совершение системой работы над внешними силами. Будем использовать именно эту формулировку первого начала термодинамики. Кроме того, в дальнейшем.
Используя, , получим: Тогда окончательно: Количество тепла, сообщенное системе, идет на приращение внутренней энергии термодинамической системы и на совершение системой работы над внешними силами. Будем использовать именно эту формулировку первого начала термодинамики. Кроме того, в дальнейшем.
 Для квазистатических процессов, когда параметры испытывают бесконечно малые изменения I-ое начало принимает вид: В этом выражении дифференциалом, а являются. является полным и таковыми не Свойства: 1) возможно, что если. 2) , т. е. означает, что система получает тепло, а - отдает. ,
Для квазистатических процессов, когда параметры испытывают бесконечно малые изменения I-ое начало принимает вид: В этом выражении дифференциалом, а являются. является полным и таковыми не Свойства: 1) возможно, что если. 2) , т. е. означает, что система получает тепло, а - отдает. ,
 Следствия. 1) В круговом процессе ( на рис. abcd) Это означает, что I-ое начало не накладывает никаких ограничений на преобразование теплоты в механическую работу. 2) Если и , то. Это означает, что невозможен процесс, единственным результатом которого является производство работы без каких-либо изменений в других телах. То есть невозможен вечный двигатель первого рода.
Следствия. 1) В круговом процессе ( на рис. abcd) Это означает, что I-ое начало не накладывает никаких ограничений на преобразование теплоты в механическую работу. 2) Если и , то. Это означает, что невозможен процесс, единственным результатом которого является производство работы без каких-либо изменений в других телах. То есть невозможен вечный двигатель первого рода.
 Теплоемкость идеального газа. Уравнение Майера. Теплоёмкость – это свойство системы накапливать тепло. Численно теплоёмкость системы равна количеству теплоты, необходимой для нагревания этого тела на один градус Кельвина. Размерность теплоемкости: [C] = Дж/К. Теплоёмкость – величина неопределённая, поэтому пользуются понятиями удельной и молярной теплоёмкости.
Теплоемкость идеального газа. Уравнение Майера. Теплоёмкость – это свойство системы накапливать тепло. Численно теплоёмкость системы равна количеству теплоты, необходимой для нагревания этого тела на один градус Кельвина. Размерность теплоемкости: [C] = Дж/К. Теплоёмкость – величина неопределённая, поэтому пользуются понятиями удельной и молярной теплоёмкости.
 Удельная теплоёмкость Суд – есть количество теплоты, необходимое для нагревания единицы массы вещества на 1 градус : ; Дл я газов удобно пользоваться молярной теплоемкостью Сμ количество теплоты, необходимое для нагревания 1 моля газа на 1 градус , [Cμ] = Дж/(моль К), [Cуд] = Дж/(кг К). -число молей
Удельная теплоёмкость Суд – есть количество теплоты, необходимое для нагревания единицы массы вещества на 1 градус : ; Дл я газов удобно пользоваться молярной теплоемкостью Сμ количество теплоты, необходимое для нагревания 1 моля газа на 1 градус , [Cμ] = Дж/(моль К), [Cуд] = Дж/(кг К). -число молей
 Различают теплоемкости при постоянном объеме и постоянном давлении, если в процессе нагревания вещества его объем или давление поддерживается постоянным. Запишем выражение первого начала термодинамики для одного моля газа с учетом формул и Если газ нагревается при постоянном объеме, то работа внешних сил равна нулю и сообщаемая газу извне теплота идет только на увеличение его внутренней энергии:
Различают теплоемкости при постоянном объеме и постоянном давлении, если в процессе нагревания вещества его объем или давление поддерживается постоянным. Запишем выражение первого начала термодинамики для одного моля газа с учетом формул и Если газ нагревается при постоянном объеме, то работа внешних сил равна нулю и сообщаемая газу извне теплота идет только на увеличение его внутренней энергии:
 Если газ нагревается при постоянном давлении, то выражение можно записать в виде: Дифференцируя уравнение Менделеева-Клайперона по (при ), получаем:
Если газ нагревается при постоянном давлении, то выражение можно записать в виде: Дифференцируя уравнение Менделеева-Клайперона по (при ), получаем:
 Тогда окончательно: Уравнение называется уравнением Майера. Оно показывает, что всегда больше на величину молярной газовой постоянной. Это объясняется тем, что при нагревании газа при постоянном давлении требуется еще дополнительное количество теплоты на совершение работы расширения газа, так как постоянство давления обеспечивается увеличением объема газа. Из сказанного следует, что физический смысл универсальной газовой постоянной в том, что R – численно равна работе, совершаемой одним молем газа при нагревании на один градус при изобарическом процессе.
Тогда окончательно: Уравнение называется уравнением Майера. Оно показывает, что всегда больше на величину молярной газовой постоянной. Это объясняется тем, что при нагревании газа при постоянном давлении требуется еще дополнительное количество теплоты на совершение работы расширения газа, так как постоянство давления обеспечивается увеличением объема газа. Из сказанного следует, что физический смысл универсальной газовой постоянной в том, что R – численно равна работе, совершаемой одним молем газа при нагревании на один градус при изобарическом процессе.
 Теплоёмкости одноатомных и многоатомных газов. Закон равнораспределения энергии по степеням свободы. В классической статистической физике вводится закон равнораспределения энергии по степеням свободы (закон Больцмана), согласно которому в состоянии термодинамического равновесия на каждую степень свободы молекулы приходится в среднем энергия, равная k. T/2. Число степеней свободы - это число независимых переменных (координат), полностью определяющих положение системы в пространстве и обозначается i.
Теплоёмкости одноатомных и многоатомных газов. Закон равнораспределения энергии по степеням свободы. В классической статистической физике вводится закон равнораспределения энергии по степеням свободы (закон Больцмана), согласно которому в состоянии термодинамического равновесия на каждую степень свободы молекулы приходится в среднем энергия, равная k. T/2. Число степеней свободы - это число независимых переменных (координат), полностью определяющих положение системы в пространстве и обозначается i.
 Колебательная степень "обладает" вдвое большей энергией потому, что на нее приходится не только кинетическая энергия (как в случае поступательного и вращательного движений), но и потенциальная, причем средние значения кинетической и потенциальной энергий одинаковы. Таким образом, средняя энергия молекулы – где Внутренняя энергия одного моля идеального газа
Колебательная степень "обладает" вдвое большей энергией потому, что на нее приходится не только кинетическая энергия (как в случае поступательного и вращательного движений), но и потенциальная, причем средние значения кинетической и потенциальной энергий одинаковы. Таким образом, средняя энергия молекулы – где Внутренняя энергия одного моля идеального газа
 Молярная теплоемкость при постоянном объеме Молярная теплоемкость при постоянном давлении Отношение где - показатель адиабаты
Молярная теплоемкость при постоянном объеме Молярная теплоемкость при постоянном давлении Отношение где - показатель адиабаты
 Теплоемкость одноатомного газа. Положение материальной точки (одноатомной молекулы) задаётся тремя координатами (x, y, z), поэтому она имеет три степени свободы: Внутренняя энергия Теплоемкости: Показатель адиабаты ,
Теплоемкость одноатомного газа. Положение материальной точки (одноатомной молекулы) задаётся тремя координатами (x, y, z), поэтому она имеет три степени свободы: Внутренняя энергия Теплоемкости: Показатель адиабаты ,
 Теплоемкость двухатомного газа. Двухатомная молекула обладает тремя поступательными степенями свободы и двумя вращательными :
Теплоемкость двухатомного газа. Двухатомная молекула обладает тремя поступательными степенями свободы и двумя вращательными :
 Теплоемкость многоатомного газа. Многоатомную молекулу классическая статистическая физика рассматривает как абсолютно твердое тело, которое может двигаться поступательно в трех взаимно перпендикулярных направлениях и может вращаться вокруг трех взаимно перпендикулярных осей Число степеней свободы: Внутренняя энергия: Теплоемкость:
Теплоемкость многоатомного газа. Многоатомную молекулу классическая статистическая физика рассматривает как абсолютно твердое тело, которое может двигаться поступательно в трех взаимно перпендикулярных направлениях и может вращаться вокруг трех взаимно перпендикулярных осей Число степеней свободы: Внутренняя энергия: Теплоемкость:
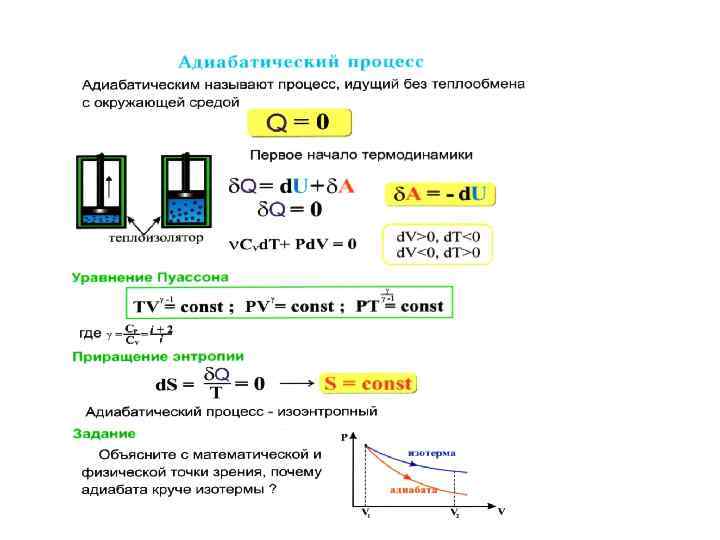
 Адиабатический процесс Адиабатическим называется процесс, идущий без теплообмена с окружающей средой: Из первого начала получаем т. е. работа совершается за внутренней энергии системы. счет изменения Для одного моля газа перепишем написанное уравнение в виде: (1)
Адиабатический процесс Адиабатическим называется процесс, идущий без теплообмена с окружающей средой: Из первого начала получаем т. е. работа совершается за внутренней энергии системы. счет изменения Для одного моля газа перепишем написанное уравнение в виде: (1)
 Продифференцировав идеального газа уравнение состояния , получим: (2) для (1) Почленно разделим уравнений (2) на (1), исключив Разделив переменные и учитывая, что найдем ,
Продифференцировав идеального газа уравнение состояния , получим: (2) для (1) Почленно разделим уравнений (2) на (1), исключив Разделив переменные и учитывая, что найдем ,
 Интегрируя это уравнение в пределах от до и соответственно от до , а затем потенцируя, придем к выражению или Так как состояния 1 и 2 выбраны произвольно, то можно записать Полученное выражение адиабатического процесса, уравнением Пуассона. есть уравнение называемое также
Интегрируя это уравнение в пределах от до и соответственно от до , а затем потенцируя, придем к выражению или Так как состояния 1 и 2 выбраны произвольно, то можно записать Полученное выражение адиабатического процесса, уравнением Пуассона. есть уравнение называемое также