Лекция 9-эрзац вариант.ppt
- Количество слайдов: 45
 Лекция 9 Аналитическая химия Введение в электрохимические методы анализа. Потенциометрические методы.
Лекция 9 Аналитическая химия Введение в электрохимические методы анализа. Потенциометрические методы.
 Электрохимические методы анализа основаны на электрохимических реакциях, в результате которых возникает аналитический сигнал – электрический параметр (потенциал, сила тока, сопротивление), функционально связанный с составом и концентрацией раствора (или расплава). Электрохимическая реакция – гетерогенная реакция переноса электронов (или ионов) через границу раздела электропроводящих фаз.
Электрохимические методы анализа основаны на электрохимических реакциях, в результате которых возникает аналитический сигнал – электрический параметр (потенциал, сила тока, сопротивление), функционально связанный с составом и концентрацией раствора (или расплава). Электрохимическая реакция – гетерогенная реакция переноса электронов (или ионов) через границу раздела электропроводящих фаз.
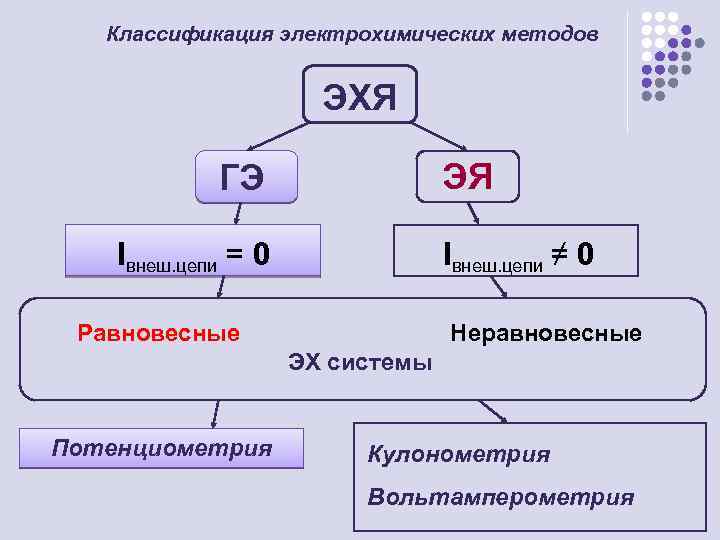 Классификация электрохимических методов ЭХЯ ЭЯ ГЭ Iвнеш. цепи = 0 Iвнеш. цепи ≠ 0 Равновесные Неравновесные ЭХ системы Потенциометрия Кулонометрия Вольтамперометрия
Классификация электрохимических методов ЭХЯ ЭЯ ГЭ Iвнеш. цепи = 0 Iвнеш. цепи ≠ 0 Равновесные Неравновесные ЭХ системы Потенциометрия Кулонометрия Вольтамперометрия
 Электрод, на котором происходит окисление, - анод Электрод, на котором происходит восстановление, - катод ГЭ анод - Zn|Zn. SO 4 (C 1) Cu. SO 4 (С 2)|Cu - катод (+) (-) ЭЯ анод - Cu. SO 4 (С 2)|Cu (+) Zn |Zn. SO 4 (C 1) - катод (-)
Электрод, на котором происходит окисление, - анод Электрод, на котором происходит восстановление, - катод ГЭ анод - Zn|Zn. SO 4 (C 1) Cu. SO 4 (С 2)|Cu - катод (+) (-) ЭЯ анод - Cu. SO 4 (С 2)|Cu (+) Zn |Zn. SO 4 (C 1) - катод (-)
 Потенциометрический метод анализа Метод потенциометрии основан на измерении напряжения на электродах ячейках в отсутствие тока. Измеряемое вольтметром напряжение на электродах ячейки (в общем случае): E = E 0 Ox/Red + RT/n. F ln αOx/αRed E = E 0 Ox/Red + 0, 059 lg αOx/αRed (при 250 С) Индикаторный электрод Электрод сравнения Ag Ag+ E = E 0 + 0, 059 lg αAg+ (при 250 С)
Потенциометрический метод анализа Метод потенциометрии основан на измерении напряжения на электродах ячейках в отсутствие тока. Измеряемое вольтметром напряжение на электродах ячейки (в общем случае): E = E 0 Ox/Red + RT/n. F ln αOx/αRed E = E 0 Ox/Red + 0, 059 lg αOx/αRed (при 250 С) Индикаторный электрод Электрод сравнения Ag Ag+ E = E 0 + 0, 059 lg αAg+ (при 250 С)
 Потенциометрический метод анализа Система является Нернстовской, если при постоянной α остальных компонентов d. E/dln αA = + a RT/n. F d. E/dln αC = - c RT/n. F …………
Потенциометрический метод анализа Система является Нернстовской, если при постоянной α остальных компонентов d. E/dln αA = + a RT/n. F d. E/dln αC = - c RT/n. F …………
 Классификация электрохимических методов по способу выполнения Прямые I (E, R, Q) = f (C) Косвенные I (E, R, Q) = f (Vтитранта)
Классификация электрохимических методов по способу выполнения Прямые I (E, R, Q) = f (C) Косвенные I (E, R, Q) = f (Vтитранта)
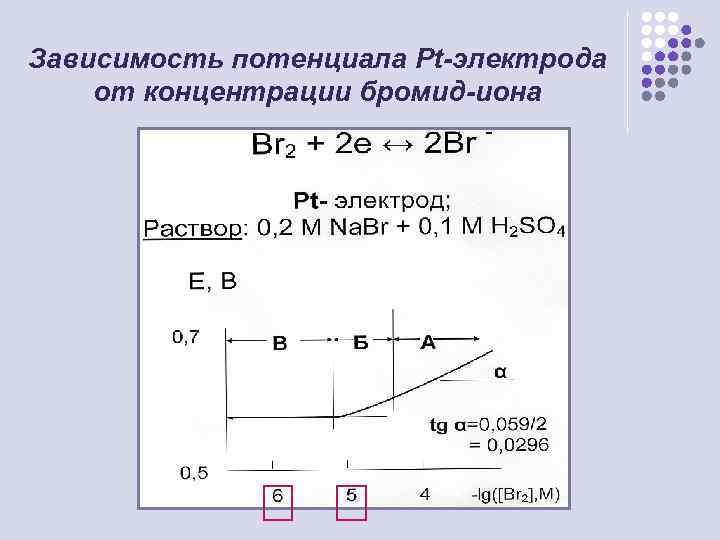 Зависимость потенциала Pt-электрода от концентрации бромид-иона
Зависимость потенциала Pt-электрода от концентрации бромид-иона
 Метод прямой потенциометрии Классификация индикаторных электродов • Металлические (активные и инертные) • Ионоселективные (мембранные)
Метод прямой потенциометрии Классификация индикаторных электродов • Металлические (активные и инертные) • Ионоселективные (мембранные)
 Металлические электроды Инертные металлические электроды – Pt, Ir, Au Активные (Ag, Hg, Zn, Cd, Cu) – I и II рода – металлические пластинки в растворе соли того же металла; обратимо реагируют на изменение активности катиона в растворе Ag–электрод: E = EAg+/Ag + 0, 059 lgαAg+ ; E = f(αAg+)
Металлические электроды Инертные металлические электроды – Pt, Ir, Au Активные (Ag, Hg, Zn, Cd, Cu) – I и II рода – металлические пластинки в растворе соли того же металла; обратимо реагируют на изменение активности катиона в растворе Ag–электрод: E = EAg+/Ag + 0, 059 lgαAg+ ; E = f(αAg+)
 Активные металлические электроды II рода – металлические пластинки (Ag), покрытые слоем малорастворимой соли того же металла (Ag. Cl) и погруженные в насыщенный раствор этой соли (Ag. Cl нас) Ag. Cl (тв) + ē → Ag + Cl. E = E Ag+/Ag + RT/n. F ln Ks. Ag. Cl /αCl- = E 0 Ag. Cl/Ag - 0, 059 lg αCl- E = f(αCl-) E =E 0 Ag. X/Ag + 0, 059 lg αX; X – Br- , I-, S 2 -
Активные металлические электроды II рода – металлические пластинки (Ag), покрытые слоем малорастворимой соли того же металла (Ag. Cl) и погруженные в насыщенный раствор этой соли (Ag. Cl нас) Ag. Cl (тв) + ē → Ag + Cl. E = E Ag+/Ag + RT/n. F ln Ks. Ag. Cl /αCl- = E 0 Ag. Cl/Ag - 0, 059 lg αCl- E = f(αCl-) E =E 0 Ag. X/Ag + 0, 059 lg αX; X – Br- , I-, S 2 -
 Ионоселективные (мембранные) электроды – «сенсоры (чувствительные элементы, датчики), потенциалы которых линейно зависят от активности определяемого иона в растворе» (IUPAС) ИСЭ функционируют по механизму переноса ионов, т. е. обладают ионной проводимостью Полупроницаемая мембрана – слой, разделяющий 2 раствора с разными концентрациями электролита, образующий резкую границу с обоими растворами и служащий электрическим контактом этих растворов.
Ионоселективные (мембранные) электроды – «сенсоры (чувствительные элементы, датчики), потенциалы которых линейно зависят от активности определяемого иона в растворе» (IUPAС) ИСЭ функционируют по механизму переноса ионов, т. е. обладают ионной проводимостью Полупроницаемая мембрана – слой, разделяющий 2 раствора с разными концентрациями электролита, образующий резкую границу с обоими растворами и служащий электрическим контактом этих растворов.
 Требования к ИСЭ: Ø химическая устойчивость; Ø электропроводность (ионная проводимость); Ø малая растворимость; Ø повышенная экстракционная растворимость жидких веществ.
Требования к ИСЭ: Ø химическая устойчивость; Ø электропроводность (ионная проводимость); Ø малая растворимость; Ø повышенная экстракционная растворимость жидких веществ.
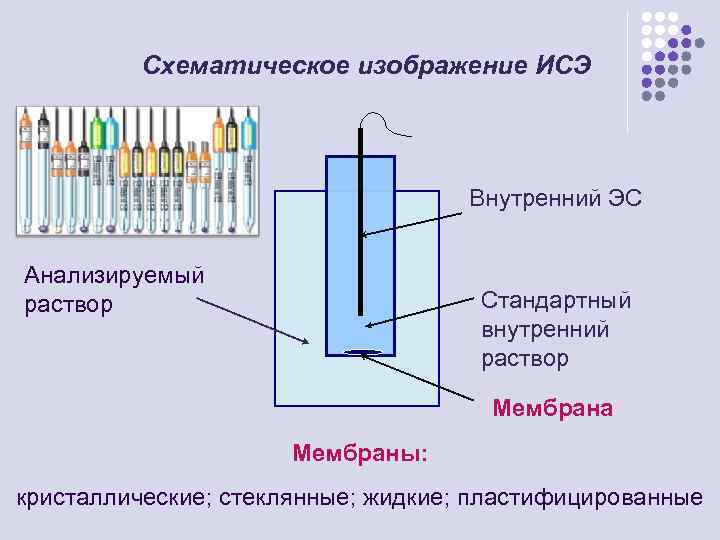 Схематическое изображение ИСЭ Внутренний ЭС Анализируемый раствор Стандартный внутренний раствор Мембрана Мембраны: кристаллические; стеклянные; жидкие; пластифицированные
Схематическое изображение ИСЭ Внутренний ЭС Анализируемый раствор Стандартный внутренний раствор Мембрана Мембраны: кристаллические; стеклянные; жидкие; пластифицированные
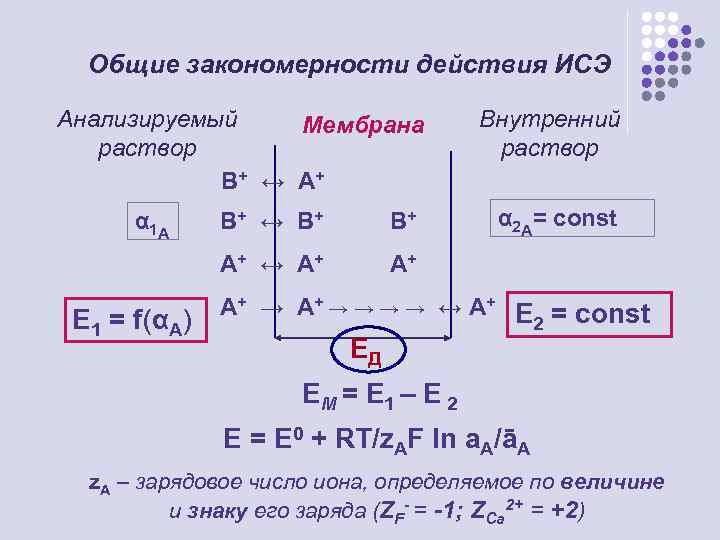 Общие закономерности действия ИСЭ Анализируемый Мембрана раствор В+ ↔ А + α 1 A В+ А+ ↔ А + Е 1 = f(αA) В+ ↔ В + Внутренний раствор α 2 A= const А+ А+ → → → → ↔ А+ Е = const 2 ЕД EM = E 1 – E 2 E = E 0 + RT/z. AF ln a. A/āA z. A – зарядовое число иона, определяемое по величине и знаку его заряда (ZF- = -1; ZCa 2+ = +2)
Общие закономерности действия ИСЭ Анализируемый Мембрана раствор В+ ↔ А + α 1 A В+ А+ ↔ А + Е 1 = f(αA) В+ ↔ В + Внутренний раствор α 2 A= const А+ А+ → → → → ↔ А+ Е = const 2 ЕД EM = E 1 – E 2 E = E 0 + RT/z. AF ln a. A/āA z. A – зарядовое число иона, определяемое по величине и знаку его заряда (ZF- = -1; ZCa 2+ = +2)
 Процесс ионного обмена А+ + В + ↔ В + + А + Константа обмена КА-В = āВ · а. А / а. В · āА КА-В · ŪВ/ŪА = Кпот. А, В (потенц. коэффициент селективности) где ŪА, ŪВ – подвижности ионов в мембране E = const + RT/z. AF·ln(a. A+КА, В а. B +КА, C а. Cz. A/z. C + …) z. A/z. B + Уравнение Нернста – Эйземанна - Никольского
Процесс ионного обмена А+ + В + ↔ В + + А + Константа обмена КА-В = āВ · а. А / а. В · āА КА-В · ŪВ/ŪА = Кпот. А, В (потенц. коэффициент селективности) где ŪА, ŪВ – подвижности ионов в мембране E = const + RT/z. AF·ln(a. A+КА, В а. B +КА, C а. Cz. A/z. C + …) z. A/z. B + Уравнение Нернста – Эйземанна - Никольского
 Характеристики ИСЭ • Электродная функция (ЭФ) – область прямолинейной зависимости Е от lg α (lg C) потенциалопределяющего иона. • Крутизна ЭФ (S) – угловой коэффициент прямолинейной зависимости E = f(a) (RT/z. АF = 59, 16/z. А м. В)
Характеристики ИСЭ • Электродная функция (ЭФ) – область прямолинейной зависимости Е от lg α (lg C) потенциалопределяющего иона. • Крутизна ЭФ (S) – угловой коэффициент прямолинейной зависимости E = f(a) (RT/z. АF = 59, 16/z. А м. В)
 Характеристики ИСЭ • Коэффициент селективности (KC) электрода характеризует селективность ИСЭ относительно определяемого иона А в присутствии иона В. КА/В < 1, электрод селективен относительно иона А; КА/В > 1, электрод селективен относительно иона В. Высокая селективность – при КС ≈ 10 -4 – 10 -3
Характеристики ИСЭ • Коэффициент селективности (KC) электрода характеризует селективность ИСЭ относительно определяемого иона А в присутствии иона В. КА/В < 1, электрод селективен относительно иона А; КА/В > 1, электрод селективен относительно иона В. Высокая селективность – при КС ≈ 10 -4 – 10 -3
 Характеристики ИСЭ • Время отклика – время достижения 95% максимальной величины потенциала (сек─мин) Еmax 95% Время отклика t, c • Температурная функция • Время жизни – ресурс работы
Характеристики ИСЭ • Время отклика – время достижения 95% максимальной величины потенциала (сек─мин) Еmax 95% Время отклика t, c • Температурная функция • Время жизни – ресурс работы
 Классификация ИСЭ • По агрегатному состоянию мембраны: жидкие, твердые • По типу электроактивного компонента мембраны: монокристаллы, стеклянные мембраны, ионообменники, нейтральные переносчики
Классификация ИСЭ • По агрегатному состоянию мембраны: жидкие, твердые • По типу электроактивного компонента мембраны: монокристаллы, стеклянные мембраны, ионообменники, нейтральные переносчики
 Классификация ИСЭ • По характеру активных ионообменных центров: фиксированные центры (стеклянные электроды, ионообменники); подвижные центры (жидкие ионообменники) • По механизму потенциалопределяющих процессов: хемосорбция (монокристаллы), ионный обмен (стеклянные электроды), экстракция (жидкие ионообменники)
Классификация ИСЭ • По характеру активных ионообменных центров: фиксированные центры (стеклянные электроды, ионообменники); подвижные центры (жидкие ионообменники) • По механизму потенциалопределяющих процессов: хемосорбция (монокристаллы), ионный обмен (стеклянные электроды), экстракция (жидкие ионообменники)
 Классификация ИСЭ Употребляемая в литературе 2) ИСЭ с твердой мембраной: кристаллической гомогенной; кристаллической гетерогенной Электрод со стеклянной мембраной ИСЭ с жесткими мембранами: анионообменники; катионообменники; нейтральные переносчики твительные Ферментные Рекомендуемая IUPAC I. Первичные Кристаллические гомогенные; гетерогенные Некристаллические 3) Электрод с жесткой матрицей 1) II. Электроды с подвижным носителем: положительно заряженные; отрицательно заряженные; незаряженные III. Сенсибилизированные Газочувс электроды: газочувствительные; ферментные; полевые транзисторы
Классификация ИСЭ Употребляемая в литературе 2) ИСЭ с твердой мембраной: кристаллической гомогенной; кристаллической гетерогенной Электрод со стеклянной мембраной ИСЭ с жесткими мембранами: анионообменники; катионообменники; нейтральные переносчики твительные Ферментные Рекомендуемая IUPAC I. Первичные Кристаллические гомогенные; гетерогенные Некристаллические 3) Электрод с жесткой матрицей 1) II. Электроды с подвижным носителем: положительно заряженные; отрицательно заряженные; незаряженные III. Сенсибилизированные Газочувс электроды: газочувствительные; ферментные; полевые транзисторы
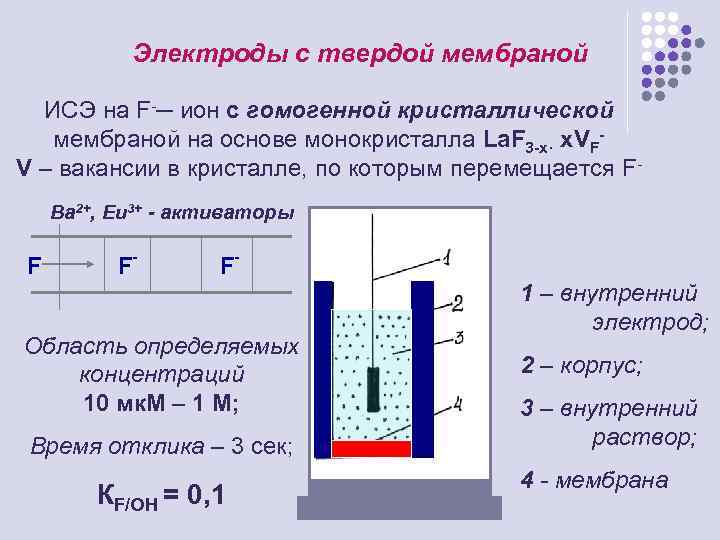 Электроды с твердой мембраной ИСЭ на F-─ ион с гомогенной кристаллической мембраной на основе монокристалла La. F 3 -x· x. VFV – вакансии в кристалле, по которым перемещается FВа 2+, Eu 3+ - активаторы F- F- F- Область определяемых концентраций 10 мк. М – 1 М; Время отклика – 3 сек; КF/OH = 0, 1 1 – внутренний электрод; 2 – корпус; 3 – внутренний раствор; 4 - мембрана
Электроды с твердой мембраной ИСЭ на F-─ ион с гомогенной кристаллической мембраной на основе монокристалла La. F 3 -x· x. VFV – вакансии в кристалле, по которым перемещается FВа 2+, Eu 3+ - активаторы F- F- F- Область определяемых концентраций 10 мк. М – 1 М; Время отклика – 3 сек; КF/OH = 0, 1 1 – внутренний электрод; 2 – корпус; 3 – внутренний раствор; 4 - мембрана
 Электроды с твердой мембраной Гетерогенные электроды электроактивное вещество диспергируют в ионном носителе (эпоксидные смолы, силиконовый каучук, поливинилхлорид) ИСЭ на Pb 2+ {Ag 2 S – Pb. S} → ЭАВ Токоотвод – графит в тефлоне Определяют 10 -6 – 10 -2 М Pb 2+
Электроды с твердой мембраной Гетерогенные электроды электроактивное вещество диспергируют в ионном носителе (эпоксидные смолы, силиконовый каучук, поливинилхлорид) ИСЭ на Pb 2+ {Ag 2 S – Pb. S} → ЭАВ Токоотвод – графит в тефлоне Определяют 10 -6 – 10 -2 М Pb 2+
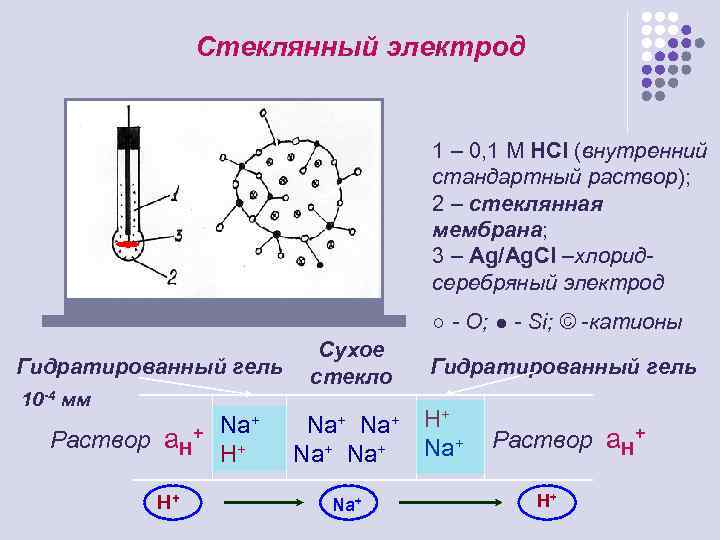 Стеклянный электрод 1 – 0, 1 М HCl (внутренний стандартный раствор); 2 – стеклянная мембрана; 3 – Ag/Ag. Cl –хлоридсеребряный электрод ○ - O; ● - Si; © -катионы Гидратированный гель 10 -4 мм Раствор а. Н+ Н+ Na+ H+ Сухое стекло Гидратированный гель + Na+ H Na+ Na+ Раствор а. Н+ Н+
Стеклянный электрод 1 – 0, 1 М HCl (внутренний стандартный раствор); 2 – стеклянная мембрана; 3 – Ag/Ag. Cl –хлоридсеребряный электрод ○ - O; ● - Si; © -катионы Гидратированный гель 10 -4 мм Раствор а. Н+ Н+ Na+ H+ Сухое стекло Гидратированный гель + Na+ H Na+ Na+ Раствор а. Н+ Н+
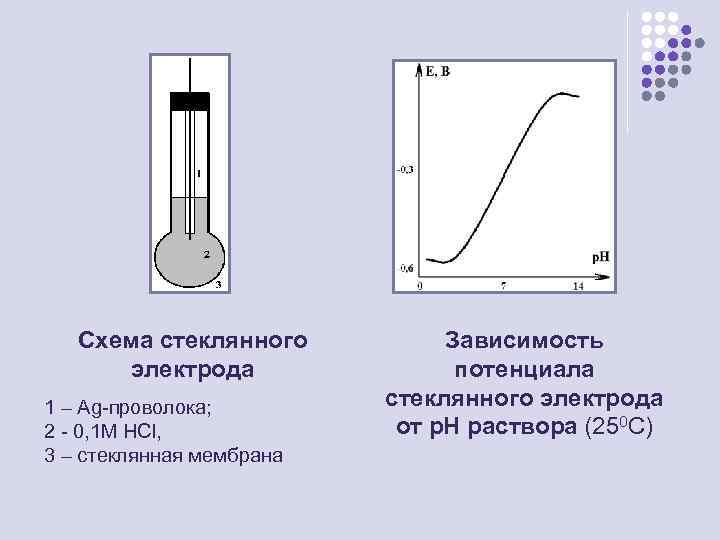 Схема стеклянного электрода 1 – Ag-проволока; 2 - 0, 1 М HCl, 3 – стеклянная мембрана Зависимость потенциала стеклянного электрода от р. Н раствора (250 С)
Схема стеклянного электрода 1 – Ag-проволока; 2 - 0, 1 М HCl, 3 – стеклянная мембрана Зависимость потенциала стеклянного электрода от р. Н раствора (250 С)
 Современные р. Н-метры
Современные р. Н-метры
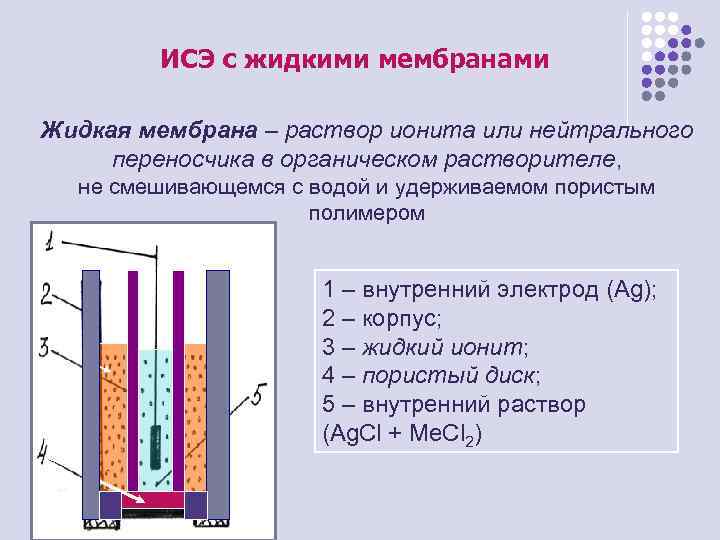 ИСЭ с жидкими мембранами Жидкая мембрана – раствор ионита или нейтрального переносчика в органическом растворителе, не смешивающемся с водой и удерживаемом пористым полимером 1 – внутренний электрод (Ag); 2 – корпус; 3 – жидкий ионит; 4 – пористый диск; 5 – внутренний раствор (Ag. Cl + Me. Cl 2)
ИСЭ с жидкими мембранами Жидкая мембрана – раствор ионита или нейтрального переносчика в органическом растворителе, не смешивающемся с водой и удерживаемом пористым полимером 1 – внутренний электрод (Ag); 2 – корпус; 3 – жидкий ионит; 4 – пористый диск; 5 – внутренний раствор (Ag. Cl + Me. Cl 2)
 Катионообменники Са─СЭ – 10 -5 – 1 М; КСа/Mg =10 -2 2(RO)2 POO-(орг)+Са 2+(вод)↔[(RO)2 POO]2 Са (орг) (диоктилфенилфосфанат) R – 8 -16 C Анионообменники NO 3 - ─ СЭ - 10 -5 – 1 М Ni. L 32+(NO 3 -)2; L – 1, 10 -фенантролин Пластифицированные мембраны – жидкие мембраны, заключенные в полимерную матрицу
Катионообменники Са─СЭ – 10 -5 – 1 М; КСа/Mg =10 -2 2(RO)2 POO-(орг)+Са 2+(вод)↔[(RO)2 POO]2 Са (орг) (диоктилфенилфосфанат) R – 8 -16 C Анионообменники NO 3 - ─ СЭ - 10 -5 – 1 М Ni. L 32+(NO 3 -)2; L – 1, 10 -фенантролин Пластифицированные мембраны – жидкие мембраны, заключенные в полимерную матрицу
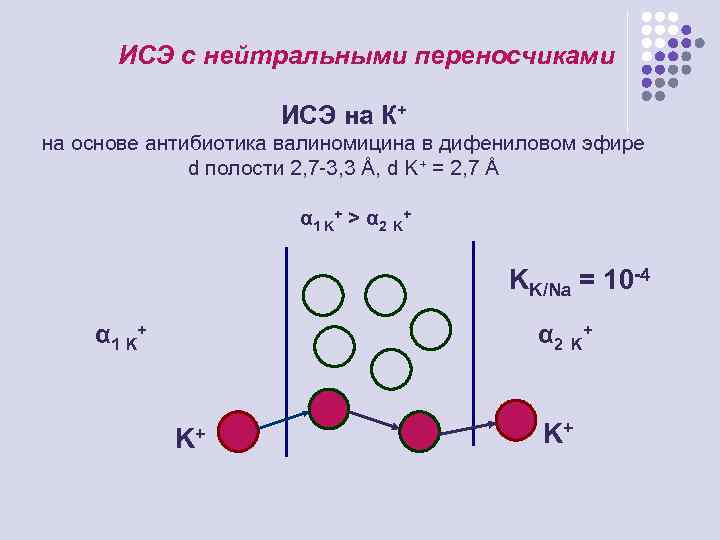 ИСЭ с нейтральными переносчиками ИСЭ на К+ на основе антибиотика валиномицина в дифениловом эфире d полости 2, 7 -3, 3 Å, d K+ = 2, 7 Å α 1 K+ > α 2 K+ KK/Na = 10 -4 α 1 K+ α 2 K+ K+ K+
ИСЭ с нейтральными переносчиками ИСЭ на К+ на основе антибиотика валиномицина в дифениловом эфире d полости 2, 7 -3, 3 Å, d K+ = 2, 7 Å α 1 K+ > α 2 K+ KK/Na = 10 -4 α 1 K+ α 2 K+ K+ K+
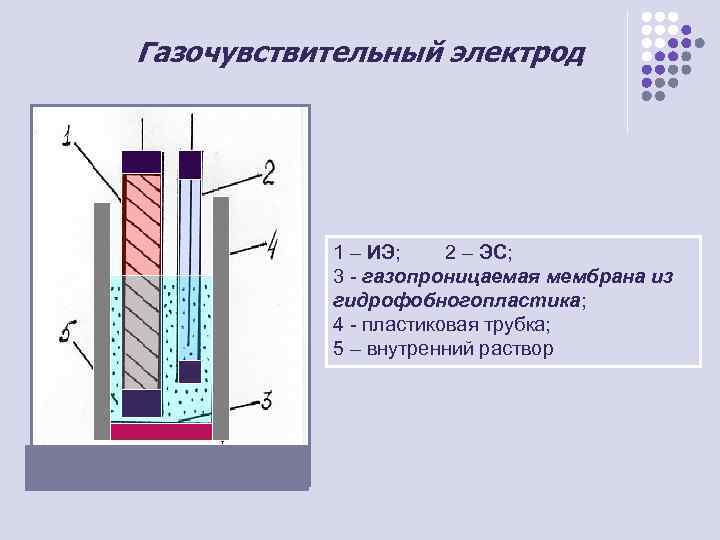 Газочувствительный электрод 1 – ИЭ; 2 – ЭС; 3 - газопроницаемая мембрана из гидрофобногопластика; 4 - пластиковая трубка; 5 – внутренний раствор
Газочувствительный электрод 1 – ИЭ; 2 – ЭС; 3 - газопроницаемая мембрана из гидрофобногопластика; 4 - пластиковая трубка; 5 – внутренний раствор
 Электрод, чувствительный к SO 2 (Ag/Ag. Cl-ЭС, стеклянный ИЭ) SO 2 (внешний р-р) ↔ SO 2 (поры мембраны) ↔ SO 2 (внутренний р-р) SO 2 + 2 H 2 O ↔ HSO 3 - + H 3 O+ Стеклянный электрод на Н+ : SO 2, СO 2, NH 3, Н 2 S Фторидный электрод - F- по изменению конц. HF
Электрод, чувствительный к SO 2 (Ag/Ag. Cl-ЭС, стеклянный ИЭ) SO 2 (внешний р-р) ↔ SO 2 (поры мембраны) ↔ SO 2 (внутренний р-р) SO 2 + 2 H 2 O ↔ HSO 3 - + H 3 O+ Стеклянный электрод на Н+ : SO 2, СO 2, NH 3, Н 2 S Фторидный электрод - F- по изменению конц. HF
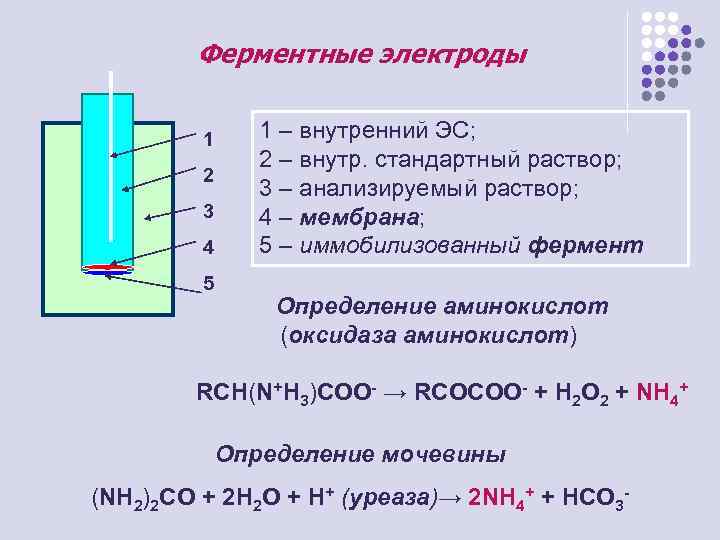 Ферментные электроды 1 2 3 4 5 1 – внутренний ЭС; 2 – внутр. стандартный раствор; 3 – анализируемый раствор; 4 – мембрана; 5 – иммобилизованный фермент Определение аминокислот (оксидаза аминокислот) RCH(N+H 3)COO- → RCOCOO- + H 2 O 2 + NH 4+ Определение мочевины (NH 2)2 CO + 2 H 2 O + H+ (уреаза)→ 2 NH 4+ + HCO 3 -
Ферментные электроды 1 2 3 4 5 1 – внутренний ЭС; 2 – внутр. стандартный раствор; 3 – анализируемый раствор; 4 – мембрана; 5 – иммобилизованный фермент Определение аминокислот (оксидаза аминокислот) RCH(N+H 3)COO- → RCOCOO- + H 2 O 2 + NH 4+ Определение мочевины (NH 2)2 CO + 2 H 2 O + H+ (уреаза)→ 2 NH 4+ + HCO 3 -
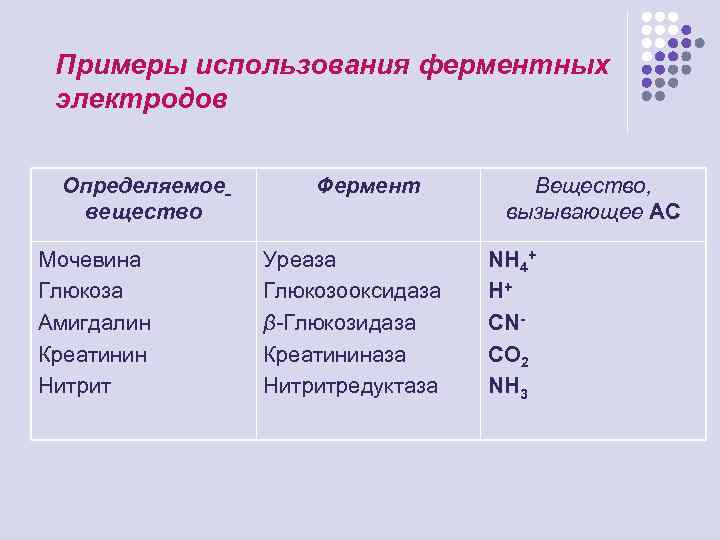 Примеры использования ферментных электродов Определяемое вещество Мочевина Глюкоза Амигдалин Креатинин Нитрит Фермент Уреаза Глюкозооксидаза β-Глюкозидаза Креатининаза Нитритредуктаза Вещество, вызывающее АС NH 4+ H+ CNCO 2 NH 3
Примеры использования ферментных электродов Определяемое вещество Мочевина Глюкоза Амигдалин Креатинин Нитрит Фермент Уреаза Глюкозооксидаза β-Глюкозидаза Креатининаза Нитритредуктаза Вещество, вызывающее АС NH 4+ H+ CNCO 2 NH 3
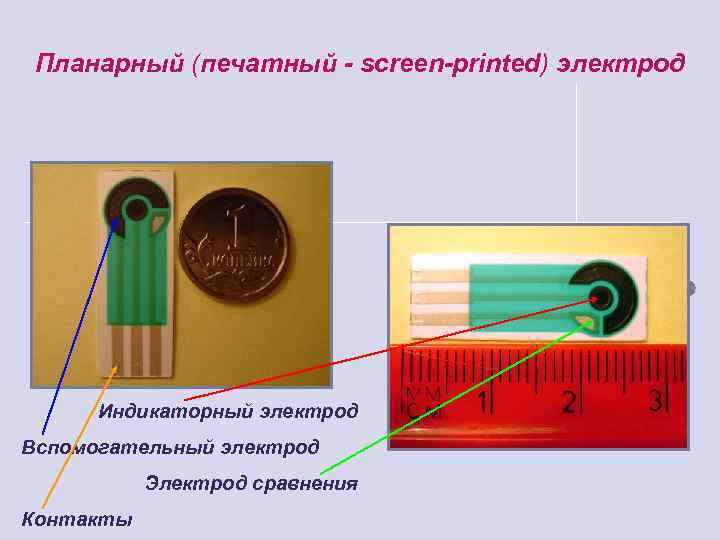 Планарный (печатный - screen-printed) электрод Индикаторный электрод Вспомогательный электрод Электрод сравнения Контакты
Планарный (печатный - screen-printed) электрод Индикаторный электрод Вспомогательный электрод Электрод сравнения Контакты
 Прямая потенциометрия (ионометрия) Еизм = ЕИЭ – ЕЭС + Еj ЕИЭ = const + (0, 059 lga. A)/z. A Как определить а. А? p. A = -lga. A = (Еизм – K’)z. A /0, 059 K’ включает постоянные ЕЭС, Еj, const
Прямая потенциометрия (ионометрия) Еизм = ЕИЭ – ЕЭС + Еj ЕИЭ = const + (0, 059 lga. A)/z. A Как определить а. А? p. A = -lga. A = (Еизм – K’)z. A /0, 059 K’ включает постоянные ЕЭС, Еj, const
 Как оценить K’? 1. Метод калибровки электрода (надо знать γ) а – известно, измеряют Е → рассчитывают К’ 2. Метод добавок (надо знать γ) Cx → E 1 Cx + Ccт → E 2 -lg. Cxγx = (E 1 - K’)z. A / 0, 059 -lg(Cx. Vx +Ccт. Vcт )γx /(Vx + Vcт) = (E 2 – K’)z. A / 0, 059
Как оценить K’? 1. Метод калибровки электрода (надо знать γ) а – известно, измеряют Е → рассчитывают К’ 2. Метод добавок (надо знать γ) Cx → E 1 Cx + Ccт → E 2 -lg. Cxγx = (E 1 - K’)z. A / 0, 059 -lg(Cx. Vx +Ccт. Vcт )γx /(Vx + Vcт) = (E 2 – K’)z. A / 0, 059
 3. Метод градуировочного графика μст = μан = const ЕИЭ = const + S lg. CA (не нужен γ) S – коэффициент чувствительности или крутизна электродной функции При проведении прямых потенциометрических измерений важно: • постоянство температуры; • оптимальный состав анализируемого раствора с учетом селективности электрода; • оптимальное значение р. Н раствора;
3. Метод градуировочного графика μст = μан = const ЕИЭ = const + S lg. CA (не нужен γ) S – коэффициент чувствительности или крутизна электродной функции При проведении прямых потенциометрических измерений важно: • постоянство температуры; • оптимальный состав анализируемого раствора с учетом селективности электрода; • оптимальное значение р. Н раствора;
 • все формы определяемого компонента следует переводить в одно ионное состояние: FHF Al(Fe)Fn(3 -n)+ Регулятор р. Н – буферная смесь с р. Н 5 -7 Демаскирователь – цитрат, тартрат
• все формы определяемого компонента следует переводить в одно ионное состояние: FHF Al(Fe)Fn(3 -n)+ Регулятор р. Н – буферная смесь с р. Н 5 -7 Демаскирователь – цитрат, тартрат
 Области применения ИСЭ Cmin ≈ 10 -7 – 10 -6 M; Определяемый компонент sr > 4 -5%; ∆E ≥ 1 м. В Объект анализа F- Морская, дождевая вода; воздух; корма; горные породы; биологические жидкости; костная ткань K+ Почвы; удобрения; биологические жидкости Ca 2+ Почвы; удобрения; биологические жидкости; пищевые продукты; растения NO 3 - Питьевая, сточные воды; пищевые продукты; удобрения Мочевина Биологические жидкости; сточные воды; воды бассейнов
Области применения ИСЭ Cmin ≈ 10 -7 – 10 -6 M; Определяемый компонент sr > 4 -5%; ∆E ≥ 1 м. В Объект анализа F- Морская, дождевая вода; воздух; корма; горные породы; биологические жидкости; костная ткань K+ Почвы; удобрения; биологические жидкости Ca 2+ Почвы; удобрения; биологические жидкости; пищевые продукты; растения NO 3 - Питьевая, сточные воды; пищевые продукты; удобрения Мочевина Биологические жидкости; сточные воды; воды бассейнов
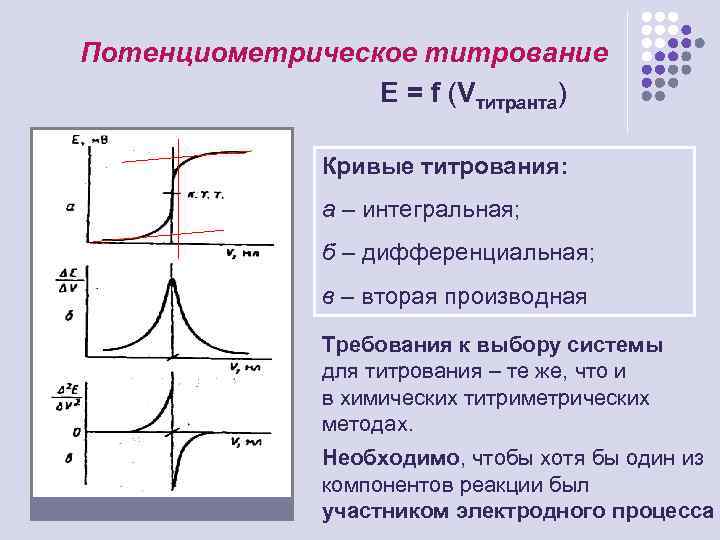 Потенциометрическое титрование E = f (Vтитранта) Кривые титрования: а – интегральная; б – дифференциальная; в – вторая производная Требования к выбору системы для титрования – те же, что и в химических титриметрических методах. Необходимо, чтобы хотя бы один из компонентов реакции был участником электродного процесса
Потенциометрическое титрование E = f (Vтитранта) Кривые титрования: а – интегральная; б – дифференциальная; в – вторая производная Требования к выбору системы для титрования – те же, что и в химических титриметрических методах. Необходимо, чтобы хотя бы один из компонентов реакции был участником электродного процесса
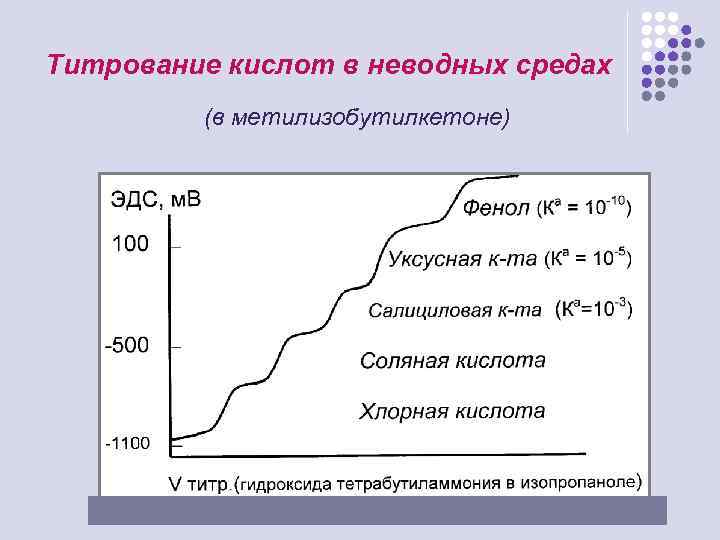 Титрование кислот в неводных средах (в метилизобутилкетоне)
Титрование кислот в неводных средах (в метилизобутилкетоне)
 Достоинства потенциометрического титрования l l l объективная оценка т. экв. ; часто бóльшая чувствительность; возможность последовательного титрования компонентов смеси без разделения; возможность титрования мутных и окрашенных растворов; возможность автоматизации титрования; документальность результатов измерений
Достоинства потенциометрического титрования l l l объективная оценка т. экв. ; часто бóльшая чувствительность; возможность последовательного титрования компонентов смеси без разделения; возможность титрования мутных и окрашенных растворов; возможность автоматизации титрования; документальность результатов измерений
 Автоматические титраторы
Автоматические титраторы
 Спасибо за внимание!
Спасибо за внимание!


