лекция 9 амины и диазо.ppt
- Количество слайдов: 27
 Лекция 9. Амины и диазо.
Лекция 9. Амины и диазо.
 Номенклатура и изомерия аминов. n n Органические соединения, содержащие группы NH 2, NHR или NR 2 где R – алифатический или ароматический радикал называются амины. В отличие от спиртов и галогенпроизводных, тривиальная номенклатура аминов основана не на замещенности атома углерода, к которому присоединен заместитель, а от количества заместителей у атома азота. Соединения с общей формулой R‑NH 2 называют первичными аминами, R 2 NH – вторичными аминами, R 3 N – третичными аминами и R 4 N+ четвертичными аммонийными основаниями или солями. В номенклатуре IUPAC в приставке аминогруппа обозначается амино-, а в окончании –амин.
Номенклатура и изомерия аминов. n n Органические соединения, содержащие группы NH 2, NHR или NR 2 где R – алифатический или ароматический радикал называются амины. В отличие от спиртов и галогенпроизводных, тривиальная номенклатура аминов основана не на замещенности атома углерода, к которому присоединен заместитель, а от количества заместителей у атома азота. Соединения с общей формулой R‑NH 2 называют первичными аминами, R 2 NH – вторичными аминами, R 3 N – третичными аминами и R 4 N+ четвертичными аммонийными основаниями или солями. В номенклатуре IUPAC в приставке аминогруппа обозначается амино-, а в окончании –амин.
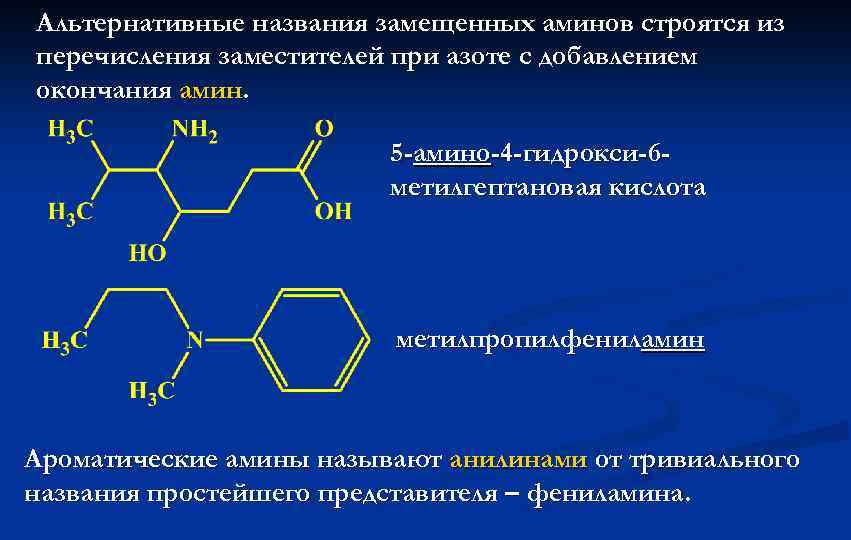 Альтернативные названия замещенных аминов строятся из перечисления заместителей при азоте с добавлением окончания амин. 5 -амино-4 -гидрокси-6 метилгептановая кислота метилпропилфениламин Ароматические амины называют анилинами от тривиального названия простейшего представителя – фениламина.
Альтернативные названия замещенных аминов строятся из перечисления заместителей при азоте с добавлением окончания амин. 5 -амино-4 -гидрокси-6 метилгептановая кислота метилпропилфениламин Ароматические амины называют анилинами от тривиального названия простейшего представителя – фениламина.
 Строение атома азота в аминах n n n Атом азота в аминах имеет тетраэдрическую конфигурацию аналогичную sp 3 для атома углерода. Роль четвертого заместителя выполняет неподеленная пара электронов атома азота. Однако, у тризамещенных аминов не наблюдается оптической изомерии в связи с тем, что в отличие от атома углерода, пара электронов, выступающая в роли четвертого заместителя, способна претерпевать инверсию через промежуточное состояние типа sp 2, и при этом конфигурация меняется на противоположную ( «выворачивается» ). Энергетический барьер инверсии очень мал (5 -6 ккал/моль), и зафиксировать отдельные изомеры при нормальных условиях не удается.
Строение атома азота в аминах n n n Атом азота в аминах имеет тетраэдрическую конфигурацию аналогичную sp 3 для атома углерода. Роль четвертого заместителя выполняет неподеленная пара электронов атома азота. Однако, у тризамещенных аминов не наблюдается оптической изомерии в связи с тем, что в отличие от атома углерода, пара электронов, выступающая в роли четвертого заместителя, способна претерпевать инверсию через промежуточное состояние типа sp 2, и при этом конфигурация меняется на противоположную ( «выворачивается» ). Энергетический барьер инверсии очень мал (5 -6 ккал/моль), и зафиксировать отдельные изомеры при нормальных условиях не удается.
 Если «зафиксировать» одну из форм в объемной каркасной структуре, то оптическая изомерия появляется, так как инверсия не возможна из-за стерических препятствий (неподеленная пара не может быть направлена внутрь каркасной структуры). Естественно, четвертичные аммонийные основания и соли, содержащие четыре различных заместителя, являются хиральными.
Если «зафиксировать» одну из форм в объемной каркасной структуре, то оптическая изомерия появляется, так как инверсия не возможна из-за стерических препятствий (неподеленная пара не может быть направлена внутрь каркасной структуры). Естественно, четвертичные аммонийные основания и соли, содержащие четыре различных заместителя, являются хиральными.
 Способы получения алифатических и ароматических аминов Нуклеофильное замещение галогенов в алкилгалогенидах под действием аммиака и аминов (реакция Гофмана). реакция используется редко, так как замещенные амины, как правило, являются более сильными нуклеофилами, чем аммиак, и остановить реакцию на стадии монозамещения практически невозможно. Используя многократный избыток аммиака, удается получить первичные амины по реакции Гофмана. Реакцию прямого алкилирования используют в основном для получения четвертичных аммонийных солей и оснований.
Способы получения алифатических и ароматических аминов Нуклеофильное замещение галогенов в алкилгалогенидах под действием аммиака и аминов (реакция Гофмана). реакция используется редко, так как замещенные амины, как правило, являются более сильными нуклеофилами, чем аммиак, и остановить реакцию на стадии монозамещения практически невозможно. Используя многократный избыток аммиака, удается получить первичные амины по реакции Гофмана. Реакцию прямого алкилирования используют в основном для получения четвертичных аммонийных солей и оснований.
 Нуклеофильное замещение галогенов в алкилгалогенидах под действием фталимида калия (реакция Габриэля). Нуклеофильное замещения галогена под действием фталимида калия – удобный метод получения первичных аминов. За счет резкого снижения нуклеофильных свойств при переходе от фталимида калия к алкилфталимиду, реакция протекает однозначно и с хорошими выходами. Образующийся N-алкилфталимид для выделения амина обрабатывают гидразином или концентрированной бромистоводородной кислотой.
Нуклеофильное замещение галогенов в алкилгалогенидах под действием фталимида калия (реакция Габриэля). Нуклеофильное замещения галогена под действием фталимида калия – удобный метод получения первичных аминов. За счет резкого снижения нуклеофильных свойств при переходе от фталимида калия к алкилфталимиду, реакция протекает однозначно и с хорошими выходами. Образующийся N-алкилфталимид для выделения амина обрабатывают гидразином или концентрированной бромистоводородной кислотой.
 По реакции Габриэля получают многие природные амины, включая аминокислоты.
По реакции Габриэля получают многие природные амины, включая аминокислоты.
 Восстановление алифатических и ароматических нитросоединений. Основной способ синтеза ароматических аминов (анилинов) заключается в восстановлении ароматических нитросоединений. Последние, легко получаются прямым нитрованием соответствующих производных ароматических соединений (см. лекции 4, 5). К числу восстановителей относятся переходные металлы (Zn, Fe) в кислой среде, хлорид олова (II) в кислой среде, а также гидросульфид натрия. Использование Na. HS часто позволяет селективно восстановить одну из нескольких нитрогрупп в молекуле.
Восстановление алифатических и ароматических нитросоединений. Основной способ синтеза ароматических аминов (анилинов) заключается в восстановлении ароматических нитросоединений. Последние, легко получаются прямым нитрованием соответствующих производных ароматических соединений (см. лекции 4, 5). К числу восстановителей относятся переходные металлы (Zn, Fe) в кислой среде, хлорид олова (II) в кислой среде, а также гидросульфид натрия. Использование Na. HS часто позволяет селективно восстановить одну из нескольких нитрогрупп в молекуле.
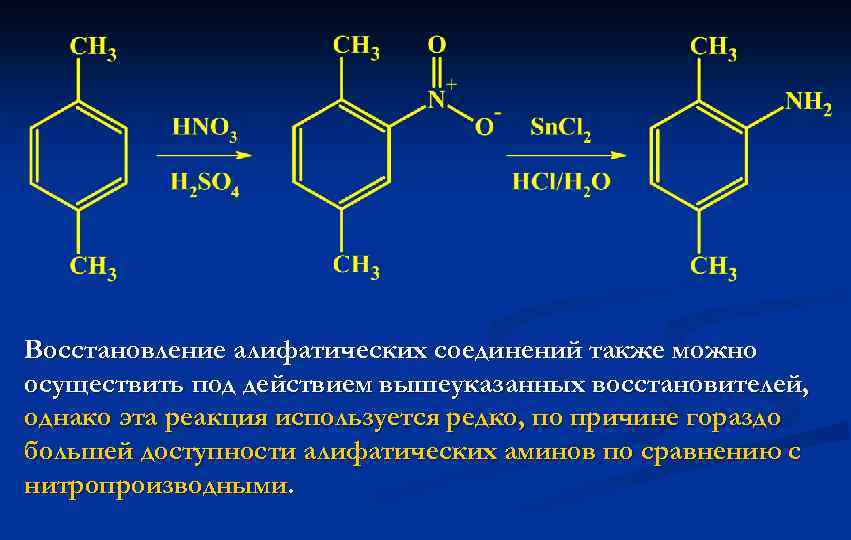 Восстановление алифатических соединений также можно осуществить под действием вышеуказанных восстановителей, однако эта реакция используется редко, по причине гораздо большей доступности алифатических аминов по сравнению с нитропроизводными.
Восстановление алифатических соединений также можно осуществить под действием вышеуказанных восстановителей, однако эта реакция используется редко, по причине гораздо большей доступности алифатических аминов по сравнению с нитропроизводными.
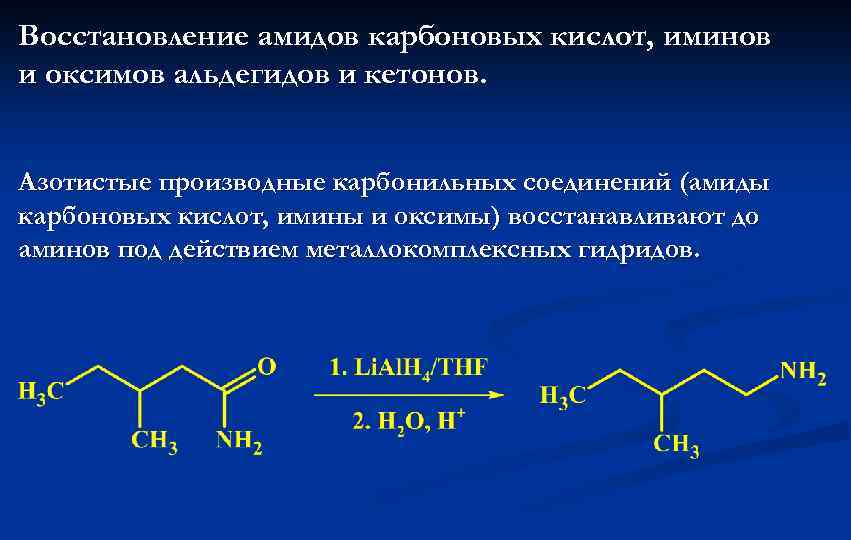 Восстановление амидов карбоновых кислот, иминов и оксимов альдегидов и кетонов. Азотистые производные карбонильных соединений (амиды карбоновых кислот, имины и оксимы) восстанавливают до аминов под действием металлокомплексных гидридов.
Восстановление амидов карбоновых кислот, иминов и оксимов альдегидов и кетонов. Азотистые производные карбонильных соединений (амиды карбоновых кислот, имины и оксимы) восстанавливают до аминов под действием металлокомплексных гидридов.
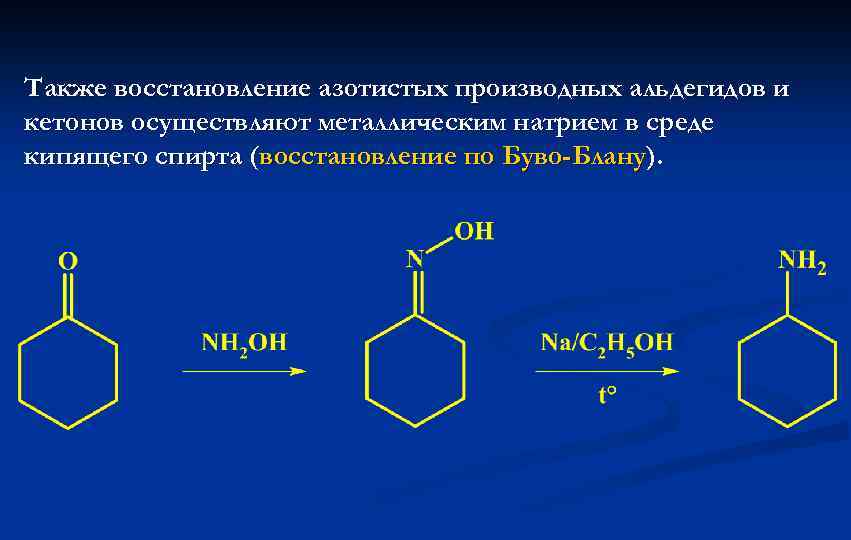 Также восстановление азотистых производных альдегидов и кетонов осуществляют металлическим натрием в среде кипящего спирта (восстановление по Буво-Блану).
Также восстановление азотистых производных альдегидов и кетонов осуществляют металлическим натрием в среде кипящего спирта (восстановление по Буво-Блану).
 Восстановление нитрилов Алифатические нитрилы легко восстанавливаются металлокомплексными гидридами и гидридом алюминия до соответствующих аминов. Исходные нитрилы синтезируют по реакции нуклеофильного замещения из алкилгалогенидов. Следует обратить внимание, что амин получается на один атом углерода длиннее, чем исходный галоидный алкил.
Восстановление нитрилов Алифатические нитрилы легко восстанавливаются металлокомплексными гидридами и гидридом алюминия до соответствующих аминов. Исходные нитрилы синтезируют по реакции нуклеофильного замещения из алкилгалогенидов. Следует обратить внимание, что амин получается на один атом углерода длиннее, чем исходный галоидный алкил.
 Химические свойства алифатических и ароматических аминов. Основность аминов. В отличие от спиртов, способных протонироваться только в сильнокислой среде, амины проявляют ярко выраженные основные свойства. Они являются донорами электронной пары (основания Льюиса), и в частности предоставляют пару электронов на свободную орбиталь Н+ (сродство к протону – основность по Бренстеду).
Химические свойства алифатических и ароматических аминов. Основность аминов. В отличие от спиртов, способных протонироваться только в сильнокислой среде, амины проявляют ярко выраженные основные свойства. Они являются донорами электронной пары (основания Льюиса), и в частности предоставляют пару электронов на свободную орбиталь Н+ (сродство к протону – основность по Бренстеду).
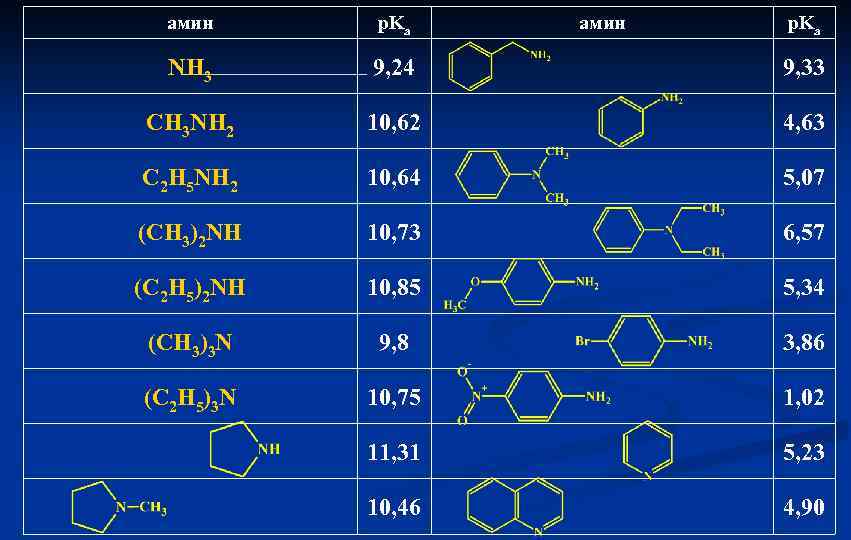 амин p. Ka NH 3 9, 24 9, 33 CH 3 NH 2 10, 62 4, 63 C 2 H 5 NH 2 10, 64 5, 07 (CH 3)2 NH 10, 73 6, 57 (C 2 H 5)2 NH 10, 85 5, 34 (CH 3)3 N 9, 8 3, 86 (C 2 H 5)3 N 10, 75 1, 02 11, 31 5, 23 10, 46 4, 90
амин p. Ka NH 3 9, 24 9, 33 CH 3 NH 2 10, 62 4, 63 C 2 H 5 NH 2 10, 64 5, 07 (CH 3)2 NH 10, 73 6, 57 (C 2 H 5)2 NH 10, 85 5, 34 (CH 3)3 N 9, 8 3, 86 (C 2 H 5)3 N 10, 75 1, 02 11, 31 5, 23 10, 46 4, 90
 Мера основности p. Kb вычисляется как 14–p. Ka, где 14 это обратный логарифм ионного произведения воды –lg[H+][OH-]. Для неводных сред берется соответствующая константа автопротолиза используемого растворителя.
Мера основности p. Kb вычисляется как 14–p. Ka, где 14 это обратный логарифм ионного произведения воды –lg[H+][OH-]. Для неводных сред берется соответствующая константа автопротолиза используемого растворителя.
 Алкилирование аминов, как и получение аминов из аммиака и галоидных алкилов имеет очень ограниченное применение. В основном она используется для получения несимметричных четвертичных аммонийных солей. Последние, действием гидроксида серебра количественно переводятся в соответствующие четвертичные аммонийные основания.
Алкилирование аминов, как и получение аминов из аммиака и галоидных алкилов имеет очень ограниченное применение. В основном она используется для получения несимметричных четвертичных аммонийных солей. Последние, действием гидроксида серебра количественно переводятся в соответствующие четвертичные аммонийные основания.
 Ацилирование аминов Первичные и вторичные амины, аналогично аммиаку, реагируют со сложными эфирами, галогенангидридами и ангидридами кислот с образованием N-замещенных амидов. Третичные алифатические амины не вступают в реакцию с производными карбоновых кислот, а некоторые гетероароматические амины, например пиридин, реагируют с ацилгалогенидами с образованием четвертичных солей.
Ацилирование аминов Первичные и вторичные амины, аналогично аммиаку, реагируют со сложными эфирами, галогенангидридами и ангидридами кислот с образованием N-замещенных амидов. Третичные алифатические амины не вступают в реакцию с производными карбоновых кислот, а некоторые гетероароматические амины, например пиридин, реагируют с ацилгалогенидами с образованием четвертичных солей.
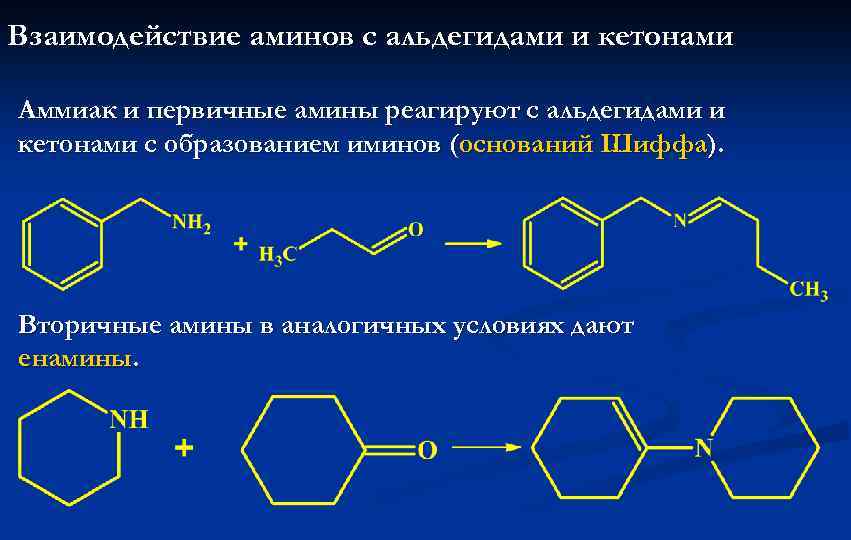 Взаимодействие аминов с альдегидами и кетонами Аммиак и первичные амины реагируют с альдегидами и кетонами с образованием иминов (оснований Шиффа). Вторичные амины в аналогичных условиях дают енамины.
Взаимодействие аминов с альдегидами и кетонами Аммиак и первичные амины реагируют с альдегидами и кетонами с образованием иминов (оснований Шиффа). Вторичные амины в аналогичных условиях дают енамины.
 Взаимодействие алифатических и ароматических аминов с азотистой кислотой. Соли диазония. В зависимости от количества заместителей, первичные алифатические амины в реакциях с азотистой кислотой могут образовывать крайне нестойкие соли диазония, вторичные амины – N-нитрозоамины, третичные амины – Nнитрозоаммонийные соли. По большей части эти реакции носят аналитический характер, так как позволяют с помощью простой качественной реакции различить первичные, вторичные и третичные амины.
Взаимодействие алифатических и ароматических аминов с азотистой кислотой. Соли диазония. В зависимости от количества заместителей, первичные алифатические амины в реакциях с азотистой кислотой могут образовывать крайне нестойкие соли диазония, вторичные амины – N-нитрозоамины, третичные амины – Nнитрозоаммонийные соли. По большей части эти реакции носят аналитический характер, так как позволяют с помощью простой качественной реакции различить первичные, вторичные и третичные амины.
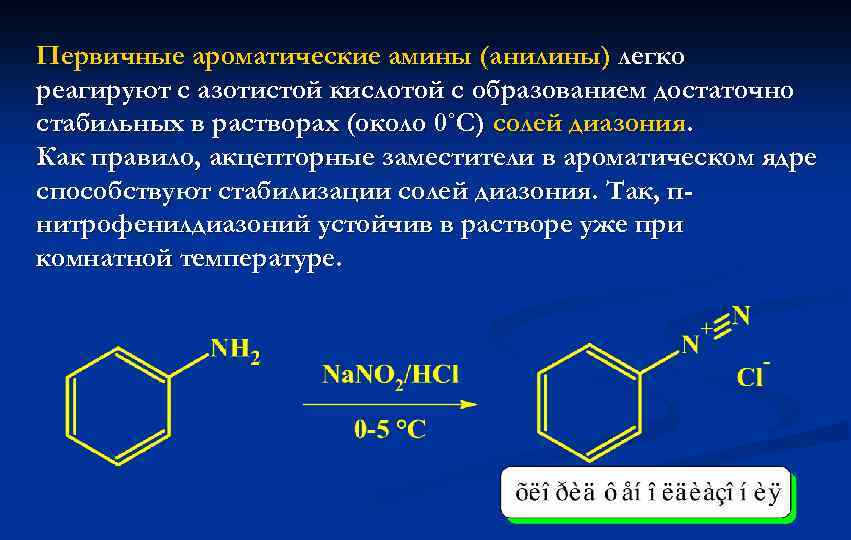 Первичные ароматические амины (анилины) легко реагируют с азотистой кислотой с образованием достаточно стабильных в растворах (около 0˚С) солей диазония. Как правило, акцепторные заместители в ароматическом ядре способствуют стабилизации солей диазония. Так, пнитрофенилдиазоний устойчив в растворе уже при комнатной температуре.
Первичные ароматические амины (анилины) легко реагируют с азотистой кислотой с образованием достаточно стабильных в растворах (около 0˚С) солей диазония. Как правило, акцепторные заместители в ароматическом ядре способствуют стабилизации солей диазония. Так, пнитрофенилдиазоний устойчив в растворе уже при комнатной температуре.
 Соли диазония легко подвергаются нуклеофильному замещению (SNAr), где диазо-группа выступает в роли нуклео-фуга. Эти реак-ции сопровож -даются выделением молекулярного азота.
Соли диазония легко подвергаются нуклеофильному замещению (SNAr), где диазо-группа выступает в роли нуклео-фуга. Эти реак-ции сопровож -даются выделением молекулярного азота.
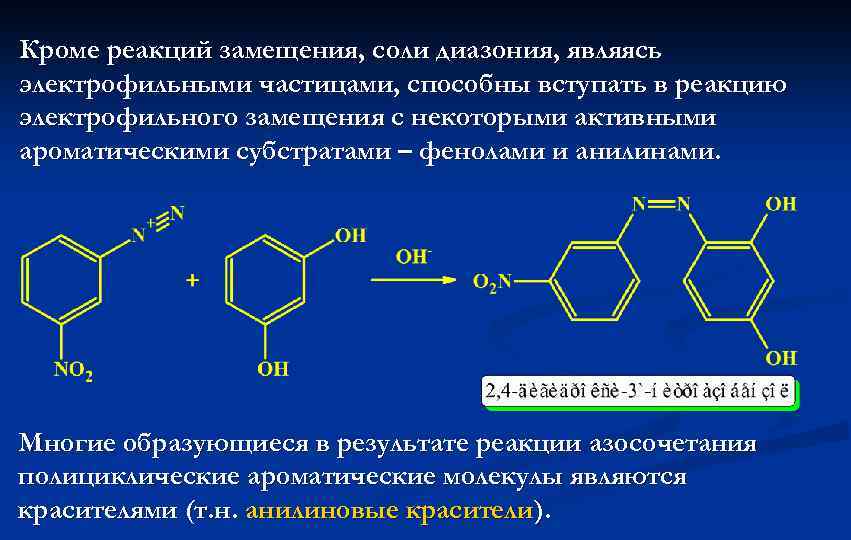 Кроме реакций замещения, соли диазония, являясь электрофильными частицами, способны вступать в реакцию электрофильного замещения с некоторыми активными ароматическими субстратами – фенолами и анилинами. Многие образующиеся в результате реакции азосочетания полициклические ароматические молекулы являются красителями (т. н. анилиновые красители).
Кроме реакций замещения, соли диазония, являясь электрофильными частицами, способны вступать в реакцию электрофильного замещения с некоторыми активными ароматическими субстратами – фенолами и анилинами. Многие образующиеся в результате реакции азосочетания полициклические ароматические молекулы являются красителями (т. н. анилиновые красители).
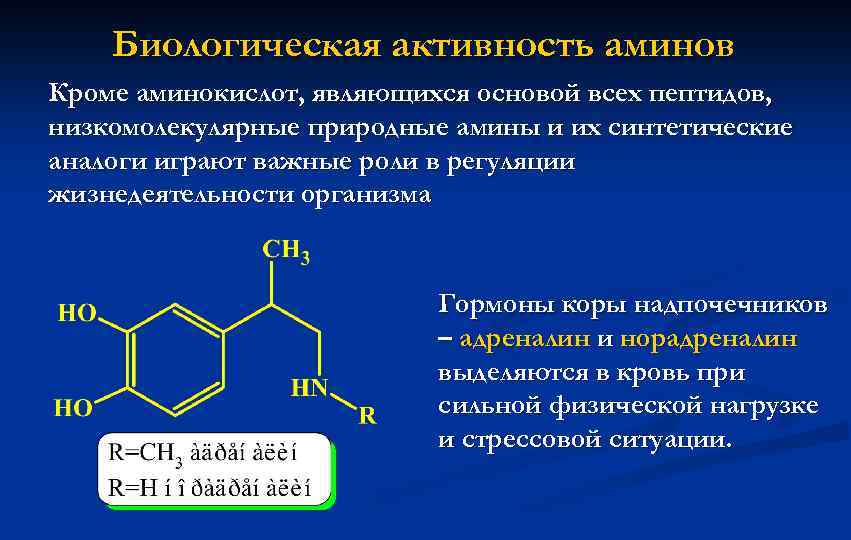 Биологическая активность аминов Кроме аминокислот, являющихся основой всех пептидов, низкомолекулярные природные амины и их синтетические аналоги играют важные роли в регуляции жизнедеятельности организма Гормоны коры надпочечников – адреналин и норадреналин выделяются в кровь при сильной физической нагрузке и стрессовой ситуации.
Биологическая активность аминов Кроме аминокислот, являющихся основой всех пептидов, низкомолекулярные природные амины и их синтетические аналоги играют важные роли в регуляции жизнедеятельности организма Гормоны коры надпочечников – адреналин и норадреналин выделяются в кровь при сильной физической нагрузке и стрессовой ситуации.
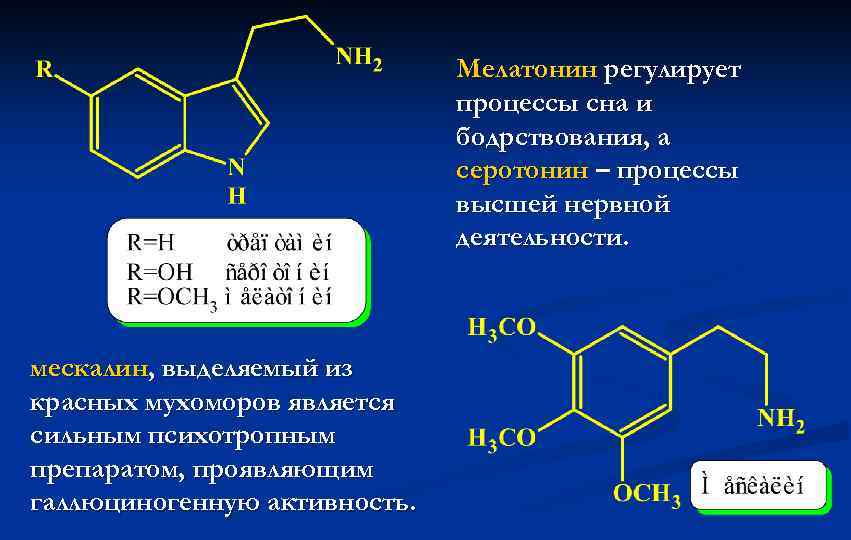 Мелатонин регулирует процессы сна и бодрствования, а серотонин – процессы высшей нервной деятельности. мескалин, выделяемый из красных мухоморов является сильным психотропным препаратом, проявляющим галлюциногенную активность.
Мелатонин регулирует процессы сна и бодрствования, а серотонин – процессы высшей нервной деятельности. мескалин, выделяемый из красных мухоморов является сильным психотропным препаратом, проявляющим галлюциногенную активность.
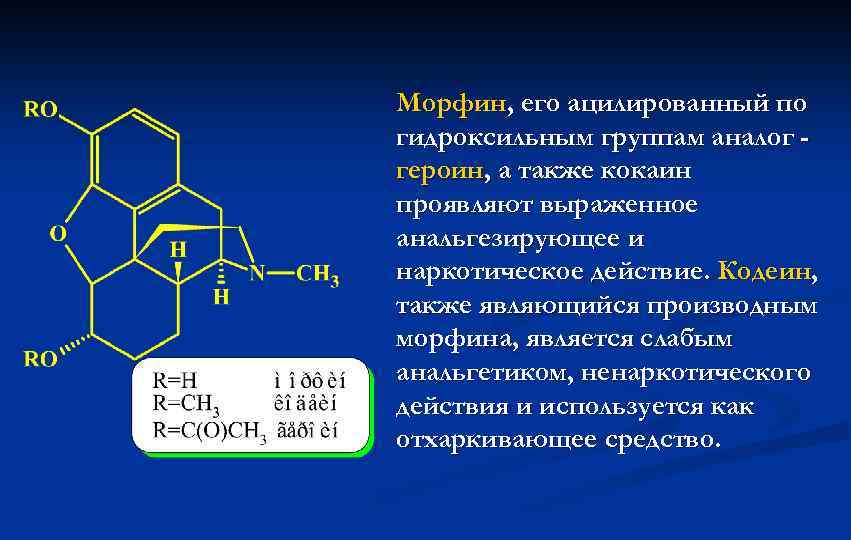 Морфин, его ацилированный по гидроксильным группам аналог героин, а также кокаин проявляют выраженное анальгезирующее и наркотическое действие. Кодеин, также являющийся производным морфина, является слабым анальгетиком, ненаркотического действия и используется как отхаркивающее средство.
Морфин, его ацилированный по гидроксильным группам аналог героин, а также кокаин проявляют выраженное анальгезирующее и наркотическое действие. Кодеин, также являющийся производным морфина, является слабым анальгетиком, ненаркотического действия и используется как отхаркивающее средство.
 На основе структурного ядра природного кокаина разработан целый ряд синтетических анальгетиков – новокаин, фентанил и др. К производным аминов относятся также витамины В 1, В 6 и РР (никотиновая кислота).
На основе структурного ядра природного кокаина разработан целый ряд синтетических анальгетиков – новокаин, фентанил и др. К производным аминов относятся также витамины В 1, В 6 и РР (никотиновая кислота).


