LecSS-9(2012).ppt
- Количество слайдов: 46

Лекция-9 Адсорбция

Лекция-9 Адсорбция -от латинского sorbco (поглощение) и приставки ad (т. е. над или у) и означает поглощение, точнее концентрирование каких – либо компонентов из объема гомогенных сопредельных фаз на поверхности раздела этих фаз. -адсорбированные молекулы взаимодействуют с молекулами или атомами поверхности и снижают как свободную поверхностную энергию конденсированной фазы, так и суммарную энергию системы, т. о. : -адсорбция самопроизвольный выделением тепла. процесс, происходит с

Лекция-9 Абсорбция – концентрирование компонента в объеме конденсированной фазы, синоним растворения, но включает растворение как в жидкости, так и в твердой фазе. Сорбция – обобщение детального механизма. термина поглощение без уточнения Десорбция – процесс, обратный адсорбции. Адсорбент или сорбент (IUPAC) – вещество, на котором происходит адсорбция. Адсорбтив или сорбтив (IUPAC) – вещество, способное адсорбироваться, но еще не адсорбированное. Адсорбат или сорбат (IUPAC) – уже адсорбированное вещество, находящееся на поверхности или в объеме пор адсорбента.
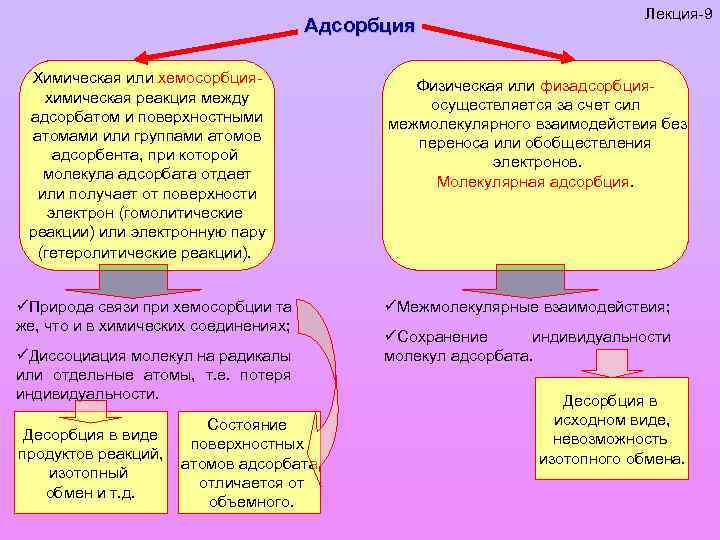
Адсорбция Химическая или хемосорбцияхимическая реакция между адсорбатом и поверхностными атомами или группами атомов адсорбента, при которой молекула адсорбата отдает или получает от поверхности электрон (гомолитические реакции) или электронную пару (гетеролитические реакции). üПрирода связи при хемосорбции та же, что и в химических соединениях; üДиссоциация молекул на радикалы или отдельные атомы, т. е. потеря индивидуальности. Десорбция в виде продуктов реакций, изотопный обмен и т. д. Состояние поверхностных атомов адсорбата отличается от объемного. Лекция-9 Физическая или физадсорбцияосуществляется за счет сил межмолекулярного взаимодействия без переноса или обобществления электронов. Молекулярная адсорбция. üМежмолекулярные взаимодействия; üСохранение индивидуальности молекул адсорбата. Десорбция в исходном виде, невозможность изотопного обмена.
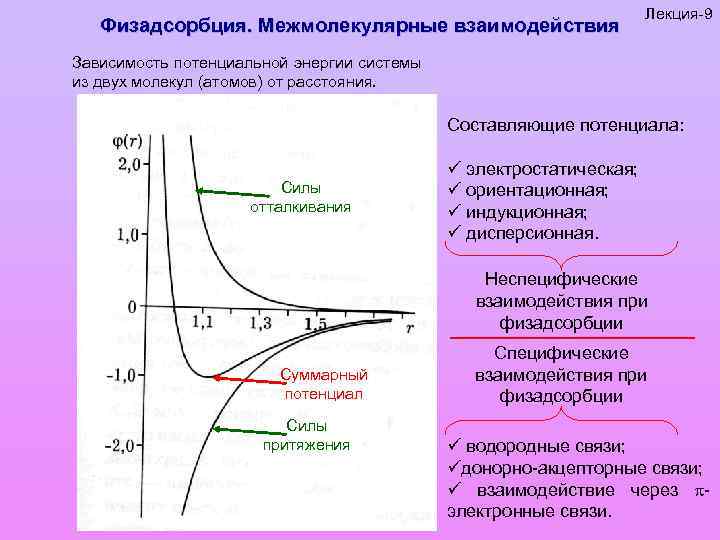
Физадсорбция. Межмолекулярные взаимодействия Лекция-9 Зависимость потенциальной энергии системы из двух молекул (атомов) от расстояния. Составляющие потенциала: Силы отталкивания ü электростатическая; ü ориентационная; ü индукционная; ü дисперсионная. Неспецифические взаимодействия при физадсорбции Суммарный потенциал Силы притяжения Специфические взаимодействия при физадсорбции ü водородные связи; üдонорно-акцепторные связи; ü взаимодействие через электронные связи.
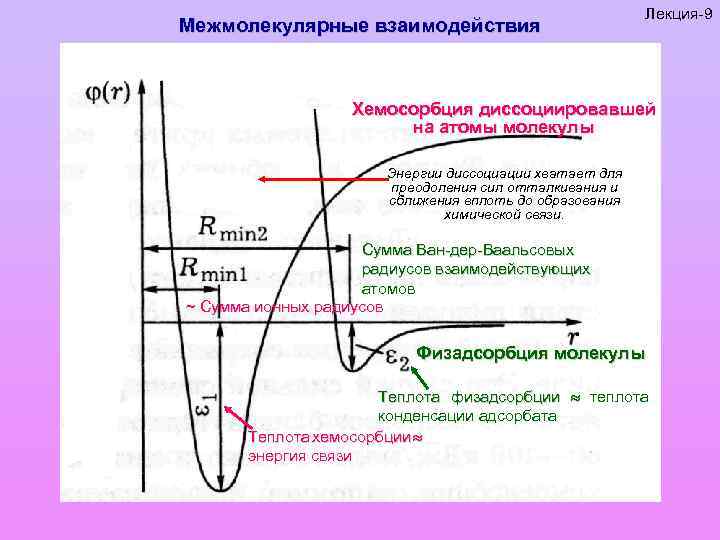
Межмолекулярные взаимодействия Лекция-9 Хемосорбция диссоциировавшей на атомы молекулы Энергии диссоциации хватает для преодоления сил отталкивания и сближения вплоть до образования химической связи. Сумма Ван-дер-Ваальсовых радиусов взаимодействующих атомов ~ Сумма ионных радиусов Физадсорбция молекулы Теплота физадсорбции теплота конденсации адсорбата Теплота хемосорбции энергия связи
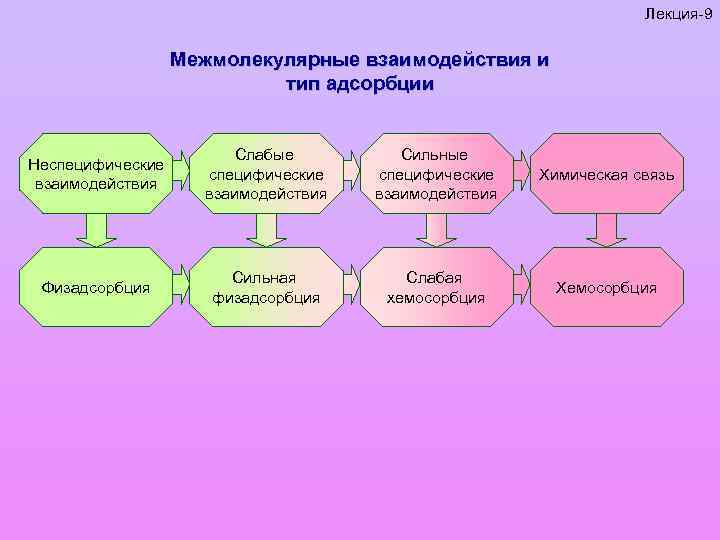
Лекция-9 Межмолекулярные взаимодействия и тип адсорбции Неспецифические взаимодействия Слабые специфические взаимодействия Сильные специфические взаимодействия Химическая связь Физадсорбция Сильная физадсорбция Слабая хемосорбция Хемосорбция

Сравнение физадсорбции и хемосорбции Физадсорбция Хемосорбция Природа взаимодействия Межмолекулярные силы Химическая связь Диссоциация, сохранение индивидуальности Нет диссоциации, индивидуальность сохраняется Диссоциация, потеря индивидуальности Участие в изотопном обмене - + Возмущение поверхностных атомов Слабые. В первом приближении – поверхность инертна Вплоть до реконструкции Лекция-9
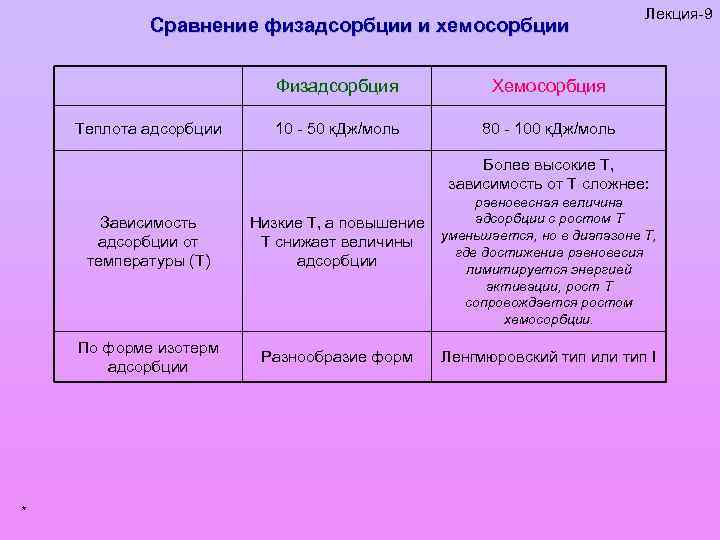
Сравнение физадсорбции и хемосорбции Физадсорбция Теплота адсорбции Хемосорбция 10 - 50 к. Дж/моль Лекция-9 80 - 100 к. Дж/моль Более высокие Т, зависимость от Т сложнее: Зависимость адсорбции от температуры (Т) По форме изотерм адсорбции * Низкие Т, а повышение Т снижает величины адсорбции Разнообразие форм равновесная величина адсорбции с ростом Т уменьшается, но в диапазоне Т, где достижение равновесия лимитируется энергией активации, рост Т сопровождается ростом хемосорбции. Ленгмюровский тип или тип I

Лекция-9 Процессы на поверхности адсорбента «Бомбардировка» поверхности Поверхность твердого тела, находящегося при температуре Т в контакте с газом при давлении Р, непрерывно бомбардируется молекулами газа. Число соударений молекул газа с поверхностью за единицу времени: n = NAP/[2 MRT]1/2, Где NА – число Авогадро, М – молекулярный вес, R – газовая постоянная. Коэффициент прилипания - доля атомов, «задерживающихся» адсорбирующихся на поверхности, от общего числа соударений. Адсорбция – избыточное содержание молекул приповерхностном слое за счет «задержавшихся» молекул. в При малых покрытиях среднее число молекул, адсорбированных на единице поверхности Г: Г = n , Где - среднее время пребывания молекулы в адсорбированном состоянии.

Процессы на поверхности адсорбента Лекция-9 Среднее время пребывания молекулы в адсорбированном состоянии (Я. Френкель, 1924 г. ) зависит от теплоты десорбции Qд: = 0 exp(Qд/RT) 0 – выражается через статистические суммы для адсорбата и активированного комплекса, но обычно принимается 0 1/ с 10 -13 с, где с величина порядка частоты колебания химической связи. Физадсорбция при 293 К Хемосорбция при 293 К Qд, к. Дж/моль 40 -60 доли секунд 80 -100 часы

Основные понятия адсорбции на пористых телах Лекция-9 Величина адсорбции компонентов – а = (Р, Т …) – используются удельные величины адсорбции с размерностью ммоль адсорбата/г адсорбента, нсм 3 адсорбированного газа/г адсорбента, см 3 жидкости/г адсорбента, также используется отнесение к единице поверхности адсорбента и т. д. Термическое уравнение однокомпонентной сорбции (Р, Т, а) = 0 – определяет некоторую поверхность в пространстве Р-Т-а, сечение этой поверхности плоскостями, проведенными при Т = const – изотерма, Р = const – изобара, а = const – изостера. Изотерма адсорбции – зависимость равновесной величина адсорбции а от давления Р при T = const. Изобара адсорбции – зависимость равновесных величин адсорбции от Т при P = const. Изостера адсорбции – зависимость равновесного давления от Т при a = const.
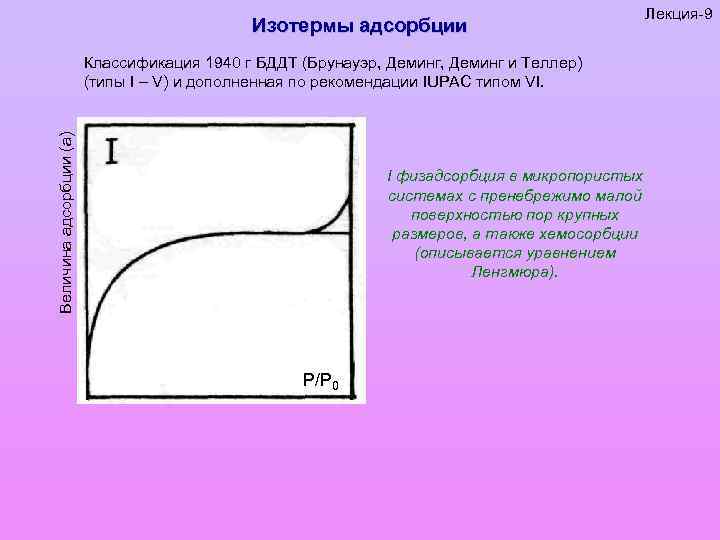
Изотермы адсорбции Величина адсорбции (а) Классификация 1940 г БДДТ (Брунауэр, Деминг и Теллер) (типы I – V) и дополненная по рекомендации IUPAC типом VI. I физадсорбция в микропористых системах с пренебрежимо малой поверхностью пор крупных размеров, а также хемосорбции (описывается уравнением Ленгмюра). P/P 0 Лекция-9
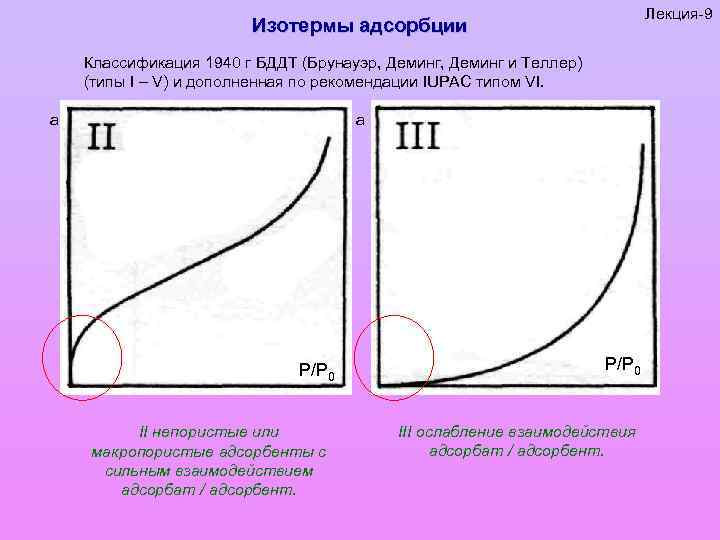
Лекция-9 Изотермы адсорбции Классификация 1940 г БДДТ (Брунауэр, Деминг и Теллер) (типы I – V) и дополненная по рекомендации IUPAC типом VI. а а P/P 0 II непористые или макропористые адсорбенты с сильным взаимодействием адсорбат / адсорбент. P/P 0 III ослабление взаимодействия адсорбат / адсорбент.
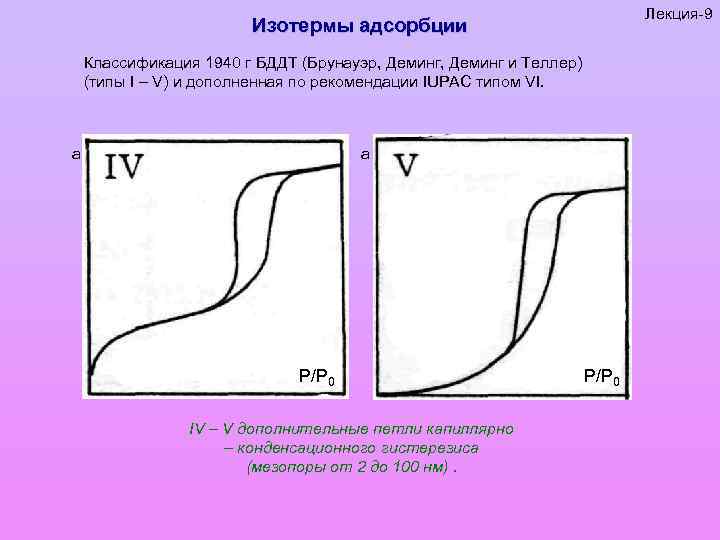
Лекция-9 Изотермы адсорбции Классификация 1940 г БДДТ (Брунауэр, Деминг и Теллер) (типы I – V) и дополненная по рекомендации IUPAC типом VI. а а P/P 0 IV – V дополнительные петли капиллярно – конденсационного гистерезиса (мезопоры от 2 до 100 нм). P/P 0
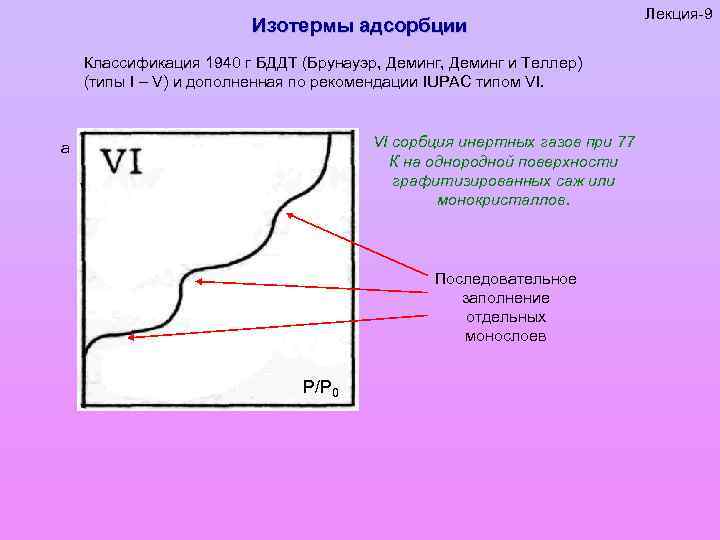
Изотермы адсорбции Классификация 1940 г БДДТ (Брунауэр, Деминг и Теллер) (типы I – V) и дополненная по рекомендации IUPAC типом VI. VI сорбция инертных газов при 77 К на однородной поверхности графитизированных саж или монокристаллов. а Последовательное заполнение отдельных монослоев P/P 0 Лекция-9
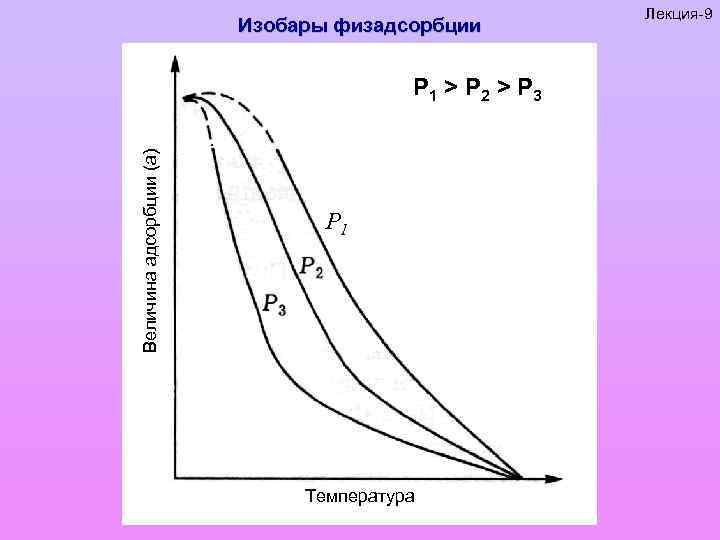
Изобары физадсорбции Величина адсорбции (а) Р 1 > P 2 > P 3 Р 1 Температура Лекция-9
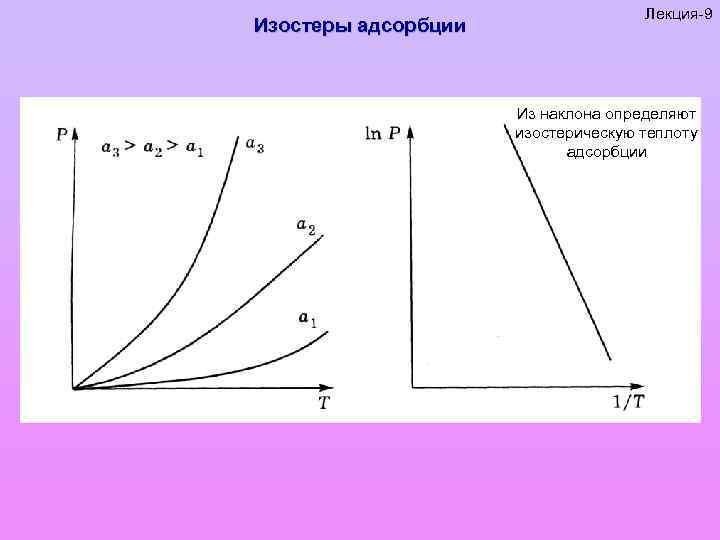
Изостеры адсорбции Лекция-9 Из наклона определяют изостерическую теплоту адсорбции

Изотермы адсорбции Изотерма адсорбции Генри Изотерма применима при минимальных заполнениях поверхности и малых давлениях, когда газ рассматривается как идеальный, а число соударений с поверхностью, не занятой другими адсорбированными молекулами, n пропорционально Р: Г = n 0 exp(Q/RT) = Kг. Р, Где Г – величина адсорбции, отнесенная к единице поверхности, Кг – константа Генри. Лекция-9

Изотермы адсорбции Изотерма адсорбции Ленгмюра Уравнение мономолекулярной адсорбции на однородной поверхности, полученное без учета взаимодействия адсорбат – адсорбат. Квазихимическая реакция между молекулой адсорбата М и активным центром Z на поверхности адсорбента с формированием локализованного адсорбционного комплекса [MZ]: М + [Z] [MZ] P (1 - ) = Г/Гmax= a/a 0 Константа равновесия этой реакции: К = /(Р(1 - )) = КР/(1+КР) = Г/Гmax a = a 0 КР/(1+КР) К=g exp(Q/RT) Где а и а 0 – соответствующие величины адсорбции, g – энтропийный множитель, Q – теплота адсорбции. Лекция-9
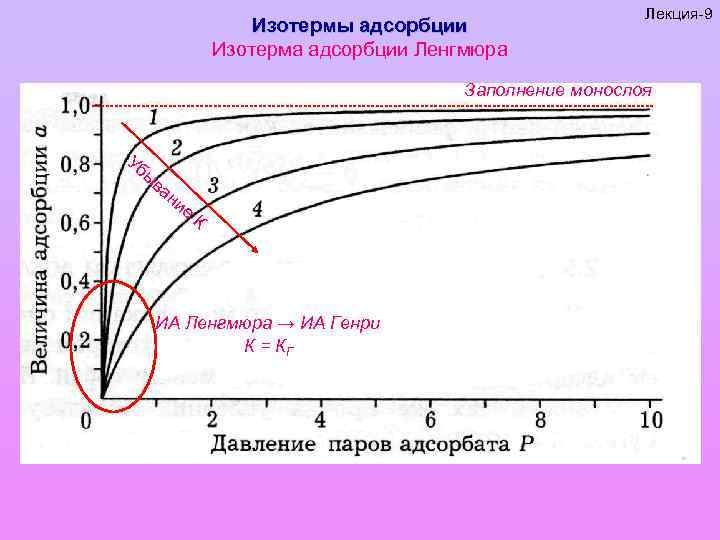
Изотермы адсорбции Изотерма адсорбции Ленгмюра Лекция-9 Заполнение монослоя Уб ыв а ни е К ИА Ленгмюра → ИА Генри К = КГ

Изотермы адсорбции Изотерма адсорбции Ленгмюра Лекция-9 Конкурентная адсорбция смеси компонентов: параллельные реакции взаимодействия А и В со свободными местами поверхности Агаз + [Z] [АZ] Вгаз + [Z] [ВZ] Константы равновесия соответствующих реакций: КА = А/(РА(1 - А- В)) и КВ = В/(РВ(1 - А- В)) А/ В = КАРА/КВРВ А = КАРА/[1+КАРА+КВРВ] и В = КВРВ/[1+КАРА+КВРВ]

Изотермы адсорбции Изотерма адсорбции Ленгмюра Одновременная адсорбция i – компонентов: Степень покрытия поверхности i-м компонентом: i = Кi. Рi/[1+ i. Кi. Рi] Суммарная степень покрытия поверхности всеми компонентами: = i. Кi. Рi/[1+ i. Кi. Рi] Хемосорбция, сопровождающаяся диссоциацией молекул на два фрагмента, каждый из которых занимает один отдельный центр: = (КР)1/2/[1+(КР)1/2] Лекция-9
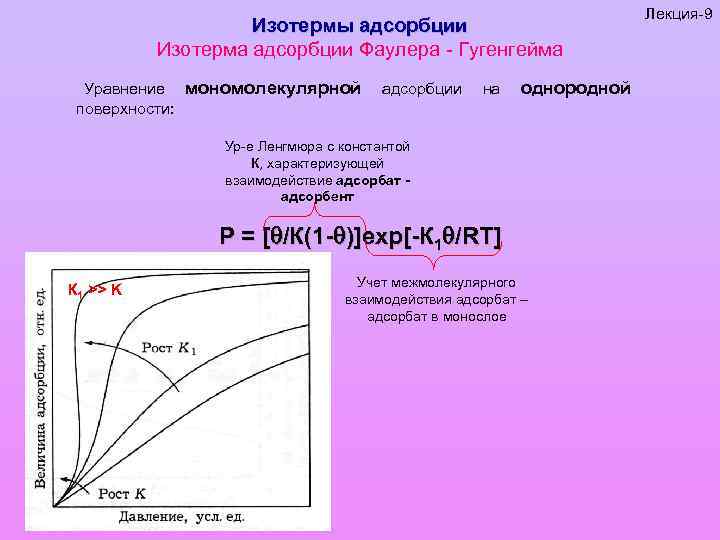
Изотермы адсорбции Изотерма адсорбции Фаулера - Гугенгейма Уравнение мономолекулярной поверхности: адсорбции на однородной Ур-е Ленгмюра с константой К, характеризующей взаимодействие адсорбат адсорбент Р = [ /К(1 - )]exp[-К 1 /RT] К 1 >> K Учет межмолекулярного взаимодействия адсорбат – адсорбат в монослое Лекция-9
![Полимолекулярная адсорбция Изотерма адсорбции Френкеля – Хелси – Хилла (ФХХ) = В 1[RTln(P/P 0)]-n Полимолекулярная адсорбция Изотерма адсорбции Френкеля – Хелси – Хилла (ФХХ) = В 1[RTln(P/P 0)]-n](https://present5.com/presentation/3/-42749098_135478355.pdf-img/-42749098_135478355.pdf-25.jpg)
Полимолекулярная адсорбция Изотерма адсорбции Френкеля – Хелси – Хилла (ФХХ) = В 1[RTln(P/P 0)]-n t = B 2[RTln(P/P 0)]-n Где t – среднестатистическая толщина полимолекулярной пленки адсорбата на поверхности адсорбента, получаемая делением объема адсорбата на величину поверхности адсорбента. Плотность адсорбата обычно отождествляется с плотностью его нормальной жидкой фазы. Уравнение записано в форме: t = 5. 27 ln(P/P 0)]-0. 3109 Лекция-9
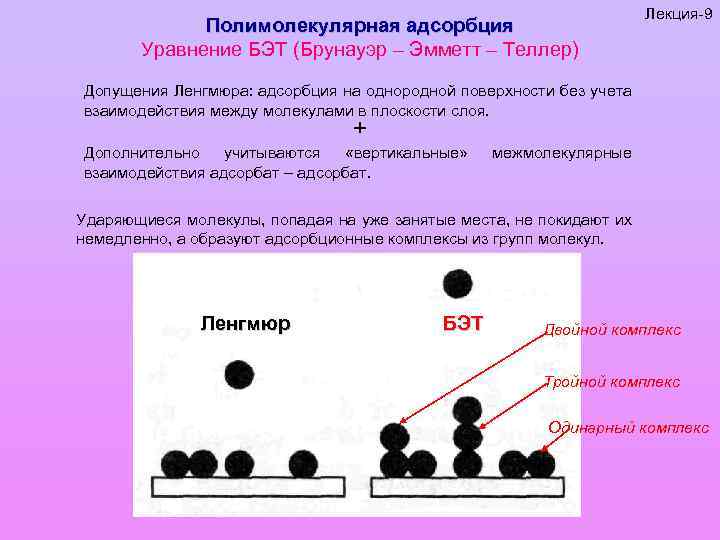
Полимолекулярная адсорбция Уравнение БЭТ (Брунауэр – Эмметт – Теллер) Лекция-9 Допущения Ленгмюра: адсорбция на однородной поверхности без учета взаимодействия между молекулами в плоскости слоя. + Дополнительно учитываются «вертикальные» взаимодействия адсорбат – адсорбат. межмолекулярные Ударяющиеся молекулы, попадая на уже занятые места, не покидают их немедленно, а образуют адсорбционные комплексы из групп молекул. Ленгмюр БЭТ Двойной комплекс Тройной комплекс Одинарный комплекс

Полимолекулярная адсорбция Уравнение БЭТ (Брунауэр – Эмметт – Теллер) 1, 2, 3, 4 и т. д. – доля поверхности, занятая единичными, двойными, тройными и т. д. комплексами. Общая величина адсорбции: а = аm( 1 + 2 + 3 + 4 + …) Где аm – емкость плотного монослоя. Выражения для констант квазихимических реакций: равновесия соответствующих К 1 = 1/(Р 0); К 2 = 2/(Р 1); К 3 = 3/(Р 2), Где 0 – доля свободной поверхности. К 1 >> K 2 K 3 К 4…, так как сила взаимодействия быстро убывает по мере увеличения расстояния от поверхности. Лекция-9

Полимолекулярная адсорбция Уравнение БЭТ (Брунауэр – Эмметт – Теллер) Лекция-9 Принимают К 2 = К 3 = К 4 = … = КL = 1/P 0 (где Р 0 – давление насыщенных паров жидкой фазы адсорбтива при данной температуре): 1 = К 1 Р 0; 2 = К 2 Р 1 = КLP 1 = (P/P 0)1 1; 3 = К 3 Р 2 = (КLP)2 2 = (P/P 0)2 1; Суммарная величина сорбции (Р/Р 0=h): a = am. K 1 P 0[1+2 h+3 h 2+…+nhn-1]; Баланс заполнения поверхности: 0 + 1 + 2 + 3 + 4 + … = 0{1+K 1 P[1+h+h 2+…+hn]} = 1 геометр. прогрессия Учитывая KL = 1/P 0 и K 1/KL = C: Уравнение БЭТ 1/(1 -h) a = am. Ch/{[1 – h][1 + (C – 1)h]}

Лекция-9 Полимолекулярная адсорбция Форма изотермы полимолекулярной адсорбции, соответствующая модели БЭТ

Полимолекулярная адсорбция Уравнение БЭТ (Брунауэр – Эмметт – Теллер) Линейная форма: Y = h/a(1 – h) = 1/(am. C) + (C – 1)h/(am. C) аm – емкость заполненного монослоя; CБЭТ ~ eΔS/R e(Q-L)/RT – энергетическая константа; Q-L – чистая теплота адсорбции, где Q – изостерическая теплота адсорбции и L – теплота конденсации чистого адсорбтива в жидкость. Лекция-9

Полимолекулярная адсорбция Уравнение БЭТ (Брунауэр – Эмметт – Теллер) Лекция-9 Удельная поверхность адсорбента в м 2/г: A = am. NAω Из БЭТ Число Авогадро Площадка, приходящаяся на одну молекулу в заполненном монослое на поверхности адсорбента. ω = [π/4(1 – εS)][(M/(NAρ))(1 – εV)6/π]2/3 Где εS – свободный межмолекулярный объем фазы адсорбата, равный отношению объема промежутков между молекулами к суммарному объему, занимаемому адсорбатом; εV – «двумерная порозноть» монослоя, равная отношению суммарной площади участков между проекциями молекул на поверхности к суммарной поверхности, занятой монослоем; M – молекулярный вес адсорбата; ρ – плотность адсорбата при температуре эксперимента. Общепринятый стандарт – адсорбция азота при 77 К ω = 1. 091(M/(NAρ))2/3 ωN 2 = 0. 162 нм 2

Адсорбция в пористых телах Тип пор Характеристика Характерный размер* Теплота адсорбции Особенности адсорбции Микропоры ультрамикропоры 2 -5 молекулярных диаметра Мезопоры Макропоры от 2 до 50 нм > 50 нм супермикропоры ~два молекулярных диаметра Лекция-9 Выше теплоты конденсации соответствующего адсорбата в жидкость Заполнение пор без образования монослоя на поверхности пор Сначала формируется монослойное покрытие, затем спонтанное объемное заполнение по кооперативному механизму Близка к теплоте конденсации соответствующего адсорбата в жидкость Моно- и полимолекулярная адсорбция, а затем объемное заполнение по механизму капиллярной конденсации. Обратимая моно -и полимолекулярная адсорбция. *Диаметр наибольшей окружности, которая может быть вписана в плоское сечение поры произвольной формы.

Капиллярная конденсация Лекция-9 Объемное заполнение мезопор пористых систем жидкой фазой адсорбата при относительном давлении паров Р/Р 0 < 1. 0 при условиях: ü наличие мезопор; ü смачивание стенок пор адсорбированной фазой; ü температура сорбции ниже критической. ПРИЧИНА КК: Образование вогнутых менисков адсорбированной фазы, равновесное давление Р над которыми определяется уравнением Кельвина, где rк – равновесное значение кельвиновского радиуса кривизны: Р/Р 0 = exp[-2 Vm/(rк. RT)]. КК начинает проявляться, когда избыточная поверхностная энергия адсорбента скомпенсирована и определяющими становятся взаимодействия адсорбат – адсорбат. ФОРМЫ КК: Обратимая Адсорбционная и десорбционная ветви ИА совпадают. Необратимая Гистерезис – несовпадение адсорбционной и десорбционной ветвей ИА.
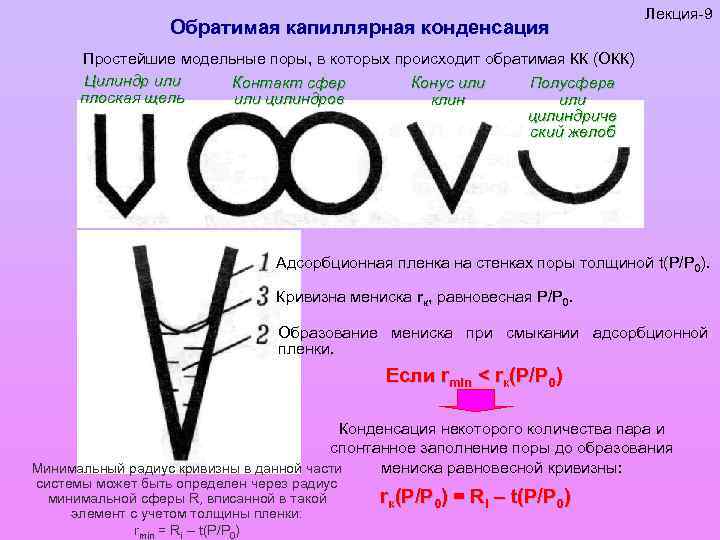
Обратимая капиллярная конденсация Лекция-9 Простейшие модельные поры, в которых происходит обратимая КК (ОКК) Цилиндр или Контакт сфер Конус или Полусфера плоская щель или цилиндров клин или цилиндриче ский желоб Адсорбционная пленка на стенках поры толщиной t(P/P 0). Кривизна мениска rк, равновесная Р/Р 0. Образование мениска при смыкании адсорбционной пленки. Если rmin < rк(Р/Р 0) Конденсация некоторого количества пара и спонтанное заполнение поры до образования мениска равновесной кривизны: Минимальный радиус кривизны в данной части системы может быть определен через радиус минимальной сферы R, вписанной в такой элемент с учетом толщины пленки: rmin = Ri – t(P/P 0) rк(Р/Р 0) = Ri – t(P/P 0)
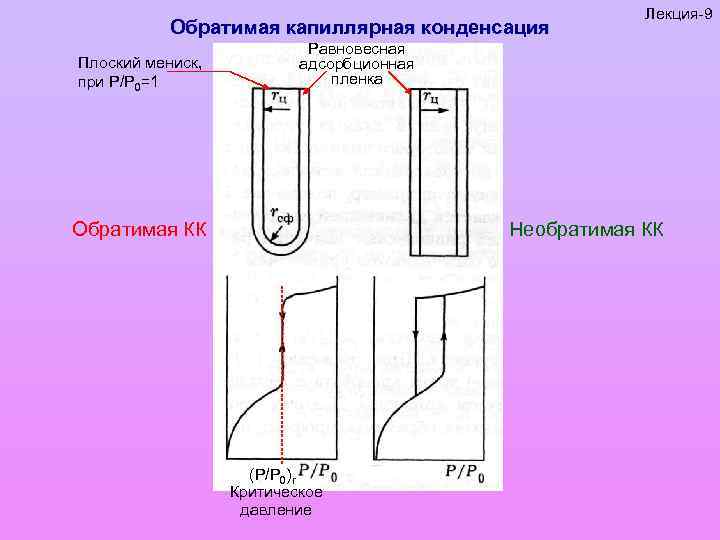
Обратимая капиллярная конденсация Плоский мениск, при Р/Р 0=1 Лекция-9 Равновесная адсорбционная пленка Обратимая КК Необратимая КК (P/P 0)r Критическое давление

Спонтанная КК Рост Р/Р 0 ~ 0. 75 Снижение Р/Р 0 rк = 2 Rц : Давление, при rк = Rс : Давление, при котором происходит освобождение пор, заполнение, определяется радиусом кривизны цилиндра. кривизны сферического мениска. Спонтанная десорбция Полимолекулярная адсорбционная пленка Мономолекулярная адсорбционная пленка Лекция-9 Адсорбция Аргона в цилиндрическом капилляре графита диаметром 4. 78 нм при 77 К, рассчитанная методом Монте-Карло Необратимая капиллярная конденсация
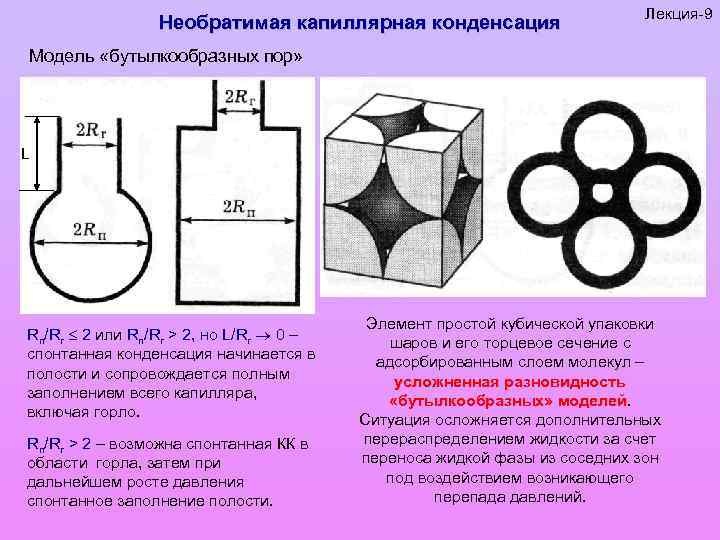
Необратимая капиллярная конденсация Лекция-9 Модель «бутылкообразных пор» L Rп/Rг 2 или Rп/Rг > 2, но L/Rг 0 – спонтанная конденсация начинается в полости и сопровождается полным заполнением всего капилляра, включая горло. Rп/Rг > 2 – возможна спонтанная КК в области горла, затем при дальнейшем росте давления спонтанное заполнение полости. Элемент простой кубической упаковки шаров и его торцевое сечение с адсорбированным слоем молекул – усложненная разновидность «бутылкообразных» моделей Ситуация осложняется дополнительных перераспределением жидкости за счет переноса жидкой фазы из соседних зон под воздействием возникающего перепада давлений.
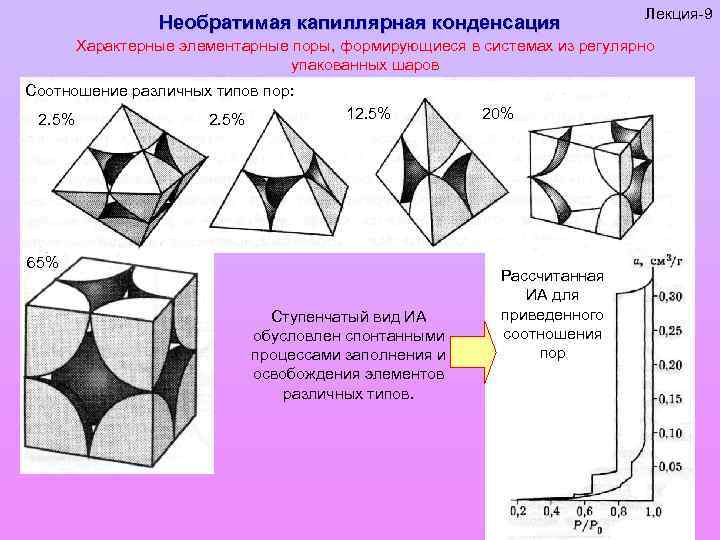
Необратимая капиллярная конденсация Лекция-9 Характерные элементарные поры, формирующиеся в системах из регулярно упакованных шаров Соотношение различных типов пор: 2. 5% 12. 5% 65% Ступенчатый вид ИА обусловлен спонтанными процессами заполнения и освобождения элементов различных типов. 20% Рассчитанная ИА для приведенного соотношения пор

Капиллярная конденсация. Гистерезис Лекция-9 Классификация петель КК гистерезиса, рекомендованная IUPAC Агломераты или Глобулярные Адсорбенты с щелевидными порами. таблетки из системы, например, Наличие микропор. Адсорбенты, сферических частиц силикагели, образованные – глобул, однородно распределение и плоскопаралупакованных и форма пор близких по размеру. неоднозначны. лельными частицами.

Расчет распределения мезопор по ИА Метод PSD (Pore Size Distribution) Используется модель индивидуальных пор простейшей формы: прямые цилиндры с дном и без; плоские щели; поры между регулярно упакованными монодисперсными глобулами. Диапазон размеров: от 3 до 50 – 100 нм. Расчеты базируются на модификациях численного решения уравнения Уилера для баланса объема при адсорбции и десорбции в системе непересекающихся капилляров постоянного сечения: V(r) = Vs - (r-t)3 L(r)dr, L(r)dr R Где V(r) – объем пор с размерами r R, где R = R(P/P 0) – функция, задаваемая уравнением Кельвина; Vs – суммарный объем пор, определяемый по предельно достигнутой величине адсорбции (предполагается, что к этому моменту все поры заполнены); L(r) – суммарная длина капилляров с радиусами r + dr; t - толщина адсорбционной пленки на поверхности, задаваемая как функция t(P/P 0). Лекция-9

Расчет распределения мезопор по ИА Метод PSD (Pore Size Distribution) V(r) = Vs - (r-t)3 L(r)dr, (r-t)3 L(r)dr R Функция L(r) обычно заменяется эквивалентным выражением A(r)/2 r или V(r)/r 2, где A(r) – геометрическая поверхность пор с размерами r R. Интегрирование на практике заменяют суммами. Алгоритм: 1. Выбирается адсорбционная или десорбционная ветвь ИА. 2. Экспериментальная ИА разбивается на интервалы. 3. Для каждого интервала рассчитывается среднее значение r. 4. Оценивается вклад полимолекулярной адсорбции на стенках освобожденных пор (t(P/P 0)). Уравнение Кельвина для идеально сферических менисков при адсорбции азота при 77 К: r. К = 0. 4078/lg(P 0/P) [нм] Лекция-9

Расчет распределения мезопор по ИА Метод PSD (Pore Size Distribution) Уравнение Кельвина для идеально сферических менисков при адсорбции азота при 77 К: r. К = 0. 4078/lg(P 0/P) [нм] ИА (десорбционная ветвь) разбивается на интервалы по оси давлений, для них рассчитывается средний кельвиновский радиус: 1 шаг. Десорбция из пор наибольшего размера: R = r. K(P/P 0) + t(P/P 0). 2 шаг. Учитывается десорбция как из сердцевины освобождающихся капилляров с радиусом r. K(P/P 0), так и из истоньшающейся адсорбционной пленки. И так для каждого интервала. 3 шаг. При заданной модельной форме капилляров и известному из ИА десорбированному объему рассчитывается геометрическая поверхность и объем капилляров. Графики кумулятивного (интегрального) и дифференциального распределения объема и поверхности пор по радиусам соответствующих модельных элементов (например, цилиндров). Лекция-9

Расчет распределения мезопор по ИА Метод PSD (Pore Size Distribution) Лекция-9 PSD расчет ИА, измеренная на механической смеси двух пористых тел с узким распределением пор по размерам По десорбционной ветви ИА По адсорбционной ветви ИА

Особенности КК в системе взаимосвязанных пор Реальные пористые тела: трехмерный статистический лабиринт из пересекающихся пор разных размеров и форм с чередующимися сужениями и расширениями. У каждой поры появляется Z – окон (горл), связывающих пору с соседней полостью. Чем больше Z, тем позже, т. е. при более высоком Р/Р 0, происходит спонтанное заполнение полости даже при одинаковом размере пор. Формально рассчитанный по уравнению Кельвина размер будет выше, чем заданный при моделировании структуры. Необходимо введение модели - решетки взаимосвязанных пор. Лекция-9

Особенности КК в системе взаимосвязанных пор Лекция-9 Результаты численного моделирования КК в решетке сферических полостей, с переменным числом окон Распределение полостей, заданное при моделировании Расчет Адс. ветви для модели взаимосвязанных пор Расчет Адс. ветви для модели индивидуально заполняемых полостей Расчет распределения объема полостей (РОП) по адсорбционной ветви. Ветвь 1 Ветвь 2 Цилиндры с дном Цилиндры без дна Расчет по методологии метода Ртутной порометрии Распределение окон, заданное при моделировании Р/Р 0 Расчет РОП по десорбционной ветви.

Особенности КК в системе взаимосвязанных пор 1. Независимое заполнение полостей происходит только на начальном этапе КК и охватывает полости с минимальным Zi. 2. Заполнение этих полостей уменьшает количество окон в соседних полостях. Эти полости переходят в разряд полостей Zi -1. Эффект «запаздывания» - снижение критического давления их спонтанного заполнения. Т. о. заполнение полостей провоцирует заполнение полостей того же размера, но с большим количеством окон – «кооперативный механизм» заполнения групп полостей. 3. Расчет по десорбционной ветви дает информацию о «перколяционных» горлах, определяющих связь полостей с внешней поверхностью пористого тела. Лекция-9
LecSS-9(2012).ppt