ЛК 9 - 11- крист., кр.охл., д.с..pptx
- Количество слайдов: 46
 Лекция № 9 -11 Кристаллизация. Кривые охлаждения. Построение диаграмм состояния.
Лекция № 9 -11 Кристаллизация. Кривые охлаждения. Построение диаграмм состояния.
 Кристаллизация металлов Различают первичную и вторичную кристаллизацию. Переход из жидкого состояния в твердое называется первичной кристаллизацией. Вторичная кристаллизация (перекристаллизация) происходит в твердом состоянии. Рассмотрим процесс первичной кристаллизации более подробно и построим кривую охлаждения.
Кристаллизация металлов Различают первичную и вторичную кристаллизацию. Переход из жидкого состояния в твердое называется первичной кристаллизацией. Вторичная кристаллизация (перекристаллизация) происходит в твердом состоянии. Рассмотрим процесс первичной кристаллизации более подробно и построим кривую охлаждения.
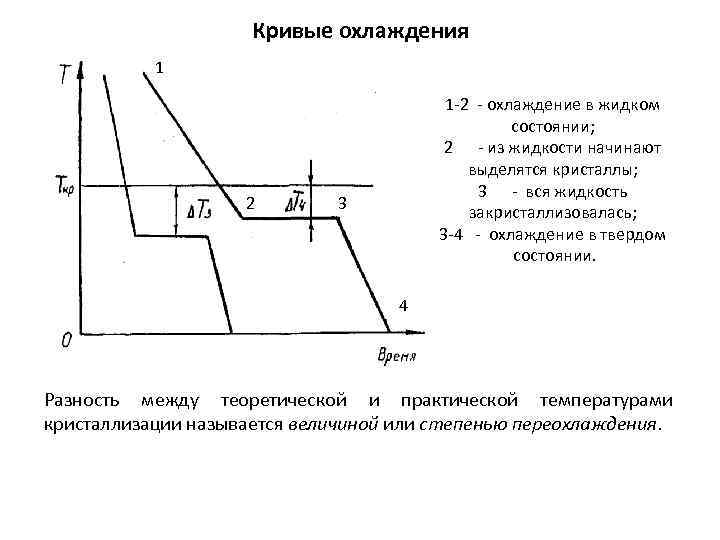 Кривые охлаждения 1 2 1 -2 - охлаждение в жидком состоянии; 2 - из жидкости начинают выделятся кристаллы; 3 - вся жидкость закристаллизовалась; 3 -4 - охлаждение в твердом состоянии. 3 4 Разность между теоретической и практической температурами кристаллизации называется величиной или степенью переохлаждения.
Кривые охлаждения 1 2 1 -2 - охлаждение в жидком состоянии; 2 - из жидкости начинают выделятся кристаллы; 3 - вся жидкость закристаллизовалась; 3 -4 - охлаждение в твердом состоянии. 3 4 Разность между теоретической и практической температурами кристаллизации называется величиной или степенью переохлаждения.
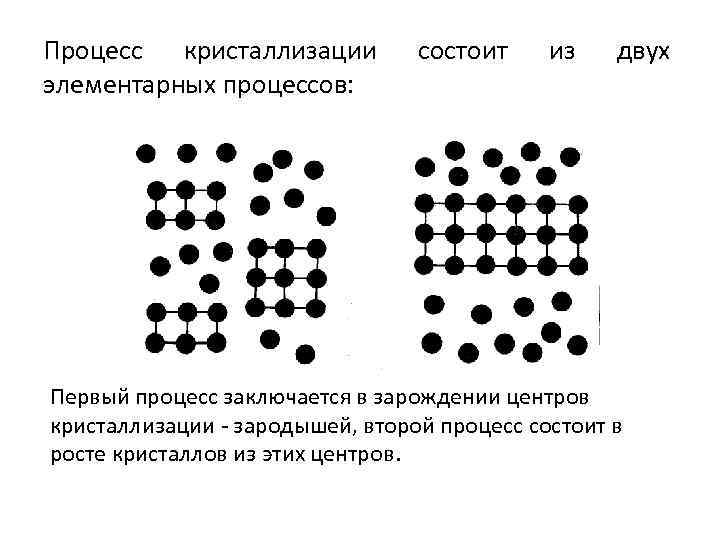 Процесс кристаллизации элементарных процессов: состоит из двух Первый процесс заключается в зарождении центров кристаллизации - зародышей, второй процесс состоит в росте кристаллов из этих центров.
Процесс кристаллизации элементарных процессов: состоит из двух Первый процесс заключается в зарождении центров кристаллизации - зародышей, второй процесс состоит в росте кристаллов из этих центров.
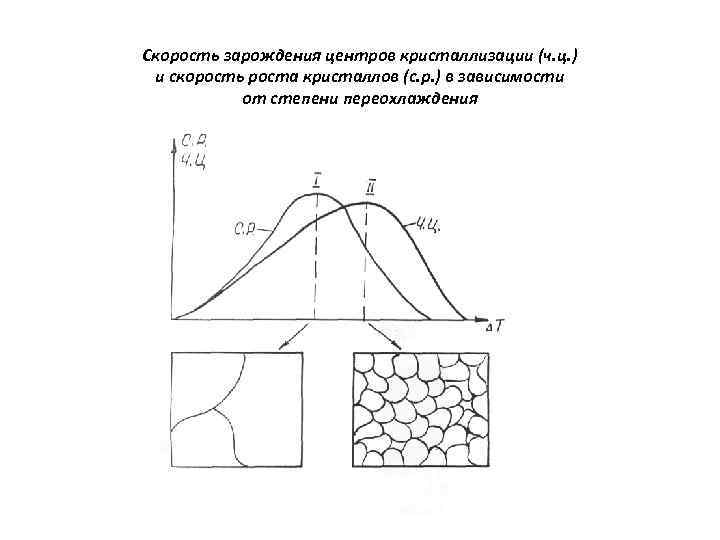 Скорость зарождения центров кристаллизации (ч. ц. ) и скорость роста кристаллов (с. р. ) в зависимости от степени переохлаждения
Скорость зарождения центров кристаллизации (ч. ц. ) и скорость роста кристаллов (с. р. ) в зависимости от степени переохлаждения
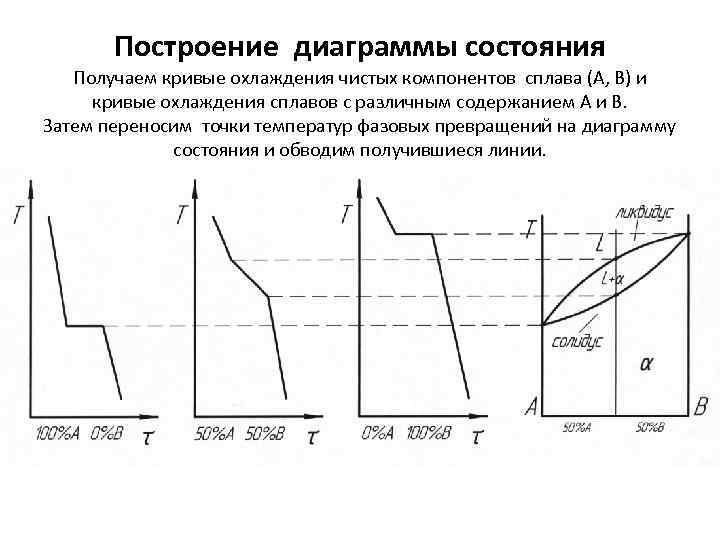 Построение диаграммы состояния Получаем кривые охлаждения чистых компонентов сплава (А, В) и кривые охлаждения сплавов с различным содержанием А и В. Затем переносим точки температур фазовых превращений на диаграмму состояния и обводим получившиеся линии.
Построение диаграммы состояния Получаем кривые охлаждения чистых компонентов сплава (А, В) и кривые охлаждения сплавов с различным содержанием А и В. Затем переносим точки температур фазовых превращений на диаграмму состояния и обводим получившиеся линии.
 Тип диаграммы состояния двойной системы определяется взаимодействием ее компонентов в жидком и твердом состояниях, а также наличием полиморфных превращений компонентов. Выделяют 5 типов диаграмм состояния.
Тип диаграммы состояния двойной системы определяется взаимодействием ее компонентов в жидком и твердом состояниях, а также наличием полиморфных превращений компонентов. Выделяют 5 типов диаграмм состояния.
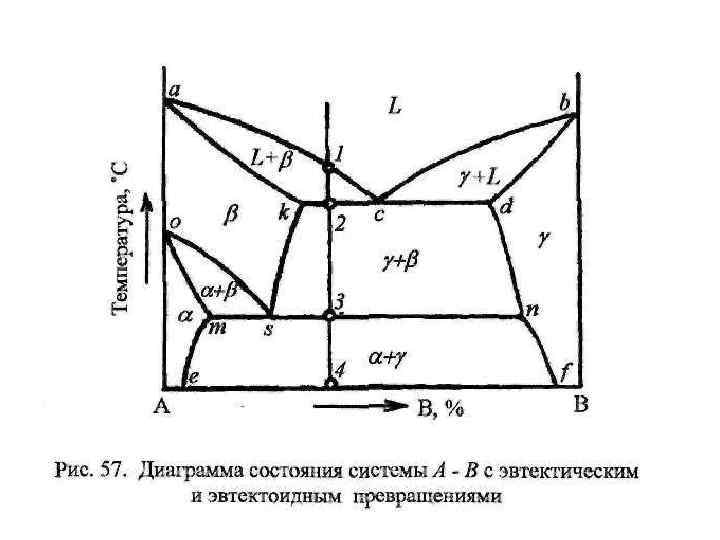
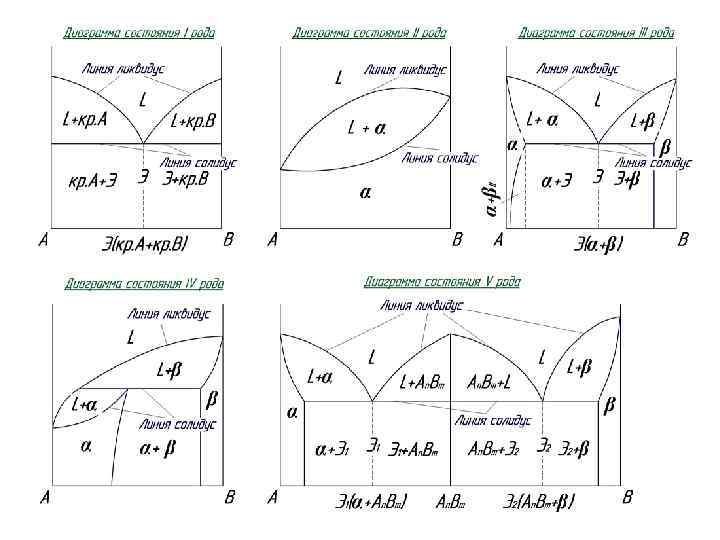
 Диаграммы состояния двухкомпонентных сплавов Диаграмма состояния представляет собой графическое изображение состояния сплава, т. е. мы можем узнать из каких фаз состоит сплав. (жидкая фаза, твердый раствор, хим. соединение, механическая смесь) Выделяют 5 типов диаграмм состояния: I рода: компоненты А и В неограниченно растворяются один в другом в жидком состоянии и не растворяются в твердом (т. е. в сплаве распределены кристаллы А и кристаллы В), а также не образуют химических соединений; I I рода: компоненты А и В образуют неограниченные твердые растворы; I I I рода: компоненты А и В образуют ограниченные твердые растворы и на диаграмме присутствует эвтектическое превращение, при котором из жидкости (L) при постоянной температуре образуется механическая смесь двух фаз (эвтектика) : L → Э (α + β). IV рода: компоненты А и В образуют ограниченные твердые растворы и на диаграмме присутствует перитектическое превращение L + β→ α : жидкость (L) реагирует с ранее выпавшими твердыми кристаллами (β) и образуется новый вид кристаллов – твердый раствор (α). V рода: компоненты А и В образуют химические соединения.
Диаграммы состояния двухкомпонентных сплавов Диаграмма состояния представляет собой графическое изображение состояния сплава, т. е. мы можем узнать из каких фаз состоит сплав. (жидкая фаза, твердый раствор, хим. соединение, механическая смесь) Выделяют 5 типов диаграмм состояния: I рода: компоненты А и В неограниченно растворяются один в другом в жидком состоянии и не растворяются в твердом (т. е. в сплаве распределены кристаллы А и кристаллы В), а также не образуют химических соединений; I I рода: компоненты А и В образуют неограниченные твердые растворы; I I I рода: компоненты А и В образуют ограниченные твердые растворы и на диаграмме присутствует эвтектическое превращение, при котором из жидкости (L) при постоянной температуре образуется механическая смесь двух фаз (эвтектика) : L → Э (α + β). IV рода: компоненты А и В образуют ограниченные твердые растворы и на диаграмме присутствует перитектическое превращение L + β→ α : жидкость (L) реагирует с ранее выпавшими твердыми кристаллами (β) и образуется новый вид кристаллов – твердый раствор (α). V рода: компоненты А и В образуют химические соединения.
 .
.
 Линия ликвидус – выше этой линии сплавы в жидком состоянии. Линия солидус - ниже этой линии сплавы в твердом состоянии. Между линиями ними сплав находится в твердо-жидком состоянии. Обозначения структурных составляющих на диаграммах I-IV рода: L - жидкость; кр. А - кристаллы компонента А в чистом виде; кр. В - кристаллы компонента В в чистом виде; α - твердый раствор компонента В в компоненте А; β – твердый раствор компонента А в компоненте В; Э – эвтектика – механическая эвтектическая смесь двух фаз: на диагр. 1: кр. А+ кр. В; на диагр. 3: α + β. Обозначения структурных составляющих на диаграмме V рода: L - жидкость; α - твердый раствор Аn. Bm в компоненте А; β – твердый раствор компонента Аn. Bm в компоненте В; Аn. Bm – химическое соединение компонентов А и В; Э 1 – эвтектика состава: α + Аn. Bm ; Э 2 – эвтектика состава: Аn. Bm + β.
Линия ликвидус – выше этой линии сплавы в жидком состоянии. Линия солидус - ниже этой линии сплавы в твердом состоянии. Между линиями ними сплав находится в твердо-жидком состоянии. Обозначения структурных составляющих на диаграммах I-IV рода: L - жидкость; кр. А - кристаллы компонента А в чистом виде; кр. В - кристаллы компонента В в чистом виде; α - твердый раствор компонента В в компоненте А; β – твердый раствор компонента А в компоненте В; Э – эвтектика – механическая эвтектическая смесь двух фаз: на диагр. 1: кр. А+ кр. В; на диагр. 3: α + β. Обозначения структурных составляющих на диаграмме V рода: L - жидкость; α - твердый раствор Аn. Bm в компоненте А; β – твердый раствор компонента Аn. Bm в компоненте В; Аn. Bm – химическое соединение компонентов А и В; Э 1 – эвтектика состава: α + Аn. Bm ; Э 2 – эвтектика состава: Аn. Bm + β.
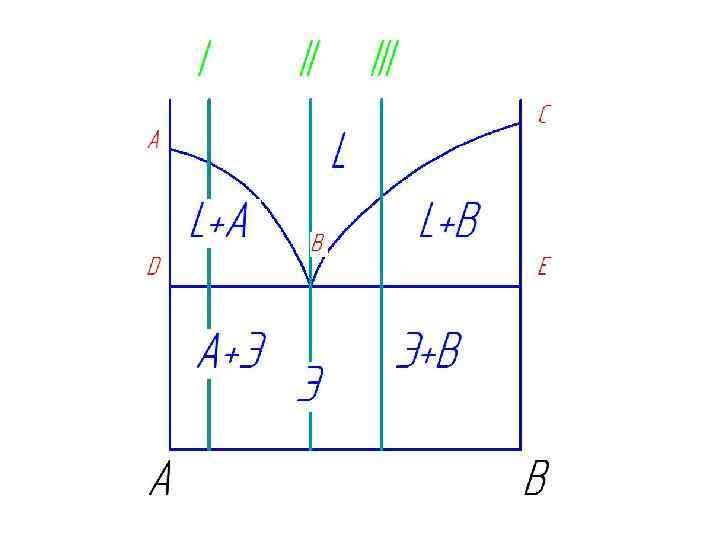
 Диаграммы состояния первого типа относятся к сплавам, компоненты которых А и В неограниченно растворяются один в другом в жидком состоянии и не растворяются в твердом (т. е. в сплаве распределены кристаллы А и кристаллы В), а также не образуют химических соединений.
Диаграммы состояния первого типа относятся к сплавам, компоненты которых А и В неограниченно растворяются один в другом в жидком состоянии и не растворяются в твердом (т. е. в сплаве распределены кристаллы А и кристаллы В), а также не образуют химических соединений.
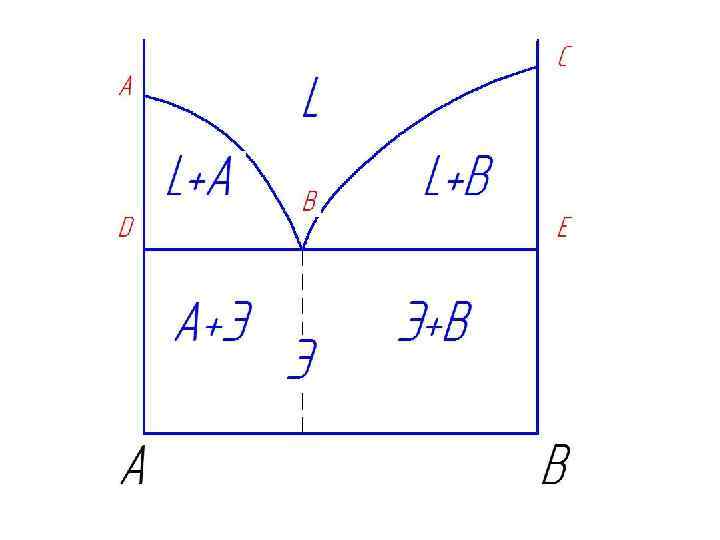
 Линия АВС – называется «линия ликвидус» , т. к. выше нее сплавы находятся в жидком состоянии (жидкость на диаграмме может обозначатся буквой Ж или L - в разных книгах по разному). Линия DBE – называется «линия солидус» , т. к. ниже нее все сплавы твердые (и разные сплавы могут включать просто кристаллы компонентов А и В, твердые растворы (тогда на диаграмме будет буква - α ), механические смеси – например , эвтектика – буква Э и т. д. ). Между линиями АВС и DBE сплав находится в твердо-жидком состоянии (т. е. L+А или L+В) Эвтектика – это механическая смесь двух твердых фаз кристаллов А и кристаллов В. Жидкость кристаллизуется с образованием 2 - х твердых фаз кристаллов А и В – это называется «Эвтектическое превращение» : Ж → Э (кр. А + кр. В)
Линия АВС – называется «линия ликвидус» , т. к. выше нее сплавы находятся в жидком состоянии (жидкость на диаграмме может обозначатся буквой Ж или L - в разных книгах по разному). Линия DBE – называется «линия солидус» , т. к. ниже нее все сплавы твердые (и разные сплавы могут включать просто кристаллы компонентов А и В, твердые растворы (тогда на диаграмме будет буква - α ), механические смеси – например , эвтектика – буква Э и т. д. ). Между линиями АВС и DBE сплав находится в твердо-жидком состоянии (т. е. L+А или L+В) Эвтектика – это механическая смесь двух твердых фаз кристаллов А и кристаллов В. Жидкость кристаллизуется с образованием 2 - х твердых фаз кристаллов А и В – это называется «Эвтектическое превращение» : Ж → Э (кр. А + кр. В)
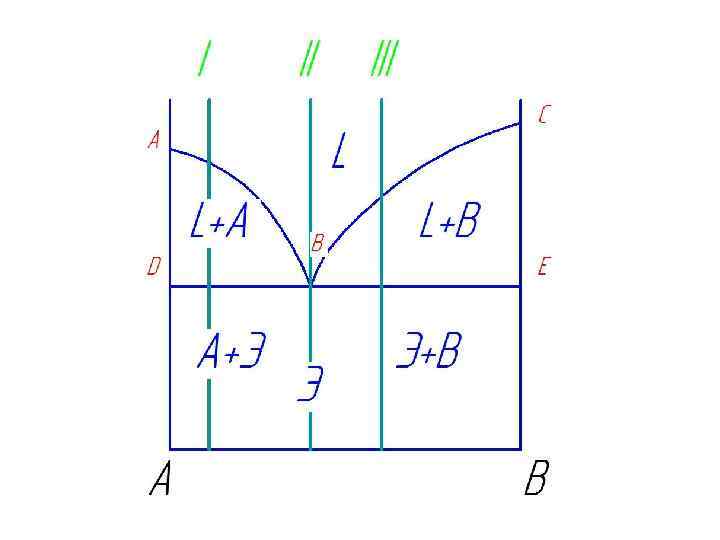
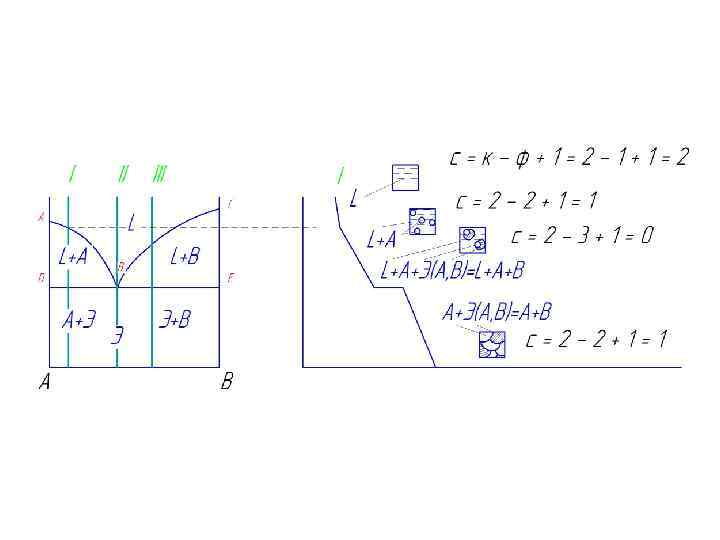
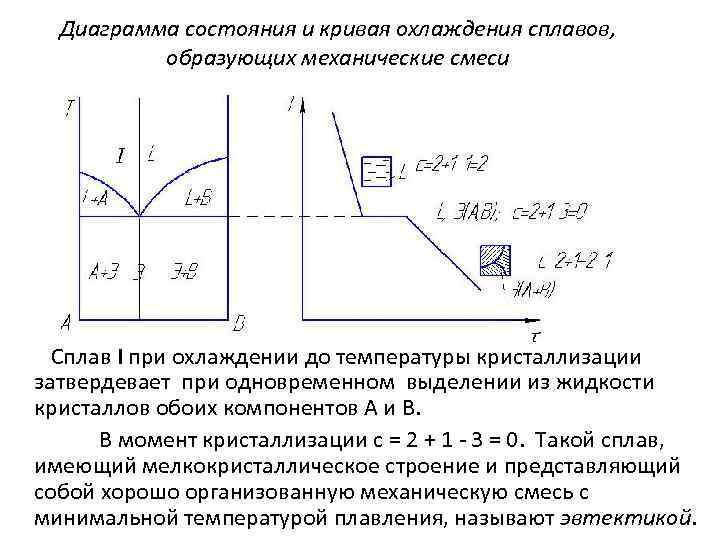 Диаграмма состояния и кривая охлаждения сплавов, образующих механические смеси из чистых компонентов Сплав І при охлаждении до температуры кристаллизации затвердевает при одновременном выделении из жидкости кристаллов обоих компонентов А и В. В момент кристаллизации с = 2 + 1 - 3 = 0. Такой сплав, имеющий мелкокристаллическое строение и представляющий собой хорошо организованную механическую смесь с минимальной температурой плавления, называют эвтектикой.
Диаграмма состояния и кривая охлаждения сплавов, образующих механические смеси из чистых компонентов Сплав І при охлаждении до температуры кристаллизации затвердевает при одновременном выделении из жидкости кристаллов обоих компонентов А и В. В момент кристаллизации с = 2 + 1 - 3 = 0. Такой сплав, имеющий мелкокристаллическое строение и представляющий собой хорошо организованную механическую смесь с минимальной температурой плавления, называют эвтектикой.
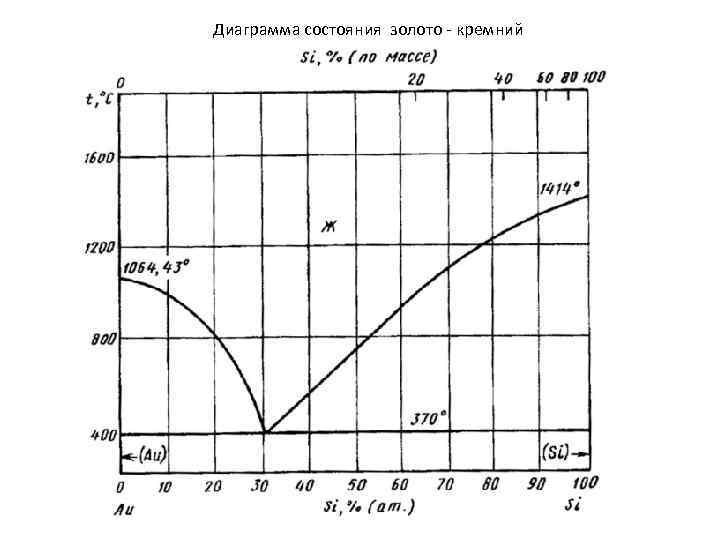 Диаграмма состояния золото - кремний
Диаграмма состояния золото - кремний
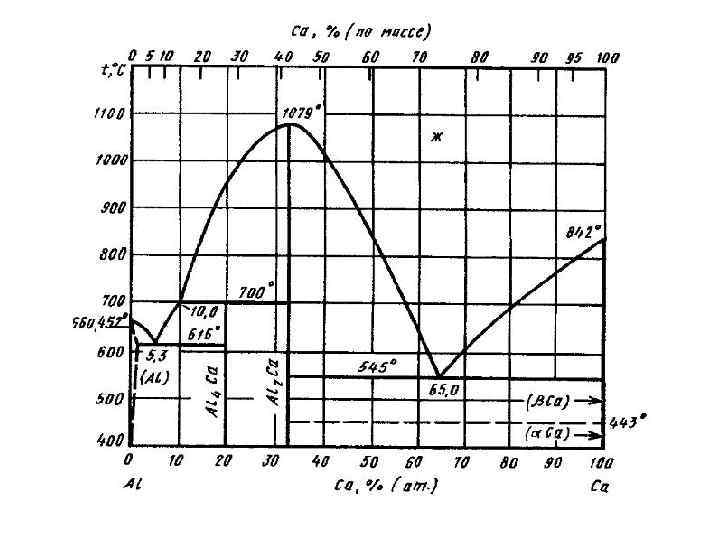
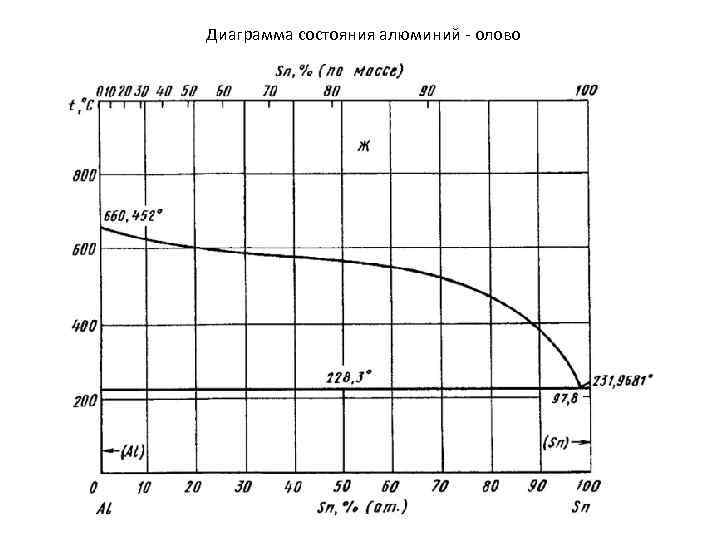 Диаграмма состояния алюминий - олово
Диаграмма состояния алюминий - олово
 Правило фаз Гиббса (закон фаз) Фазовый анализ кривых охлаждения проводят, используя правило фаз: «число равновесно существующих в какой либо системе фаз не может быть больше числа, образующих эти фазы компонентов + 2» . Это правило связывает число существующих фаз Ф, число компонентов сплава К и число степеней свободы С в одно уравнение: С=К–Ф+2 Степенями свободы системы называются такие независимые параметры (температура, давление, концентрация) при изменении которых число фаз, находящихся в равновесии не меняется. Цифра « 2» в уравнении отражает допущение, что фазовое состояние системы определяется двумя параметрами – температурой и давлением.
Правило фаз Гиббса (закон фаз) Фазовый анализ кривых охлаждения проводят, используя правило фаз: «число равновесно существующих в какой либо системе фаз не может быть больше числа, образующих эти фазы компонентов + 2» . Это правило связывает число существующих фаз Ф, число компонентов сплава К и число степеней свободы С в одно уравнение: С=К–Ф+2 Степенями свободы системы называются такие независимые параметры (температура, давление, концентрация) при изменении которых число фаз, находящихся в равновесии не меняется. Цифра « 2» в уравнении отражает допущение, что фазовое состояние системы определяется двумя параметрами – температурой и давлением.
 Для металлических систем, рассматриваемых при постоянном давлении, равном атмосферному, закон фаз принимает вид: С = К – Ф + 1; где С – число степеней свободы (вариантность), т. е. число внешних и внутренних факторов, которое может изменяться без изменения числа фаз в системе; К – количество компонентов (веществ, образующих систему); 1 – число внешних и внутренних факторов (температура), воздействующих на систему; Ф – число фаз; фаза – это однородная часть системы, отделенная от других частей системы поверхностью раздела, при переходе через которую свойства изменяются скачкообразно.
Для металлических систем, рассматриваемых при постоянном давлении, равном атмосферному, закон фаз принимает вид: С = К – Ф + 1; где С – число степеней свободы (вариантность), т. е. число внешних и внутренних факторов, которое может изменяться без изменения числа фаз в системе; К – количество компонентов (веществ, образующих систему); 1 – число внешних и внутренних факторов (температура), воздействующих на систему; Ф – число фаз; фаза – это однородная часть системы, отделенная от других частей системы поверхностью раздела, при переходе через которую свойства изменяются скачкообразно.
 Правило отрезков (правило рычага): Для того, чтобы определить концентрации компонентов в фазах через данную точку, характеризующую состояние сплава, проводят горизонтальную линию до пересечения с линиями, ограничивающими данную область, проекции точек пересечения на ось концентраций укажут на содержание компонентов в фазах. Для того чтобы определить количественное соотношение фаз в сплаве через заданную точку проводят горизонтальную линию до пересечения с линиями, ограничивающими данную область, отрезки этой линии между заданной точкой (т. О) и точками пересечения (т. В и т. С), определяющими составы фаз обратно пропорциональны количествам этих фаз.
Правило отрезков (правило рычага): Для того, чтобы определить концентрации компонентов в фазах через данную точку, характеризующую состояние сплава, проводят горизонтальную линию до пересечения с линиями, ограничивающими данную область, проекции точек пересечения на ось концентраций укажут на содержание компонентов в фазах. Для того чтобы определить количественное соотношение фаз в сплаве через заданную точку проводят горизонтальную линию до пересечения с линиями, ограничивающими данную область, отрезки этой линии между заданной точкой (т. О) и точками пересечения (т. В и т. С), определяющими составы фаз обратно пропорциональны количествам этих фаз.
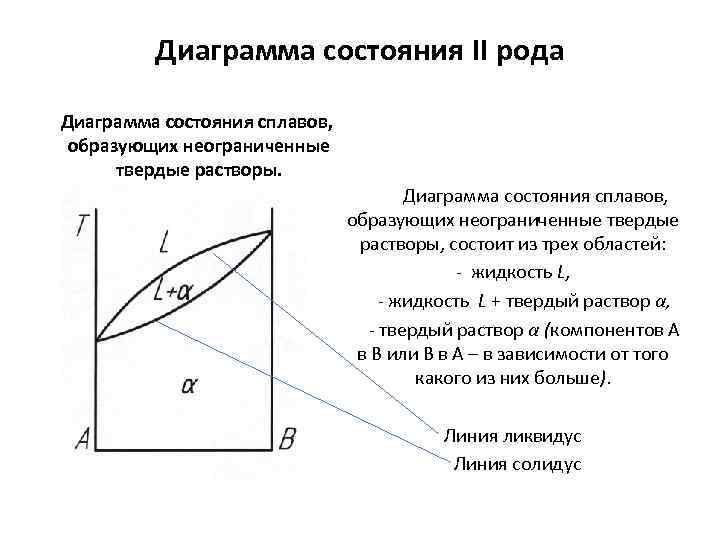 Диаграмма состояния II рода Диаграмма состояния сплавов, образующих неограниченные твердые растворы, состоит из трех областей: - жидкость L, - жидкость L + твердый раствор α, - твердый раствор α (компонентов А в В или В в А – в зависимости от того какого из них больше). Линия ликвидус Линия солидус
Диаграмма состояния II рода Диаграмма состояния сплавов, образующих неограниченные твердые растворы, состоит из трех областей: - жидкость L, - жидкость L + твердый раствор α, - твердый раствор α (компонентов А в В или В в А – в зависимости от того какого из них больше). Линия ликвидус Линия солидус
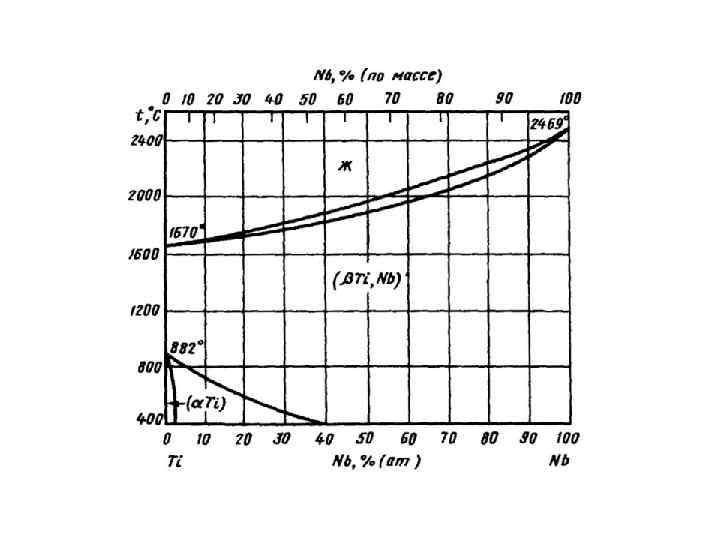
 Диаграмма состояния сплавов, образующих ограниченные твердые растворы – это диаграммы состояния III и IV рода Оба компонента неограниченно растворимы в жидком состоянии, ограниченно в твердом и не образуют химических соединений. В сплавах такого рода возможно существование: жидкой фазы L, жидкого раствора компонента В в А, который будет называться α-раствором, и (или) твердого раствора компонента А в В, который обозначается через β. В этих сплавах возможно равновесие при одновременном сосуществовании трех фаз: L, α и β. В зависимости от того, какая реакция протекает в условиях существования трех фаз, могут быть два вида диаграмм: - диаграмма с эвтектическим превращением (III рода), - диаграмма с перитектическим превращением (IV рода).
Диаграмма состояния сплавов, образующих ограниченные твердые растворы – это диаграммы состояния III и IV рода Оба компонента неограниченно растворимы в жидком состоянии, ограниченно в твердом и не образуют химических соединений. В сплавах такого рода возможно существование: жидкой фазы L, жидкого раствора компонента В в А, который будет называться α-раствором, и (или) твердого раствора компонента А в В, который обозначается через β. В этих сплавах возможно равновесие при одновременном сосуществовании трех фаз: L, α и β. В зависимости от того, какая реакция протекает в условиях существования трех фаз, могут быть два вида диаграмм: - диаграмма с эвтектическим превращением (III рода), - диаграмма с перитектическим превращением (IV рода).
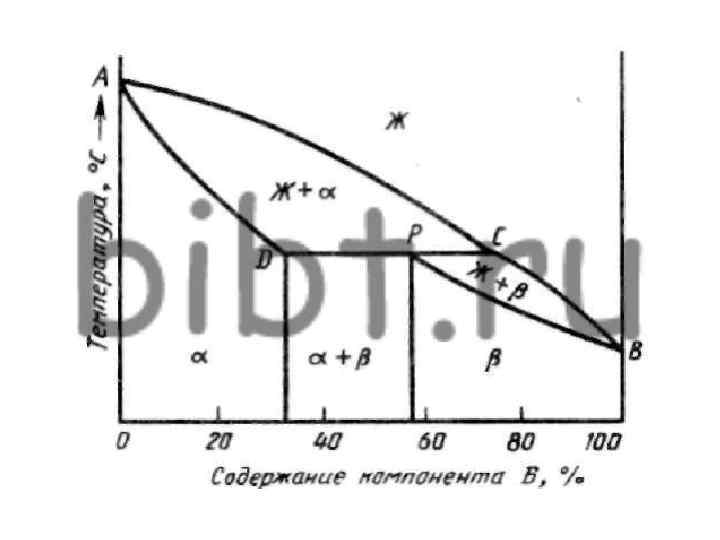
 Диаграмма состояния III рода ABC - линия ликвидус; ADBE и DBEC - линия солидус. Обозначения фаз и структурных составляющих на диаграмме: α – твердый раствор компонента В в компоненте А; Э – эвтектика (механическая смесь фаз) состава α + В; В – кристаллы компонента В; L - жидкость. На диаграмме присутствует эвтектическое превращение, при котором из жидкости (L) при постоянной температуре образуется механическая смесь (эвтектика) двух фаз: твердый раствор α + кристаллы В. L → Э (α + кр. В)
Диаграмма состояния III рода ABC - линия ликвидус; ADBE и DBEC - линия солидус. Обозначения фаз и структурных составляющих на диаграмме: α – твердый раствор компонента В в компоненте А; Э – эвтектика (механическая смесь фаз) состава α + В; В – кристаллы компонента В; L - жидкость. На диаграмме присутствует эвтектическое превращение, при котором из жидкости (L) при постоянной температуре образуется механическая смесь (эвтектика) двух фаз: твердый раствор α + кристаллы В. L → Э (α + кр. В)
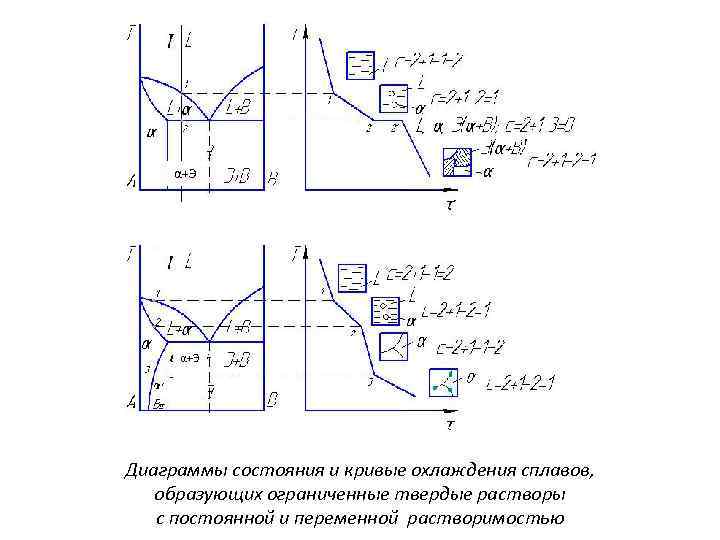 α+Э Диаграммы состояния и кривые охлаждения сплавов, образующих ограниченные твердые растворы с постоянной и переменной растворимостью
α+Э Диаграммы состояния и кривые охлаждения сплавов, образующих ограниченные твердые растворы с постоянной и переменной растворимостью
 В отличие от первой диаграммы, на диаграмме, представленной сбоку, видно, что растворимость В в А с понижением температуры уменьшается. Это приводит к пересыщению раствора І, и из него должен выделиться избыточный компонент В. Кристаллы В, выделяющиеся из твердого раствора, называют вторичными кристаллами и часто обозначают символом, имеющим индекс ІІ: в данном случае ВІІ. Процесс выделения вторичных кристаллов из твердой фазы носит название вторичной кристаллизации. Если компонент В также как и А может являться растворителем (т. е. растворять какое-то количество компонента А), тогда на диаграмме этот раствор обозначим β – твердый раствор компонента А в компоненте В. И диаграмма будет иметь вид…….
В отличие от первой диаграммы, на диаграмме, представленной сбоку, видно, что растворимость В в А с понижением температуры уменьшается. Это приводит к пересыщению раствора І, и из него должен выделиться избыточный компонент В. Кристаллы В, выделяющиеся из твердого раствора, называют вторичными кристаллами и часто обозначают символом, имеющим индекс ІІ: в данном случае ВІІ. Процесс выделения вторичных кристаллов из твердой фазы носит название вторичной кристаллизации. Если компонент В также как и А может являться растворителем (т. е. растворять какое-то количество компонента А), тогда на диаграмме этот раствор обозначим β – твердый раствор компонента А в компоненте В. И диаграмма будет иметь вид…….
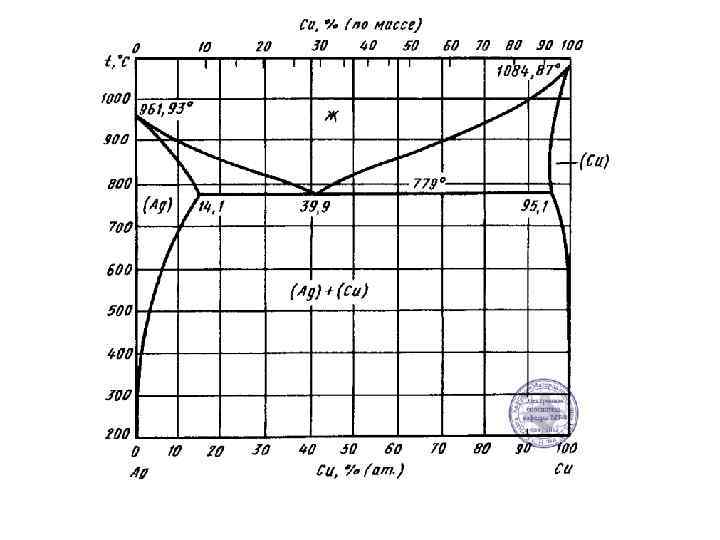
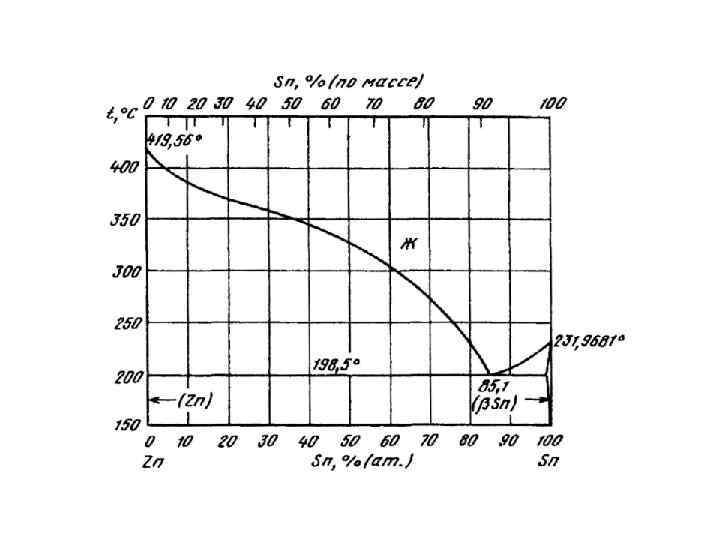
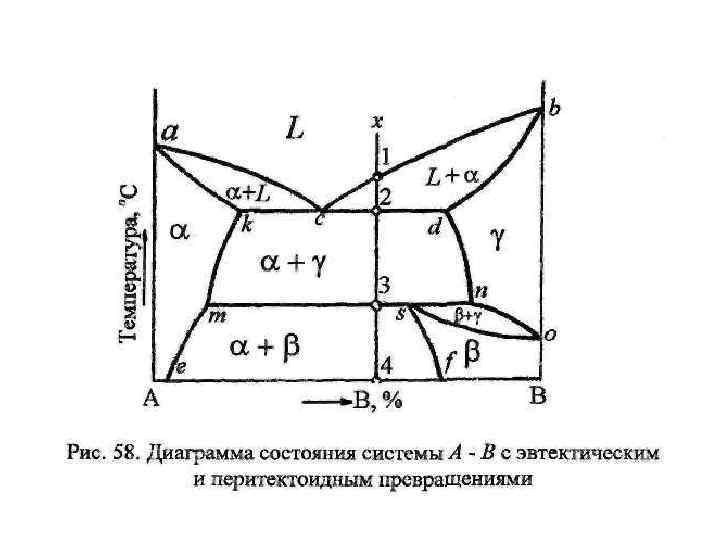
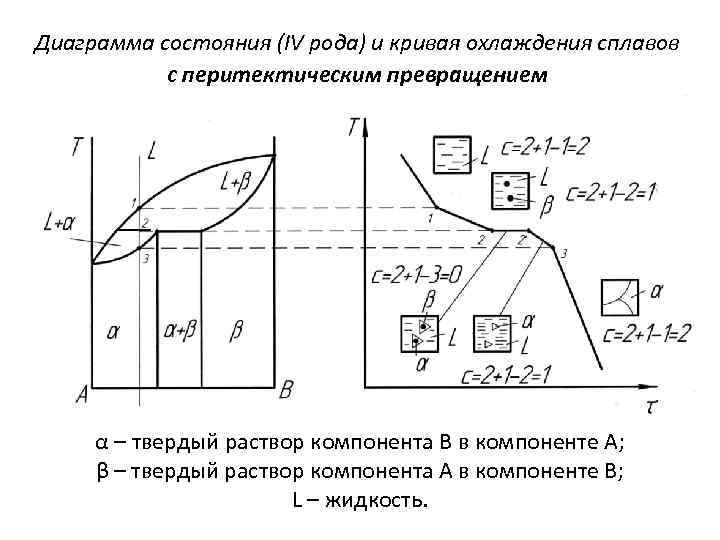 Диаграмма состояния (IV рода) и кривая охлаждения сплавов с перитектическим превращением α – твердый раствор компонента В в компоненте А; β – твердый раствор компонента А в компоненте В; L – жидкость.
Диаграмма состояния (IV рода) и кривая охлаждения сплавов с перитектическим превращением α – твердый раствор компонента В в компоненте А; β – твердый раствор компонента А в компоненте В; L – жидкость.
 В рассмотренном ранее эвтектическом превращении жидкость кристаллизуется с образованием двух твердых фаз. Возможен и другой тип превращения, когда жидкость (L) реагирует с ранее выпавшими твердыми кристаллами (β) и образуется новый вид кристаллов – твердый раствор (α). Реакция подобного типа называется перитектической: L + β→ α
В рассмотренном ранее эвтектическом превращении жидкость кристаллизуется с образованием двух твердых фаз. Возможен и другой тип превращения, когда жидкость (L) реагирует с ранее выпавшими твердыми кристаллами (β) и образуется новый вид кристаллов – твердый раствор (α). Реакция подобного типа называется перитектической: L + β→ α


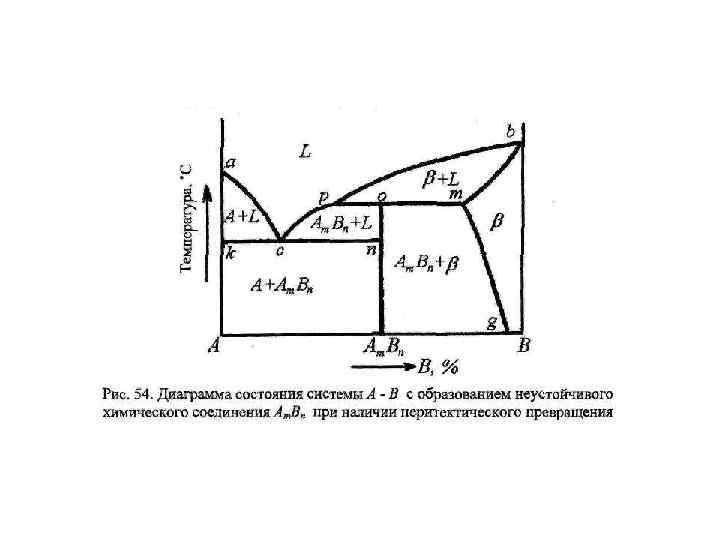
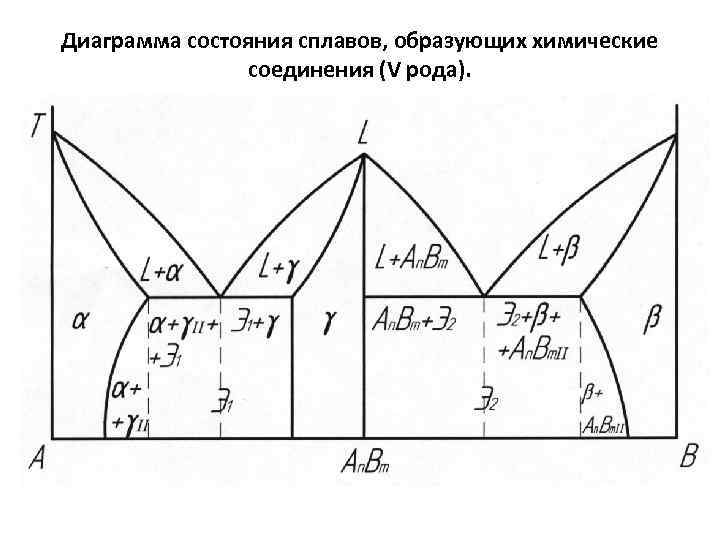 Диаграмма состояния сплавов, образующих химические соединения (V рода).
Диаграмма состояния сплавов, образующих химические соединения (V рода).
 L – жидкость (жидкий раствор компонентов А в В или В в А – в зависимости от того какого из них больше). α - твердый раствор Аn. Вm в компоненте А , γ - твердый раствор компонента А в химическом соединении Аn. Вm, Э 1 (эвтектика состава 1) – механическая смесь твердых растворов α + γ; β – твердый раствор Аn. Вm в компоненте В, Э 2 (эвтектика состава 2) – механическая смесь Аn. Вm + β.
L – жидкость (жидкий раствор компонентов А в В или В в А – в зависимости от того какого из них больше). α - твердый раствор Аn. Вm в компоненте А , γ - твердый раствор компонента А в химическом соединении Аn. Вm, Э 1 (эвтектика состава 1) – механическая смесь твердых растворов α + γ; β – твердый раствор Аn. Вm в компоненте В, Э 2 (эвтектика состава 2) – механическая смесь Аn. Вm + β.
 Химическое соединение Аn. Bm устойчиво, поэтому может быть нагрето без разложения до своей температуры плавления. Химическое соединение Аn. Bm плавится при постоянной температуре и можно рассматривать как однокомпонентную смесь. Кристаллизация сплавов по этой диаграмме происходит совершенно аналогично кристаллизации сплавов, образующих диаграммы с ограниченной растворимостью. Отличие состоит в том, что кроме выделения кристаллов чистых компонентов А и В и кристаллов твердых растворов, происходит еще образование кристаллов химического соединения.
Химическое соединение Аn. Bm устойчиво, поэтому может быть нагрето без разложения до своей температуры плавления. Химическое соединение Аn. Bm плавится при постоянной температуре и можно рассматривать как однокомпонентную смесь. Кристаллизация сплавов по этой диаграмме происходит совершенно аналогично кристаллизации сплавов, образующих диаграммы с ограниченной растворимостью. Отличие состоит в том, что кроме выделения кристаллов чистых компонентов А и В и кристаллов твердых растворов, происходит еще образование кристаллов химического соединения.
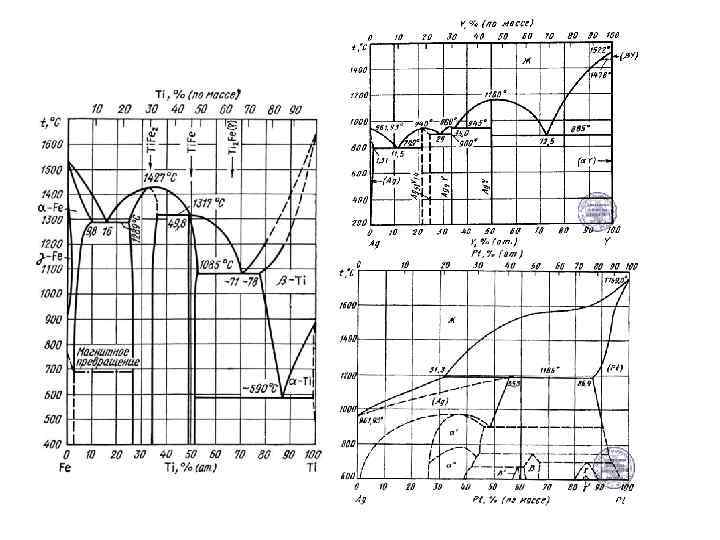
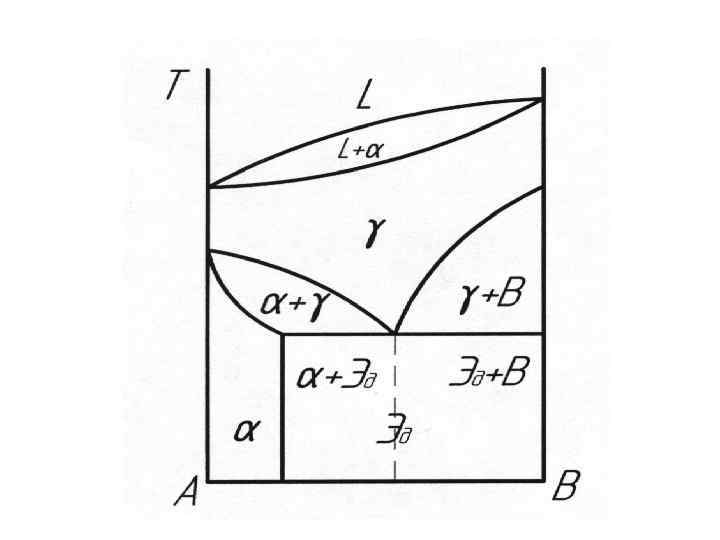
 Диаграммы состояния сплавов, испытывающих полиморфные превращения (т. е. когда происходит изменение кристаллической решетки в зависимости от температуры при которой находится компонент). γ α – твердый раствор компонента В в компоненте А (огр. ); γ - твердый раствор компонента В в компоненте А (неогр. ); В – кристаллы компонента В в чистом виде; L – жидкость; Эд – механическая эвтектоидная смесь состава α + В.
Диаграммы состояния сплавов, испытывающих полиморфные превращения (т. е. когда происходит изменение кристаллической решетки в зависимости от температуры при которой находится компонент). γ α – твердый раствор компонента В в компоненте А (огр. ); γ - твердый раствор компонента В в компоненте А (неогр. ); В – кристаллы компонента В в чистом виде; L – жидкость; Эд – механическая эвтектоидная смесь состава α + В.
 Вид диаграммы состояния зависит от соединений, образующихся между аллотропическими формами обоих компонентов. Если полиморфизм присущ обоим компонентам, и высокотемпературные модификации неограниченно растворимы друг в друге, а низкотемпературные нерастворимы, то диаграмма состояния имеет такой вид. Ниже некоторой температуры образовавшийся твердый раствор γ распадается в механическую смесь, которая подобна эвтектике, но образуется не из жидкой фазы, а из твердого раствора и называется эвтектоидом. В данном случае Эд = α +В.
Вид диаграммы состояния зависит от соединений, образующихся между аллотропическими формами обоих компонентов. Если полиморфизм присущ обоим компонентам, и высокотемпературные модификации неограниченно растворимы друг в друге, а низкотемпературные нерастворимы, то диаграмма состояния имеет такой вид. Ниже некоторой температуры образовавшийся твердый раствор γ распадается в механическую смесь, которая подобна эвтектике, но образуется не из жидкой фазы, а из твердого раствора и называется эвтектоидом. В данном случае Эд = α +В.