 Лекция № 8 Коррозия металлов
Лекция № 8 Коррозия металлов
 Corrodere (лат. ) – разъедать Основные виды коррозии по механизму протекания коррозии: Химическая (газовая, неэлектролитная) Электрохимическая (электролитная, влажноатмосферная, почвенная)
Corrodere (лат. ) – разъедать Основные виды коррозии по механизму протекания коррозии: Химическая (газовая, неэлектролитная) Электрохимическая (электролитная, влажноатмосферная, почвенная)
 по характеру разрушения поверхности металла: Виды коррозии: а – сплошная равномерная; б - сплошная неравномерная; в – структурно-избирательная; г – пятнами; д – язвами; е – точками (питтинговая); ж – подповерхностная; з - межкристаллитная. 3
по характеру разрушения поверхности металла: Виды коррозии: а – сплошная равномерная; б - сплошная неравномерная; в – структурно-избирательная; г – пятнами; д – язвами; е – точками (питтинговая); ж – подповерхностная; з - межкристаллитная. 3
 ХИМИЧЕСКАЯ КОРРОЗИЯ газовая и неэлектролитная (жидкостная неэлектролитная коррозия) Fe 3 C (цементит) + 2 H 2 ⇄ 3 Fe + CH 4 Карбонильная – Me + n. CO ⇄ Me(CO)n
ХИМИЧЕСКАЯ КОРРОЗИЯ газовая и неэлектролитная (жидкостная неэлектролитная коррозия) Fe 3 C (цементит) + 2 H 2 ⇄ 3 Fe + CH 4 Карбонильная – Me + n. CO ⇄ Me(CO)n
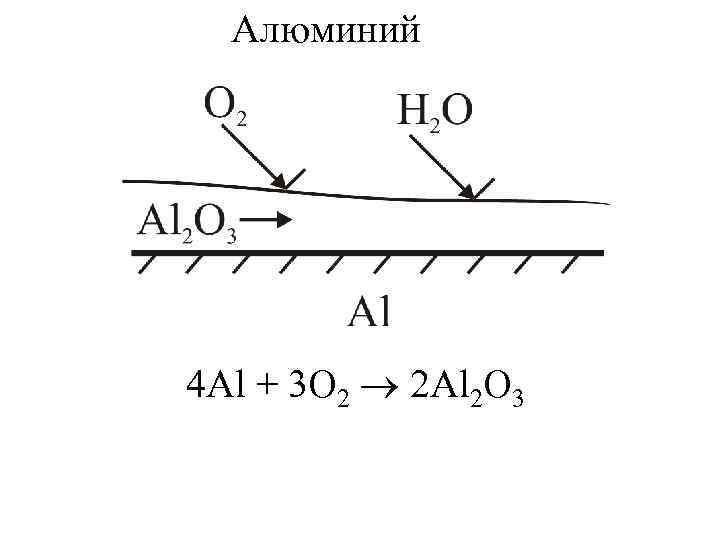 Алюминий 4 Al + 3 O 2 2 Al 2 O 3
Алюминий 4 Al + 3 O 2 2 Al 2 O 3
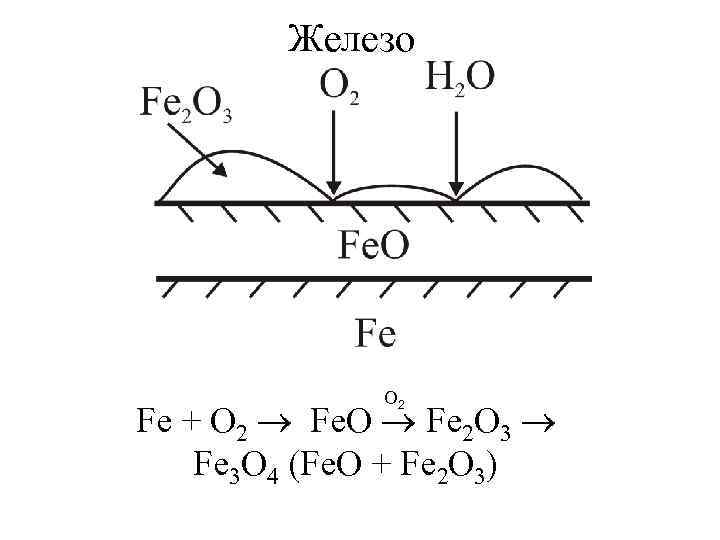 Железо O 2 Fe + O 2 Fe. O Fe 2 O 3 Fe 3 O 4 (Fe. O + Fe 2 O 3)
Железо O 2 Fe + O 2 Fe. O Fe 2 O 3 Fe 3 O 4 (Fe. O + Fe 2 O 3)
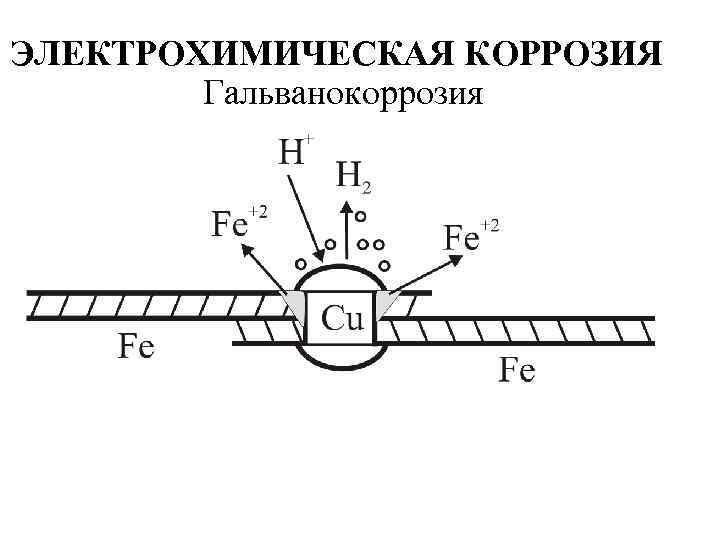 ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ Гальванокоррозия
ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ Гальванокоррозия
 (–) А, Fe | H 2 SO 4| Cu, К (+) А (–) Fe – 2ē Fe 2+ Вторичный процесс: SO 42 -+ Fe 2+ Fe. SO 4 К (+) 2 Н++ 2ē Н 2 Fe + 2 Н+ Fe 2+ + Н 2 Fe + H 2 SO 4 Fe. SO 4+ Н 2
(–) А, Fe | H 2 SO 4| Cu, К (+) А (–) Fe – 2ē Fe 2+ Вторичный процесс: SO 42 -+ Fe 2+ Fe. SO 4 К (+) 2 Н++ 2ē Н 2 Fe + 2 Н+ Fe 2+ + Н 2 Fe + H 2 SO 4 Fe. SO 4+ Н 2
 Электролит Вода (H 2 O) Кислота (HCl) Влажный воздух (H 2 O, O 2) Катодный процесс 2 H 2 O + 2ē → 2 OH– + H 2↑ 2 Н++ 2ē Н 2 2 H 2 O + O 2↑ + 4ē → 4 OH–
Электролит Вода (H 2 O) Кислота (HCl) Влажный воздух (H 2 O, O 2) Катодный процесс 2 H 2 O + 2ē → 2 OH– + H 2↑ 2 Н++ 2ē Н 2 2 H 2 O + O 2↑ + 4ē → 4 OH–
 МЕТОДЫ БОРЬБЫ С КОРРОЗИЕЙ Анодное покрытие
МЕТОДЫ БОРЬБЫ С КОРРОЗИЕЙ Анодное покрытие
 (–) А, Zn | H 2 SO 4| Fe, К (+) А (–) Zn – 2ē Zn 2+ Вторичный процесс: SO 42 -+ Zn 2+ Zn. SO 4 К (+) 2 Н++ 2ē Н 2 Zn + 2 Н+ Zn 2+ + Н 2 Zn + H 2 SO 4 Zn. SO 4+ Н 2
(–) А, Zn | H 2 SO 4| Fe, К (+) А (–) Zn – 2ē Zn 2+ Вторичный процесс: SO 42 -+ Zn 2+ Zn. SO 4 К (+) 2 Н++ 2ē Н 2 Zn + 2 Н+ Zn 2+ + Н 2 Zn + H 2 SO 4 Zn. SO 4+ Н 2
 Катодное покрытие
Катодное покрытие
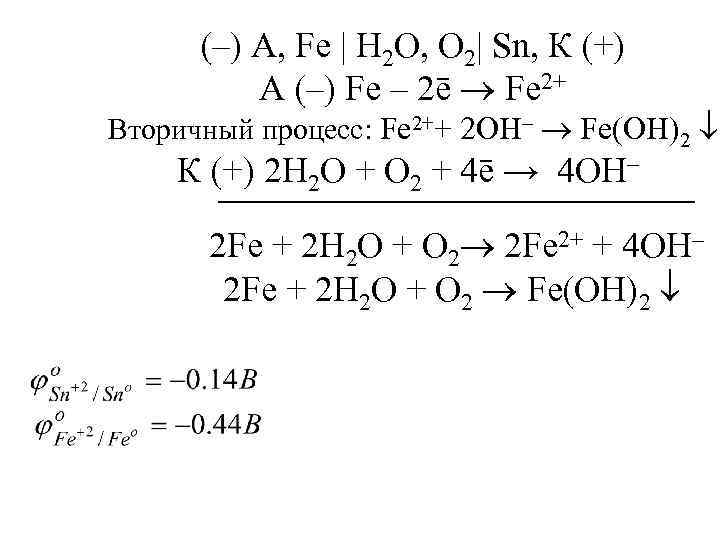 (–) А, Fe | H 2 O, O 2| Sn, К (+) А (–) Fe – 2ē Fe 2+ Вторичный процесс: Fe 2++ 2 OH– Fe(OH)2 К (+) 2 H 2 O + O 2 + 4ē → 4 OH– 2 Fe + 2 H 2 O + O 2 2 Fe 2+ + 4 OH– 2 Fe + 2 H 2 O + O 2 Fe(OH)2
(–) А, Fe | H 2 O, O 2| Sn, К (+) А (–) Fe – 2ē Fe 2+ Вторичный процесс: Fe 2++ 2 OH– Fe(OH)2 К (+) 2 H 2 O + O 2 + 4ē → 4 OH– 2 Fe + 2 H 2 O + O 2 2 Fe 2+ + 4 OH– 2 Fe + 2 H 2 O + O 2 Fe(OH)2
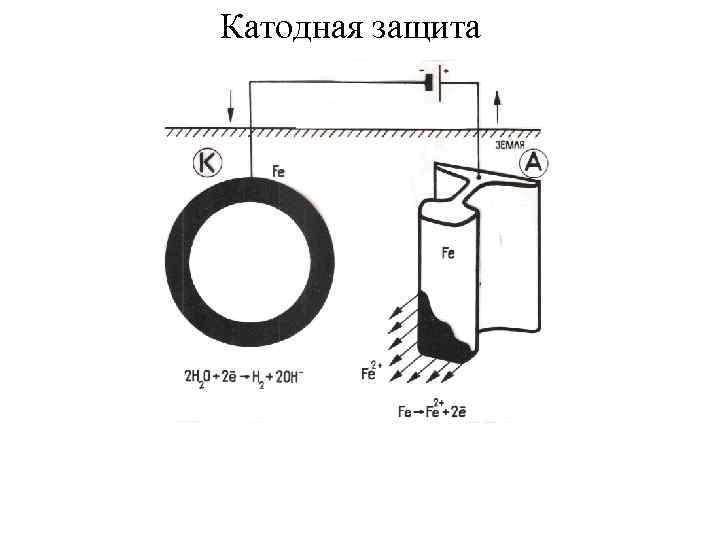 Катодная защита
Катодная защита
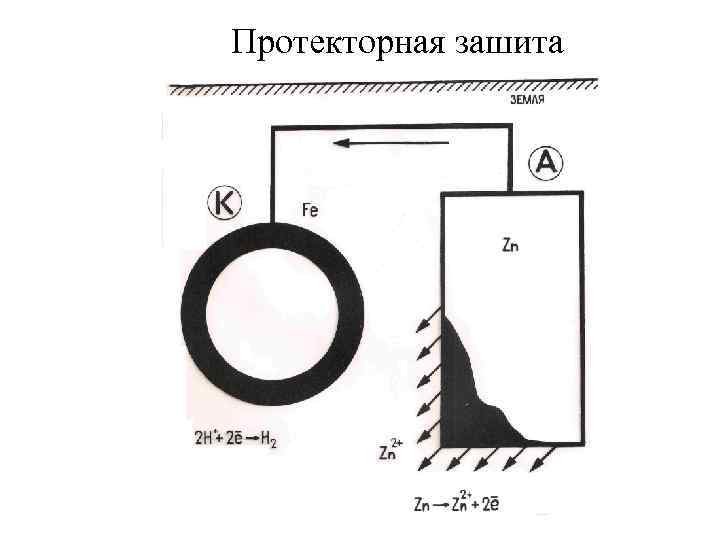 Протекторная зашита
Протекторная зашита
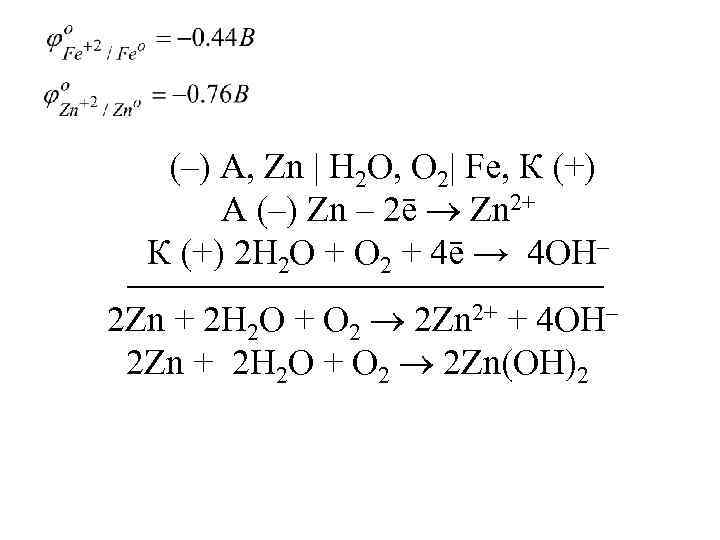 (–) А, Zn | H 2 O, O 2| Fe, К (+) А (–) Zn – 2ē Zn 2+ К (+) 2 H 2 O + O 2 + 4ē → 4 OH– 2 Zn + 2 H 2 O + O 2 2 Zn 2+ + 4 OH– 2 Zn + 2 H 2 O + O 2 2 Zn(OH)2
(–) А, Zn | H 2 O, O 2| Fe, К (+) А (–) Zn – 2ē Zn 2+ К (+) 2 H 2 O + O 2 + 4ē → 4 OH– 2 Zn + 2 H 2 O + O 2 2 Zn 2+ + 4 OH– 2 Zn + 2 H 2 O + O 2 2 Zn(OH)2