08 Лекция Гидрокси и оксиеислоты.ppt
- Количество слайдов: 60
 Лекция 8 Гетерофункциональные соединения: гидрокси – и оксокислоты. Оптическая изомерия. 1
Лекция 8 Гетерофункциональные соединения: гидрокси – и оксокислоты. Оптическая изомерия. 1
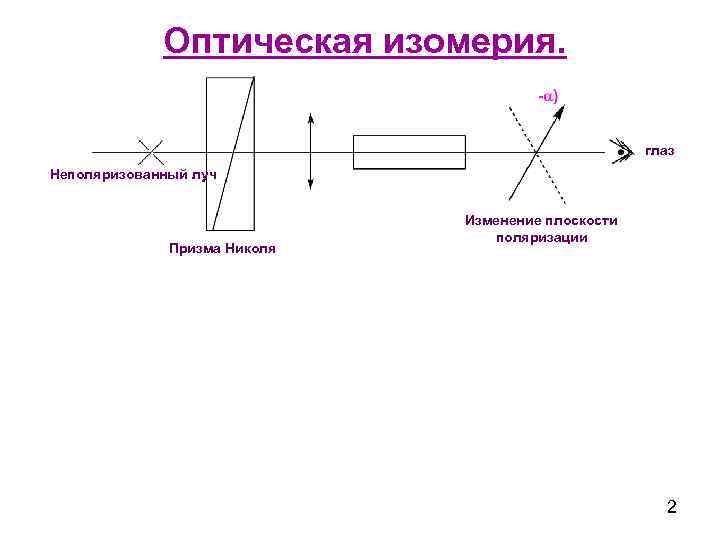 Оптическая изомерия. глаз Неполяризованный луч Призма Николя Изменение плоскости поляризации 2
Оптическая изомерия. глаз Неполяризованный луч Призма Николя Изменение плоскости поляризации 2
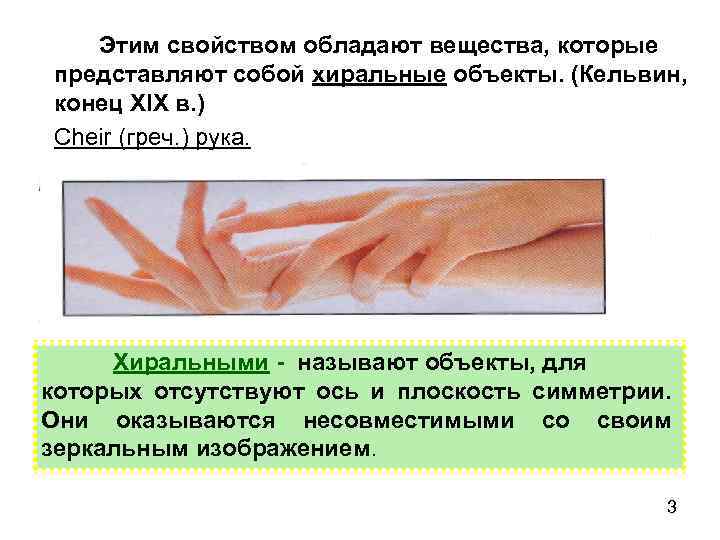 Этим свойством обладают вещества, которые представляют собой хиральные объекты. (Кельвин, конец XIX в. ) Cheir (греч. ) рука. Хиральными - называют объекты, для которых отсутствуют ось и плоскость симметрии. Они оказываются несовместимыми со своим зеркальным изображением. 3
Этим свойством обладают вещества, которые представляют собой хиральные объекты. (Кельвин, конец XIX в. ) Cheir (греч. ) рука. Хиральными - называют объекты, для которых отсутствуют ось и плоскость симметрии. Они оказываются несовместимыми со своим зеркальным изображением. 3
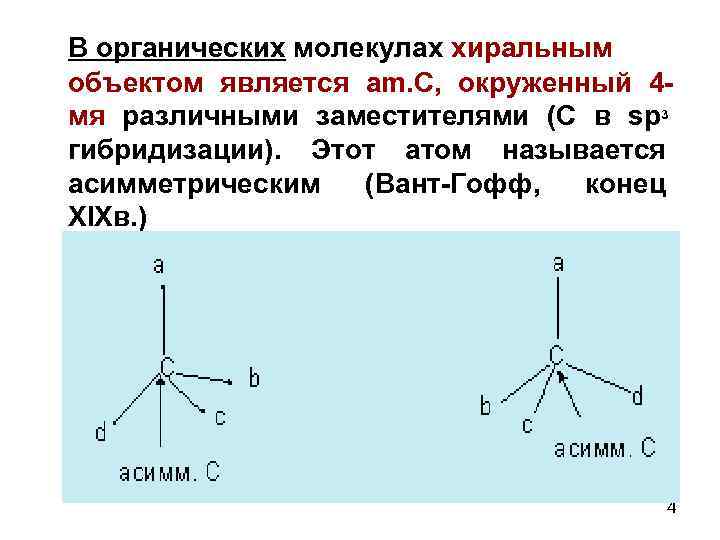 В органических молекулах хиральным объектом является am. С, окруженный 4 мя различными заместителями (С в sp 3 гибридизации). Этот атом называется асимметрическим (Вант-Гофф, конец XIXв. ) 4
В органических молекулах хиральным объектом является am. С, окруженный 4 мя различными заместителями (С в sp 3 гибридизации). Этот атом называется асимметрическим (Вант-Гофф, конец XIXв. ) 4
 Если молекула имеет один такой атом, то она хиральна, а растворы такого вещества, проявляют оптическую активность. Хиральные молекулы всегда имеют своих зеркальных «двойников» оптических антиподов, по строению являющихся их зеркальным отображением. 5
Если молекула имеет один такой атом, то она хиральна, а растворы такого вещества, проявляют оптическую активность. Хиральные молекулы всегда имеют своих зеркальных «двойников» оптических антиподов, по строению являющихся их зеркальным отображением. 5
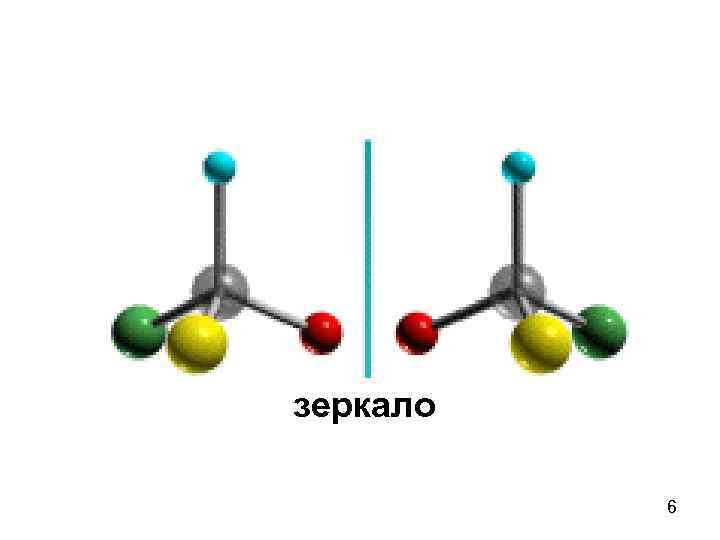 зеркало 6
зеркало 6
 Изомеры, относящиеся друг к другу как предмет и зеркальное отображение и имеющие одинаковые химические и физические свойства называются энантиомерами (оптические изомеры). Энантиомер, отклоняющий луч света по часовой стрелке, называют правовращающим и обозначают (+), а его антипод – левовращающим (-). 7
Изомеры, относящиеся друг к другу как предмет и зеркальное отображение и имеющие одинаковые химические и физические свойства называются энантиомерами (оптические изомеры). Энантиомер, отклоняющий луч света по часовой стрелке, называют правовращающим и обозначают (+), а его антипод – левовращающим (-). 7
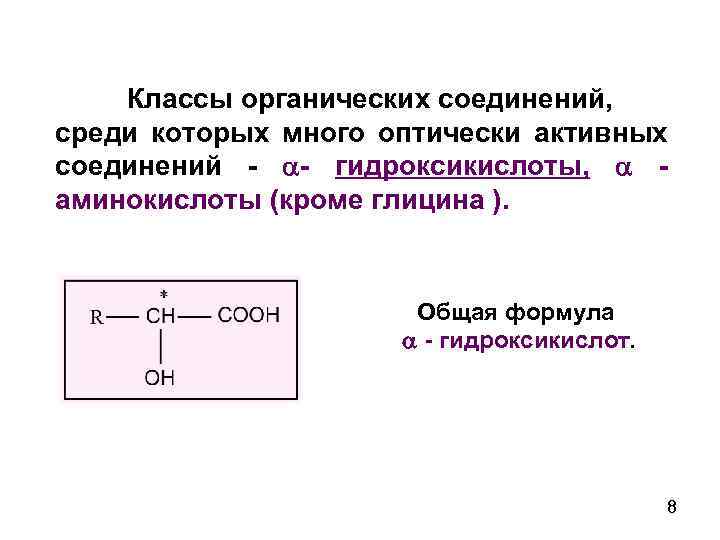 Классы органических соединений, среди которых много оптически активных соединений - - гидроксикислоты, аминокислоты (кроме глицина ). Общая формула - гидроксикислот. 8
Классы органических соединений, среди которых много оптически активных соединений - - гидроксикислоты, аминокислоты (кроме глицина ). Общая формула - гидроксикислот. 8
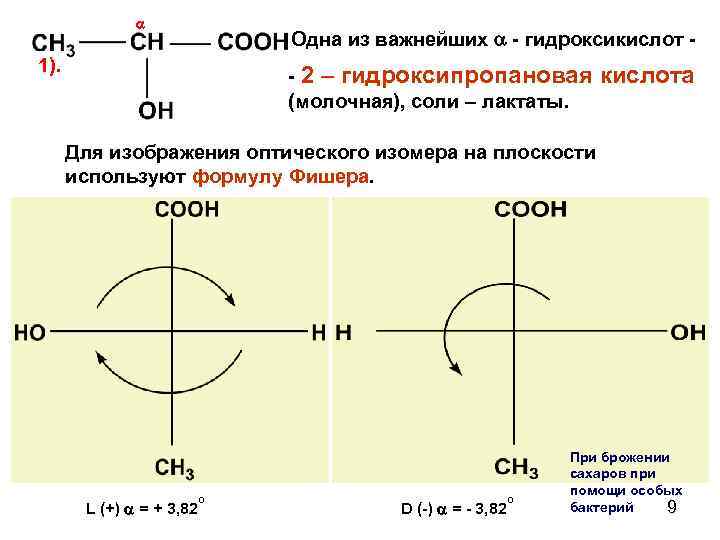 Одна из важнейших - гидроксикислот - 1). - 2 – гидроксипропановая (молочная), соли – лактаты. кислота Для изображения оптического изомера на плоскости используют формулу Фишера. L (+) = + 3, 82 о D (-) = - 3, 82 о При брожении сахаров при помощи особых бактерий 9
Одна из важнейших - гидроксикислот - 1). - 2 – гидроксипропановая (молочная), соли – лактаты. кислота Для изображения оптического изомера на плоскости используют формулу Фишера. L (+) = + 3, 82 о D (-) = - 3, 82 о При брожении сахаров при помощи особых бактерий 9
 (+) – правовращающая молочная кислота – называется мясомолочной. 10
(+) – правовращающая молочная кислота – называется мясомолочной. 10
 Количество энантиомеров определяется по формуле N=2 n, где n – количество хиральных атомов. Для молочной кислоты n = 1, следовательно N = 2, это (+) и (-) формы. Но кроме оптических изомеров всегда существует смесь, состоящая из равных количеств (+) и (-) антиподов. Она называется активной. рацемической и не является оптически 11
Количество энантиомеров определяется по формуле N=2 n, где n – количество хиральных атомов. Для молочной кислоты n = 1, следовательно N = 2, это (+) и (-) формы. Но кроме оптических изомеров всегда существует смесь, состоящая из равных количеств (+) и (-) антиподов. Она называется активной. рацемической и не является оптически 11
 Такой , например, является молочная кислота, полученная под действием молочнокислых бактерий при скисании молока, квашении капусты, солении огурцов, помидоров. 12
Такой , например, является молочная кислота, полученная под действием молочнокислых бактерий при скисании молока, квашении капусты, солении огурцов, помидоров. 12
 способы разделения рацемической смеси: • • 1. Механический – отбор кристаллов по внешнему виду скошенные грани); (кристаллы имеют зеркально- 2. Микробиологический – (+) и (-) оказывают разное физиологическое действие на микроорганизмы, которые избирательно поглощают один антипод. • 3. Хроматографический – расщепление рацематов на оптически активных сорбентах. 13
способы разделения рацемической смеси: • • 1. Механический – отбор кристаллов по внешнему виду скошенные грани); (кристаллы имеют зеркально- 2. Микробиологический – (+) и (-) оказывают разное физиологическое действие на микроорганизмы, которые избирательно поглощают один антипод. • 3. Хроматографический – расщепление рацематов на оптически активных сорбентах. 13
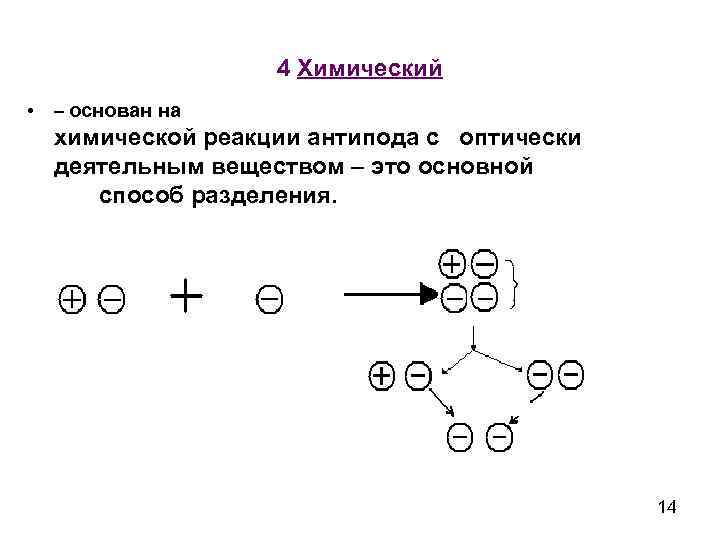 4 Химический • – основан на химической реакции антипода с оптически деятельным веществом – это основной способ разделения. 14
4 Химический • – основан на химической реакции антипода с оптически деятельным веществом – это основной способ разделения. 14
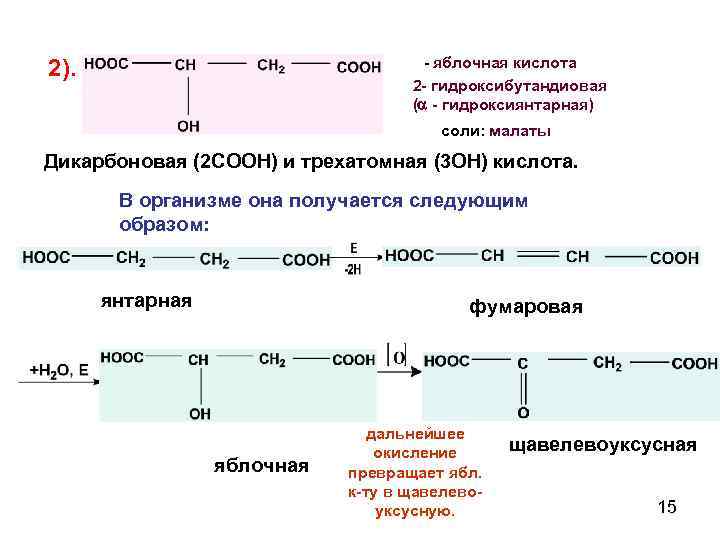 - яблочная кислота 2). 2 - гидроксибутандиовая ( - гидроксиянтарная) соли: малаты Дикарбоновая (2 СООН) и трехатомная (3 ОН) кислота. В организме она получается следующим образом: янтарная фумаровая яблочная дальнейшее окисление превращает ябл. к-ту в щавелевоуксусную. щавелевоуксусная 15
- яблочная кислота 2). 2 - гидроксибутандиовая ( - гидроксиянтарная) соли: малаты Дикарбоновая (2 СООН) и трехатомная (3 ОН) кислота. В организме она получается следующим образом: янтарная фумаровая яблочная дальнейшее окисление превращает ябл. к-ту в щавелевоуксусную. щавелевоуксусная 15
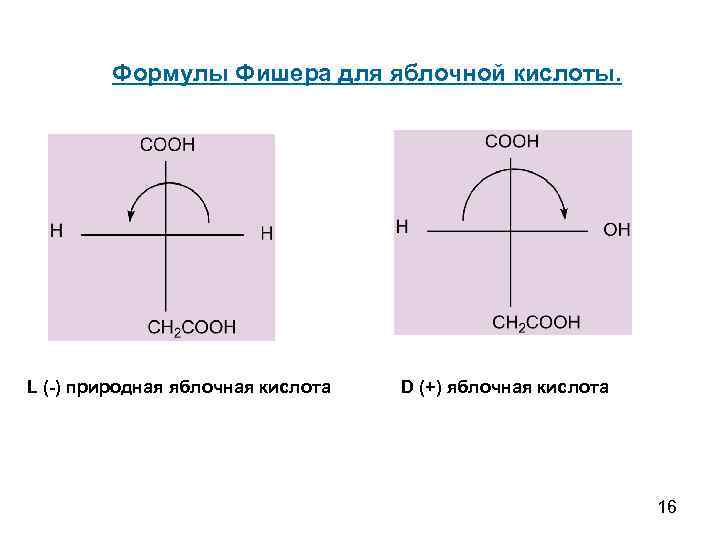 Формулы Фишера для яблочной кислоты. L (-) природная яблочная кислота D (+) яблочная кислота 16
Формулы Фишера для яблочной кислоты. L (-) природная яблочная кислота D (+) яблочная кислота 16
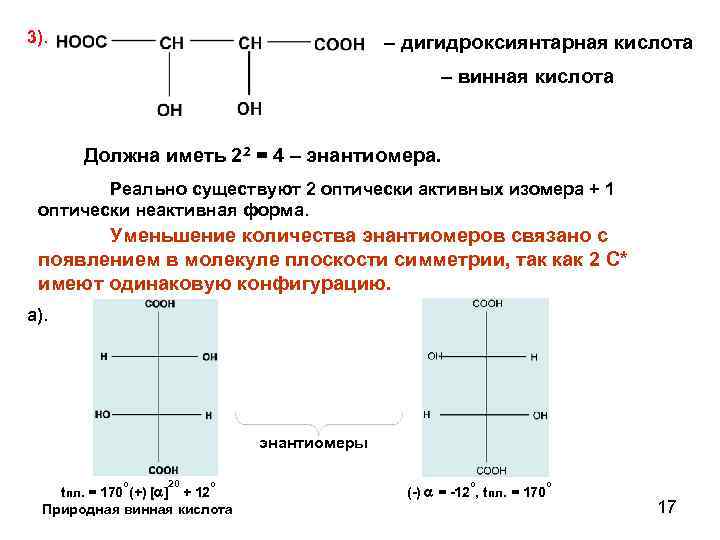 3). – дигидроксиянтарная кислота – винная кислота Должна иметь 22 = 4 – энантиомера. Реально существуют 2 оптически активных изомера + 1 оптически неактивная форма. Уменьшение количества энантиомеров связано с появлением в молекуле плоскости симметрии, так как 2 С* имеют одинаковую конфигурацию. а). энантиомеры о 20 о tпл. = 170 (+) [ ] + 12 Природная винная кислота о (-) = -12 , tпл. = 170 о 17
3). – дигидроксиянтарная кислота – винная кислота Должна иметь 22 = 4 – энантиомера. Реально существуют 2 оптически активных изомера + 1 оптически неактивная форма. Уменьшение количества энантиомеров связано с появлением в молекуле плоскости симметрии, так как 2 С* имеют одинаковую конфигурацию. а). энантиомеры о 20 о tпл. = 170 (+) [ ] + 12 Природная винная кислота о (-) = -12 , tпл. = 170 о 17
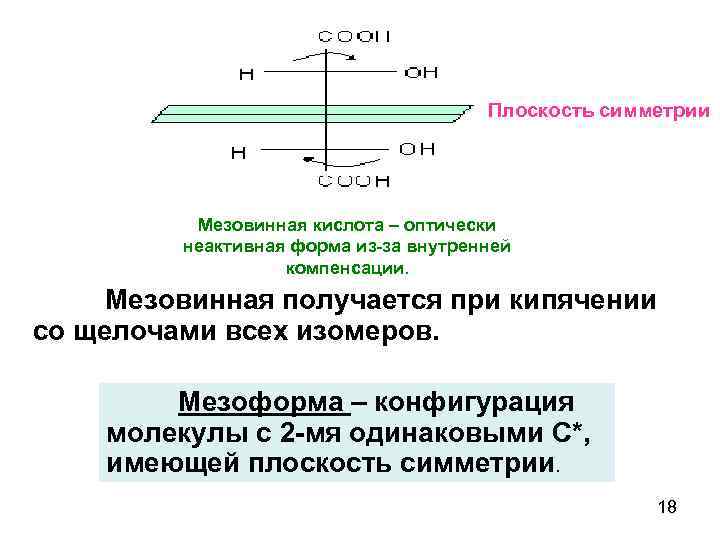 Плоскость симметрии Мезовинная кислота – оптически неактивная форма из-за внутренней компенсации. Мезовинная получается при кипячении со щелочами всех изомеров. Мезоформа – конфигурация молекулы с 2 -мя одинаковыми С*, имеющей плоскость симметрии. 18
Плоскость симметрии Мезовинная кислота – оптически неактивная форма из-за внутренней компенсации. Мезовинная получается при кипячении со щелочами всех изомеров. Мезоформа – конфигурация молекулы с 2 -мя одинаковыми С*, имеющей плоскость симметрии. 18
 г). Рацемическая смесь получается при длительном кипячении с Н 2 О любого изомера. Она называется виноградной кислотой. Это смесь (+) и (-) кислот. Виноградная кислота оптически не активна, отличается по физическим свойствам (tпл. =205 С). При её синтезе всегда получается рацемическая смесь. 19
г). Рацемическая смесь получается при длительном кипячении с Н 2 О любого изомера. Она называется виноградной кислотой. Это смесь (+) и (-) кислот. Виноградная кислота оптически не активна, отличается по физическим свойствам (tпл. =205 С). При её синтезе всегда получается рацемическая смесь. 19
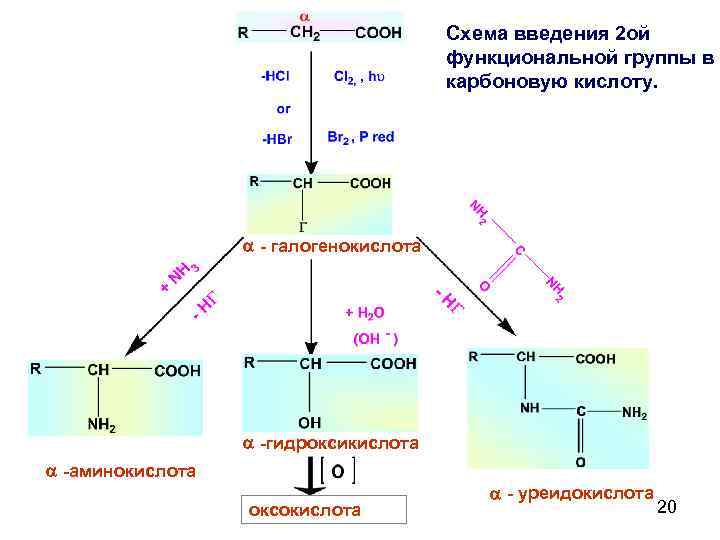 Схема введения 2 ой функциональной группы в карбоновую кислоту. - галогенокислота -гидроксикислота -аминокислота оксокислота - уреидокислота 20
Схема введения 2 ой функциональной группы в карбоновую кислоту. - галогенокислота -гидроксикислота -аминокислота оксокислота - уреидокислота 20
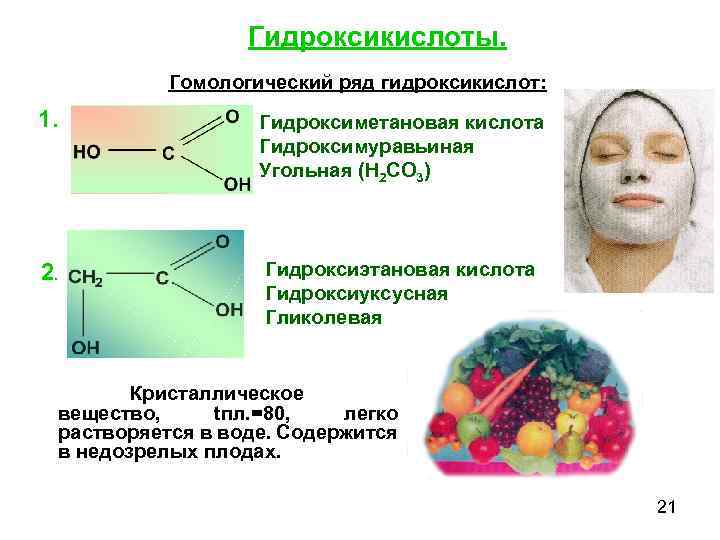 Гидроксикислоты. Гомологический ряд гидроксикислот: 1. Гидроксиметановая кислота Гидроксимуравьиная Угольная (H 2 CO 3) 2. Гидроксиэтановая кислота Гидроксиуксусная Гликолевая Кристаллическое вещество, tпл. =80, легко растворяется в воде. Содержится в недозрелых плодах. 21
Гидроксикислоты. Гомологический ряд гидроксикислот: 1. Гидроксиметановая кислота Гидроксимуравьиная Угольная (H 2 CO 3) 2. Гидроксиэтановая кислота Гидроксиуксусная Гликолевая Кристаллическое вещество, tпл. =80, легко растворяется в воде. Содержится в недозрелых плодах. 21
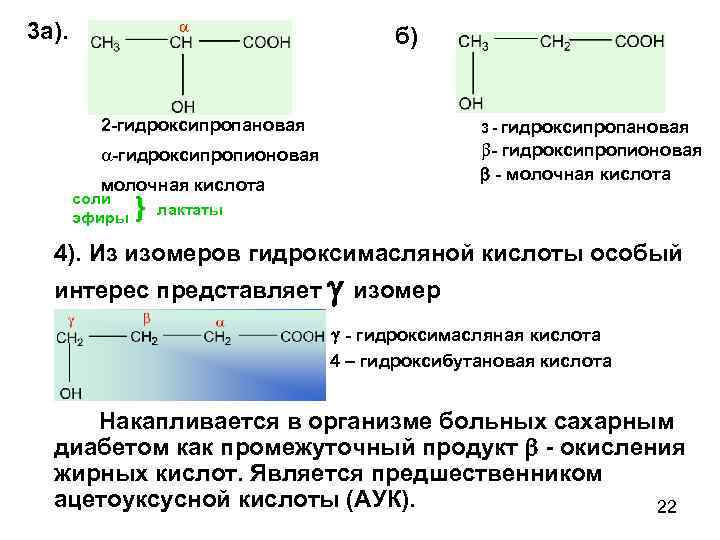 3 а). б) 2 -гидроксипропановая 3 - гидроксипропановая a-гидроксипропионовая b- гидроксипропионовая - молочная кислота соли эфиры } лактаты 4). Из изомеров гидроксимасляной кислоты особый интерес представляет изомер - гидроксимасляная кислота 4 – гидроксибутановая кислота Накапливается в организме больных сахарным диабетом как промежуточный продукт - окисления жирных кислот. Является предшественником ацетоуксусной кислоты (АУК). 22
3 а). б) 2 -гидроксипропановая 3 - гидроксипропановая a-гидроксипропионовая b- гидроксипропионовая - молочная кислота соли эфиры } лактаты 4). Из изомеров гидроксимасляной кислоты особый интерес представляет изомер - гидроксимасляная кислота 4 – гидроксибутановая кислота Накапливается в организме больных сахарным диабетом как промежуточный продукт - окисления жирных кислот. Является предшественником ацетоуксусной кислоты (АУК). 22
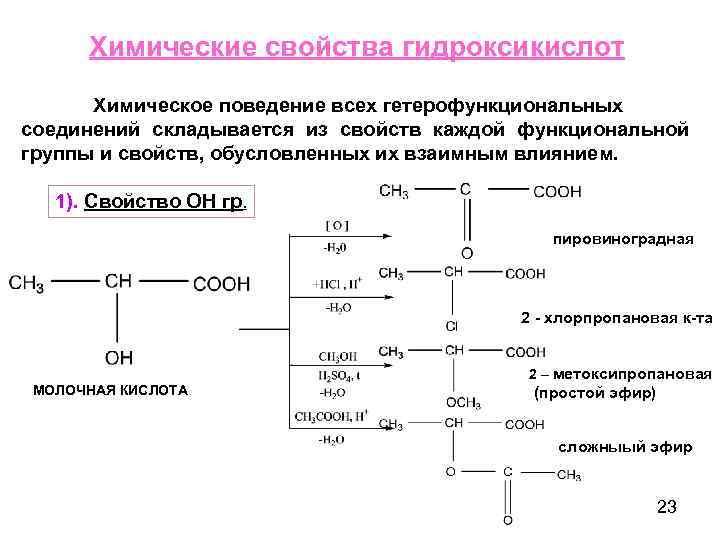 Химические свойства гидроксикислот Химическое поведение всех гетерофункциональных соединений складывается из свойств каждой функциональной группы и свойств, обусловленных их взаимным влиянием. 1). Свойство ОН гр. пировиноградная 2 - хлорпропановая к-та МОЛОЧНАЯ КИСЛОТА 2 – метоксипропановая (простой эфир) сложныый эфир 23
Химические свойства гидроксикислот Химическое поведение всех гетерофункциональных соединений складывается из свойств каждой функциональной группы и свойств, обусловленных их взаимным влиянием. 1). Свойство ОН гр. пировиноградная 2 - хлорпропановая к-та МОЛОЧНАЯ КИСЛОТА 2 – метоксипропановая (простой эфир) сложныый эфир 23
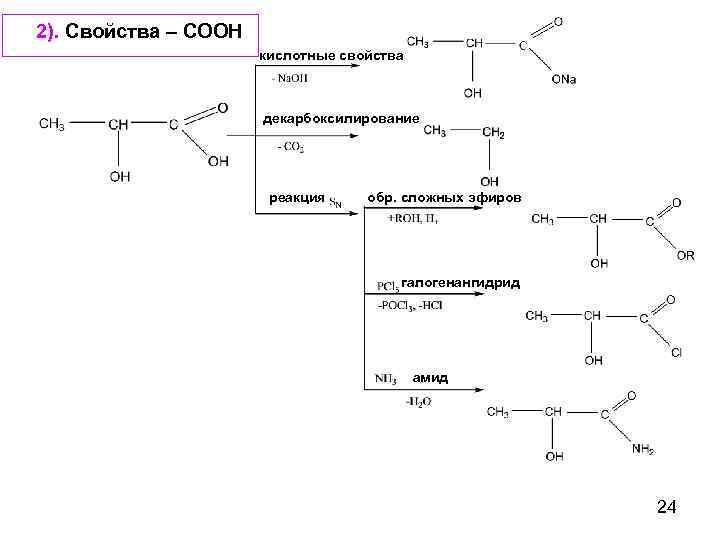 2). Свойства – СООН кислотные свойства декарбоксилирование реакция обр. сложных эфиров галогенангидрид амид 24
2). Свойства – СООН кислотные свойства декарбоксилирование реакция обр. сложных эфиров галогенангидрид амид 24
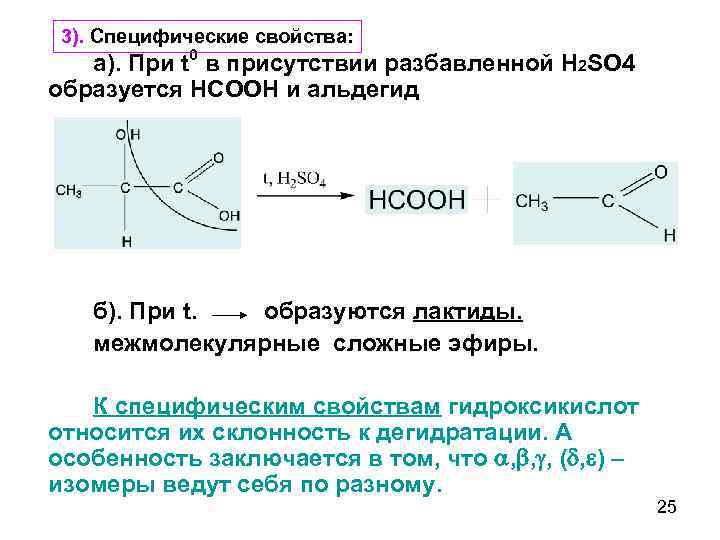 3). Специфические свойства: а). При t 0 в присутствии разбавленной Н 2 SO 4 образуется НСООН и альдегид б). При t. образуются лактиды. межмолекулярные сложные эфиры. К специфическим свойствам гидроксикислот относится их склонность к дегидратации. А особенность заключается в том, что , , , ( , ) – изомеры ведут себя по разному. 25
3). Специфические свойства: а). При t 0 в присутствии разбавленной Н 2 SO 4 образуется НСООН и альдегид б). При t. образуются лактиды. межмолекулярные сложные эфиры. К специфическим свойствам гидроксикислот относится их склонность к дегидратации. А особенность заключается в том, что , , , ( , ) – изомеры ведут себя по разному. 25
 Специфические реакции , , , гидроксикарбоновых кислот при нагревании. 1). - ОН карбоновые кислоты при температуре образуют межмолекулярные циклические сложные эфиры - лактиды. + – УСТОЙЧИВЫЙ ШЕСТИЧЛЕННЫЙ ЦИКЛ - лактид молочной кислоты 26
Специфические реакции , , , гидроксикарбоновых кислот при нагревании. 1). - ОН карбоновые кислоты при температуре образуют межмолекулярные циклические сложные эфиры - лактиды. + – УСТОЙЧИВЫЙ ШЕСТИЧЛЕННЫЙ ЦИКЛ - лактид молочной кислоты 26
 2). - ОН карбоновые кислоты при температуре образуют непредельные кислоты - гидроксимасляная кислота Кротоновая кислота 27
2). - ОН карбоновые кислоты при температуре образуют непредельные кислоты - гидроксимасляная кислота Кротоновая кислота 27
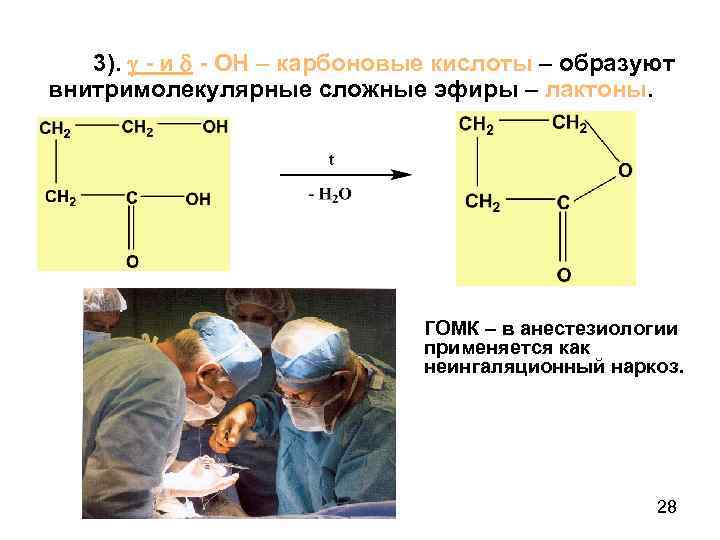 3). - и - ОН – карбоновые кислоты – образуют внитримолекулярные сложные эфиры – лактоны. ГОМК – в анестезиологии применяется как неингаляционный наркоз. 28
3). - и - ОН – карбоновые кислоты – образуют внитримолекулярные сложные эфиры – лактоны. ГОМК – в анестезиологии применяется как неингаляционный наркоз. 28
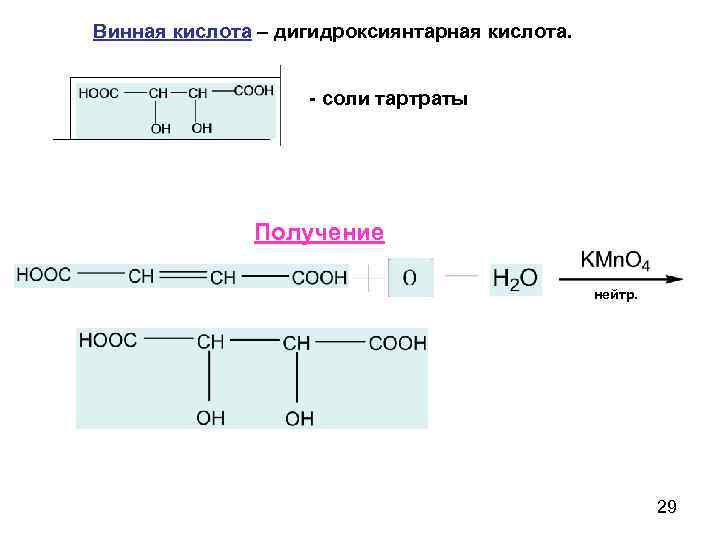 Винная кислота – дигидроксиянтарная кислота. - соли тартраты Получение нейтр. 29
Винная кислота – дигидроксиянтарная кислота. - соли тартраты Получение нейтр. 29
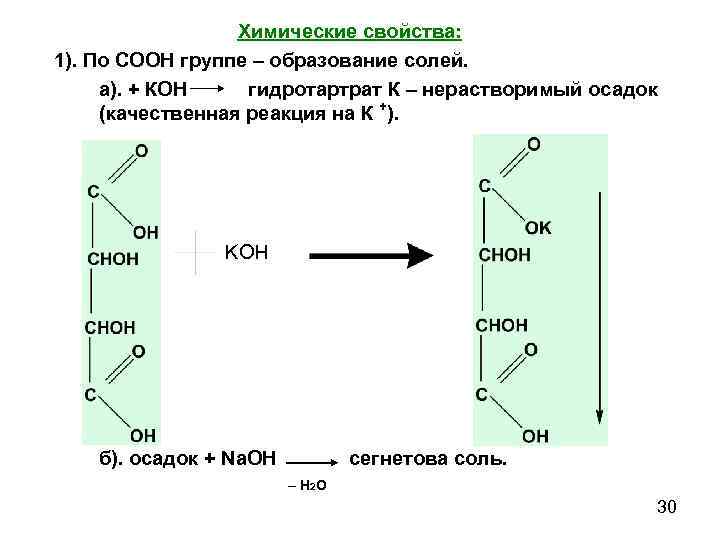 Химические свойства: 1). По СООН группе – образование солей. а). + КОН гидротартрат К – нерастворимый осадок (качественная реакция на К +). KOH б). осадок + Na. OH cегнетова соль. – Н 2 О 30
Химические свойства: 1). По СООН группе – образование солей. а). + КОН гидротартрат К – нерастворимый осадок (качественная реакция на К +). KOH б). осадок + Na. OH cегнетова соль. – Н 2 О 30
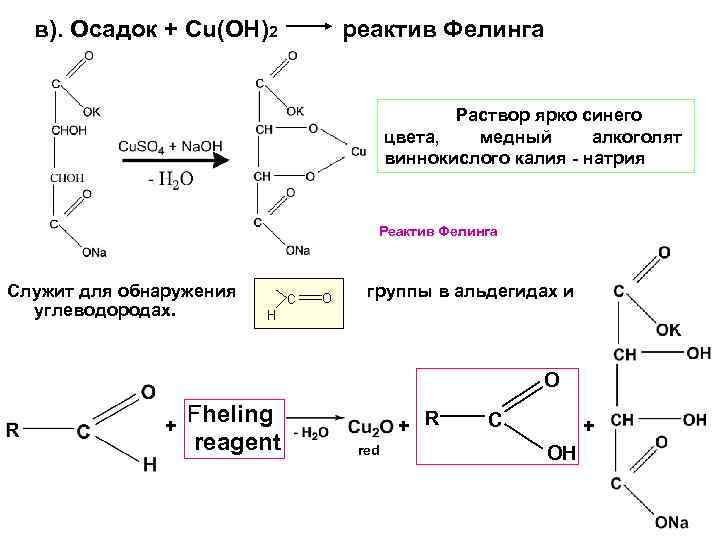 в). Осадок + Cu(OH)2 реактив Фелинга Раствор ярко синего цвета, медный алкоголят виннокислого калия - натрия Реактив Фелинга Служит для обнаружения углеводородах. группы в альдегидах и O + Fheling reagent + R red C + OH 31
в). Осадок + Cu(OH)2 реактив Фелинга Раствор ярко синего цвета, медный алкоголят виннокислого калия - натрия Реактив Фелинга Служит для обнаружения углеводородах. группы в альдегидах и O + Fheling reagent + R red C + OH 31
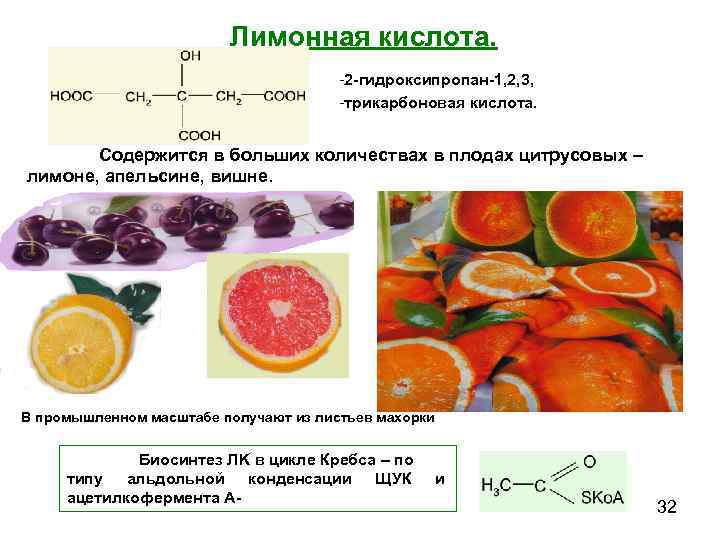 Лимонная кислота. -2 -гидроксипропан-1, 2, 3, -трикарбоновая кислота. Содержится в больших количествах в плодах цитрусовых – лимоне, апельсине, вишне. В промышленном масштабе получают из листьев махорки Биосинтез ЛK в цикле Кребса – по типу альдольной конденсации ЩУК ацетилкофермента А- и 32
Лимонная кислота. -2 -гидроксипропан-1, 2, 3, -трикарбоновая кислота. Содержится в больших количествах в плодах цитрусовых – лимоне, апельсине, вишне. В промышленном масштабе получают из листьев махорки Биосинтез ЛK в цикле Кребса – по типу альдольной конденсации ЩУК ацетилкофермента А- и 32
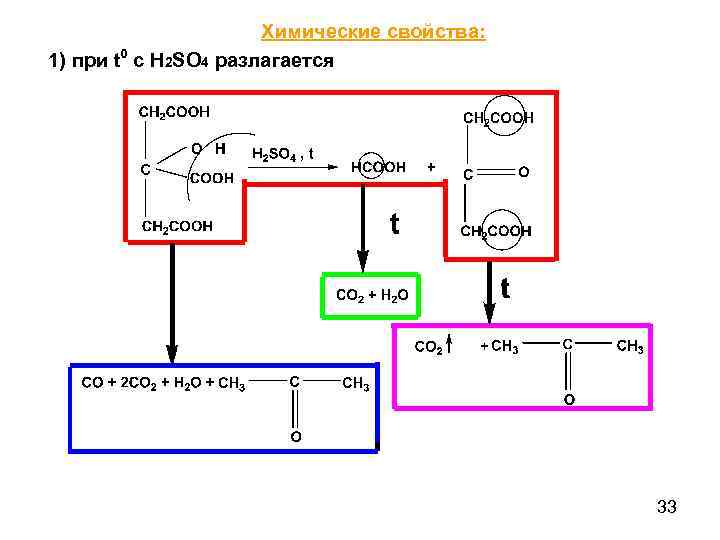 Химические свойства: 1) при t 0 с Н 2 SО 4 разлагается 33
Химические свойства: 1) при t 0 с Н 2 SО 4 разлагается 33
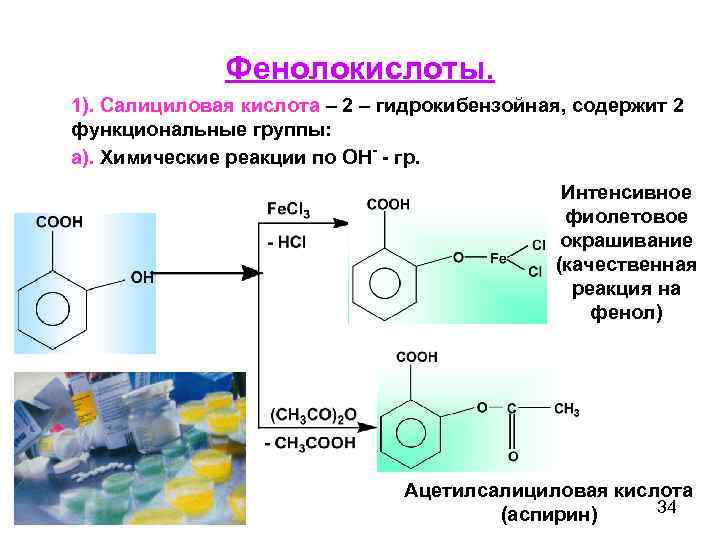 Фенолокислоты. 1). Салициловая кислота – 2 – гидрокибензойная, содержит 2 функциональные группы: а). Химические реакции по ОН- - гр. Интенсивное фиолетовое окрашивание (качественная реакция на фенол) Ацетилсалициловая кислота 34 (аспирин)
Фенолокислоты. 1). Салициловая кислота – 2 – гидрокибензойная, содержит 2 функциональные группы: а). Химические реакции по ОН- - гр. Интенсивное фиолетовое окрашивание (качественная реакция на фенол) Ацетилсалициловая кислота 34 (аспирин)
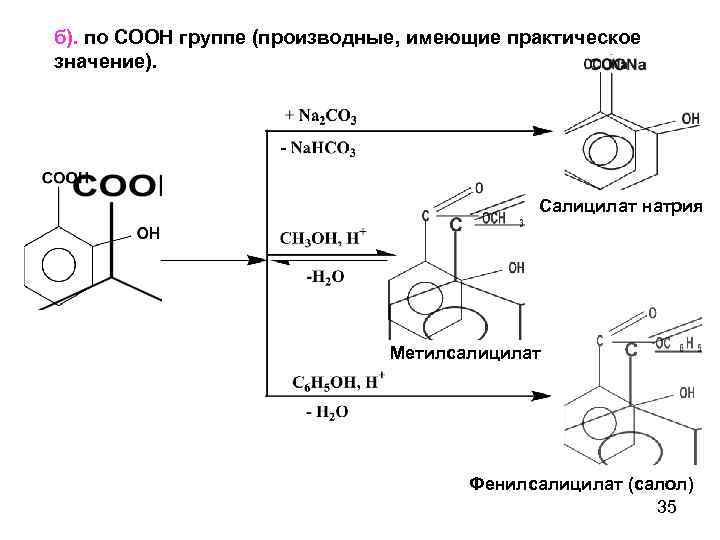 б). по СООН группе (производные, имеющие практическое значение). Салицилат натрия Метилсалицилат Фенилсалицилат (салол) 35
б). по СООН группе (производные, имеющие практическое значение). Салицилат натрия Метилсалицилат Фенилсалицилат (салол) 35
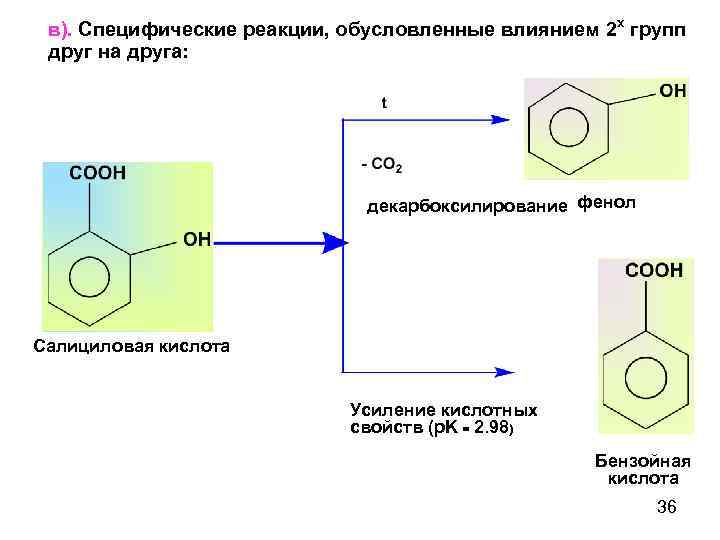 в). Специфические реакции, обусловленные влиянием 2 х групп друг на друга: декарбоксилирование фенол Салициловая кислота Усиление кислотных свойств (p. K = 2. 98) Бензойная кислота 36
в). Специфические реакции, обусловленные влиянием 2 х групп друг на друга: декарбоксилирование фенол Салициловая кислота Усиление кислотных свойств (p. K = 2. 98) Бензойная кислота 36
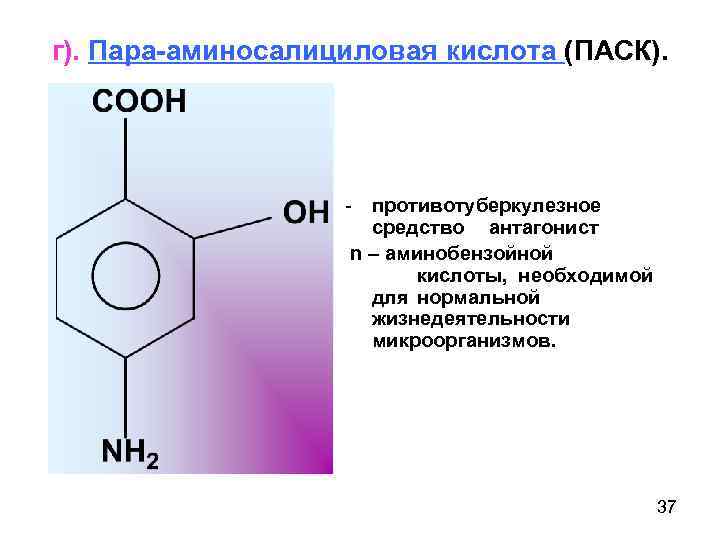 г). Пара-аминосалициловая кислота (ПАСК). - противотуберкулезное средство антагонист n – аминобензойной кислоты, необходимой для нормальной жизнедеятельности микроорганизмов. 37
г). Пара-аминосалициловая кислота (ПАСК). - противотуберкулезное средство антагонист n – аминобензойной кислоты, необходимой для нормальной жизнедеятельности микроорганизмов. 37
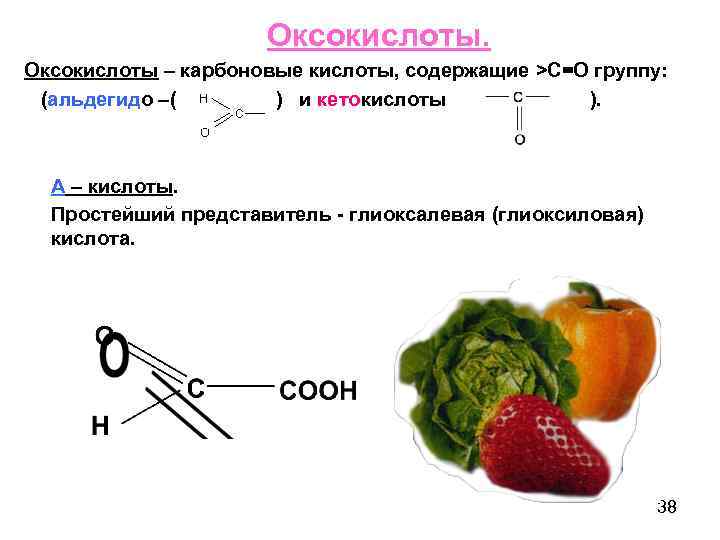 Оксокислоты – карбоновые кислоты, содержащие >С=О группу: (альдегидо –( ) и кетокислоты ). А – кислоты. Простейший представитель - глиоксалевая (глиоксиловая) кислота. 38
Оксокислоты – карбоновые кислоты, содержащие >С=О группу: (альдегидо –( ) и кетокислоты ). А – кислоты. Простейший представитель - глиоксалевая (глиоксиловая) кислота. 38
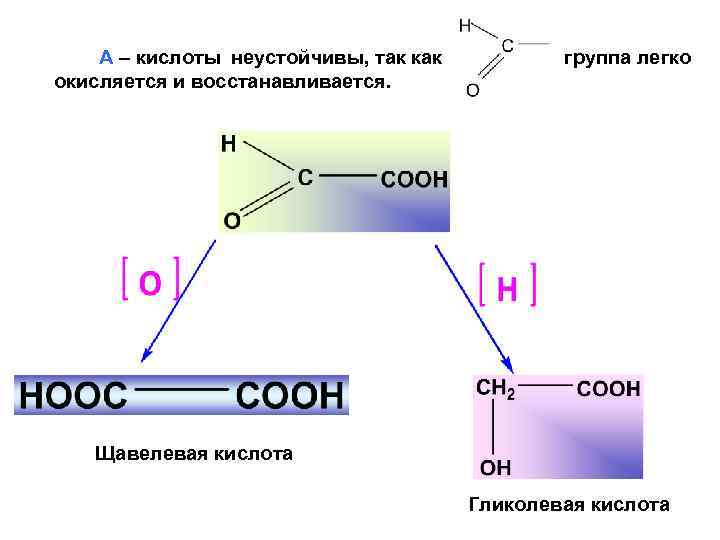 А – кислоты неустойчивы, так как окисляется и восстанавливается. группа легко Щавелевая кислота Гликолевая кислота 39
А – кислоты неустойчивы, так как окисляется и восстанавливается. группа легко Щавелевая кислота Гликолевая кислота 39
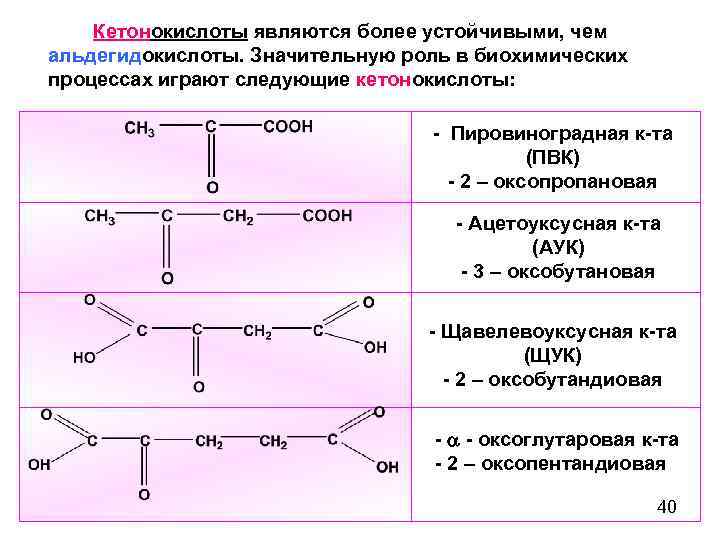 Кетонокислоты являются более устойчивыми, чем альдегидокислоты. Значительную роль в биохимических процессах играют следующие кетонокислоты: - Пировиноградная к-та (ПВК) - 2 – оксопропановая - Ацетоуксусная к-та (АУК) - 3 – оксобутановая - Щавелевоуксусная к-та (ЩУК) - 2 – оксобутандиовая - - оксоглутаровая к-та - 2 – оксопентандиовая 40
Кетонокислоты являются более устойчивыми, чем альдегидокислоты. Значительную роль в биохимических процессах играют следующие кетонокислоты: - Пировиноградная к-та (ПВК) - 2 – оксопропановая - Ацетоуксусная к-та (АУК) - 3 – оксобутановая - Щавелевоуксусная к-та (ЩУК) - 2 – оксобутандиовая - - оксоглутаровая к-та - 2 – оксопентандиовая 40
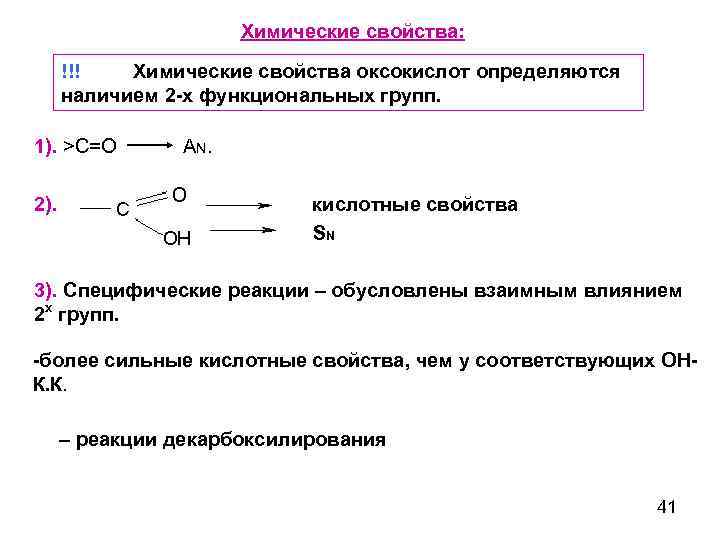 Химические свойства: !!! Химические свойства оксокислот определяются наличием 2 -х функциональных групп. 1). >С=О 2). A N. кислотные свойства SN 3). Специфические реакции – обусловлены взаимным влиянием 2 х групп. -более сильные кислотные свойства, чем у соответствующих ОНК. К. – реакции декарбоксилирования 41
Химические свойства: !!! Химические свойства оксокислот определяются наличием 2 -х функциональных групп. 1). >С=О 2). A N. кислотные свойства SN 3). Специфические реакции – обусловлены взаимным влиянием 2 х групп. -более сильные кислотные свойства, чем у соответствующих ОНК. К. – реакции декарбоксилирования 41
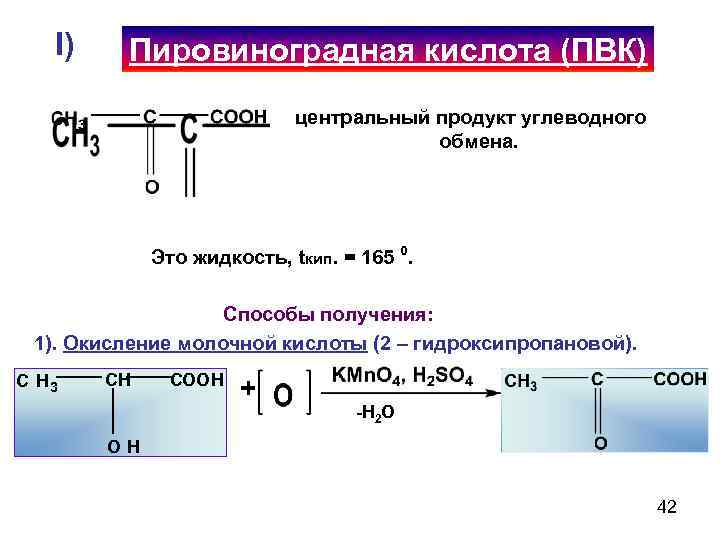 I) Пировиноградная кислота (ПВК) центральный продукт углеводного обмена. Это жидкость, tкип. = 165 0. Cпособы получения: 1). Окисление молочной кислоты (2 – гидроксипропановой). C H 3 CH COOH + -H 2 O OH 42
I) Пировиноградная кислота (ПВК) центральный продукт углеводного обмена. Это жидкость, tкип. = 165 0. Cпособы получения: 1). Окисление молочной кислоты (2 – гидроксипропановой). C H 3 CH COOH + -H 2 O OH 42
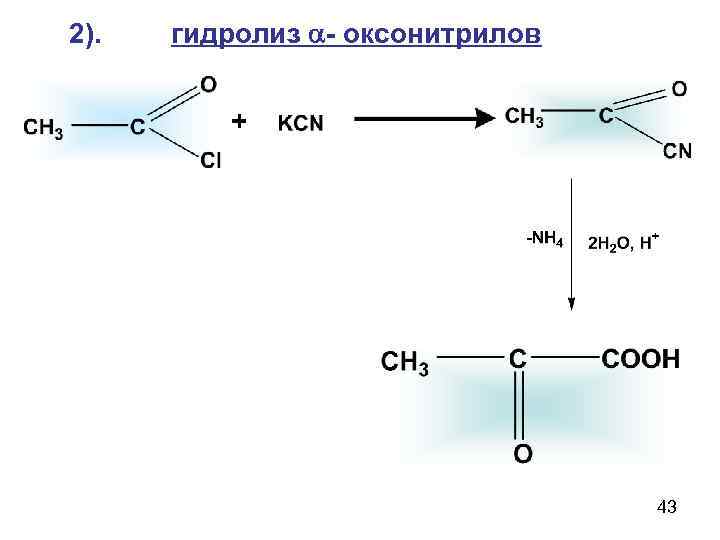 2). гидролиз - оксонитрилов + 43
2). гидролиз - оксонитрилов + 43
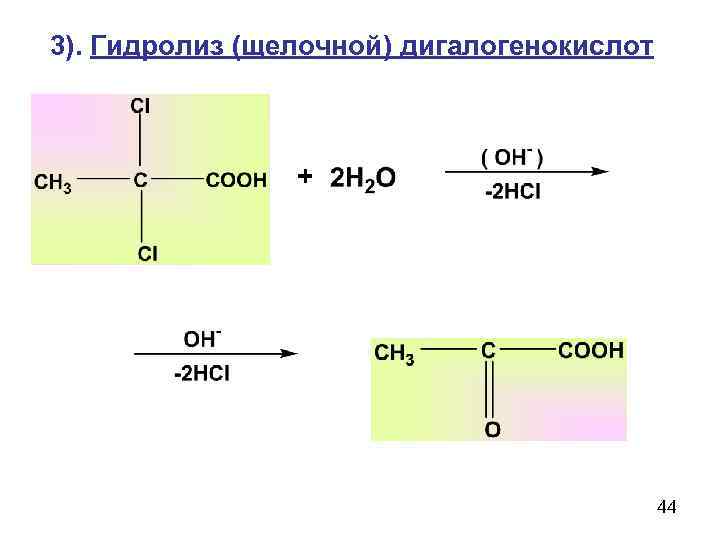 3). Гидролиз (щелочной) дигалогенокислот + 44
3). Гидролиз (щелочной) дигалогенокислот + 44
 Химические свойства. 1)Реакция >С=О - АN. 2) Реакции – СООН – кислые свойства, реакции SN. 3) Специфические реакции, обусловленные влиянием 2 х этих групп друг на друга – декарбоксилирование ( с расщеплением С – С связей). 45
Химические свойства. 1)Реакция >С=О - АN. 2) Реакции – СООН – кислые свойства, реакции SN. 3) Специфические реакции, обусловленные влиянием 2 х этих групп друг на друга – декарбоксилирование ( с расщеплением С – С связей). 45
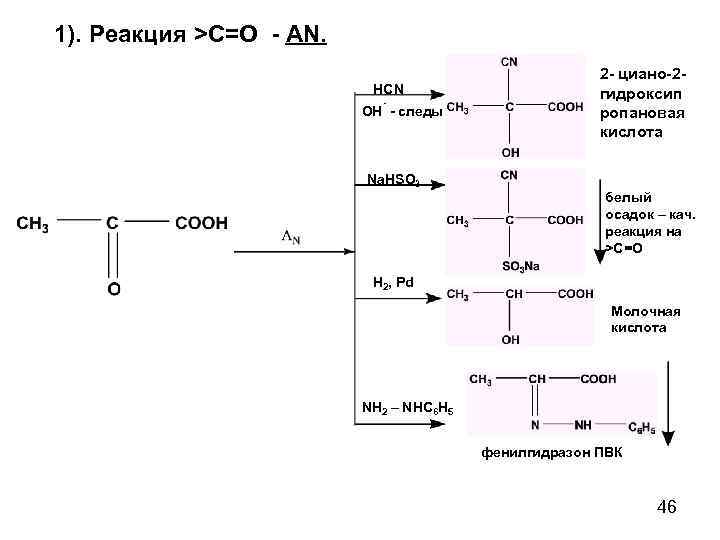 1). Реакция >С=О - AN. HCN - OH - следы 2 - циано-2 гидроксип ропановая кислота Na. HSO 3 белый осадок – кач. реакция на >C=O H 2, Pd Молочная кислота NH 2 – NHC 6 H 5 фенилгидразон ПВК 46
1). Реакция >С=О - AN. HCN - OH - следы 2 - циано-2 гидроксип ропановая кислота Na. HSO 3 белый осадок – кач. реакция на >C=O H 2, Pd Молочная кислота NH 2 – NHC 6 H 5 фенилгидразон ПВК 46
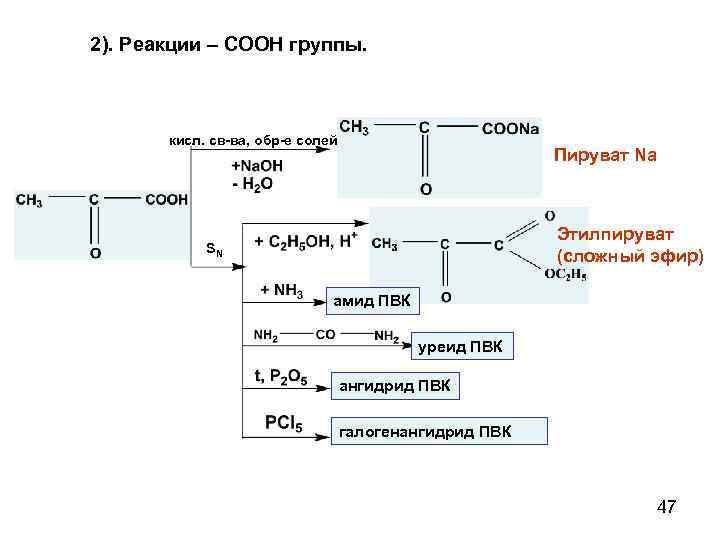 2). Реакции – СООН группы. кисл. св-ва, обр-е солей Пируват Na Этилпируват (сложный эфир) SN амид ПВК уреид ПВК ангидрид ПВК галогенангидрид ПВК 47
2). Реакции – СООН группы. кисл. св-ва, обр-е солей Пируват Na Этилпируват (сложный эфир) SN амид ПВК уреид ПВК ангидрид ПВК галогенангидрид ПВК 47
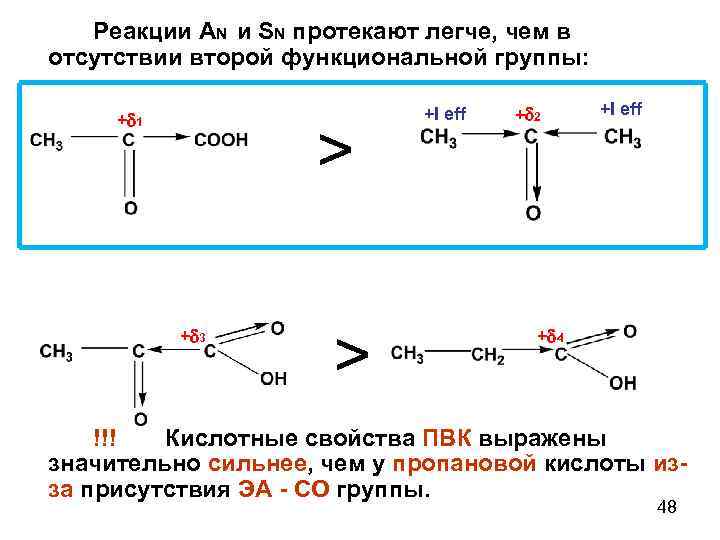 Реакции AN и SN протекают легче, чем в отсутствии второй функциональной группы: + 1 > + 3 > +I eff + 2 +I eff + 4 !!! Кислотные свойства ПВК выражены значительно сильнее, чем у пропановой кислоты изза присутствия ЭА - СО группы. 48
Реакции AN и SN протекают легче, чем в отсутствии второй функциональной группы: + 1 > + 3 > +I eff + 2 +I eff + 4 !!! Кислотные свойства ПВК выражены значительно сильнее, чем у пропановой кислоты изза присутствия ЭА - СО группы. 48
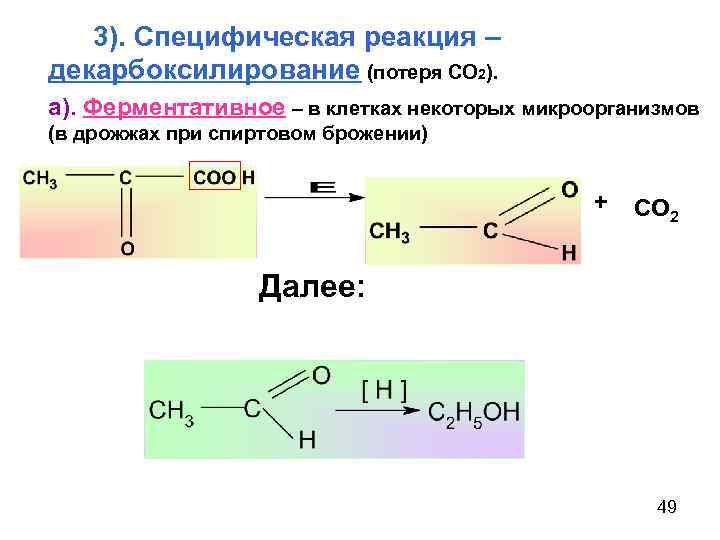 3). Специфическая реакция – декарбоксилирование (потеря СО 2). а). Ферментативное – в клетках некоторых микроорганизмов (в дрожжах при спиртовом брожении) + CO 2 Далее: 49
3). Специфическая реакция – декарбоксилирование (потеря СО 2). а). Ферментативное – в клетках некоторых микроорганизмов (в дрожжах при спиртовом брожении) + CO 2 Далее: 49
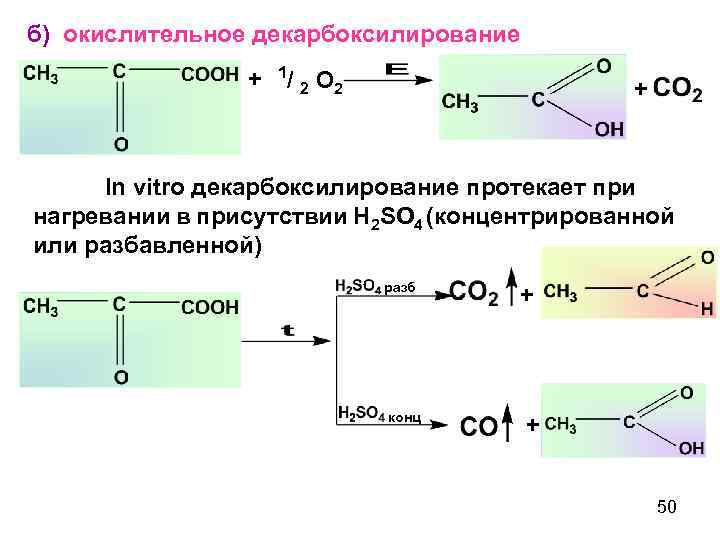 б) окислительное декарбоксилирование + 1 / 2 O 2 + In vitro декарбоксилирование протекает при нагревании в присутствии H 2 SO 4 (концентрированной или разбавленной) разб конц + + 50
б) окислительное декарбоксилирование + 1 / 2 O 2 + In vitro декарбоксилирование протекает при нагревании в присутствии H 2 SO 4 (концентрированной или разбавленной) разб конц + + 50
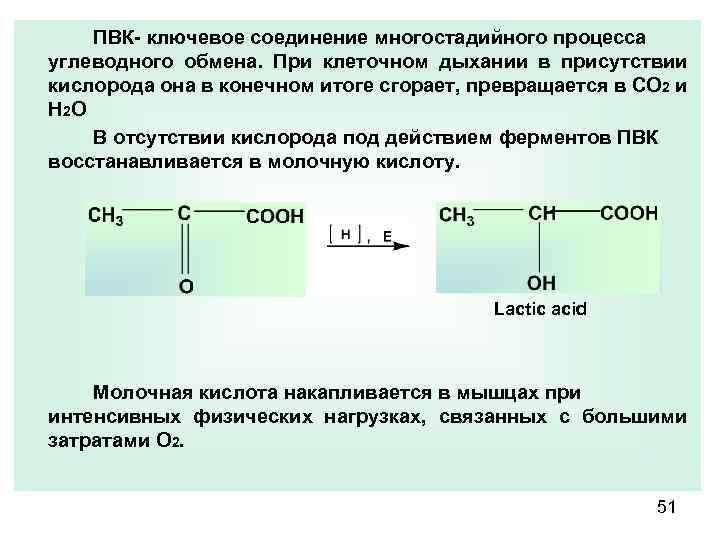 ПВК- ключевое соединение многостадийного процесса углеводного обмена. При клеточном дыхании в присутствии кислорода она в конечном итоге сгорает, превращается в СО 2 и Н 2 О В отсутствии кислорода под действием ферментов ПВК восстанавливается в молочную кислоту. Lactic acid Молочная кислота накапливается в мышцах при интенсивных физических нагрузках, связанных с большими затратами О 2. 51
ПВК- ключевое соединение многостадийного процесса углеводного обмена. При клеточном дыхании в присутствии кислорода она в конечном итоге сгорает, превращается в СО 2 и Н 2 О В отсутствии кислорода под действием ферментов ПВК восстанавливается в молочную кислоту. Lactic acid Молочная кислота накапливается в мышцах при интенсивных физических нагрузках, связанных с большими затратами О 2. 51
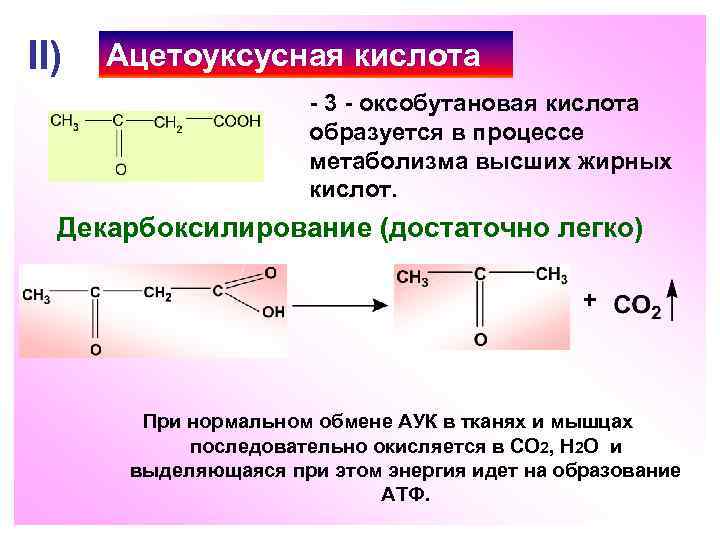 II) Ацетоуксусная кислота - 3 - оксобутановая кислота образуется в процессе метаболизма высших жирных кислот. Декарбоксилирование (достаточно легко) + При нормальном обмене АУК в тканях и мышцах последовательно окисляется в СО 2, Н 2 О и выделяющаяся при этом энергия идет на образование АТФ. 52
II) Ацетоуксусная кислота - 3 - оксобутановая кислота образуется в процессе метаболизма высших жирных кислот. Декарбоксилирование (достаточно легко) + При нормальном обмене АУК в тканях и мышцах последовательно окисляется в СО 2, Н 2 О и выделяющаяся при этом энергия идет на образование АТФ. 52
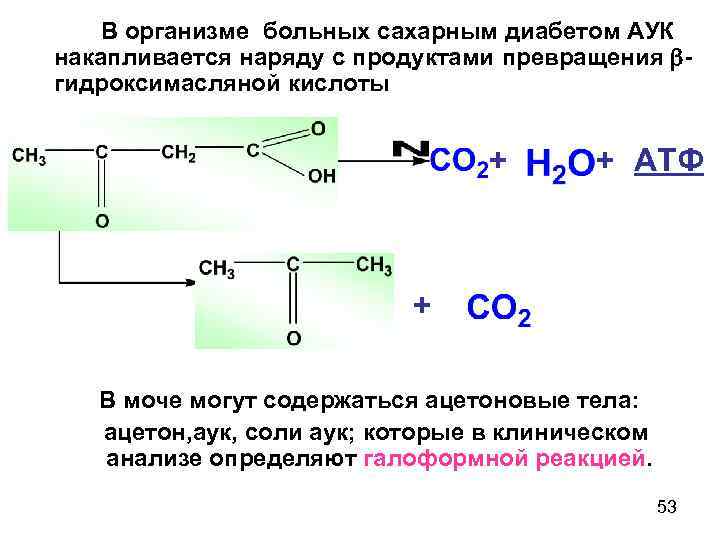 В организме больных сахарным диабетом АУК накапливается наряду с продуктами превращения гидроксимасляной кислоты + + ATФ + В моче могут содержаться ацетоновые тела: ацетон, аук, соли аук; которые в клиническом анализе определяют галоформной реакцией. 53
В организме больных сахарным диабетом АУК накапливается наряду с продуктами превращения гидроксимасляной кислоты + + ATФ + В моче могут содержаться ацетоновые тела: ацетон, аук, соли аук; которые в клиническом анализе определяют галоформной реакцией. 53
 -ацетоуксусный эфир !!! Ацетоуксусный эфир обладает двойственной природой: кетонной и енольной. Кетонная форма - 92. 3% tкип = 78º % содержание кетонных форм зависит от растворителя Енольная форма - 7. 7% tкип = 44º 54
-ацетоуксусный эфир !!! Ацетоуксусный эфир обладает двойственной природой: кетонной и енольной. Кетонная форма - 92. 3% tкип = 78º % содержание кетонных форм зависит от растворителя Енольная форма - 7. 7% tкип = 44º 54
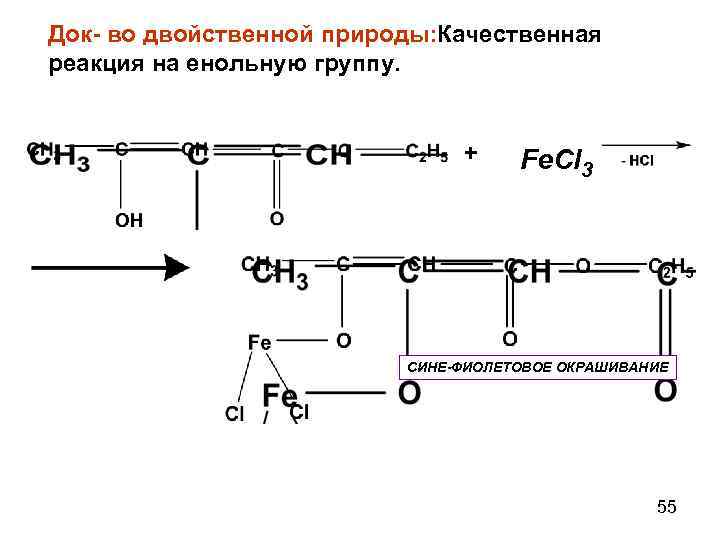 Док- во двойственной природы: Качественная реакция на енольную группу. + Fe. Cl 3 СИНЕ-ФИОЛЕТОВОЕ ОКРАШИВАНИЕ 55
Док- во двойственной природы: Качественная реакция на енольную группу. + Fe. Cl 3 СИНЕ-ФИОЛЕТОВОЕ ОКРАШИВАНИЕ 55
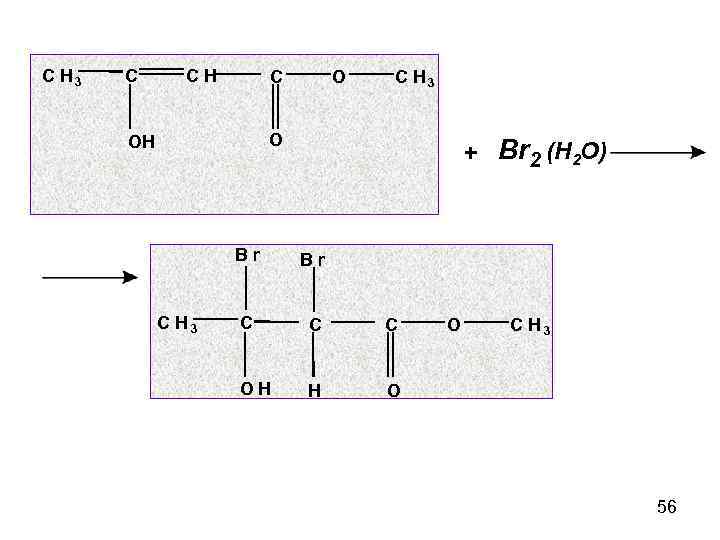 C H 3 C CH C O C H 3 O OH + Br 2 (H 2 O) Br C H 3 Br C C C OH H O O C H 3 56
C H 3 C CH C O C H 3 O OH + Br 2 (H 2 O) Br C H 3 Br C C C OH H O O C H 3 56
 Существование равновесия между кетонной и енольной формами подтверждается этими реакциями. При добавлении избытка Fe. Cl 3 появляется синефиолетовая окраска. При приливании Br 2 фиолетовый цвет исчезает, так комплекс разрушается, бром присоединяется, но появляется вследствие отщепления Fe. Cl 3 желтая окраска. Через некоторое время сине-фиолетовая окраска вновь постепенно появляется в результате превращения новых порций кетонной формы в енольную. 57
Существование равновесия между кетонной и енольной формами подтверждается этими реакциями. При добавлении избытка Fe. Cl 3 появляется синефиолетовая окраска. При приливании Br 2 фиолетовый цвет исчезает, так комплекс разрушается, бром присоединяется, но появляется вследствие отщепления Fe. Cl 3 желтая окраска. Через некоторое время сине-фиолетовая окраска вновь постепенно появляется в результате превращения новых порций кетонной формы в енольную. 57
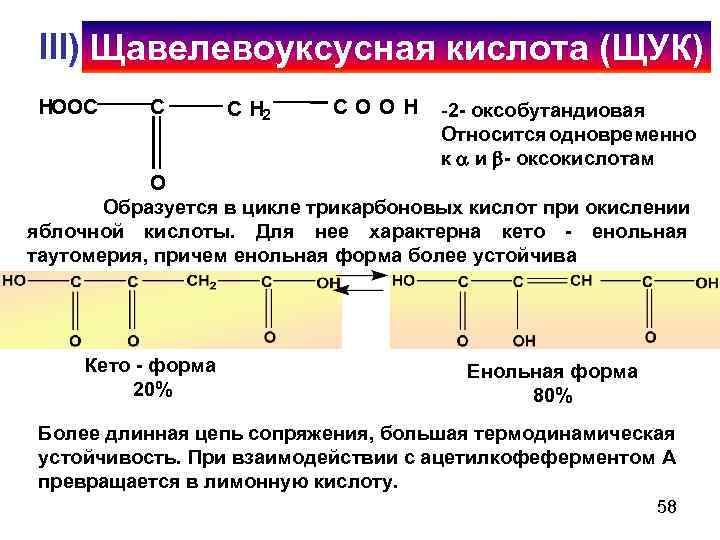 III) Щавелевоуксусная кислота (ЩУК) HOOC C C H 2 COOH -2 - оксобутандиовая Относится одновременно к и - оксокислотам O Образуется в цикле трикарбоновых кислот при окислении яблочной кислоты. Для нее характерна кето - енольная таутомерия, причем енольная форма более устойчива Кето - форма 20% Енольная форма 80% Более длинная цепь сопряжения, большая термодинамическая устойчивость. При взаимодействии с ацетилкофеферментом А превращается в лимонную кислоту. 58
III) Щавелевоуксусная кислота (ЩУК) HOOC C C H 2 COOH -2 - оксобутандиовая Относится одновременно к и - оксокислотам O Образуется в цикле трикарбоновых кислот при окислении яблочной кислоты. Для нее характерна кето - енольная таутомерия, причем енольная форма более устойчива Кето - форма 20% Енольная форма 80% Более длинная цепь сопряжения, большая термодинамическая устойчивость. При взаимодействии с ацетилкофеферментом А превращается в лимонную кислоту. 58
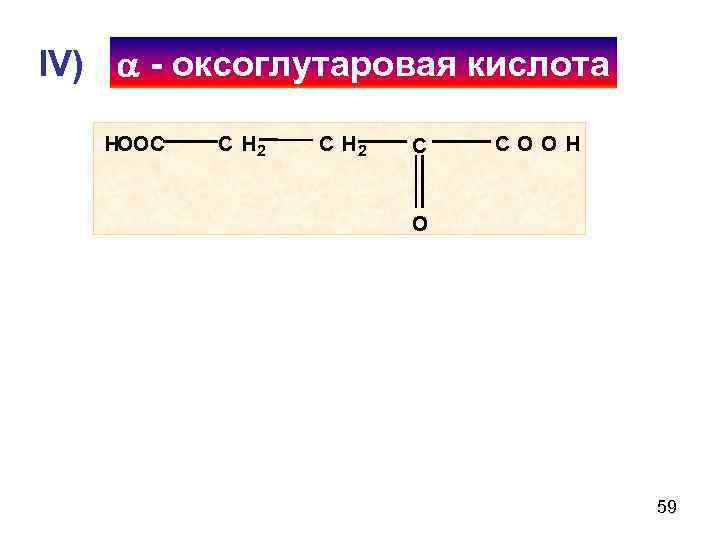 IV) - оксоглутаровая кислота HOOC C H 2 C COOH O 59
IV) - оксоглутаровая кислота HOOC C H 2 C COOH O 59
 Спасибо за внимание! 60
Спасибо за внимание! 60


