ЛЕКЦИЯ 8 Поверхн явл. Адсорбция.ppt
- Количество слайдов: 40
 ЛЕКЦИЯ 8 ФИЗИКО- ХИМИЯ ПОВЕРХНОСТНЫХ ЯВЛЕНИЙ В ФУНКЦИОНИРОВАНИИ ЖИВЫХ ОРГАНИЗМОВ АДСОРБЦИОННЫЕ РАВНОВЕСИЯ
ЛЕКЦИЯ 8 ФИЗИКО- ХИМИЯ ПОВЕРХНОСТНЫХ ЯВЛЕНИЙ В ФУНКЦИОНИРОВАНИИ ЖИВЫХ ОРГАНИЗМОВ АДСОРБЦИОННЫЕ РАВНОВЕСИЯ
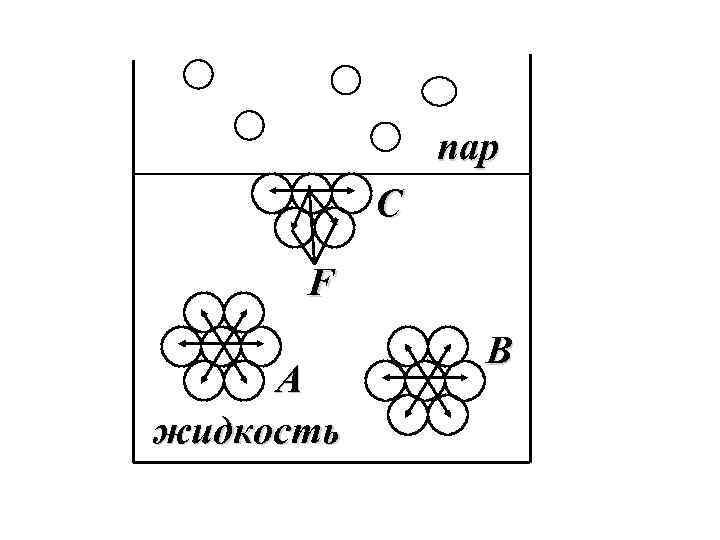 пар С F А жидкость В
пар С F А жидкость В
 Сила, действующая на единицу длины границы раздела и обуславливающая сокращение поверхности жидкости называется поверхностным натяжением (σ) [σ] = Дж/м 2 = H×м/м 2 = [H/м]
Сила, действующая на единицу длины границы раздела и обуславливающая сокращение поверхности жидкости называется поверхностным натяжением (σ) [σ] = Дж/м 2 = H×м/м 2 = [H/м]
 σглицерин=64, 7 Н/м σводы=72, 8 Н/м σсыв. крови=45, 4 Н/м σртути=436 Н/м
σглицерин=64, 7 Н/м σводы=72, 8 Н/м σсыв. крови=45, 4 Н/м σртути=436 Н/м
 Величина поверхностной энергии F = σ×S σ – поверхностное (Дж/м 2) натяжение, S – площадь межфазной поверхности, м 2
Величина поверхностной энергии F = σ×S σ – поверхностное (Дж/м 2) натяжение, S – площадь межфазной поверхности, м 2
 Поверхностная активность d. C и dσ - бесконечно малые изменения концентрации и поверхностного натяжения
Поверхностная активность d. C и dσ - бесконечно малые изменения концентрации и поверхностного натяжения
 1) Растворённое вещество понижает поверхностное натяжение растворителя (ПАВ) (σр-р < σo) g >0
1) Растворённое вещество понижает поверхностное натяжение растворителя (ПАВ) (σр-р < σo) g >0
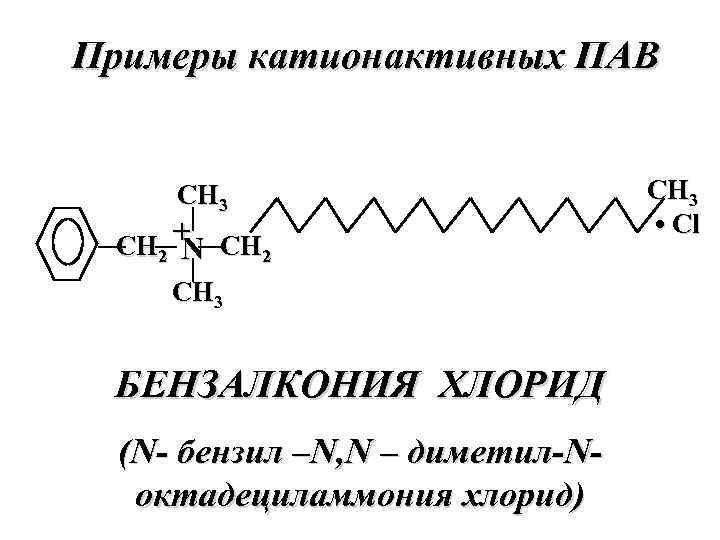 Примеры катионактивных ПАВ СН 3 СН 2 + СН 2 N СН 3 БЕНЗАЛКОНИЯ ХЛОРИД (N- бензил –N, N – диметил-Nоктадециламмония хлорид) СН 3 • Cl
Примеры катионактивных ПАВ СН 3 СН 2 + СН 2 N СН 3 БЕНЗАЛКОНИЯ ХЛОРИД (N- бензил –N, N – диметил-Nоктадециламмония хлорид) СН 3 • Cl
![Пример анионактивных ПАВ Na+[H 3 C – (CH 2)11 – SO 3]лаурилсульфат натрия Пример анионактивных ПАВ Na+[H 3 C – (CH 2)11 – SO 3]лаурилсульфат натрия](https://present5.com/presentation/33918382_133375644/image-9.jpg) Пример анионактивных ПАВ Na+[H 3 C – (CH 2)11 – SO 3]лаурилсульфат натрия
Пример анионактивных ПАВ Na+[H 3 C – (CH 2)11 – SO 3]лаурилсульфат натрия
 2) Растворённое вещество повышает поверхностное натяжение растворителя (ПИВ) (σр-р > σ0) g<0
2) Растворённое вещество повышает поверхностное натяжение растворителя (ПИВ) (σр-р > σ0) g<0
 3) Растворённое вещество практически не изменяет поверхностного натяжения растворителя (ПНА) (σр-р = σ0)
3) Растворённое вещество практически не изменяет поверхностного натяжения растворителя (ПНА) (σр-р = σ0)
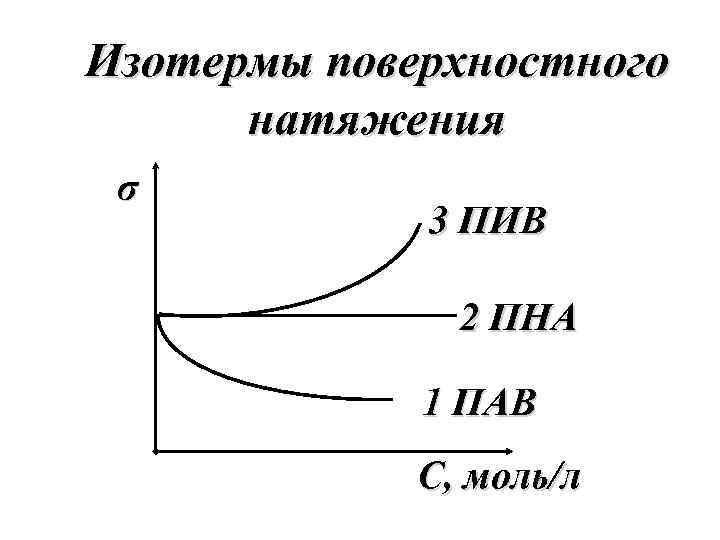 Изотермы поверхностного натяжения σ 3 ПИВ 2 ПНА 1 ПАВ С, моль/л
Изотермы поверхностного натяжения σ 3 ПИВ 2 ПНА 1 ПАВ С, моль/л
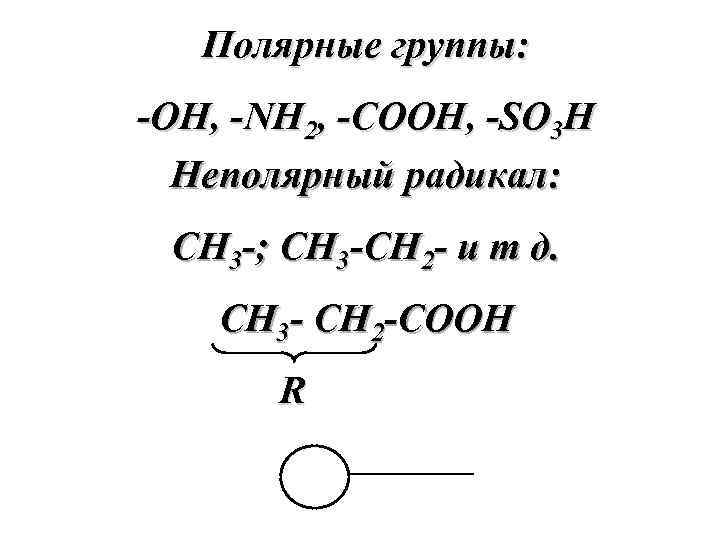 Полярные группы: -OH, -NH 2, -COOH, -SO 3 H Неполярный радикал: СH 3 -; CH 3 -CH 2 - и т д. СH 3 - CH 2 -COOH R
Полярные группы: -OH, -NH 2, -COOH, -SO 3 H Неполярный радикал: СH 3 -; CH 3 -CH 2 - и т д. СH 3 - CH 2 -COOH R
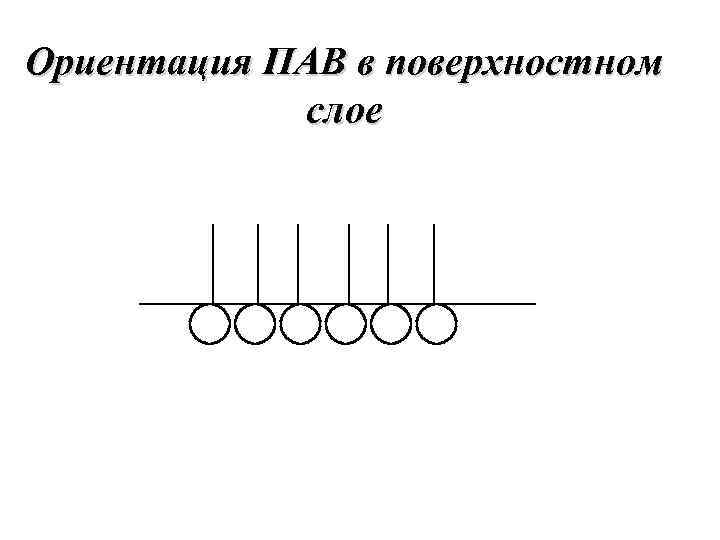 Ориентация ПАВ в поверхностном слое
Ориентация ПАВ в поверхностном слое
 ПРАВИЛО ДЮКЛО-ТРАУБЕ: Поверхностная активность вещества одного и того же гомологического ряда возрастает в 3, 2 раза при удлинении углеводородной цепи на одно звено – СН 2 - (метиленовая группа)
ПРАВИЛО ДЮКЛО-ТРАУБЕ: Поверхностная активность вещества одного и того же гомологического ряда возрастает в 3, 2 раза при удлинении углеводородной цепи на одно звено – СН 2 - (метиленовая группа)
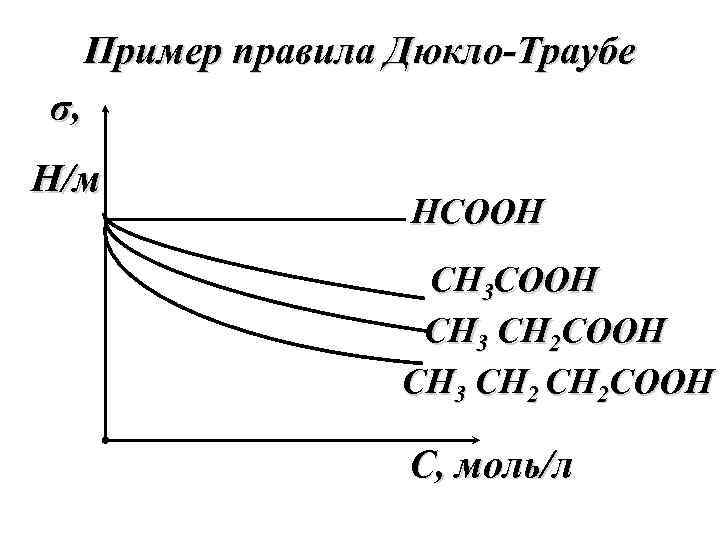 Пример правила Дюкло-Траубе σ, Н/м HCOOH CH 3 CH 2 COOH C, моль/л
Пример правила Дюкло-Траубе σ, Н/м HCOOH CH 3 CH 2 COOH C, моль/л
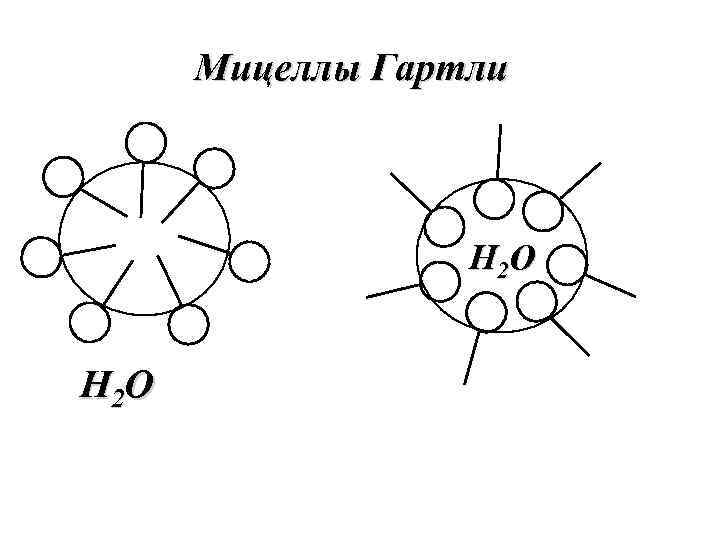 Мицеллы Гартли Н 2 О
Мицеллы Гартли Н 2 О
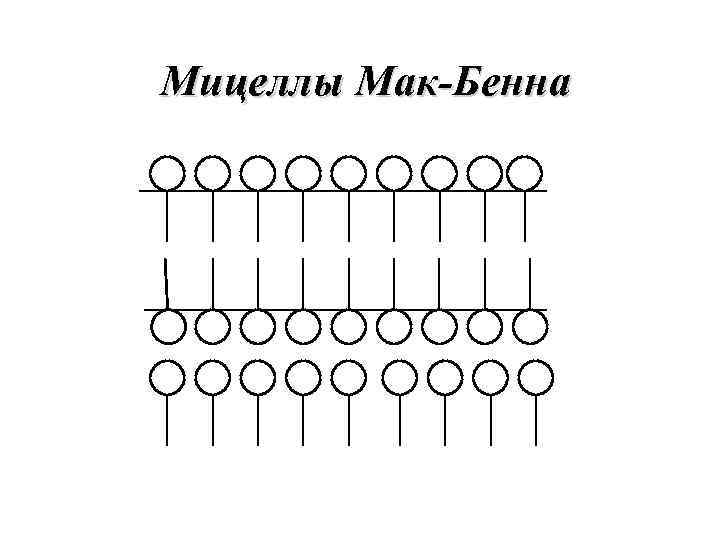 Мицеллы Мак-Бенна
Мицеллы Мак-Бенна
 ЛИПОСОМА
ЛИПОСОМА
![Адсорбция обозначается Г Размерность адсорбции: 2], [моль/см 2] [моль/м Адсорбция обозначается Г Размерность адсорбции: 2], [моль/см 2] [моль/м](https://present5.com/presentation/33918382_133375644/image-20.jpg) Адсорбция обозначается Г Размерность адсорбции: 2], [моль/см 2] [моль/м
Адсорбция обозначается Г Размерность адсорбции: 2], [моль/см 2] [моль/м
 ТИПЫ АДСОРБЦИОННЫХ СИСТЕМ АДСОРБЕНТ АДСОРБТИВ (АДСОРБАТ) твёрдая фаза газ твёрдая фаза жидкость жидкая фаза газ жидкая фаза жидкость
ТИПЫ АДСОРБЦИОННЫХ СИСТЕМ АДСОРБЕНТ АДСОРБТИВ (АДСОРБАТ) твёрдая фаза газ твёрдая фаза жидкость жидкая фаза газ жидкая фаза жидкость
 Адсорбция на границе раздела жидкость/газ и жидкость/жидкость Уравнение ГИББСА
Адсорбция на границе раздела жидкость/газ и жидкость/жидкость Уравнение ГИББСА
 Г – количество адсорбированного вещества (моль/м 2); С – молярная концентрация растворённого вещества (моль/л); R- газовая постоянная, равная 8, 31 Дж/моль×К; - поверхностная активность
Г – количество адсорбированного вещества (моль/м 2); С – молярная концентрация растворённого вещества (моль/л); R- газовая постоянная, равная 8, 31 Дж/моль×К; - поверхностная активность
 АНАЛИЗ УРАВНЕНИЯ ГИББСА 1)Если поверхностное натяжение с ростом концентрации уменьшается, то адсорбция положительная. то Г > 0 2) Если поверхностное натяжение увеличивается с ростом концентрации, то то Г<0
АНАЛИЗ УРАВНЕНИЯ ГИББСА 1)Если поверхностное натяжение с ростом концентрации уменьшается, то адсорбция положительная. то Г > 0 2) Если поверхностное натяжение увеличивается с ростом концентрации, то то Г<0
 АНАЛИЗ УРАВНЕНИЯ ГИББСА 3) Если σ не зависит от концентрации, тогда dσ/d. C=0 и Г=0, адсорбция не наблюдается.
АНАЛИЗ УРАВНЕНИЯ ГИББСА 3) Если σ не зависит от концентрации, тогда dσ/d. C=0 и Г=0, адсорбция не наблюдается.
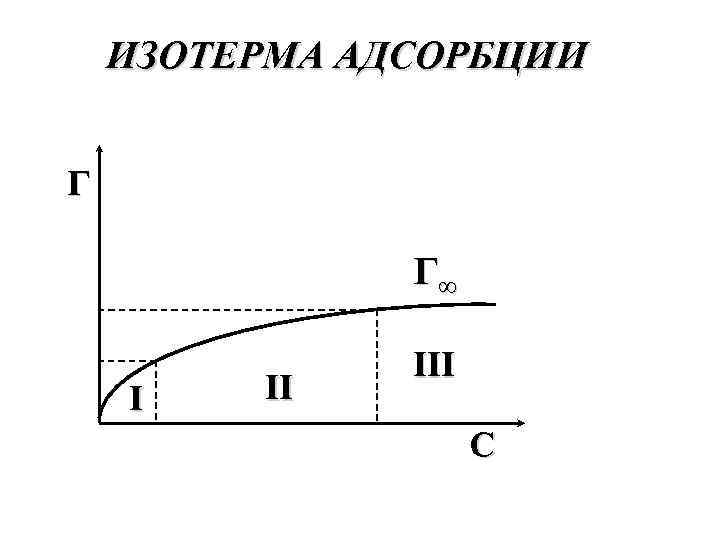 ИЗОТЕРМА АДСОРБЦИИ Г Г∞ I II III С
ИЗОТЕРМА АДСОРБЦИИ Г Г∞ I II III С
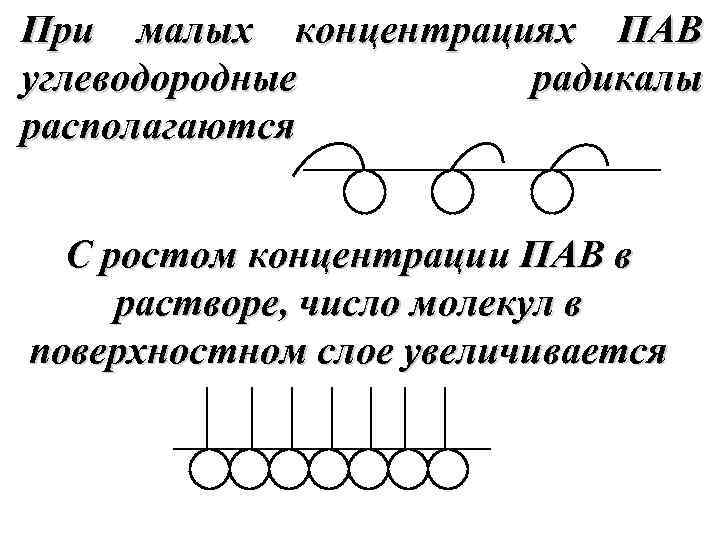 При малых концентрациях ПАВ углеводородные радикалы располагаются С ростом концентрации ПАВ в растворе, число молекул в поверхностном слое увеличивается
При малых концентрациях ПАВ углеводородные радикалы располагаются С ростом концентрации ПАВ в растворе, число молекул в поверхностном слое увеличивается
 Площадь, приходящуюся на 1 молекулу, расположенную в вертикальном положении равна: NA – число Авогадро Г∞ -предельная адсорбция, (моль/м 2)
Площадь, приходящуюся на 1 молекулу, расположенную в вертикальном положении равна: NA – число Авогадро Г∞ -предельная адсорбция, (моль/м 2)
 Длина молекулы ПАВ ρ – плотность ПАВ, кг/м 3; Г∞- предельная адсорбция, моль/м 2; М – молярная масса, кг/моль
Длина молекулы ПАВ ρ – плотность ПАВ, кг/м 3; Г∞- предельная адсорбция, моль/м 2; М – молярная масса, кг/моль
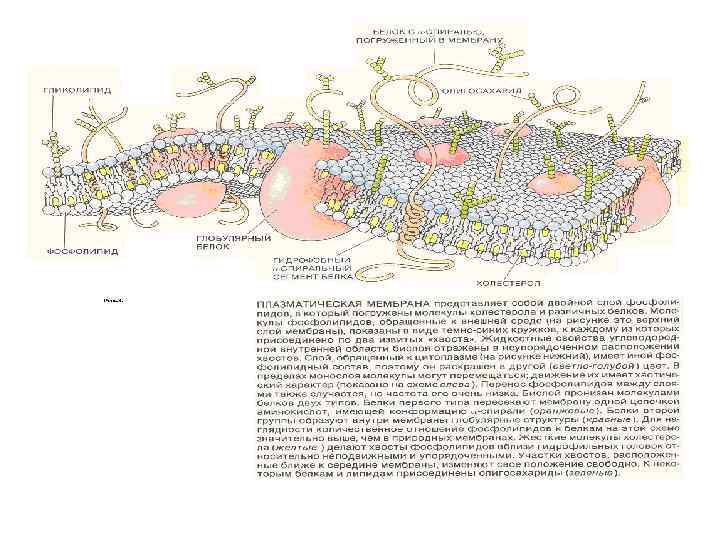
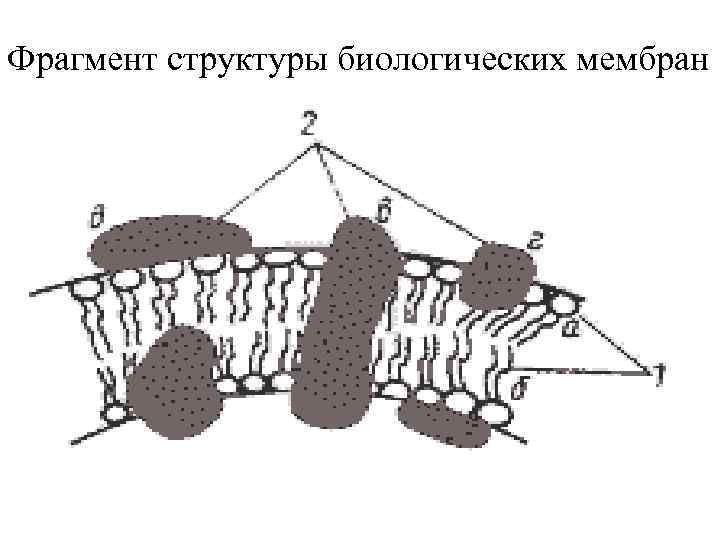 Фрагмент структуры биологических мембран
Фрагмент структуры биологических мембран
 Адсорбция на неподвижных поверхностях раздела Х – количество молей адсорбтива; m – масса адсорбента
Адсорбция на неподвижных поверхностях раздела Х – количество молей адсорбтива; m – масса адсорбента
 УРАВНЕНИЕ ЛЭНГМЮРА для расчёта адсорбции газообразных веществ в случае адсорбции жидких веществ уравнение принимает вид
УРАВНЕНИЕ ЛЭНГМЮРА для расчёта адсорбции газообразных веществ в случае адсорбции жидких веществ уравнение принимает вид
 Гmax- предельная величина адсорбции, моль/см 2; K – константа адсорбционного равновесия, равная отношению констант скоростей процессов десорбции и адсорбции; Р и С – равновесное давление или равновесная концентрация адсорбирующего вещества
Гmax- предельная величина адсорбции, моль/см 2; K – константа адсорбционного равновесия, равная отношению констант скоростей процессов десорбции и адсорбции; Р и С – равновесное давление или равновесная концентрация адсорбирующего вещества
 1) В области низких концентраций и давлений уравнение примет вид:
1) В области низких концентраций и давлений уравнение примет вид:
 2) В области высоких концентраций ( или давлений) (Р>K) и (C>K), тогда уравнение принимает вид
2) В области высоких концентраций ( или давлений) (Р>K) и (C>K), тогда уравнение принимает вид
 3) Для определения адсорбции в области средних концентраций пользуются уравнением ФРЕЙНДЛИХА Г = Кф × С n Кф- константа Фрейндлиха; Кф и n – константы, которые находятся графически по логарифмическому выражению уравнения Фрейндлиха
3) Для определения адсорбции в области средних концентраций пользуются уравнением ФРЕЙНДЛИХА Г = Кф × С n Кф- константа Фрейндлиха; Кф и n – константы, которые находятся графически по логарифмическому выражению уравнения Фрейндлиха
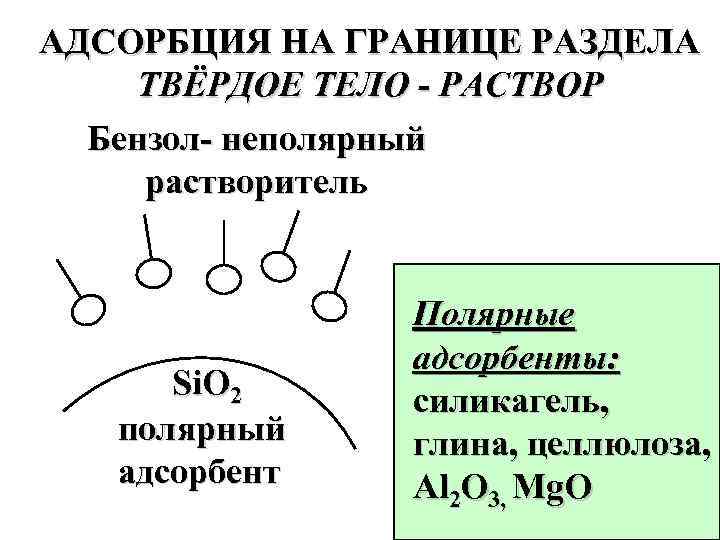 АДСОРБЦИЯ НА ГРАНИЦЕ РАЗДЕЛА ТВЁРДОЕ ТЕЛО - РАСТВОР Бензол- неполярный растворитель Si. O 2 полярный адсорбент Полярные адсорбенты: силикагель, глина, целлюлоза, Аl 2 O 3, Mg. O
АДСОРБЦИЯ НА ГРАНИЦЕ РАЗДЕЛА ТВЁРДОЕ ТЕЛО - РАСТВОР Бензол- неполярный растворитель Si. O 2 полярный адсорбент Полярные адсорбенты: силикагель, глина, целлюлоза, Аl 2 O 3, Mg. O
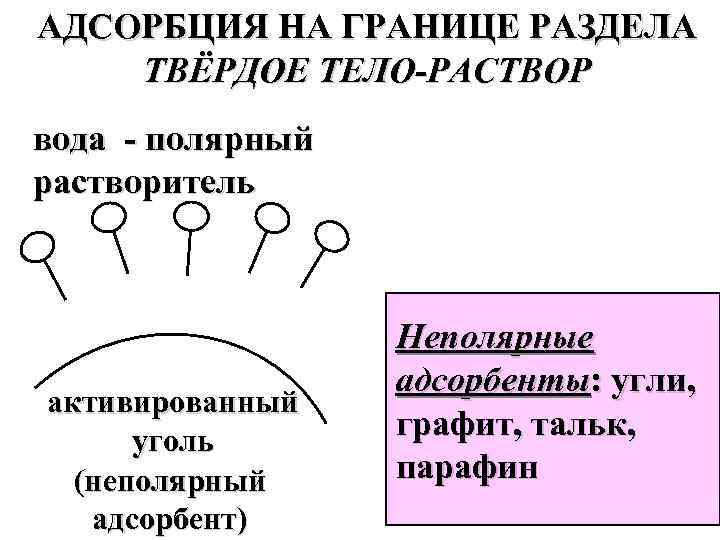 АДСОРБЦИЯ НА ГРАНИЦЕ РАЗДЕЛА ТВЁРДОЕ ТЕЛО-РАСТВОР вода - полярный растворитель активированный уголь (неполярный адсорбент) Неполярные адсорбенты: угли, графит, тальк, парафин
АДСОРБЦИЯ НА ГРАНИЦЕ РАЗДЕЛА ТВЁРДОЕ ТЕЛО-РАСТВОР вода - полярный растворитель активированный уголь (неполярный адсорбент) Неполярные адсорбенты: угли, графит, тальк, парафин
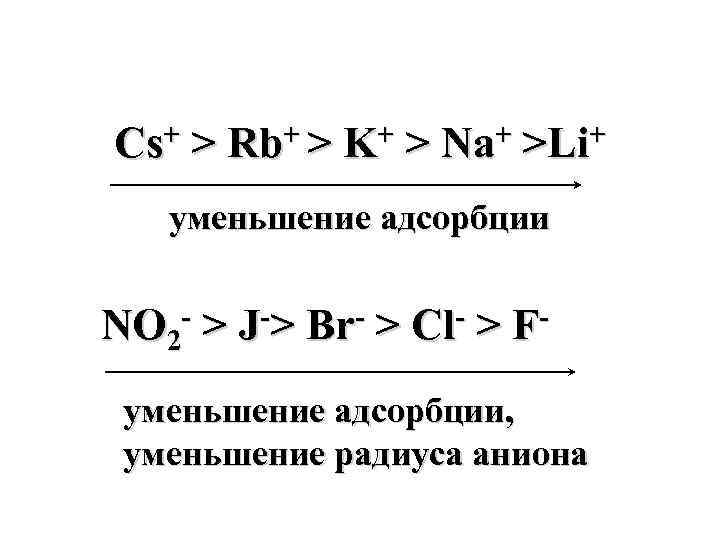 Cs+ > Rb+ > K+ > Na+ >Li+ уменьшение адсорбции NO 2 - > J-> Br- > Cl- > Fуменьшение адсорбции, уменьшение радиуса аниона
Cs+ > Rb+ > K+ > Na+ >Li+ уменьшение адсорбции NO 2 - > J-> Br- > Cl- > Fуменьшение адсорбции, уменьшение радиуса аниона


