Л_08-SPA-Метод осаждения_Механизм осаждения.ppt
- Количество слайдов: 26
 Лекция 8 7. Получение массивных катализаторов методом осаждения 7. 1. Технологические аспекты метода осаждения из растворов 7. 1. 1. Основные этапы синтеза катализаторов методом осаждения 7. 1. 2. Технологические приёмы проведения стадии осаждения 7. 1. 3. Основные параметры и факторы осаждения 7. 2. Механизмы формирования гидроксидов металлов 7. 2. 1. Старение осадков под маточным раствором 7. 2. 2. Классификация осадков по способности к кристаллизации при старении 7. 3. Основы классической теории конденсации 7. 3. 1. Классическая теория конденсации и общий механизм осаждения гидроксидов 7. 3. 2. Причины неадекватности классической теории конденсации в интерпретации закономерностей формирования ПЧ гидроксидов катионов I-III групп
Лекция 8 7. Получение массивных катализаторов методом осаждения 7. 1. Технологические аспекты метода осаждения из растворов 7. 1. 1. Основные этапы синтеза катализаторов методом осаждения 7. 1. 2. Технологические приёмы проведения стадии осаждения 7. 1. 3. Основные параметры и факторы осаждения 7. 2. Механизмы формирования гидроксидов металлов 7. 2. 1. Старение осадков под маточным раствором 7. 2. 2. Классификация осадков по способности к кристаллизации при старении 7. 3. Основы классической теории конденсации 7. 3. 1. Классическая теория конденсации и общий механизм осаждения гидроксидов 7. 3. 2. Причины неадекватности классической теории конденсации в интерпретации закономерностей формирования ПЧ гидроксидов катионов I-III групп
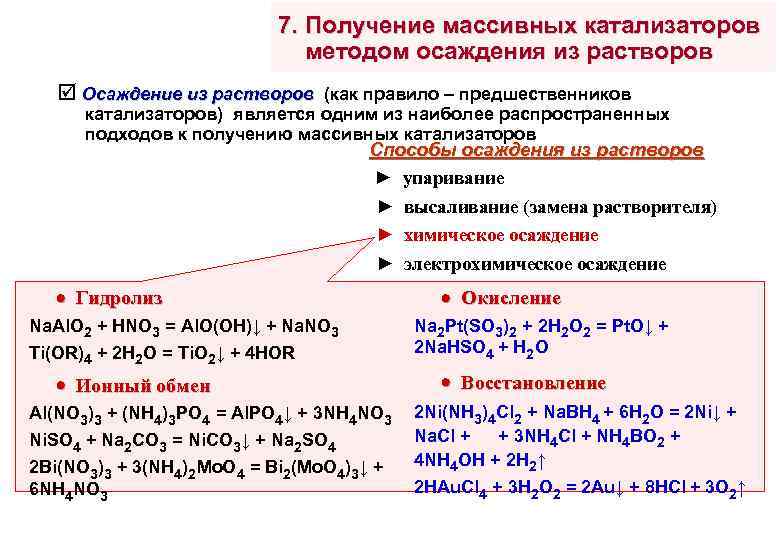 7. Получение массивных катализаторов методом осаждения из растворов Осаждение из растворов (как правило – предшественников катализаторов) является одним из наиболее распространенных подходов к получению массивных катализаторов Способы осаждения из растворов ► упаривание ► высаливание (замена растворителя) ► химическое осаждение ► электрохимическое осаждение Гидролиз Na. Al. O 2 + HNO 3 = Al. O(OH)↓ + Na. NO 3 Ti(OR)4 + 2 H 2 O = Ti. O 2↓ + 4 HOR Ионный обмен Al(NO 3)3 + (NH 4)3 PO 4 = Al. PO 4↓ + 3 NH 4 NO 3 Ni. SO 4 + Na 2 CO 3 = Ni. CO 3↓ + Na 2 SO 4 2 Bi(NO 3)3 + 3(NH 4)2 Mo. O 4 = Bi 2(Mo. O 4)3↓ + 6 NH 4 NO 3 Окисление Na 2 Pt(SO 3)2 + 2 H 2 O 2 = Pt. O↓ + 2 Na. HSO 4 + H 2 O Восстановление 2 Ni(NH 3)4 Cl 2 + Na. BH 4 + 6 H 2 O = 2 Ni↓ + Na. Cl + + 3 NH 4 Cl + NH 4 BO 2 + 4 NH 4 OH + 2 H 2↑ 2 HAu. Cl 4 + 3 H 2 O 2 = 2 Au↓ + 8 HCl + 3 O 2↑
7. Получение массивных катализаторов методом осаждения из растворов Осаждение из растворов (как правило – предшественников катализаторов) является одним из наиболее распространенных подходов к получению массивных катализаторов Способы осаждения из растворов ► упаривание ► высаливание (замена растворителя) ► химическое осаждение ► электрохимическое осаждение Гидролиз Na. Al. O 2 + HNO 3 = Al. O(OH)↓ + Na. NO 3 Ti(OR)4 + 2 H 2 O = Ti. O 2↓ + 4 HOR Ионный обмен Al(NO 3)3 + (NH 4)3 PO 4 = Al. PO 4↓ + 3 NH 4 NO 3 Ni. SO 4 + Na 2 CO 3 = Ni. CO 3↓ + Na 2 SO 4 2 Bi(NO 3)3 + 3(NH 4)2 Mo. O 4 = Bi 2(Mo. O 4)3↓ + 6 NH 4 NO 3 Окисление Na 2 Pt(SO 3)2 + 2 H 2 O 2 = Pt. O↓ + 2 Na. HSO 4 + H 2 O Восстановление 2 Ni(NH 3)4 Cl 2 + Na. BH 4 + 6 H 2 O = 2 Ni↓ + Na. Cl + + 3 NH 4 Cl + NH 4 BO 2 + 4 NH 4 OH + 2 H 2↑ 2 HAu. Cl 4 + 3 H 2 O 2 = 2 Au↓ + 8 HCl + 3 O 2↑
 Достоинства метода ● Многостадийность, что позволяет надежно контролировать протекание физико-химических процессов и благодаря этому целенаправленно регулировать химический и фазовый состав, дисперсность и морфологию частиц промежуточных продуктов ● Универсален для получения предшественников различной природы: гидроксидов и оксидов, солей и комплексов, металлических черней, поэтому применим для синтеза широкого ассортимента катализаторов (массивных и нанесенных, одно- и многокомпонентных) ● Достигается однородное на молекулярном уровне смешение и равномерное распределение компонентов в катализаторе Недостатки метода ● Многостадийность, что усложняет технологию производства ● Использование агрессивных реагентов ● Большое количество сточных вод и вредных выбросов
Достоинства метода ● Многостадийность, что позволяет надежно контролировать протекание физико-химических процессов и благодаря этому целенаправленно регулировать химический и фазовый состав, дисперсность и морфологию частиц промежуточных продуктов ● Универсален для получения предшественников различной природы: гидроксидов и оксидов, солей и комплексов, металлических черней, поэтому применим для синтеза широкого ассортимента катализаторов (массивных и нанесенных, одно- и многокомпонентных) ● Достигается однородное на молекулярном уровне смешение и равномерное распределение компонентов в катализаторе Недостатки метода ● Многостадийность, что усложняет технологию производства ● Использование агрессивных реагентов ● Большое количество сточных вод и вредных выбросов
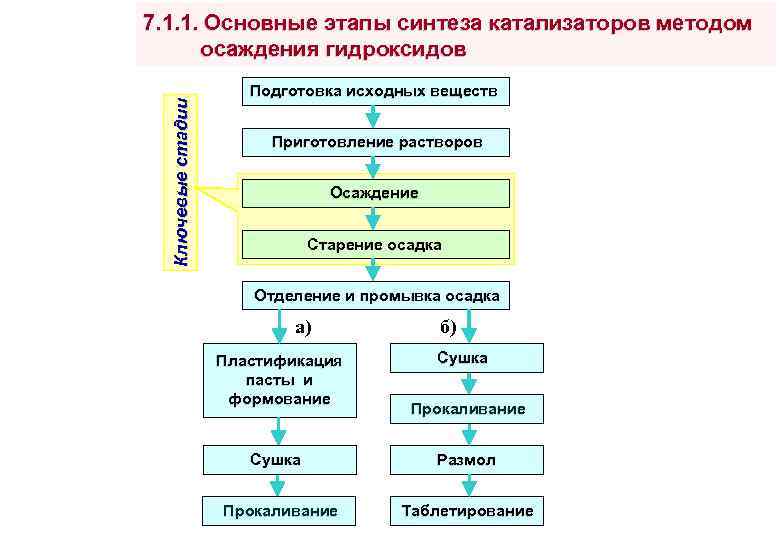 Ключевые стадии 7. 1. 1. Основные этапы синтеза катализаторов методом осаждения гидроксидов Подготовка исходных веществ Приготовление растворов Осаждение Старение осадка Отделение и промывка осадка а) Пластификация пасты и формование Сушка Прокаливание б) Сушка Прокаливание Размол Таблетирование
Ключевые стадии 7. 1. 1. Основные этапы синтеза катализаторов методом осаждения гидроксидов Подготовка исходных веществ Приготовление растворов Осаждение Старение осадка Отделение и промывка осадка а) Пластификация пасты и формование Сушка Прокаливание б) Сушка Прокаливание Размол Таблетирование
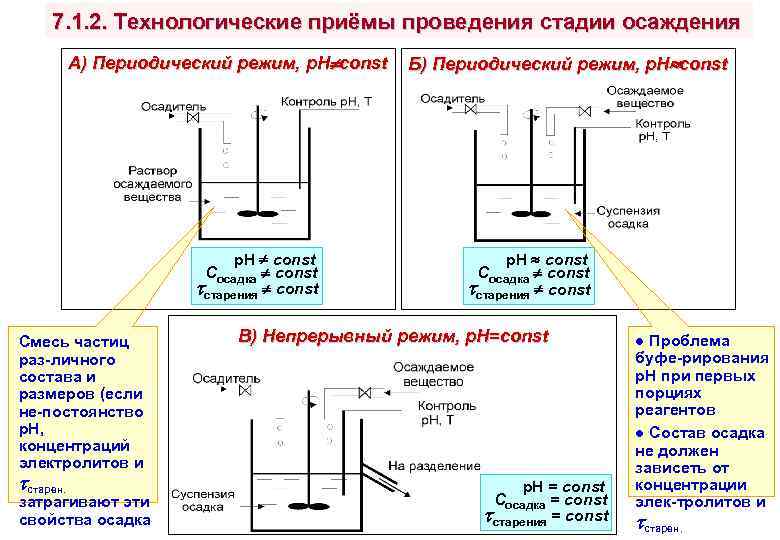 7. 1. 2. Технологические приёмы проведения стадии осаждения А) Периодический режим, р. Н const p. H const Cосадка const старения const Смесь частиц раз-личного состава и размеров (если не-постоянство р. Н, концентраций электролитов и старен. затрагивают эти свойства осадка Б) Периодический режим, р. Н const p. H const Cосадка const старения const В) Непрерывный режим, р. Н=const p. H = const Cосадка = const старения = const ● Проблема буфе-рирования р. Н при первых порциях реагентов ● Состав осадка не должен зависеть от концентрации элек-тролитов и старен.
7. 1. 2. Технологические приёмы проведения стадии осаждения А) Периодический режим, р. Н const p. H const Cосадка const старения const Смесь частиц раз-личного состава и размеров (если не-постоянство р. Н, концентраций электролитов и старен. затрагивают эти свойства осадка Б) Периодический режим, р. Н const p. H const Cосадка const старения const В) Непрерывный режим, р. Н=const p. H = const Cосадка = const старения = const ● Проблема буфе-рирования р. Н при первых порциях реагентов ● Состав осадка не должен зависеть от концентрации элек-тролитов и старен.
 Г) «Гомогенное» осаждение Основной принцип – эксплуатация кинетически затруднённых химических процессов, скорость протекания которых легко контролируется нагреванием ► гидролитическое разложение веществ, которое вызывает сдвиг р. Н среды в область выпадения осадка осаждаемого компонента, присутствующего в растворе: HS + H 2 O = H 2 S↑ + OH Осаждение Mg(OH)2 из солей (NH 2)2 CO + 3 H 2 O = CO 2↑ + 2 NH 4 OH Осаждение Ni(OH)2 из солей 3 NO 2 + H 2 O = 2 NO↑ + NO 3 + 2 OH (NH)4(CH 2)6 + 10 H 2 O 6 H 2 CO + 4 NH 4 OH HOCH 2 Cl + H 2 O = HOCH 2 OH + HCl Осаждение Al. O(OH) из Al(NO 3)3 Осаждение Al. O(OH) из Na. Al. O 2 Гидролиз в гомогенных условиях используется в случае, когда необходимо получить кристаллы совершенной формы, совместить или провести стадию гидролитического осаждения (гелеобразования) позже стадии формования сферических
Г) «Гомогенное» осаждение Основной принцип – эксплуатация кинетически затруднённых химических процессов, скорость протекания которых легко контролируется нагреванием ► гидролитическое разложение веществ, которое вызывает сдвиг р. Н среды в область выпадения осадка осаждаемого компонента, присутствующего в растворе: HS + H 2 O = H 2 S↑ + OH Осаждение Mg(OH)2 из солей (NH 2)2 CO + 3 H 2 O = CO 2↑ + 2 NH 4 OH Осаждение Ni(OH)2 из солей 3 NO 2 + H 2 O = 2 NO↑ + NO 3 + 2 OH (NH)4(CH 2)6 + 10 H 2 O 6 H 2 CO + 4 NH 4 OH HOCH 2 Cl + H 2 O = HOCH 2 OH + HCl Осаждение Al. O(OH) из Al(NO 3)3 Осаждение Al. O(OH) из Na. Al. O 2 Гидролиз в гомогенных условиях используется в случае, когда необходимо получить кристаллы совершенной формы, совместить или провести стадию гидролитического осаждения (гелеобразования) позже стадии формования сферических
 ► редокс-реакции: между одноименно заряженными ионами осадителя (восстанавливающего агента) и комплексами осаждаемого металла, между слабыми органическими восстановителями (спирты, гликоли, сахара, оксикислоты) и ионами металлов, между комплексами металлов с легкоокисляющимися органическими лигандами (например, EDTА, En) и окислителями (Н 2 О 2) Другой принцип – облучение растворов легковосстанавливаемых ионов металлов пучком электронов в ускорителе
► редокс-реакции: между одноименно заряженными ионами осадителя (восстанавливающего агента) и комплексами осаждаемого металла, между слабыми органическими восстановителями (спирты, гликоли, сахара, оксикислоты) и ионами металлов, между комплексами металлов с легкоокисляющимися органическими лигандами (например, EDTА, En) и окислителями (Н 2 О 2) Другой принцип – облучение растворов легковосстанавливаемых ионов металлов пучком электронов в ускорителе
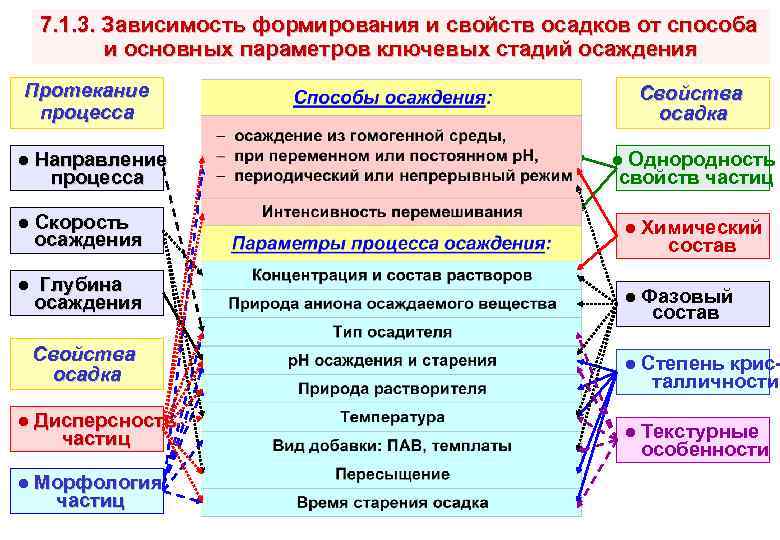 7. 1. 3. Зависимость формирования и свойств осадков от способа и основных параметров ключевых стадий осаждения Протекание процесса Свойства осадка ● Направление процесса ● Однородность свойств частиц ● Скорость осаждения ● Химический состав ● Глубина осаждения ● Фазовый состав Свойства осадка ● Дисперсность частиц ● Морфология частиц ● Степень кристалличности ● Текстурные особенности
7. 1. 3. Зависимость формирования и свойств осадков от способа и основных параметров ключевых стадий осаждения Протекание процесса Свойства осадка ● Направление процесса ● Однородность свойств частиц ● Скорость осаждения ● Химический состав ● Глубина осаждения ● Фазовый состав Свойства осадка ● Дисперсность частиц ● Морфология частиц ● Степень кристалличности ● Текстурные особенности
 Условие начала осаждения Условие окончания осаждения Men++ n OH Полнота осаждения достигается, когда концентрация ионов металла в растворе становится ПР = [Men+] [OH ]n пренебрежимо малой. Условно: Условие образования осадка гидроксида: [Men+] < 10 5 M Ме(OH)n [Men+] [OH ]n > ПР или lg[Men+] + nlg[OH ] > lg. ПР Поскольку тогда p. OH = 14 p. H, p. Hн > 14 + (lg. ПР – lg[Men+])/n Отсюда p. Hк > 14 + (1/n) lg. ПР + (5/n) или p. Hк > p. Hн + (5/n)
Условие начала осаждения Условие окончания осаждения Men++ n OH Полнота осаждения достигается, когда концентрация ионов металла в растворе становится ПР = [Men+] [OH ]n пренебрежимо малой. Условно: Условие образования осадка гидроксида: [Men+] < 10 5 M Ме(OH)n [Men+] [OH ]n > ПР или lg[Men+] + nlg[OH ] > lg. ПР Поскольку тогда p. OH = 14 p. H, p. Hн > 14 + (lg. ПР – lg[Men+])/n Отсюда p. Hк > 14 + (1/n) lg. ПР + (5/n) или p. Hк > p. Hн + (5/n)
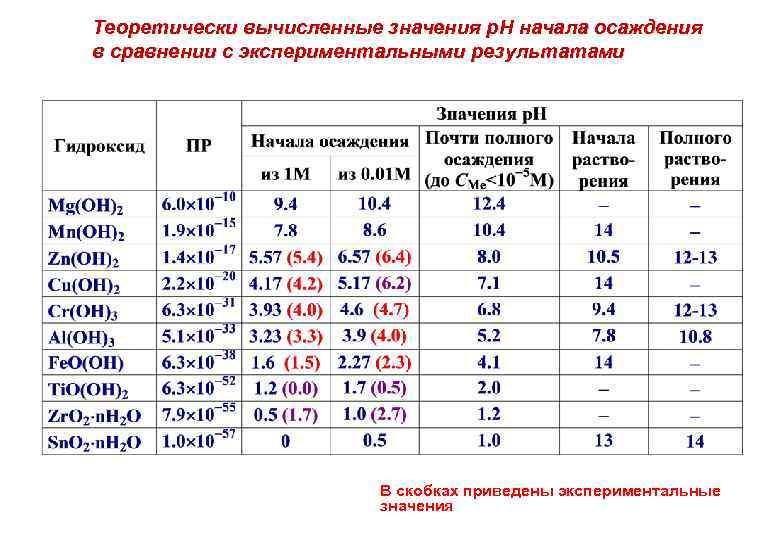 Теоретически вычисленные значения р. Н начала осаждения в сравнении с экспериментальными результатами В скобках приведены экспериментальные значения
Теоретически вычисленные значения р. Н начала осаждения в сравнении с экспериментальными результатами В скобках приведены экспериментальные значения
 7. 2. Механизмы формирования гидроксидов металлов Развитие представлений о механизмах процессов осаждения Наибольшего прогресса в области управления процессом осаждения удалось достигнуть в 70 – 80 -х гг. прошлого столетия, когда были раскрыты механизмы образования осадков гидроокисей, начиная с наиболее ранних стадий их формирования Основные достижения 70 -80 гг. XX в. : в. • Установление единого стадийного механизма образования гидроксидов • Классификация гидроксидов по их способности к кристаллизации [Дзисько В. А. ] • Раскрытие механизмов формирования и старения аморфного силикагеля [Айлер Р. К. , Симонова Л. Г. , Фенелонов В. Б. ] • Создание теории кристаллизации малорастворимых гидроксидов по механизму ориентированного наращивания [Буянов Р. А. , Криворучко О. П. ] Основные достижения последних 10 – 15 лет: • Развитие экспериментальных и теоретических основ золь-гель синтеза через алкоксидные соединения • Синтез нового класса мезопористых мезофазных материалов
7. 2. Механизмы формирования гидроксидов металлов Развитие представлений о механизмах процессов осаждения Наибольшего прогресса в области управления процессом осаждения удалось достигнуть в 70 – 80 -х гг. прошлого столетия, когда были раскрыты механизмы образования осадков гидроокисей, начиная с наиболее ранних стадий их формирования Основные достижения 70 -80 гг. XX в. : в. • Установление единого стадийного механизма образования гидроксидов • Классификация гидроксидов по их способности к кристаллизации [Дзисько В. А. ] • Раскрытие механизмов формирования и старения аморфного силикагеля [Айлер Р. К. , Симонова Л. Г. , Фенелонов В. Б. ] • Создание теории кристаллизации малорастворимых гидроксидов по механизму ориентированного наращивания [Буянов Р. А. , Криворучко О. П. ] Основные достижения последних 10 – 15 лет: • Развитие экспериментальных и теоретических основ золь-гель синтеза через алкоксидные соединения • Синтез нового класса мезопористых мезофазных материалов
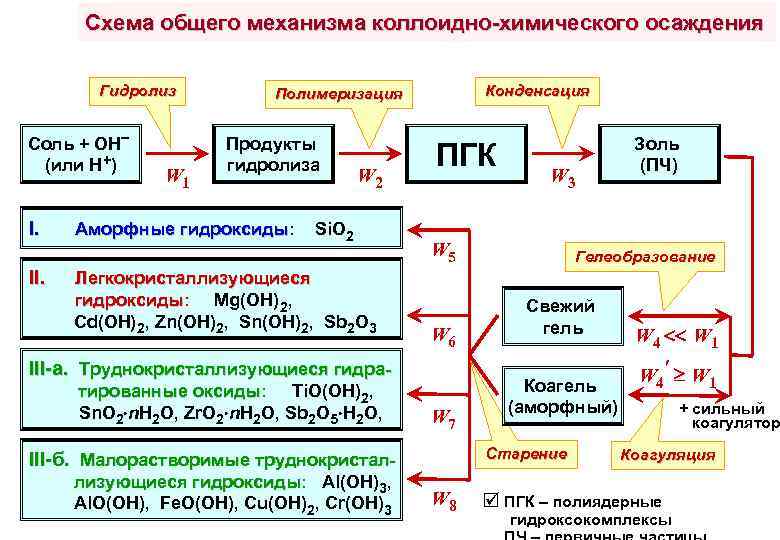 Схема общего механизма коллоидно-химического осаждения Гидролиз Соль + ОН (или Н+) I. II. W 1 Конденсация Полимеризация Продукты гидролиза Аморфные гидроксиды: гидроксиды W 2 Si. O 2 Легкокристаллизующиеся гидроксиды: Mg(OH)2, гидроксиды Cd(OH)2, Zn(OH)2, Sb 2 O 3 ПГК W 5 W 6 III-а. Труднокристаллизующиеся гидратированные оксиды: Ti. O(OH)2, оксиды Sn. O 2 n. H 2 O, Zr. O 2 n. H 2 O, Sb 2 O 5 H 2 O, W 7 Гелеобразование Свежий гель Коагель (аморфный) Старение III-б. Малорастворимые труднокристаллизующиеся гидроксиды: Al(OH)3, гидроксиды Al. O(OH), Fe. O(OH), Cu(OH)2, Cr(OH)3 W 8 Золь (ПЧ) W 4 W 1 W 4′ W 1 + сильный коагулятор Коагуляция ПГК – полиядерные гидроксокомплексы
Схема общего механизма коллоидно-химического осаждения Гидролиз Соль + ОН (или Н+) I. II. W 1 Конденсация Полимеризация Продукты гидролиза Аморфные гидроксиды: гидроксиды W 2 Si. O 2 Легкокристаллизующиеся гидроксиды: Mg(OH)2, гидроксиды Cd(OH)2, Zn(OH)2, Sb 2 O 3 ПГК W 5 W 6 III-а. Труднокристаллизующиеся гидратированные оксиды: Ti. O(OH)2, оксиды Sn. O 2 n. H 2 O, Zr. O 2 n. H 2 O, Sb 2 O 5 H 2 O, W 7 Гелеобразование Свежий гель Коагель (аморфный) Старение III-б. Малорастворимые труднокристаллизующиеся гидроксиды: Al(OH)3, гидроксиды Al. O(OH), Fe. O(OH), Cu(OH)2, Cr(OH)3 W 8 Золь (ПЧ) W 4 W 1 W 4′ W 1 + сильный коагулятор Коагуляция ПГК – полиядерные гидроксокомплексы
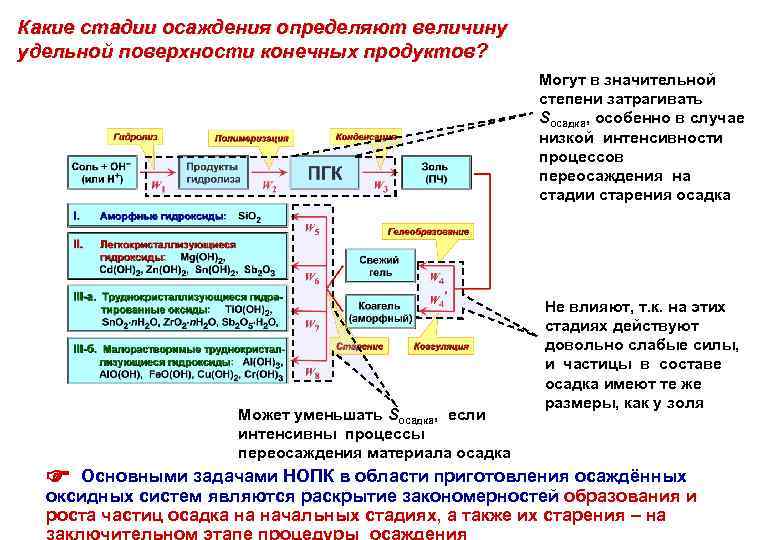 Какие стадии осаждения определяют величину удельной поверхности конечных продуктов? Могут в значительной степени затрагивать Sосадка, особенно в случае низкой интенсивности процессов переосаждения на стадии старения осадка Может уменьшать Sосадка, если интенсивны процессы переосаждения материала осадка Не влияют, т. к. на этих стадиях действуют довольно слабые силы, и частицы в составе осадка имеют те же размеры, как у золя осаждённых Основными задачами НОПК в области приготовленияобразования и оксидных систем являются раскрытие закономерностей роста частиц осадка на начальных стадиях, а также их старения – на
Какие стадии осаждения определяют величину удельной поверхности конечных продуктов? Могут в значительной степени затрагивать Sосадка, особенно в случае низкой интенсивности процессов переосаждения на стадии старения осадка Может уменьшать Sосадка, если интенсивны процессы переосаждения материала осадка Не влияют, т. к. на этих стадиях действуют довольно слабые силы, и частицы в составе осадка имеют те же размеры, как у золя осаждённых Основными задачами НОПК в области приготовленияобразования и оксидных систем являются раскрытие закономерностей роста частиц осадка на начальных стадиях, а также их старения – на
 7. 3. Основы классической теории конденсации Процесс конденсации предполагает образование новой фазы и увеличение её объёма на уже имеющихся инородных поверхностях (гетерогенная конденсация) или на поверхности зародышей этой же конденсация фазы, появляющихся самопроизвольно в результате флуктуаций плотности среды и концентрации вещества (гомогенная конденсация) конденсация Линия растворимости Линия суперрастворимости A 1 1 – область абсолютной устойчивости B 2 – область метастабильных состояний 2 C 3 (для фазового перехода в пересыщенном растворе требуется преодоление активацион- ного барьера в образовании зародыша новой фазы – описывается в рамках классической теории кристаллизации ) 3 – область абсолютной неустойчивости Диаграмма растворимости вещества (безактивационный фазовый распад пересыщен- ного раствора –
7. 3. Основы классической теории конденсации Процесс конденсации предполагает образование новой фазы и увеличение её объёма на уже имеющихся инородных поверхностях (гетерогенная конденсация) или на поверхности зародышей этой же конденсация фазы, появляющихся самопроизвольно в результате флуктуаций плотности среды и концентрации вещества (гомогенная конденсация) конденсация Линия растворимости Линия суперрастворимости A 1 1 – область абсолютной устойчивости B 2 – область метастабильных состояний 2 C 3 (для фазового перехода в пересыщенном растворе требуется преодоление активацион- ного барьера в образовании зародыша новой фазы – описывается в рамках классической теории кристаллизации ) 3 – область абсолютной неустойчивости Диаграмма растворимости вещества (безактивационный фазовый распад пересыщен- ного раствора –
 Теория гомогенной конденсации по Гиббсу-Фольмеру-Оствальд 1) Критический радиус зародыша новой фазы Полное изменение энергии Гиббса при гомогенном образовании новой фазы где GV объёмная составляющая: а G S поверхностная составляющая: тв. , р-р – значения химического потенциала вещества в твердой фазе и в растворе, V, S, r, – величины объёма, поверхности, радиуса и поверхностного натяжения зародыш n, Vm – количество молей и мольный объём вещества новой фазы
Теория гомогенной конденсации по Гиббсу-Фольмеру-Оствальд 1) Критический радиус зародыша новой фазы Полное изменение энергии Гиббса при гомогенном образовании новой фазы где GV объёмная составляющая: а G S поверхностная составляющая: тв. , р-р – значения химического потенциала вещества в твердой фазе и в растворе, V, S, r, – величины объёма, поверхности, радиуса и поверхностного натяжения зародыш n, Vm – количество молей и мольный объём вещества новой фазы
 Из условия экстремума в точке (rкр. , Gкр. . ): легко получить Следовательно, где С/С 0 – степень пересыщения в точке (rкр. , Gкр. . ). Координаты (rкр. , Gкр. . ) экстремума G : Критический радиус зародыша новой фазы: Энергия Гиббса образования зародыша новой фазы: Чем больше степень пересыщения раствора, тем выше вероятность образования и меньше размер способных к росту зародышей новой фазы
Из условия экстремума в точке (rкр. , Gкр. . ): легко получить Следовательно, где С/С 0 – степень пересыщения в точке (rкр. , Gкр. . ). Координаты (rкр. , Gкр. . ) экстремума G : Критический радиус зародыша новой фазы: Энергия Гиббса образования зародыша новой фазы: Чем больше степень пересыщения раствора, тем выше вероятность образования и меньше размер способных к росту зародышей новой фазы
 2) Скорость образования и роста зародыша новой фазы Скорость образования стабильных зародышей новой фазы (штук в ед. времени): Скорость роста зародыша новой фазы (по Брандесу): 2 и – толщина двумерного зародыша и его периферийная энергия (на ед. длины), b – коэффициент, учитывающий форму зародыша, – плотность, NA – число Авогадро, К 1 , К 2 , a – постоянные Общие выводы классической теории конденсации ► Скорость образования зародышей гидро- ксида, их размер и скорость дальнейшего роста будут зависеть от физико-химических свойств ( , , Vm) и растворимости (С 0) гидроксида, ► С повышением температуры T и степени пересыщения C/C 0 дисперсность частиц осадка будет возрастать, а с ростом их мольного объёма Vm и поверхностного натяжения падать
2) Скорость образования и роста зародыша новой фазы Скорость образования стабильных зародышей новой фазы (штук в ед. времени): Скорость роста зародыша новой фазы (по Брандесу): 2 и – толщина двумерного зародыша и его периферийная энергия (на ед. длины), b – коэффициент, учитывающий форму зародыша, – плотность, NA – число Авогадро, К 1 , К 2 , a – постоянные Общие выводы классической теории конденсации ► Скорость образования зародышей гидро- ксида, их размер и скорость дальнейшего роста будут зависеть от физико-химических свойств ( , , Vm) и растворимости (С 0) гидроксида, ► С повышением температуры T и степени пересыщения C/C 0 дисперсность частиц осадка будет возрастать, а с ростом их мольного объёма Vm и поверхностного натяжения падать
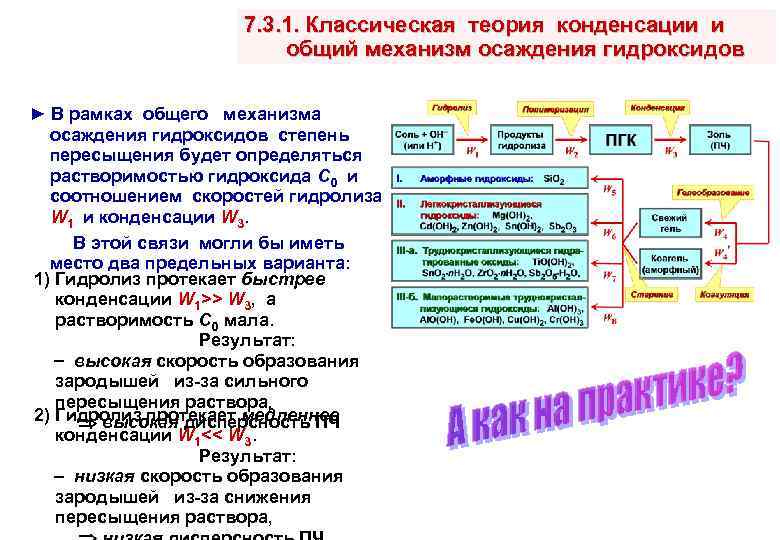 7. 3. 1. Классическая теория конденсации и общий механизм осаждения гидроксидов ► В рамках общего механизма осаждения гидроксидов степень пересыщения будет определяться растворимостью гидроксида С 0 и соотношением скоростей гидролиза W 1 и конденсации W 3. В этой связи могли бы иметь место два предельных варианта: 1) Гидролиз протекает быстрее конденсации W 1>> W 3, а растворимость С 0 мала. Результат: высокая скорость образования зародышей из-за сильного пересыщения раствора, 2) Гидролиз протекает медленнее высокая дисперсность ПЧ конденсации W 1<< W 3. Результат: низкая скорость образования зародышей из-за снижения пересыщения раствора,
7. 3. 1. Классическая теория конденсации и общий механизм осаждения гидроксидов ► В рамках общего механизма осаждения гидроксидов степень пересыщения будет определяться растворимостью гидроксида С 0 и соотношением скоростей гидролиза W 1 и конденсации W 3. В этой связи могли бы иметь место два предельных варианта: 1) Гидролиз протекает быстрее конденсации W 1>> W 3, а растворимость С 0 мала. Результат: высокая скорость образования зародышей из-за сильного пересыщения раствора, 2) Гидролиз протекает медленнее высокая дисперсность ПЧ конденсации W 1<< W 3. Результат: низкая скорость образования зародышей из-за снижения пересыщения раствора,
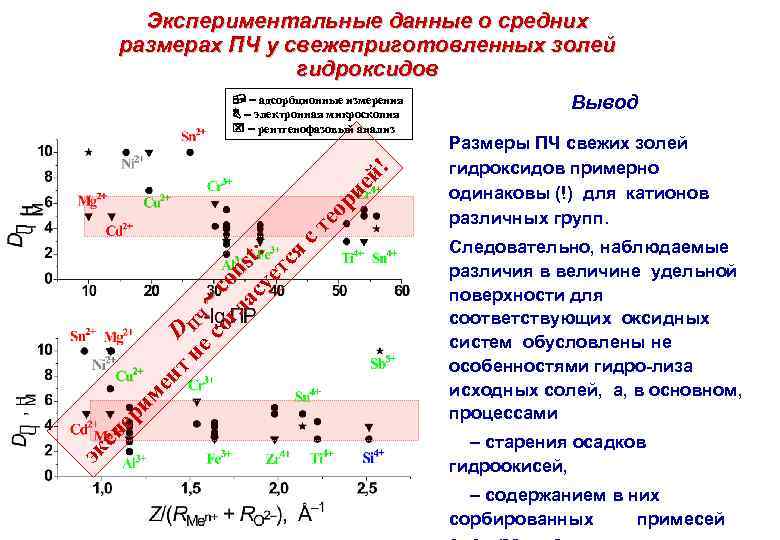 Экспериментальные данные о средних размерах ПЧ у свежеприготовленных золей гидроксидов эк сп ер им ен т не D П Ч со c гл on ас st: уе тс я ст ео ри ей ! адсорбционные измерения электронная микроскопия рентгенофазовый анализ Вывод Размеры ПЧ свежих золей гидроксидов примерно одинаковы (!) для катионов различных групп. Следовательно, наблюдаемые различия в величине удельной поверхности для соответствующих оксидных систем обусловлены не особенностями гидро-лиза исходных солей, а, в основном, процессами старения осадков гидроокисей, содержанием в них сорбированных примесей
Экспериментальные данные о средних размерах ПЧ у свежеприготовленных золей гидроксидов эк сп ер им ен т не D П Ч со c гл on ас st: уе тс я ст ео ри ей ! адсорбционные измерения электронная микроскопия рентгенофазовый анализ Вывод Размеры ПЧ свежих золей гидроксидов примерно одинаковы (!) для катионов различных групп. Следовательно, наблюдаемые различия в величине удельной поверхности для соответствующих оксидных систем обусловлены не особенностями гидро-лиза исходных солей, а, в основном, процессами старения осадков гидроокисей, содержанием в них сорбированных примесей
 В Общие закономерности влияния свойств свежих гидрогелей на удельную поверхность получаемых ксерогелей большинстве случаев удельная поверхность Sº нестаревших ксерогелей с минимальным содержанием примесей посторонних катионов и анионов равна суммарной поверхности составляющих их ПЧ (имеющих размеры 3 -4 нм независимо от типа катиона) и приближенно выражается как Sº = (1. 5 0. 4) 103/ [м 2/г], где плотность [г/см 3] Зависимость между содержанием С примесей электролитов и величиной поверхности ксерогеля S эмпирически выражается как lg. S = lg. Sº C где коэффициент, характеризующий чувствительность S к изменению содержания посторонних ионов в гидрогеле При наличии в исходном гидрогеле продуктов неполного гидролиза величина поверхности ксерогеля снижается пропорционально содержанию основной соли
В Общие закономерности влияния свойств свежих гидрогелей на удельную поверхность получаемых ксерогелей большинстве случаев удельная поверхность Sº нестаревших ксерогелей с минимальным содержанием примесей посторонних катионов и анионов равна суммарной поверхности составляющих их ПЧ (имеющих размеры 3 -4 нм независимо от типа катиона) и приближенно выражается как Sº = (1. 5 0. 4) 103/ [м 2/г], где плотность [г/см 3] Зависимость между содержанием С примесей электролитов и величиной поверхности ксерогеля S эмпирически выражается как lg. S = lg. Sº C где коэффициент, характеризующий чувствительность S к изменению содержания посторонних ионов в гидрогеле При наличии в исходном гидрогеле продуктов неполного гидролиза величина поверхности ксерогеля снижается пропорционально содержанию основной соли
 7. 3. 2. Причины неадекватности классической теории конденсации для интерпретации закономерностей формирования ПЧ гидроксидов катионов I-III групп Идеализированность модели конденсации в рамках классического подхода 1. Не привлекаются представления о диффузионном переносе материала к растущим зародышам 2. Игнорируется существование бóльших локальных пересыщений с момента добавления осадителя до достижения равномерного его распределения в объёме раствора благодаря перемешиванию 3. Не принимается во внимание роль различных примесей (химических и механических) в образовании зародышей новой фазы
7. 3. 2. Причины неадекватности классической теории конденсации для интерпретации закономерностей формирования ПЧ гидроксидов катионов I-III групп Идеализированность модели конденсации в рамках классического подхода 1. Не привлекаются представления о диффузионном переносе материала к растущим зародышам 2. Игнорируется существование бóльших локальных пересыщений с момента добавления осадителя до достижения равномерного его распределения в объёме раствора благодаря перемешиванию 3. Не принимается во внимание роль различных примесей (химических и механических) в образовании зародышей новой фазы
 “Из-за строгости математических формул легко забывается гипотетическая природа предпосылок…” Ф. Энгельс Неприменимость классической модели конденсации к частицам полимеров 4. В основе классической теории конденсации лежит допущение о равновероятности присоединения (или удаления) “неделимых” элементов структуры частицы в любой точке её поверхности. Однако в случае ПЧ гидроксидов это допущение неправомочно, т. к. они являются полимерными клубками, для которых в этом отношении следует ожидать наличия энергетической неравноценности связи концевых и внутрицепных звеньев, а также возможность появления “неделимых” элементов бóльшего размера, создающих иные условия конденсации 5. В классической теории конденсации задействованы неспецифические физические силы (ван-дер-ваальсовы, кулоновские), отличающиеся ненаправленностью действия, тогда как высокая доля ковалентности связей Э О в гидроксидах (особенно для I и III групп) подразумевает стерические эффекты при образовании и разрыве этих связей
“Из-за строгости математических формул легко забывается гипотетическая природа предпосылок…” Ф. Энгельс Неприменимость классической модели конденсации к частицам полимеров 4. В основе классической теории конденсации лежит допущение о равновероятности присоединения (или удаления) “неделимых” элементов структуры частицы в любой точке её поверхности. Однако в случае ПЧ гидроксидов это допущение неправомочно, т. к. они являются полимерными клубками, для которых в этом отношении следует ожидать наличия энергетической неравноценности связи концевых и внутрицепных звеньев, а также возможность появления “неделимых” элементов бóльшего размера, создающих иные условия конденсации 5. В классической теории конденсации задействованы неспецифические физические силы (ван-дер-ваальсовы, кулоновские), отличающиеся ненаправленностью действия, тогда как высокая доля ковалентности связей Э О в гидроксидах (особенно для I и III групп) подразумевает стерические эффекты при образовании и разрыве этих связей
 7. 3. 3. Спинодальный распад абсолютно неустойчивых фаз Особенности протекания спинодального распада 1. В отличие от конденсации в метастабильных системах (величина Gкр. конечна), при спинодальном распаде Gкр. → 0. Поэтому спинодальный распад характеризуется диффузионной кинетикой. 2. Система, вследствие ничтожных флуктуаций плотности или температуры, быстро теряет пространственную однородность и, релаксируя, приобретает особую зернисто-ячеечную структуру без фазовых границ (обычная гетерогенность появляется на более поздних стадиях). 3. Неоднородности состава возникают практически одновременно во всём объёме системы и всегда усиливаются реакцией системы на эти флуктуации, что отвечает отрицательному коэффициенту диффузии (т. н. «восходящая» диффузия). 4. Из всего набора частот флуктуаций усиливаются только отвечающие определенному критерию, в результате чего в системе получают преимущество концентрационные волны с близкой длиной волны (но со случайными ориентациями, фазами и амплитудами), что обуславливает
7. 3. 3. Спинодальный распад абсолютно неустойчивых фаз Особенности протекания спинодального распада 1. В отличие от конденсации в метастабильных системах (величина Gкр. конечна), при спинодальном распаде Gкр. → 0. Поэтому спинодальный распад характеризуется диффузионной кинетикой. 2. Система, вследствие ничтожных флуктуаций плотности или температуры, быстро теряет пространственную однородность и, релаксируя, приобретает особую зернисто-ячеечную структуру без фазовых границ (обычная гетерогенность появляется на более поздних стадиях). 3. Неоднородности состава возникают практически одновременно во всём объёме системы и всегда усиливаются реакцией системы на эти флуктуации, что отвечает отрицательному коэффициенту диффузии (т. н. «восходящая» диффузия). 4. Из всего набора частот флуктуаций усиливаются только отвечающие определенному критерию, в результате чего в системе получают преимущество концентрационные волны с близкой длиной волны (но со случайными ориентациями, фазами и амплитудами), что обуславливает
 7. 4. Старение осадков под маточным раствором Старение совокупность физико-химических процессов, самопроизвольно протекающих в осадках, находящихся под маточным раствором Причины старения осадков ● образование осадков протекает в не-равновесных условиях – по концентрациям реагентов, – по физическим свойствам дисперсионной среды (ионная сила, вязкость, микронеоднородность и др. ), ● частицы осадка термодинамически неустойчивы, т. к. обладают большой избыточной энергией из-за развитой поверхности и многочисленных де-фектов структуры Процессы при старении осадков с массопереносом через дисперсионную среду: ● конденсация – превращение агрегатов частиц в конденсационнокристаллизационные структуры (вплоть до их полного слияния), ● рекристаллизация – укрупнение частиц за счет растворения более мелких, а также изменение их габитуса (формы), ● переосаждение с образованием новых частиц более устойчивой фазы с массопереносом внутри твердого тела: ● кристаллизация – упорядочение внутренней структуры частиц,
7. 4. Старение осадков под маточным раствором Старение совокупность физико-химических процессов, самопроизвольно протекающих в осадках, находящихся под маточным раствором Причины старения осадков ● образование осадков протекает в не-равновесных условиях – по концентрациям реагентов, – по физическим свойствам дисперсионной среды (ионная сила, вязкость, микронеоднородность и др. ), ● частицы осадка термодинамически неустойчивы, т. к. обладают большой избыточной энергией из-за развитой поверхности и многочисленных де-фектов структуры Процессы при старении осадков с массопереносом через дисперсионную среду: ● конденсация – превращение агрегатов частиц в конденсационнокристаллизационные структуры (вплоть до их полного слияния), ● рекристаллизация – укрупнение частиц за счет растворения более мелких, а также изменение их габитуса (формы), ● переосаждение с образованием новых частиц более устойчивой фазы с массопереносом внутри твердого тела: ● кристаллизация – упорядочение внутренней структуры частиц,
 Механизм массопереноса в осадках через дисперсионную среду Концентрация вещества в растворе над искривлёной поверхностью частицы: выпуклой (+) и вогнутой ( ) (аналогично уравнению Кельвина. Оствальда для равновесия паржидкость) Cr – концентрация вещества над частицей, r – радиус частицы (или радиус вписанной окружности для искривлённой поверхности), C 0 – концентрация вещества над плоской поверхностью (т. е. при r→ ), – поверхностное натяжение, Следствия 1. Растворимость кристаллитов возрастает с уменьшением их размера (эффект Гиббса-Томпсона) 2. Концентрация раствора, находящаяся в равновесии с частицей твердого тела, зависит от ее размера чем крупнее частица, тем ниже соответствующая равновесная концентрация: – для частиц меньших, чем равновесный размер при заданной концентрации, раствор является ненасыщенным (частицы растворяются), – этот раствор пересыщен по отношению к более крупным частицам (частицы растут) 3. Концентрация вещества над вогнутой поверхностью ниже, а над выпуклой – выше, чем над плоской поверхностью
Механизм массопереноса в осадках через дисперсионную среду Концентрация вещества в растворе над искривлёной поверхностью частицы: выпуклой (+) и вогнутой ( ) (аналогично уравнению Кельвина. Оствальда для равновесия паржидкость) Cr – концентрация вещества над частицей, r – радиус частицы (или радиус вписанной окружности для искривлённой поверхности), C 0 – концентрация вещества над плоской поверхностью (т. е. при r→ ), – поверхностное натяжение, Следствия 1. Растворимость кристаллитов возрастает с уменьшением их размера (эффект Гиббса-Томпсона) 2. Концентрация раствора, находящаяся в равновесии с частицей твердого тела, зависит от ее размера чем крупнее частица, тем ниже соответствующая равновесная концентрация: – для частиц меньших, чем равновесный размер при заданной концентрации, раствор является ненасыщенным (частицы растворяются), – этот раствор пересыщен по отношению к более крупным частицам (частицы растут) 3. Концентрация вещества над вогнутой поверхностью ниже, а над выпуклой – выше, чем над плоской поверхностью
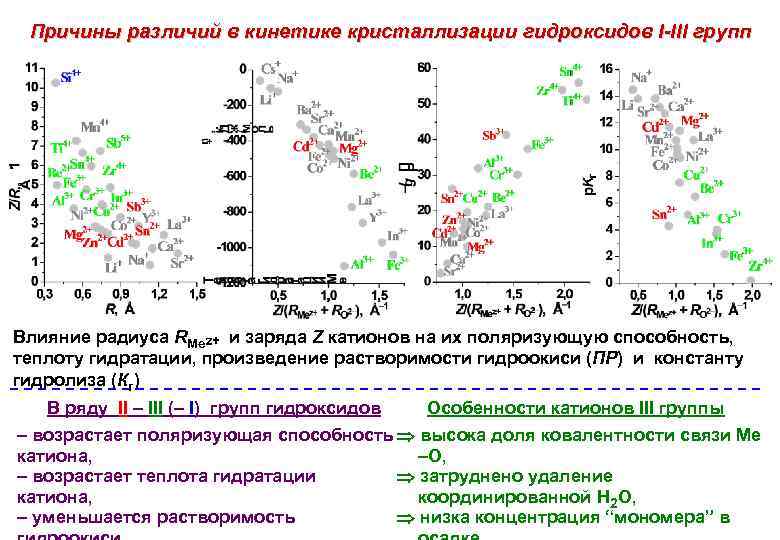 Причины различий в кинетике кристаллизации гидроксидов I-III групп Влияние радиуса RMez+ и заряда Z катионов на их поляризующую способность, теплоту гидратации, произведение растворимости гидроокиси (ПР) и константу гидролиза (Кг) В ряду II – III (– I) групп гидроксидов Особенности катионов III группы – возрастает поляризующая способность высока доля ковалентности связи Me –O, катиона, затруднено удаление – возрастает теплота гидратации координированной H 2 O, катиона, низка концентрация “мономера” в – уменьшается растворимость
Причины различий в кинетике кристаллизации гидроксидов I-III групп Влияние радиуса RMez+ и заряда Z катионов на их поляризующую способность, теплоту гидратации, произведение растворимости гидроокиси (ПР) и константу гидролиза (Кг) В ряду II – III (– I) групп гидроксидов Особенности катионов III группы – возрастает поляризующая способность высока доля ковалентности связи Me –O, катиона, затруднено удаление – возрастает теплота гидратации координированной H 2 O, катиона, низка концентрация “мономера” в – уменьшается растворимость


