Лекция 7. Химическая кинетика и равновесие.ppt
- Количество слайдов: 17
 Лекция № 7 Химическая кинетика Изучение cкорости и механизмов химических процессов –предмет химической кинетики. Формальная кинетика позволяет количественно описать ход химического процесса во времени при постоянной температуре в зависимости от концентрации реагирующих веществ и их фазового состава.
Лекция № 7 Химическая кинетика Изучение cкорости и механизмов химических процессов –предмет химической кинетики. Формальная кинетика позволяет количественно описать ход химического процесса во времени при постоянной температуре в зависимости от концентрации реагирующих веществ и их фазового состава.
 Типы реакций • Гомогенные (~концентрация) – газ, раствор, расплав, . . . – различный порядок, молекулярность Гетерогенные (~граница/площадь раздела) – гетерофазные катализ осадок в растворе, . . . твердофазные
Типы реакций • Гомогенные (~концентрация) – газ, раствор, расплав, . . . – различный порядок, молекулярность Гетерогенные (~граница/площадь раздела) – гетерофазные катализ осадок в растворе, . . . твердофазные
 Скорость реакции Средняя – конечное изменение концентрации c 2 – c 1, относящееся к промежутку времени t 2 – t 1 Vсредн. = ±(c 2 – c 1)/(t 2 – t 1) Истинная. • При данной температуре истинная скорость гомогенной реакции Vi определяется убылью или приращением концентрации реагента d. Ci за бесконечно малое время dτ: Vi=±d. Ci /dti
Скорость реакции Средняя – конечное изменение концентрации c 2 – c 1, относящееся к промежутку времени t 2 – t 1 Vсредн. = ±(c 2 – c 1)/(t 2 – t 1) Истинная. • При данной температуре истинная скорость гомогенной реакции Vi определяется убылью или приращением концентрации реагента d. Ci за бесконечно малое время dτ: Vi=±d. Ci /dti
 Основной закон химической кинетики Основной постулат (К. Гульдберг-П. Вааге, 1867 г. з-н действующих масс): Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях их стехиометрических коэффициентов.
Основной закон химической кинетики Основной постулат (К. Гульдберг-П. Вааге, 1867 г. з-н действующих масс): Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях их стехиометрических коэффициентов.
 Для реакции: a. A+b. B=c. C+d. D VAB = k٠(CA)a٠(CB)b Молекулярность реакции -минимальное число молекул, участвующих в элементарном химическом процессе. мономолекулярные: N 2 O 5 = N 2 O 4 +1/2 O 2, J 2 = 2 J
Для реакции: a. A+b. B=c. C+d. D VAB = k٠(CA)a٠(CB)b Молекулярность реакции -минимальное число молекул, участвующих в элементарном химическом процессе. мономолекулярные: N 2 O 5 = N 2 O 4 +1/2 O 2, J 2 = 2 J
 бимолекулярные: H 2 + J 2 = 2 HJ (Br, Cl, F – другой механизм!) CH 3 CO 2 C 2 H 5 + Na. OH(р-р) =. . . A+A = A* + A (Линдеманн), A* = продукты реакции тримолекулярные: 2 NO + H 2 = N 2 O + H 2 O
бимолекулярные: H 2 + J 2 = 2 HJ (Br, Cl, F – другой механизм!) CH 3 CO 2 C 2 H 5 + Na. OH(р-р) =. . . A+A = A* + A (Линдеманн), A* = продукты реакции тримолекулярные: 2 NO + H 2 = N 2 O + H 2 O
 Порядок реакции • Если реакция протекает через несколько последовательных гомогенных или гетерогенных элементарных стадий, то понятие “молекулярность” вынуждены заменять на формальный показатель при концентрациях реагентов (“порядок реакции”). -кинетическое уравнение = закон действующих масс применимо только для элементарных стадий
Порядок реакции • Если реакция протекает через несколько последовательных гомогенных или гетерогенных элементарных стадий, то понятие “молекулярность” вынуждены заменять на формальный показатель при концентрациях реагентов (“порядок реакции”). -кинетическое уравнение = закон действующих масс применимо только для элементарных стадий
 -молекулярность – целое число -порядок реакции может быть дробным (особенно для гетерогенных и сложных реакций) -молекулярность <3 -порядок реакции может быть > 3
-молекулярность – целое число -порядок реакции может быть дробным (особенно для гетерогенных и сложных реакций) -молекулярность <3 -порядок реакции может быть > 3
 Для реакции a. А + b. В →. . . кинетические уравнения: VA=k. CAX ; VB =k. CBy частный порядок по реагентам: x и y Общее кинетическое уравнение: V= k. CAX ٠CBy = k. CZ Z –общий порядок реакции, зависящий от механизма реакции
Для реакции a. А + b. В →. . . кинетические уравнения: VA=k. CAX ; VB =k. CBy частный порядок по реагентам: x и y Общее кинетическое уравнение: V= k. CAX ٠CBy = k. CZ Z –общий порядок реакции, зависящий от механизма реакции
 Энергия активации – избыточное количество энергии (по сравнению со средней величиной), которой должна обладать молекула в момент столкновения, чтобы быть способной к данному химическому взаимодействию ( «энергетический барьер реакции» ). Чем выше энергия активации, тем при более высокой температуре начинается реакция (80 к. Дж – 250 С, 160 к. Дж – 3000 С, . . . ).
Энергия активации – избыточное количество энергии (по сравнению со средней величиной), которой должна обладать молекула в момент столкновения, чтобы быть способной к данному химическому взаимодействию ( «энергетический барьер реакции» ). Чем выше энергия активации, тем при более высокой температуре начинается реакция (80 к. Дж – 250 С, 160 к. Дж – 3000 С, . . . ).
 Уравнение Аррениуса k = A٠exp(-Ea/RT) ln (k) = const – (Ea/R) ٠ (1/T), T = t + 273. 15 Правило Вант-Гоффа: kt 1 / kt 2 =γ(t 2 -t 1)/10 (Если Ea = 50– 100 к. Дж·моль– 1, то…) при изменении температуры реакции на 10 градусов ее скорость изменится в 2– 4 раза.
Уравнение Аррениуса k = A٠exp(-Ea/RT) ln (k) = const – (Ea/R) ٠ (1/T), T = t + 273. 15 Правило Вант-Гоффа: kt 1 / kt 2 =γ(t 2 -t 1)/10 (Если Ea = 50– 100 к. Дж·моль– 1, то…) при изменении температуры реакции на 10 градусов ее скорость изменится в 2– 4 раза.
 Химическое равновесие Обратимые реакции. Реакции, которые при одной и той же температуре в зависимости от соотношения реагентов могут протекать как в прямом , так и в обратном направлениях называются обратимыми. а. А+b. B↔c. C+d. D (простая).
Химическое равновесие Обратимые реакции. Реакции, которые при одной и той же температуре в зависимости от соотношения реагентов могут протекать как в прямом , так и в обратном направлениях называются обратимыми. а. А+b. B↔c. C+d. D (простая).
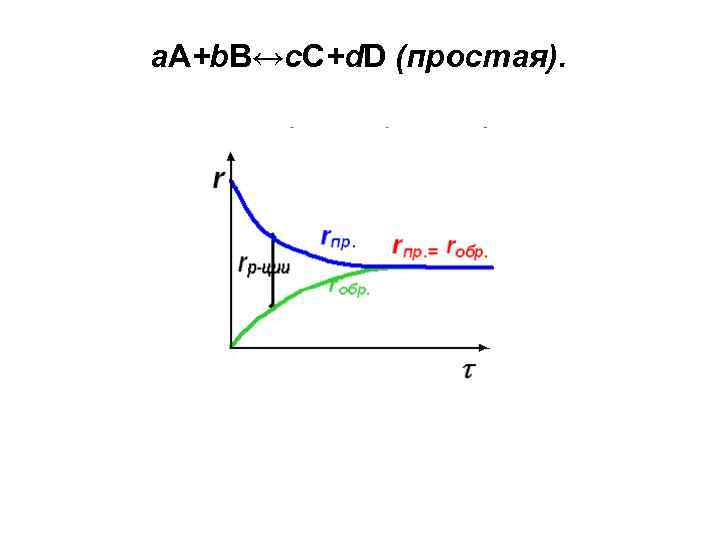 а. А+b. B↔c. C+d. D (простая).
а. А+b. B↔c. C+d. D (простая).
 Для реакции а. А+b. B↔c. C+d. D (простая). r 1= k 1٠ C Aa٠ C Bb r 2 = k 2٠ Ccc٠ CDd Равновесие динамическое, т. е r 1= r 2 и k 1٠ C Aa٠ C Bb = k 2٠ C cc٠ C Dd
Для реакции а. А+b. B↔c. C+d. D (простая). r 1= k 1٠ C Aa٠ C Bb r 2 = k 2٠ Ccc٠ CDd Равновесие динамическое, т. е r 1= r 2 и k 1٠ C Aa٠ C Bb = k 2٠ C cc٠ C Dd
 УСЛОВИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ 1. Состояние равновесия может быть достигнуто только в закрытой системе как со стороны исходных веществ, так и со стороны продуктов реакции 2. В состоянии равновесия ΔGпр. = ΔGобр. = 0 3. При изменении внешних условий(Т, Р, аi ) состояние равновесия изменяется (смещается)
УСЛОВИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ 1. Состояние равновесия может быть достигнуто только в закрытой системе как со стороны исходных веществ, так и со стороны продуктов реакции 2. В состоянии равновесия ΔGпр. = ΔGобр. = 0 3. При изменении внешних условий(Т, Р, аi ) состояние равновесия изменяется (смещается)
 СМЕЩЕНИЕ ХИМИЧЕСКОГО РАВНОВЕСИЯ. Смещение химического равновесия это изменение относительных количеств участников реакции (реагентов и продуктов), вызванное действием внешних условий. 1. Изменение концентраций реагентов или продуктов реакции(изменение давления или объема) 2. Изменение температуры 3. Участие в реакции катализатора
СМЕЩЕНИЕ ХИМИЧЕСКОГО РАВНОВЕСИЯ. Смещение химического равновесия это изменение относительных количеств участников реакции (реагентов и продуктов), вызванное действием внешних условий. 1. Изменение концентраций реагентов или продуктов реакции(изменение давления или объема) 2. Изменение температуры 3. Участие в реакции катализатора
 Принцип Ле Шателье Если на систему, находящуюся в равновесии, оказывается внешнее воздействие, смещающее это равновесие, то данное равновесие смещается в сторону, ослабляющее это воздействие, до тех пор, пока нарастающее в системе противодействие не станет равным оказываемому действию.
Принцип Ле Шателье Если на систему, находящуюся в равновесии, оказывается внешнее воздействие, смещающее это равновесие, то данное равновесие смещается в сторону, ослабляющее это воздействие, до тех пор, пока нарастающее в системе противодействие не станет равным оказываемому действию.


