Cлайд_к_л_7.ppt
- Количество слайдов: 25
 Лекция № 7 Строение атома и периодическая система химических элементов (продолжение)
Лекция № 7 Строение атома и периодическая система химических элементов (продолжение)
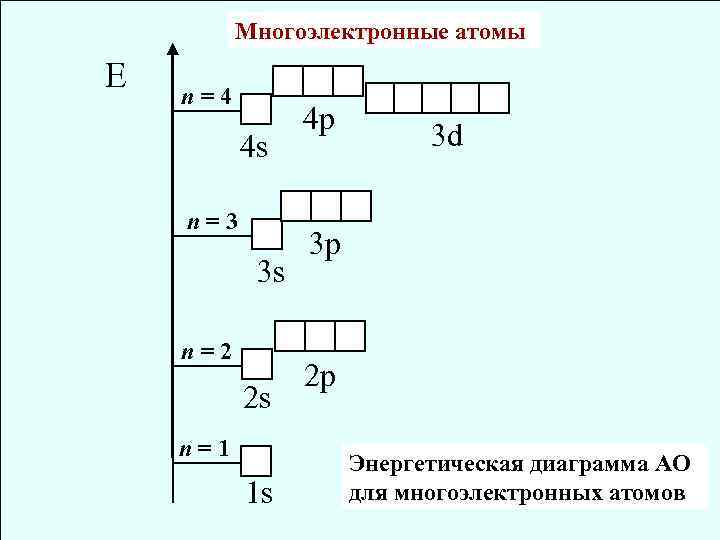 Многоэлектронные атомы Е n=4 4 s n=3 3 s n=2 2 s n=1 1 s 4 p 3 d 3 p 2 p Энергетическая диаграмма АО для многоэлектронных атомов
Многоэлектронные атомы Е n=4 4 s n=3 3 s n=2 2 s n=1 1 s 4 p 3 d 3 p 2 p Энергетическая диаграмма АО для многоэлектронных атомов
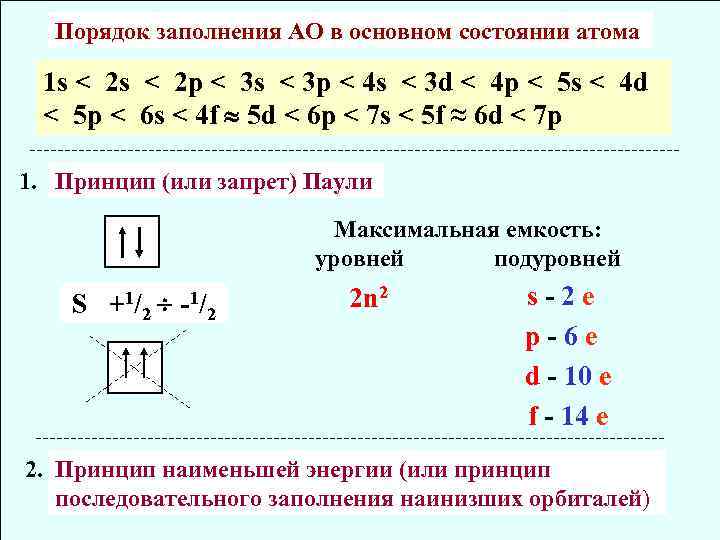 Порядок заполнения АО в основном состоянии атома 1 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p < 5 s < 4 d < 5 p < 6 s < 4 f 5 d < 6 p < 7 s < 5 f ≈ 6 d < 7 p 1. Принцип (или запрет) Паули Максимальная емкость: уровней подуровней S +1/ 2 -1/ 2 2 n 2 s-2 е p-6 e d - 10 e f - 14 e 2. Принцип наименьшей энергии (или принцип последовательного заполнения наинизших орбиталей)
Порядок заполнения АО в основном состоянии атома 1 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p < 5 s < 4 d < 5 p < 6 s < 4 f 5 d < 6 p < 7 s < 5 f ≈ 6 d < 7 p 1. Принцип (или запрет) Паули Максимальная емкость: уровней подуровней S +1/ 2 -1/ 2 2 n 2 s-2 е p-6 e d - 10 e f - 14 e 2. Принцип наименьшей энергии (или принцип последовательного заполнения наинизших орбиталей)
 3. Правило Хунда При данном значении l (т. е. в пределах одного подуровня) электроны располагаются таким образом, чтобы суммарный спин был максимальным Суммарный спин электронов 1/ 2 3/ 2
3. Правило Хунда При данном значении l (т. е. в пределах одного подуровня) электроны располагаются таким образом, чтобы суммарный спин был максимальным Суммарный спин электронов 1/ 2 3/ 2
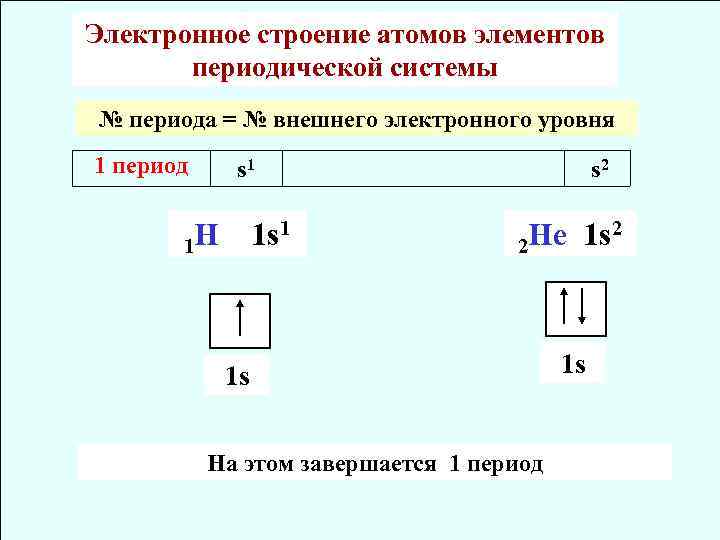 Электронное строение атомов элементов периодической системы № периода = № внешнего электронного уровня 1 период s 1 1 H 1 s 1 s 2 He 1 s 2 2 1 s На этом завершается 1 период 1 s
Электронное строение атомов элементов периодической системы № периода = № внешнего электронного уровня 1 период s 1 1 H 1 s 1 s 2 He 1 s 2 2 1 s На этом завершается 1 период 1 s
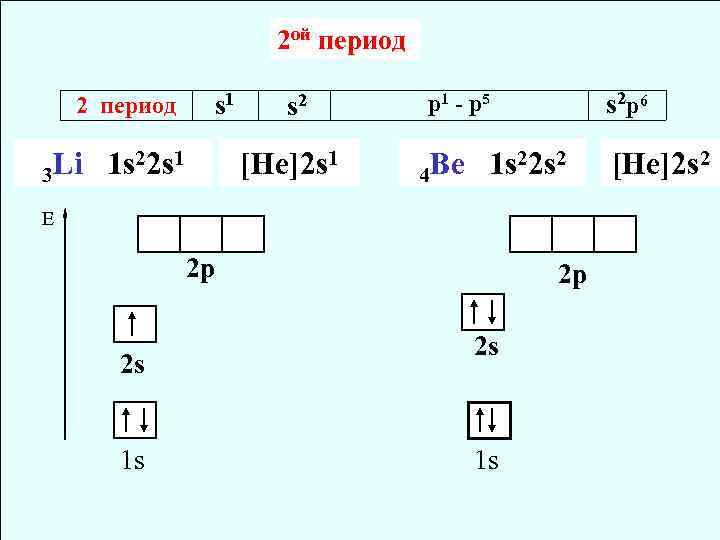 2 ой период 2 период s 1 Li 1 s 22 s 1 3 s 2 [He]2 s 1 s 2 p 6 p 1 - p 5 Be 1 s 22 s 2 4 E 2 p 2 s 1 s [He]2 s 2
2 ой период 2 период s 1 Li 1 s 22 s 1 3 s 2 [He]2 s 1 s 2 p 6 p 1 - p 5 Be 1 s 22 s 2 4 E 2 p 2 s 1 s [He]2 s 2
![В 1 s 22 p 1 5 [He]2 s 22 p 1 C 1 В 1 s 22 p 1 5 [He]2 s 22 p 1 C 1](https://present5.com/presentation/3/26150394_161124070.pdf-img/26150394_161124070.pdf-7.jpg) В 1 s 22 p 1 5 [He]2 s 22 p 1 C 1 s 22 p 2 6 [He]2 s 22 p 2 E 2 p 2 p 2 s 2 s 1 s 1 s Противоречит правилу Хунда
В 1 s 22 p 1 5 [He]2 s 22 p 1 C 1 s 22 p 2 6 [He]2 s 22 p 2 E 2 p 2 p 2 s 2 s 1 s 1 s Противоречит правилу Хунда
![7 N 1 s 22 p 3 [He]2 s 22 p 3 O 1 7 N 1 s 22 p 3 [He]2 s 22 p 3 O 1](https://present5.com/presentation/3/26150394_161124070.pdf-img/26150394_161124070.pdf-8.jpg) 7 N 1 s 22 p 3 [He]2 s 22 p 3 O 1 s 22 p 4 8 [He]2 s 224 E 2 p 2 p 2 s 2 s 1 s 1 s
7 N 1 s 22 p 3 [He]2 s 22 p 3 O 1 s 22 p 4 8 [He]2 s 224 E 2 p 2 p 2 s 2 s 1 s 1 s
![9 F 1 s 22 p 5 10 Ne [He]2 s 22 p 5 9 F 1 s 22 p 5 10 Ne [He]2 s 22 p 5](https://present5.com/presentation/3/26150394_161124070.pdf-img/26150394_161124070.pdf-9.jpg) 9 F 1 s 22 p 5 10 Ne [He]2 s 22 p 5 1 s 22 p 6 [He]2 s 22 p 6 = [Ne] E 2 p 2 p 2 s 1 s
9 F 1 s 22 p 5 10 Ne [He]2 s 22 p 5 1 s 22 p 6 [He]2 s 22 p 6 = [Ne] E 2 p 2 p 2 s 1 s
 3 ий период 3 период s 1 s 2 Na 1 s 22 p 63 s 1 11 Mg 1 s 22 p 63 s 2 12 Al 1 s 22 p 63 s 23 p 1 13 Si 1 s 22 p 63 s 23 p 2 14 P 1 s 22 p 63 s 23 p 3 15 S 1 s 22 p 63 s 23 p 4 16 Cl 1 s 22 p 63 s 23 p 5 17 Ar 1 s 22 p 63 s 23 p 6 18 p 1 - p 5 s 2 p 6 [Ne]3 s 1 [Ne]3 s 23 p 2 [Ne]3 s 23 p 3 [Ne]3 s 23 p 4 [Ne]3 s 23 p 5 [Ne]3 s 23 p 6 = [Ar]
3 ий период 3 период s 1 s 2 Na 1 s 22 p 63 s 1 11 Mg 1 s 22 p 63 s 2 12 Al 1 s 22 p 63 s 23 p 1 13 Si 1 s 22 p 63 s 23 p 2 14 P 1 s 22 p 63 s 23 p 3 15 S 1 s 22 p 63 s 23 p 4 16 Cl 1 s 22 p 63 s 23 p 5 17 Ar 1 s 22 p 63 s 23 p 6 18 p 1 - p 5 s 2 p 6 [Ne]3 s 1 [Ne]3 s 23 p 2 [Ne]3 s 23 p 3 [Ne]3 s 23 p 4 [Ne]3 s 23 p 5 [Ne]3 s 23 p 6 = [Ar]
 4 ый период 4 период s 1 s 2 p 1 - p 5 d 1 - d 10 s 2 p 6 К [Ar] 4 s 1 Ca [Ar] 4 s 2 Sc [Ar] 3 d 14 s 2 энергия 3 d < 4 p Ti [Ar] 3 d 24 s 2 V [Ar] 3 d 34 s 2 Cr [Ar] 3 d 54 s 1 Mn [Ar] 3 d 54 s 2 “проскок” 3 d е 4 s исключение из правил
4 ый период 4 период s 1 s 2 p 1 - p 5 d 1 - d 10 s 2 p 6 К [Ar] 4 s 1 Ca [Ar] 4 s 2 Sc [Ar] 3 d 14 s 2 энергия 3 d < 4 p Ti [Ar] 3 d 24 s 2 V [Ar] 3 d 34 s 2 Cr [Ar] 3 d 54 s 1 Mn [Ar] 3 d 54 s 2 “проскок” 3 d е 4 s исключение из правил
![Fe [Ar] 3 d 64 s 2 Co [Ar] 3 d 74 s 2 Fe [Ar] 3 d 64 s 2 Co [Ar] 3 d 74 s 2](https://present5.com/presentation/3/26150394_161124070.pdf-img/26150394_161124070.pdf-12.jpg) Fe [Ar] 3 d 64 s 2 Co [Ar] 3 d 74 s 2 Ni [Ar] 3 d 84 s 2 Cu [Ar] 3 d 104 s 1 Zn [Ar] 3 d 104 s 2 Ga [Ar] 3 d 104 s 24 p 1 ………… Kr [Ar] 3 d 104 s 24 p 6 исключение из правил “провал” или “ проскок ” е 3 d 4 s Устойчивая электронная конфигурация d 0, d 5, d 10
Fe [Ar] 3 d 64 s 2 Co [Ar] 3 d 74 s 2 Ni [Ar] 3 d 84 s 2 Cu [Ar] 3 d 104 s 1 Zn [Ar] 3 d 104 s 2 Ga [Ar] 3 d 104 s 24 p 1 ………… Kr [Ar] 3 d 104 s 24 p 6 исключение из правил “провал” или “ проскок ” е 3 d 4 s Устойчивая электронная конфигурация d 0, d 5, d 10
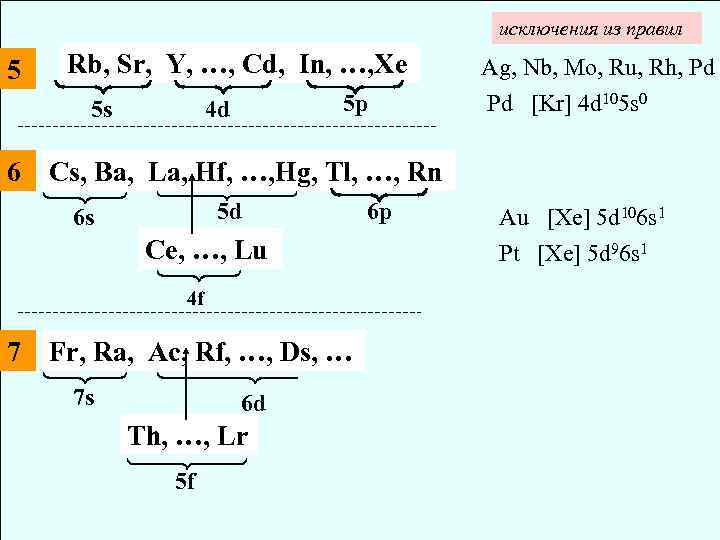 исключения из правил 5 Rb, Sr, Y, …, Cd, In, …, Xe 5 s 5 p 4 d 6 Cs, Ba, La, Hf, …, Hg, Tl, …, Rn 5 d 6 s Ce, …, Lu 4 f 7 Fr, Ra, Ac, Rf, …, Ds, … 7 s 6 d Th, …, Lr 5 f 6 p Ag, Nb, Mo, Ru, Rh, Pd Pd [Kr] 4 d 105 s 0 Au [Xe] 5 d 106 s 1 Pt [Xe] 5 d 96 s 1
исключения из правил 5 Rb, Sr, Y, …, Cd, In, …, Xe 5 s 5 p 4 d 6 Cs, Ba, La, Hf, …, Hg, Tl, …, Rn 5 d 6 s Ce, …, Lu 4 f 7 Fr, Ra, Ac, Rf, …, Ds, … 7 s 6 d Th, …, Lr 5 f 6 p Ag, Nb, Mo, Ru, Rh, Pd Pd [Kr] 4 d 105 s 0 Au [Xe] 5 d 106 s 1 Pt [Xe] 5 d 96 s 1
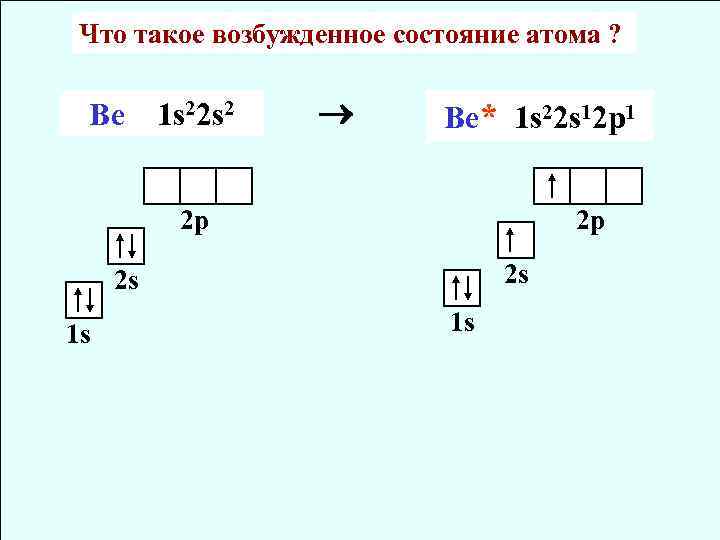 Что такое возбужденное состояние атома ? Ве 1 s 22 s 2 Be* 1 s 22 s 12 p 1 2 p 2 p 2 s 2 s 1 s 1 s
Что такое возбужденное состояние атома ? Ве 1 s 22 s 2 Be* 1 s 22 s 12 p 1 2 p 2 p 2 s 2 s 1 s 1 s
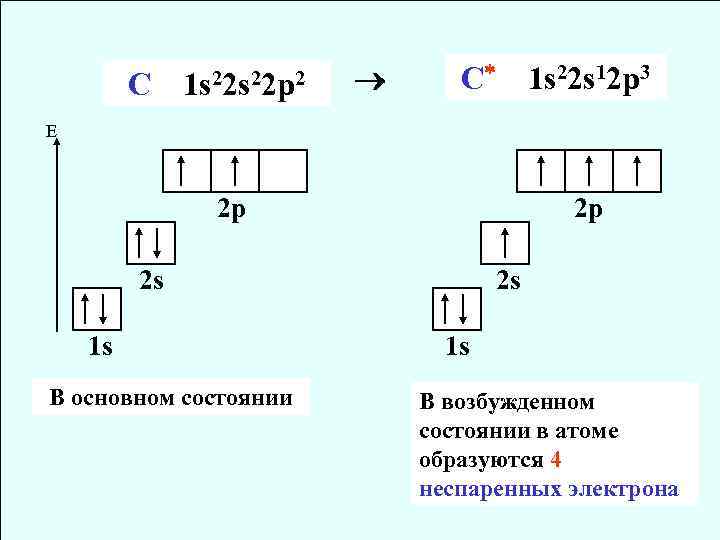 С 1 s 22 p 2 C 1 s 22 s 12 p 3 E 2 p 2 p 2 s 1 s В основном состоянии 2 s 1 s В возбужденном состоянии в атоме образуются 4 неспаренных электрона
С 1 s 22 p 2 C 1 s 22 s 12 p 3 E 2 p 2 p 2 s 1 s В основном состоянии 2 s 1 s В возбужденном состоянии в атоме образуются 4 неспаренных электрона
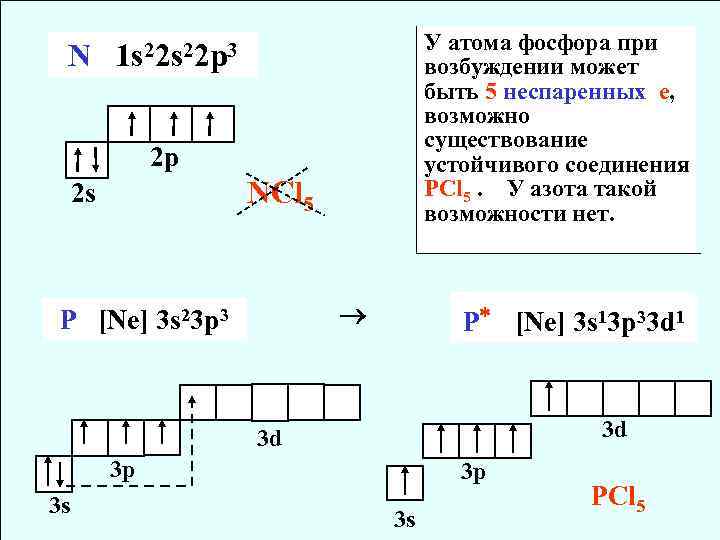 N У атома фосфора при возбуждении может быть 5 неспаренных е, возможно существование устойчивого соединения PCl 5. У азота такой возможности нет. 1 s 22 p 3 2 p NCl 5 2 s P [Ne] 3 s 23 p 3 P [Ne] 3 s 13 p 33 d 1 3 d 3 d 3 p 3 s PCl 5
N У атома фосфора при возбуждении может быть 5 неспаренных е, возможно существование устойчивого соединения PCl 5. У азота такой возможности нет. 1 s 22 p 3 2 p NCl 5 2 s P [Ne] 3 s 23 p 3 P [Ne] 3 s 13 p 33 d 1 3 d 3 d 3 p 3 s PCl 5
![Парамагнитные и диамагнитные свойства веществ Zn [Ar] 3 d 104 s 2 3 d Парамагнитные и диамагнитные свойства веществ Zn [Ar] 3 d 104 s 2 3 d](https://present5.com/presentation/3/26150394_161124070.pdf-img/26150394_161124070.pdf-17.jpg) Парамагнитные и диамагнитные свойства веществ Zn [Ar] 3 d 104 s 2 3 d 4 s Диамагнитные свойства Cr [Ar] 3 d 54 s 1 Парамагнитные свойства 3 d 4 s
Парамагнитные и диамагнитные свойства веществ Zn [Ar] 3 d 104 s 2 3 d 4 s Диамагнитные свойства Cr [Ar] 3 d 54 s 1 Парамагнитные свойства 3 d 4 s
 Структура периодической системы Короткопериодная система 1. По горизонтали – периоды. Всего 7 периодов. 2. По вертикали – группы. Всего 8 групп. 3. Группы делятся на подгруппы ( А и В ): А - подгруппы – главные В - подгруппы – побочные 4. В А-подгруппах находятся s- и p-элементы В В-подгруппах находятся d- и f- элементы
Структура периодической системы Короткопериодная система 1. По горизонтали – периоды. Всего 7 периодов. 2. По вертикали – группы. Всего 8 групп. 3. Группы делятся на подгруппы ( А и В ): А - подгруппы – главные В - подгруппы – побочные 4. В А-подгруппах находятся s- и p-элементы В В-подгруппах находятся d- и f- элементы
![Характеристика семейств элементов s - элементы [благ. газ]nsх IA, IIA х= 1, 2 n Характеристика семейств элементов s - элементы [благ. газ]nsх IA, IIA х= 1, 2 n](https://present5.com/presentation/3/26150394_161124070.pdf-img/26150394_161124070.pdf-19.jpg) Характеристика семейств элементов s - элементы [благ. газ]nsх IA, IIA х= 1, 2 n - № периода х - № подгруппы p - элементы [благ. газ]ns 2 px IIIA - VIIIA n = 2, 3 x =1 -6 [благ. газ](n-1)d 10 ns 2 npx n = 4, … 2 + x - № подгруппы
Характеристика семейств элементов s - элементы [благ. газ]nsх IA, IIA х= 1, 2 n - № периода х - № подгруппы p - элементы [благ. газ]ns 2 px IIIA - VIIIA n = 2, 3 x =1 -6 [благ. газ](n-1)d 10 ns 2 npx n = 4, … 2 + x - № подгруппы
dxnsy х + d - элементы IB - VIIIB n = 4, … [благ. газ](n-1)dxnsy х +](https://present5.com/presentation/3/26150394_161124070.pdf-img/26150394_161124070.pdf-20.jpg) d - элементы IB - VIIIB n = 4, … [благ. газ](n-1)dxnsy х + y - № подгруппы x=1 -10, y=2, 1 исключение: IB, IIB, VIIIB f - элементы IIIB Лантаноиды (4 f) Актиноиды (5 f)
d - элементы IB - VIIIB n = 4, … [благ. газ](n-1)dxnsy х + y - № подгруппы x=1 -10, y=2, 1 исключение: IB, IIB, VIIIB f - элементы IIIB Лантаноиды (4 f) Актиноиды (5 f)
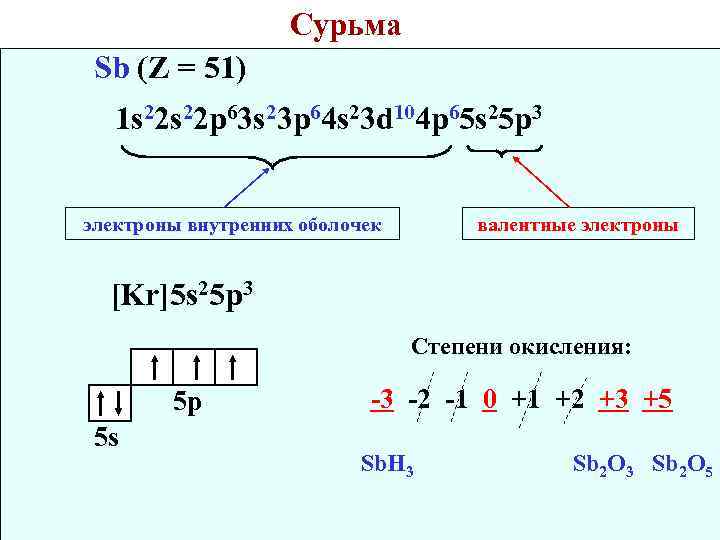 Сурьма Sb (Z = 51) 1 s 22 p 63 s 23 p 64 s 23 d 104 p 65 s 25 p 3 электроны внутренних оболочек валентные электроны [Kr]5 s 25 p 3 Степени окисления: 5 p 5 s -3 -2 -1 0 +1 +2 +3 +5 Sb. H 3 Sb 2 O 5
Сурьма Sb (Z = 51) 1 s 22 p 63 s 23 p 64 s 23 d 104 p 65 s 25 p 3 электроны внутренних оболочек валентные электроны [Kr]5 s 25 p 3 Степени окисления: 5 p 5 s -3 -2 -1 0 +1 +2 +3 +5 Sb. H 3 Sb 2 O 5
 Цирконий Zr (Z = 40) 1 s 22 p 63 s 23 p 64 s 23 d 104 p 65 s 24 d 2 электроны внутренних оболочек валентные электроны [Kr]4 d 25 s 2 Степени окисления: 4 d 5 s 0 +2 +3 +4 Zr. O 2
Цирконий Zr (Z = 40) 1 s 22 p 63 s 23 p 64 s 23 d 104 p 65 s 24 d 2 электроны внутренних оболочек валентные электроны [Kr]4 d 25 s 2 Степени окисления: 4 d 5 s 0 +2 +3 +4 Zr. O 2
 Правило октета На орбитали с n = 2 общее число е = 8 (2 s 22 p 6) На орбитали с n = 3 на s и p подуровнях число е = 8 (3 s 23 p 6 ) Атомы s- и p- элементов имеют тенденцию отдавать, принимать или объединять электроны так, чтобы заполнить восьмью электронами внешнюю оболочку F [He]2 s 22 p 5 F + 1 е = F-1 [He]2 s 22 p 6 ns 2 np 6
Правило октета На орбитали с n = 2 общее число е = 8 (2 s 22 p 6) На орбитали с n = 3 на s и p подуровнях число е = 8 (3 s 23 p 6 ) Атомы s- и p- элементов имеют тенденцию отдавать, принимать или объединять электроны так, чтобы заполнить восьмью электронами внешнюю оболочку F [He]2 s 22 p 5 F + 1 е = F-1 [He]2 s 22 p 6 ns 2 np 6
![N [He]2 s 22 p 3 N-3 [He]2 s 22 p 6 N + N [He]2 s 22 p 3 N-3 [He]2 s 22 p 6 N +](https://present5.com/presentation/3/26150394_161124070.pdf-img/26150394_161124070.pdf-24.jpg) N [He]2 s 22 p 3 N-3 [He]2 s 22 p 6 N + 3 е = N 3 - C*[He]2 s 12 p 3 O C [He]2 s 22 p 6 H H C H H Правило октета – инструмент для предсказания возможности образования ионов или ковалентной связи
N [He]2 s 22 p 3 N-3 [He]2 s 22 p 6 N + 3 е = N 3 - C*[He]2 s 12 p 3 O C [He]2 s 22 p 6 H H C H H Правило октета – инструмент для предсказания возможности образования ионов или ковалентной связи
 Периодический закон и Периодическая система химических элементов Д. И. Менделеева 1869 г. Свойства элементов и их соединений находятся в периодической зависимости от заряда ядра атома (или порядкового номера элемента)
Периодический закон и Периодическая система химических элементов Д. И. Менделеева 1869 г. Свойства элементов и их соединений находятся в периодической зависимости от заряда ядра атома (или порядкового номера элемента)


