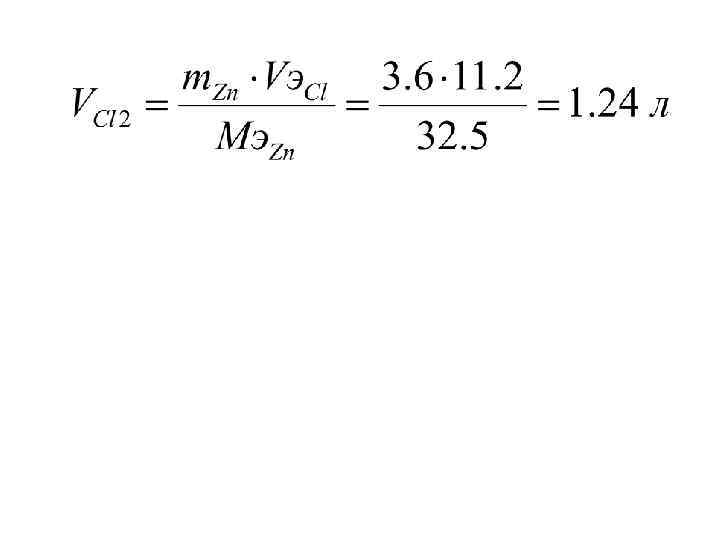лекция 7-электрохимия.ppt
- Количество слайдов: 41
 Лекция 7 Электрохимические процессы 1
Лекция 7 Электрохимические процессы 1
 Двойной электрический слой. Электродные потенциалы по схеме: Ме 0 – nē Меn+ + nē Ме 0
Двойной электрический слой. Электродные потенциалы по схеме: Ме 0 – nē Меn+ + nē Ме 0
 С течением времени устанавливается равновесие: Ме 0 + m. H 2 O ⇄ Me(H 2 O)mn+ + nē Или упрощенно: 0 Ме ⇄ n++ Ме nē 3
С течением времени устанавливается равновесие: Ме 0 + m. H 2 O ⇄ Me(H 2 O)mn+ + nē Или упрощенно: 0 Ме ⇄ n++ Ме nē 3
 Влияние природы металла Активные металлы Zn 0 – 2ē Zn 2+
Влияние природы металла Активные металлы Zn 0 – 2ē Zn 2+
 Малоактивные металлы Сu 2+ + 2ē → Cu 0 5
Малоактивные металлы Сu 2+ + 2ē → Cu 0 5
![Электродный потенциал (Е, , [В]) Если концентрация ионов равна 1 моль/л при температуре 25 Электродный потенциал (Е, , [В]) Если концентрация ионов равна 1 моль/л при температуре 25](https://present5.com/presentation/43238305_454430522/image-6.jpg) Электродный потенциал (Е, , [В]) Если концентрация ионов равна 1 моль/л при температуре 25 о. С, то электродный потенциал называют стандартным электродным потенциалом Ео( о). 6
Электродный потенциал (Е, , [В]) Если концентрация ионов равна 1 моль/л при температуре 25 о. С, то электродный потенциал называют стандартным электродным потенциалом Ео( о). 6
 Водородный электрод Н 2 – 2ē ⇄ 2 Н+ 7
Водородный электрод Н 2 – 2ē ⇄ 2 Н+ 7
 Пример: Fe + Cu. Cl 2 = Fe. Cl 2 +Cu Cu + Hg(NO 3)2 = Hg + Cu(NO 3)2 Zn+2 HCl=Zn. Cl 2+H 2 8
Пример: Fe + Cu. Cl 2 = Fe. Cl 2 +Cu Cu + Hg(NO 3)2 = Hg + Cu(NO 3)2 Zn+2 HCl=Zn. Cl 2+H 2 8
 Таблица стандартных электродных потенциалов характеризует химическую активность металлов. 1. чем меньше электродный потенциал металла, тем больше его восстановительная способность и тем активнее металл 2. металлы, имеющие отрицательный электродный потенциал и стоящие в ряду напряжений до водорода, вытесняют его из разбавленных растворов кислот (кроме азотной кислоты); 3. каждый металл способен вытеснять (восстанавливать) из растворов солей те металлы, которые в ряду напряжений стоят после него.
Таблица стандартных электродных потенциалов характеризует химическую активность металлов. 1. чем меньше электродный потенциал металла, тем больше его восстановительная способность и тем активнее металл 2. металлы, имеющие отрицательный электродный потенциал и стоящие в ряду напряжений до водорода, вытесняют его из разбавленных растворов кислот (кроме азотной кислоты); 3. каждый металл способен вытеснять (восстанавливать) из растворов солей те металлы, которые в ряду напряжений стоят после него.
 формула Нернста: о – стандартный электродный потенциал (В); F – постоянная Фарадея (96500 Кл/экв);
формула Нернста: о – стандартный электродный потенциал (В); F – постоянная Фарадея (96500 Кл/экв);
 R – универсальная газовая постоянная (8, 314 Дж/моль); T – фактическая температура (298 К); n – число электронов, принимающих участие в процессе; – концентрация (активность) ионов металла в растворе (моль/л) 11
R – универсальная газовая постоянная (8, 314 Дж/моль); T – фактическая температура (298 К); n – число электронов, принимающих участие в процессе; – концентрация (активность) ионов металла в растворе (моль/л) 11
 Цинковая пластинка погружена в 0, 01 М раствор её соли 12
Цинковая пластинка погружена в 0, 01 М раствор её соли 12
 Гальванические элементы (ГЭ) 13
Гальванические элементы (ГЭ) 13
 Элемент Даниэля-Якоби (К) (А) 14
Элемент Даниэля-Якоби (К) (А) 14
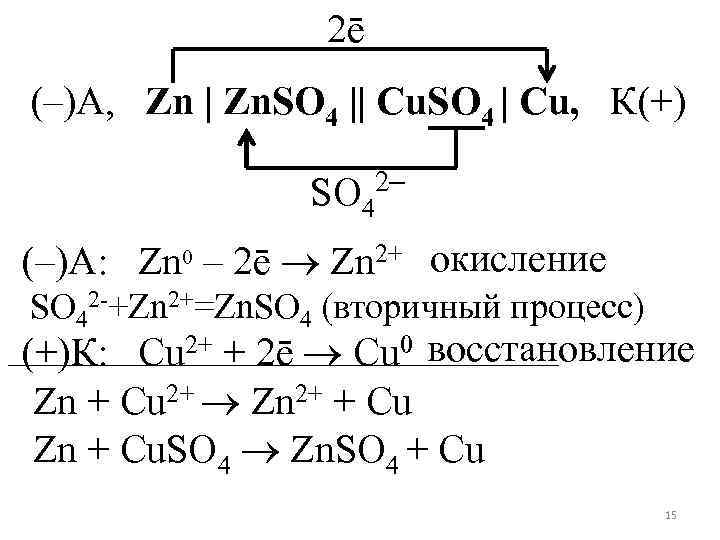 2ē (–)А, Zn | Zn. SO 4 || Cu. SO 4 | Cu, К(+) 2– SO 4 (–)А: Zn 0 – 2ē Zn 2+ окисление SO 42 -+Zn 2+=Zn. SO 4 (вторичный процесс) (+)К: Сu 2+ + 2ē Cu 0 восстановление Zn + Сu 2+ Zn 2+ + Cu Zn + Cu. SO 4 Zn. SO 4 + Cu 15
2ē (–)А, Zn | Zn. SO 4 || Cu. SO 4 | Cu, К(+) 2– SO 4 (–)А: Zn 0 – 2ē Zn 2+ окисление SO 42 -+Zn 2+=Zn. SO 4 (вторичный процесс) (+)К: Сu 2+ + 2ē Cu 0 восстановление Zn + Сu 2+ Zn 2+ + Cu Zn + Cu. SO 4 Zn. SO 4 + Cu 15
 ЭДС при стандартных условиях: – ЭДС = Для элемента Даниэля-Якоби: ЭДС = – = = 0, 34 + 0, 76 = 1, 1 В 16
ЭДС при стандартных условиях: – ЭДС = Для элемента Даниэля-Якоби: ЭДС = – = = 0, 34 + 0, 76 = 1, 1 В 16
 Формула Нернста о – стандартный электродный потенциал (В); n – число отданных или принятых электронов; – концентрация ионов металла в растворе (моль/л).
Формула Нернста о – стандартный электродный потенциал (В); n – число отданных или принятых электронов; – концентрация ионов металла в растворе (моль/л).
 Пример: Цинковая пластинка погружена в 0, 01 м раствор её соли. 18
Пример: Цинковая пластинка погружена в 0, 01 м раствор её соли. 18
 Элемент Вольта (К) (А) 19
Элемент Вольта (К) (А) 19
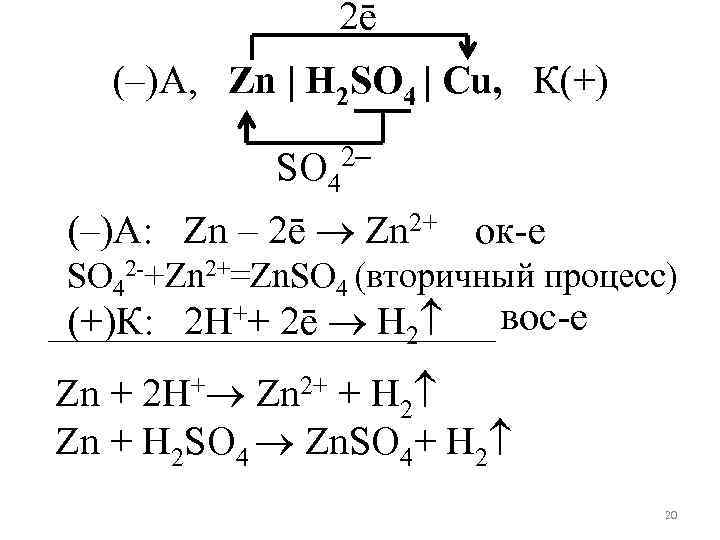 2ē (–)А, Zn | H 2 SO 4 | Cu, К(+) SO 42– (–)А: Zn – 2ē Zn 2+ ок-е SO 42 -+Zn 2+=Zn. SO 4 (вторичный процесс) (+)К: 2 Н++ 2ē Н 2 вос-е Zn + 2 Н+ Zn 2+ + Н 2 Zn + H 2 SO 4 Zn. SO 4+ Н 2 20
2ē (–)А, Zn | H 2 SO 4 | Cu, К(+) SO 42– (–)А: Zn – 2ē Zn 2+ ок-е SO 42 -+Zn 2+=Zn. SO 4 (вторичный процесс) (+)К: 2 Н++ 2ē Н 2 вос-е Zn + 2 Н+ Zn 2+ + Н 2 Zn + H 2 SO 4 Zn. SO 4+ Н 2 20
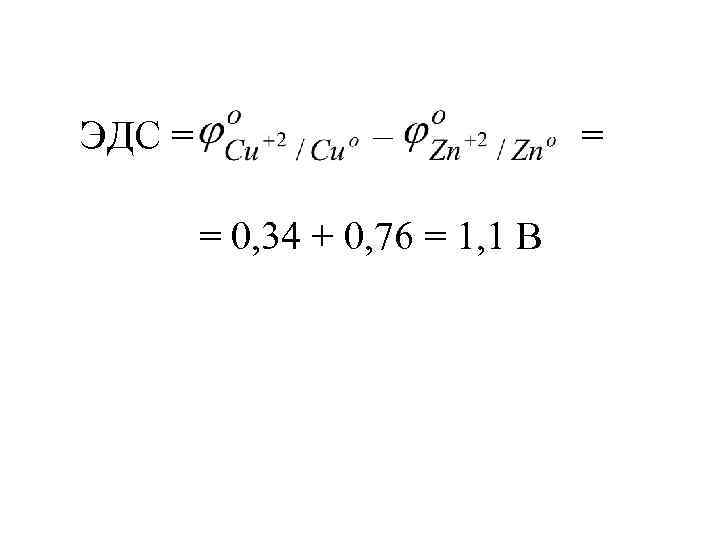 ЭДС = – = 0, 34 + 0, 76 = 1, 1 В =
ЭДС = – = 0, 34 + 0, 76 = 1, 1 В =
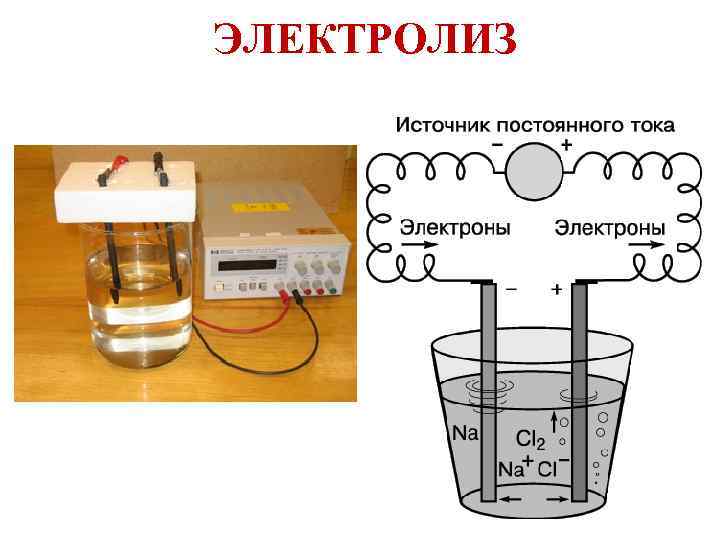 ЭЛЕКТРОЛИЗ
ЭЛЕКТРОЛИЗ
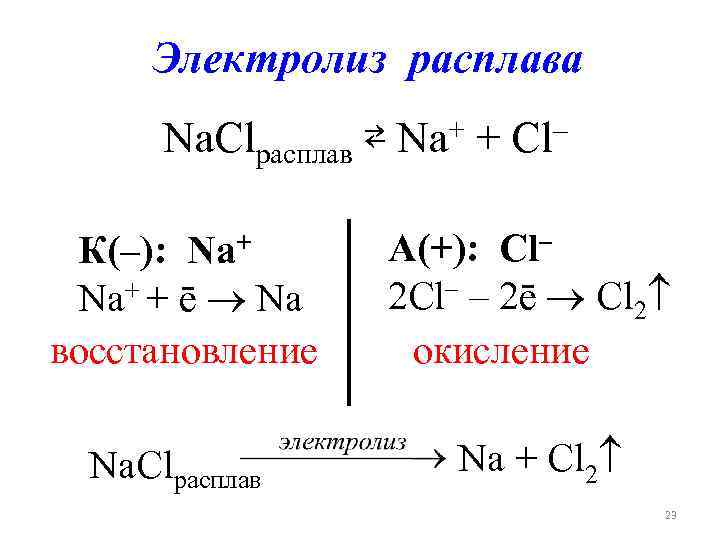 Электролиз расплава Na. Clрасплав ⇄ Na+ + Cl– К(–): Na+ + ē Na восстановление А(+): Cl– 2 Cl– – 2ē Cl 2 окисление Na. Clрасплав Na + Cl 2 23
Электролиз расплава Na. Clрасплав ⇄ Na+ + Cl– К(–): Na+ + ē Na восстановление А(+): Cl– 2 Cl– – 2ē Cl 2 окисление Na. Clрасплав Na + Cl 2 23
 Na 2 SO 4 расплав ⇄ 2 Na+ + SO 4– 2 К (–): Na+ А (+): SO 4– 2 Na++ ē Na SO 4– 2– 2ē SO 3 +1/2 O 2 2 Na 2 SO 4 расплав 4 Na + 2 SO 3 + O 2
Na 2 SO 4 расплав ⇄ 2 Na+ + SO 4– 2 К (–): Na+ А (+): SO 4– 2 Na++ ē Na SO 4– 2– 2ē SO 3 +1/2 O 2 2 Na 2 SO 4 расплав 4 Na + 2 SO 3 + O 2
 Электролиз водных растворов 25
Электролиз водных растворов 25
 Последовательность разрядки ионов и молекул на электродах 1) На катоде: в первую очередь разряжается (восстанавливается) ион металла, имеющий больший потенциал. о, В Zn 2+ + Ag – 0. 76 +0. 85 1 3 2+ Cu +0, 34 2 – + 1ē → Ag 0 Ag 2+ + 2ē → Cu 0 Ca 26
Последовательность разрядки ионов и молекул на электродах 1) На катоде: в первую очередь разряжается (восстанавливается) ион металла, имеющий больший потенциал. о, В Zn 2+ + Ag – 0. 76 +0. 85 1 3 2+ Cu +0, 34 2 – + 1ē → Ag 0 Ag 2+ + 2ē → Cu 0 Ca 26
 Металл о, В Li … Al Mn … Pb Cu … Au Процесс восстановления 2 H 2 O + 2ē → 2 OH– + H 2↑ о = – 0. 41 B В кислой среде: 2 H+ + 2ē → H 2↑ φо = 0 B Mn 2+ + 2ē Mn 2 H 2 O + 2ē → 2 OH– + H 2↑ восстановление и металла, и воды. Cu 2+ + 2ē Cu
Металл о, В Li … Al Mn … Pb Cu … Au Процесс восстановления 2 H 2 O + 2ē → 2 OH– + H 2↑ о = – 0. 41 B В кислой среде: 2 H+ + 2ē → H 2↑ φо = 0 B Mn 2+ + 2ē Mn 2 H 2 O + 2ē → 2 OH– + H 2↑ восстановление и металла, и воды. Cu 2+ + 2ē Cu
 2) На аноде: окисляются более сильные восстановители – вещества, имеющие меньшее значение потенциала. о, В SO 42– +2. 05 3 OH– (H 2 O) Cl– +1. 4 +1, 36 2 1 – – 2ē → Cl ↑ 2 Cl 2 2 H 2 O – 4ē → 4 H+ + O 2↑ 28
2) На аноде: окисляются более сильные восстановители – вещества, имеющие меньшее значение потенциала. о, В SO 42– +2. 05 3 OH– (H 2 O) Cl– +1. 4 +1, 36 2 1 – – 2ē → Cl ↑ 2 Cl 2 2 H 2 O – 4ē → 4 H+ + O 2↑ 28
 Асm– Анод бескислородных кислот кислородсодержащих кислот Растворимый Me – nē Men+ Инертный Асm– – mē Асо В кислой и нейтральной (кроме F–) среде: 2 H 2 O – 4ē → 4 H+ + O 2↑ о = – 1, 23 B для прямой полуреакции В щелочной среде: 4 OH– – 4ē → 2 H 2 O+O 2↑ о = – 0. 401 B для прямой полуреакции 29
Асm– Анод бескислородных кислот кислородсодержащих кислот Растворимый Me – nē Men+ Инертный Асm– – mē Асо В кислой и нейтральной (кроме F–) среде: 2 H 2 O – 4ē → 4 H+ + O 2↑ о = – 1, 23 B для прямой полуреакции В щелочной среде: 4 OH– – 4ē → 2 H 2 O+O 2↑ о = – 0. 401 B для прямой полуреакции 29
 Электролиз водного раствора иодида калия с инертными электродами KI ⇄ K+ + I– H 2 O ⇄ H+ + OH– К(–): K+; H+(H 2 O) А(+): I–; OH–(H 2 O) о о +0. 54 < +1. 4 – 2. 9 0 2 H 2 O + 2ē → – – 2ē → I 2 I 2 –+ H ↑ → 2 OH 2 вторичный процесс: K+ + OH– → KOH p. H > 7
Электролиз водного раствора иодида калия с инертными электродами KI ⇄ K+ + I– H 2 O ⇄ H+ + OH– К(–): K+; H+(H 2 O) А(+): I–; OH–(H 2 O) о о +0. 54 < +1. 4 – 2. 9 0 2 H 2 O + 2ē → – – 2ē → I 2 I 2 –+ H ↑ → 2 OH 2 вторичный процесс: K+ + OH– → KOH p. H > 7
 Электролиз водного раствора Na 2 SO 4 с инертными электродами Na 2 SO 4 ⇄ 2 Na+ + SO 42– H 2 O ⇄ H+ + OH– К(–): Na+, H+(H о – 3 0 2 O) 2 H 2 O + 2ē → 2 OH– + H 2↑ вторичный процесс: Na+ + OH– → Na. OH p. H > 7 SO 42–, –(H OH А(+): о +2. 05 +1. 4 2 O) 2 H 2 O – 4ē → → 4 H+ + O 2↑ вторичный процесс: 2 H++SO 42– → H 2 SO 4 p. H < 7
Электролиз водного раствора Na 2 SO 4 с инертными электродами Na 2 SO 4 ⇄ 2 Na+ + SO 42– H 2 O ⇄ H+ + OH– К(–): Na+, H+(H о – 3 0 2 O) 2 H 2 O + 2ē → 2 OH– + H 2↑ вторичный процесс: Na+ + OH– → Na. OH p. H > 7 SO 42–, –(H OH А(+): о +2. 05 +1. 4 2 O) 2 H 2 O – 4ē → → 4 H+ + O 2↑ вторичный процесс: 2 H++SO 42– → H 2 SO 4 p. H < 7
 Электролиз водного раствора Ni. SO 4 с инертными электродами Ni. SO 4 ⇄ Ni 2+ + SO 42– H 2 O ⇄ H+ + OH– К(–): Ni 2+, H+(H о – 0, 25 0 2 O) 2 H 2 O + 2ē → 2 OH– + H 2↑ Ni 2+ + 2ē → Ni 0 SO 42–, –(H OH А(+): о +2. 05 +1. 4 2 H 2 O – 4ē → → 4 H+ + O 2↑ 2 O)
Электролиз водного раствора Ni. SO 4 с инертными электродами Ni. SO 4 ⇄ Ni 2+ + SO 42– H 2 O ⇄ H+ + OH– К(–): Ni 2+, H+(H о – 0, 25 0 2 O) 2 H 2 O + 2ē → 2 OH– + H 2↑ Ni 2+ + 2ē → Ni 0 SO 42–, –(H OH А(+): о +2. 05 +1. 4 2 H 2 O – 4ē → → 4 H+ + O 2↑ 2 O)
 Электролиз водного раствора Ni. SO 4 с никелевым анодом Ni. SO 4 ⇄ Ni 2+ + SO 42– H 2 O ⇄ H+ + OH– H+(H Ni 2+ + 2ē → Ni 0 SO 42–, –, OH Ni 0 O) А(+): 2 о – 0, 25 0 о +2. 05 +1. 4>– 0, 25 2 H 2 O + 2ē → Ni 0 – 2ē → Ni 2+ 2 OH– + H 2↑ К(–): Ni 2+,
Электролиз водного раствора Ni. SO 4 с никелевым анодом Ni. SO 4 ⇄ Ni 2+ + SO 42– H 2 O ⇄ H+ + OH– H+(H Ni 2+ + 2ē → Ni 0 SO 42–, –, OH Ni 0 O) А(+): 2 о – 0, 25 0 о +2. 05 +1. 4>– 0, 25 2 H 2 O + 2ē → Ni 0 – 2ē → Ni 2+ 2 OH– + H 2↑ К(–): Ni 2+,
 Законы электролиза I закон Фарадея m = k. Q m – количество вещества, г; k – электрохимический эквивалент, г/Кл; Q – количество электричества, Кл.
Законы электролиза I закон Фарадея m = k. Q m – количество вещества, г; k – электрохимический эквивалент, г/Кл; Q – количество электричества, Кл.
 Q = I I – сила тока, А; – время, с. m = k. I
Q = I I – сила тока, А; – время, с. m = k. I
 Мэ – молярная масса эквивалента металла, г/моль; I – сила тока, А; F – число Фарадея (96500 Кл). – время, с.
Мэ – молярная масса эквивалента металла, г/моль; I – сила тока, А; F – число Фарадея (96500 Кл). – время, с.
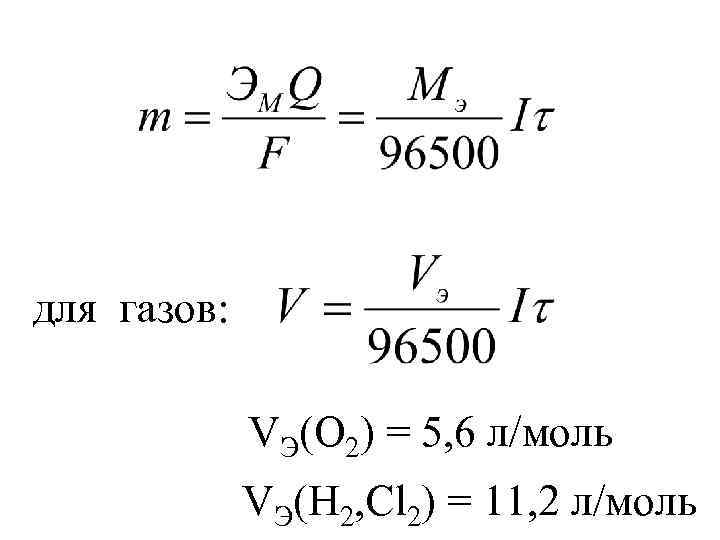 для газов: VЭ(O 2) = 5, 6 л/моль VЭ(H 2, Cl 2) = 11, 2 л/моль
для газов: VЭ(O 2) = 5, 6 л/моль VЭ(H 2, Cl 2) = 11, 2 л/моль
 II закон Фарадея m 1 : m 2 : … : mn = ЭМ 1 : ЭМ 2 : … : ЭМn Эм – химические эквиваленты веществ.
II закон Фарадея m 1 : m 2 : … : mn = ЭМ 1 : ЭМ 2 : … : ЭМn Эм – химические эквиваленты веществ.
 Пример: Zn. Cl 2 ⇄ Zn 2++ 2 Cl– Zn 2+, К (–): H 2 O о – 0. 76 – 0. 41 А (+): Cl–, H 2 O 1. 36 1. 23 Zn 2+ + 2ē → Zn 2 Cl– – 2ē → Cl 2↑
Пример: Zn. Cl 2 ⇄ Zn 2++ 2 Cl– Zn 2+, К (–): H 2 O о – 0. 76 – 0. 41 А (+): Cl–, H 2 O 1. 36 1. 23 Zn 2+ + 2ē → Zn 2 Cl– – 2ē → Cl 2↑
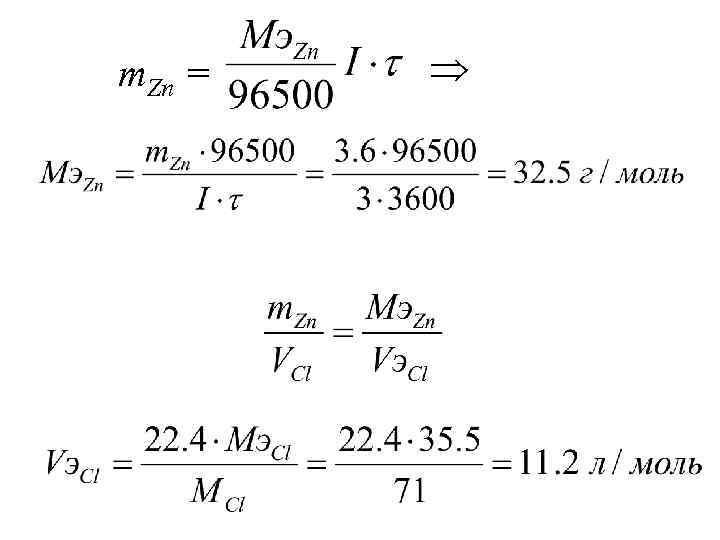 m. Zn =
m. Zn =