Cлайд_к_л_6.ppt
- Количество слайдов: 14
 Лекция № 6 Строение атома и периодическая система химических элементов
Лекция № 6 Строение атома и периодическая система химических элементов
 Развитие теории строения атома Атом - мельчайшая частица элемента Электрон ( е ) – элементарная частица, -1, 602 10 -19 Кл. Масса электрона - 9, 1 10 -28 г, что почти в 2000 раз меньше массы атома водорода (или протона) Масса протона - 1, 67 · 10 -24 г, диаметр атома - 10 -8 см, диаметр ядра атома - 10 -13 - 10 -12 см 1. Планетарная (ядерная) модель строения атома (Э. Резерфорд, 1911 г. ) 2. Теория Бора квантовая теория строения атома (1913 г. )
Развитие теории строения атома Атом - мельчайшая частица элемента Электрон ( е ) – элементарная частица, -1, 602 10 -19 Кл. Масса электрона - 9, 1 10 -28 г, что почти в 2000 раз меньше массы атома водорода (или протона) Масса протона - 1, 67 · 10 -24 г, диаметр атома - 10 -8 см, диаметр ядра атома - 10 -13 - 10 -12 см 1. Планетарная (ядерная) модель строения атома (Э. Резерфорд, 1911 г. ) 2. Теория Бора квантовая теория строения атома (1913 г. )
 Квантовая теория света Двойственная природа света - корпускулярно-волновой дуализм 1. Свет - это излучение электромагнитных волн различных частот Скорость света С = где - длина волны, - частота излучения (сек-1 или герц (Гц), 400 -800 нм Отражение , преломление, дифракция, интерференция
Квантовая теория света Двойственная природа света - корпускулярно-волновой дуализм 1. Свет - это излучение электромагнитных волн различных частот Скорость света С = где - длина волны, - частота излучения (сек-1 или герц (Гц), 400 -800 нм Отражение , преломление, дифракция, интерференция
 Квантовая природа излучения Е=h Ур-е Планка: с Е= Ур-е Эйнштейна: m· c 2 h = 6, 63 10 -34 Дж ·c Это уравнение связывает корпускулярную энергию фотона (кванта) Е с его волновой характеристикой hс Е = m · с2 = h·c = h m·c
Квантовая природа излучения Е=h Ур-е Планка: с Е= Ур-е Эйнштейна: m· c 2 h = 6, 63 10 -34 Дж ·c Это уравнение связывает корпускулярную энергию фотона (кванта) Е с его волновой характеристикой hс Е = m · с2 = h·c = h m·c
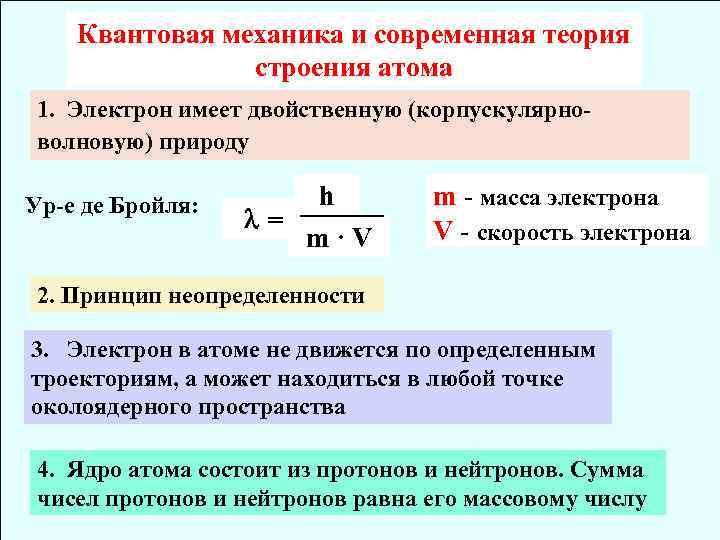 Квантовая механика и современная теория строения атома 1. Электрон имеет двойственную (корпускулярноволновую) природу Ур-е де Бройля: = h m·V m - масса электрона V - скорость электрона 2. Принцип неопределенности 3. Электрон в атоме не движется по определенным троекториям, а может находиться в любой точке околоядерного пространства 4. Ядро атома состоит из протонов и нейтронов. Сумма чисел протонов и нейтронов равна его массовому числу
Квантовая механика и современная теория строения атома 1. Электрон имеет двойственную (корпускулярноволновую) природу Ур-е де Бройля: = h m·V m - масса электрона V - скорость электрона 2. Принцип неопределенности 3. Электрон в атоме не движется по определенным троекториям, а может находиться в любой точке околоядерного пространства 4. Ядро атома состоит из протонов и нейтронов. Сумма чисел протонов и нейтронов равна его массовому числу
 Волновое уравнение Шредингера 8 2 me 2 2 + h 2 Австрийский физик Э. Шредингер, 1925 (E - Eп) = 0 (пси-функция) - волновая функция 2 - вероятность нахождения е в соответствующей области пространства Е и Еп - полная и потенциальная энергия е mе - масса е 2 - оператор Лапласа Электронное облако Точные решения уравнения Шредингера возможны только для атома водорода Решением уравнения Шредингера являются некоторые целочисленные значения n , l, m, называемые квантовыми числами
Волновое уравнение Шредингера 8 2 me 2 2 + h 2 Австрийский физик Э. Шредингер, 1925 (E - Eп) = 0 (пси-функция) - волновая функция 2 - вероятность нахождения е в соответствующей области пространства Е и Еп - полная и потенциальная энергия е mе - масса е 2 - оператор Лапласа Электронное облако Точные решения уравнения Шредингера возможны только для атома водорода Решением уравнения Шредингера являются некоторые целочисленные значения n , l, m, называемые квантовыми числами
 Квантовые числа. Четыре квантовых числа (n, l, m, s) n = 1, 2, 3, 4, К L M N l 0 1 2 3 s p d f nmax = 7 (сегодня) ( n - 1) Всего значений n l=0 n=2 l = 0, 1 n=3 m n=1 l = 0, 1, 2 n=4 l = 0, 1, 2, 3 - l , 0 , +l l =0 l=1 l=2 s - 1/2, + 1/2 Всего значений 2 l + 1 m = 0 m = -1, 0, +1 m = -2, -1, 0, +1, +2
Квантовые числа. Четыре квантовых числа (n, l, m, s) n = 1, 2, 3, 4, К L M N l 0 1 2 3 s p d f nmax = 7 (сегодня) ( n - 1) Всего значений n l=0 n=2 l = 0, 1 n=3 m n=1 l = 0, 1, 2 n=4 l = 0, 1, 2, 3 - l , 0 , +l l =0 l=1 l=2 s - 1/2, + 1/2 Всего значений 2 l + 1 m = 0 m = -1, 0, +1 m = -2, -1, 0, +1, +2
 Что означают квантовые числа? Квантовое число n определяет энергию е и размер атома r = 0, 529 ·n 2, А Квантовое число l определяет форму атомной орбитали Квантовое число m характеризует ориентацию АО в пространстве Спин проявляется в существовании у е магнитного момента за счет движения е вокруг собственной оси S = +½ - S = -½ - Что такое атомная орбиталь (АО) ?
Что означают квантовые числа? Квантовое число n определяет энергию е и размер атома r = 0, 529 ·n 2, А Квантовое число l определяет форму атомной орбитали Квантовое число m характеризует ориентацию АО в пространстве Спин проявляется в существовании у е магнитного момента за счет движения е вокруг собственной оси S = +½ - S = -½ - Что такое атомная орбиталь (АО) ?
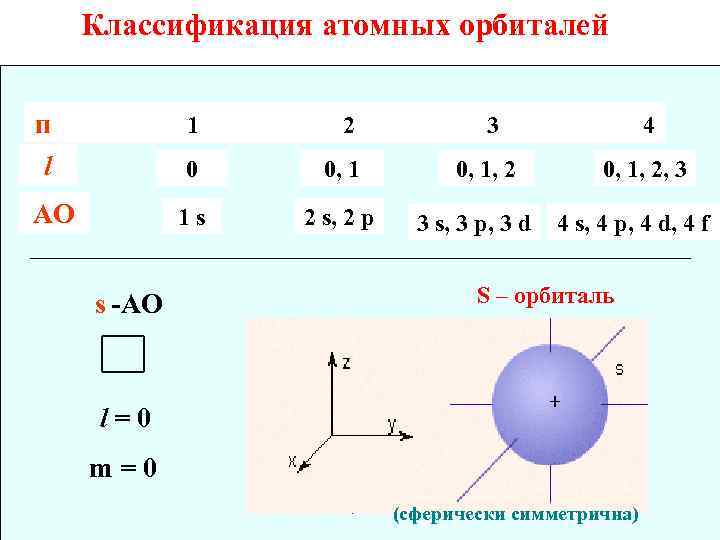 Классификация атомных орбиталей п 1 2 3 4 l 0 0, 1, 2, 3 АО 1 s 2 s, 2 p s -АО 3 s, 3 p, 3 d 4 s, 4 p, 4 d, 4 f S – орбиталь l=0 m=0 (сферически симметрична)
Классификация атомных орбиталей п 1 2 3 4 l 0 0, 1, 2, 3 АО 1 s 2 s, 2 p s -АО 3 s, 3 p, 3 d 4 s, 4 p, 4 d, 4 f S – орбиталь l=0 m=0 (сферически симметрична)
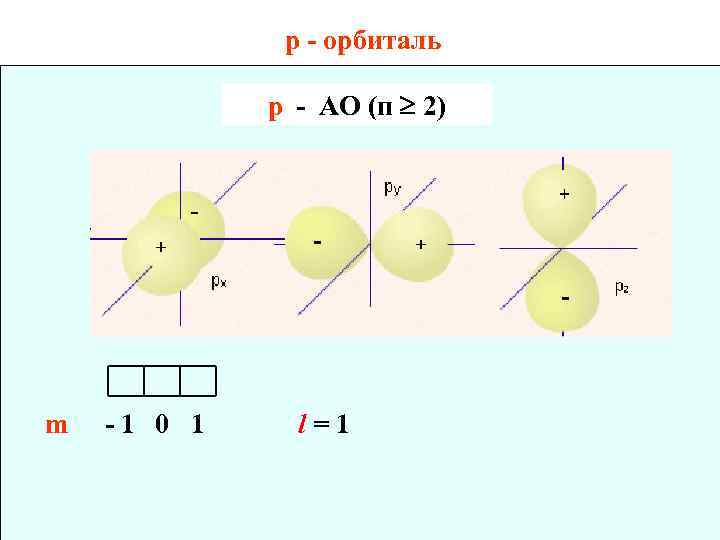 р - орбиталь p - АО (п 2) m -1 0 1 l=1
р - орбиталь p - АО (п 2) m -1 0 1 l=1
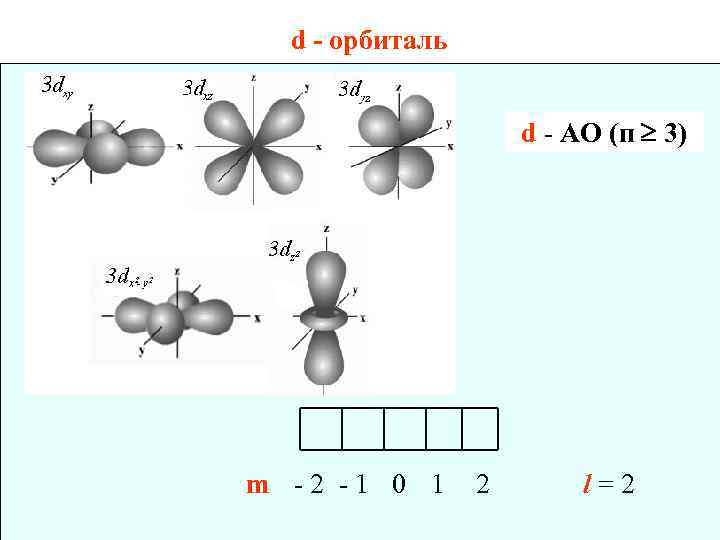 d - орбиталь d - АО (п 3) m -2 -1 0 1 2 l=2
d - орбиталь d - АО (п 3) m -2 -1 0 1 2 l=2
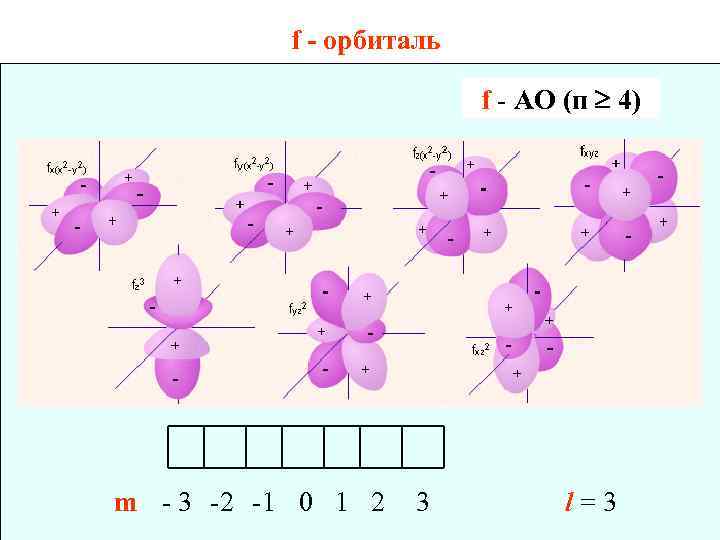 f - орбиталь f - АО (п 4) m - 3 -2 -1 0 1 2 3 l=3
f - орбиталь f - АО (п 4) m - 3 -2 -1 0 1 2 3 l=3
 Электронные уровни и подуровни Число подуровней на уровне Число АО на подуровне l m E 4 s 4 p 4 d 3 s 3 p 3 d 2 s 4 f 2 p Число АО на уровне 1 + 3 + 5+… = n 2 1 s
Электронные уровни и подуровни Число подуровней на уровне Число АО на подуровне l m E 4 s 4 p 4 d 3 s 3 p 3 d 2 s 4 f 2 p Число АО на уровне 1 + 3 + 5+… = n 2 1 s
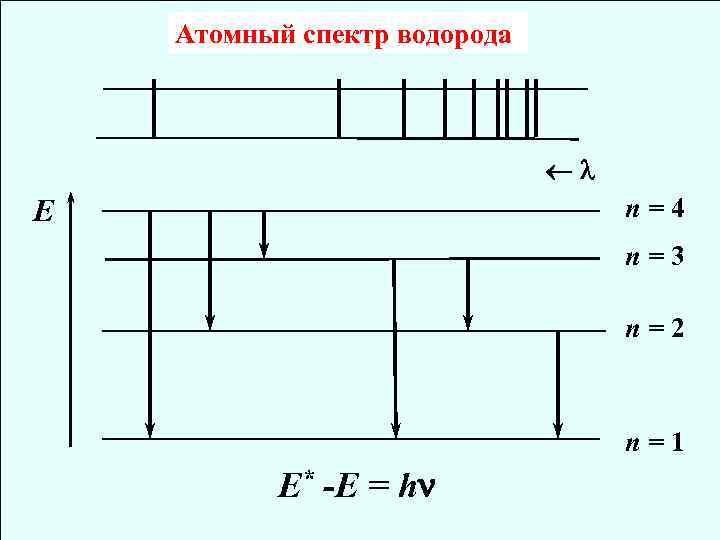 Атомный спектр водорода │ ││║║ Е n=4 n=3 n=2 n=1 Е* -E = h
Атомный спектр водорода │ ││║║ Е n=4 n=3 n=2 n=1 Е* -E = h


