lection_6_Yanukovich.ppt
- Количество слайдов: 29
 Лекция 6. Молекулярно-кинетическая теория газов 1. 2. 3. 4. 5. 6. Предмет молекулярной физики. Основное уравнение молекулярнокинетической теории. Уравнение Клайперона – Менделеева Законы поведения идеального газа. Распределение молекул идеального газа по скоростям. Распределение Больцмана.
Лекция 6. Молекулярно-кинетическая теория газов 1. 2. 3. 4. 5. 6. Предмет молекулярной физики. Основное уравнение молекулярнокинетической теории. Уравнение Клайперона – Менделеева Законы поведения идеального газа. Распределение молекул идеального газа по скоростям. Распределение Больцмана.
 1. ПРЕДМЕТ МОЛЕКУЛЯРНОЙ ФИЗИКИ n n Молекулярная физика – раздел физики, изучающий строение и свойства вещества, исходя из молекулярно-кинетических представлений. Они основаны на том, что все тела состоят из молекул, находящихся в непрерывном хаотическом движении. Термодинамика – раздел физики, изучающий общие свойства макроскопических систем, находящихся в состоянии термодинамического равновесия и процессы перехода между этими состояниями.
1. ПРЕДМЕТ МОЛЕКУЛЯРНОЙ ФИЗИКИ n n Молекулярная физика – раздел физики, изучающий строение и свойства вещества, исходя из молекулярно-кинетических представлений. Они основаны на том, что все тела состоят из молекул, находящихся в непрерывном хаотическом движении. Термодинамика – раздел физики, изучающий общие свойства макроскопических систем, находящихся в состоянии термодинамического равновесия и процессы перехода между этими состояниями.
 Термодинамические системы n n Термодинамика имеет дело с термодинамическими системами – совокупностью макроскопических тел, которые взаимодействуют и обмениваются энергией, как между собой, так и с другими телами. Состояние системы задаётся термодинамическими параметрами (параметрами состояния). Обычно в качестве параметров состояния используют: давление, удельный объём, температуру.
Термодинамические системы n n Термодинамика имеет дело с термодинамическими системами – совокупностью макроскопических тел, которые взаимодействуют и обмениваются энергией, как между собой, так и с другими телами. Состояние системы задаётся термодинамическими параметрами (параметрами состояния). Обычно в качестве параметров состояния используют: давление, удельный объём, температуру.
 Термодинамические параметры n n n Давление – физическая величина, характеризующая интенсивность нормальных к поверхности сил, с которыми одно тело действует на поверхность другого. Удельный объем представляет собой объем, занимаемый единицей массы вещества. Температура – физическая величина, характеризующая состояние термодинамического равновесия макроскопической системы.
Термодинамические параметры n n n Давление – физическая величина, характеризующая интенсивность нормальных к поверхности сил, с которыми одно тело действует на поверхность другого. Удельный объем представляет собой объем, занимаемый единицей массы вещества. Температура – физическая величина, характеризующая состояние термодинамического равновесия макроскопической системы.
 Температурная шкала n Термодинамическая температурная шкала определяется по реперной точке, в качестве которой взята тройная точка воды (температура, при которой лед, вода и насыщенный пар при давлении 609 Па находятся в термодинамическом равновесии). Температура этой точки 273, 16 К. Вторая – шкала Цельсия. В Международной практической шкале температура замерзания и кипения воды при давлении 1, 013 103 Па соответственно равна 0 и 100°С.
Температурная шкала n Термодинамическая температурная шкала определяется по реперной точке, в качестве которой взята тройная точка воды (температура, при которой лед, вода и насыщенный пар при давлении 609 Па находятся в термодинамическом равновесии). Температура этой точки 273, 16 К. Вторая – шкала Цельсия. В Международной практической шкале температура замерзания и кипения воды при давлении 1, 013 103 Па соответственно равна 0 и 100°С.
 Идеальный газ n n собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда; между молекулами газа отсутствуют силы взаимодействия; столкновения молекул газа между собой и со стенками сосуда абсолютно упругие Макроскопическая система находится в термодинамическом равновесии, если ее состояние с течением времени не меняется
Идеальный газ n n собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда; между молекулами газа отсутствуют силы взаимодействия; столкновения молекул газа между собой и со стенками сосуда абсолютно упругие Макроскопическая система находится в термодинамическом равновесии, если ее состояние с течением времени не меняется
 2. Основное уравнение молекулярнокинетической теории n n давление, оказываемое газом на стенки сосуда концентрация молекул масса молекулы среднеквадратическая скорость молекул газа
2. Основное уравнение молекулярнокинетической теории n n давление, оказываемое газом на стенки сосуда концентрация молекул масса молекулы среднеквадратическая скорость молекул газа
 Средняя квадратичная скорость n n число молекул газа в единице объема общее количество молекул газа, получим
Средняя квадратичная скорость n n число молекул газа в единице объема общее количество молекул газа, получим
 Связь давления и энергии n суммарная кинетическая энергия поступательного движения всех молекул газа
Связь давления и энергии n суммарная кинетическая энергия поступательного движения всех молекул газа
 Связь средней квадратичной скорости и макроскопических характеристик газа масса газа n молярная газовая постоянная =8, 31 Дж/(моль К) n
Связь средней квадратичной скорости и макроскопических характеристик газа масса газа n молярная газовая постоянная =8, 31 Дж/(моль К) n
 Связь средней квадратичной скорости и массы молекулы n n постоянная Авогадро = 6, 02 1023 моль-1 постоянная Больцмана =1, 38 10 -23 Дж/К
Связь средней квадратичной скорости и массы молекулы n n постоянная Авогадро = 6, 02 1023 моль-1 постоянная Больцмана =1, 38 10 -23 Дж/К
 Средняя кинетическая энергия поступательного движения всех молекул идеального газа. n n Из этого уравнения следует, что при условиях T=0, E 0=0, т. е. при 00 К прекращается поступательное движение молекул газа, а, следовательно, его давление равно нулю термодинамическая температура является мерой средней кинетической энергии поступательного движения молекул идеального газа
Средняя кинетическая энергия поступательного движения всех молекул идеального газа. n n Из этого уравнения следует, что при условиях T=0, E 0=0, т. е. при 00 К прекращается поступательное движение молекул газа, а, следовательно, его давление равно нулю термодинамическая температура является мерой средней кинетической энергии поступательного движения молекул идеального газа
 3. Уравнение Клайперона. Менделеева n n p. V=RT n уравнение состояния идеального газа Для одного моля любого газа уравнение Клапейрона– Менделеева
3. Уравнение Клайперона. Менделеева n n p. V=RT n уравнение состояния идеального газа Для одного моля любого газа уравнение Клапейрона– Менделеева
 Закон Авогадро n Если температура газа равна Tн = 273, 15 К (0 °С), а давление pн = 1 атм = 1, 013· 105 Па, то говорят, что газ находится при нормальных что газ находится условиях. Как следует из уравнения состояния идеального газа, один моль любого газа при нормальных условиях занимает один и тот же объем V 0, равный V 0 = 0, 0224 м 3/моль = 22, 4 дм 3/моль.
Закон Авогадро n Если температура газа равна Tн = 273, 15 К (0 °С), а давление pн = 1 атм = 1, 013· 105 Па, то говорят, что газ находится при нормальных что газ находится условиях. Как следует из уравнения состояния идеального газа, один моль любого газа при нормальных условиях занимает один и тот же объем V 0, равный V 0 = 0, 0224 м 3/моль = 22, 4 дм 3/моль.
 4. Уравнение состояния идеального газа. Изопроцессы n n n Газ может участвовать в различных тепловых процессах, при которых могут изменяться все параметры, описывающие его состояние (p, V и T). Если процесс протекает достаточно медленно, то в любой момент система близка к своему равновесному состоянию. Такие процессы называются квазистатическими. Квазистатические процессы могут быть изображены на диаграмме состояний (например, в координатах p, V) в виде некоторой траектории, каждая точка которой представляет равновесное состояние. Интерес представляют процессы, в которых один из параметров (p, V или T) остается неизменным. Такие процессы называются изопроцессами
4. Уравнение состояния идеального газа. Изопроцессы n n n Газ может участвовать в различных тепловых процессах, при которых могут изменяться все параметры, описывающие его состояние (p, V и T). Если процесс протекает достаточно медленно, то в любой момент система близка к своему равновесному состоянию. Такие процессы называются квазистатическими. Квазистатические процессы могут быть изображены на диаграмме состояний (например, в координатах p, V) в виде некоторой траектории, каждая точка которой представляет равновесное состояние. Интерес представляют процессы, в которых один из параметров (p, V или T) остается неизменным. Такие процессы называются изопроцессами
 Изотермический процесс (T = const) n Изотермическим процессом называют квазистатический процесс, протекающий при постоянной температуре T. Из уравнения состояния идеального газа следует, что при постоянной температуре T и неизменном количестве вещества ν в сосуде произведение давления p газа на его объем V должно оставаться постоянным: p. V = const.
Изотермический процесс (T = const) n Изотермическим процессом называют квазистатический процесс, протекающий при постоянной температуре T. Из уравнения состояния идеального газа следует, что при постоянной температуре T и неизменном количестве вещества ν в сосуде произведение давления p газа на его объем V должно оставаться постоянным: p. V = const.
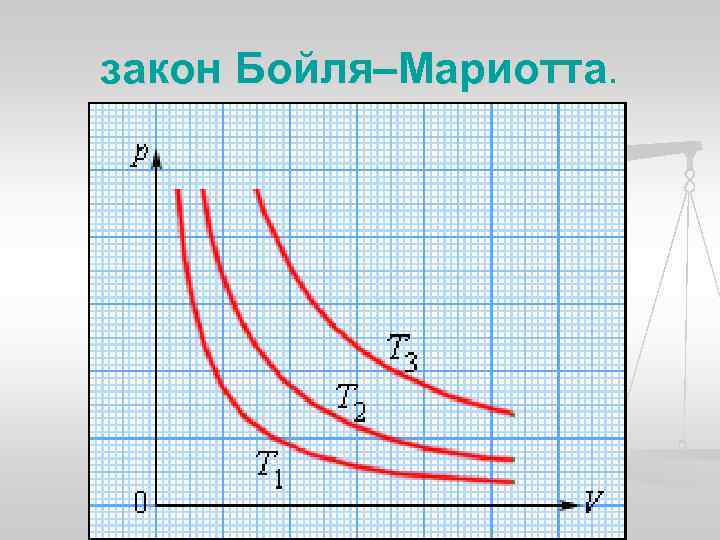 закон Бойля–Мариотта.
закон Бойля–Мариотта.
 Изохорный процесс (V = const) n n Изохорный процесс – это процесс квазистатического нагревания или охлаждения газа при постоянном объеме V и при условии, что количество вещества ν в сосуде остается неизменным. Как следует из уравнения состояния идеального газа, при этих условиях давление газа p изменяется прямо пропорционально его абсолютной температуре: p ~ T или
Изохорный процесс (V = const) n n Изохорный процесс – это процесс квазистатического нагревания или охлаждения газа при постоянном объеме V и при условии, что количество вещества ν в сосуде остается неизменным. Как следует из уравнения состояния идеального газа, при этих условиях давление газа p изменяется прямо пропорционально его абсолютной температуре: p ~ T или
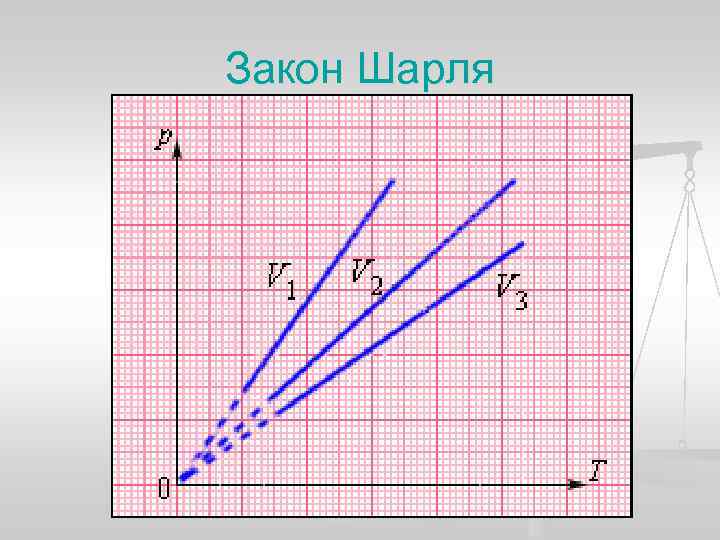 Закон Шарля
Закон Шарля
 Уравнение изохорного процесса n p 0 – давление газа при T = T 0 = 273, 15 К (т. е. при температуре 0 °С). Коэффициент α, равный (1/273, 15) К– 1, называют температурным коэффициентом давления
Уравнение изохорного процесса n p 0 – давление газа при T = T 0 = 273, 15 К (т. е. при температуре 0 °С). Коэффициент α, равный (1/273, 15) К– 1, называют температурным коэффициентом давления
 Изобарный процесс (p = const) n n n Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. Уравнение изобарного процесса для некоторого неизменного количества вещества ν имеет вид: V 0 – объем газа при температуре 0 °С. Коэффициент α равен (1/273, 15) К– 1. Его называют температурным коэффициентом объемного расширения газов.
Изобарный процесс (p = const) n n n Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. Уравнение изобарного процесса для некоторого неизменного количества вещества ν имеет вид: V 0 – объем газа при температуре 0 °С. Коэффициент α равен (1/273, 15) К– 1. Его называют температурным коэффициентом объемного расширения газов.
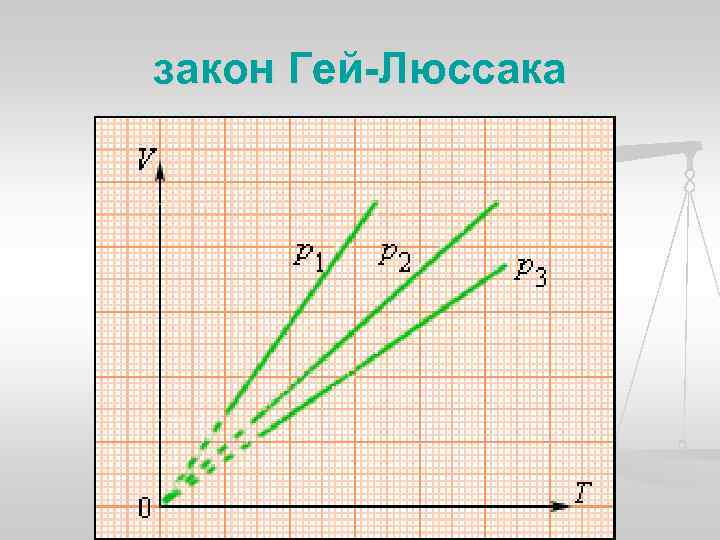 закон Гей-Люссака
закон Гей-Люссака
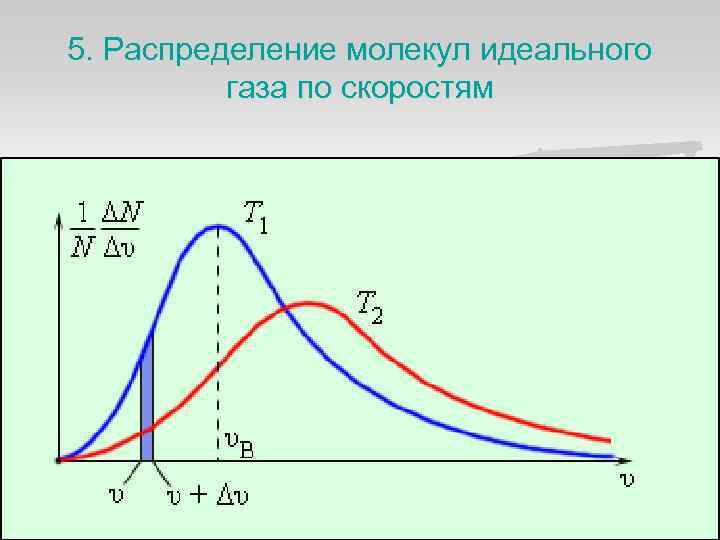 5. Распределение молекул идеального газа по скоростям
5. Распределение молекул идеального газа по скоростям
 функция распределения молекул по скоростям n Функция f(v) определяет относительное число молекул d. N(v)/N, скорости которых лежат в интервале от v до v+dv,
функция распределения молекул по скоростям n Функция f(v) определяет относительное число молекул d. N(v)/N, скорости которых лежат в интервале от v до v+dv,
 Наиболее вероятная и средняя скорость молекул газа
Наиболее вероятная и средняя скорость молекул газа
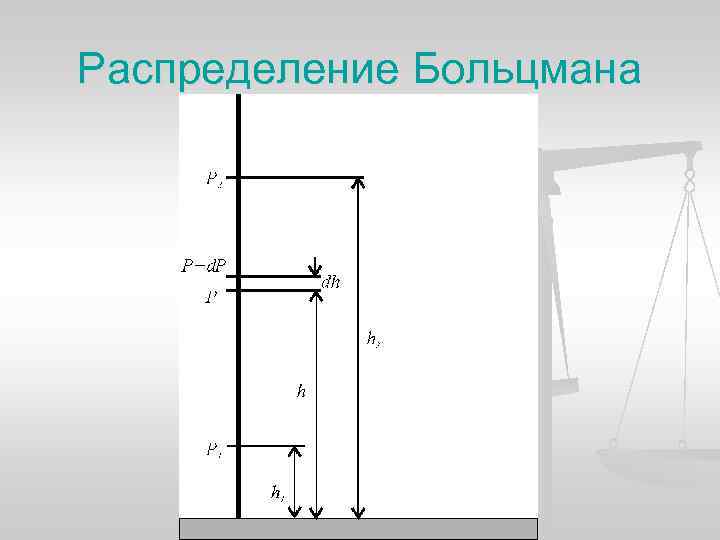 Распределение Больцмана
Распределение Больцмана
 Зависимость плотности от высоты n Плотность газа на высоте h
Зависимость плотности от высоты n Плотность газа на высоте h
 Барометрическая формула
Барометрическая формула
 Распределение Больцмана n n концентрация молекул на высоте h то же, на высоте h 0
Распределение Больцмана n n концентрация молекул на высоте h то же, на высоте h 0


