Механизм ХР.ppt
- Количество слайдов: 23
 Лекция 6 Механизм химической реакции. Катализ.
Лекция 6 Механизм химической реакции. Катализ.
 План лекции 1. Химическая термодинамика и ее структура 2. Системы, параметры, состояния, функции, процессы. 3. Постулаты термодинамики. Уравнения состояния. 4. Первое начало термодинамики 5. Второе начало термодинамики. Энтропия.
План лекции 1. Химическая термодинамика и ее структура 2. Системы, параметры, состояния, функции, процессы. 3. Постулаты термодинамики. Уравнения состояния. 4. Первое начало термодинамики 5. Второе начало термодинамики. Энтропия.
 Механизм реакции Это совокупность простых реакций, которые протекают в реакционной системе и реализуют стехиометрическое превращение исходных веществ в продукты. В зависимости от природы реагирующих веществ в реакциях могут принимать участие атомы, молекулы, радикалы, ионы Механизм реакции: 1. Простые 2. Ионные 3. Радикальные 4
Механизм реакции Это совокупность простых реакций, которые протекают в реакционной системе и реализуют стехиометрическое превращение исходных веществ в продукты. В зависимости от природы реагирующих веществ в реакциях могут принимать участие атомы, молекулы, радикалы, ионы Механизм реакции: 1. Простые 2. Ионные 3. Радикальные 4
 Простые реакции Протекают между молекулами Н 2(г) + I 2(г) = 2 HI(г) Реакции между валентнонасыщенными молекулами редки, т. к. для их протекания требуется большая энергия активации. 5
Простые реакции Протекают между молекулами Н 2(г) + I 2(г) = 2 HI(г) Реакции между валентнонасыщенными молекулами редки, т. к. для их протекания требуется большая энергия активации. 5
 Ионные реакции Реакции, в которых принимают участие заряженными частицы. Ионы образуются при растворении веществ, под действием электроразряда, нагревания, излучения достаточной энергии и др. 6
Ионные реакции Реакции, в которых принимают участие заряженными частицы. Ионы образуются при растворении веществ, под действием электроразряда, нагревания, излучения достаточной энергии и др. 6
 Радикальные реакции Реакции с промежуточным образованием радикалов и атомов. Свободные радикалы – валентнонасыщенные частицы, которые можно представить как осколки молекул ( • ОН, • NH 2), и свободные атомы. • Cl + H 2 = HCl + • H H 2 + • Cl = HCl + • Cl • H + • Cl = HCl Свободные радикалы еще более активны чем ионы. Свободные радикалы образуются в результате распада вещества при нагревании, освещении, под действием ядерных излучений, при электроразряде и т. д. Радикальные реакции обычно протекают по цепному механизму. 7
Радикальные реакции Реакции с промежуточным образованием радикалов и атомов. Свободные радикалы – валентнонасыщенные частицы, которые можно представить как осколки молекул ( • ОН, • NH 2), и свободные атомы. • Cl + H 2 = HCl + • H H 2 + • Cl = HCl + • Cl • H + • Cl = HCl Свободные радикалы еще более активны чем ионы. Свободные радикалы образуются в результате распада вещества при нагревании, освещении, под действием ядерных излучений, при электроразряде и т. д. Радикальные реакции обычно протекают по цепному механизму. 7
 Цепные реакции Один первичный активации приводит к превращению огромного числа исходных веществ. Примеры: 1) окисление органических соединений 2) полимеризация 3) термический и каталитический крекинг алканов 4) 5) 6) 7) Основные стадии: Зарождение цепи Продолжение и разветвление цепи Обрыв цепи 8
Цепные реакции Один первичный активации приводит к превращению огромного числа исходных веществ. Примеры: 1) окисление органических соединений 2) полимеризация 3) термический и каталитический крекинг алканов 4) 5) 6) 7) Основные стадии: Зарождение цепи Продолжение и разветвление цепи Обрыв цепи 8
 • • • • • 9
• • • • • 9
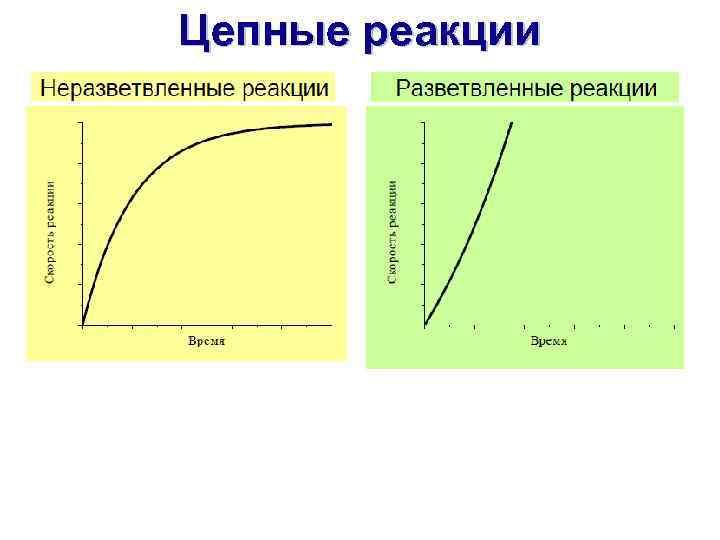 Цепные реакции 10
Цепные реакции 10
 Применение цепных реакций 1. Реакции полимеризации. Возникающие радикалы не генерируются, а образуют радикалы с большей молекулярной массой за счет их присоединения к мономерам. 2. Реакции сжигания топлива в двигателях внутреннего сгорания. Поэтому в топливо добавляют антидетонаторы. 3. Окисление органических соединений 4. Ядерные реакции 11
Применение цепных реакций 1. Реакции полимеризации. Возникающие радикалы не генерируются, а образуют радикалы с большей молекулярной массой за счет их присоединения к мономерам. 2. Реакции сжигания топлива в двигателях внутреннего сгорания. Поэтому в топливо добавляют антидетонаторы. 3. Окисление органических соединений 4. Ядерные реакции 11
 Физические методы стимулирования химических превращений На реакционную способность веществ существенное влияние оказывает свет, ионизирующие излучения, давление, механическое взаимодействие и др. 12
Физические методы стимулирования химических превращений На реакционную способность веществ существенное влияние оказывает свет, ионизирующие излучения, давление, механическое взаимодействие и др. 12
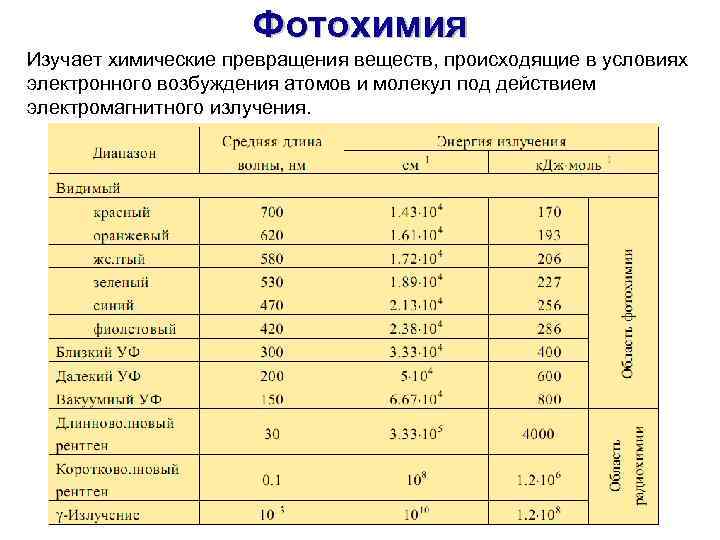 Фотохимия Изучает химические превращения веществ, происходящие в условиях электронного возбуждения атомов и молекул под действием электромагнитного излучения. 13
Фотохимия Изучает химические превращения веществ, происходящие в условиях электронного возбуждения атомов и молекул под действием электромагнитного излучения. 13
 Основные понятия фотохимии 14
Основные понятия фотохимии 14
 Законы фотохимии 15
Законы фотохимии 15
 Квантовый выход Важнейший параметр фотохимической реакции В зависимости от типа фотохимической реакции φ может сильно меняться, что связано с возможностью потери поглощенной энергии до фотопревращения. Если поглощенный фотон вызывает одно фотохимическое превращение, то φ = 1. При φ >> 1 фотореакция идет по цепному механизму: Н 2 + Cl 2 = 2 HСl φ = 105 16
Квантовый выход Важнейший параметр фотохимической реакции В зависимости от типа фотохимической реакции φ может сильно меняться, что связано с возможностью потери поглощенной энергии до фотопревращения. Если поглощенный фотон вызывает одно фотохимическое превращение, то φ = 1. При φ >> 1 фотореакция идет по цепному механизму: Н 2 + Cl 2 = 2 HСl φ = 105 16
 Типы фотохимических реакций 1. Фотолиз (фотодиссоциация) – приводит к разложению исходного вещества, поглотившего световую энергию: CH 3 – CH 3 → CO + C 2 H 6 ║ O 2. Фотосинтез а) неорганических соединений О 2 → О + О фотодиссоциация УФ О 2 +О → О 3 фотосинтез б) органических соединений 6 СО 2 +6 Н 2 О → С 6 Н 12 О 6 + 6 О 2 17
Типы фотохимических реакций 1. Фотолиз (фотодиссоциация) – приводит к разложению исходного вещества, поглотившего световую энергию: CH 3 – CH 3 → CO + C 2 H 6 ║ O 2. Фотосинтез а) неорганических соединений О 2 → О + О фотодиссоциация УФ О 2 +О → О 3 фотосинтез б) органических соединений 6 СО 2 +6 Н 2 О → С 6 Н 12 О 6 + 6 О 2 17
 Типы фотохимических реакций 3. Фотохромизм – явление обратимого изменения пространственного и электронного строения молекул под действием света, сопровождающееся изменением окраски вещества. Применение: изготовление линз с переменным светопропусканием, оконные стекла 18
Типы фотохимических реакций 3. Фотохромизм – явление обратимого изменения пространственного и электронного строения молекул под действием света, сопровождающееся изменением окраски вещества. Применение: изготовление линз с переменным светопропусканием, оконные стекла 18
 Отличия фотохимических реакций от темновых е 19
Отличия фотохимических реакций от темновых е 19
 Радиационная химия Изучает химические превращения веществ, происходящие под действием ионизирующих излучений (рентгеновские лучи, альфа-частицы, гамма-лучи, нейтроны и др. излучения большой энергии). Примеры: О 2 → О 3, алмаз → графит, Н 2 О → Н 2 +О 2 + Н 2 О 2 20
Радиационная химия Изучает химические превращения веществ, происходящие под действием ионизирующих излучений (рентгеновские лучи, альфа-частицы, гамма-лучи, нейтроны и др. излучения большой энергии). Примеры: О 2 → О 3, алмаз → графит, Н 2 О → Н 2 +О 2 + Н 2 О 2 20
 Механохимия Изучает химические превращения веществ, происходящие под действием механических сил (вальцевание, дробление, перетирание и др. ). Примеры: 1. Растирание порошка V 2 O 5 • P 2 O 5 • 4 H 2 O → 2 H 3 PO 4 + V 2 O 5 • H 2 O 2. Превращение графита в алмаз под действием сверхвысоких давлений (десятки тыс. атм. ) 3. Сырой каучук при сжатии ударной волной (например при детонации взрывчатых веществ) превращается в резину, аминокислоты – в белки. 4. Получение сплава вольфрама и марганца при прохождении ударной волны и сильном нагревании одновременно. Другим способом этот сплав не получить. 21
Механохимия Изучает химические превращения веществ, происходящие под действием механических сил (вальцевание, дробление, перетирание и др. ). Примеры: 1. Растирание порошка V 2 O 5 • P 2 O 5 • 4 H 2 O → 2 H 3 PO 4 + V 2 O 5 • H 2 O 2. Превращение графита в алмаз под действием сверхвысоких давлений (десятки тыс. атм. ) 3. Сырой каучук при сжатии ударной волной (например при детонации взрывчатых веществ) превращается в резину, аминокислоты – в белки. 4. Получение сплава вольфрама и марганца при прохождении ударной волны и сильном нагревании одновременно. Другим способом этот сплав не получить. 21
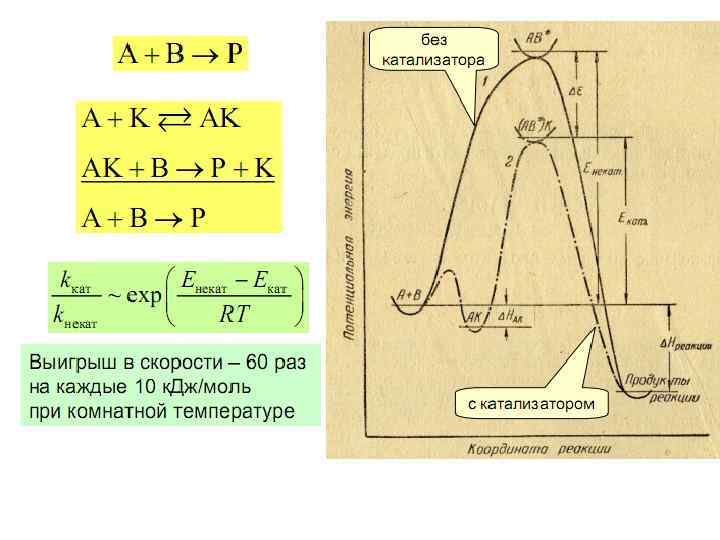
 Катализ 22
Катализ 22
 Классификация каталитических реакций 23
Классификация каталитических реакций 23
 24
24


