Презентация Комплексн соед Лекц 6.ppt
- Количество слайдов: 28

ЛЕКЦИЯ 6 КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
![СПОСОБЫ ПОЛУЧЕНИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ Аg. Cl + 2 NH 4 OH → [Аg(NH 3)2]Cl СПОСОБЫ ПОЛУЧЕНИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ Аg. Cl + 2 NH 4 OH → [Аg(NH 3)2]Cl](https://present5.com/presentation/3/33918382_133375653.pdf-img/33918382_133375653.pdf-2.jpg)
СПОСОБЫ ПОЛУЧЕНИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ Аg. Cl + 2 NH 4 OH → [Аg(NH 3)2]Cl +2 H 2 O белый бесцветный раствор Cu(OH)2↓ + 4 NH 4 OH → [Cu(NH 3)4](OH)2 + + 4 H 2 O раствор синего цвета
![Координационная теория Вернера (1893) [MLn]Xm [Fe+3(CN)6] 3← заряд ЛИГАНД (L) ЦЕНТРАЛЬНЫЙ ИОН (М) внутренней Координационная теория Вернера (1893) [MLn]Xm [Fe+3(CN)6] 3← заряд ЛИГАНД (L) ЦЕНТРАЛЬНЫЙ ИОН (М) внутренней](https://present5.com/presentation/3/33918382_133375653.pdf-img/33918382_133375653.pdf-3.jpg)
Координационная теория Вернера (1893) [MLn]Xm [Fe+3(CN)6] 3← заряд ЛИГАНД (L) ЦЕНТРАЛЬНЫЙ ИОН (М) внутренней сферы КООРДИНАЦИОН НОЕ ЧИСЛО (n)
![ПРИМЕРЫ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ АНИОННОГО И КАТИОННОГО ТИПОВ К 3+1[Fe+3(CN)6] 3 внешняя сфера K 2[Cu. ПРИМЕРЫ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ АНИОННОГО И КАТИОННОГО ТИПОВ К 3+1[Fe+3(CN)6] 3 внешняя сфера K 2[Cu.](https://present5.com/presentation/3/33918382_133375653.pdf-img/33918382_133375653.pdf-4.jpg)
ПРИМЕРЫ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ АНИОННОГО И КАТИОННОГО ТИПОВ К 3+1[Fe+3(CN)6] 3 внешняя сфера K 2[Cu. Br 4] внешняя сфера
![[Cu+2(NH 3)4]SO 4 ВНЕШНЯЯ СФЕРА [Fe+3(NH 3)6]Cl 3 ВНЕШНЯЯ СФЕРА [Cu+2(NH 3)4]SO 4 ВНЕШНЯЯ СФЕРА [Fe+3(NH 3)6]Cl 3 ВНЕШНЯЯ СФЕРА](https://present5.com/presentation/3/33918382_133375653.pdf-img/33918382_133375653.pdf-5.jpg)
[Cu+2(NH 3)4]SO 4 ВНЕШНЯЯ СФЕРА [Fe+3(NH 3)6]Cl 3 ВНЕШНЯЯ СФЕРА

ПРИМЕРЫ НЕЙТРАЛЬНЫХ КОМПЛЕКСОВ +3(OH) [Co +2(H [Cu (NH 3)3 3 2 O)2 Cl 2 0 ]
![НАЗВАНИЕ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ [Cu(NH 3)4]Cl 2 –хлорид тетрааминмеди (II) K 3[Fe(CN)6] – гексацианоферрат (III) НАЗВАНИЕ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ [Cu(NH 3)4]Cl 2 –хлорид тетрааминмеди (II) K 3[Fe(CN)6] – гексацианоферрат (III)](https://present5.com/presentation/3/33918382_133375653.pdf-img/33918382_133375653.pdf-7.jpg)
НАЗВАНИЕ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ [Cu(NH 3)4]Cl 2 –хлорид тетрааминмеди (II) K 3[Fe(CN)6] – гексацианоферрат (III) калия [Pt(NH 3)2 Br 4] тетрабромодиамин платина (IV)
![СТРОЕНИЕ КОМПЛЕКСА [Cu(NH 3)2]Cl Cu 0: 1 S 22 p 63 S 23 p СТРОЕНИЕ КОМПЛЕКСА [Cu(NH 3)2]Cl Cu 0: 1 S 22 p 63 S 23 p](https://present5.com/presentation/3/33918382_133375653.pdf-img/33918382_133375653.pdf-8.jpg)
СТРОЕНИЕ КОМПЛЕКСА [Cu(NH 3)2]Cl Cu 0: 1 S 22 p 63 S 23 p 63 d 10 4 S 1 +29 Cu+1: 1 S 22 p 63 S 23 p 63 d 10 4 S 0 4 p 4 s 3 d ●●● ●● NH 3 Sp гибр
![ПРИМЕРЫ КОМПЛЕКСОВ, ИМЕЮЩИХ sp 3 - ГИБРИДИЗАЦИЮ [Cu 2+(NH 3)4]2+ Cu+2: 1 S 22 ПРИМЕРЫ КОМПЛЕКСОВ, ИМЕЮЩИХ sp 3 - ГИБРИДИЗАЦИЮ [Cu 2+(NH 3)4]2+ Cu+2: 1 S 22](https://present5.com/presentation/3/33918382_133375653.pdf-img/33918382_133375653.pdf-9.jpg)
ПРИМЕРЫ КОМПЛЕКСОВ, ИМЕЮЩИХ sp 3 - ГИБРИДИЗАЦИЮ [Cu 2+(NH 3)4]2+ Cu+2: 1 S 22 p 63 S 23 p 63 d 9 4 S 0 АКЦЕПТОР 4 p 4 S 3 d ●● ●● NH 3 Sp 3 гибр ДОНОРЫ

ПОЛЯИЗУЮЩЕЕ ДЕЙСТВИЕ ЛИГАНДОВ УБЫВАЕТ В СЛЕДУЮЩЕЙ ПОСЛЕДОВАТЕЛЬНОСТИ (СПЕКТРОХИМИЧЕСКИЙ РЯД) СО >CN >NH 3 >SCN >H 2 O >OH >F >Cl >Br >J СИЛЬНОЕ ПОЛЕ СРЕДНЕЕ ПОЛЕ СЛАБОЕ ПОЛЕ
![ПРИМЕР СОЕДИНЕНИЯ, ИМЕЮЩЕГО sp 3 d 2 ГИБРИДИЗАЦИЮ [Fe+2 F 6 ]4 Fe 0: ПРИМЕР СОЕДИНЕНИЯ, ИМЕЮЩЕГО sp 3 d 2 ГИБРИДИЗАЦИЮ [Fe+2 F 6 ]4 Fe 0:](https://present5.com/presentation/3/33918382_133375653.pdf-img/33918382_133375653.pdf-11.jpg)
ПРИМЕР СОЕДИНЕНИЯ, ИМЕЮЩЕГО sp 3 d 2 ГИБРИДИЗАЦИЮ [Fe+2 F 6 ]4 Fe 0: 1 S 2 2 p 6 3 S 2 3 p 6 3 d 6 4 s 2 Fe+2: 1 S 2 2 p 6 3 S 2 3 p 6 3 d 6 4 S 0 АКЦЕПТОР 4 d 4 p 4 S 3 d ●●● ●● F F F ДОНОРЫ
![ПРИМЕР СОЕДИНЕНИЯ, ИМЕЮЩЕГО d 2 sp 3 ГИБРИДИЗАЦИЮ [Fe+2(CN)6]4 Fe+2: 1 S 2 2 ПРИМЕР СОЕДИНЕНИЯ, ИМЕЮЩЕГО d 2 sp 3 ГИБРИДИЗАЦИЮ [Fe+2(CN)6]4 Fe+2: 1 S 2 2](https://present5.com/presentation/3/33918382_133375653.pdf-img/33918382_133375653.pdf-12.jpg)
ПРИМЕР СОЕДИНЕНИЯ, ИМЕЮЩЕГО d 2 sp 3 ГИБРИДИЗАЦИЮ [Fe+2(CN)6]4 Fe+2: 1 S 2 2 p 6 3 S 2 3 p 6 3 d 6 4 S 0 АКЦЕПТОР 3 d ●●● 4 S ●● 4 p ●● ●● ●● 4 d ●● ●● CN CN CN ДОНОРЫ
![УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ [Ag(NH 3)2]Cl → [Ag(NH 3)2]+ + Cl [Ag(NH 3)2]+ ↔ Ag+ УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ [Ag(NH 3)2]Cl → [Ag(NH 3)2]+ + Cl [Ag(NH 3)2]+ ↔ Ag+](https://present5.com/presentation/3/33918382_133375653.pdf-img/33918382_133375653.pdf-13.jpg)
УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ [Ag(NH 3)2]Cl → [Ag(NH 3)2]+ + Cl [Ag(NH 3)2]+ ↔ Ag+ + 2 NH 3
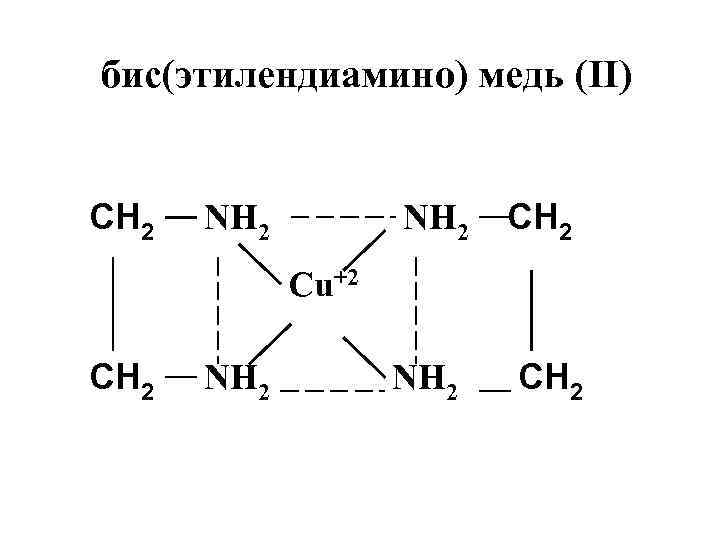
бис(этилендиамино) медь (II) СН 2 NH 2 СН 2 Cu+2 СН 2 NH 2
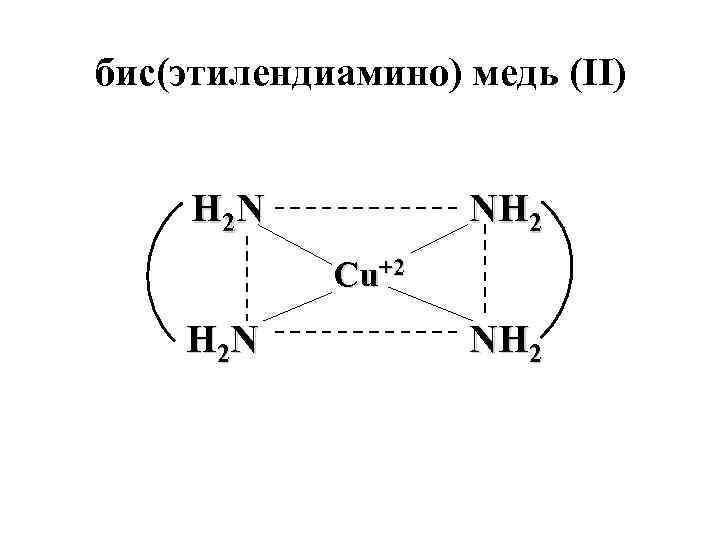
бис(этилендиамино) медь (II) H 2 N NH 2 Cu+2 H 2 N NH 2
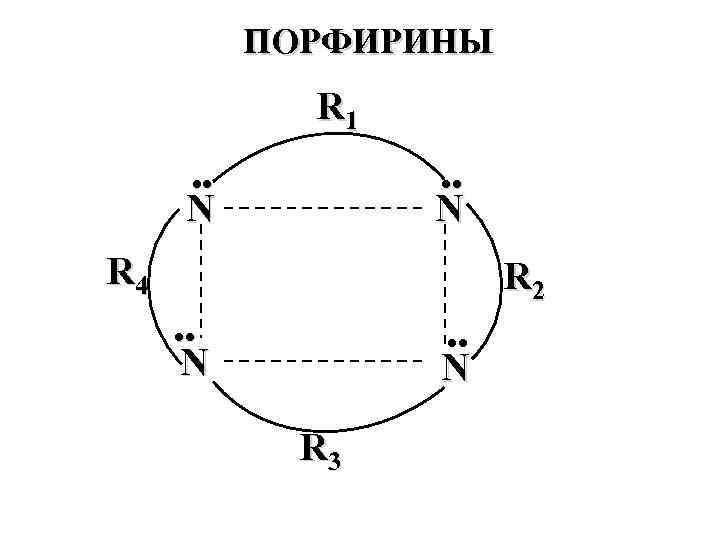
ПОРФИРИНЫ R 1 ●● ●● N N R 4 R 2 ●● ●● N N R 3
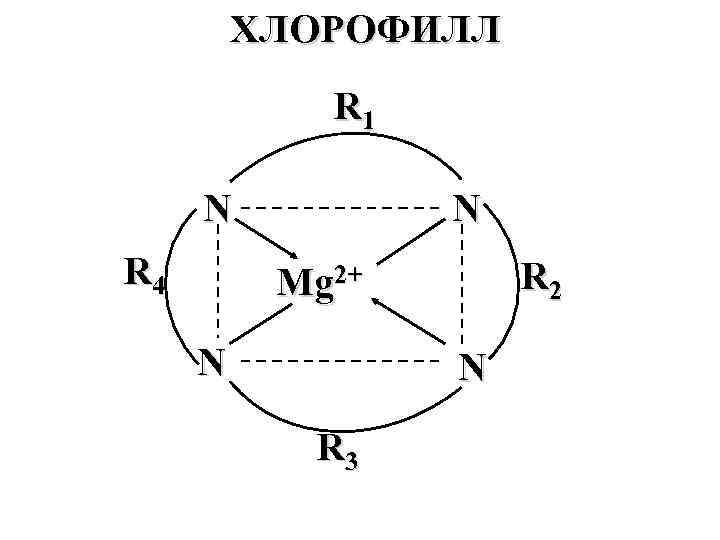
ХЛОРОФИЛЛ R 1 N R 4 N R 2 Мg 2+ N N R 3
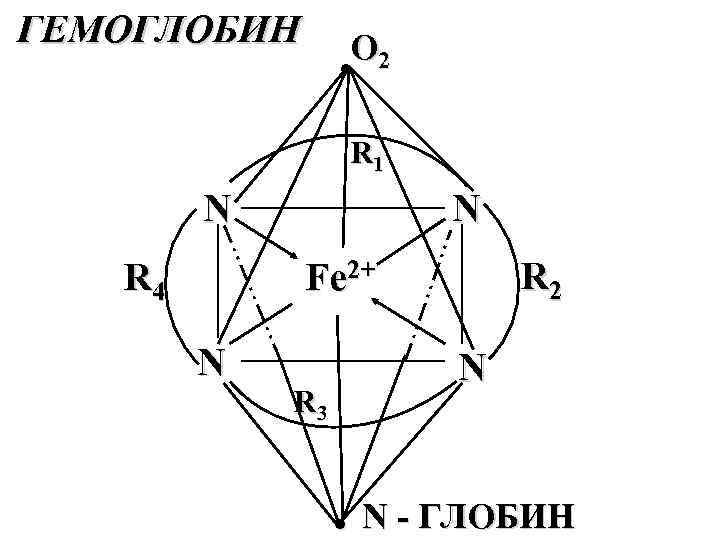
ГЕМОГЛОБИН O 2 ● R 1 N R 4 N R 2 Fe 2+ N N R 3 ● N ГЛОБИН
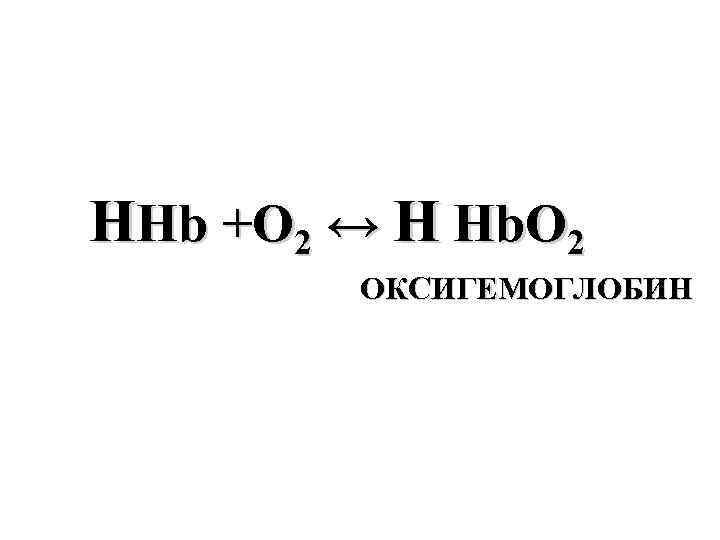
HHb +O 2 ↔ H Hb. O 2 ОКСИГЕМОГЛОБИН
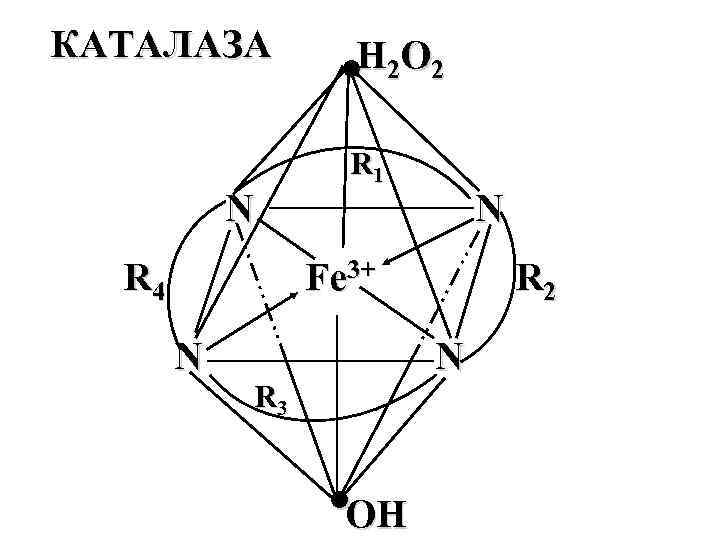
КАТАЛАЗА N R 4 ●Н 2 O 2 R 1 N Fe 3+ N R 2 N R 3 ●ОН
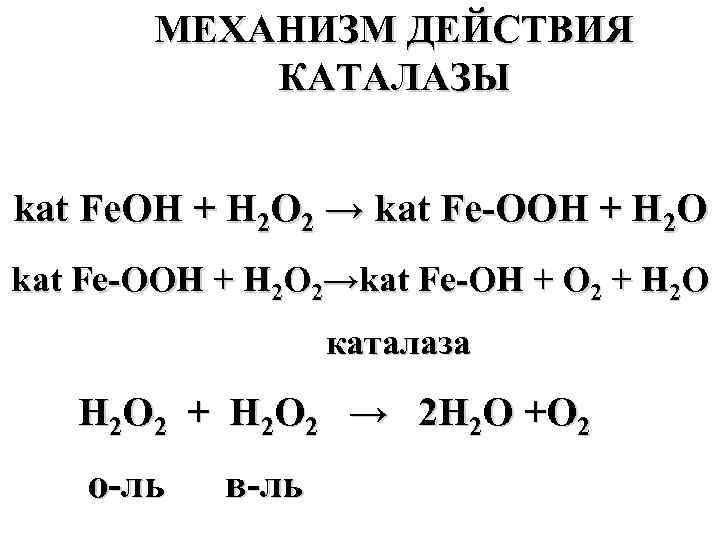
МЕХАНИЗМ ДЕЙСТВИЯ КАТАЛАЗЫ kat Fe. OH + H 2 O 2 → kat Fe OOH + H 2 O 2→kat Fe OH + O 2 + H 2 O каталаза H 2 O 2 + H 2 O 2 → 2 H 2 O +O 2 о ль в ль
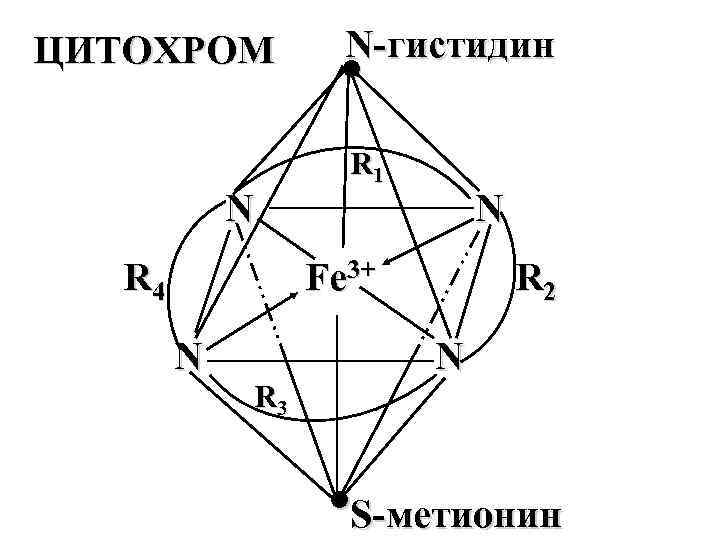
ЦИТОХРОМ N R 4 N гистидин ● R 1 N Fe 3+ N R 3 R 2 N ●S метионин
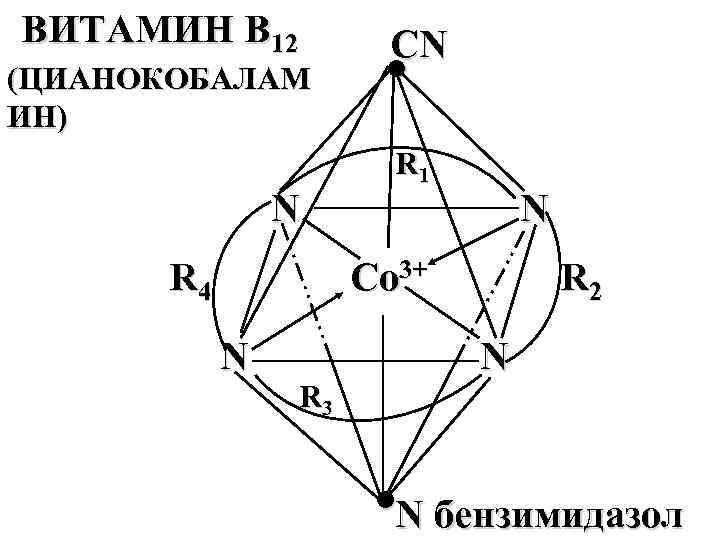
ВИТАМИН В 12 (ЦИАНОКОБАЛАМ ИН) N R 4 СN ● R 1 N Со 3+ N R 3 R 2 N ●N бензимидазол
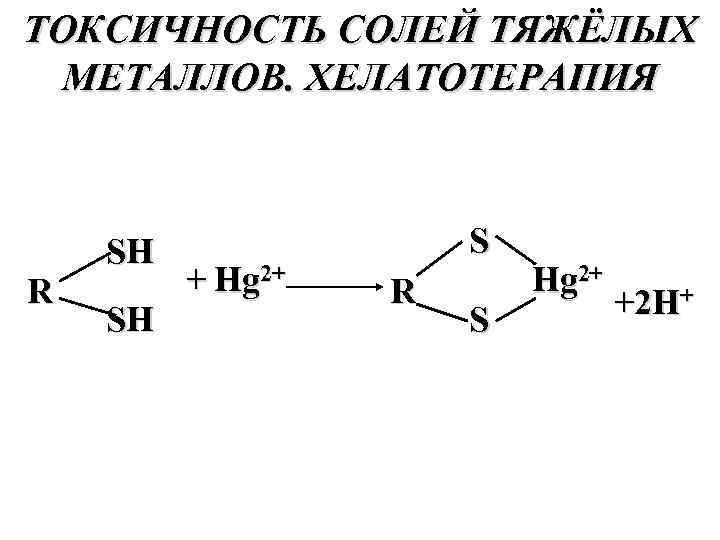
ТОКСИЧНОСТЬ СОЛЕЙ ТЯЖЁЛЫХ МЕТАЛЛОВ. ХЕЛАТОТЕРАПИЯ R SH SH + Hg 2+ S R S Hg 2+ +2 H+
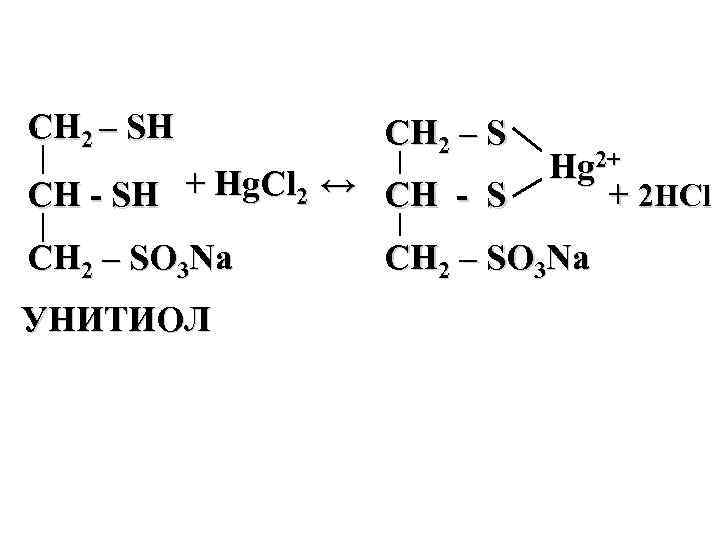
CH 2 – SH CH 2 – S CH SH + Hg. Cl 2 ↔ CH S CH 2 – SO 3 Na УНИТИОЛ Hg 2+ + 2 HCl CH 2 – SO 3 Na
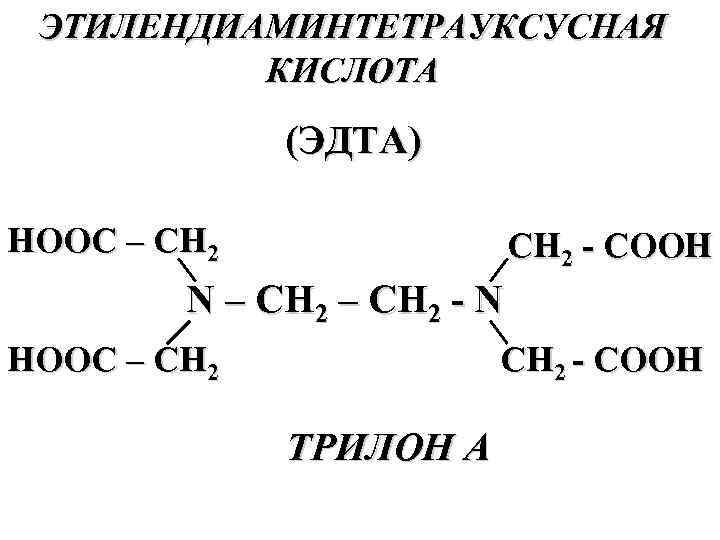
ЭТИЛЕНДИАМИНТЕТРАУКСУСНАЯ КИСЛОТА (ЭДТА) HOOC – CH 2 COOH N – CH 2 N HOOC – CH 2 COOH ТРИЛОН А
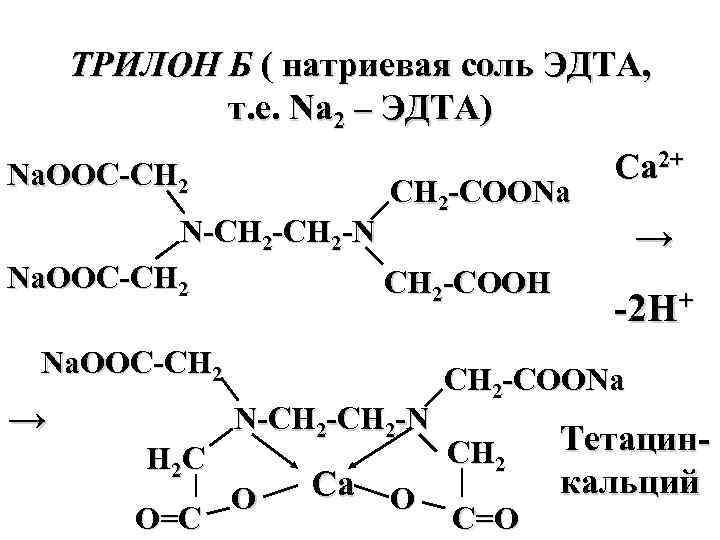
ТРИЛОН Б ( натриевая соль ЭДТА, т. е. Na 2 – ЭДТА) Na. OOC CH 2 N Na. OOC CH 2 COONa CH 2 COOH Na. OOC CH 2 → H 2 C O=C N CH 2 N O Ca 2+ → 2 H+ CH 2 COONa CH 2 C=O Тетацин кальций
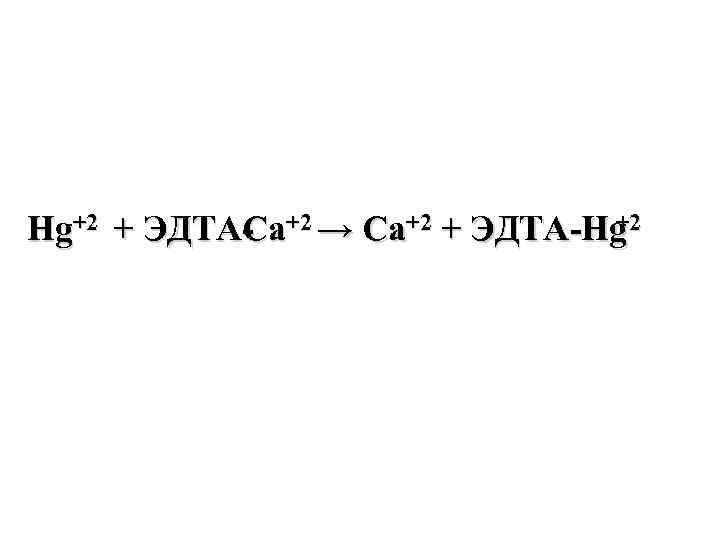
+2 Hg+2 + ЭДТА a+2 → Ca+2 + ЭДТА Hg С
Презентация Комплексн соед Лекц 6.ppt