ХИМИЯ лек.6 коллоидные.ppt
- Количество слайдов: 39
 Лекция 6 КОЛЛОИДНЫЕ СИСТЕМЫ
Лекция 6 КОЛЛОИДНЫЕ СИСТЕМЫ
 Дисперсные системы – гетерогенные системы из двух или большего числа фаз с сильно развитой поверхностью раздела между ними. Дисперсные системы состоят как минимум из двух компонентов: ¡ дисперсионной среды, которая играет роль растворителя и, следовательно, является непрерывной фазой; ¡ дисперсной фазы, играющей роль растворённого вещества. Коллоидные системы относятся к дисперсным системам – системам, где одно вещество в виде частиц различной величины распределено в другом.
Дисперсные системы – гетерогенные системы из двух или большего числа фаз с сильно развитой поверхностью раздела между ними. Дисперсные системы состоят как минимум из двух компонентов: ¡ дисперсионной среды, которая играет роль растворителя и, следовательно, является непрерывной фазой; ¡ дисперсной фазы, играющей роль растворённого вещества. Коллоидные системы относятся к дисперсным системам – системам, где одно вещество в виде частиц различной величины распределено в другом.
 Коллоидные системы − тонкодисперсные системы, в которых частицы имеют размеры от 1 мкм до 1 нм при условии сохранения гетерогенности и имеют сильно развитую удельную поверхность. Для объектов коллоидной химии характерны два общих признака: гетерогенность и дисперсность. Дисперсность является чисто количественным параметром, указывающим на степень раздробленности, размер межфазной поверхности; гетерогенность же указывает на качественную характеристику объектов.
Коллоидные системы − тонкодисперсные системы, в которых частицы имеют размеры от 1 мкм до 1 нм при условии сохранения гетерогенности и имеют сильно развитую удельную поверхность. Для объектов коллоидной химии характерны два общих признака: гетерогенность и дисперсность. Дисперсность является чисто количественным параметром, указывающим на степень раздробленности, размер межфазной поверхности; гетерогенность же указывает на качественную характеристику объектов.
 Термин «коллоиды» был введен в 1861 г. Т. Грэмом. ¡ Коллоидами Грэм назвал вещества, которые образуют водные растворы с клееподобными свойствами и не проходят через полупроницаемые перегородки – мембраны. По гречески колла означает клей. ¡
Термин «коллоиды» был введен в 1861 г. Т. Грэмом. ¡ Коллоидами Грэм назвал вещества, которые образуют водные растворы с клееподобными свойствами и не проходят через полупроницаемые перегородки – мембраны. По гречески колла означает клей. ¡
 ¡ ¡ ¡ Т. Грем также применил термины «золь» для коллоидных растворов и «гель» – для студнеобразных коллоидных систем. Золь – высокодисперсная коллоидная система с жидкой дисперсионной средой и изолированными друг от друга коллоидными частицами. Гель – коллоидно-дисперсная система с соприкасающимися (агрессивными) коллоидными частицами. Мицелла − частицы дисперсной фазы золя вместе с окружающей их сольватной оболочкой из молекул дисперсионной фазы. Студни (гель) − системы «полимер – растворитель» , характеризующиеся большими обратимыми деформациями практическом отсутствии вязкого течения.
¡ ¡ ¡ Т. Грем также применил термины «золь» для коллоидных растворов и «гель» – для студнеобразных коллоидных систем. Золь – высокодисперсная коллоидная система с жидкой дисперсионной средой и изолированными друг от друга коллоидными частицами. Гель – коллоидно-дисперсная система с соприкасающимися (агрессивными) коллоидными частицами. Мицелла − частицы дисперсной фазы золя вместе с окружающей их сольватной оболочкой из молекул дисперсионной фазы. Студни (гель) − системы «полимер – растворитель» , характеризующиеся большими обратимыми деформациями практическом отсутствии вязкого течения.
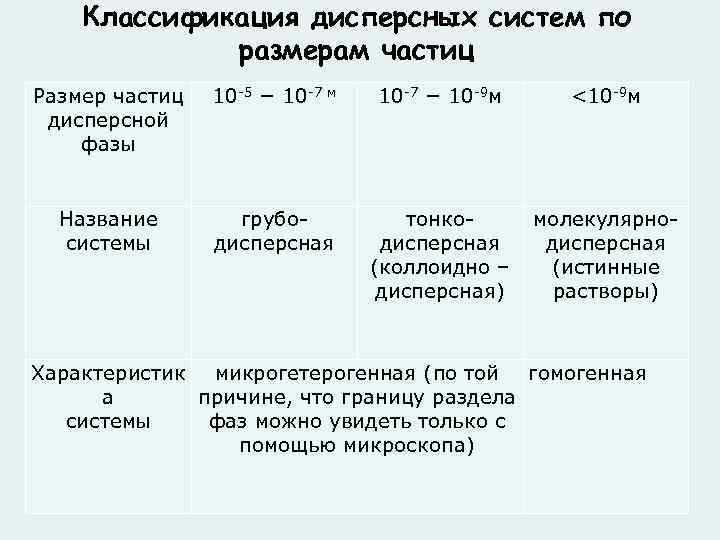 Классификация дисперсных систем по размерам частиц Размер частиц дисперсной фазы 10 -5 − 10 -7 м Название системы грубодисперсная 10 -7 − 10 -9 м <10 -9 м тонкомолекулярно- дисперсная (коллоидно – (истинные дисперсная) растворы) Характеристик микрогетерогенная (по той гомогенная а причине, что границу раздела системы фаз можно увидеть только с помощью микроскопа)
Классификация дисперсных систем по размерам частиц Размер частиц дисперсной фазы 10 -5 − 10 -7 м Название системы грубодисперсная 10 -7 − 10 -9 м <10 -9 м тонкомолекулярно- дисперсная (коллоидно – (истинные дисперсная) растворы) Характеристик микрогетерогенная (по той гомогенная а причине, что границу раздела системы фаз можно увидеть только с помощью микроскопа)
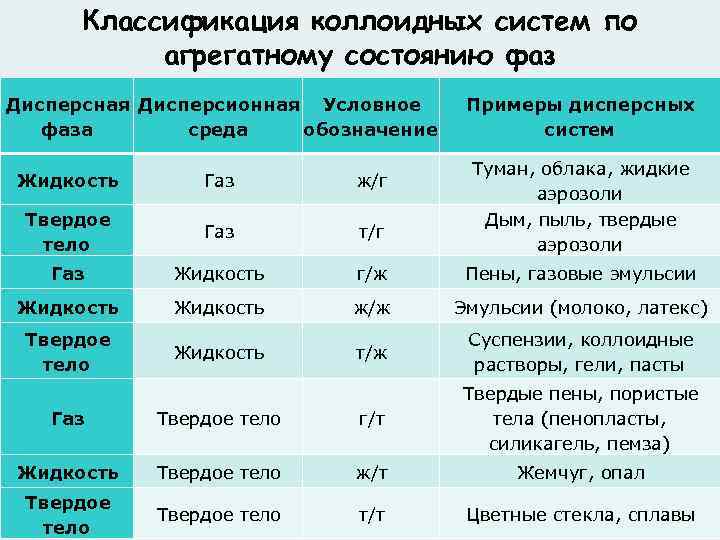 Классификация коллоидных систем по агрегатному состоянию фаз Дисперсная Дисперсионная Условное фаза среда обозначение Примеры дисперсных систем Туман, облака, жидкие аэрозоли Дым, пыль, твердые аэрозоли Жидкость Газ ж/г Твердое тело Газ т/г Газ Жидкость г/ж Пены, газовые эмульсии Жидкость ж/ж Эмульсии (молоко, латекс) Твердое тело Жидкость т/ж Суспензии, коллоидные растворы, гели, пасты Газ Твердое тело г/т Твердые пены, пористые тела (пенопласты, силикагель, пемза) Жидкость Твердое тело ж/т Жемчуг, опал Твердое тело т/т Цветные стекла, сплавы
Классификация коллоидных систем по агрегатному состоянию фаз Дисперсная Дисперсионная Условное фаза среда обозначение Примеры дисперсных систем Туман, облака, жидкие аэрозоли Дым, пыль, твердые аэрозоли Жидкость Газ ж/г Твердое тело Газ т/г Газ Жидкость г/ж Пены, газовые эмульсии Жидкость ж/ж Эмульсии (молоко, латекс) Твердое тело Жидкость т/ж Суспензии, коллоидные растворы, гели, пасты Газ Твердое тело г/т Твердые пены, пористые тела (пенопласты, силикагель, пемза) Жидкость Твердое тело ж/т Жемчуг, опал Твердое тело т/т Цветные стекла, сплавы
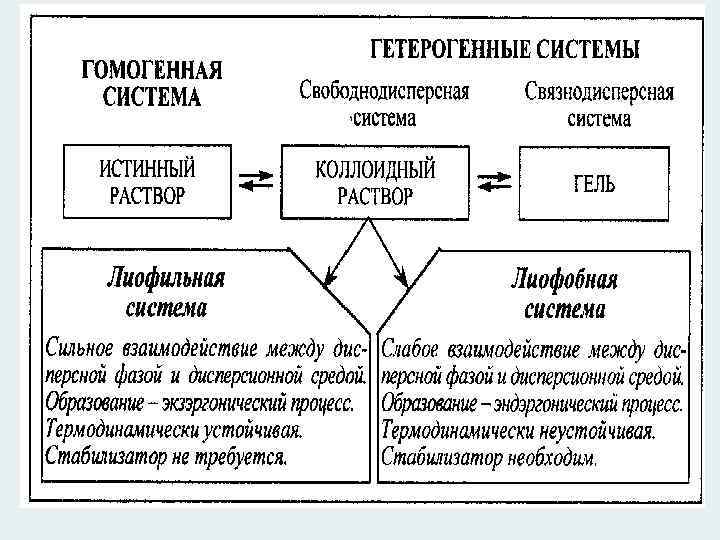
 По характеру взаимодействия дисперсной фазы с дисперсионной средой дисперсные системы подразделяются: Лиофобные: коллоидные растворы со стабилизаторами (золи), суспензии, эмульсии, пены, аэрозоли Лиофильные: коллоидные растворы ПАВ (поверхностноактивных веществ) и ВМС (высокомолекулярных соединений) слабое взаимодействие между ДФ и ДС сильное взаимодействие между ДФ и ДС образуются за счет затраты энергии извне образуются самопроизвольно эндергонический процесс экзергонический процесс термодинамически неустойчивы термодинамически устойчивы необходим стабилизатор не требуется
По характеру взаимодействия дисперсной фазы с дисперсионной средой дисперсные системы подразделяются: Лиофобные: коллоидные растворы со стабилизаторами (золи), суспензии, эмульсии, пены, аэрозоли Лиофильные: коллоидные растворы ПАВ (поверхностноактивных веществ) и ВМС (высокомолекулярных соединений) слабое взаимодействие между ДФ и ДС сильное взаимодействие между ДФ и ДС образуются за счет затраты энергии извне образуются самопроизвольно эндергонический процесс экзергонический процесс термодинамически неустойчивы термодинамически устойчивы необходим стабилизатор не требуется
 При протекании химических реакций в живом организме самопроизвольно идут те процессы, в которых изменение свободной энергии будет отрицательным. Такие процессы называются экзергоническими. ¡ Процессы, для которых изменение свободной энергии является величиной положительной, называются эндергоническими. ¡
При протекании химических реакций в живом организме самопроизвольно идут те процессы, в которых изменение свободной энергии будет отрицательным. Такие процессы называются экзергоническими. ¡ Процессы, для которых изменение свободной энергии является величиной положительной, называются эндергоническими. ¡
 В коллоидных системах поверхность раздела фаз – это не просто граница, не имеющая толщины. На границе раздела фаз формируется поверхностный слой толщиной в один или несколько молекулярных размеров. ¡ Состояние вещества в поверхностных слоях – это коллоидное состояние вещества. ¡
В коллоидных системах поверхность раздела фаз – это не просто граница, не имеющая толщины. На границе раздела фаз формируется поверхностный слой толщиной в один или несколько молекулярных размеров. ¡ Состояние вещества в поверхностных слоях – это коллоидное состояние вещества. ¡
 ЛИОФОБНЫЕ КОЛЛОИДНЫЕ РАСТВОРЫ - ЗОЛИ Получение золей А. Дисперсионный метод ¡ ¡ Диспергация гетерогенных систем осуществляется механическим путем в коллоидных мельницах, электрическим распылением в вольтовой дуге или с помощью ультразвука. Диспергационные методы основаны на измельчении (диспергировании) грубых частиц и распределении их в объеме дисперсионной среды.
ЛИОФОБНЫЕ КОЛЛОИДНЫЕ РАСТВОРЫ - ЗОЛИ Получение золей А. Дисперсионный метод ¡ ¡ Диспергация гетерогенных систем осуществляется механическим путем в коллоидных мельницах, электрическим распылением в вольтовой дуге или с помощью ультразвука. Диспергационные методы основаны на измельчении (диспергировании) грубых частиц и распределении их в объеме дисперсионной среды.
 Дисперсионный метод а/ Механические методы - дроблением, измельчением, истиранием б/ Ультразвуковой метод - под действием сжатий и расширений системы, но механизм еще мало изучен. в/ Метод пептизации. Пептизацией называют переход свежеприготовленного осадка в раствор под действием пептизаторов (Fe. Cl 3), образовавшихся при коагуляции осадков, частицы которых имеют коллоидный размер. Пептизация бывает двух видов: ¡ непосредственная; ¡ посредственная.
Дисперсионный метод а/ Механические методы - дроблением, измельчением, истиранием б/ Ультразвуковой метод - под действием сжатий и расширений системы, но механизм еще мало изучен. в/ Метод пептизации. Пептизацией называют переход свежеприготовленного осадка в раствор под действием пептизаторов (Fe. Cl 3), образовавшихся при коагуляции осадков, частицы которых имеют коллоидный размер. Пептизация бывает двух видов: ¡ непосредственная; ¡ посредственная.
 Пептизацией ¡ Непосредственной называется такая пептизация, при которой осадок и пептизатор имеют общий ион. Например, осадок Cu. S можно пептизировать с помощью ионов меди или серы (Cu 2+; S 2 -). ¡ Посредственной называется такая пептизация, при которой осадок и пептизатор не имеют общих ионов, но взаимодействуют между собой химически. Например, гидроксид алюминия – осадок, соляная кислота – пептизатор.
Пептизацией ¡ Непосредственной называется такая пептизация, при которой осадок и пептизатор имеют общий ион. Например, осадок Cu. S можно пептизировать с помощью ионов меди или серы (Cu 2+; S 2 -). ¡ Посредственной называется такая пептизация, при которой осадок и пептизатор не имеют общих ионов, но взаимодействуют между собой химически. Например, гидроксид алюминия – осадок, соляная кислота – пептизатор.
 Б. Конденсационный метод основан на переводе веществ в нерастворимое состояние при помощи химических реакций а/ Метод окисления. 2 H 2 S + SO 2 3 S + 2 H 2 O б/ Метод восстановления. Ag 2 O + H 2 2 Ag + H 2 O [так образуется золь серебра] в/ Реакция двойного обмена с образованием труднорастворимого вещества: Ba. Cl 2 + K 2 SO 4 Ba. SO 4 + 2 KCl [золь сульфата бария] г / Метод гидролиза. Fe. Cl 3 + 3 H 2 O Fe(OH)3 + 3 HCl д/ Метод замены растворителя.
Б. Конденсационный метод основан на переводе веществ в нерастворимое состояние при помощи химических реакций а/ Метод окисления. 2 H 2 S + SO 2 3 S + 2 H 2 O б/ Метод восстановления. Ag 2 O + H 2 2 Ag + H 2 O [так образуется золь серебра] в/ Реакция двойного обмена с образованием труднорастворимого вещества: Ba. Cl 2 + K 2 SO 4 Ba. SO 4 + 2 KCl [золь сульфата бария] г / Метод гидролиза. Fe. Cl 3 + 3 H 2 O Fe(OH)3 + 3 HCl д/ Метод замены растворителя.
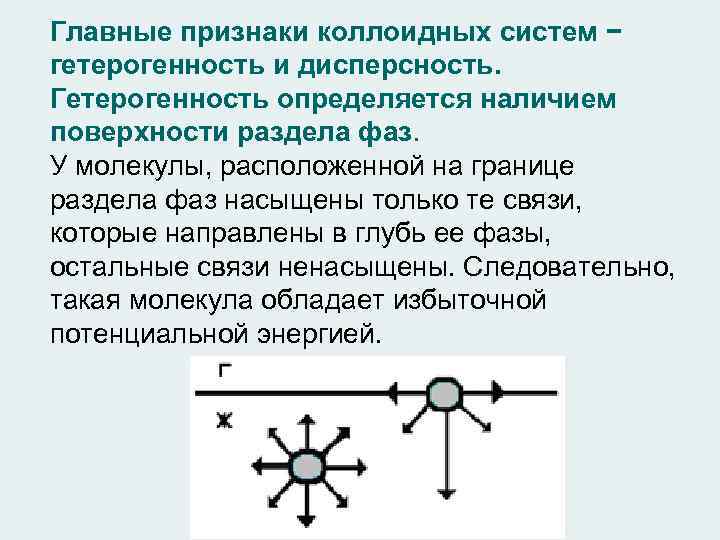 Главные признаки коллоидных систем − гетерогенность и дисперсность. Гетерогенность определяется наличием поверхности раздела фаз. У молекулы, расположенной на границе раздела фаз насыщены только те связи, которые направлены в глубь ее фазы, остальные связи ненасыщены. Следовательно, такая молекула обладает избыточной потенциальной энергией.
Главные признаки коллоидных систем − гетерогенность и дисперсность. Гетерогенность определяется наличием поверхности раздела фаз. У молекулы, расположенной на границе раздела фаз насыщены только те связи, которые направлены в глубь ее фазы, остальные связи ненасыщены. Следовательно, такая молекула обладает избыточной потенциальной энергией.
 Свободная поверхность жидкости или твердого тела обладает избытком поверхностной энергии. ¡ Следовательно, для выведения молекул из объема на поверхность надо преодолеть эту силу, т. е. совершить работу и сообщить молекулам определенную энергию. Увеличение площади поверхности приводит к увеличению числа поверхностных молекул, и поверхностная энергия возрастает. ¡
Свободная поверхность жидкости или твердого тела обладает избытком поверхностной энергии. ¡ Следовательно, для выведения молекул из объема на поверхность надо преодолеть эту силу, т. е. совершить работу и сообщить молекулам определенную энергию. Увеличение площади поверхности приводит к увеличению числа поверхностных молекул, и поверхностная энергия возрастает. ¡
 Поверхностная энергия Gs равна произведению удельной поверхностной энергии σ на площадь поверхности раздела фаз S: G s = σ · ΔS где ΔS – площадь поверхности раздела фаз, м 2; σ − удельная поверхностная энергия, равная работе, необходимой для образования единицы площади свободной поверхности, Дж/м 2.
Поверхностная энергия Gs равна произведению удельной поверхностной энергии σ на площадь поверхности раздела фаз S: G s = σ · ΔS где ΔS – площадь поверхности раздела фаз, м 2; σ − удельная поверхностная энергия, равная работе, необходимой для образования единицы площади свободной поверхности, Дж/м 2.
 ¡ Поверхностное натяжение − это работа образования единицы площади свободной поверхности. В случае жидкой поверхности раздела поверхностное натяжение правомерно также рассматривать как работу, необходимую для увеличения единицы длины контура свободной поверхности: G s = σ · ΔL где ΔL– увеличение длины контура свободной поверхности, м; σ – поверхностное натяжение, н/м.
¡ Поверхностное натяжение − это работа образования единицы площади свободной поверхности. В случае жидкой поверхности раздела поверхностное натяжение правомерно также рассматривать как работу, необходимую для увеличения единицы длины контура свободной поверхности: G s = σ · ΔL где ΔL– увеличение длины контура свободной поверхности, м; σ – поверхностное натяжение, н/м.
 Явления, связанные с превращениями поверхностной энергии Возможны следующие превращения поверхностной энергии: а) в теплоту; б) механическую энергию; в) химическую энергию; д) электрическую энергию. ¡ Эти превращения сопровождают такие явления, как изменение реакционной способности с изменением дисперсности, адгезия и смачивание, капиллярность, адсорбция, электрические явления.
Явления, связанные с превращениями поверхностной энергии Возможны следующие превращения поверхностной энергии: а) в теплоту; б) механическую энергию; в) химическую энергию; д) электрическую энергию. ¡ Эти превращения сопровождают такие явления, как изменение реакционной способности с изменением дисперсности, адгезия и смачивание, капиллярность, адсорбция, электрические явления.
 Адгезия − сцепление поверхностей разнородных тел. ¡ Смачивание − способность впитывать, удерживать влагу. ¡ Капиллярность − явление проникновения жидкости во взаимосвязанные мелкие поры и каналы в твердом материале за счет поверхностного натяжения. ¡ Адсорбция − поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. ¡
Адгезия − сцепление поверхностей разнородных тел. ¡ Смачивание − способность впитывать, удерживать влагу. ¡ Капиллярность − явление проникновения жидкости во взаимосвязанные мелкие поры и каналы в твердом материале за счет поверхностного натяжения. ¡ Адсорбция − поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. ¡
 Как любая система, дисперсные системы стремятся понизить избыточную энергию. Понизить поверхностную энергию дисперсная система может, уменьшив площадь поверхности раздела. Для этого частицы должны укрупниться. ¡ Слияние частиц дисперсной фазы и их укрупнение называется коагуляцией. ¡ Укрупненные частицы под действием собственной тяжести начинают выпадать в осадок. Этот процесс медленный и носит название седиментации. ¡
Как любая система, дисперсные системы стремятся понизить избыточную энергию. Понизить поверхностную энергию дисперсная система может, уменьшив площадь поверхности раздела. Для этого частицы должны укрупниться. ¡ Слияние частиц дисперсной фазы и их укрупнение называется коагуляцией. ¡ Укрупненные частицы под действием собственной тяжести начинают выпадать в осадок. Этот процесс медленный и носит название седиментации. ¡
 Очистка коллоидных растворов Диализ –метод очистки с использованием мембран. Электродиализ — это диализ при использовании постоянного электрического тока. Вивидиффузия. Через трубочки из коллодия протекает кровь, из которой в окружающий физраствор или воду выходят НМС обмена веществ — «система искусственной почки» — АИП. Ультрафильтрация — это отделение дисперсной фазы от дисперсионной среды путем фильтрования через мембраны под давлением или в вакууме. Гельфильтрация. В поры декстринового геля НМС входят и выходят, а ВМС (белки) нет. При элюировании сначала появится фракция ВМС, а затем НМС.
Очистка коллоидных растворов Диализ –метод очистки с использованием мембран. Электродиализ — это диализ при использовании постоянного электрического тока. Вивидиффузия. Через трубочки из коллодия протекает кровь, из которой в окружающий физраствор или воду выходят НМС обмена веществ — «система искусственной почки» — АИП. Ультрафильтрация — это отделение дисперсной фазы от дисперсионной среды путем фильтрования через мембраны под давлением или в вакууме. Гельфильтрация. В поры декстринового геля НМС входят и выходят, а ВМС (белки) нет. При элюировании сначала появится фракция ВМС, а затем НМС.
 Молекулярно-кинетические свойства коллоидных систем 1. Броуновское движение для КС замедленно и не зависит от природы вещества. Зависит: от размеров частиц, от температуры [абсолютной], от вязкости дисперсионной среды, внутреннего трения, от коэффициента диффузии. 2. Диффузия для КС замедленна, т. к. крупные частицы. 3. Росм КС ниже Росм истинных растворов вследствие большого размера частиц и малых концентраций 4. Способность дисперсной системы сохранять по всему объёму распределение частиц называется седиментационной или кинетической устойчивостью. 5. Ультрацентрифугирование. Оседание коллоидов под действием центробежной силы. А. В. Думанский в 1913 г. , Сведберг(ультрацентрифуга)
Молекулярно-кинетические свойства коллоидных систем 1. Броуновское движение для КС замедленно и не зависит от природы вещества. Зависит: от размеров частиц, от температуры [абсолютной], от вязкости дисперсионной среды, внутреннего трения, от коэффициента диффузии. 2. Диффузия для КС замедленна, т. к. крупные частицы. 3. Росм КС ниже Росм истинных растворов вследствие большого размера частиц и малых концентраций 4. Способность дисперсной системы сохранять по всему объёму распределение частиц называется седиментационной или кинетической устойчивостью. 5. Ультрацентрифугирование. Оседание коллоидов под действием центробежной силы. А. В. Думанский в 1913 г. , Сведберг(ультрацентрифуга)
 Оптические свойства Рассеяние света. Дифракционное рассеивание света в результате огибания частиц световой волной- (конус. Тиндаля) Формула Рэлея [1871 г. ]: где I — интенсивность рассеяния света; I 0 — интенсивность падающего света в направлении, перпендикулярном к лучу падающего света; К — константа, зависящая от показателей преломления дисперсионной среды и дисперсной фазы частиц; n — число частиц; V — объём частиц; — длина волны падающего света.
Оптические свойства Рассеяние света. Дифракционное рассеивание света в результате огибания частиц световой волной- (конус. Тиндаля) Формула Рэлея [1871 г. ]: где I — интенсивность рассеяния света; I 0 — интенсивность падающего света в направлении, перпендикулярном к лучу падающего света; К — константа, зависящая от показателей преломления дисперсионной среды и дисперсной фазы частиц; n — число частиц; V — объём частиц; — длина волны падающего света.
 Конус Тиндаля n n Если рассматривать путь светового луча, проходящего через совершенно прозрачный коллоидный раствор, сбоку на темном фоне, то он становится види мым. Этот оптический эффект называется конусом Тиндаля. Он вызывается рассеянием света частицами дисперсной фазы коллоидного раствора и является следствием коллоидной сте пени дисперсности этих частиц. При сильном увеличении каждая частица в конусе Тиндаля кажется светящейся точкой. Размеры и форму частиц нельзя установить, можно лишь подсчитать их число.
Конус Тиндаля n n Если рассматривать путь светового луча, проходящего через совершенно прозрачный коллоидный раствор, сбоку на темном фоне, то он становится види мым. Этот оптический эффект называется конусом Тиндаля. Он вызывается рассеянием света частицами дисперсной фазы коллоидного раствора и является следствием коллоидной сте пени дисперсности этих частиц. При сильном увеличении каждая частица в конусе Тиндаля кажется светящейся точкой. Размеры и форму частиц нельзя установить, можно лишь подсчитать их число.
 • Нефелометрия - метод определения концентрации и степени дисперсности коллоидных систем на явлении светорассеяния. • Интенсивность рассеянного света прямо пропорциональна концентрации частиц, и весовой концентрации дисперсной фазы • Зная концентрацию одного из золей С 1 [стандартный золь известной концентрации], можно определить концентрацию второго золя:
• Нефелометрия - метод определения концентрации и степени дисперсности коллоидных систем на явлении светорассеяния. • Интенсивность рассеянного света прямо пропорциональна концентрации частиц, и весовой концентрации дисперсной фазы • Зная концентрацию одного из золей С 1 [стандартный золь известной концентрации], можно определить концентрацию второго золя:
 Окраска золей связана с избирательным поглощением световых лучей. Если золь только рассеивает, а не поглощает световые лучи — он бесцветен. Опалесценция- рассеяние света в коллоидных системах и изменение окраски коллоида По Рэлею : светорассеяние обратно пропорционально длине волны падающего света Дихроизм— наложение опалесценции на собственную окраску золя.
Окраска золей связана с избирательным поглощением световых лучей. Если золь только рассеивает, а не поглощает световые лучи — он бесцветен. Опалесценция- рассеяние света в коллоидных системах и изменение окраски коллоида По Рэлею : светорассеяние обратно пропорционально длине волны падающего света Дихроизм— наложение опалесценции на собственную окраску золя.
 n n СТРОЕНИЕ МИЦЕЛЛ Мицеллы являются сложными комплексами из многих тысяч атомов, молекул, ионов. Средний размер мицеллы – от 10 5 до 10 7 см. Мицеллы типичных лиофильных золей состоят из: ядра (представляющего собой ультрамикрокристаллическое образование), окруженного двойным электрическим слоем ионов. Один слой ионов (т. н. адсорбционный) находится на поверхности ядра, сообщая ему электрический заряд. Этот слой образуется в результате адсорбции какого либо одного вида ионов из раствора. Эти ионы, сообщающие ядру заряд, называются потенциалопределяющими. В состав адсорбционного слоя входит также часть ионов противоположного знака – компенсирующих ионов. Основная масса этих ионов образует второй слой (слой противоионов), который вследствие теплового движения размыт (диффузный слой). Мицелла обычно окружена ориентированными молекулами растворителя – сольватной оболочкой.
n n СТРОЕНИЕ МИЦЕЛЛ Мицеллы являются сложными комплексами из многих тысяч атомов, молекул, ионов. Средний размер мицеллы – от 10 5 до 10 7 см. Мицеллы типичных лиофильных золей состоят из: ядра (представляющего собой ультрамикрокристаллическое образование), окруженного двойным электрическим слоем ионов. Один слой ионов (т. н. адсорбционный) находится на поверхности ядра, сообщая ему электрический заряд. Этот слой образуется в результате адсорбции какого либо одного вида ионов из раствора. Эти ионы, сообщающие ядру заряд, называются потенциалопределяющими. В состав адсорбционного слоя входит также часть ионов противоположного знака – компенсирующих ионов. Основная масса этих ионов образует второй слой (слой противоионов), который вследствие теплового движения размыт (диффузный слой). Мицелла обычно окружена ориентированными молекулами растворителя – сольватной оболочкой.
 n n Мицелла гетерогенная микросистема, которая состоит из микрокристалла дисперсной фазы, окруженного сольватированными ионами стабилизатора. Ядро мицеллы микрокристалл малорастворимого вещества, на поверхности которого адсорбированы, потенциалопределяющие ионы, сообщающие заряд ядру мицеллы.
n n Мицелла гетерогенная микросистема, которая состоит из микрокристалла дисперсной фазы, окруженного сольватированными ионами стабилизатора. Ядро мицеллы микрокристалл малорастворимого вещества, на поверхности которого адсорбированы, потенциалопределяющие ионы, сообщающие заряд ядру мицеллы.
 n n Противоионы вместе с ядром составляют гранулу: Остальные противоионы, образуют диффузный слой.
n n Противоионы вместе с ядром составляют гранулу: Остальные противоионы, образуют диффузный слой.
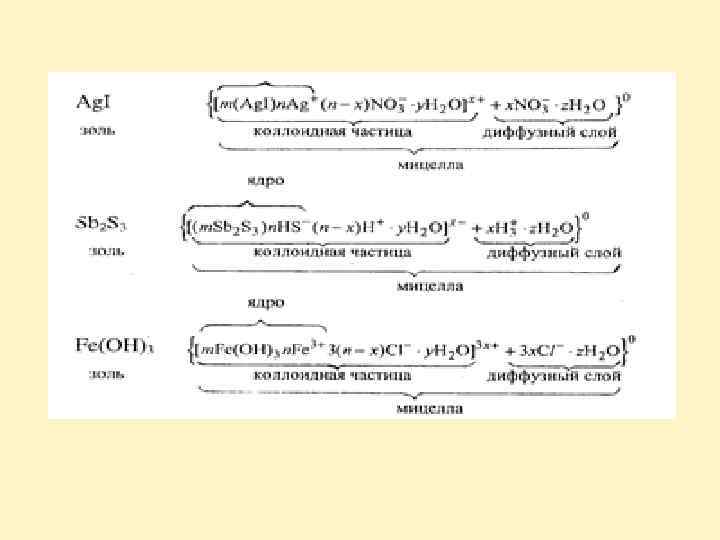
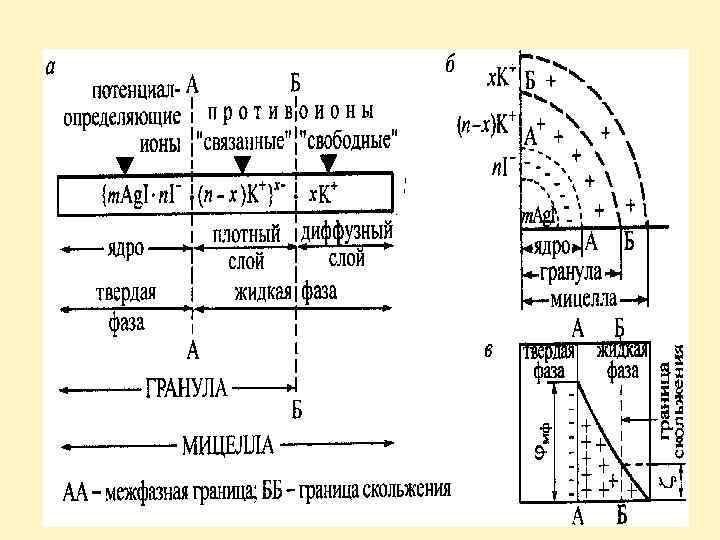
 • Межфазным потенциалом – (электродинамическим)(фи) называется потенциал ДЭС на границе раздела между твердой и жидкой фазами в мицелле (на схемах мицеллы граница АА). • Электрокинетическим потенциалом (дзета) называется потенциал на границе скольжения между адсорбционной и диффузионной частями ДЭС
• Межфазным потенциалом – (электродинамическим)(фи) называется потенциал ДЭС на границе раздела между твердой и жидкой фазами в мицелле (на схемах мицеллы граница АА). • Электрокинетическим потенциалом (дзета) называется потенциал на границе скольжения между адсорбционной и диффузионной частями ДЭС
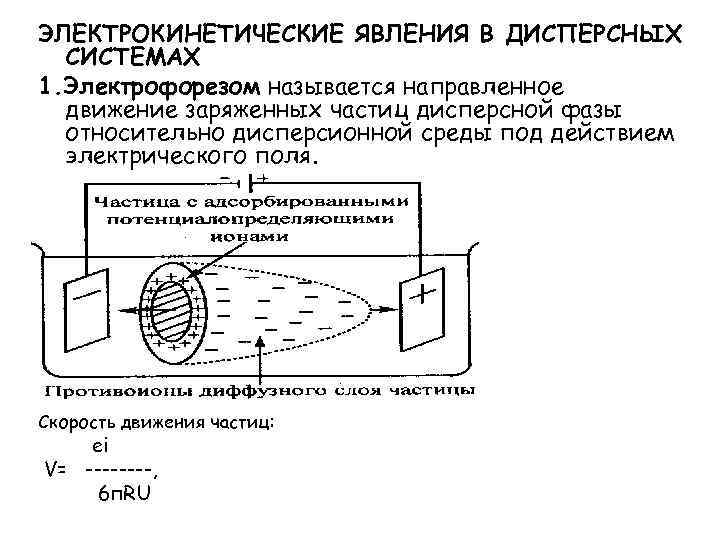 ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ В ДИСПЕРСНЫХ СИСТЕМАХ 1. Электрофорезом называется направленное движение заряженных частиц дисперсной фазы относительно дисперсионной среды под действием электрического поля. Скорость движения частиц: ei V= ----, 6 п. RU
ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ В ДИСПЕРСНЫХ СИСТЕМАХ 1. Электрофорезом называется направленное движение заряженных частиц дисперсной фазы относительно дисперсионной среды под действием электрического поля. Скорость движения частиц: ei V= ----, 6 п. RU
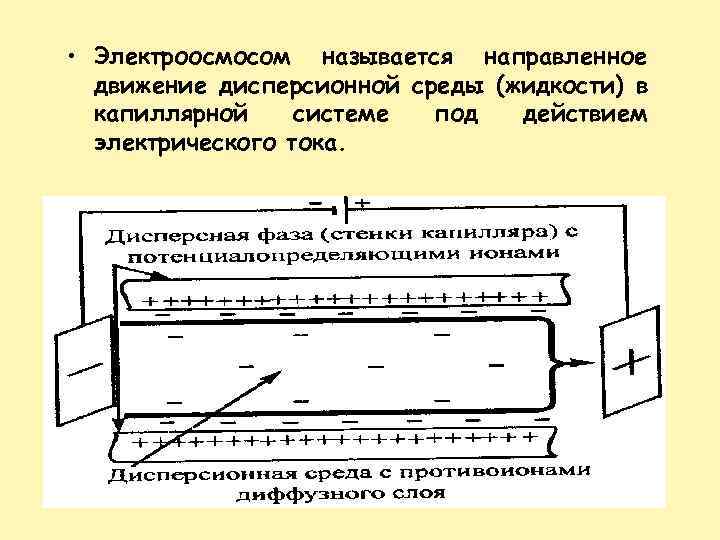 • Электроосмосом называется направленное движение дисперсионной среды (жидкости) в капиллярной системе под действием электрического тока.
• Электроосмосом называется направленное движение дисперсионной среды (жидкости) в капиллярной системе под действием электрического тока.
 Коагуляция – процесс слипания коллоидных частиц с образованием более крупных агрегатов из-за потери коллоидным раствором агрегативной устойчивости. Коагуляцию можно вызвать воздействиями: -добавлением электролита, -концентрированием коллоидного раствора, -изменением температуры, -действием ультразвука, -электромагнитного поля и др.
Коагуляция – процесс слипания коллоидных частиц с образованием более крупных агрегатов из-за потери коллоидным раствором агрегативной устойчивости. Коагуляцию можно вызвать воздействиями: -добавлением электролита, -концентрированием коллоидного раствора, -изменением температуры, -действием ультразвука, -электромагнитного поля и др.
 Коагуляция смесями электролитов: 1. аддитивное действие, 2. антагонизм 3. синергизм n n Аддитивность - это суммирование коагулирующего действия ионов, вызывающих коагуляцию - не взаимодействуют химически между собой. Например, смесь солей КС 1 и Na. NO 3
Коагуляция смесями электролитов: 1. аддитивное действие, 2. антагонизм 3. синергизм n n Аддитивность - это суммирование коагулирующего действия ионов, вызывающих коагуляцию - не взаимодействуют химически между собой. Например, смесь солей КС 1 и Na. NO 3
 n n Антагонизм — это ослабление электролита в присутствии другого- ионы связываются в нерастворимое соединение. Например, у РЬ 2+ по отношению к отрицательно заряженным гранулам ослабляется в присутствии Na. Cl: РЬ 2+ + 2 Сl-= РЬС 12 Синергизм — это усиление у одного электролита в присутствии другого- - химическое взаимодействие c образованием многозарядного иона, обладающего очень высокой коагулирующей способностью. Fe. Cl 3 + 6 KCNS —K 3[Fe(CNS)6] + 3 KC 1
n n Антагонизм — это ослабление электролита в присутствии другого- ионы связываются в нерастворимое соединение. Например, у РЬ 2+ по отношению к отрицательно заряженным гранулам ослабляется в присутствии Na. Cl: РЬ 2+ + 2 Сl-= РЬС 12 Синергизм — это усиление у одного электролита в присутствии другого- - химическое взаимодействие c образованием многозарядного иона, обладающего очень высокой коагулирующей способностью. Fe. Cl 3 + 6 KCNS —K 3[Fe(CNS)6] + 3 KC 1


