 Лекция 5 Химия аминокислот
Лекция 5 Химия аминокислот
 План • • Аминокислоты. Строение. Физико-химические свойства. Классификация. Заменимые и незаменимые аминокислоты
План • • Аминокислоты. Строение. Физико-химические свойства. Классификация. Заменимые и незаменимые аминокислоты
 Белки • Белки - это высокомолекулярные азотсодержащие соединения, состоящие из аминокислот, соединенных пептидной связью (-CО-NН-). Белки называют также протеинами (от греч. protos - первый, важнейший). • Молекулы, содержащие менее 50 аминокислотных остатков, называют пептидами. • В организме человека насчитывается до 5 млн. различных видов белков.
Белки • Белки - это высокомолекулярные азотсодержащие соединения, состоящие из аминокислот, соединенных пептидной связью (-CО-NН-). Белки называют также протеинами (от греч. protos - первый, важнейший). • Молекулы, содержащие менее 50 аминокислотных остатков, называют пептидами. • В организме человека насчитывается до 5 млн. различных видов белков.
 Функции белков • • • Ферментативная Строительная Сократительная Регуляторная Рецепторная Транспортная Защитная Специальная Питательная
Функции белков • • • Ферментативная Строительная Сократительная Регуляторная Рецепторная Транспортная Защитная Специальная Питательная
 Методы выделения и очистки белков • • • Осаждение с помощью дегидратации Изоэлектрическое осаждение Центрифугирование Сорбция Ситовой эффект Диализ
Методы выделения и очистки белков • • • Осаждение с помощью дегидратации Изоэлектрическое осаждение Центрифугирование Сорбция Ситовой эффект Диализ
 Структурным компонентом белковой молекулы является аминокислота. Аминокислотами называются органические кислоты, содержащие одну или несколько аминогрупп. В зависимости от положения аминогруппы по отношению к карбоксилу различают α, β и γаминокислоты α-аминомасляная β-аминопропионовая γ-аминомасляная
Структурным компонентом белковой молекулы является аминокислота. Аминокислотами называются органические кислоты, содержащие одну или несколько аминогрупп. В зависимости от положения аминогруппы по отношению к карбоксилу различают α, β и γаминокислоты α-аминомасляная β-аминопропионовая γ-аминомасляная
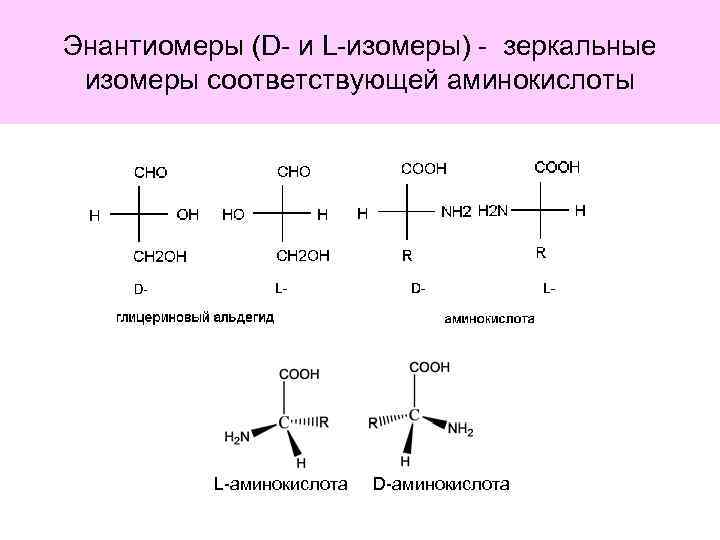 Энантиомеры (D- и L-изомеры) - зеркальные изомеры соответствующей аминокислоты L-аминокислота D-аминокислота
Энантиомеры (D- и L-изомеры) - зеркальные изомеры соответствующей аминокислоты L-аминокислота D-аминокислота
 Биполярный ион аминокислоты (цвиттер-ион) На диссоциацию аминокислот оказывает влияние p. H среды. В очень кислых растворах NH 2 протонирована полностью, щелочных растворах – COOH-группа депротонирована
Биполярный ион аминокислоты (цвиттер-ион) На диссоциацию аминокислот оказывает влияние p. H среды. В очень кислых растворах NH 2 протонирована полностью, щелочных растворах – COOH-группа депротонирована
 Основные аминокислоты в водном растворе дают щелочную реакцию и несут положительный заряд: Кислые аминокислоты в водном растворе проявляют кислотные свойства и оладают отрицательным зарядом:
Основные аминокислоты в водном растворе дают щелочную реакцию и несут положительный заряд: Кислые аминокислоты в водном растворе проявляют кислотные свойства и оладают отрицательным зарядом:
 Амфотерные свойства аминокислот проявляются и в их способности образовывать соли, реагируя как с кислотами, так и с основаниями: Проявлением амфотерности является способность аминокислот образовывать окрашенные растворимые комплексные соединения с Cu 2+:
Амфотерные свойства аминокислот проявляются и в их способности образовывать соли, реагируя как с кислотами, так и с основаниями: Проявлением амфотерности является способность аминокислот образовывать окрашенные растворимые комплексные соединения с Cu 2+:
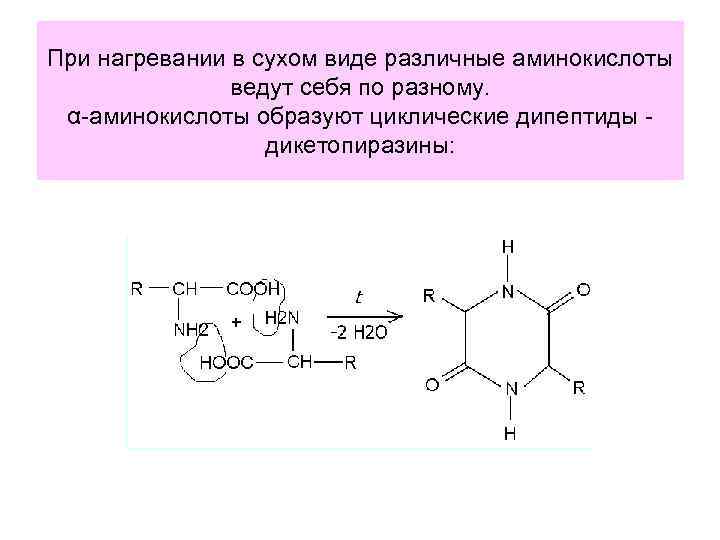 При нагревании в сухом виде различные аминокислоты ведут себя по разному. α-аминокислоты образуют циклические дипептиды дикетопиразины:
При нагревании в сухом виде различные аминокислоты ведут себя по разному. α-аминокислоты образуют циклические дипептиды дикетопиразины:
 Свойства аминокислот • Аминокислоты: – хорошо растворимы в воде, мало растворимы в органических растворителях; – хорошо кристаллизуются; – имеют высокую плотность и высокие температуры плавления. Эти свойства указывают на взаимодействие аминных и кислотных групп, вследствие чего аминокислоты в твёрдом состоянии и в растворе (в широком интервале р. Н) находятся в цвиттерионной форме. Взаимное влияние групп особенно ярко проявляется у α-аминокислот, где обе группы находятся в непосредственной близости.
Свойства аминокислот • Аминокислоты: – хорошо растворимы в воде, мало растворимы в органических растворителях; – хорошо кристаллизуются; – имеют высокую плотность и высокие температуры плавления. Эти свойства указывают на взаимодействие аминных и кислотных групп, вследствие чего аминокислоты в твёрдом состоянии и в растворе (в широком интервале р. Н) находятся в цвиттерионной форме. Взаимное влияние групп особенно ярко проявляется у α-аминокислот, где обе группы находятся в непосредственной близости.
 Аминокислоты классифицируются по: • Строению • Полярности • Заменимости-незаменимости. Классификация по строению: 1. Моноаминомонокарбоновые 2. Диаминомонокарбоновые (лизин, аргинин, цитруллин 3. Моноаминодикарбоновые (аспарагиновая и глутаминовая кислоты) 4. Диаминодикарбоновые (цистин)
Аминокислоты классифицируются по: • Строению • Полярности • Заменимости-незаменимости. Классификация по строению: 1. Моноаминомонокарбоновые 2. Диаминомонокарбоновые (лизин, аргинин, цитруллин 3. Моноаминодикарбоновые (аспарагиновая и глутаминовая кислоты) 4. Диаминодикарбоновые (цистин)
 По характеру заряженности боковых радикалов аминокислоты подразделяют на: • Неполярные гидрофобные (Гли, Ала, Вал, Лей, Иле, Про, Фен, Тир, Три, Мет) • Полярные, но незаряженные (Сер, Тре, Цис, Асн, Глн) • Полярные с отрицательным зарядом (Асп, Глу) • Полярные с положительным зарядом (Лиз, Арг, Гис)
По характеру заряженности боковых радикалов аминокислоты подразделяют на: • Неполярные гидрофобные (Гли, Ала, Вал, Лей, Иле, Про, Фен, Тир, Три, Мет) • Полярные, но незаряженные (Сер, Тре, Цис, Асн, Глн) • Полярные с отрицательным зарядом (Асп, Глу) • Полярные с положительным зарядом (Лиз, Арг, Гис)
 Аминокислоты • Заменимые • Аспарагин • Аспартат • Глицин • Глутамат • Глутамин • Аланин • Условно заменимые Пролин • Тирозин • • Серин Цистеин Незаменимые Для взрослого: • Валин • Изолейцин • Лейцин • Треонин • Метионин • Лизин • Триптофан • Фенилаланин Для детей: • Гистидин • Аргинин
Аминокислоты • Заменимые • Аспарагин • Аспартат • Глицин • Глутамат • Глутамин • Аланин • Условно заменимые Пролин • Тирозин • • Серин Цистеин Незаменимые Для взрослого: • Валин • Изолейцин • Лейцин • Треонин • Метионин • Лизин • Триптофан • Фенилаланин Для детей: • Гистидин • Аргинин

 Литература • • • Биохимия: Учебник /Под. ред. Е. С. Северина. - М. : ГЭОТАР-МЕД, 2003. - 784 с. Биохимия. Краткий курс с упражнениями и задачами / Под ред. Е. С. Северина, А. Я. Николаева. - М. : ГЭОТАР-МЕД, 2001. -448 с. Березов Т. Т. , Коровкин Б. Ф. Биологическая химия. - М. : Медицина, 2008. - 704 с.
Литература • • • Биохимия: Учебник /Под. ред. Е. С. Северина. - М. : ГЭОТАР-МЕД, 2003. - 784 с. Биохимия. Краткий курс с упражнениями и задачами / Под ред. Е. С. Северина, А. Я. Николаева. - М. : ГЭОТАР-МЕД, 2001. -448 с. Березов Т. Т. , Коровкин Б. Ф. Биологическая химия. - М. : Медицина, 2008. - 704 с.


