СЖД_Лекция 05_Фаз равн_Неэлектр.ppt
- Количество слайдов: 26
 Лекция № 5 Химические и фазовые равновесия Растворы неэлектролитов
Лекция № 5 Химические и фазовые равновесия Растворы неэлектролитов
 Динамическое равновесие химическое N 2 + 3 H 2 2 NH 3 физическое фазовые равновесия (твердое вещество жидкость пар)
Динамическое равновесие химическое N 2 + 3 H 2 2 NH 3 физическое фазовые равновесия (твердое вещество жидкость пар)
 Фазовые равновесия Фаза – гомогенная часть гетерогенной системы (часть, имеющая одинаковый состав и свойства во всех точках, отделенная от других частей поверхностями раздела) Фазовый переход – переход из одной фазы в другую (твердое вещество жидкость пар) Компоненты – индивидуальные вещества, составляющие систему
Фазовые равновесия Фаза – гомогенная часть гетерогенной системы (часть, имеющая одинаковый состав и свойства во всех точках, отделенная от других частей поверхностями раздела) Фазовый переход – переход из одной фазы в другую (твердое вещество жидкость пар) Компоненты – индивидуальные вещества, составляющие систему
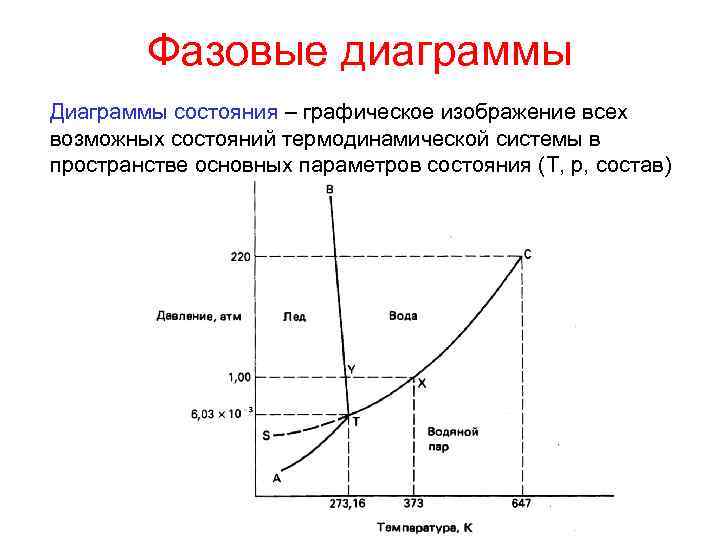 Фазовые диаграммы Диаграммы состояния – графическое изображение всех возможных состояний термодинамической системы в пространстве основных параметров состояния (Т, р, состав)
Фазовые диаграммы Диаграммы состояния – графическое изображение всех возможных состояний термодинамической системы в пространстве основных параметров состояния (Т, р, состав)
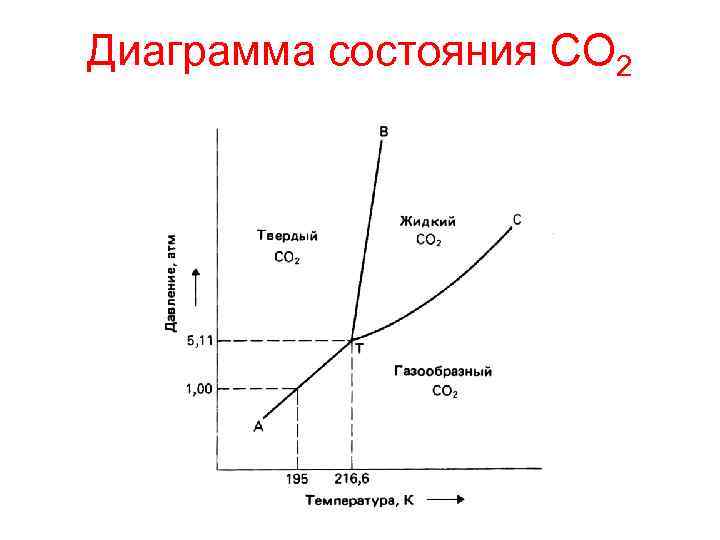 Диаграмма состояния СО 2
Диаграмма состояния СО 2
 Растворы гомогенные системы, состоящие из двух или более компонентов, состав которых можно изменять в некоторых пределах без нарушения однородности жидкие твердые газообразные Раствор = растворитель + растворенное вещество
Растворы гомогенные системы, состоящие из двух или более компонентов, состав которых можно изменять в некоторых пределах без нарушения однородности жидкие твердые газообразные Раствор = растворитель + растворенное вещество
 Концентрация раствора Молярная концентрация (С) – число молей растворенного вещества в одном литре раствора. Нормальная концентрация Cн (N) – число молей эквивалентов растворенного вещества в одном литре раствора.
Концентрация раствора Молярная концентрация (С) – число молей растворенного вещества в одном литре раствора. Нормальная концентрация Cн (N) – число молей эквивалентов растворенного вещества в одном литре раствора.
 Концентрация раствора Моляльная концентрация Сm – число молей растворенного вещества в одном килограмме растворителя. Процентная концентрация ω – число граммов растворенного вещества в 100 граммах раствора.
Концентрация раствора Моляльная концентрация Сm – число молей растворенного вещества в одном килограмме растворителя. Процентная концентрация ω – число граммов растворенного вещества в 100 граммах раствора.
 Растворы электролитов неэлектролитов (проводят эл. ток, распадаются на ионы) (не проводят эл. ток, не распадаются на ионы)
Растворы электролитов неэлектролитов (проводят эл. ток, распадаются на ионы) (не проводят эл. ток, не распадаются на ионы)
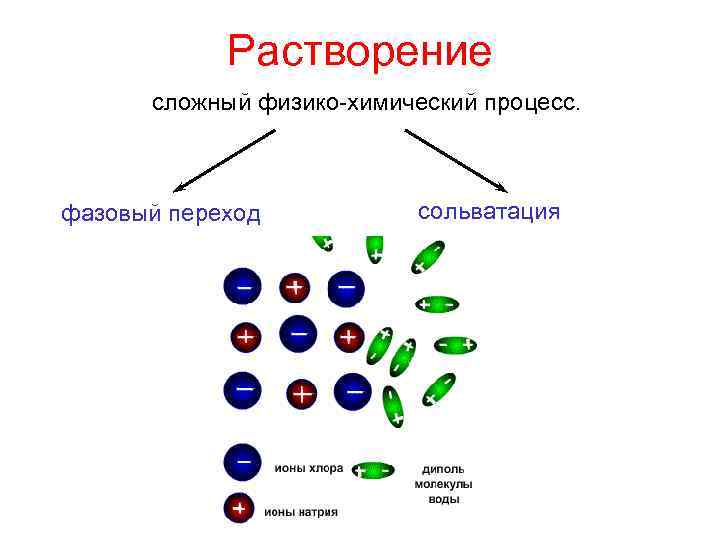 Растворение сложный физико-химический процесс. фазовый переход сольватация
Растворение сложный физико-химический процесс. фазовый переход сольватация
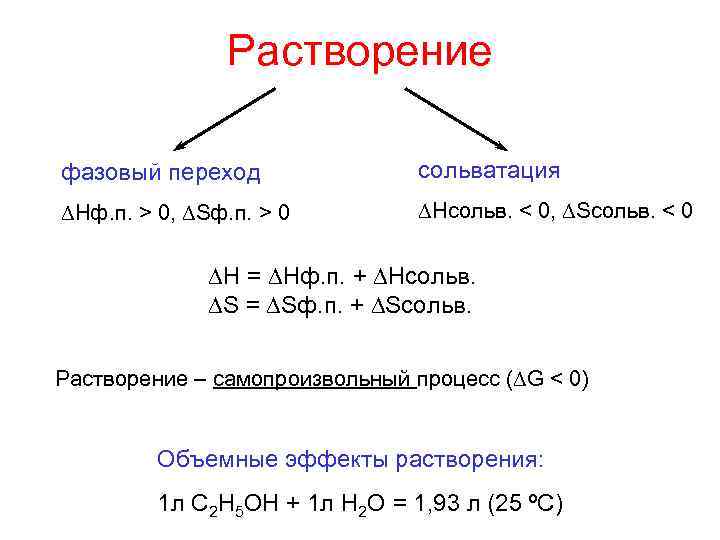 Растворение фазовый переход сольватация Нф. п. > 0, Sф. п. > 0 Hсольв. < 0, Sсольв. < 0 H = Hф. п. + Hсольв. S = Sф. п. + Sсольв. Растворение – самопроизвольный процесс ( G < 0) Объемные эффекты растворения: 1 л С 2 Н 5 ОН + 1 л Н 2 О = 1, 93 л (25 ºС)
Растворение фазовый переход сольватация Нф. п. > 0, Sф. п. > 0 Hсольв. < 0, Sсольв. < 0 H = Hф. п. + Hсольв. S = Sф. п. + Sсольв. Растворение – самопроизвольный процесс ( G < 0) Объемные эффекты растворения: 1 л С 2 Н 5 ОН + 1 л Н 2 О = 1, 93 л (25 ºС)
 Растворимость Ненасыщенный раствор (самопроизвольный процесс растворения) G < 0 Насыщенный раствор (равновесие) G = 0 Пересыщенный раствор (кажущееся равновесие) G > 0 Растворимость – концентрация вещества в насыщенном растворе Растворимость зависит от: • природы вещества ("подобное в подобном") • внешних условий (Т, р)
Растворимость Ненасыщенный раствор (самопроизвольный процесс растворения) G < 0 Насыщенный раствор (равновесие) G = 0 Пересыщенный раствор (кажущееся равновесие) G > 0 Растворимость – концентрация вещества в насыщенном растворе Растворимость зависит от: • природы вещества ("подобное в подобном") • внешних условий (Т, р)
 Растворимость газов в газах Газовые смеси: закон Дальтона
Растворимость газов в газах Газовые смеси: закон Дальтона
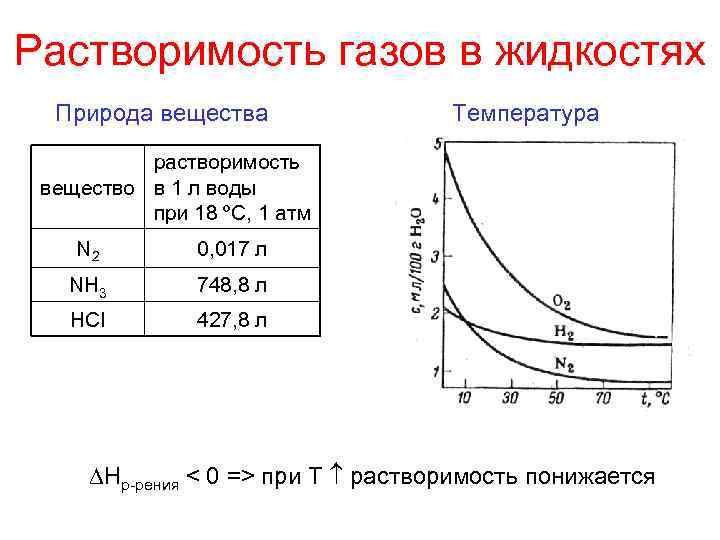 Растворимость газов в жидкостях Природа вещества Температура растворимость вещество в 1 л воды при 18 ºС, 1 атм N 2 0, 017 л NH 3 748, 8 л HCl 427, 8 л Hр-рения < 0 => при Т растворимость понижается
Растворимость газов в жидкостях Природа вещества Температура растворимость вещество в 1 л воды при 18 ºС, 1 атм N 2 0, 017 л NH 3 748, 8 л HCl 427, 8 л Hр-рения < 0 => при Т растворимость понижается
 Растворимость газов в жидкостях Давление V уменьшается => при р растворимость увеличивается Закон Генри Растворимость газа в жидкости прямо пропорциональна его давлению над жидкостью
Растворимость газов в жидкостях Давление V уменьшается => при р растворимость увеличивается Закон Генри Растворимость газа в жидкости прямо пропорциональна его давлению над жидкостью
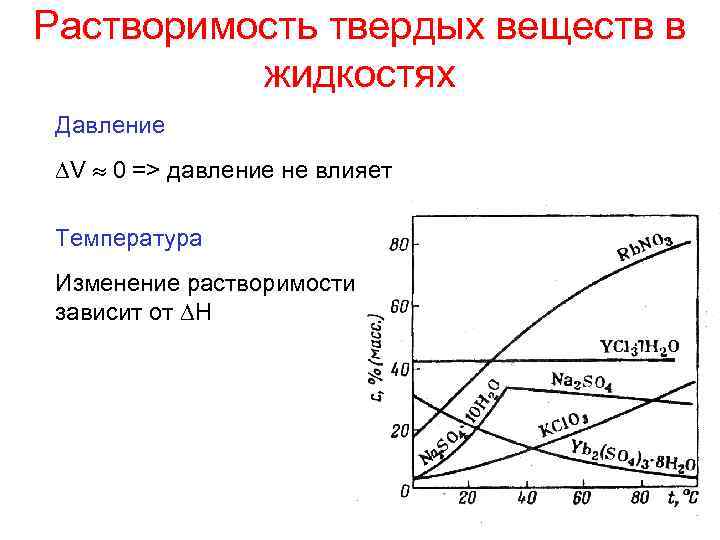 Растворимость твердых веществ в жидкостях Давление V 0 => давление не влияет Температура Изменение растворимости зависит от H
Растворимость твердых веществ в жидкостях Давление V 0 => давление не влияет Температура Изменение растворимости зависит от H
 Коллигативные свойства растворов – свойства, которые зависят только от концентрации растворенного вещества, от природы вещества не зависят. Идеальные растворы – разбавленные растворы, при образовании которых тепловой и объемный эффекты равны нулю (приближение – растворы неэлектролитов)
Коллигативные свойства растворов – свойства, которые зависят только от концентрации растворенного вещества, от природы вещества не зависят. Идеальные растворы – разбавленные растворы, при образовании которых тепловой и объемный эффекты равны нулю (приближение – растворы неэлектролитов)
 Давление пара над раствором 1– растворитель; 2 – нелетучее вещество Первый закон Рауля: давление насыщенного пара раствора равно произведению давления над чистым растворителем на мольную долю растворителя
Давление пара над раствором 1– растворитель; 2 – нелетучее вещество Первый закон Рауля: давление насыщенного пара раствора равно произведению давления над чистым растворителем на мольную долю растворителя
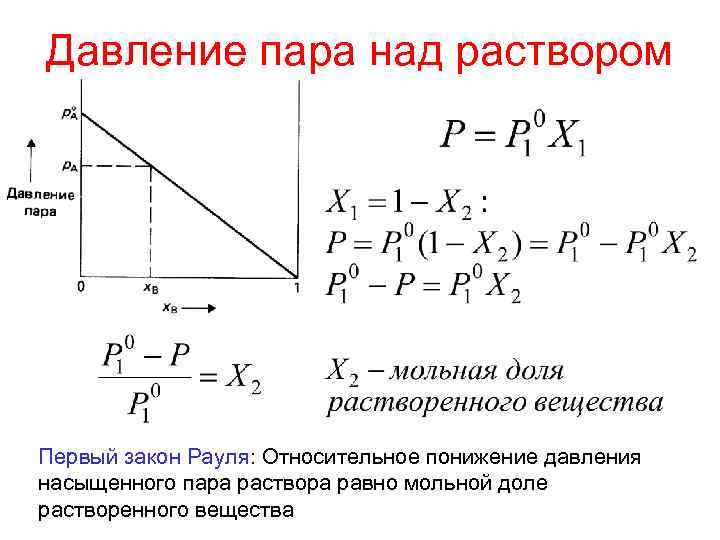 Давление пара над раствором Первый закон Рауля: Относительное понижение давления насыщенного пара раствора равно мольной доле растворенного вещества
Давление пара над раствором Первый закон Рауля: Относительное понижение давления насыщенного пара раствора равно мольной доле растворенного вещества
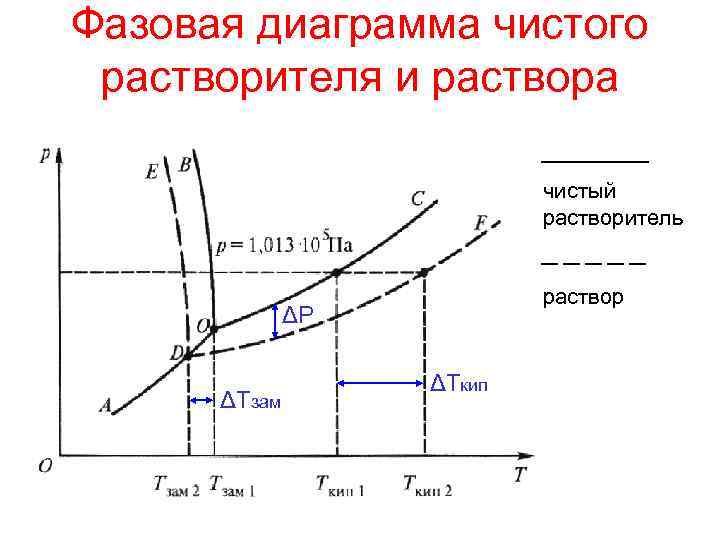 Фазовая диаграмма чистого растворителя и раствора чистый растворитель раствор ΔР ΔТзам ΔТкип
Фазовая диаграмма чистого растворителя и раствора чистый растворитель раствор ΔР ΔТзам ΔТкип
 Повышение температуры кипения Р-р, содержащий нелетучее вещество, обладает меньшей летучестью, чем чистый растворитель Температура кипения раствора выше, чем температура кипения чистого растворителя
Повышение температуры кипения Р-р, содержащий нелетучее вещество, обладает меньшей летучестью, чем чистый растворитель Температура кипения раствора выше, чем температура кипения чистого растворителя
 Понижение температуры замерзания Температура замерзания раствора ниже, чем температура кипения чистого растворителя
Понижение температуры замерзания Температура замерзания раствора ниже, чем температура кипения чистого растворителя
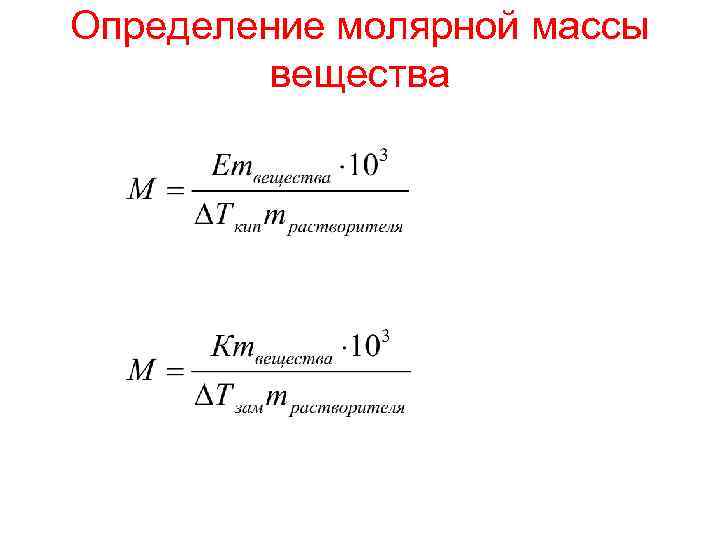 Определение молярной массы вещества
Определение молярной массы вещества
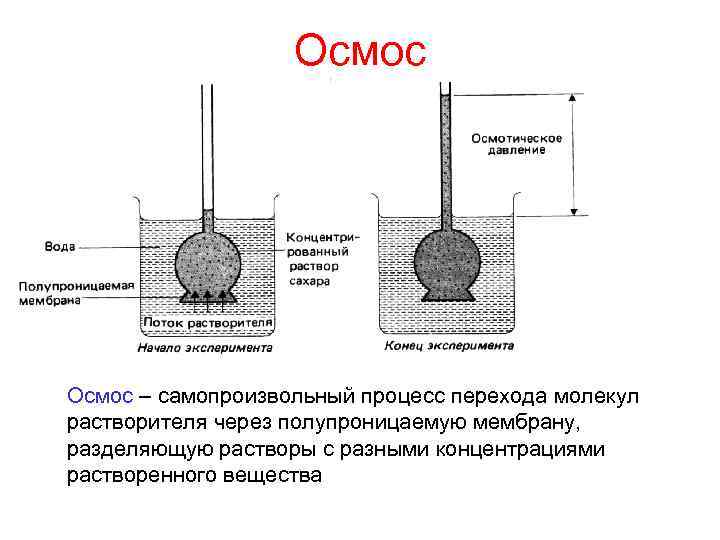 Осмос – самопроизвольный процесс перехода молекул растворителя через полупроницаемую мембрану, разделяющую растворы с разными концентрациями растворенного вещества
Осмос – самопроизвольный процесс перехода молекул растворителя через полупроницаемую мембрану, разделяющую растворы с разными концентрациями растворенного вещества
 Осмотическое давление ( ) равно силе, приходящейся на единицу поверхности мембраны, которую нужно приложить, чтобы предотвратить проникновение молекул растворителя из раствора с меньшей концентрацией в раствор с большей концентрацией Закон Вант-Гоффа:
Осмотическое давление ( ) равно силе, приходящейся на единицу поверхности мембраны, которую нужно приложить, чтобы предотвратить проникновение молекул растворителя из раствора с меньшей концентрацией в раствор с большей концентрацией Закон Вант-Гоффа:
 Растворы • гипотонический раствора < раствора клетки • изотонический раствора = раствора клетки (физ. раствор: 0, 9% Na. Cl) • гипертонический раствора > раствора клетки
Растворы • гипотонический раствора < раствора клетки • изотонический раствора = раствора клетки (физ. раствор: 0, 9% Na. Cl) • гипертонический раствора > раствора клетки


