Лекция_N5_2013.ppt
- Количество слайдов: 33
 Лекция 5. Устойчивость дисперсных систем. Агрегация. Теория ДЛФО. Потенциал Ленарда. Джонса. Типы взаимодействия частиц. Силы Вандер-Ваальса. Водородные связи. Электростатические силы для заряженных частиц. Двойной электрический слой. Расклинивающее давление. Гидрофобное/гидрофильное взаимодействие. Сольватация. Теория Лифшица – Слезова - Вагнера. Стабилизация наночастиц. 1
Лекция 5. Устойчивость дисперсных систем. Агрегация. Теория ДЛФО. Потенциал Ленарда. Джонса. Типы взаимодействия частиц. Силы Вандер-Ваальса. Водородные связи. Электростатические силы для заряженных частиц. Двойной электрический слой. Расклинивающее давление. Гидрофобное/гидрофильное взаимодействие. Сольватация. Теория Лифшица – Слезова - Вагнера. Стабилизация наночастиц. 1
 Дисперсные системы занимают промежуточное положение между макроскопическими гетерогенными системами и молекулярными растворами – гомогенными системами Дисперсные системы Лиофильные системы Ø термодинамически стабильны Ø образуются самопроизвольно при очень низких значениях межфазного натяжения Ø характеризуются равновесным распределением частиц по размерам, не зависящим от способа получения системы Лиофобные системы Ø термодинамически неустойчивые системы Ø образуются несамопроизвольно в результате диспергирования или конденсации при высоких значениях межфазной энергии 2
Дисперсные системы занимают промежуточное положение между макроскопическими гетерогенными системами и молекулярными растворами – гомогенными системами Дисперсные системы Лиофильные системы Ø термодинамически стабильны Ø образуются самопроизвольно при очень низких значениях межфазного натяжения Ø характеризуются равновесным распределением частиц по размерам, не зависящим от способа получения системы Лиофобные системы Ø термодинамически неустойчивые системы Ø образуются несамопроизвольно в результате диспергирования или конденсации при высоких значениях межфазной энергии 2
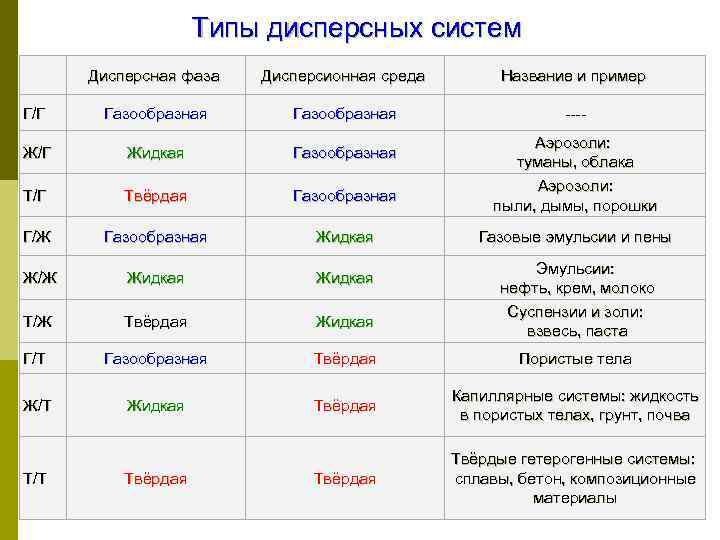 Типы дисперсных систем Дисперсная фаза Дисперсионная среда Название и пример Г/Г Газообразная ---- Ж/Г Жидкая Газообразная Т/Г Твёрдая Газообразная Г/Ж Газообразная Жидкая Ж/Ж Жидкая Т/Ж Твёрдая Жидкая Г/Т Газообразная Твёрдая Пористые тела Ж/Т Жидкая Твёрдая Капиллярные системы: жидкость в пористых телах, грунт, почва Твёрдая Твёрдые гетерогенные системы: сплавы, бетон, композиционные материалы 3 Т/Т Твёрдая Аэрозоли: туманы, облака Аэрозоли: пыли, дымы, порошки Газовые эмульсии и пены Эмульсии: нефть, крем, молоко Суспензии и золи: взвесь, паста
Типы дисперсных систем Дисперсная фаза Дисперсионная среда Название и пример Г/Г Газообразная ---- Ж/Г Жидкая Газообразная Т/Г Твёрдая Газообразная Г/Ж Газообразная Жидкая Ж/Ж Жидкая Т/Ж Твёрдая Жидкая Г/Т Газообразная Твёрдая Пористые тела Ж/Т Жидкая Твёрдая Капиллярные системы: жидкость в пористых телах, грунт, почва Твёрдая Твёрдые гетерогенные системы: сплавы, бетон, композиционные материалы 3 Т/Т Твёрдая Аэрозоли: туманы, облака Аэрозоли: пыли, дымы, порошки Газовые эмульсии и пены Эмульсии: нефть, крем, молоко Суспензии и золи: взвесь, паста
 Условие самопроизвольного образования дисперсной системы из макрофазы Общее изменение свободной энергии при образовании дисперсной системы с n 1 частицами дисперсной фазы радиусом r в N 2 молях растворителя d – линейный размер для несферических частиц, α – коэффициент формы возможно самопроизвольное отщепление частиц коллоидного размера от макрофазы, если межфазное натяжение мало 4
Условие самопроизвольного образования дисперсной системы из макрофазы Общее изменение свободной энергии при образовании дисперсной системы с n 1 частицами дисперсной фазы радиусом r в N 2 молях растворителя d – линейный размер для несферических частиц, α – коэффициент формы возможно самопроизвольное отщепление частиц коллоидного размера от макрофазы, если межфазное натяжение мало 4
 Устойчивость лиофобных систем Седиментационная устойчивость системы против снижения потенциальной энергии частиц дисперсной фазы при их оседании под действием силы тяжести Условие седиментационной устойчивости Агрегативная устойчивость способность системы противостоять процессам, ведущим к уменьшению свободной энергии поверхностей раздела частиц дисперсной фазы с дисперсионной средой: Ø Изотермическая перегонка (переконденсация, оствальдово созревание) Ø Коалесценция (слияние, срастание) Ø Коагуляция (агрегирование при слипании) Условие устойчивости к агрегированию вес частиц плотностью ρ в среде плотностью ρ0 5
Устойчивость лиофобных систем Седиментационная устойчивость системы против снижения потенциальной энергии частиц дисперсной фазы при их оседании под действием силы тяжести Условие седиментационной устойчивости Агрегативная устойчивость способность системы противостоять процессам, ведущим к уменьшению свободной энергии поверхностей раздела частиц дисперсной фазы с дисперсионной средой: Ø Изотермическая перегонка (переконденсация, оствальдово созревание) Ø Коалесценция (слияние, срастание) Ø Коагуляция (агрегирование при слипании) Условие устойчивости к агрегированию вес частиц плотностью ρ в среде плотностью ρ0 5
 Механизм оствальдовского созревания 6
Механизм оствальдовского созревания 6
 Срастание, гидрогель, ксерогель 7
Срастание, гидрогель, ксерогель 7
 Теория ДЛФО Расклинивающее давление Π возникает при сильном уменьшении толщины пленки (прослойки) между двумя межфазными поверхностями в результате перекрывания поверхностных слоев; это то избыточное давление, которое нужно приложить к поверхностям, ограничивающим тонкую пленку, чтобы ее толщина h оставалась постоянной или могла быть обратимо изменена в термодинамически равновесном процессе. 8
Теория ДЛФО Расклинивающее давление Π возникает при сильном уменьшении толщины пленки (прослойки) между двумя межфазными поверхностями в результате перекрывания поверхностных слоев; это то избыточное давление, которое нужно приложить к поверхностям, ограничивающим тонкую пленку, чтобы ее толщина h оставалась постоянной или могла быть обратимо изменена в термодинамически равновесном процессе. 8
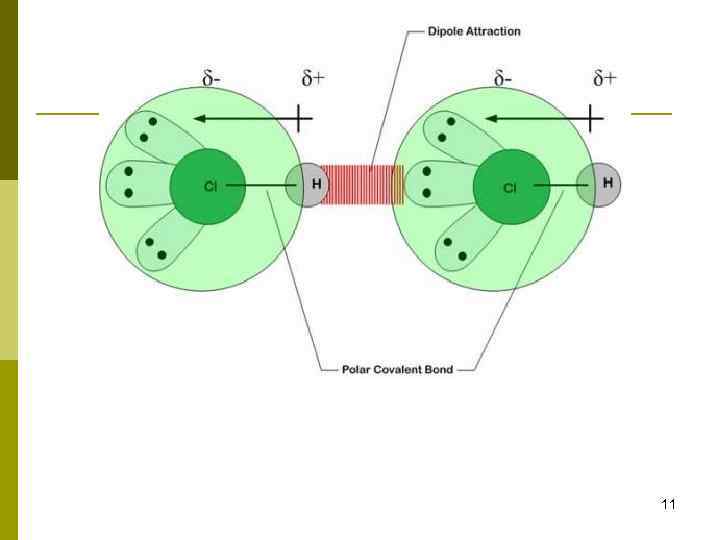
 Типы взаимодействия частиц 1. ковалентное 2. заряд-заряд (Кулоновское) 3. заряд-диполь 4. диполь-диполь 5. заряд-неполярная частица 6. диполь-неполярная частица 7. две неполярные частицы 8. водородная связь 9
Типы взаимодействия частиц 1. ковалентное 2. заряд-заряд (Кулоновское) 3. заряд-диполь 4. диполь-диполь 5. заряд-неполярная частица 6. диполь-неполярная частица 7. две неполярные частицы 8. водородная связь 9
 Сильные взаимодействия Ковалентное – короткие 0. 1 -0. 2 нм (расстояния между атомами) Энергия 200 -800 к. Дж/моль направленные Кулоновское Na. Cl : r = 0. 276 nm w(r)=8. 4 10 -19 Дж (200 к. Т) w(r)=880 к. Дж/моль r=56 nm w(r)=к. Т 10
Сильные взаимодействия Ковалентное – короткие 0. 1 -0. 2 нм (расстояния между атомами) Энергия 200 -800 к. Дж/моль направленные Кулоновское Na. Cl : r = 0. 276 nm w(r)=8. 4 10 -19 Дж (200 к. Т) w(r)=880 к. Дж/моль r=56 nm w(r)=к. Т 10
 11
11
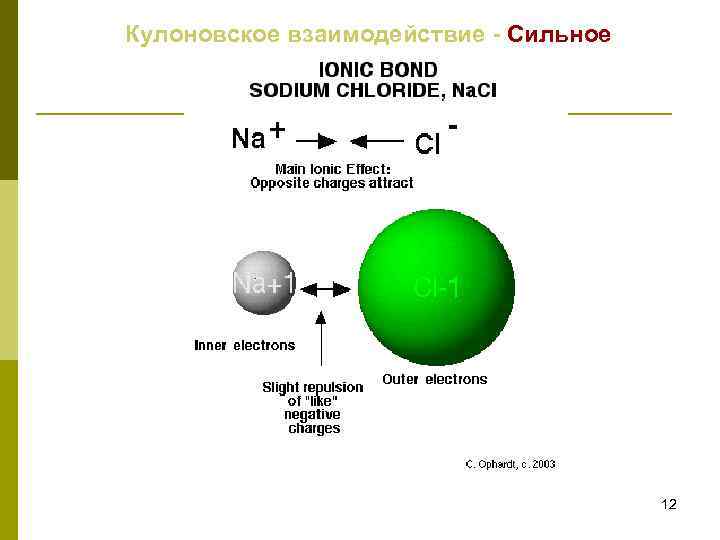 Кулоновское взаимодействие - Сильное 12
Кулоновское взаимодействие - Сильное 12
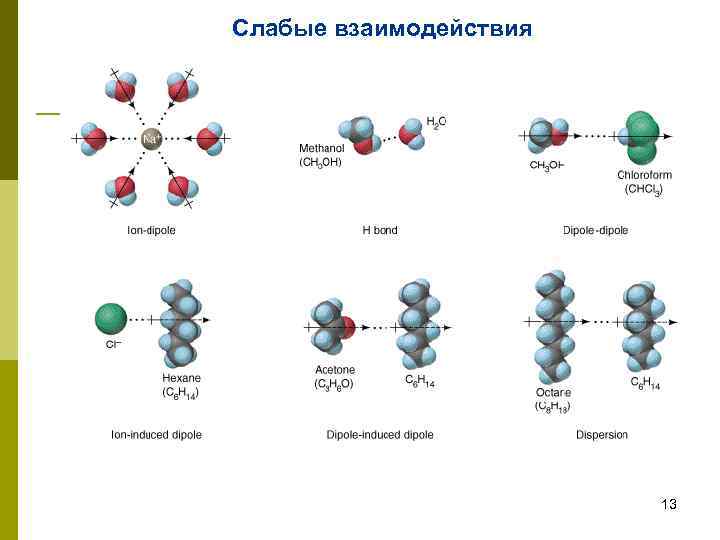 Слабые взаимодействия 13
Слабые взаимодействия 13
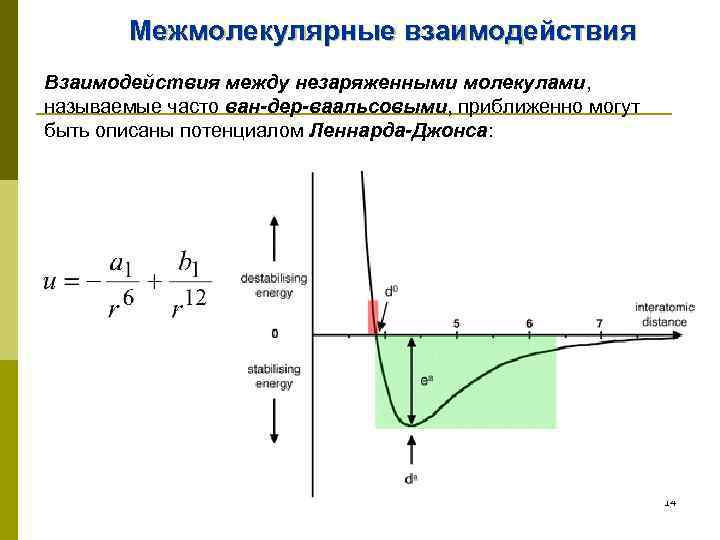 Межмолекулярные взаимодействия Взаимодействия между незаряженными молекулами, называемые часто ван-дер-ваальсовыми, приближенно могут быть описаны потенциалом Леннарда-Джонса: 14
Межмолекулярные взаимодействия Взаимодействия между незаряженными молекулами, называемые часто ван-дер-ваальсовыми, приближенно могут быть описаны потенциалом Леннарда-Джонса: 14
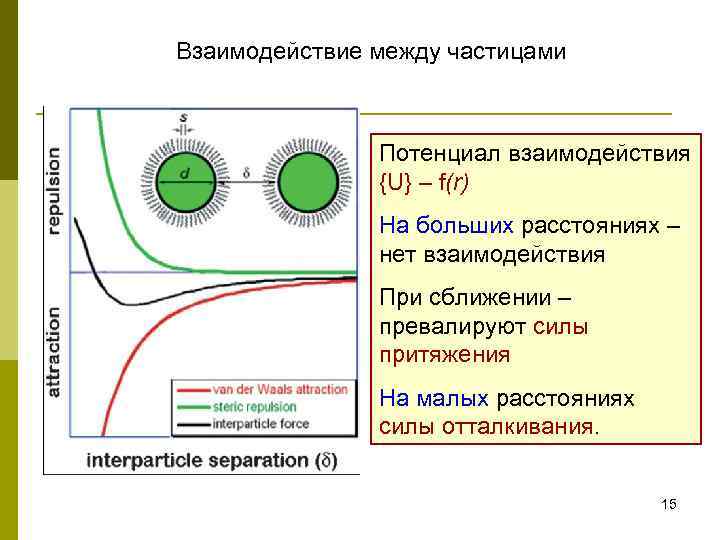 Взаимодействие между частицами Потенциал взаимодействия {U} – f(r) На больших расстояниях – нет взаимодействия При сближении – превалируют силы притяжения На малых расстояниях силы отталкивания. 15
Взаимодействие между частицами Потенциал взаимодействия {U} – f(r) На больших расстояниях – нет взаимодействия При сближении – превалируют силы притяжения На малых расстояниях силы отталкивания. 15
 Дальнодействующие силы - Электростатические силы Наличие у молекул постоянных дипольных моментов (монополь, диполь, квадруполь) Средний потенциал взаимодействия диполей 16
Дальнодействующие силы - Электростатические силы Наличие у молекул постоянных дипольных моментов (монополь, диполь, квадруполь) Средний потенциал взаимодействия диполей 16
 Влияние полярного растворителя Диссоциация Сольватация Природа взаимодействия – водородные связи
Влияние полярного растворителя Диссоциация Сольватация Природа взаимодействия – водородные связи
 Индукционное взаимодействие «постоянный диполь – наведенный диполь» Все молекулы поляризуются при наложении электрического поля. ( нейтральная частица + диполь) Величина индуцированного диполя определяется поляризуемостью вещества χ 18
Индукционное взаимодействие «постоянный диполь – наведенный диполь» Все молекулы поляризуются при наложении электрического поля. ( нейтральная частица + диполь) Величина индуцированного диполя определяется поляризуемостью вещества χ 18
 Дисперсионное взаимодействие «мгновенный диполь – наведенный диполь» Квантовые флуктуации заряда в нейтральных молекулах – силы Лондона 19
Дисперсионное взаимодействие «мгновенный диполь – наведенный диполь» Квантовые флуктуации заряда в нейтральных молекулах – силы Лондона 19
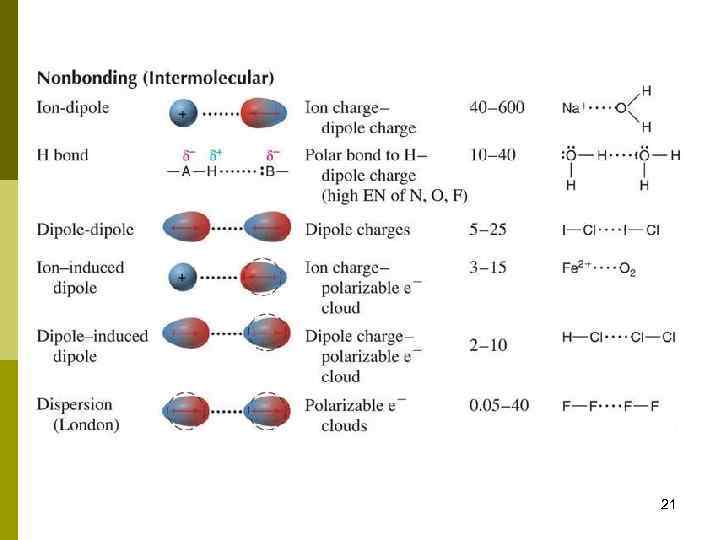
 Силы Ван-дер-Ваальса E = 0. 4 - 4. 0 k. J/mol Электростатические силы – между диполями Индукционные силы- между диполем и незаряженной частицей Дисперсионные силы – между незаряженными частицами 20
Силы Ван-дер-Ваальса E = 0. 4 - 4. 0 k. J/mol Электростатические силы – между диполями Индукционные силы- между диполем и незаряженной частицей Дисперсионные силы – между незаряженными частицами 20
 21
21
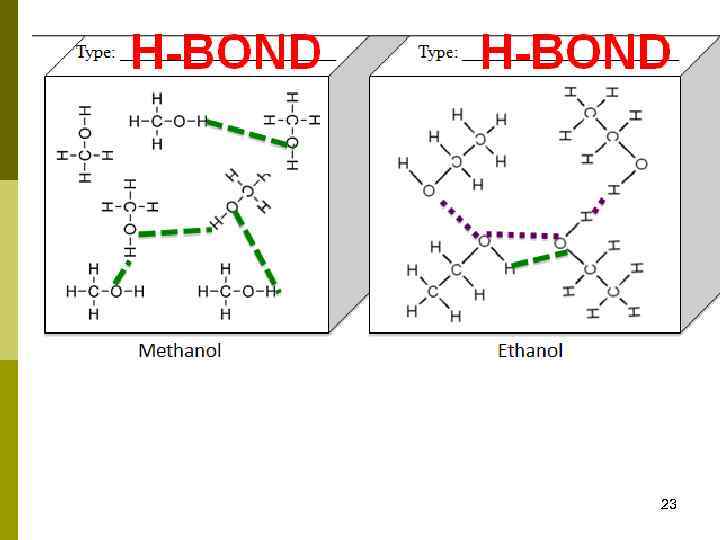
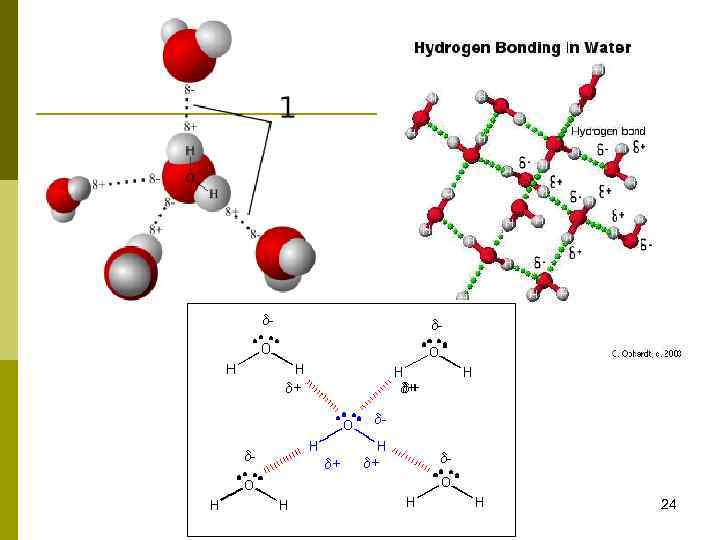
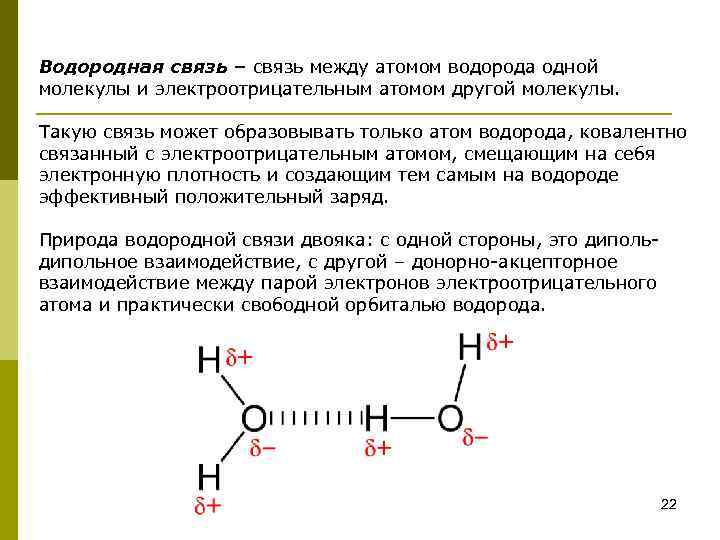 Водородная связь – связь между атомом водорода одной молекулы и электроотрицательным атомом другой молекулы. Такую связь может образовывать только атом водорода, ковалентно связанный с электроотрицательным атомом, смещающим на себя электронную плотность и создающим тем самым на водороде эффективный положительный заряд. Природа водородной связи двояка: с одной стороны, это дипольное взаимодействие, с другой – донорно-акцепторное взаимодействие между парой электронов электроотрицательного атома и практически свободной орбиталью водорода. 22
Водородная связь – связь между атомом водорода одной молекулы и электроотрицательным атомом другой молекулы. Такую связь может образовывать только атом водорода, ковалентно связанный с электроотрицательным атомом, смещающим на себя электронную плотность и создающим тем самым на водороде эффективный положительный заряд. Природа водородной связи двояка: с одной стороны, это дипольное взаимодействие, с другой – донорно-акцепторное взаимодействие между парой электронов электроотрицательного атома и практически свободной орбиталью водорода. 22
 23
23
 24
24
 25
25
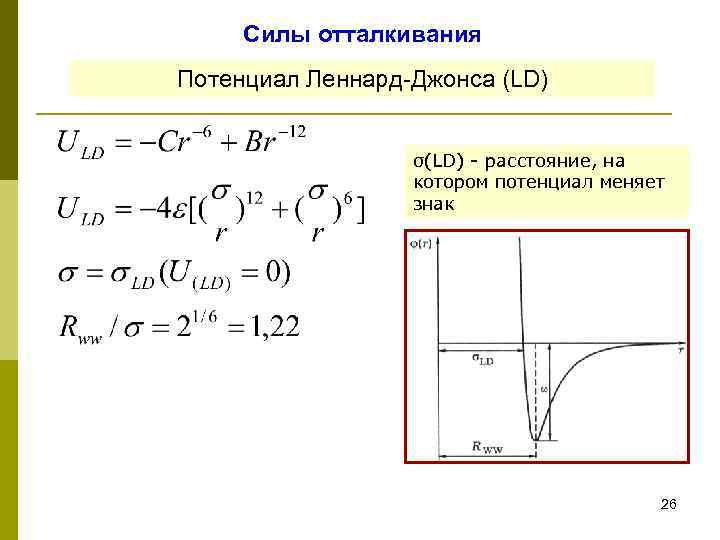 Силы отталкивания Потенциал Леннард-Джонса (LD) σ(LD) - расстояние, на котором потенциал меняет знак 26
Силы отталкивания Потенциал Леннард-Джонса (LD) σ(LD) - расстояние, на котором потенциал меняет знак 26
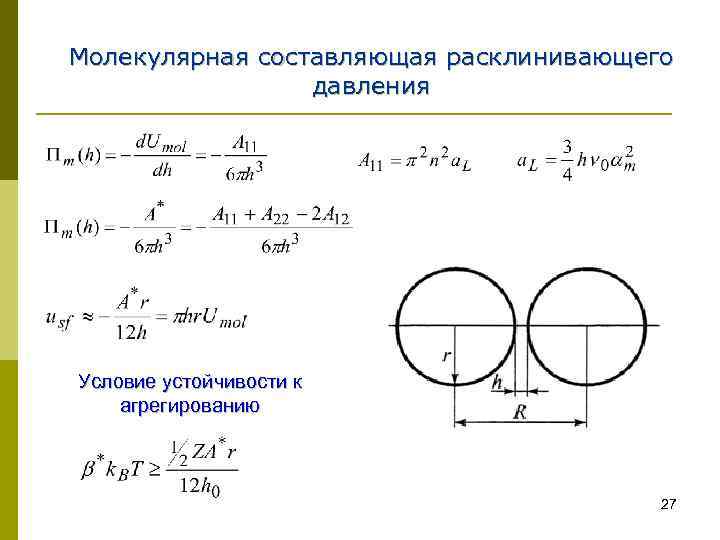 Молекулярная составляющая расклинивающего давления Условие устойчивости к агрегированию 27
Молекулярная составляющая расклинивающего давления Условие устойчивости к агрегированию 27
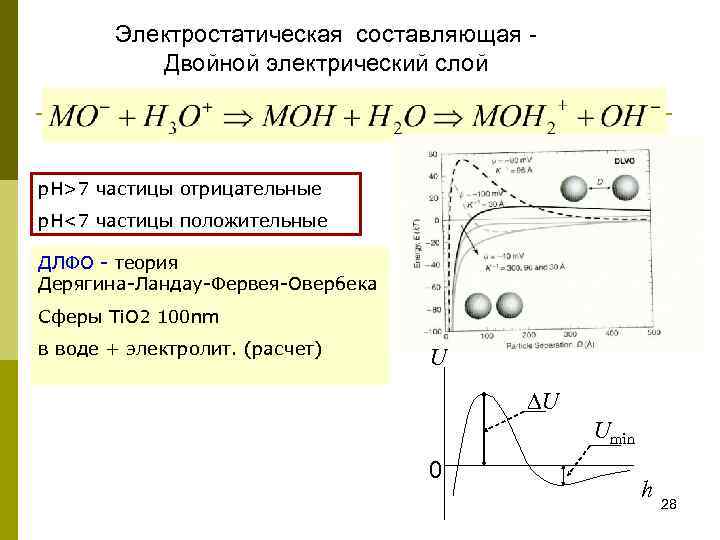 Электростатическая составляющая - Двойной электрический слой p. H>7 частицы отрицательные p. H<7 частицы положительные ДЛФО - теория Дерягина-Ландау-Фервея-Овербека Сферы Ti. O 2 100 nm в воде + электролит. (расчет) U DU Umin 0 h 28
Электростатическая составляющая - Двойной электрический слой p. H>7 частицы отрицательные p. H<7 частицы положительные ДЛФО - теория Дерягина-Ландау-Фервея-Овербека Сферы Ti. O 2 100 nm в воде + электролит. (расчет) U DU Umin 0 h 28
 29
29
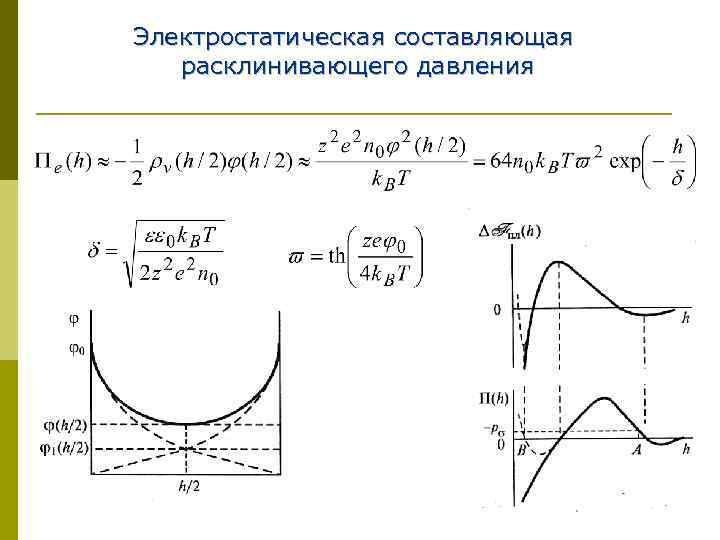 Электростатическая составляющая расклинивающего давления 30
Электростатическая составляющая расклинивающего давления 30
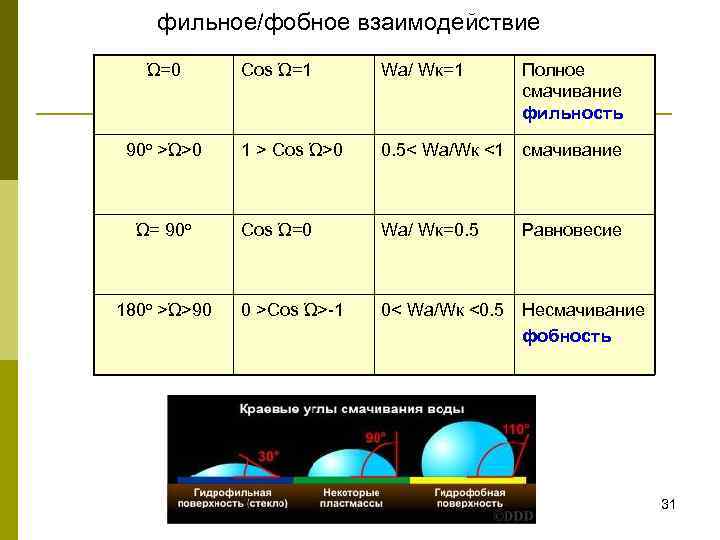 фильное/фобное взаимодействие Ώ=0 90 o >Ώ>0 Ώ= 90 o 180 o >Ώ>90 Cos Ώ=1 Wa/ Wк=1 Полное смачивание фильность 1 > Cos Ώ>0 0. 5< Wa/Wк <1 смачивание Cos Ώ=0 Wa/ Wк=0. 5 0 >Cos Ώ>-1 0< Wa/Wк <0. 5 Несмачивание фобность Равновесие 31
фильное/фобное взаимодействие Ώ=0 90 o >Ώ>0 Ώ= 90 o 180 o >Ώ>90 Cos Ώ=1 Wa/ Wк=1 Полное смачивание фильность 1 > Cos Ώ>0 0. 5< Wa/Wк <1 смачивание Cos Ώ=0 Wa/ Wк=0. 5 0 >Cos Ώ>-1 0< Wa/Wк <0. 5 Несмачивание фобность Равновесие 31
 Гидрофобное взаимодействие Притяжение гидрофобных частиц в воде Потенциал молекулы воды резко повышается при условии отсутствия водородных связей. Только на некотором расстоянии от неполярной молекулы возмущение потенциала снимается. Радиус действия 2 нм. Природа - снижение плотности молекул воды между частицами. 32
Гидрофобное взаимодействие Притяжение гидрофобных частиц в воде Потенциал молекулы воды резко повышается при условии отсутствия водородных связей. Только на некотором расстоянии от неполярной молекулы возмущение потенциала снимается. Радиус действия 2 нм. Природа - снижение плотности молекул воды между частицами. 32
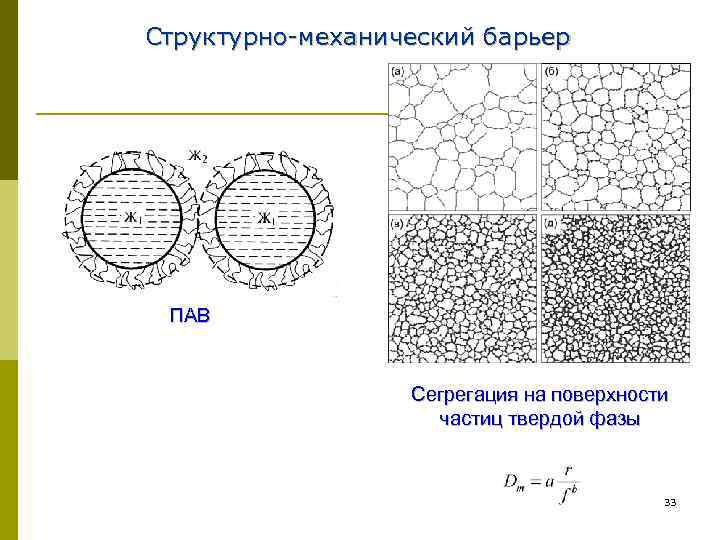 Структурно-механический барьер ПАВ Сегрегация на поверхности частиц твердой фазы 33
Структурно-механический барьер ПАВ Сегрегация на поверхности частиц твердой фазы 33


