лекция_5 биология.ppt
- Количество слайдов: 22
 Лекция 5. Синтез ДНК. Нарушения в структуре ДНК. Репарация ДНК.
Лекция 5. Синтез ДНК. Нарушения в структуре ДНК. Репарация ДНК.
 Принципы репликации: n n n матричность и комплементарность антипараллельность униполярность прерывистость полуконсервативность (М. Мезелсон, Ф. Сталь, 1958) Возможный механизм репликации предложили Ф. Крик и Дж. Уотсон, 1953 г. А. Корнберг, 1957, открытие ДНК-полимеразы I
Принципы репликации: n n n матричность и комплементарность антипараллельность униполярность прерывистость полуконсервативность (М. Мезелсон, Ф. Сталь, 1958) Возможный механизм репликации предложили Ф. Крик и Дж. Уотсон, 1953 г. А. Корнберг, 1957, открытие ДНК-полимеразы I
 Условия репликации матрица n ферменты (реплисома n многокомпонентный белковый комплекс, осуществляющий двунаправленный синтез ДНК) d. NTP (дезоксирибонуклеозидтрифосфаты) n Mg 2+ n ATP n NTP (для синтеза олигорибонуклеотидов - праймеров) n
Условия репликации матрица n ферменты (реплисома n многокомпонентный белковый комплекс, осуществляющий двунаправленный синтез ДНК) d. NTP (дезоксирибонуклеозидтрифосфаты) n Mg 2+ n ATP n NTP (для синтеза олигорибонуклеотидов - праймеров) n
 Способы репликации n (тета) – тип n (сигма) – тип n репликация линейных молекул
Способы репликации n (тета) – тип n (сигма) – тип n репликация линейных молекул
 инициация → элонгация → терминация q точка Ori, от англ. Origin q репликон q скорость репликации: • прокариоты: 1500 пн/сек • эукариоты: 10 -100 пн/сек q (d. NMP)n + d. NTP → (d. NMP)n+1 + P-P q
инициация → элонгация → терминация q точка Ori, от англ. Origin q репликон q скорость репликации: • прокариоты: 1500 пн/сек • эукариоты: 10 -100 пн/сек q (d. NMP)n + d. NTP → (d. NMP)n+1 + P-P q
 Инициация репликации инициаторные белки DNA A, В, С… n АТР-зависимая ДНК-геликаза n SSB – белки n ДНК-топоизомераза n
Инициация репликации инициаторные белки DNA A, В, С… n АТР-зависимая ДНК-геликаза n SSB – белки n ДНК-топоизомераза n
 Элонгация репликации праймаза, праймосома, праймер n ДНК-полимеразы n фрагменты Оказаки n ДНК-лигаза n
Элонгация репликации праймаза, праймосома, праймер n ДНК-полимеразы n фрагменты Оказаки n ДНК-лигаза n
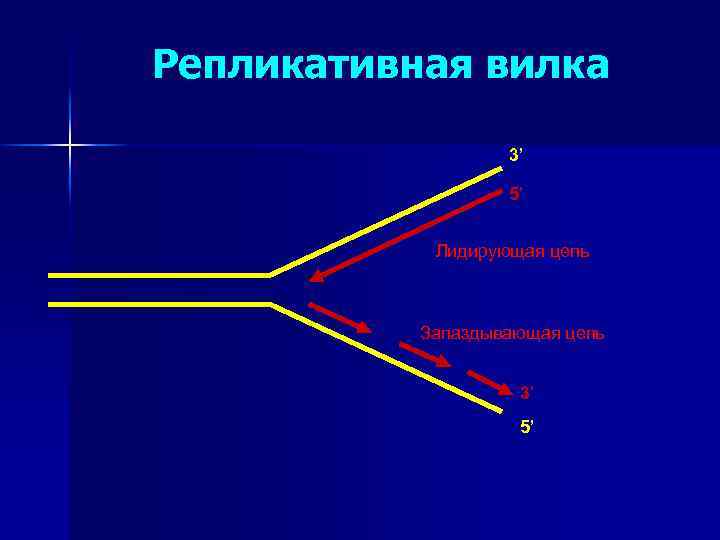 Репликативная вилка 3’ 5’ Лидирующая цепь Запаздывающая цепь 3’ 5’
Репликативная вилка 3’ 5’ Лидирующая цепь Запаздывающая цепь 3’ 5’
 ДНК-полимеразы прокариот ДНК-полимераза I ü ü ü 3’-экзонуклеаза конец, фрагмент Кленова) 5’- экзонуклеаза -конец) одиночный полипептид ДНК-полимераза III (С- ü ü (N ü ü основной фермент элогнации 3’-экзонуклеаза высокое сродство к матрице (процессивность в 60 раз выше, чем у ДНКполимеразы I) много субъединиц
ДНК-полимеразы прокариот ДНК-полимераза I ü ü ü 3’-экзонуклеаза конец, фрагмент Кленова) 5’- экзонуклеаза -конец) одиночный полипептид ДНК-полимераза III (С- ü ü (N ü ü основной фермент элогнации 3’-экзонуклеаза высокое сродство к матрице (процессивность в 60 раз выше, чем у ДНКполимеразы I) много субъединиц
 Репликация у эукариот q q q • • • много репликонов, их длина 20 -300 т. п. н. в S-фазе клеточного цикла ДНК-полимеразы: α – основной фермент (полимераза, праймаза), синтез фрагментов Оказаки (или только праймаза? ) β - фермент репарации γ - синтез мтх. ДНК δ - синтез лидирующей цепи - при репарации замещает
Репликация у эукариот q q q • • • много репликонов, их длина 20 -300 т. п. н. в S-фазе клеточного цикла ДНК-полимеразы: α – основной фермент (полимераза, праймаза), синтез фрагментов Оказаки (или только праймаза? ) β - фермент репарации γ - синтез мтх. ДНК δ - синтез лидирующей цепи - при репарации замещает
 Репликация у эукариот q ь q q факторы репликации: факторы FEN-1 или MF-1 обладают активностью 5’→ 3’-экзонуклеазы и участвуют в созревании фрагментов Оказаки. Для удаления праймеров также используется РНКаза H 1 длина фрагментов Оказаки 100 -200 н. теломераза
Репликация у эукариот q ь q q факторы репликации: факторы FEN-1 или MF-1 обладают активностью 5’→ 3’-экзонуклеазы и участвуют в созревании фрагментов Оказаки. Для удаления праймеров также используется РНКаза H 1 длина фрагментов Оказаки 100 -200 н. теломераза
 Теломераза 1971 г. , А. М. Оловников, предсказал механизм защиты хромосом от укорачивания при каждом делении клетки 1984 г. , К. Грейдер – открытие теломеразы 2009 г. , К. Грейдер, Э. Блекберн, Д. Шостак – Нобелевская премия рибозим, 150 н. РНК удлиняет 3’ конец матрицы ДНК
Теломераза 1971 г. , А. М. Оловников, предсказал механизм защиты хромосом от укорачивания при каждом делении клетки 1984 г. , К. Грейдер – открытие теломеразы 2009 г. , К. Грейдер, Э. Блекберн, Д. Шостак – Нобелевская премия рибозим, 150 н. РНК удлиняет 3’ конец матрицы ДНК
 Регуляция репликации n n n сфингозин – в малых дозах стимулирует, в больших – подавляет синтез ДНК рифампицин и актиномицин D блокируют репликацию ингибиторы гираз (ДНК-топоизомераз)
Регуляция репликации n n n сфингозин – в малых дозах стимулирует, в больших – подавляет синтез ДНК рифампицин и актиномицин D блокируют репликацию ингибиторы гираз (ДНК-топоизомераз)
 Полимеразная цепная реакция n n 1983 г. К. Мюллис (1993 г. – Нобелевская премия) В основе – принципы и механизмы естественной репликации ДНК. Позволяет амплифицировать (многократно увеличить количество копий, клонировать) in vitro фрагмент ДНК с известной последовательностью нуклеотидов. Амплификатор, термоциклер
Полимеразная цепная реакция n n 1983 г. К. Мюллис (1993 г. – Нобелевская премия) В основе – принципы и механизмы естественной репликации ДНК. Позволяет амплифицировать (многократно увеличить количество копий, клонировать) in vitro фрагмент ДНК с известной последовательностью нуклеотидов. Амплификатор, термоциклер
 Применение ПЦР n ь ь ь n Используется: в диагностике инфекционных заболеваний для определения генотипа организма для изучения экспрессии генов для идентификации личности для установления родственных связей в молекулярно-биологических и молекулярно-генетических исследованиях с помощью ПЦР удалось амплифицировать фрагменты мтх. ДНК из ископаемых останков мозга человека возраста 7 тысяч лет
Применение ПЦР n ь ь ь n Используется: в диагностике инфекционных заболеваний для определения генотипа организма для изучения экспрессии генов для идентификации личности для установления родственных связей в молекулярно-биологических и молекулярно-генетических исследованиях с помощью ПЦР удалось амплифицировать фрагменты мтх. ДНК из ископаемых останков мозга человека возраста 7 тысяч лет
 Master. Mix n n n n праймер R праймер L буфер 10 х смесь d. NTP матрица (ДНК) вода деионизированная ДНК-полимераза (Taq-полимераза) вазелиновое масло
Master. Mix n n n n праймер R праймер L буфер 10 х смесь d. NTP матрица (ДНК) вода деионизированная ДНК-полимераза (Taq-полимераза) вазелиновое масло
 Полимеразы для ПЦР n Taq – полимераза (Thermus aquaticus, обитает в горячих источниках), лишена 3’-экзонуклеазной автивности n Pfu-полимераза (Pyrococcus furiosus, ( «яростные огненные шарики» , экстремально термофильные бактерии, до 103°С), обладает 3’-экзонуклеазной автивностью, но низкой процессивностью
Полимеразы для ПЦР n Taq – полимераза (Thermus aquaticus, обитает в горячих источниках), лишена 3’-экзонуклеазной автивности n Pfu-полимераза (Pyrococcus furiosus, ( «яростные огненные шарики» , экстремально термофильные бактерии, до 103°С), обладает 3’-экзонуклеазной автивностью, но низкой процессивностью
 Каждый цикл ПЦР включает 3 этапа: 1. Денатурация (плавление) t 92 -95°С 2. Отжиг с праймерами t 50 -60°C 3. Полимеризация (элонгация) t 72°
Каждый цикл ПЦР включает 3 этапа: 1. Денатурация (плавление) t 92 -95°С 2. Отжиг с праймерами t 50 -60°C 3. Полимеризация (элонгация) t 72°
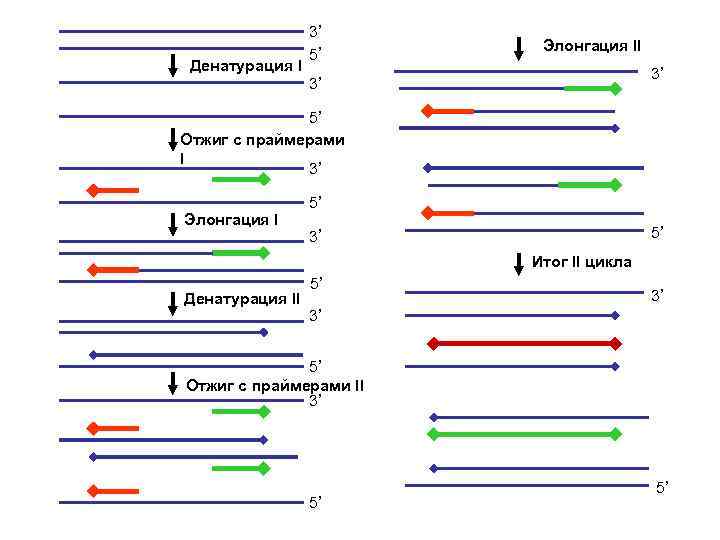 Денатурация I 3’ 5’ Элонгация II 3’ 3’ 5’ Отжиг с праймерами I 3’ Элонгация I 5’ 5’ 3’ Итог II цикла Денатурация II 5’ 3’ 3’ 5’ Отжиг с праймерами II 3’ 5’ 5’
Денатурация I 3’ 5’ Элонгация II 3’ 3’ 5’ Отжиг с праймерами I 3’ Элонгация I 5’ 5’ 3’ Итог II цикла Денатурация II 5’ 3’ 3’ 5’ Отжиг с праймерами II 3’ 5’ 5’
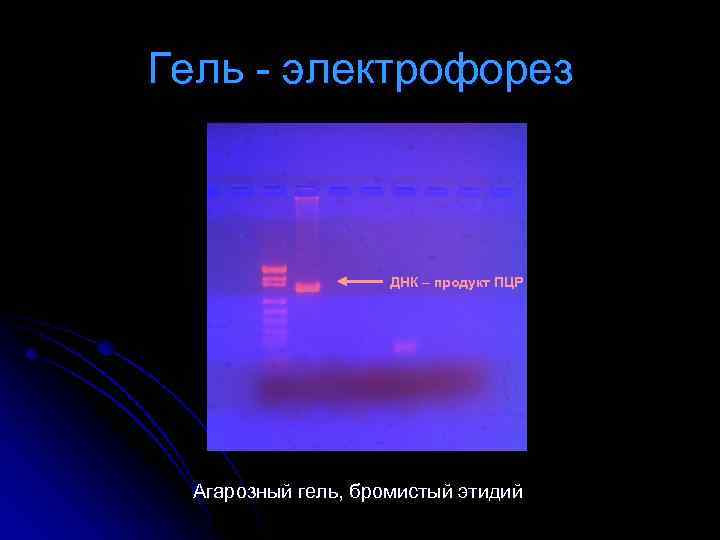 Гель - электрофорез ДНК – продукт ПЦР Агарозный гель, бромистый этидий
Гель - электрофорез ДНК – продукт ПЦР Агарозный гель, бромистый этидий
 Разновидности ПЦР n «Вложенная» ПЦР (Nested PCR) – c используется вторая пара праймеров, , с помощь которой амплифицируется полученный ранее ампликон n RT-PCR (Reverse Transcription PCR, ПЦР с обратной транскрипцией). Для изучения экспрессии генов. РНК → ДНК → ПЦР. n Ассиметричная ПЦР (Аssimetric PCR) – для амплификации преимущественно одной цепи; используют разные количества праймеров n ПЦР длинных фрагментов (Long-range PCR) для амплификации фрагментов более 10 т. п. н. Используют две полимеразы (Taq и Pfu).
Разновидности ПЦР n «Вложенная» ПЦР (Nested PCR) – c используется вторая пара праймеров, , с помощь которой амплифицируется полученный ранее ампликон n RT-PCR (Reverse Transcription PCR, ПЦР с обратной транскрипцией). Для изучения экспрессии генов. РНК → ДНК → ПЦР. n Ассиметричная ПЦР (Аssimetric PCR) – для амплификации преимущественно одной цепи; используют разные количества праймеров n ПЦР длинных фрагментов (Long-range PCR) для амплификации фрагментов более 10 т. п. н. Используют две полимеразы (Taq и Pfu).
 Разновидности ПЦР n Количественная ПЦР в реальном времени (Quantitative real -time PCR) c использованием флуоресцентно меченых атомов, позволяющая отслеживать количество наработанного продукта в каждом цикле ПЦР в реальном времени n Multiplex PCR – при использовании нескольких пар праймеров одновременная амплификация несколькоких фрагментов
Разновидности ПЦР n Количественная ПЦР в реальном времени (Quantitative real -time PCR) c использованием флуоресцентно меченых атомов, позволяющая отслеживать количество наработанного продукта в каждом цикле ПЦР в реальном времени n Multiplex PCR – при использовании нескольких пар праймеров одновременная амплификация несколькоких фрагментов


