 Лекция № 5 Растворы электролитов
Лекция № 5 Растворы электролитов
 Возьмем 0, 1 моляльные растворы СO(NH 2)2, CH 3 COOH, Na. NO 3, KCl Трасч = Ккр Сm = 1, 86 ∙ 0, 1 = 0, 186 Tэксп : 0, 186 i=1 0, 190 0, 353 0, 340 i = Tэксп / Трасч i>1
Возьмем 0, 1 моляльные растворы СO(NH 2)2, CH 3 COOH, Na. NO 3, KCl Трасч = Ккр Сm = 1, 86 ∙ 0, 1 = 0, 186 Tэксп : 0, 186 i=1 0, 190 0, 353 0, 340 i = Tэксп / Трасч i>1
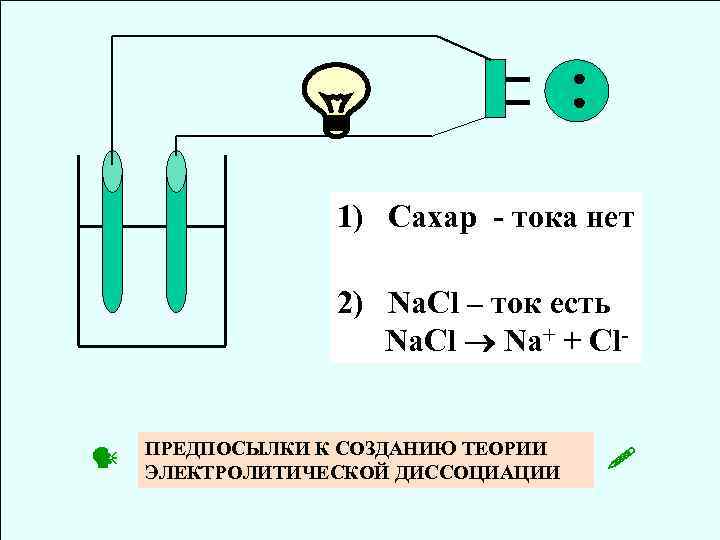 1) Сахар тока нет 2) Na. Cl – ток есть Na. Cl Na+ + Cl ПРЕДПОСЫЛКИ К СОЗДАНИЮ ТЕОРИИ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ
1) Сахар тока нет 2) Na. Cl – ток есть Na. Cl Na+ + Cl ПРЕДПОСЫЛКИ К СОЗДАНИЮ ТЕОРИИ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ
 Теория электролитической диссоциации Причины электролитической диссоциации Ослабление кулонов ского взаимодействия частиц вещества за счет высокой диэлектрической проницаемости р ля Ионизация молекул в растворе как следствие их взаимодействия с полярными молекулами Н 2 О z+ z─ F = - k ——— r 2 Na. OH Na+ + OH (H 2 O) = 81 H 2 SO 4 2 H++(SO 4)2 диэлектрическая проницаемость среды HCl H++Cl
Теория электролитической диссоциации Причины электролитической диссоциации Ослабление кулонов ского взаимодействия частиц вещества за счет высокой диэлектрической проницаемости р ля Ионизация молекул в растворе как следствие их взаимодействия с полярными молекулами Н 2 О z+ z─ F = - k ——— r 2 Na. OH Na+ + OH (H 2 O) = 81 H 2 SO 4 2 H++(SO 4)2 диэлектрическая проницаемость среды HCl H++Cl
 Следствие из закона Рауля для электролитов Tкип = i Kэб. Cm Tкр = i Kкр Cm Tэксп i = ———— Трасч i 1 lim i = n C 0 HCl n 2 Fe(NO 3)3 Al 2(SO 4)3 4 5 вещества неэлектролиты не проводят эл. ток оксиды, орг. в-ва электролиты проводят эл. ток соли, к-ты, основания
Следствие из закона Рауля для электролитов Tкип = i Kэб. Cm Tкр = i Kкр Cm Tэксп i = ———— Трасч i 1 lim i = n C 0 HCl n 2 Fe(NO 3)3 Al 2(SO 4)3 4 5 вещества неэлектролиты не проводят эл. ток оксиды, орг. в-ва электролиты проводят эл. ток соли, к-ты, основания
 Степень электролитической диссоциации = Nдис = N Сдис Собщ 0 100 % Для слабых электролитов = 0, i = 1 Связь и i i = 1 +α (n 1) i 1 α = ——— n 1
Степень электролитической диссоциации = Nдис = N Сдис Собщ 0 100 % Для слабых электролитов = 0, i = 1 Связь и i i = 1 +α (n 1) i 1 α = ——— n 1
 Слабые и сильные электролиты слабые 0 3% средней силы 3 % 30 % 1. H 2 O 2. Кислоты H 2 CO 3, H 2 S, HCN, HNO 3 CH 3 COOH 3. Основания, NH 4 OH 4. Некоторые соли сильные 30 % 100 % 1. Кислоты: H 2 SO 4, HNO 3, HCl, HBr, HI, HCl. O 4 2. Основания: Li. OH, Na. OH … Ca(OH)2, Sr(OH)2, Ba(OH)2 3. Все соли
Слабые и сильные электролиты слабые 0 3% средней силы 3 % 30 % 1. H 2 O 2. Кислоты H 2 CO 3, H 2 S, HCN, HNO 3 CH 3 COOH 3. Основания, NH 4 OH 4. Некоторые соли сильные 30 % 100 % 1. Кислоты: H 2 SO 4, HNO 3, HCl, HBr, HI, HCl. O 4 2. Основания: Li. OH, Na. OH … Ca(OH)2, Sr(OH)2, Ba(OH)2 3. Все соли
 Факторы, влияющие на степень электролитической диссоциации 1. Природа растворенного вещества 2. Природа растворителя 3. Т 4. С C ростом Т значение увеличивается АВ А+ + В , Н > 0 (эндо ) При уменьшении С (при разбавлении) значение растет ( 1, когда V ) 5. Одноименные ионы NH 4 H 2 O NH 4 + OH NH 4+ +NH 4 Cl Введение одноименного иона в растворе подавляет диссоциацию
Факторы, влияющие на степень электролитической диссоциации 1. Природа растворенного вещества 2. Природа растворителя 3. Т 4. С C ростом Т значение увеличивается АВ А+ + В , Н > 0 (эндо ) При уменьшении С (при разбавлении) значение растет ( 1, когда V ) 5. Одноименные ионы NH 4 H 2 O NH 4 + OH NH 4+ +NH 4 Cl Введение одноименного иона в растворе подавляет диссоциацию
 6. Связывание ионов H 2 S 2 H+ + S 2 Cu 2+ + S 2 = Cu. S При связывании ионов диссоциация усиливается
6. Связывание ионов H 2 S 2 H+ + S 2 Cu 2+ + S 2 = Cu. S При связывании ионов диссоциация усиливается
 Cпособы определения степени электролитической диссоциации 1. Способ основан на измерении Ткип или Тзам раствора АВ А+ + В N(1 ) N N Т эксп i = ———— Трасч i 1 = ——— n 1 n – число ионов из одной молекулы
Cпособы определения степени электролитической диссоциации 1. Способ основан на измерении Ткип или Тзам раствора АВ А+ + В N(1 ) N N Т эксп i = ———— Трасч i 1 = ——— n 1 n – число ионов из одной молекулы
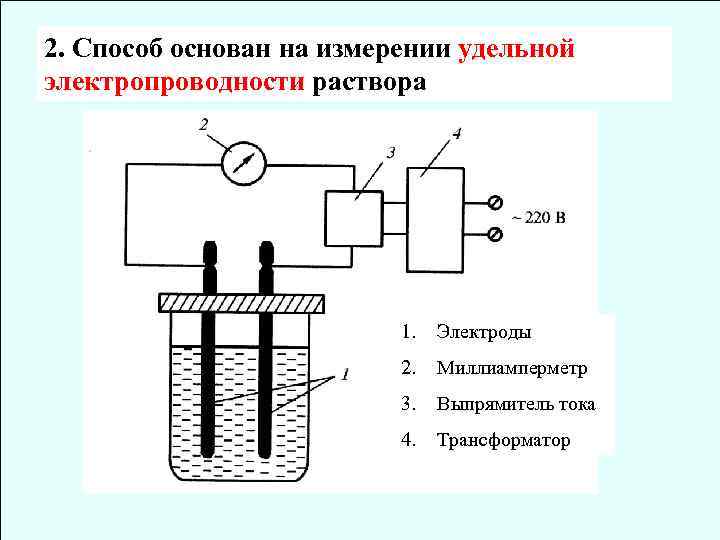 2. Способ основан на измерении удельной электропроводности раствора 1. Электроды 2. Миллиамперметр 3. Выпрямитель тока 4. Трансформатор
2. Способ основан на измерении удельной электропроводности раствора 1. Электроды 2. Миллиамперметр 3. Выпрямитель тока 4. Трансформатор
 Удельная электропроводность раствора æ (ом 1 · см 1) Молярная электропроводность (ом 1 · см 1 · моль 1) = æ V 1000 V = ——— C V – разбавление, моль 1 C – молярная концентрация , моль/л = ——— электропроводность бесконечно разбавленного раствора
Удельная электропроводность раствора æ (ом 1 · см 1) Молярная электропроводность (ом 1 · см 1 · моль 1) = æ V 1000 V = ——— C V – разбавление, моль 1 C – молярная концентрация , моль/л = ——— электропроводность бесконечно разбавленного раствора
![Свойства растворов слабых электролитов Константа диссоциации T = const HCN H+ + CN─ [H+] Свойства растворов слабых электролитов Константа диссоциации T = const HCN H+ + CN─ [H+]](https://present5.com/presentation/3/26150394_158453249.pdf-img/26150394_158453249.pdf-13.jpg) Свойства растворов слабых электролитов Константа диссоциации T = const HCN H+ + CN─ [H+] [CN─] Kд = ————— = 5 ∙ 10 -10 [HCN] Значения Kд табулированы СН 3 СООН СН 3 СОO- + H+ [СН 3 СОО─] H+] Kд = ———— = 2 ∙ 10 -5 [СН 3 СООН] HCl = H+ + Cl─ [H+] [Cl─] Kд = ————— [HCl]
Свойства растворов слабых электролитов Константа диссоциации T = const HCN H+ + CN─ [H+] [CN─] Kд = ————— = 5 ∙ 10 -10 [HCN] Значения Kд табулированы СН 3 СООН СН 3 СОO- + H+ [СН 3 СОО─] H+] Kд = ———— = 2 ∙ 10 -5 [СН 3 СООН] HCl = H+ + Cl─ [H+] [Cl─] Kд = ————— [HCl]
![Ступенчатая диссоциация H 2 S H+ + HS─ [H+] [HS─] Kд = ————— 10 Ступенчатая диссоциация H 2 S H+ + HS─ [H+] [HS─] Kд = ————— 10](https://present5.com/presentation/3/26150394_158453249.pdf-img/26150394_158453249.pdf-14.jpg) Ступенчатая диссоциация H 2 S H+ + HS─ [H+] [HS─] Kд = ————— 10 7 [H 2 S] HS─ H+ + S 2─ [H+] [S 2─] K д= ————— 10 13 [HS ] K 1 > K 2 > …
Ступенчатая диссоциация H 2 S H+ + HS─ [H+] [HS─] Kд = ————— 10 7 [H 2 S] HS─ H+ + S 2─ [H+] [S 2─] K д= ————— 10 13 [HS ] K 1 > K 2 > …
 Закон оазбавлени Оствальда ( для слабых бинарных электролитов) HCN H+ + CNС(1 - ) С С С • С С 2 Kд = ———— = ——— C(1 - ) 1 - 1 Kд = C 2 = Kд / C
Закон оазбавлени Оствальда ( для слабых бинарных электролитов) HCN H+ + CNС(1 - ) С С С • С С 2 Kд = ———— = ——— C(1 - ) 1 - 1 Kд = C 2 = Kд / C
 Диссоциация воды Водородный показатель
Диссоциация воды Водородный показатель
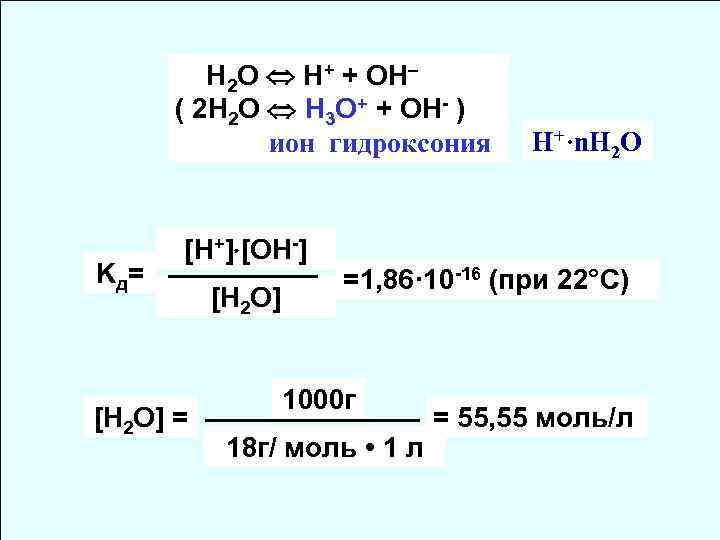 H 2 O H+ + OH– ( 2 H 2 O H 3 O+ + OH- ) ион гидроксония Kд = [H+] [OH-] [H 2 O] = [H 2 O] Н+·n. H 2 O =1, 86· 10 -16 (при 22°С) 1000 г 18 г/ моль • 1 л = 55, 55 моль/л
H 2 O H+ + OH– ( 2 H 2 O H 3 O+ + OH- ) ион гидроксония Kд = [H+] [OH-] [H 2 O] = [H 2 O] Н+·n. H 2 O =1, 86· 10 -16 (при 22°С) 1000 г 18 г/ моль • 1 л = 55, 55 моль/л
![Ионное произведение воды К Н 2 О = Кд ·[Н 2 О] = [Н+ Ионное произведение воды К Н 2 О = Кд ·[Н 2 О] = [Н+](https://present5.com/presentation/3/26150394_158453249.pdf-img/26150394_158453249.pdf-18.jpg) Ионное произведение воды К Н 2 О = Кд ·[Н 2 О] = [Н+ ] · [ОН ] = =1, 86 · 10 16 · 55, 55 = 10 14 КН 2 О = [Н+ ] ·[ОН ] = 10 14 Т, С КН 2 О 0 0, 12 10 14 22 100 1 10 14 75 10 14 [ Н+] = [ ОН ] = 10 7 моль/л в чистой воде
Ионное произведение воды К Н 2 О = Кд ·[Н 2 О] = [Н+ ] · [ОН ] = =1, 86 · 10 16 · 55, 55 = 10 14 КН 2 О = [Н+ ] ·[ОН ] = 10 14 Т, С КН 2 О 0 0, 12 10 14 22 100 1 10 14 75 10 14 [ Н+] = [ ОН ] = 10 7 моль/л в чистой воде
![Добавим в раствор кислоту: Чистая вода Добавим в раствор щелочь: [Н+] >10 7 (~10 Добавим в раствор кислоту: Чистая вода Добавим в раствор щелочь: [Н+] >10 7 (~10](https://present5.com/presentation/3/26150394_158453249.pdf-img/26150394_158453249.pdf-19.jpg) Добавим в раствор кислоту: Чистая вода Добавим в раствор щелочь: [Н+] >10 7 (~10 3) 10 7 <10 7 (~10 10) [OH ] <10 7 (~10 11) 10 7 >10 7 (~10 4) Кисл. Нейтр. Щел. Реакция среды
Добавим в раствор кислоту: Чистая вода Добавим в раствор щелочь: [Н+] >10 7 (~10 3) 10 7 <10 7 (~10 10) [OH ] <10 7 (~10 11) 10 7 >10 7 (~10 4) Кисл. Нейтр. Щел. Реакция среды
![Водородный показатель р. Н = lg Н+] р. ОН = lg ОН р. Н Водородный показатель р. Н = lg Н+] р. ОН = lg ОН р. Н](https://present5.com/presentation/3/26150394_158453249.pdf-img/26150394_158453249.pdf-20.jpg) Водородный показатель р. Н = lg Н+] р. ОН = lg ОН р. Н + р. ОН = 14 Нейтральный Н+ = ОН = 10 7; р. Н =7 Кислый Н+ 10 7 р. Н < 7 Щелочной Н+ < 10 7 р. Н 7 р. Н 0 кислая 7 щелочная 14
Водородный показатель р. Н = lg Н+] р. ОН = lg ОН р. Н + р. ОН = 14 Нейтральный Н+ = ОН = 10 7; р. Н =7 Кислый Н+ 10 7 р. Н < 7 Щелочной Н+ < 10 7 р. Н 7 р. Н 0 кислая 7 щелочная 14
 Методы определения р. Н 1. Инструментальный (р. Н метры) 2. C помощью индикаторов (лакмус, метиловый красный, фенолфталеин, метиловый оранжевый) 3. С помощью индикаторных бумажек р. Н 1 -3 4 -5 6 7 8 9 -10 11 -13 эталон цветов р. Н 4. Расчетные методы
Методы определения р. Н 1. Инструментальный (р. Н метры) 2. C помощью индикаторов (лакмус, метиловый красный, фенолфталеин, метиловый оранжевый) 3. С помощью индикаторных бумажек р. Н 1 -3 4 -5 6 7 8 9 -10 11 -13 эталон цветов р. Н 4. Расчетные методы
 Посмотрите на сайте кафедры дополнительный материал Лекция № 5 Основные положения теории электролитической диссоциации Ионные реакции Расчетные методы определения р. Н Примеры гидрометаллургических процессов, в которых р. Н среды имеет большое значение
Посмотрите на сайте кафедры дополнительный материал Лекция № 5 Основные положения теории электролитической диссоциации Ионные реакции Расчетные методы определения р. Н Примеры гидрометаллургических процессов, в которых р. Н среды имеет большое значение
 Лекция № 5 РАСТВОРЫ ЭЛЕКТРОЛИТОВ
Лекция № 5 РАСТВОРЫ ЭЛЕКТРОЛИТОВ
 ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕОРИИ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ 1. Электролиты при растворении в воде диссоциируют на ионы Na 2 SO 4 2 Na+ + SO 42 2. Ионы бывают: - простые - сложные - окрашенные - бесцветные Na+, Mg 2+ NO 3 , PO 43 Mn. O 4 , Cr 2 O 72 SO 42
ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕОРИИ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ 1. Электролиты при растворении в воде диссоциируют на ионы Na 2 SO 4 2 Na+ + SO 42 2. Ионы бывают: - простые - сложные - окрашенные - бесцветные Na+, Mg 2+ NO 3 , PO 43 Mn. O 4 , Cr 2 O 72 SO 42
 3. Свойства ионов отличаются от свойств простых веществ Na + H 2 O → Na. OH + H 2 Na+ + H 2 O → 4. Ионы более устойчивы, чем атомы Na: [Ne]3 s 1 Na+: [Ne]
3. Свойства ионов отличаются от свойств простых веществ Na + H 2 O → Na. OH + H 2 Na+ + H 2 O → 4. Ионы более устойчивы, чем атомы Na: [Ne]3 s 1 Na+: [Ne]
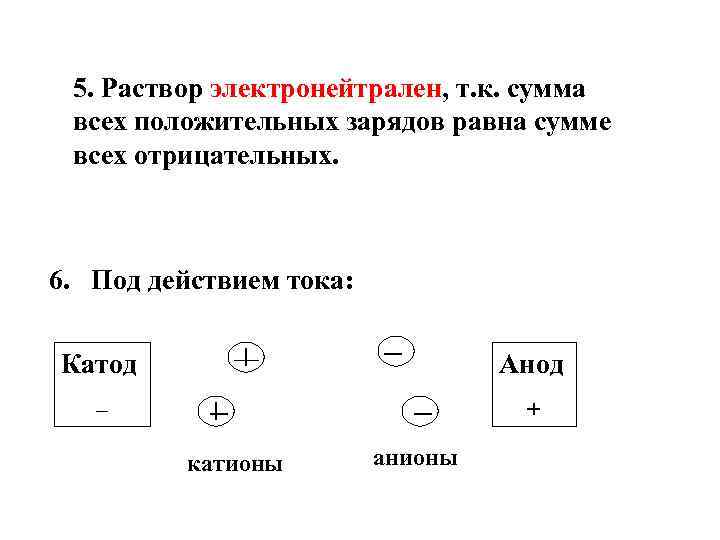 5. Раствор электронейтрален, т. к. сумма всех положительных зарядов равна сумме всех отрицательных. 6. Под действием тока: Катод Анод – + катионы анионы
5. Раствор электронейтрален, т. к. сумма всех положительных зарядов равна сумме всех отрицательных. 6. Под действием тока: Катод Анод – + катионы анионы
 7. Диссоциация – процесс обратимый КИСЛОТЫ HCl ↔ H+ + Cl H 2 SO 4 ↔ 2 H+ + SO 42 ОСНОВАНИЯ Na. OH ↔ Na+ + OH Ba(OH)2 ↔ Ba 2+ + 2 OH СОЛИ K 2 CO 3 ↔ 2 K+ + CO 3 2 Fe 2(SO 4)3 ↔ 2 Fe 3+ + 3 SO 42
7. Диссоциация – процесс обратимый КИСЛОТЫ HCl ↔ H+ + Cl H 2 SO 4 ↔ 2 H+ + SO 42 ОСНОВАНИЯ Na. OH ↔ Na+ + OH Ba(OH)2 ↔ Ba 2+ + 2 OH СОЛИ K 2 CO 3 ↔ 2 K+ + CO 3 2 Fe 2(SO 4)3 ↔ 2 Fe 3+ + 3 SO 42
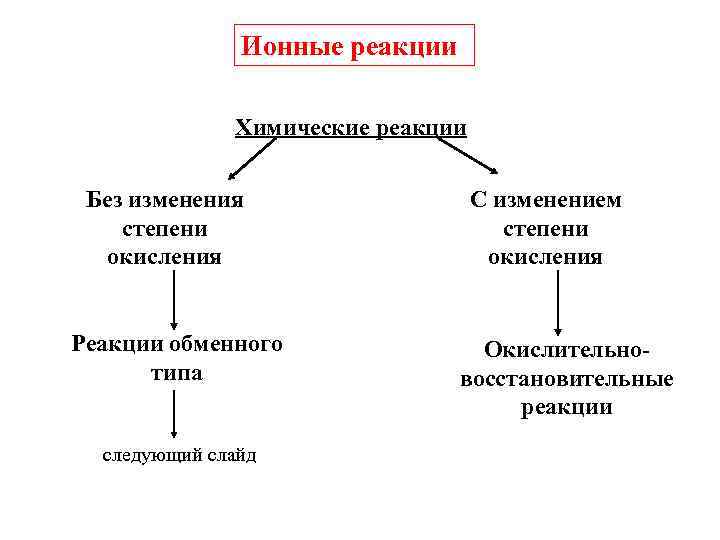 Ионные реакции Химические реакции Без изменения степени окисления Реакции обменного типа следующий слайд С изменением степени окисления Окислительно восстановительные реакции
Ионные реакции Химические реакции Без изменения степени окисления Реакции обменного типа следующий слайд С изменением степени окисления Окислительно восстановительные реакции
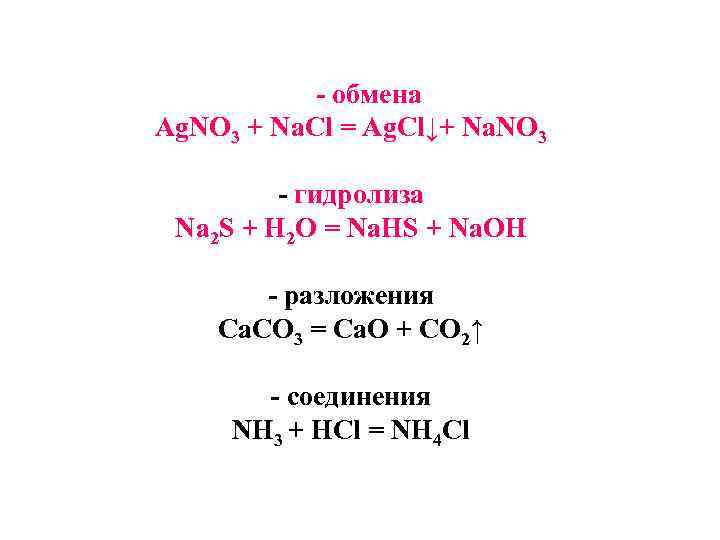 обмена Ag. NO 3 + Na. Cl = Ag. Cl↓+ Na. NO 3 гидролиза Na 2 S + H 2 O = Na. HS + Na. OH разложения Ca. CO 3 = Ca. O + CO 2↑ соединения NH 3 + HCl = NH 4 Cl
обмена Ag. NO 3 + Na. Cl = Ag. Cl↓+ Na. NO 3 гидролиза Na 2 S + H 2 O = Na. HS + Na. OH разложения Ca. CO 3 = Ca. O + CO 2↑ соединения NH 3 + HCl = NH 4 Cl
 Все реакции, протекающие в водных растворах электролитов – это реакции между ионами, т. е. ИОННЫЕ РЕАКЦИИ
Все реакции, протекающие в водных растворах электролитов – это реакции между ионами, т. е. ИОННЫЕ РЕАКЦИИ
 Обменные рекции в водных растворах протекают до конца ( необратимо), если образуется: 1) осадок Ag. NO 3 + Na. Cl = Ag. Cl↓+ Na. NO 3 2) газ Na 2 CO 3 +H 2 SO 4 = Na 2 SO 4 + CO 2↑+ H 2 O 3) малодиссоциирующий электролит (H 2 O) HCl + KOH = KCl + H 2 O 4) комплексное соединение Cu. SO 4 + 4 NH 3 = [Cu(NH 3)4]SO 4
Обменные рекции в водных растворах протекают до конца ( необратимо), если образуется: 1) осадок Ag. NO 3 + Na. Cl = Ag. Cl↓+ Na. NO 3 2) газ Na 2 CO 3 +H 2 SO 4 = Na 2 SO 4 + CO 2↑+ H 2 O 3) малодиссоциирующий электролит (H 2 O) HCl + KOH = KCl + H 2 O 4) комплексное соединение Cu. SO 4 + 4 NH 3 = [Cu(NH 3)4]SO 4
 При составлении ионных уравнений осадки (↓) газы (↑) воду H 2 O комплексную частицу [Cu(NH 3)4]2+ записываем одной формулой
При составлении ионных уравнений осадки (↓) газы (↑) воду H 2 O комплексную частицу [Cu(NH 3)4]2+ записываем одной формулой
 ПРИМЕР 1) Молекулярное уравнение: Na 2 SO 4 + Ba. Cl 2 = Ba. SO 4↓ + 2 Na. C 2) Полное ионное уравнение: 2 Na+ + SO 42 + Ba 2+ + 2 Cl = Ba. SO 4↓ + 2 Na+ + 2 Cl 3) Cокращенное ионное уравнение: SO 42 + Ba 2+ = Ba. SO 4↓ Качественная реакция на SO 42 ион
ПРИМЕР 1) Молекулярное уравнение: Na 2 SO 4 + Ba. Cl 2 = Ba. SO 4↓ + 2 Na. C 2) Полное ионное уравнение: 2 Na+ + SO 42 + Ba 2+ + 2 Cl = Ba. SO 4↓ + 2 Na+ + 2 Cl 3) Cокращенное ионное уравнение: SO 42 + Ba 2+ = Ba. SO 4↓ Качественная реакция на SO 42 ион
 Расчетные методы определения р. Н Р р НF, СN = 10 3 г экв/л, = 10 %, р. Н ? HF H+ + F [H+] = C Э = Мr, СN = CM = 10 3 моль/л [H+] = 10 3 10 1 = 10 4 моль/л р. Н = 4
Расчетные методы определения р. Н Р р НF, СN = 10 3 г экв/л, = 10 %, р. Н ? HF H+ + F [H+] = C Э = Мr, СN = CM = 10 3 моль/л [H+] = 10 3 10 1 = 10 4 моль/л р. Н = 4
 Р р Са(ОН)2 СМ = 10 3 моль/л = 50 % р. Н = ? Са(ОН)2 Са 2+ + 2 ОН [ОН ] = 2 С [ОН ] =2 10 3 0, 5 = 10 3 моль/л р. ОН = lg [ОН ] = lg 10 3 = 3 р. Н = 14 3 = 11
Р р Са(ОН)2 СМ = 10 3 моль/л = 50 % р. Н = ? Са(ОН)2 Са 2+ + 2 ОН [ОН ] = 2 С [ОН ] =2 10 3 0, 5 = 10 3 моль/л р. ОН = lg [ОН ] = lg 10 3 = 3 р. Н = 14 3 = 11
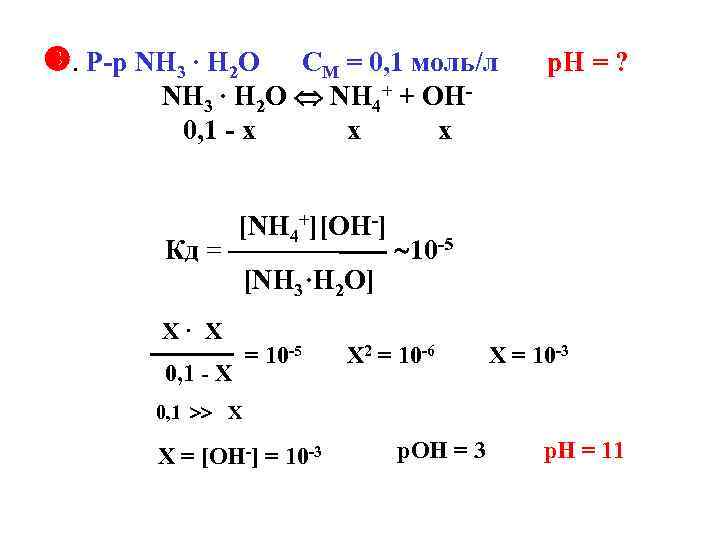 . Р р NH 3 · H 2 O CM = 0, 1 моль/л NH 3 · H 2 O NH 4+ + OH 0, 1 х х х Кд = [NH 4+][OH ] Х· Х 0, 1 Х [NH 3·H 2 O] = 10 5 р. Н = ? 10 5 Х 2 = 10 6 Х = 10 3 0, 1 Х Х = [OH ] = 10 3 р. ОН = 3 р. Н = 11
. Р р NH 3 · H 2 O CM = 0, 1 моль/л NH 3 · H 2 O NH 4+ + OH 0, 1 х х х Кд = [NH 4+][OH ] Х· Х 0, 1 Х [NH 3·H 2 O] = 10 5 р. Н = ? 10 5 Х 2 = 10 6 Х = 10 3 0, 1 Х Х = [OH ] = 10 3 р. ОН = 3 р. Н = 11
 Примеры гидрометаллургических процессов, в которых р. Н среды имеет большое значение Гидрометаллургия цинка 1. Окислительный обжиг концентрата и получение огарка (Zn. O): 2 Zn. S + 3 O 2 = 2 Zn. O +2 SO 2 2. Выщелачивание цинкового огарка ( 70 ºC): Zn. O + H 2 SO 4 = Zn. SO 4 + H 2 O Контроль величины р. Н растворов лежит в основе процесса выщелачивания цинковых огарков (Zn. O) раствором серной кислоты и гидролитической очистки полученных растворов сульфата цинка от примесей. В процессе выщелачивания цинкового огарка решающее значение имеет поведение соединений трех компонентов: основного компонента – цинка и примесных компонентов – железа и кремнезема. Железо и кремнезем относятся к макропримесям, к микропримесям относятся – As, Sb, Al, Cu, In, Ga, Ge и др.
Примеры гидрометаллургических процессов, в которых р. Н среды имеет большое значение Гидрометаллургия цинка 1. Окислительный обжиг концентрата и получение огарка (Zn. O): 2 Zn. S + 3 O 2 = 2 Zn. O +2 SO 2 2. Выщелачивание цинкового огарка ( 70 ºC): Zn. O + H 2 SO 4 = Zn. SO 4 + H 2 O Контроль величины р. Н растворов лежит в основе процесса выщелачивания цинковых огарков (Zn. O) раствором серной кислоты и гидролитической очистки полученных растворов сульфата цинка от примесей. В процессе выщелачивания цинкового огарка решающее значение имеет поведение соединений трех компонентов: основного компонента – цинка и примесных компонентов – железа и кремнезема. Железо и кремнезем относятся к макропримесям, к микропримесям относятся – As, Sb, Al, Cu, In, Ga, Ge и др.
 Изменяя кислотность раствора при выщелачивании, можно осадить растворившееся железо и Si. O 2 и, таким образом, отделить их от цинка. Осаждение железа из растворов сульфата цинка происходит за счет гидролиза ионов Fe 3+ с водой и образования прочных гидроксокомплексов. Fe 2(SO 4)3 · аq + 2 n. H 2 O = Fe 2(OH)2 n(SO 4)2 · aq + n. H 2 SO 4 В зависимости от температуры могут осаждаться и другие кристаллические фазы: (H 3 O)Fe 3(OH)6(SO 4)2; Fe. OHSO 4; Fe. OOH. Осаждение малорастворимых cоединений железа происходит в кислых растворах, имеющих значение р. Н в пределах 1, 7 – 2, 5. Таким образом, нейтрализация кислых растворов сульфата цинка огарком (до р. Н 1, 7 2, 5) способствует насыщению раствора малорастворимыми соединениями железа, которые начинают выпадать в осадок. Этот процесс называется гидролитическое осаждение.
Изменяя кислотность раствора при выщелачивании, можно осадить растворившееся железо и Si. O 2 и, таким образом, отделить их от цинка. Осаждение железа из растворов сульфата цинка происходит за счет гидролиза ионов Fe 3+ с водой и образования прочных гидроксокомплексов. Fe 2(SO 4)3 · аq + 2 n. H 2 O = Fe 2(OH)2 n(SO 4)2 · aq + n. H 2 SO 4 В зависимости от температуры могут осаждаться и другие кристаллические фазы: (H 3 O)Fe 3(OH)6(SO 4)2; Fe. OHSO 4; Fe. OOH. Осаждение малорастворимых cоединений железа происходит в кислых растворах, имеющих значение р. Н в пределах 1, 7 – 2, 5. Таким образом, нейтрализация кислых растворов сульфата цинка огарком (до р. Н 1, 7 2, 5) способствует насыщению раствора малорастворимыми соединениями железа, которые начинают выпадать в осадок. Этот процесс называется гидролитическое осаждение.
 Кремнезем в огарках присутствует в виде силиката цинка, который при выщелачивании серной кислотой переходит в раствор в виде ортокремниевой кислоты: Zn 2 Si. O 4 + 2 H 2 SO 4 · aq = 2 Zn. SO 4 · aq + H 4 Si. O 4 · aq Очистка растворов от кремнезема в виде осадков кремнекислоты H 4 Si. O 4, благоприятных для отстоя и фильтрации, происходит в области р. Н = 3– 3, 5. Таким образом, дальнейшее нейтрализация растворов сульфата цинка огарком до р. Н раствора, равным 3 3, 5, приводит к очистке раствора от кремнезема. Выщелачивание цинкового огарка заканчивается при р. Н = 4, 8 5, 4, что обеспечивает высокую степень извлечения цинка в раствор (до 90 %). Микропримеси удаляют из раствора сульфата цинка либо попутно с железом при гидролитической очистке (As, Sb, Ga), либо специальными методами, как то цементация, экстракция (Cd, Cu, Ni, Co).
Кремнезем в огарках присутствует в виде силиката цинка, который при выщелачивании серной кислотой переходит в раствор в виде ортокремниевой кислоты: Zn 2 Si. O 4 + 2 H 2 SO 4 · aq = 2 Zn. SO 4 · aq + H 4 Si. O 4 · aq Очистка растворов от кремнезема в виде осадков кремнекислоты H 4 Si. O 4, благоприятных для отстоя и фильтрации, происходит в области р. Н = 3– 3, 5. Таким образом, дальнейшее нейтрализация растворов сульфата цинка огарком до р. Н раствора, равным 3 3, 5, приводит к очистке раствора от кремнезема. Выщелачивание цинкового огарка заканчивается при р. Н = 4, 8 5, 4, что обеспечивает высокую степень извлечения цинка в раствор (до 90 %). Микропримеси удаляют из раствора сульфата цинка либо попутно с железом при гидролитической очистке (As, Sb, Ga), либо специальными методами, как то цементация, экстракция (Cd, Cu, Ni, Co).
 3. Электролиз растворов сульфата цинка. Электролиз проводится в электролизных ваннах, температура электролита – 35 -38 ºС. Zn. SO 4 + H 2 O = Zn + H 2 SO 4 + 1/2 O 2 На катоде выделяется цинк и водород: На аноде выделяется кислород: Zn 2+ + 2 e = Zn 2 H+ + 2 e = H 2 2 OH 2 e = H 2 O + 1/2 O 2 В качестве катодов используются алюминиевые листы, аноды выполнены из свинца. Осадок цинка периодически сдирается с катода и подвергается переплавке. При гидрометаллугическом способе производства Zn достигается высокая степень комплексного использования сырья. Извлечение Zn составляет 95 -97 %. Кроме того, извлекают Cd, Pb, Cu, а также Au, Ag, Ge, Tl In, Se, Te.
3. Электролиз растворов сульфата цинка. Электролиз проводится в электролизных ваннах, температура электролита – 35 -38 ºС. Zn. SO 4 + H 2 O = Zn + H 2 SO 4 + 1/2 O 2 На катоде выделяется цинк и водород: На аноде выделяется кислород: Zn 2+ + 2 e = Zn 2 H+ + 2 e = H 2 2 OH 2 e = H 2 O + 1/2 O 2 В качестве катодов используются алюминиевые листы, аноды выполнены из свинца. Осадок цинка периодически сдирается с катода и подвергается переплавке. При гидрометаллугическом способе производства Zn достигается высокая степень комплексного использования сырья. Извлечение Zn составляет 95 -97 %. Кроме того, извлекают Cd, Pb, Cu, а также Au, Ag, Ge, Tl In, Se, Te.
 Металлургия вольфрама Основными минералами вольфрама, имеющими практическое значение, являются вольфрамит (Fe, Mn)WO 4 и шеелит Сa. WO 4. Принципиальная схема переработки вольфрамовых руда обогащение концентрат выщелачивание спека водой раствор Ca. Cl 2 спекание с Na 2 CO 3 спек Na WO 2 4 раствор Na 2 WO 4 + примеси Ca. WO 4 HCl H 2 WO 4 обжиг очистка от примесей WO 3 восстановление W
Металлургия вольфрама Основными минералами вольфрама, имеющими практическое значение, являются вольфрамит (Fe, Mn)WO 4 и шеелит Сa. WO 4. Принципиальная схема переработки вольфрамовых руда обогащение концентрат выщелачивание спека водой раствор Ca. Cl 2 спекание с Na 2 CO 3 спек Na WO 2 4 раствор Na 2 WO 4 + примеси Ca. WO 4 HCl H 2 WO 4 обжиг очистка от примесей WO 3 восстановление W
 Вскрытие вольфрамитового концентрата производят путем спекания содой при 800 -900 ºС. 2 Fe. WO 4 + 2 Na 2 CO 3 + 0, 5 O 2 = 2 Na 2 WO 4 + Fe 2 O 3 + 2 CO 2 3 Mn. WO 4 + 3 Na 2 CO 3 + 0, 5 O 2 = 3 Na 2 WO 4 + Mn 3 O 4 + 3 CO 2 Шеелитовый концентрат разлагается раствором соды при 225 ºС c образованием растворимого Na 2 WO 4. 2 Ca. WO 4(т) + 2 Na 2 CO 3(ж) = 2 Na 2 WO 4(ж) + 2 Ca. O(т) + 2 CO 2 После вскрытия концентратов образуются растворы вольфрамата натрия (Na 2 WO 4), загрязненные примесями, главными из которых являются Si, P, As, F, Mo. Поэтому следующей операцией является очистки раствора от примесей.
Вскрытие вольфрамитового концентрата производят путем спекания содой при 800 -900 ºС. 2 Fe. WO 4 + 2 Na 2 CO 3 + 0, 5 O 2 = 2 Na 2 WO 4 + Fe 2 O 3 + 2 CO 2 3 Mn. WO 4 + 3 Na 2 CO 3 + 0, 5 O 2 = 3 Na 2 WO 4 + Mn 3 O 4 + 3 CO 2 Шеелитовый концентрат разлагается раствором соды при 225 ºС c образованием растворимого Na 2 WO 4. 2 Ca. WO 4(т) + 2 Na 2 CO 3(ж) = 2 Na 2 WO 4(ж) + 2 Ca. O(т) + 2 CO 2 После вскрытия концентратов образуются растворы вольфрамата натрия (Na 2 WO 4), загрязненные примесями, главными из которых являются Si, P, As, F, Mo. Поэтому следующей операцией является очистки раствора от примесей.
 Очистка от кремния. Кремний присутствует в растворе в виде силиката натрия (Na 2 Si. O 3). Раствор вольфрамата натрия имеет сильно щелочную среду (р. Н~14). Очистка основана на гидролитическом разложении Na 2 Si. O 3 при кипячении и нейтрализации раствора соляной кислотой до р. Н=8 9 с выделением кремниевой кислоты в виде белого осадка. Na 2 Si. O 3 + HCl = H 2 Si. O 3 + Na. Cl C гидролитическим выделением кремниевой кислоты совмещают очистку раствора от фторид-иона. Для этого в нейтрализованный раствор добавляют хлорид магния (Mg. Cl 2) и осаждают малорастворимый фторид магния (Mg. F 2). Далее последовательно удаляют примеси P и As осаждением нерастворимых солей Mg(NH 4)PO 4 и Mg(NH 4)As. O 4, а молибден в виде осадка Mo. S 3. Осадки отделяют от раствора на фильтре.
Очистка от кремния. Кремний присутствует в растворе в виде силиката натрия (Na 2 Si. O 3). Раствор вольфрамата натрия имеет сильно щелочную среду (р. Н~14). Очистка основана на гидролитическом разложении Na 2 Si. O 3 при кипячении и нейтрализации раствора соляной кислотой до р. Н=8 9 с выделением кремниевой кислоты в виде белого осадка. Na 2 Si. O 3 + HCl = H 2 Si. O 3 + Na. Cl C гидролитическим выделением кремниевой кислоты совмещают очистку раствора от фторид-иона. Для этого в нейтрализованный раствор добавляют хлорид магния (Mg. Cl 2) и осаждают малорастворимый фторид магния (Mg. F 2). Далее последовательно удаляют примеси P и As осаждением нерастворимых солей Mg(NH 4)PO 4 и Mg(NH 4)As. O 4, а молибден в виде осадка Mo. S 3. Осадки отделяют от раствора на фильтре.
 Из очищенного от примесей раствора вольфрамата натрия, нагретого до 8090 ºС, осаждают вольфрамат кальция: Na 2 WO 4 + Ca. Cl 2 = Ca. WO 4 + 2 Na. Cl Осадок Ca. WO 4 обрабатывают при 90 ºС соляной кислотой, а затем прокаливанием H 2 WO 4 при 500 -600 ºС получают оксид вольфрама WO 3. Ca. WO 4 + HCl = H 2 WO 4 = Ca. Cl 2 t H 2 WO 4 = WO 3 + H 2 O Восстановление WO 3 ведут водородом при 700 -850 ºС. Процесс осуществляют в две стадии: WO 3 + H 2 = WO 2 + H 2 O WO 2 + 2 H 2 = W + 2 H 2 O
Из очищенного от примесей раствора вольфрамата натрия, нагретого до 8090 ºС, осаждают вольфрамат кальция: Na 2 WO 4 + Ca. Cl 2 = Ca. WO 4 + 2 Na. Cl Осадок Ca. WO 4 обрабатывают при 90 ºС соляной кислотой, а затем прокаливанием H 2 WO 4 при 500 -600 ºС получают оксид вольфрама WO 3. Ca. WO 4 + HCl = H 2 WO 4 = Ca. Cl 2 t H 2 WO 4 = WO 3 + H 2 O Восстановление WO 3 ведут водородом при 700 -850 ºС. Процесс осуществляют в две стадии: WO 3 + H 2 = WO 2 + H 2 O WO 2 + 2 H 2 = W + 2 H 2 O


