 ЛЕКЦИЯ 5 р-Элементы VI группы O, S, Se, Te, Po Халькогены (относящиеся к медным рудам)
ЛЕКЦИЯ 5 р-Элементы VI группы O, S, Se, Te, Po Халькогены (относящиеся к медным рудам)
 Атомные характеристики Элемент O S Se Te Po Вал. эл-ны 2 s 22 p 4 3 s 23 p 4 4 s 24 p 4 5 s 25 p 4 6 s 26 p 4 Rат, нм 0. 073 0. 102 0. 117 0. 136 0. 146 Иониз. , э. В 13. 6 10. 4 9. 8 9. 0 8. 4 ЭО 3. 5 2. 4 2. 1 1. 76 неметаллы металлоид О - Se - Te - Po Усиление металлических свойств
Атомные характеристики Элемент O S Se Te Po Вал. эл-ны 2 s 22 p 4 3 s 23 p 4 4 s 24 p 4 5 s 25 p 4 6 s 26 p 4 Rат, нм 0. 073 0. 102 0. 117 0. 136 0. 146 Иониз. , э. В 13. 6 10. 4 9. 8 9. 0 8. 4 ЭО 3. 5 2. 4 2. 1 1. 76 неметаллы металлоид О - Se - Te - Po Усиление металлических свойств
 Кислород и его соединения
Кислород и его соединения
 Природные ресурсы • Самый распространенный элемент в природе • В земной коре - 47% (песок, Si. O 2, . Al O. 2 Si. O , горные глина, Na 2 O 2 3 2 породы, вода) • Воздух - 22% O 2
Природные ресурсы • Самый распространенный элемент в природе • В земной коре - 47% (песок, Si. O 2, . Al O. 2 Si. O , горные глина, Na 2 O 2 3 2 породы, вода) • Воздух - 22% O 2
 o. C -229 o. C -183 tпл = tкип = Молекула О 2 парамагнитна Есв = 498 к. Дж/моль О 2 = 2 О при t = 2000 о. С О 2 - сильный окис-ль, но из-за прочности связи реакции окисл-я идут при высоких t-рах 0, 5 O 2 + 2 H+ + 2 e H 2 O Eo = +1. 23 V
o. C -229 o. C -183 tпл = tкип = Молекула О 2 парамагнитна Есв = 498 к. Дж/моль О 2 = 2 О при t = 2000 о. С О 2 - сильный окис-ль, но из-за прочности связи реакции окисл-я идут при высоких t-рах 0, 5 O 2 + 2 H+ + 2 e H 2 O Eo = +1. 23 V
 Получение • В промышленности: 1) из жидкого воздуха 2) электролиз воды K(-) 4 H 2 O + 4 e = 2 H 2 + 4 OH A(+) 4 OH - 4 e = O 2 + 2 H 2 O • В лаборатории: 2 H 2 O 2 = (to. C, Mn. O 2) 2 H 2 O + O 2 2 Hg. O = 2 Hg + O 2 2 KCl. O 3 = (to. C, Mn. O 2) KCl + 3 O 2
Получение • В промышленности: 1) из жидкого воздуха 2) электролиз воды K(-) 4 H 2 O + 4 e = 2 H 2 + 4 OH A(+) 4 OH - 4 e = O 2 + 2 H 2 O • В лаборатории: 2 H 2 O 2 = (to. C, Mn. O 2) 2 H 2 O + O 2 2 Hg. O = 2 Hg + O 2 2 KCl. O 3 = (to. C, Mn. O 2) KCl + 3 O 2
 Химические свойства O 2 • c. о. +2, +1, -2 • По реакционной способности уступает только галогенам • Образует химические соединения со всеми элементами кроме He, Ne, Ar
Химические свойства O 2 • c. о. +2, +1, -2 • По реакционной способности уступает только галогенам • Образует химические соединения со всеми элементами кроме He, Ne, Ar
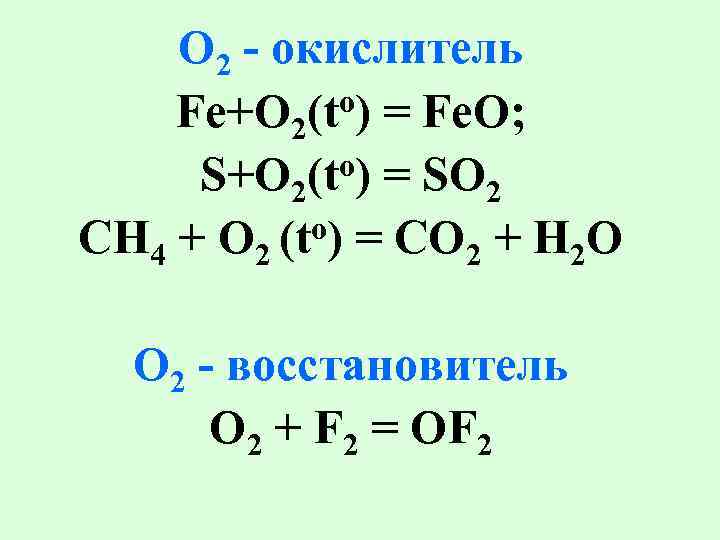 O 2 - окислитель Fe+O 2(to) = Fe. O; o) = SO S+O 2(t 2 o) = CO + H O CH 4 + O 2 (t 2 2 O 2 - восстановитель O 2 + F 2 = OF 2
O 2 - окислитель Fe+O 2(to) = Fe. O; o) = SO S+O 2(t 2 o) = CO + H O CH 4 + O 2 (t 2 2 O 2 - восстановитель O 2 + F 2 = OF 2
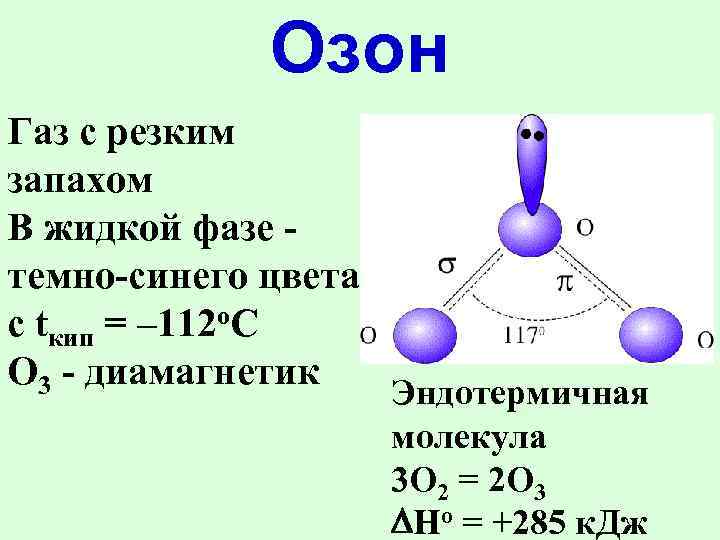 Озон Газ с резким запахом В жидкой фазе темно-синего цвета с tкип = – 112 o. C О 3 - диамагнетик Эндотермичная молекула 3 O 2 = 2 O 3 Ho = +285 к. Дж
Озон Газ с резким запахом В жидкой фазе темно-синего цвета с tкип = – 112 o. C О 3 - диамагнетик Эндотермичная молекула 3 O 2 = 2 O 3 Ho = +285 к. Дж
 • О 3 - сильнейший окислитель 2 О 3 = 3 О 2 р-ция идет в 2 стадии: 1) O 3 =O 2 + O 2) O + O 3 = 2 O 2 O 3 + 2 H+ + 2 e O 2 + H 2 O Eo = +2. 07 В S + O 3 + H 2 O = H 2 SO 4 Кач. и колич. р-ция на O 3: O 3 + 2 KI + H 2 O = O 2 + I 2 + 2 KOH
• О 3 - сильнейший окислитель 2 О 3 = 3 О 2 р-ция идет в 2 стадии: 1) O 3 =O 2 + O 2) O + O 3 = 2 O 2 O 3 + 2 H+ + 2 e O 2 + H 2 O Eo = +2. 07 В S + O 3 + H 2 O = H 2 SO 4 Кач. и колич. р-ция на O 3: O 3 + 2 KI + H 2 O = O 2 + I 2 + 2 KOH
 Соединения кислорода Кислород образует 4 типа соединений: 1. Оксиды (О-2) ( со всеми элементами) 2. Пероксиды (О 2 -2) (с водородом и некот. металлами, H 2 O 2, Na 2 O 2, Ba. O 2, др) 3. Надпероксиды (О 2 -) (KO 2, Rb. O 2, Cs. O 2) 4. Озониды (О 3 -) (KO 3, Rb. O 3, Cs. O 3)
Соединения кислорода Кислород образует 4 типа соединений: 1. Оксиды (О-2) ( со всеми элементами) 2. Пероксиды (О 2 -2) (с водородом и некот. металлами, H 2 O 2, Na 2 O 2, Ba. O 2, др) 3. Надпероксиды (О 2 -) (KO 2, Rb. O 2, Cs. O 2) 4. Озониды (О 3 -) (KO 3, Rb. O 3, Cs. O 3)
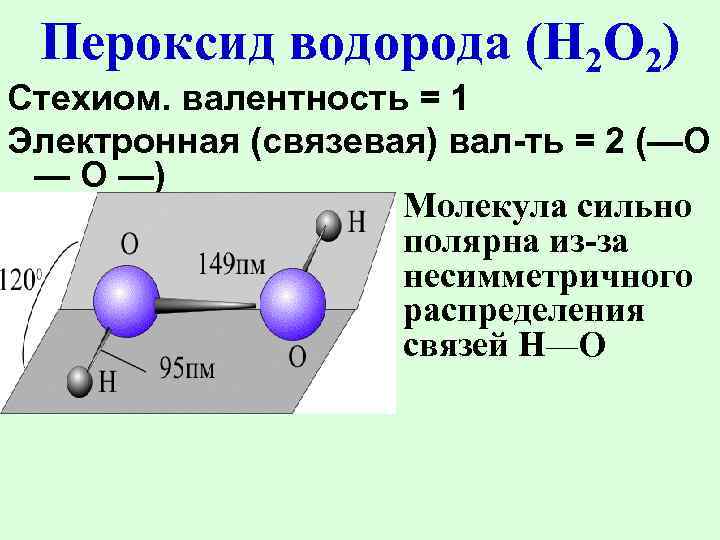 Пероксид водорода (H 2 O 2) Стехиом. валентность = 1 Электронная (связевая) вал-ть = 2 (—О — О —) Молекула сильно полярна из-за несимметричного распределения связей Н—О
Пероксид водорода (H 2 O 2) Стехиом. валентность = 1 Электронная (связевая) вал-ть = 2 (—О — О —) Молекула сильно полярна из-за несимметричного распределения связей Н—О
 • H 2 O 2 - сиропообразная бледно- голубая жидкость с tкип = +150 о. С (из-за водородной связи между молекулами) • H 2 O 2 хороший ионизирующий растворитель + + HO H 2 O 2 ----H 2 O 2 <=> H 3 O 2 2
• H 2 O 2 - сиропообразная бледно- голубая жидкость с tкип = +150 о. С (из-за водородной связи между молекулами) • H 2 O 2 хороший ионизирующий растворитель + + HO H 2 O 2 ----H 2 O 2 <=> H 3 O 2 2
 • с водой смешивается в любых соотношениях с образованием новых водородных связей и диссоциирует как слабая кислота H 2 O 2 H+ + HO 2 Kд = 2. 10 12 • Конц. раствор H 2 O 2 - 30% • Из растворов выделяется в виде неуст. кристаллогидрата H 2 O 2. 2 H 2 O
• с водой смешивается в любых соотношениях с образованием новых водородных связей и диссоциирует как слабая кислота H 2 O 2 H+ + HO 2 Kд = 2. 10 12 • Конц. раствор H 2 O 2 - 30% • Из растворов выделяется в виде неуст. кристаллогидрата H 2 O 2. 2 H 2 O
 Получение H 2 O 2 • В промышленности в две стадии: 1) электролиз H 2 SO 4 до пероксодисерной к-ты H 2 S 2 O 8 2) H 2 S 2 O 8 + 2 H 2 O = 2 H 2 SO 4 + H 2 O 2 • В лаборатории: Ba. O 2 + H 2 SO 4 = Ba. SO 4 + H 2 O 2
Получение H 2 O 2 • В промышленности в две стадии: 1) электролиз H 2 SO 4 до пероксодисерной к-ты H 2 S 2 O 8 2) H 2 S 2 O 8 + 2 H 2 O = 2 H 2 SO 4 + H 2 O 2 • В лаборатории: Ba. O 2 + H 2 SO 4 = Ba. SO 4 + H 2 O 2
 Ок-вос. свойства H 2 O 2 • 3 типа ок-вос. р-ций возможны в водных растворах: 1. O 22 =1/2 O 2+O 2 диспроп-е (-1) (0)+(-2) 2. O 22 + 2 e = 2 O 2 восст-е (-1) (-2) 3. O 22 - 2 e = O 2 окисление (-1) (0) • Ок-вос. потенциалы для полуреакций: H 2 O 2 + 2 H+ + 2 e 2 H 2 O Eo = +1. 77 V O 2 + 2 H+ + 2 e H 2 O 2 Eo = +0. 68 V
Ок-вос. свойства H 2 O 2 • 3 типа ок-вос. р-ций возможны в водных растворах: 1. O 22 =1/2 O 2+O 2 диспроп-е (-1) (0)+(-2) 2. O 22 + 2 e = 2 O 2 восст-е (-1) (-2) 3. O 22 - 2 e = O 2 окисление (-1) (0) • Ок-вос. потенциалы для полуреакций: H 2 O 2 + 2 H+ + 2 e 2 H 2 O Eo = +1. 77 V O 2 + 2 H+ + 2 e H 2 O 2 Eo = +0. 68 V
 Примеры • Ок-ные св-ва сильнее, чем вос-е 2 H 2 O 2 = 2 H 2 O + O 2 3 H 2 O 2 + KI = KIO 3 + 3 H 2 O ок-ль 2 KMn. O 4 + 5 H 2 O 2 + 3 H 2 SO 4 = вос-ль Mn. SO 4 + K 2 SO 4 + 8 H 2 O + O 2 Cl 2 + H 2 O 2 = 2 HCl + O 2
Примеры • Ок-ные св-ва сильнее, чем вос-е 2 H 2 O 2 = 2 H 2 O + O 2 3 H 2 O 2 + KI = KIO 3 + 3 H 2 O ок-ль 2 KMn. O 4 + 5 H 2 O 2 + 3 H 2 SO 4 = вос-ль Mn. SO 4 + K 2 SO 4 + 8 H 2 O + O 2 Cl 2 + H 2 O 2 = 2 HCl + O 2
 Пероксиды металлов • Это соед-я катионов щел. и щ-з. металлов с пероксид-анионом O 22 Na + H 2 O 2 2 Na + O 2 = Na 2 O 2 (расплав) o. C) =2 Ca. O + O 2 Ca. O 2(t 2 2 K 2 O 2 + 2 H 2 O = 4 KOH + O 2 2 Na 2 O 2 + 2 CO 2 = Na 2 CO 3 + O 2
Пероксиды металлов • Это соед-я катионов щел. и щ-з. металлов с пероксид-анионом O 22 Na + H 2 O 2 2 Na + O 2 = Na 2 O 2 (расплав) o. C) =2 Ca. O + O 2 Ca. O 2(t 2 2 K 2 O 2 + 2 H 2 O = 4 KOH + O 2 2 Na 2 O 2 + 2 CO 2 = Na 2 CO 3 + O 2
 Кислород в с. о. +2, +1 • O 2 F 2 и OF 2 сильнейшие ок-ли и фторирующие агенты OF 2 + H 2 O = O 3 + O 2 + HF OF 2 + Na. OH = H 2 O + O 2 + Na. F OF 2 + Xe = Xe. F 2 + Xe. OF 2 • Получены и другие соединения: O 3 F 2, O 4 F 2, O 5 F 2, O 6 F 2
Кислород в с. о. +2, +1 • O 2 F 2 и OF 2 сильнейшие ок-ли и фторирующие агенты OF 2 + H 2 O = O 3 + O 2 + HF OF 2 + Na. OH = H 2 O + O 2 + Na. F OF 2 + Xe = Xe. F 2 + Xe. OF 2 • Получены и другие соединения: O 3 F 2, O 4 F 2, O 5 F 2, O 6 F 2
 Применение • О 2 - в металлургии при получении чугуна и стали, в медицине, в качестве окислителя ракетного топлива • О 3 - для обработки питьевой воды, для отбеливания бумаги • Н 2 О 2 - для отбеливания шелка, шерсти, меха, для протравливания семян, в медицине, в аналитической химии, в качестве окислителя в реактивных двигателях торпед • Na 2 O 2 - для регенерации воздуха в подводных лодках и на космических станциях
Применение • О 2 - в металлургии при получении чугуна и стали, в медицине, в качестве окислителя ракетного топлива • О 3 - для обработки питьевой воды, для отбеливания бумаги • Н 2 О 2 - для отбеливания шелка, шерсти, меха, для протравливания семян, в медицине, в аналитической химии, в качестве окислителя в реактивных двигателях торпед • Na 2 O 2 - для регенерации воздуха в подводных лодках и на космических станциях
 S, Se, Te, Po
S, Se, Te, Po
 ПРИРОДНЫЕ РЕСУРСЫ S - земной кларк 0, 05% Вулканическая сера
ПРИРОДНЫЕ РЕСУРСЫ S - земной кларк 0, 05% Вулканическая сера
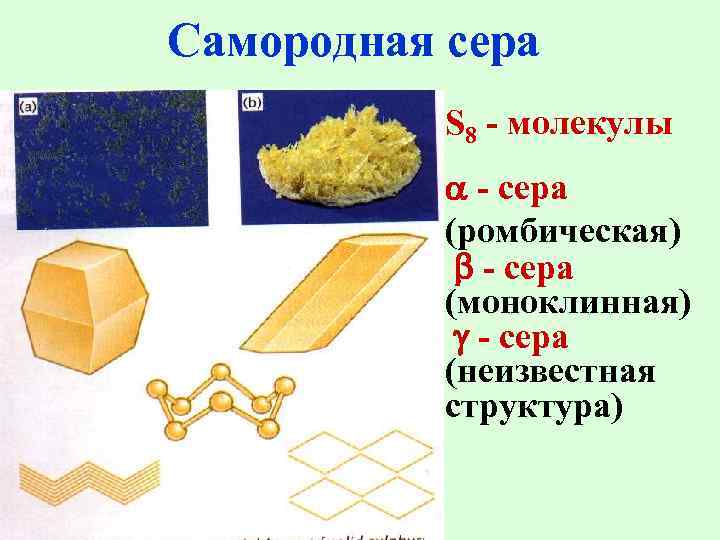 Самородная сера S 8 - молекулы - сера (ромбическая) - сера (моноклинная) - сера (неизвестная структура)
Самородная сера S 8 - молекулы - сера (ромбическая) - сера (моноклинная) - сера (неизвестная структура)
 Сульфаты: Na 2 SO 4. 10 H 2 O-мирабилит Сa. SO 4. 2 H 2 O - гибс • Сульфиды: Pb. S - галенит, Zn. S - сфалерит, Cu. S - ковелин, Cu 2 S - халькозин, Н 2 S - газ • Se и Te - редкие рассеянные элементы, сопутствуют сульфидам
Сульфаты: Na 2 SO 4. 10 H 2 O-мирабилит Сa. SO 4. 2 H 2 O - гибс • Сульфиды: Pb. S - галенит, Zn. S - сфалерит, Cu. S - ковелин, Cu 2 S - халькозин, Н 2 S - газ • Se и Te - редкие рассеянные элементы, сопутствуют сульфидам
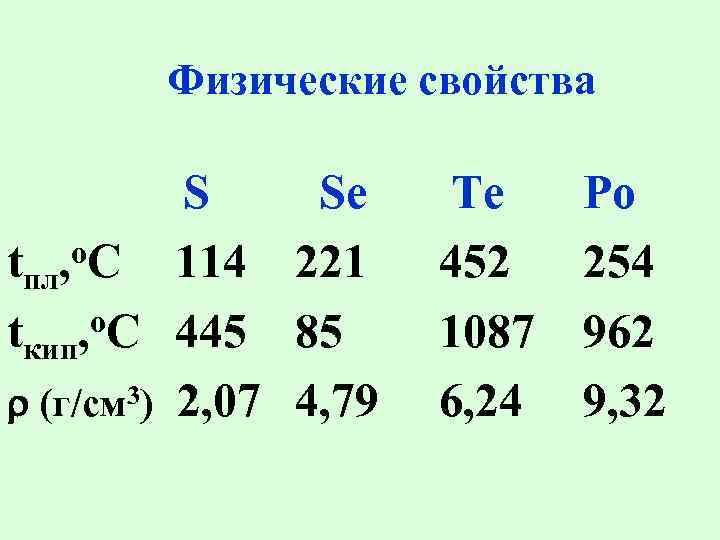 Физические свойства S Se o. C tпл, 114 221 tкип, o. C 445 85 (г/см 3) 2, 07 4, 79 Te 452 1087 6, 24 Po 254 962 9, 32
Физические свойства S Se o. C tпл, 114 221 tкип, o. C 445 85 (г/см 3) 2, 07 4, 79 Te 452 1087 6, 24 Po 254 962 9, 32
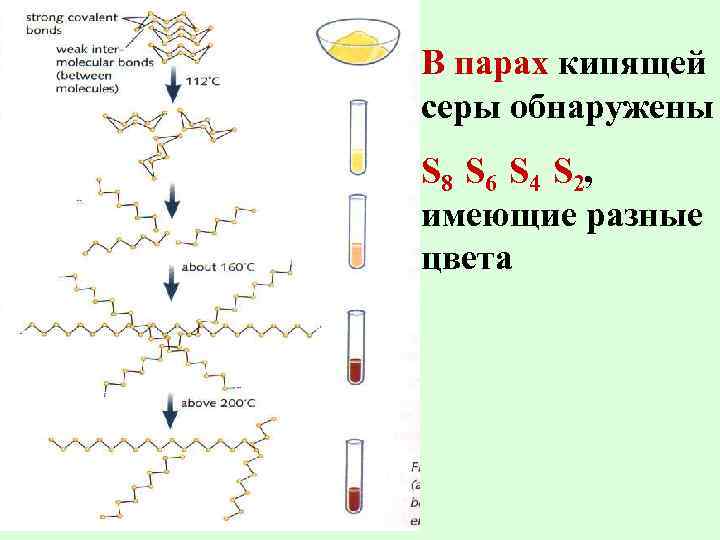 В парах кипящей серы обнаружены S 8 S 6 S 4 S 2, имеющие разные цвета
В парах кипящей серы обнаружены S 8 S 6 S 4 S 2, имеющие разные цвета
 • Se - по строению похож на серу (п/п св-ва) • Тe - серебристо-белое металлоподобное кристаллич. в-во, хрупок, легко растирается в порошок (п/п) • При высоких to-рах в виде Se 2 Te 2 • При низких to-рах в виде Э 4, Э 6, Э 8 • Ро - мягкий метал серебристо-белого цвета с металлич. проводимостью
• Se - по строению похож на серу (п/п св-ва) • Тe - серебристо-белое металлоподобное кристаллич. в-во, хрупок, легко растирается в порошок (п/п) • При высоких to-рах в виде Se 2 Te 2 • При низких to-рах в виде Э 4, Э 6, Э 8 • Ро - мягкий метал серебристо-белого цвета с металлич. проводимостью
 Химические свойства • Степени окисления в соединениях: S -2 0 +2 +4 +6 Se Te Po -2 -2 -2 0 0 0 +2 +2 +2 +4 +4 +4 +6 +6 -
Химические свойства • Степени окисления в соединениях: S -2 0 +2 +4 +6 Se Te Po -2 -2 -2 0 0 0 +2 +2 +2 +4 +4 +4 +6 +6 -
 Простые вещества S, Se, Te - неметаллы; Po - метал S (Se) + H 2 O Te + H 2 O = Te. O 2 + 2 H 2 S (Se, Te) + HCl Po + 2 HCl = Po. Cl 2 + H 2
Простые вещества S, Se, Te - неметаллы; Po - метал S (Se) + H 2 O Te + H 2 O = Te. O 2 + 2 H 2 S (Se, Te) + HCl Po + 2 HCl = Po. Cl 2 + H 2
 S, Se - ок-вос двойственность S - окислитель: Zn + S (to)= Zn. S
S, Se - ок-вос двойственность S - окислитель: Zn + S (to)= Zn. S
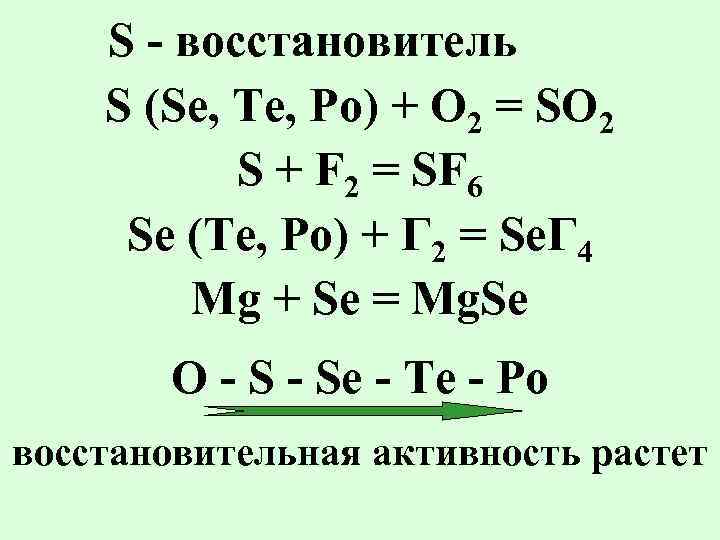 S - восстановитель S (Se, Te, Po) + O 2 = SO 2 S + F 2 = SF 6 Se (Te, Po) + Г 2 = Se. Г 4 Mg + Se = Mg. Se O - Se - Te - Po восстановительная активность растет
S - восстановитель S (Se, Te, Po) + O 2 = SO 2 S + F 2 = SF 6 Se (Te, Po) + Г 2 = Se. Г 4 Mg + Se = Mg. Se O - Se - Te - Po восстановительная активность растет
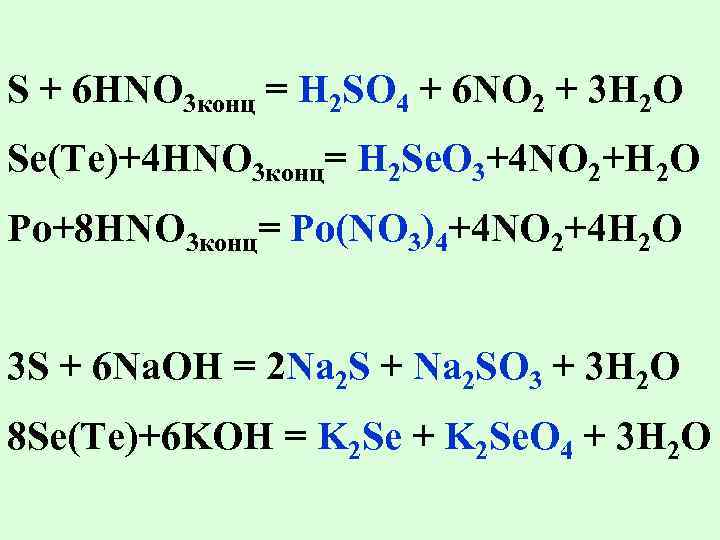 S + 6 HNO 3 конц = H 2 SO 4 + 6 NO 2 + 3 H 2 O Se(Te)+4 HNO 3 конц= H 2 Se. O 3+4 NO 2+H 2 O Po+8 HNO 3 конц= Po(NO 3)4+4 NO 2+4 H 2 O 3 S + 6 Na. OH = 2 Na 2 S + Na 2 SO 3 + 3 H 2 O 8 Se(Te)+6 KOH = K 2 Se + K 2 Se. O 4 + 3 H 2 O
S + 6 HNO 3 конц = H 2 SO 4 + 6 NO 2 + 3 H 2 O Se(Te)+4 HNO 3 конц= H 2 Se. O 3+4 NO 2+H 2 O Po+8 HNO 3 конц= Po(NO 3)4+4 NO 2+4 H 2 O 3 S + 6 Na. OH = 2 Na 2 S + Na 2 SO 3 + 3 H 2 O 8 Se(Te)+6 KOH = K 2 Se + K 2 Se. O 4 + 3 H 2 O
 Получение простых веществ 1) S - извлекают из пустой породы с помощью воды под давлением 2) H 2 S + O 2 недост. = S + H 2 O • Se и Te извлекают из отходов сульфидных руд цветных металлов
Получение простых веществ 1) S - извлекают из пустой породы с помощью воды под давлением 2) H 2 S + O 2 недост. = S + H 2 O • Se и Te извлекают из отходов сульфидных руд цветных металлов
 Применение простых веществ • S для получения H 2 SO 4 и вулканизации резины • Se и Te - в качестве полупроводников, выпрямителей тока и фотоэлементов
Применение простых веществ • S для получения H 2 SO 4 и вулканизации резины • Se и Te - в качестве полупроводников, выпрямителей тока и фотоэлементов
 Бинарные соединения
Бинарные соединения
 Степень окисления -2 Сульфиды - H 2 S, Na 2 S, CS 2 Селениды - H 2 Se, Na 2 Se, CSe 2 Теллуриды - H 2 Te, Na 2 Te, CTe 2 халькогениды Po. H 2 - очень неустойчив
Степень окисления -2 Сульфиды - H 2 S, Na 2 S, CS 2 Селениды - H 2 Se, Na 2 Se, CSe 2 Теллуриды - H 2 Te, Na 2 Te, CTe 2 халькогениды Po. H 2 - очень неустойчив
 Получение сульфидов, селенидов, теллуридов H 2 + S (Se) = H 2 S Fe. S + 2 HCl = Fe. Cl 2 + H 2 S 3 Al 2 Э 3 + 6 H 2 O = 2 Al(OH)3 + 3 H 2 Э Na 2 Э + 2 HCl = H 2 Э + 2 Na. Cl (Э = S, Se, Te)
Получение сульфидов, селенидов, теллуридов H 2 + S (Se) = H 2 S Fe. S + 2 HCl = Fe. Cl 2 + H 2 S 3 Al 2 Э 3 + 6 H 2 O = 2 Al(OH)3 + 3 H 2 Э Na 2 Э + 2 HCl = H 2 Э + 2 Na. Cl (Э = S, Se, Te)
 Химические свойства • H 2 S, H 2 Se, H 2 Te - газы с неприятным запахом, в воде слабые кислоты H 2 O H 2 Se H 2 Te Eсв, k. Дж/моль 463 347 276 238 Kд 1. 8. 10 -16 1. 10 -7 1. 7. 10 -4 1. 10 -3 Устойчимость молекул ум-ся Сила к-т и восс-ная активность ув-ся
Химические свойства • H 2 S, H 2 Se, H 2 Te - газы с неприятным запахом, в воде слабые кислоты H 2 O H 2 Se H 2 Te Eсв, k. Дж/моль 463 347 276 238 Kд 1. 8. 10 -16 1. 10 -7 1. 7. 10 -4 1. 10 -3 Устойчимость молекул ум-ся Сила к-т и восс-ная активность ув-ся
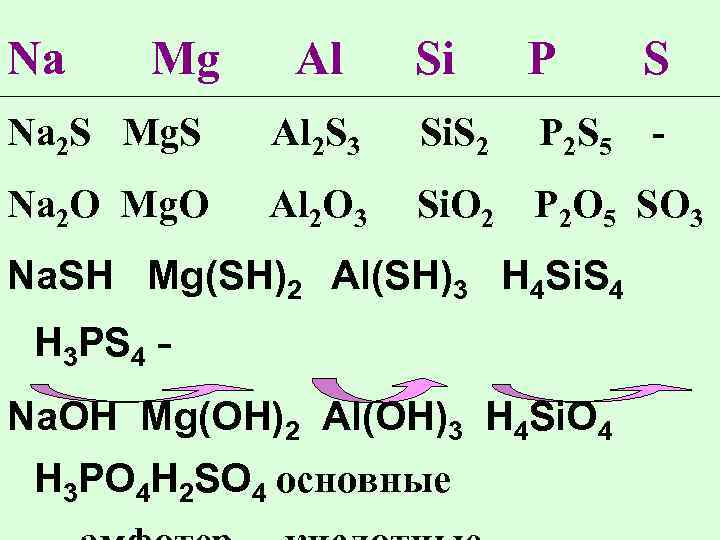 Na Mg Al Si P S - Na 2 S Mg. S Al 2 S 3 Si. S 2 P 2 S 5 Na 2 O Mg. O Al 2 O 3 Si. O 2 P 2 O 5 SO 3 Na. SH Mg(SH)2 Al(SH)3 H 4 Si. S 4 H 3 PS 4 Na. OH Mg(OH)2 Al(OH)3 H 4 Si. O 4 H 3 PO 4 H 2 SO 4 основные
Na Mg Al Si P S - Na 2 S Mg. S Al 2 S 3 Si. S 2 P 2 S 5 Na 2 O Mg. O Al 2 O 3 Si. O 2 P 2 O 5 SO 3 Na. SH Mg(SH)2 Al(SH)3 H 4 Si. S 4 H 3 PS 4 Na. OH Mg(OH)2 Al(OH)3 H 4 Si. O 4 H 3 PO 4 H 2 SO 4 основные
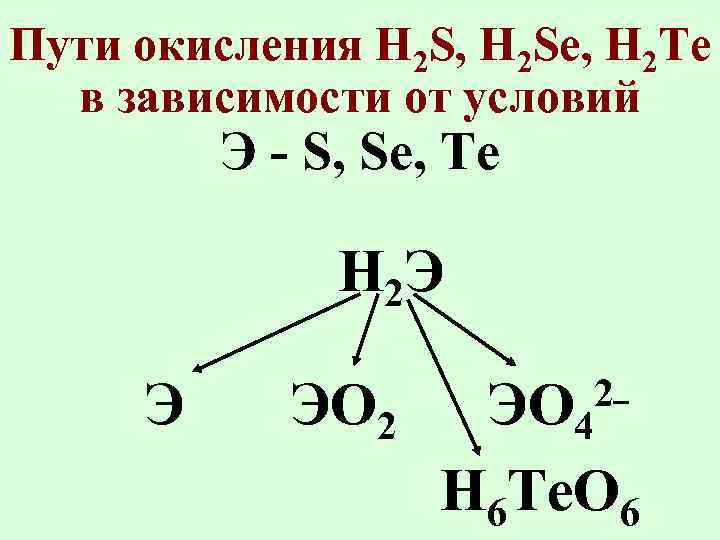 Пути окисления H 2 S, H 2 Se, H 2 Te в зависимости от условий Э - S, Se, Te H 2 Э Э ЭO 2 2 ЭO 4 H 6 Te. O 6
Пути окисления H 2 S, H 2 Se, H 2 Te в зависимости от условий Э - S, Se, Te H 2 Э Э ЭO 2 2 ЭO 4 H 6 Te. O 6
 Примеры 2 H 2 S + K 2 Cr 2 O 7 + 4 H 2 SO 4 = 3 S + Cr 2(SO 4)3 + K 2 SO 4 + 7 H 2 O 3 H 2 S + 4 HCl. O 3 = 3 H 2 SO 4 + 4 HCl 2 H 2 Э + O 2 = 2 Э + 2 H 2 O 2 H 2 Э + O 2 (to) = 2 ЭO 2 + 2 H 2 O (Э = S, Se, Te)
Примеры 2 H 2 S + K 2 Cr 2 O 7 + 4 H 2 SO 4 = 3 S + Cr 2(SO 4)3 + K 2 SO 4 + 7 H 2 O 3 H 2 S + 4 HCl. O 3 = 3 H 2 SO 4 + 4 HCl 2 H 2 Э + O 2 = 2 Э + 2 H 2 O 2 H 2 Э + O 2 (to) = 2 ЭO 2 + 2 H 2 O (Э = S, Se, Te)
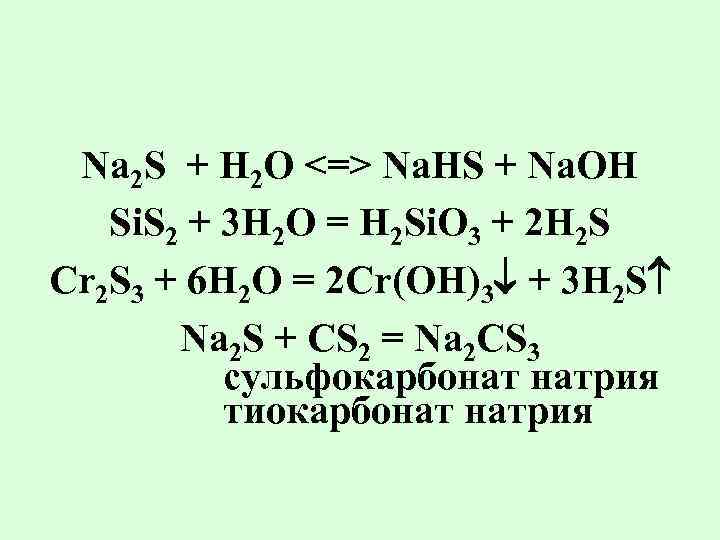 Na 2 S + H 2 O <=> Na. HS + Na. OH Si. S 2 + 3 H 2 O = H 2 Si. O 3 + 2 H 2 S Cr 2 S 3 + 6 H 2 O = 2 Cr(OH)3 + 3 H 2 S Na 2 S + СS 2 = Na 2 СS 3 сульфокарбонат натрия тиокарбонат натрия
Na 2 S + H 2 O <=> Na. HS + Na. OH Si. S 2 + 3 H 2 O = H 2 Si. O 3 + 2 H 2 S Cr 2 S 3 + 6 H 2 O = 2 Cr(OH)3 + 3 H 2 S Na 2 S + СS 2 = Na 2 СS 3 сульфокарбонат натрия тиокарбонат натрия
 Pb. S Hg. S Fe. S 2 галенит свинцовый блеск киноварь пирит железный колчедан Zn. S бленда
Pb. S Hg. S Fe. S 2 галенит свинцовый блеск киноварь пирит железный колчедан Zn. S бленда
 As 2 S 3 Sb 2 S 3 Bi 2 S 3
As 2 S 3 Sb 2 S 3 Bi 2 S 3
 • По растворимости сульфиды делят на 4 группы: 1) растворимые в воде - Na 2 S, K 2 S, Li 2 S, Ca. S, Sr. S, (NH 4)2 S и др. 2) не раств-е в воде, но растворимые в кислотах слабых окислителях (HCl, H 2 SO 4 разб. ) - Zn. S, Fe. S, Mn. S, La 2 S 3 и др. Zn. S + 2 HCl = Zn. Cl 2 + H 2 S
• По растворимости сульфиды делят на 4 группы: 1) растворимые в воде - Na 2 S, K 2 S, Li 2 S, Ca. S, Sr. S, (NH 4)2 S и др. 2) не раств-е в воде, но растворимые в кислотах слабых окислителях (HCl, H 2 SO 4 разб. ) - Zn. S, Fe. S, Mn. S, La 2 S 3 и др. Zn. S + 2 HCl = Zn. Cl 2 + H 2 S
 3) растворимые в кислотах сильных ок-лях (HNO 3, H 2 SO 4 конц. , HCl. O 4 конц. ) Pb. S, Cu 2 S, Cu. S, Bi 2 S 3, Ag 2 S, Mo. S 2 Cu. S+10 HNO 3=Cu(NO 3)2+8 NO 2+4 H 2 O 4) растворимые в растворах Na 2 S, K 2 S, (NH 4)2 S : Sn. S 2, Ge. S 2, Si. S 2, CS 2, Al 2 S 3, As 2 S 5, Sb 2 S 3, Sb 2 S 5 сульфоангидриды As 2 S 5 + 3 Na 2 S = 2 Na 3 As. S 4 + HCl = Na. Cl + As 2 S 5 + H 2 S
3) растворимые в кислотах сильных ок-лях (HNO 3, H 2 SO 4 конц. , HCl. O 4 конц. ) Pb. S, Cu 2 S, Cu. S, Bi 2 S 3, Ag 2 S, Mo. S 2 Cu. S+10 HNO 3=Cu(NO 3)2+8 NO 2+4 H 2 O 4) растворимые в растворах Na 2 S, K 2 S, (NH 4)2 S : Sn. S 2, Ge. S 2, Si. S 2, CS 2, Al 2 S 3, As 2 S 5, Sb 2 S 3, Sb 2 S 5 сульфоангидриды As 2 S 5 + 3 Na 2 S = 2 Na 3 As. S 4 + HCl = Na. Cl + As 2 S 5 + H 2 S
 Персульфиды (Ме 2 Sn) • Na 2 Sконц. + (n-1)S = Na 2 Sn Строение персульфид ионов (S 32 -, S 42 -): S 2 S 32 - S S S 42 - S S Окраска S 22 - до S 92(NH 4)2 Sn + 2 HCl = H 2 Sn + 2 NH 4 Cl H 2 Sn - персульфиды водорода (сульфаны) H 2 S 2 - персульфид водорода - аналог Н 2 О 2
Персульфиды (Ме 2 Sn) • Na 2 Sконц. + (n-1)S = Na 2 Sn Строение персульфид ионов (S 32 -, S 42 -): S 2 S 32 - S S S 42 - S S Окраска S 22 - до S 92(NH 4)2 Sn + 2 HCl = H 2 Sn + 2 NH 4 Cl H 2 Sn - персульфиды водорода (сульфаны) H 2 S 2 - персульфид водорода - аналог Н 2 О 2
 Химические свойства персульфидов • Персульфиды (подобно) пероксидам проявляют ок-вос двойственность, а также диспрпорционируют Na 2 S 2 + Sn. S = Sn. S 2 + Na 2 S 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 пирит Na 2 S 2 = Na 2 S + S
Химические свойства персульфидов • Персульфиды (подобно) пероксидам проявляют ок-вос двойственность, а также диспрпорционируют Na 2 S 2 + Sn. S = Sn. S 2 + Na 2 S 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 пирит Na 2 S 2 = Na 2 S + S
 Применение сульфидов • Различная раствор-сть сульфидов используется для разделения и анализа химических элементов • в качестве люминофоров • пигментов полупроводников • в химических синтезах • в кожевенном производстве • с вредителями с/х культур
Применение сульфидов • Различная раствор-сть сульфидов используется для разделения и анализа химических элементов • в качестве люминофоров • пигментов полупроводников • в химических синтезах • в кожевенном производстве • с вредителями с/х культур
 Лекция 6 План 1. Соединения серы и ее аналогов в с. о. +4 2. Соединения серы и ее аналогов в в с. о. +6
Лекция 6 План 1. Соединения серы и ее аналогов в с. о. +4 2. Соединения серы и ее аналогов в в с. о. +6
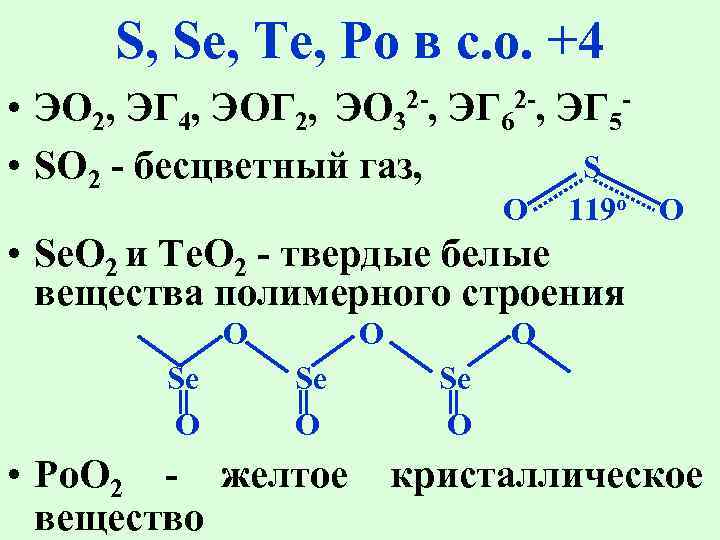 S, Se, Te, Po в с. о. +4 • ЭО 2, ЭГ 4, ЭОГ 2, ЭО 32 -, ЭГ 62 -, ЭГ 5 • SO 2 - бесцветный газ, S O 119 o O • Se. O 2 и Te. O 2 - твердые белые вещества полимерного строения O Se O • Po. O 2 - желтое вещество O Se O кристаллическое
S, Se, Te, Po в с. о. +4 • ЭО 2, ЭГ 4, ЭОГ 2, ЭО 32 -, ЭГ 62 -, ЭГ 5 • SO 2 - бесцветный газ, S O 119 o O • Se. O 2 и Te. O 2 - твердые белые вещества полимерного строения O Se O • Po. O 2 - желтое вещество O Se O кристаллическое
 Получение Промышленное: S(Se, Te) + O 2 (600 -700 o. C) = SO 2 Ca. SO 4 + C(1350°C) = Ca. O + SO 2 + CO 4 Fe. S 2 + 11 O 2 (to. C) = 2 Fe 2 O 3 + 8 SO 2 Лабораторное: Na 2 SO 3 + 2 HCl = SO 2 + 2 Na. Cl+ H 2 O
Получение Промышленное: S(Se, Te) + O 2 (600 -700 o. C) = SO 2 Ca. SO 4 + C(1350°C) = Ca. O + SO 2 + CO 4 Fe. S 2 + 11 O 2 (to. C) = 2 Fe 2 O 3 + 8 SO 2 Лабораторное: Na 2 SO 3 + 2 HCl = SO 2 + 2 Na. Cl+ H 2 O
 SO 2 - Se. O 2 - Te. O 2 - Po. O 2 ум-ся раств-ть в воде, кислотные св-ва, вос-ная активность tпло. С -75 возг. 337 733 разлаг. 500
SO 2 - Se. O 2 - Te. O 2 - Po. O 2 ум-ся раств-ть в воде, кислотные св-ва, вос-ная активность tпло. С -75 возг. 337 733 разлаг. 500
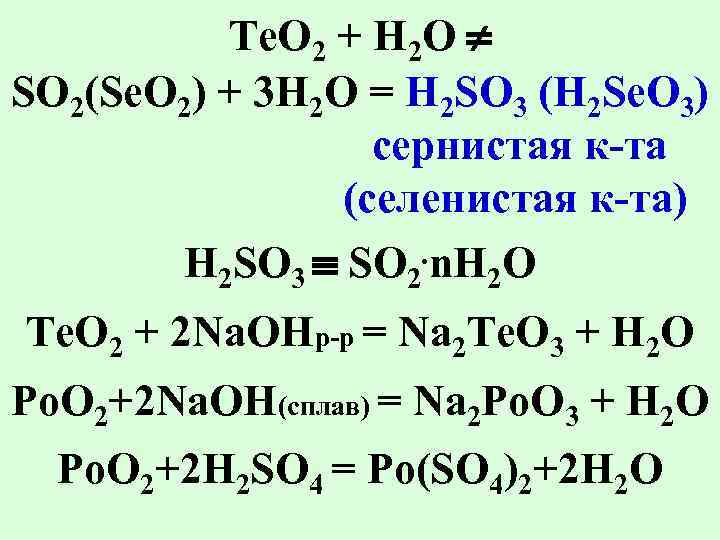 Te. O 2 + H 2 O SO 2(Se. O 2) + 3 H 2 O = H 2 SO 3 (H 2 Se. O 3) сернистая к-та (селенистая к-та) H 2 SO 3 SO 2. n. H 2 O Te. O 2 + 2 Na. OHp-p = Na 2 Te. O 3 + H 2 O Po. O 2+2 Na. OH(сплав) = Na 2 Po. O 3 + H 2 O Po. O 2+2 H 2 SO 4 = Po(SO 4)2+2 H 2 O
Te. O 2 + H 2 O SO 2(Se. O 2) + 3 H 2 O = H 2 SO 3 (H 2 Se. O 3) сернистая к-та (селенистая к-та) H 2 SO 3 SO 2. n. H 2 O Te. O 2 + 2 Na. OHp-p = Na 2 Te. O 3 + H 2 O Po. O 2+2 Na. OH(сплав) = Na 2 Po. O 3 + H 2 O Po. O 2+2 H 2 SO 4 = Po(SO 4)2+2 H 2 O
 SO 2 (SО 32 -)- болee вос-ль, чем ок-ль Se. O 2 (Se. О 32 -) - более ок-ль, чем вос-ль 2 SO 2 + Se. O 2 = Se + 2 SO 3 вос-ль ок-ль SO 2 + H 2 S = S + H 2 O SO 2 + Cl 2 = SO 2 Cl 2 SF 4 + 3 H 2 O = H 2 SO 3 + 4 HF SOCl 2 + 2 H 2 O = H 2 SO 3 + 2 HCl Se. Cl 4 + 3 H 2 O = H 2 Se. O 3 + 4 HCl Te. I 4 + 2 KI = K 2[Te. I 6] Po. Cl 4 + 2 KCl = K 2[Po. Cl 6]
SO 2 (SО 32 -)- болee вос-ль, чем ок-ль Se. O 2 (Se. О 32 -) - более ок-ль, чем вос-ль 2 SO 2 + Se. O 2 = Se + 2 SO 3 вос-ль ок-ль SO 2 + H 2 S = S + H 2 O SO 2 + Cl 2 = SO 2 Cl 2 SF 4 + 3 H 2 O = H 2 SO 3 + 4 HF SOCl 2 + 2 H 2 O = H 2 SO 3 + 2 HCl Se. Cl 4 + 3 H 2 O = H 2 Se. O 3 + 4 HCl Te. I 4 + 2 KI = K 2[Te. I 6] Po. Cl 4 + 2 KCl = K 2[Po. Cl 6]
 S, Se, Te, Po в с. о. +6 • SO 3 - триоксид серы, серный газ, серный ангидрид, б/ц летучая жидкость • Se. O 3 - белое твердое в-во • Te. O 3 - желтое твердое в-во • SF 6 - гексафторид серы • SOF 4 - оксотетрафторид серы • SO 2 Г 2 - диоксодигалогенид
S, Se, Te, Po в с. о. +6 • SO 3 - триоксид серы, серный газ, серный ангидрид, б/ц летучая жидкость • Se. O 3 - белое твердое в-во • Te. O 3 - желтое твердое в-во • SF 6 - гексафторид серы • SOF 4 - оксотетрафторид серы • SO 2 Г 2 - диоксодигалогенид
 Получение SO 3, Se. O 3, Te. O 3 • Получение SO 3 1. Контактный способ получения SO 3 : 2 SO 2 + O 2 = 2 SO 3 (500 o. C, кат- V 2 O 5) 2. Нитрозный способ для SO 3 в присутствии кат-ра смеси NO+NO 2, 1) SO 2 + NO 2 = SO 3 + NO 2) NO + 0, 5 O 2 = NO 2 3) SO 2 + NO 2 = SO 3 + NO и. т. д. • K 2 Se. O 4 + SO 3 = K 2 SO 4 + Se. O 3 • H 6 Te. O 6 (to) = Te. O 3 + 3 H 2 O
Получение SO 3, Se. O 3, Te. O 3 • Получение SO 3 1. Контактный способ получения SO 3 : 2 SO 2 + O 2 = 2 SO 3 (500 o. C, кат- V 2 O 5) 2. Нитрозный способ для SO 3 в присутствии кат-ра смеси NO+NO 2, 1) SO 2 + NO 2 = SO 3 + NO 2) NO + 0, 5 O 2 = NO 2 3) SO 2 + NO 2 = SO 3 + NO и. т. д. • K 2 Se. O 4 + SO 3 = K 2 SO 4 + Se. O 3 • H 6 Te. O 6 (to) = Te. O 3 + 3 H 2 O
 Химические свойства оксидов SO 3, Se. O 3, Te. O 3 - кислотные оксиды SO 3 + H 2 O = H 2 SO 4 Ho = -130 к. Дж/моль Se. O 3 + H 2 O = H 2 Se. O 4 селеновая к-та Te. O 3 + H 2 O Te. O 3 + 2 Na. OH (to)= Na 2 Te. O 4 + H 2
Химические свойства оксидов SO 3, Se. O 3, Te. O 3 - кислотные оксиды SO 3 + H 2 O = H 2 SO 4 Ho = -130 к. Дж/моль Se. O 3 + H 2 O = H 2 Se. O 4 селеновая к-та Te. O 3 + H 2 O Te. O 3 + 2 Na. OH (to)= Na 2 Te. O 4 + H 2
 2 ЭО 3 o) (t = 2 ЭО 2 + О 2 SO 3 + H 2 SO 4 = H 2 SO 4. SO 3 (или H 2 S 2 O 7)- олеум H 2 SO 4. SO 3 + H 2 O = 2 H 2 SO 4 Se. O 3 и SO 3 - сильные ок-е свойства SO 3 + 2 KI = K 2 SO 4 + I 2 5 SO 3 + 2 P = P 2 O 5 + 5 SO 2
2 ЭО 3 o) (t = 2 ЭО 2 + О 2 SO 3 + H 2 SO 4 = H 2 SO 4. SO 3 (или H 2 S 2 O 7)- олеум H 2 SO 4. SO 3 + H 2 O = 2 H 2 SO 4 Se. O 3 и SO 3 - сильные ок-е свойства SO 3 + 2 KI = K 2 SO 4 + I 2 5 SO 3 + 2 P = P 2 O 5 + 5 SO 2
 Применение оксидов • SO 2 - в производстве серной кислоты • для дизенфекции овощехранилищ • для обесцвечивания шерсти, шелка и сахара • в органическом производстве • SO 3 - промежуточный продукт в производстве серной кислоты
Применение оксидов • SO 2 - в производстве серной кислоты • для дизенфекции овощехранилищ • для обесцвечивания шерсти, шелка и сахара • в органическом производстве • SO 3 - промежуточный продукт в производстве серной кислоты
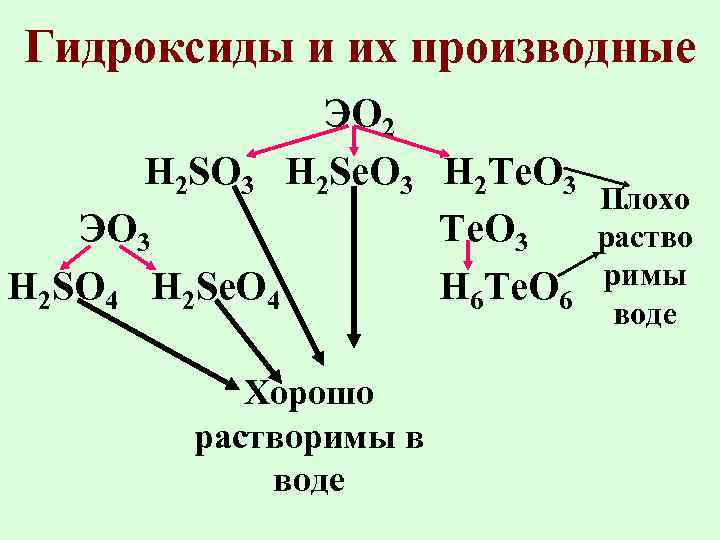 Гидроксиды и их производные ЭО 2 H 2 SO 3 H 2 Se. O 3 H 2 Te. O 3 ЭО 3 Te. O 3 H 2 SO 4 H 2 Se. O 4 H 6 Te. O 6 Хорошо растворимы в воде Плохо раство римы воде
Гидроксиды и их производные ЭО 2 H 2 SO 3 H 2 Se. O 3 H 2 Te. O 3 ЭО 3 Te. O 3 H 2 SO 4 H 2 Se. O 4 H 6 Te. O 6 Хорошо растворимы в воде Плохо раство римы воде
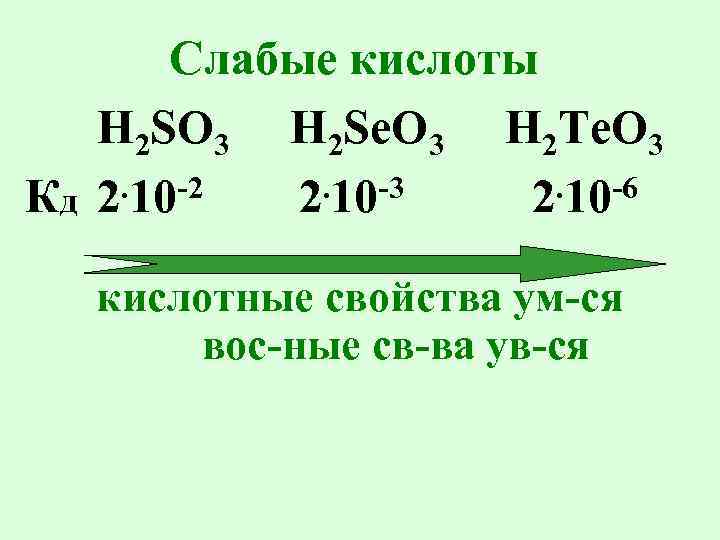 Слабые кислоты H 2 SO 3 H 2 Se. O 3 H 2 Te. O 3. 10 -2. 10 -3. 10 -6 Кд 2 2 2 кислотные свойства ум-ся вос-ные св-ва ув-ся
Слабые кислоты H 2 SO 3 H 2 Se. O 3 H 2 Te. O 3. 10 -2. 10 -3. 10 -6 Кд 2 2 2 кислотные свойства ум-ся вос-ные св-ва ув-ся
 Сильные кислоты H 2 Te. O 4 H 2 Se. O 4 H 6 Te. O 6 жидкость крист. в-во сильные кислоты слабая к-та рост окислительной активности
Сильные кислоты H 2 Te. O 4 H 2 Se. O 4 H 6 Te. O 6 жидкость крист. в-во сильные кислоты слабая к-та рост окислительной активности
 Обугливание сахара серной кислотой
Обугливание сахара серной кислотой

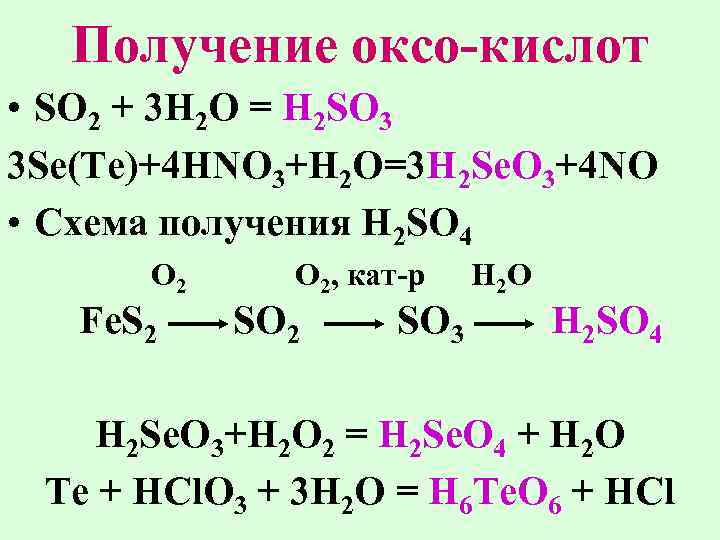 Получение оксо-кислот • SO 2 + 3 H 2 O = H 2 SO 3 3 Se(Te)+4 HNO 3+H 2 O=3 H 2 Se. O 3+4 NO • Схема получения H 2 SO 4 O 2 Fe. S 2 O 2, кат-р SO 2 SO 3 H 2 O H 2 SO 4 H 2 Se. O 3+H 2 O 2 = H 2 Se. O 4 + H 2 O Te + HCl. O 3 + 3 H 2 O = H 6 Te. O 6 + HCl
Получение оксо-кислот • SO 2 + 3 H 2 O = H 2 SO 3 3 Se(Te)+4 HNO 3+H 2 O=3 H 2 Se. O 3+4 NO • Схема получения H 2 SO 4 O 2 Fe. S 2 O 2, кат-р SO 2 SO 3 H 2 O H 2 SO 4 H 2 Se. O 3+H 2 O 2 = H 2 Se. O 4 + H 2 O Te + HCl. O 3 + 3 H 2 O = H 6 Te. O 6 + HCl
 Химические свойства оксо-кислот
Химические свойства оксо-кислот
 Химические свойства оксо-кислот H 2 SO 3 + 2 H 2 S = H 2 SO 4+ 2 HI H 2 SO 3 + I 2 + H 2 O = 3 S + 3 H 2 O H 2 SO 3+4 Fe. Cl 2+4 HCl=S+4 Fe. Cl 3 +3 H 2 O H 2 SO 3 + H 2 ЭO 3 = Э + H 2 SO 4 +
Химические свойства оксо-кислот H 2 SO 3 + 2 H 2 S = H 2 SO 4+ 2 HI H 2 SO 3 + I 2 + H 2 O = 3 S + 3 H 2 O H 2 SO 3+4 Fe. Cl 2+4 HCl=S+4 Fe. Cl 3 +3 H 2 O H 2 SO 3 + H 2 ЭO 3 = Э + H 2 SO 4 +
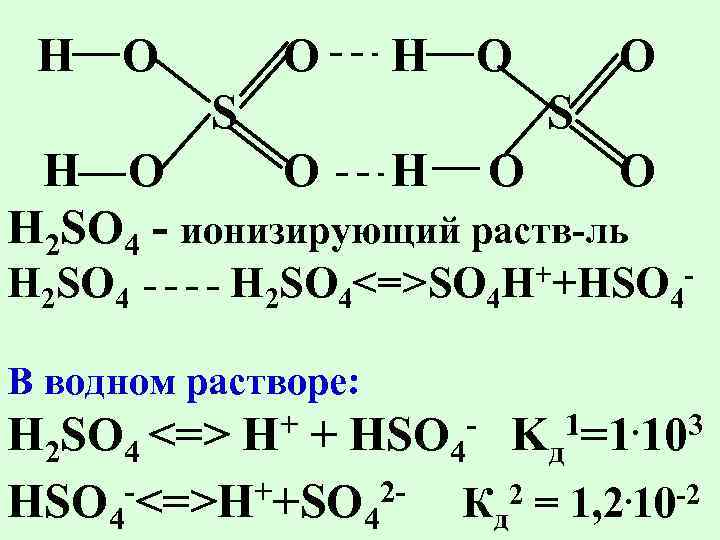 Н O O S H O O Н O O H 2 SO 4 - ионизирующий раств-ль H 2 SO 4 ++HSO H 2 SO 4<=>SO 4 H 4 В водном растворе: + H - K 1=1. 103 H 2 SO 4 <=> + HSO 4 д -<=>H++SO 22 = 1, 2. 10 -2 HSO 4 Кд 4
Н O O S H O O Н O O H 2 SO 4 - ионизирующий раств-ль H 2 SO 4 ++HSO H 2 SO 4<=>SO 4 H 4 В водном растворе: + H - K 1=1. 103 H 2 SO 4 <=> + HSO 4 д -<=>H++SO 22 = 1, 2. 10 -2 HSO 4 Кд 4
 Химические свойства оксо-кислот 8 Na+5 H 2 SO 4 конц. = 4 Na 2 SO 4+ H 2 S + 4 H 2 O 3 Sn + 8 H 2 SO 4 конц. = Sn(SO 4)2+ 2 S + 8 H 2 O Cu + 2 H 2 SO 4 конц. = Cu. SO 4 + SO 2 + 2 H O
Химические свойства оксо-кислот 8 Na+5 H 2 SO 4 конц. = 4 Na 2 SO 4+ H 2 S + 4 H 2 O 3 Sn + 8 H 2 SO 4 конц. = Sn(SO 4)2+ 2 S + 8 H 2 O Cu + 2 H 2 SO 4 конц. = Cu. SO 4 + SO 2 + 2 H O
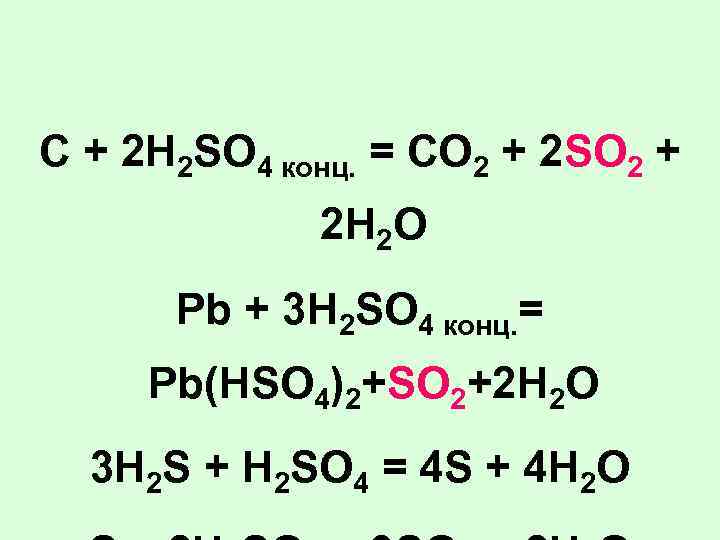 C + 2 H 2 SO 4 конц. = CO 2 + 2 SO 2 + 2 H 2 O Pb + 3 H 2 SO 4 конц. = Pb(HSO 4)2+SO 2+2 H 2 O 3 H 2 S + H 2 SO 4 = 4 S + 4 H 2 O
C + 2 H 2 SO 4 конц. = CO 2 + 2 SO 2 + 2 H 2 O Pb + 3 H 2 SO 4 конц. = Pb(HSO 4)2+SO 2+2 H 2 O 3 H 2 S + H 2 SO 4 = 4 S + 4 H 2 O

 Сульфиты и сульфаты • Это бесцветные или белые кристаллические вещества • Сульфиты нерастворимы в воде (исключене сульфиты щел. металлов и гидросульфиты) • Сульфаты хорошо растворимы в воде (исключение сульфаты Ca, Sr, Ba, Pb, Ag)
Сульфиты и сульфаты • Это бесцветные или белые кристаллические вещества • Сульфиты нерастворимы в воде (исключене сульфиты щел. металлов и гидросульфиты) • Сульфаты хорошо растворимы в воде (исключение сульфаты Ca, Sr, Ba, Pb, Ag)
 Кристаллогидраты • • Na 2 SO 4. 10 H 2 O - Глауберова соль Ca. SO 4. 2 H 2 O - Гиббс Ca. SO 4. 0, 5 H 2 O - Алебастр Mg. SO 4. 7 H 2 O - Горькая соль Fe. SO 4. 6 H 2 O - Железный купорос Co. SO 4. 6 H 2 O - Кобальтовый купорос Cu. SO 4. 5 H 2 O - Медный купорос
Кристаллогидраты • • Na 2 SO 4. 10 H 2 O - Глауберова соль Ca. SO 4. 2 H 2 O - Гиббс Ca. SO 4. 0, 5 H 2 O - Алебастр Mg. SO 4. 7 H 2 O - Горькая соль Fe. SO 4. 6 H 2 O - Железный купорос Co. SO 4. 6 H 2 O - Кобальтовый купорос Cu. SO 4. 5 H 2 O - Медный купорос
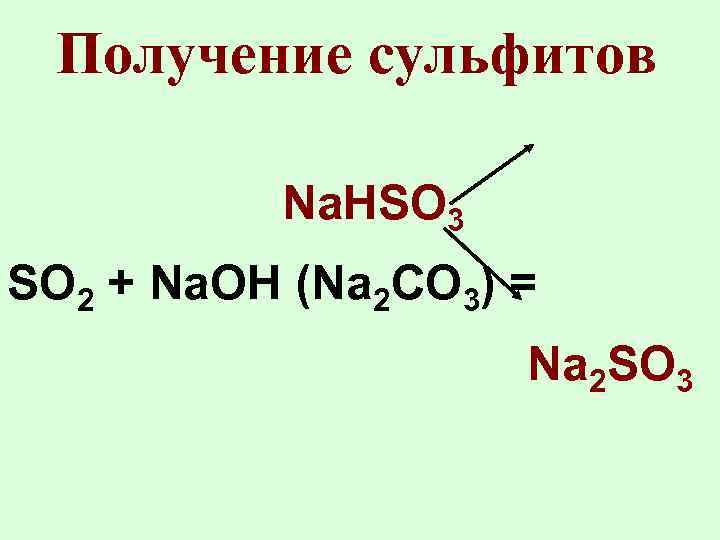 Получение сульфитов Na. HSO 3 SO 2 + Na. OH (Na 2 CO 3) = Na 2 SO 3
Получение сульфитов Na. HSO 3 SO 2 + Na. OH (Na 2 CO 3) = Na 2 SO 3
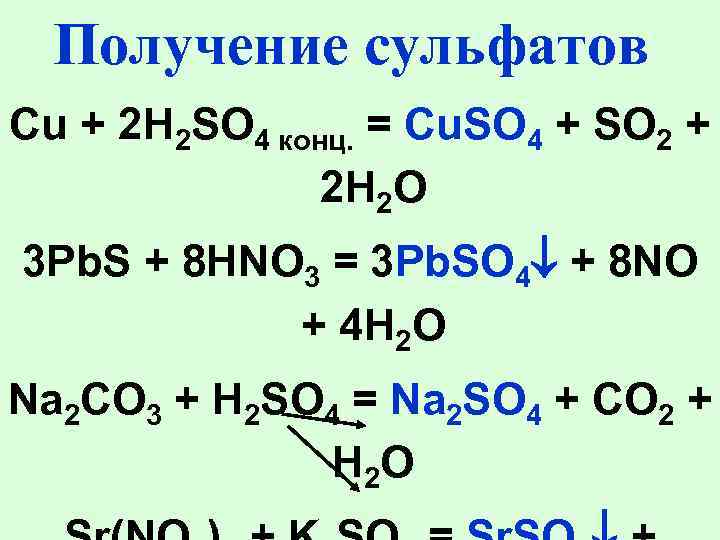 Получение сульфатов Cu + 2 H 2 SO 4 конц. = Cu. SO 4 + SO 2 + 2 H 2 O 3 Pb. S + 8 HNO 3 = 3 Pb. SO 4 + 8 NO + 4 H 2 O Na 2 CO 3 + H 2 SO 4 = Na 2 SO 4 + CO 2 + H 2 O
Получение сульфатов Cu + 2 H 2 SO 4 конц. = Cu. SO 4 + SO 2 + 2 H 2 O 3 Pb. S + 8 HNO 3 = 3 Pb. SO 4 + 8 NO + 4 H 2 O Na 2 CO 3 + H 2 SO 4 = Na 2 SO 4 + CO 2 + H 2 O
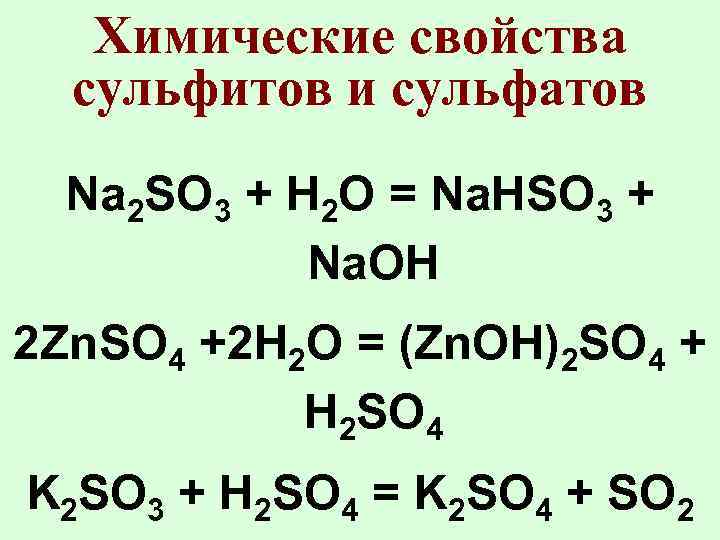 Химические свойства сульфитов и сульфатов Na 2 SO 3 + H 2 O = Na. HSO 3 + Na. OH 2 Zn. SO 4 +2 H 2 O = (Zn. OH)2 SO 4 + H 2 SO 4 K 2 SO 3 + H 2 SO 4 = K 2 SO 4 + SO 2
Химические свойства сульфитов и сульфатов Na 2 SO 3 + H 2 O = Na. HSO 3 + Na. OH 2 Zn. SO 4 +2 H 2 O = (Zn. OH)2 SO 4 + H 2 SO 4 K 2 SO 3 + H 2 SO 4 = K 2 SO 4 + SO 2
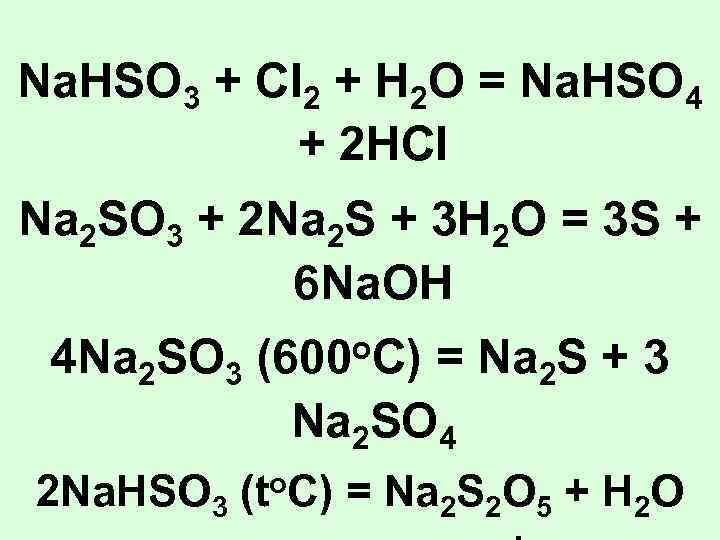 Na. HSO 3 + Cl 2 + H 2 O = Na. HSO 4 + 2 HCl Na 2 SO 3 + 2 Na 2 S + 3 H 2 O = 3 S + 6 Na. OH 4 Na 2 SO 3 o. C) (600 = Na 2 S + 3 Na 2 SO 4 2 Na. HSO 3 (to. C) = Na 2 S 2 O 5 + H 2 O
Na. HSO 3 + Cl 2 + H 2 O = Na. HSO 4 + 2 HCl Na 2 SO 3 + 2 Na 2 S + 3 H 2 O = 3 S + 6 Na. OH 4 Na 2 SO 3 o. C) (600 = Na 2 S + 3 Na 2 SO 4 2 Na. HSO 3 (to. C) = Na 2 S 2 O 5 + H 2 O
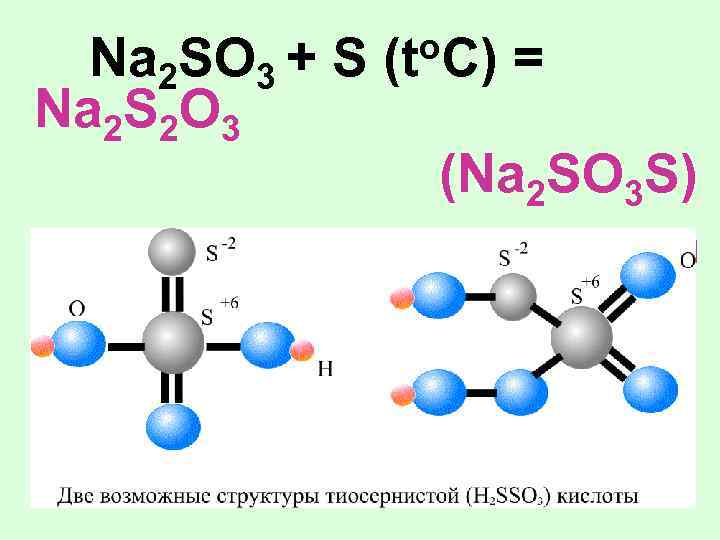 Na 2 SO 3 + S Na 2 S 2 O 3 o. C) (t = (Na 2 SO 3 S) тиосульфат Na - сильный вос-ль
Na 2 SO 3 + S Na 2 S 2 O 3 o. C) (t = (Na 2 SO 3 S) тиосульфат Na - сильный вос-ль
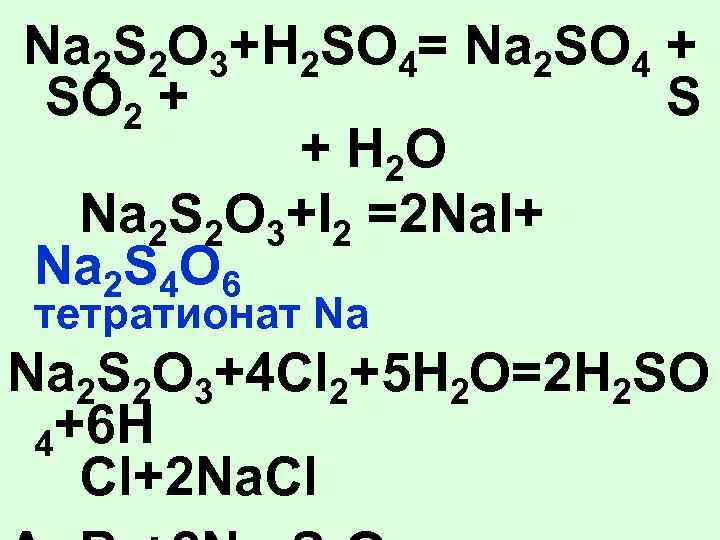 Na 2 S 2 O 3+H 2 SO 4= Na 2 SO 4 + SO 2 + S + H 2 O Na 2 S 2 O 3+I 2 =2 Na. I+ Na 2 S 4 O 6 тетратионат Na Na 2 S 2 O 3+4 Cl 2+5 H 2 O=2 H 2 SO +6 H 4 Cl+2 Na. Cl
Na 2 S 2 O 3+H 2 SO 4= Na 2 SO 4 + SO 2 + S + H 2 O Na 2 S 2 O 3+I 2 =2 Na. I+ Na 2 S 4 O 6 тетратионат Na Na 2 S 2 O 3+4 Cl 2+5 H 2 O=2 H 2 SO +6 H 4 Cl+2 Na. Cl
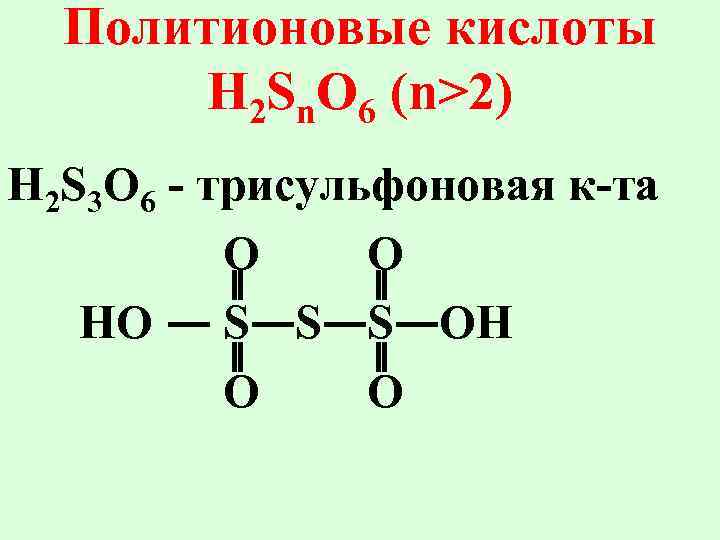 Политионовые кислоты H 2 Sn. O 6 (n>2) H 2 S 3 O 6 - триcульфоновая к-та O O HO S S S OH O O
Политионовые кислоты H 2 Sn. O 6 (n>2) H 2 S 3 O 6 - триcульфоновая к-та O O HO S S S OH O O
 H 2 S 4 O 6 - тетратионовая к-та
H 2 S 4 O 6 - тетратионовая к-та
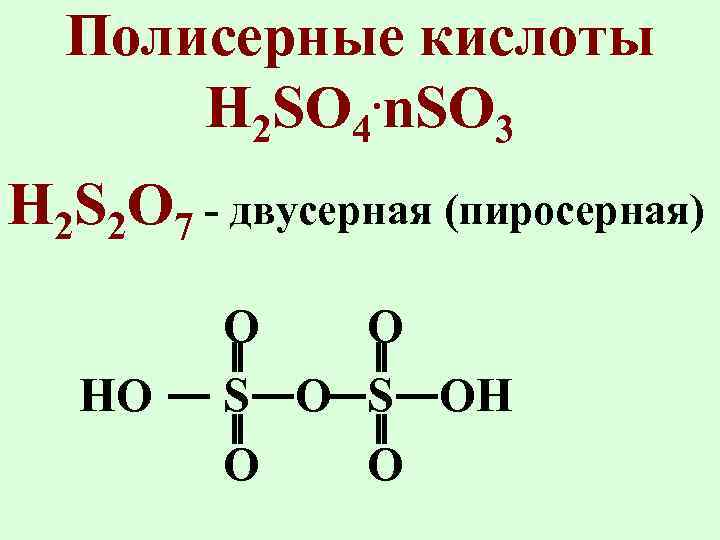 Полисерные кислоты. n. SO H 2 SO 4 3 H 2 S 2 O 7 - двусерная (пиросерная) HO O O S OH O O
Полисерные кислоты. n. SO H 2 SO 4 3 H 2 S 2 O 7 - двусерная (пиросерная) HO O O S OH O O
 H 2 S 3 O 10 - трисерная к-та HO O S O S О S OH O O O
H 2 S 3 O 10 - трисерная к-та HO O S O S О S OH O O O
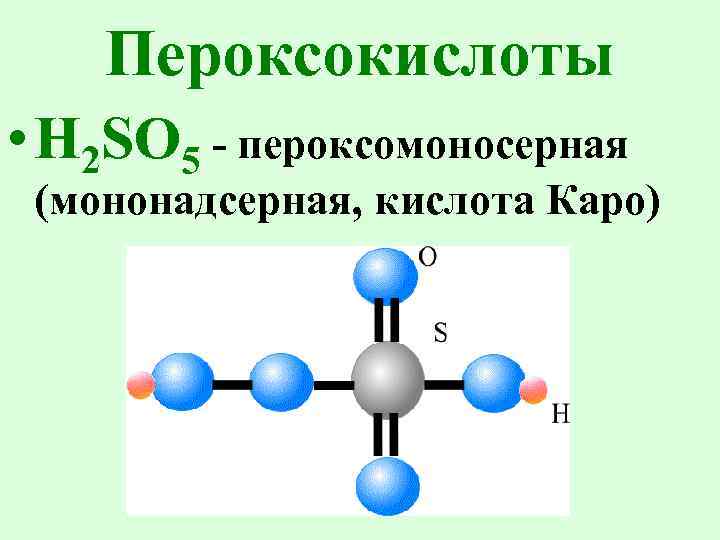 Пероксокислоты • H 2 SO 5 - пероксомоносерная (мононадсерная, кислота Каро)
Пероксокислоты • H 2 SO 5 - пероксомоносерная (мононадсерная, кислота Каро)
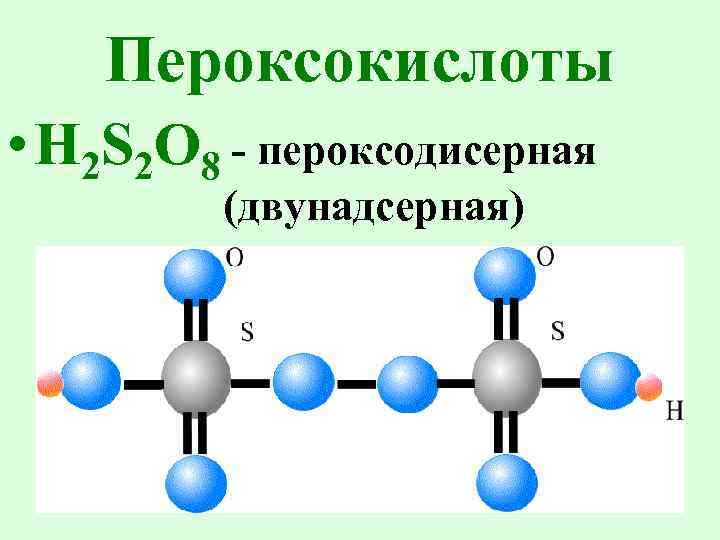 Пероксокислоты • H 2 S 2 O 8 - пероксодисерная (двунадсерная)
Пероксокислоты • H 2 S 2 O 8 - пероксодисерная (двунадсерная)
 Получение кислот • H 2 SO 4 + SO 3 = H 2 S 2 O 7 • H 2 SO 4 + 2 SO 3 = H 2 S 3 O 10 • H 2 SO 4 + H 2 O 2 = H 2 SO 5 + H 2 O • H 2 S 2 O 8 + H 2 O 2 = 2 H 2 SO 5 • H 2 SO 4 Электролиз H 2 S 2 O 8 (2 HSO 4 --2 e = H 2 S 2 O 8)
Получение кислот • H 2 SO 4 + SO 3 = H 2 S 2 O 7 • H 2 SO 4 + 2 SO 3 = H 2 S 3 O 10 • H 2 SO 4 + H 2 O 2 = H 2 SO 5 + H 2 O • H 2 S 2 O 8 + H 2 O 2 = 2 H 2 SO 5 • H 2 SO 4 Электролиз H 2 S 2 O 8 (2 HSO 4 --2 e = H 2 S 2 O 8)
 Химические свойства H 2 S 2 O 7 + H 2 O = 2 H 2 SO 4 H 2 SO 5 + H 2 O = H 2 SO 4 + H 2 O 2 H 2 S 2 O 8 + 2 H 2 O = 2 H 2 SO 4 + H 2 O 2 2 H 2 SO 5 o) (t = 2 H 2 SO 4 + O 2 K 2 S 2 O 8 + Cu = Cu. SO 4 + K 2 SO 4
Химические свойства H 2 S 2 O 7 + H 2 O = 2 H 2 SO 4 H 2 SO 5 + H 2 O = H 2 SO 4 + H 2 O 2 H 2 S 2 O 8 + 2 H 2 O = 2 H 2 SO 4 + H 2 O 2 2 H 2 SO 5 o) (t = 2 H 2 SO 4 + O 2 K 2 S 2 O 8 + Cu = Cu. SO 4 + K 2 SO 4
 Применение • H 2 SO 4 - важнейший продукт химической промышленности, ее используют: - в производстве HCl, CH 3 COOH, - фосфорных удобрений, - взрывчатых веществ, - органических красителей, - лекарственных препаратов, - для очистки нефтепродуктов, - в гидрометаллургии, - органическом синтезе
Применение • H 2 SO 4 - важнейший продукт химической промышленности, ее используют: - в производстве HCl, CH 3 COOH, - фосфорных удобрений, - взрывчатых веществ, - органических красителей, - лекарственных препаратов, - для очистки нефтепродуктов, - в гидрометаллургии, - органическом синтезе
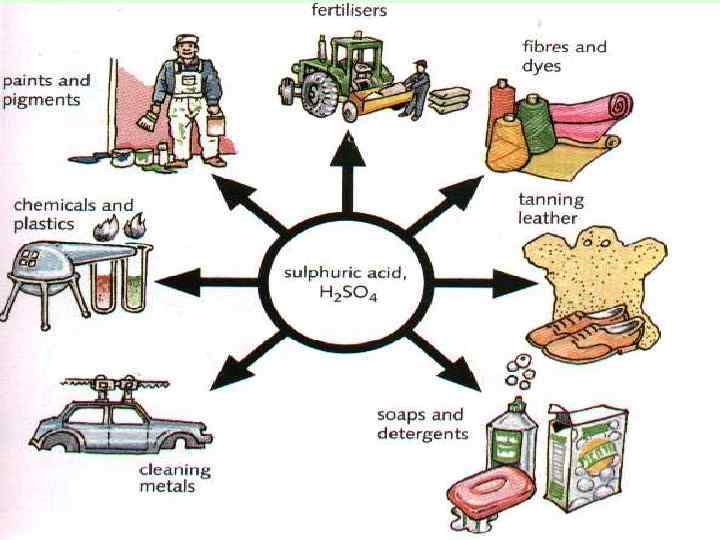
 • Na. HSO 3, NH 4 HSO 3, Ca(HSO 3)2 в целлюлозной промышленности • Na 2 S 2 O 3 - фотографии, в аналитической химии • (NH 4)2 SO 4 - удобрение • Na 2 SO 4 - в стекольной, бумажной, мыловаренной промышленности • Al 2(SO 4)3 - для осветления воды • Cu. SO 4. 5 H 2 O - для борьбы с вредителями в с/х
• Na. HSO 3, NH 4 HSO 3, Ca(HSO 3)2 в целлюлозной промышленности • Na 2 S 2 O 3 - фотографии, в аналитической химии • (NH 4)2 SO 4 - удобрение • Na 2 SO 4 - в стекольной, бумажной, мыловаренной промышленности • Al 2(SO 4)3 - для осветления воды • Cu. SO 4. 5 H 2 O - для борьбы с вредителями в с/х


