Л__ж_п_5.ppt
- Количество слайдов: 17

Лекция 5 Нарушение устойчивости растворов ВМС. Структурообразование. 1

Растворы ВМС как истинные растворы Межмолекулярные взаимодействия в растворах ВМС Ассоциация в растворах ВМС 2
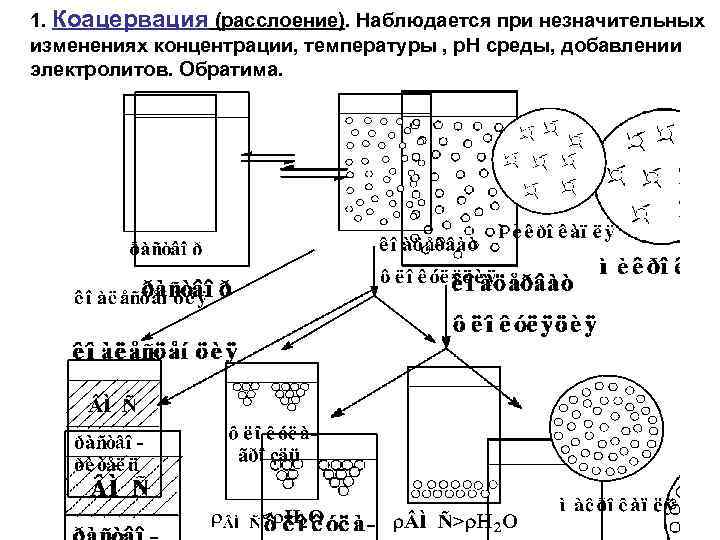
1. Коацервация (расслоение). Наблюдается при незначительных изменениях концентрации, температуры , р. Н среды, добавлении электролитов. Обратима. 3

2. Комплексная коацервация – нарушение устойчивости растворов белков при действии других биополимеров. Пример комплексного коацервата в организме — цитоплазма. 4

3. Высаливание — осаждение белка из раствора. Наблюдается при действии достаточно больших количеств негидролизующихся электролитов – солей ( или сильно гидратирующихся органических веществ: спирта, ацетона) Отличия высаливания белка и коагуляции золя Высаливание белка Коагуляция золя 1. Большое количество электролита. 1. Небольшое количество электролита. 2. Не подчиняется правилу Шульце-Гарди. 2. Подчиняется правилу Шульце-Гарди. 3. Причина – конкуренция за “свободную воду” между ионами добавляемого электролита и макромолекулами. 3. Причина – сжатие ДЭС, адсорбция ионов, уменьшение -потенциала. 4. Чаще всего необратима. 4. Обратима. 5
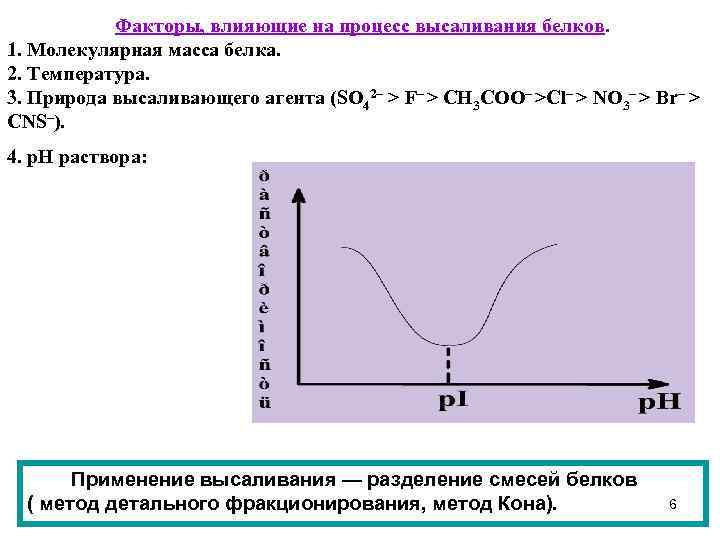
Факторы, влияющие на процесс высаливания белков. 1. Молекулярная масса белка. 2. Температура. 3. Природа высаливающего агента (SO 42– > F– > CH 3 COO– >Cl– > NO 3– > Br– > CNS–). 4. р. Н раствора: Применение высаливания — разделение смесей белков ( метод детального фракционирования, метод Кона). 6
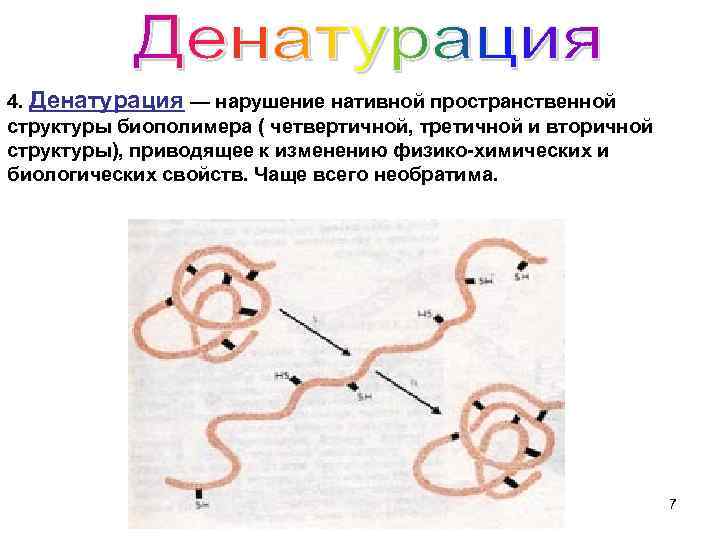
4. Денатурация — нарушение нативной пространственной структуры биополимера ( четвертичной, третичной и вторичной структуры), приводящее к изменению физико-химических и биологических свойств. Чаще всего необратима. 7

Факторы, вызывающие денатурацию Физические Химические Повышение температуры (глубокое Кислоты и щелочи (резкое нарушение конформации белков, разрушение водородных связей). Замораживание и оттаивание (то же что и при повышении температуры) Ультразвук (разворачивание макромолекул, вплоть до разрыва) Давление (то же, что под действием ультразвука) Проникающая радиация и УФизлучение (разрушение водородных связей, образование свободных радикалов, окисление дисульфидных мостиков) изменение р. Н среды, приводящее к изменению пространственной структуры) Соли тяжелых металлов (образование комплексных соединений и труднорастворимых солей по SHгруппам) Сильногидратирующиеся соли в больших количествах (обезвоживание белковых молекул) Органические растворители (обезвоживание белковых молекул) Гуанидин, мочевина (конкуренция за водородные связи в молекуле белка) Окислители и восстановители (разрушение и образование дисульфидных мостиков в третичной структуре белка) 8

Медико-биологическое значение денатурации – дезинфицирующие, дубящие, вяжущие средства; – лечение отравлений тяжелыми металлами; – термическая обработка пищевых продуктов; – медленная денатурация белковых систем организма — причина старения. 9

Коллоидные дисперсные системы и растворы ВМС при некоторых условиях способны образовывать пространственные структуры. Гели — коллоидные системы, потерявшие текучесть в результате образования в них внутренних структур; обычно эластичны, но могут быть и хрупкими. Студни — растворы ВМС, потерявшие текучесть в результате образования в них внутренних структур, эластичны. Гелеобразование — процесс превращения золей в гели. Застудневание — процесс превращения растворов ВМС в студни. Гели и студни — связнодисперсные системы. 10

1. Механизм гелеобразования В частично астабилизованных золях факторы устойчивости ослаблены на выступах, ребрах, углах коллоидных частиц, которыми они контактируют между собой. Коагуляционные структуры — в местах контактов коллоидных частиц остаются прослойки диcперсионной среды. Эти структуры эластичны. Конденсационно-кристаллизационные структуры — возникают либо в результате образования химических связей между частицами, либо вследствие сращивания кристаллов, возникших в результате выкристаллизовывания новой фазы в местах контактов (совершенствование контактов). Эти структуры более прочные и хрупкие. Образование таких структур лежит в основе сращивания обломков костей после переломов. 11
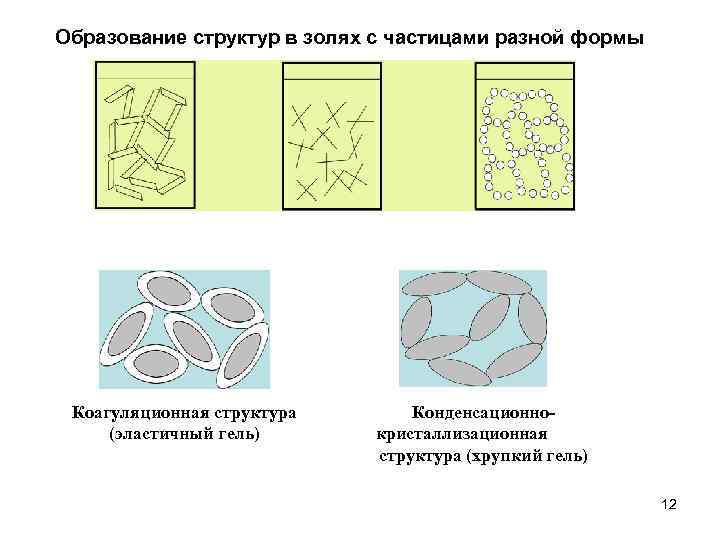
Образование структур в золях с частицами разной формы Коагуляционная структура (эластичный гель) Конденсационнокристаллизационная структура (хрупкий гель) 12

На гелеобразование влияют: — концентрация золя; — форма частиц и их размеры; — температура; — механические воздействия. 2. Механизм застудневания При определенных условиях время существования ассоциатов макромолекул становится очень большим и временные связи между ними могут превратиться в постоянные: — за счет сильновзаимодействующих полярных групп; — за счет взаимодействия противоположно заряженных ионизированных групп; — за счет возникновения химических связей (-S-S-); — за счет образования водородных связей; 13 — за счет гидрофобных взаимодействий.

Связи образуются между любыми участками макромолекул, на которых ослаблена или отсутствует гидратная оболочка (оголенные участки). Структура студня, образованного фибриллярным белком. На застудневание влияют: — концентрация раствора; — температура; — р. Н среды; — электролиты. 14

Особенности гелей и студней Гели при высыхании уменьшаются в объеме и становятся хрупкими, потом рассыпаются в порошок. Студни также уменьшаются в объеме, но сохраняют эластичность. Студни способны к набуханию, гели не набухают. Тиксотропия — способность структурированных систем (за исключением конденсационно-кристаллизационных структур) постепенно самопроизвольно восстанавливаться после их механического разрушения. 15

Синерезис — уменьшение объема эластичного геля или студня за счет усовершенствования контактов между мицеллами и перегруппировки их или увеличения числа контактов между макромолекулами. Скорость синерезиса увеличивается при незначительном повышении температуры; у белковых студней синерезис идет быстрее при р. Н = р. I и при действии электролитов, ухудшающих набухание. 16

Медико-биологическое значение студней, тиксотропии и синерезиса 17
Л__ж_п_5.ppt