Лек_5.ppt
- Количество слайдов: 26

Лекция 5. Метаболизм - основные понятия Синтез аминокислот в клетке Основные реакции: восстановительное аминирование прямое аминирование перенос амидной группы трансаминирование(переаминирование) Синтез аминокислот в клетке Семейства аминокислот Катаболизм аминокислот

Метаболизм – координированная и целенаправленная клеточная активность, которую обеспечивает участие многих взаимосвязанных мультиферментных систем. Четыре специфических функции метаболизма: • Снабжение химической энергией за счет расщепления субстратов или путем улавливания энергии солнечного света • Превращение молекул субстратов в блоки, которые используются для построения макромолекул • Синтез (сборка) белков, нуклеиновых кислот, липидов, полисахаридов и прочих клеточных компонентов • Синтез и разрушение молекул, которые необходимы для выполнения специфических функций

Метаболические пути – последовательность реакций, катализируемых мультиферментными системами. Метаболизм (в широком смысле) – обмен веществ и энергии в клетке Метаболизм (в узком смысле) – промежу точный метаболизм – превращение веществ внутри клетки с момента поступления до образования конечных продуктов.

Две фазы промежуточного метаболизма • • Катаболизм – расщепление сложных молекул до более простых конечных продуктов Анаболизм – биосинтез из малых молекул полимеров: белков, НК, липидов, полисахаридов и т. п.

Три стадии аэробного катаболизма 1. Макромолекулы распадаются на «строительные блоки» : полисахариды на гексозы и пентозы, жиры на жирные кислоты и глицерин, белки на аминокислоты и т. д. 2. Продукты первой стадии превращаются в еще более простые соединения: пируват (С 3) и Ацетил-Ко. А (перенос С 2) 3. Ацетил-Ко. А вступает в ЦЛК (цикл лимонной кислот) и окисляется до СО 2, Н 2 О и NH 3
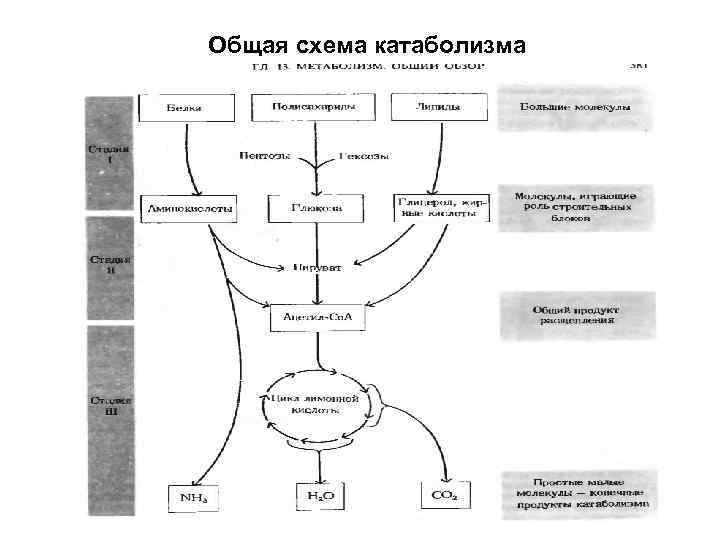
Общая схема катаболизма

Три стадии анаболизма (на примере белков) 1. Цикл лимонной кислоты поставляет кетокислоты и другие предшественники аминокислот 2. Кетокислоты + аминогруппы → аминокислоты 3. Синтез специфических полимеров (аминокислоты – белки)

Катаболические и анаболические пути не совпадают (они специфичны): 1. 2. 3. Пути по которым идет расщепление биомолекул могут быть непригодны для их синтеза по энергетическим соображениям Пути катаболизма и анаболизма локализованы в разных частях клетки (компартментах) Различия в регуляции (аллостерическая и биоэнергетическая) Катаболические и анаболические пути связывает общая стадия – амфиболическая. Она выполняет двойную функцию: в катаболизме – распад молекул, в анаболизме – поставка молекул предшественников для биосинтеза аминокислот, жирных кислот и углеводов
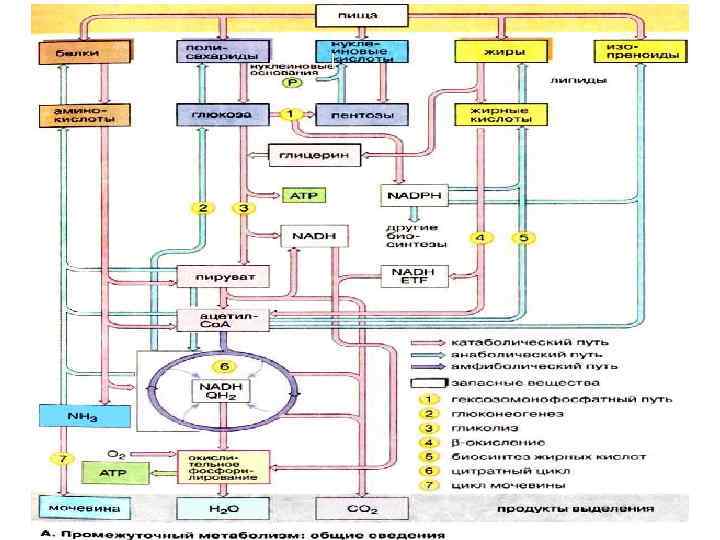

Химическая энергия, запасенная в молекулах АТФ, идет на следующие виды работы в клетке 1. 2. 3. 4. АТФ для химической работы биосинтеза АТФ как источник энергии для процессов движения и сокращения АТФ необходима для переноса веществ через мембрану (транспорта) АТФ используется в процессах передачи информации при синтезе НК

Регуляция метаболических путей (три уровня) • • • Действие аллостерических ферментов (наиболее быстрая) Гормональная регуляция (у высших животных) Изменение концентрации фермента в клетке (индукция ферментов)

Образование аминокислот в клетке (4 основные реакции) 1. Реакция восстановительного аминирования (аланин, аспарагиновая, глютаминовая) – L-аланиндегидрогеназа, L-аспартатдегидрогеназа, L-глютаматдегидрогеназа CH 3 COCOOH + NH 4+ + НАДH 2 → CH 3 CH(NH 2)COOH + НАД + H 2 O 2. Реакция прямого аминирования аминокислоты с образованием амида аминокислоты – глютаминсинтетаза COOH(CH 2)2 CH(NH 2)COOH + NH 4+ + АТФ → → CO(NH 2)(CH 2)2 CH(NH 2)COOH + АДФ + H 2 O 3. Перенос амидной группы с глютамина на кетогруппу – глютаматсинтаза (трансфераза) CH 3(CH 2)2 COCOOH + CO(NH 2)(CH 2)2 CH(NH 2)COOH → → 2 COOH(CH 2)2 CH(NH 2)COOH 4. Перенос амино-группы с глютаминовой кислоты, аланина, валина на другие аминокислоты – реакция трансаминирования (трансаминаза) CH 3 COCOOH + COOH(CH 2)2 CH(NH 2)COOH → → CH 3 CH(NH 2)COOH + CH 3(CH 2)2 COCOOH
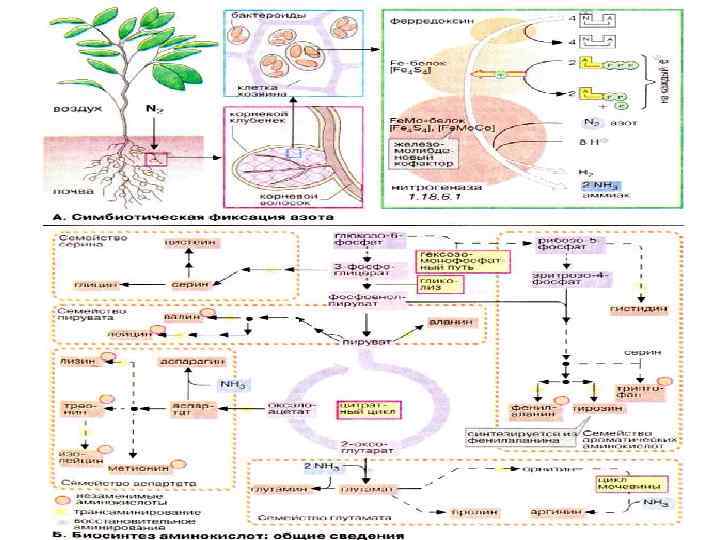

Семейства аминокислот • Семейство глутамата: глутаминовая, глутамин, пролин, аргинин, орнитин, цитруллин • Семейство аспартата: лизин, ДАПК, аспарагиновая, аспарагин, гомосерин, метионин, треонин, изолейцин, • Семество пирувата (аланина): аланин, валин, лейцин • Семейство серина: серин, глицин, цистеин, цистин • Семейство ароматических аминокислот: триптофан, тирозин, фенилаланин • Семейство гистидина Таблица

Семейство пирувата (аланина): аланин, валин, лейцин • Аланин образуется в результате восстановительного аминирования пирувата (реакция 1) – аланиндегидрогеназа CH 3 COCOOH + NH 4+ + НАДH 2 → CH 3 CH(NH 2)COOH + НАД + H 2 O • Аланин образуется в результате трансаминирования из пирувата и глутамата (реакция 4) – трансаминаза CH 3 COCOOH + COOH(CH 2)2 CH(NH 2)COOH → → CH 3 CH(NH 2)COOH + CH 3(CH 2)2 COCOOH

Семейство ароматических аминокислот (фенилаланин, тирозин, триптофан) • Пути синтеза этих аминокислот сложные и длинные, включают в себя от 5 до 15 этапов. Неспособность высших животных синтезировать незаменимые аминокислоты связана с отсутствием у них ферментов дегидрогеназ и редуктаз ароматических соединений, необходимых для этого синтеза. • Наибольшей сложностью отличаются пути, ведущие к синтезу фениналанина, триптофана, гистидина, содержащих бензольные кольца или гетероциклы, особенно триптофан – два кольца. • Важные промежуточные соединения, ведущие к синтезу ароматических аминокислот: шикимовая и хоризмовая кислоты. • Ароматические аминокислоты служат важными субстратами для синтеза вторичных метаболитов (производные фенолов, хинонов, витаминов, стероидов и т. д. )

Катаболизм аминокислот Протеолиз и расщепление аминокислот (протеиназа и пептидазы) Белок → полипептид → олигопептид → аминокислоты Пептидазы – протеолитические ферменты Белки + пепсин → пептон ( полипептиды + олигопептиды + 30% свободных аминокислот) Экзопептидазы: аминопептидазы – расщепляют с N-конца карбоксипептидазы - расщепляют с С-конца Эндопептидазы – расщепление пептидных связей внутри пептидной цепи – ферменты микробного происхождения: субтилизин, эндопептидаза из Alternaria sp. , клостридиопептидаза
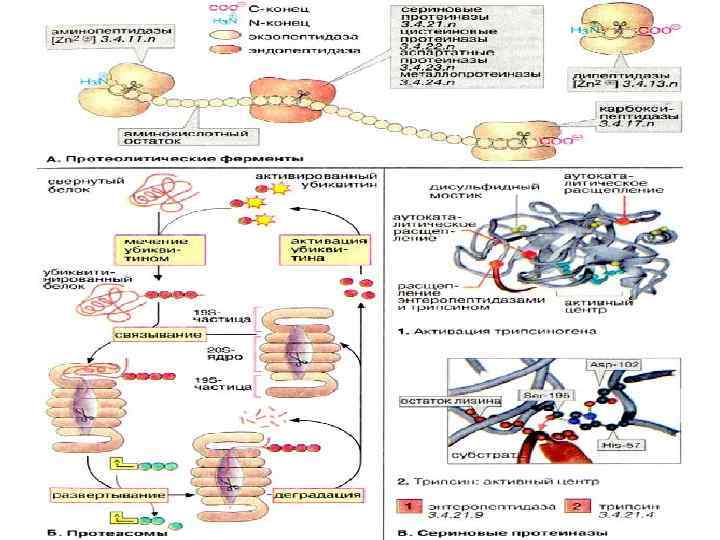

Катаболизм аминокислот Дезаминирование: окислительное аммиаклиаза –→ жирная кислота с двойной связью дегидрогеназа –→ кетокислота гидролитическое трансаминаза –→ гидроксижирная кислота окислительно-восстановительное: реакция Стикленда Декарбоксилирование декарбоксилазы аминокислота → другая аминокислота (аспартат → аланин) аминокислота → амин (гистидин → гистамин)

Катаболизм аминокислот Дезаминирование: окислительное (аммиак-лиаза) R – CH 2 – CH (NH 2) – COOH → R – CH=CH – COOH + NH 3 окислительное (дегидрогеназа) R – CH 2 – CH (NH 2) – COOH → R – CH 2 – COOH + NH 3 восстановительное R – CH 2 – CH (NH 2) – COOH → R – CH 2 – COOH + NH 3 гидролитическое (трансамидаза) R – CH 2 – CH (NH 2) – CONH 2 → R – CH 2 – CH (NH 2) – COOH + NH 3 R – CH 2 – CH (NH 2) – COOH → R – CH 2 – CH (OH) – COOH + NH 3 окислительно-восстановительное (реакция Стикленда) O 2 2 R – CH (NH 2) – COOH → R – COOH + R – CH 2 – COOH + 2 NH 3 NAD
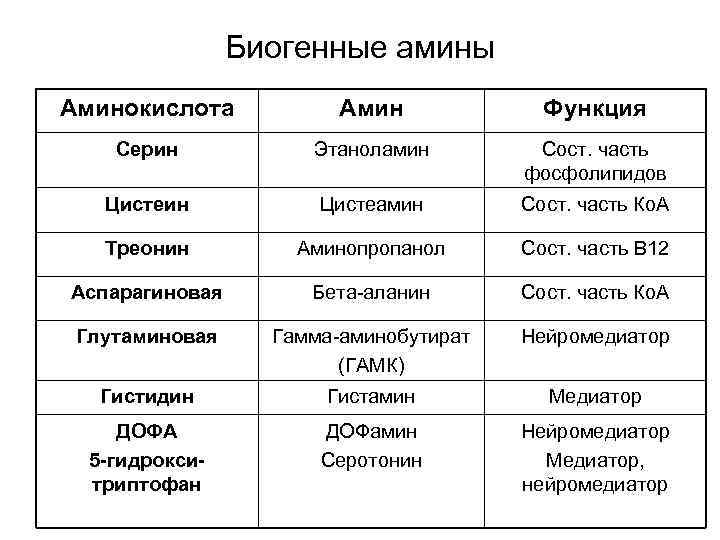
Биогенные амины Аминокислота Амин Функция Серин Этаноламин Сост. часть фосфолипидов Цистеин Цистеамин Сост. часть Ко. А Треонин Аминопропанол Сост. часть В 12 Аспарагиновая Бета-аланин Сост. часть Ко. А Глутаминовая Гамма-аминобутират (ГАМК) Нейромедиатор Гистидин Гистамин Медиатор ДОФА 5 -гидрокситриптофан ДОФамин Серотонин Нейромедиатор Медиатор, нейромедиатор

Выведение из организма аминного азота • Аммониотелические животные → NH 4+ водные позвоночные, костные рыбы, личинки амфибий глутамин → глутамат → NH 4+ (в воду) (глутаминаза) • Уреотелические животные → CO(NH 2)2 – большинство наземных позвоночных животных, акулы • Урикотелические животные → мочевая кислота (азотистое основание – 4 атома азота) – птицы, змеи, ящерицы
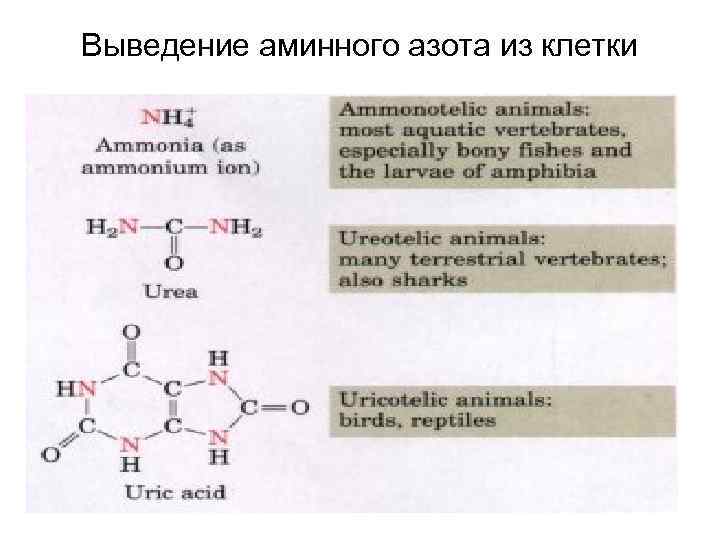
Выведение аминного азота из клетки
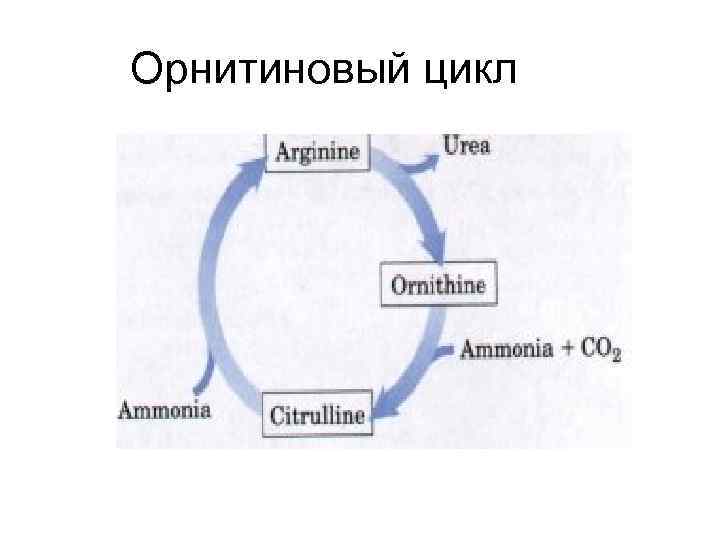
Орнитиновый цикл

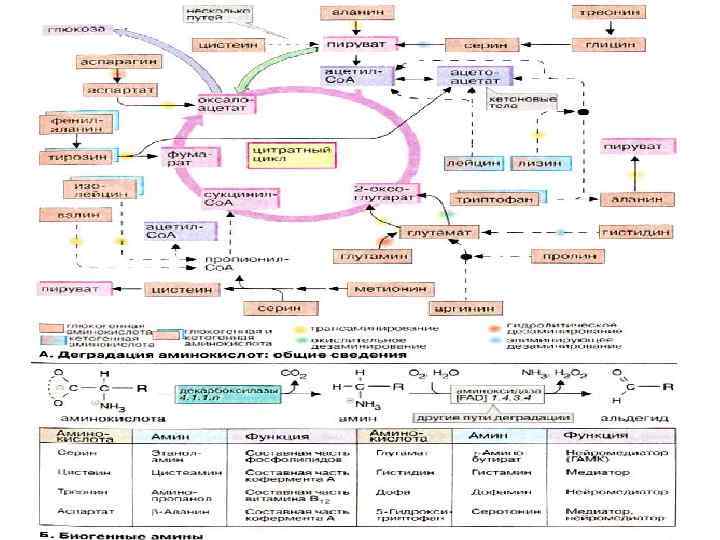
Деградация углеродных скелетов • Глюкогенные – служат предшественниками в процессе глюконеогенеза – аланин, аргинин, аспарагиновая, аспарагин, валин, гистидин, глицин, глутаминовая, глутамин, метионин, пролин, серин, треонин, цистеин, триптофан • Кетогенные – превращаются в ацетоацетат и ацетил-Ко. А, используются для синтеза жирных кислот и изопреноидов – лейцин, лизин • Кетогенные и глюкогенные – фенилаланин, тирозин, триптофан, изолейцин
Лек_5.ppt