Лекция №5 «Лекарственные средства производные р-элементов VI гр.




![4 Во второй реакции подлинности используют образование [CrO5L], имеющего синюю окраску в эфире. К 4 Во второй реакции подлинности используют образование [CrO5L], имеющего синюю окраску в эфире. К](https://present5.com/presentacii-2/20171208\18854-prod._vi_gr.___v_gr._2012.ppt\18854-prod_vi_gr___v_gr_2012_4.jpg)



















![26 Определение сульфидов проводят в аммиачном растворе с нитропруссидом натрия: Na2S + Na2[Fe(CN)5NO] 26 Определение сульфидов проводят в аммиачном растворе с нитропруссидом натрия: Na2S + Na2[Fe(CN)5NO]](https://present5.com/presentacii-2/20171208\18854-prod._vi_gr.___v_gr._2012.ppt\18854-prod_vi_gr___v_gr_2012_26.jpg)



















































18854-prod._vi_gr.___v_gr._2012.ppt
- Количество слайдов: 86
 Лекция №5 «Лекарственные средства производные р-элементов VI гр. ПСЭ» (продолжение) 11.10.2012 Кафедра фармацевтической и токсикологической химии доц. Богословская О.А.
Лекция №5 «Лекарственные средства производные р-элементов VI гр. ПСЭ» (продолжение) 11.10.2012 Кафедра фармацевтической и токсикологической химии доц. Богословская О.А.
 2 ЛЕКАРСТВЕННЫЕ СРЕДСТВА Кислород вода очищенная вода для инъекций растворы пероксида водорода пероксид магния гидроперит тиосульфат натрия
2 ЛЕКАРСТВЕННЫЕ СРЕДСТВА Кислород вода очищенная вода для инъекций растворы пероксида водорода пероксид магния гидроперит тиосульфат натрия
 3 Первая реакция подлинности. Основана на окислительных свойствах H2O2. К раствору Н2О2 добавляют разведенную H2SO4 и KI, а затем хлороформ. Смесь взбалтывают. Образовавшийся в результате реакции свободный I2 окрашивает слой хлороформа в фиолетовый цвет: H2O2 + 2KI + H2SO4 I2 + K2SO4 + 2H2O
3 Первая реакция подлинности. Основана на окислительных свойствах H2O2. К раствору Н2О2 добавляют разведенную H2SO4 и KI, а затем хлороформ. Смесь взбалтывают. Образовавшийся в результате реакции свободный I2 окрашивает слой хлороформа в фиолетовый цвет: H2O2 + 2KI + H2SO4 I2 + K2SO4 + 2H2O
![>4 Во второй реакции подлинности используют образование [CrO5L], имеющего синюю окраску в эфире. К >4 Во второй реакции подлинности используют образование [CrO5L], имеющего синюю окраску в эфире. К](https://present5.com/presentacii-2/20171208\18854-prod._vi_gr.___v_gr._2012.ppt\18854-prod_vi_gr___v_gr_2012_4.jpg) 4 Во второй реакции подлинности используют образование [CrO5L], имеющего синюю окраску в эфире. К подкисленному раствору H2O2 добавляют диэтиловый эфир и несколько капель раствора дихромата калия. После взбалтывания эфирный слой окрашивается в синий цвет: K2Cr2O7+H2SO4(разб.) + 4H2O2 (конц) 2[Cr(H2O)O(O2)2] + 3H2O + K2SO4 пероксохромат [Cr(H2O)O(O2)2](р-р) + L(ж) [Cr(L)O(O2)2] + H2O (синий р-р) [CrO5L]- комплексы представляют собой пентагональную пирамиду, в которой хром находится вне плоскости основания
4 Во второй реакции подлинности используют образование [CrO5L], имеющего синюю окраску в эфире. К подкисленному раствору H2O2 добавляют диэтиловый эфир и несколько капель раствора дихромата калия. После взбалтывания эфирный слой окрашивается в синий цвет: K2Cr2O7+H2SO4(разб.) + 4H2O2 (конц) 2[Cr(H2O)O(O2)2] + 3H2O + K2SO4 пероксохромат [Cr(H2O)O(O2)2](р-р) + L(ж) [Cr(L)O(O2)2] + H2O (синий р-р) [CrO5L]- комплексы представляют собой пентагональную пирамиду, в которой хром находится вне плоскости основания
 5 В MgO2 дополнительно определяют Mg2+ по образованию белого кристаллического осадка NH4MgPO4 при взаимодействии с раствором водородфосфата натрия в присутствии хлорида аммония и аммиака: MgCl2 + Na2HPO4 + NH3 NH4MgPO4 + 2NaCl
5 В MgO2 дополнительно определяют Mg2+ по образованию белого кристаллического осадка NH4MgPO4 при взаимодействии с раствором водородфосфата натрия в присутствии хлорида аммония и аммиака: MgCl2 + Na2HPO4 + NH3 NH4MgPO4 + 2NaCl
 6 Подлинность ЕР: HYDROGEN PEROXIDE SOLUTION (3 PER CENT) HYDROGEN PEROXIDE SOLUTION (30 PER CENT) перманганатометрическим методом в кислой среде К подкисленному раствору H2O2 добавляют диэтиловый эфир и несколько капель раствора дихромата калия. После взбалтывания эфирный слой окрашивается в синий цвет MAGNESIUM PEROXIDE На Mg2+ добавляют диэтиловый эфир и несколько капель раствора дихромата калия. 6
6 Подлинность ЕР: HYDROGEN PEROXIDE SOLUTION (3 PER CENT) HYDROGEN PEROXIDE SOLUTION (30 PER CENT) перманганатометрическим методом в кислой среде К подкисленному раствору H2O2 добавляют диэтиловый эфир и несколько капель раствора дихромата калия. После взбалтывания эфирный слой окрашивается в синий цвет MAGNESIUM PEROXIDE На Mg2+ добавляют диэтиловый эфир и несколько капель раствора дихромата калия. 6
 7 Количественное определение Используя восстановительные свойства пероксида водорода, количественное определение проводят перманганатометрическим методом в кислой среде: (фармакопейный метод) 2KМnO4 + 5Н2О2 + 3Н2SО4 2MnSO4 + К2SО4 + 8Н2O + 5O2 Точку эквивалентности определяют по исчезновению окраски перманаганат-иона. Используя окислительные свойства пероксида водорода, количественное определение можно проводить йодометрическим методом: 2KI + H2O2 + H2SO4 I2 + K2SO4 + 2H2О Образующийся йод оттитровывают стандартным раствором тиосульфата натрия: I2 + 2Nа2S2O3 2 NaI + Na2S4O6
7 Количественное определение Используя восстановительные свойства пероксида водорода, количественное определение проводят перманганатометрическим методом в кислой среде: (фармакопейный метод) 2KМnO4 + 5Н2О2 + 3Н2SО4 2MnSO4 + К2SО4 + 8Н2O + 5O2 Точку эквивалентности определяют по исчезновению окраски перманаганат-иона. Используя окислительные свойства пероксида водорода, количественное определение можно проводить йодометрическим методом: 2KI + H2O2 + H2SO4 I2 + K2SO4 + 2H2О Образующийся йод оттитровывают стандартным раствором тиосульфата натрия: I2 + 2Nа2S2O3 2 NaI + Na2S4O6
 8 Количественное определение магния пероксида проводят перманганатометрическим титрованием. Препарат должен содержать не менее 25 % пероксида магния. Содержание пероксида водорода в таблетках гидроперита устанавливают йодометрическим титрованием. Таблетка массой 1,5 г должна содержать не менее 0,48 г пероксида водорода.
8 Количественное определение магния пероксида проводят перманганатометрическим титрованием. Препарат должен содержать не менее 25 % пероксида магния. Содержание пероксида водорода в таблетках гидроперита устанавливают йодометрическим титрованием. Таблетка массой 1,5 г должна содержать не менее 0,48 г пероксида водорода.
 Количественное определение ЕР: HYDROGEN PEROXIDE SOLUTION (3 PER CENT) HYDROGEN PEROXIDE SOLUTION (30 PER CENT) MAGNESIUM PEROXIDE перманганатометрическим методом в кислой среде 9
Количественное определение ЕР: HYDROGEN PEROXIDE SOLUTION (3 PER CENT) HYDROGEN PEROXIDE SOLUTION (30 PER CENT) MAGNESIUM PEROXIDE перманганатометрическим методом в кислой среде 9
 Чистота (ЕР): HYDROGEN PEROXIDE SOLUTION (3 PER CENT) HYDROGEN PEROXIDE SOLUTION (30 PER CENT) Кислотность Содержание органического стабилизатора (250ppm) [по ГФ стабилизатор –антифебрин (ацетанилид) 0,05% определяют по реакции подлинности на первичные ароматические амины] Нелетучий остаток -2г/л 10
Чистота (ЕР): HYDROGEN PEROXIDE SOLUTION (3 PER CENT) HYDROGEN PEROXIDE SOLUTION (30 PER CENT) Кислотность Содержание органического стабилизатора (250ppm) [по ГФ стабилизатор –антифебрин (ацетанилид) 0,05% определяют по реакции подлинности на первичные ароматические амины] Нелетучий остаток -2г/л 10
 MAGNESIUM PEROXIDE Кислотность и щелочность. К р-ру добавляют 0,1 мл фенолфталеина , требуется не более 0.2 мл 0.1 M HCl для изменения окраски индикатора Нерастворимые вещества: до 0.1 %. Растворимые вещества: мах.1.5 %. Chlorides : мах.0.1 %. Sulphates : мах. 0.5 %. Arsenic : мах. 4 ppm. Calcium : мах. 1.0 %. Iron (2.4.9) : мах. 500 ppm. Heavy metals (2.4.8) : мах. 30 ppm. 11
MAGNESIUM PEROXIDE Кислотность и щелочность. К р-ру добавляют 0,1 мл фенолфталеина , требуется не более 0.2 мл 0.1 M HCl для изменения окраски индикатора Нерастворимые вещества: до 0.1 %. Растворимые вещества: мах.1.5 %. Chlorides : мах.0.1 %. Sulphates : мах. 0.5 %. Arsenic : мах. 4 ppm. Calcium : мах. 1.0 %. Iron (2.4.9) : мах. 500 ppm. Heavy metals (2.4.8) : мах. 30 ppm. 11
 12 Применение Раствор пероксида водорода применяют в качестве Антисептического средства Антисептическое действие обусловлено оксидантным эффектом — при контакте с поврежденной кожей и слизистыми водорода пероксид под влиянием каталазы и пероксидазы распадается с выделением кислорода, что создает неблагоприятные условия для развития микроорганизмов, особенно анаэробной и гнилостной флоры; Но действие пероксида характеризуется малой продолжительностью и слабой выраженностью эффекта.
12 Применение Раствор пероксида водорода применяют в качестве Антисептического средства Антисептическое действие обусловлено оксидантным эффектом — при контакте с поврежденной кожей и слизистыми водорода пероксид под влиянием каталазы и пероксидазы распадается с выделением кислорода, что создает неблагоприятные условия для развития микроорганизмов, особенно анаэробной и гнилостной флоры; Но действие пероксида характеризуется малой продолжительностью и слабой выраженностью эффекта.
 кровеостанавливающего, При попадании раствора в рану происходит разрушение (окисление) протеинов, крови, гноя, и механическое ее очищение вследствие обильного пенообразования (за счет пузырьков газа, поднимающихся со стенок) от загрязняющих частиц, мелких инородных тел, сгустков крови. Это вспенивание способствует тромбообразованию и остановке кровотечений из мелких сосудов. 13
кровеостанавливающего, При попадании раствора в рану происходит разрушение (окисление) протеинов, крови, гноя, и механическое ее очищение вследствие обильного пенообразования (за счет пузырьков газа, поднимающихся со стенок) от загрязняющих частиц, мелких инородных тел, сгустков крови. Это вспенивание способствует тромбообразованию и остановке кровотечений из мелких сосудов. 13
 дезодорирующего депигментирующего средства. для промываний для полосканий, (предварительно разбавляя 3% раствор пероксида водорода водой до 0,25 %) в качестве антидота (в комбинации с 3% раствором уксусной кислоты) при отравлении перманганатом калия. 14
дезодорирующего депигментирующего средства. для промываний для полосканий, (предварительно разбавляя 3% раствор пероксида водорода водой до 0,25 %) в качестве антидота (в комбинации с 3% раствором уксусной кислоты) при отравлении перманганатом калия. 14
 15 Одна таблетка гидроперита (1,5 г) соответствует 15 мл 3 % раствора пероксида водорода. При растворении таблетки в стакане воды получают 0.25 % раствор пероксида водорода. Пероксид магния применяют при желудочно-кишечных заболеваниях по 0,25— 0.5 г 3—4 раза в день.
15 Одна таблетка гидроперита (1,5 г) соответствует 15 мл 3 % раствора пероксида водорода. При растворении таблетки в стакане воды получают 0.25 % раствор пероксида водорода. Пероксид магния применяют при желудочно-кишечных заболеваниях по 0,25— 0.5 г 3—4 раза в день.
 16 Хранение 3% р-р пероксида водорода хранят в склянках с притертыми стеклянными пробками, в прохладном защищенном от света месте. Твердые препараты пероксида водорода хранят в сухом, защищенном от света месте, в хорошо закрытой таре при комнатной температуре. В присутствии влаги пероксида магния образует гидраты: MgO2.H2O и MgO2.2H2O.
16 Хранение 3% р-р пероксида водорода хранят в склянках с притертыми стеклянными пробками, в прохладном защищенном от света месте. Твердые препараты пероксида водорода хранят в сухом, защищенном от света месте, в хорошо закрытой таре при комнатной температуре. В присутствии влаги пероксида магния образует гидраты: MgO2.H2O и MgO2.2H2O.
 17 В соответствии с требованиями ФС концентрированные и разбавленные растворы пероксида водорода должны содержать стабилизатор. В качестве стабилизатора используют бензоат натрия (раствор пероксида водорода должен в 100 мл содержать 10 г пероксида водорода (30%) и 0,05г стабилизатора). Стабилизатор добавляют для предотвращения разложения пероксида водорода ферментами: каталазой, пероксидазой, содержащихся в крови, слюне и других биологических жидкостях.
17 В соответствии с требованиями ФС концентрированные и разбавленные растворы пероксида водорода должны содержать стабилизатор. В качестве стабилизатора используют бензоат натрия (раствор пероксида водорода должен в 100 мл содержать 10 г пероксида водорода (30%) и 0,05г стабилизатора). Стабилизатор добавляют для предотвращения разложения пероксида водорода ферментами: каталазой, пероксидазой, содержащихся в крови, слюне и других биологических жидкостях.
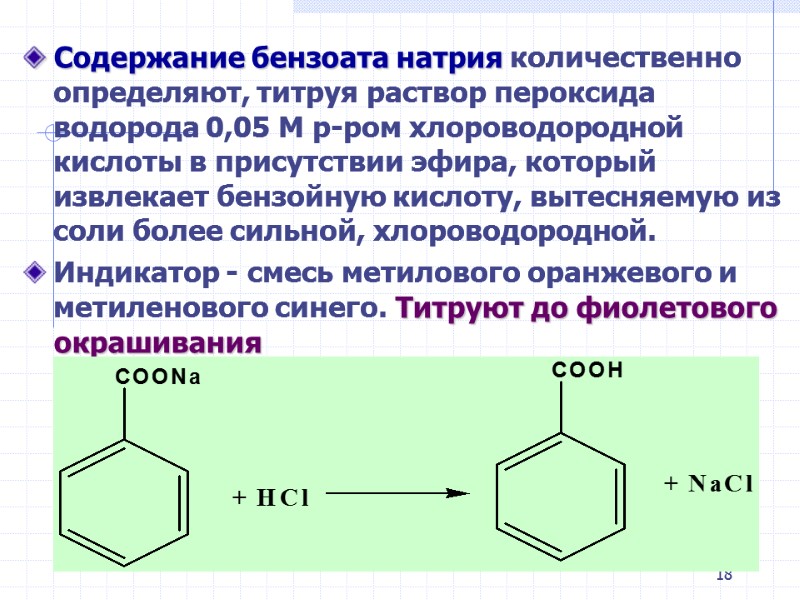
 18 Содержание бензоата натрия количественно определяют, титруя раствор пероксида водорода 0,05 М р-ром хлороводородной кислоты в присутствии эфира, который извлекает бензойную кислоту, вытесняемую из соли более сильной, хлороводородной. Индикатор - смесь метилового оранжевого и метиленового синего. Титруют до фиолетового окрашивания
18 Содержание бензоата натрия количественно определяют, титруя раствор пероксида водорода 0,05 М р-ром хлороводородной кислоты в присутствии эфира, который извлекает бензойную кислоту, вытесняемую из соли более сильной, хлороводородной. Индикатор - смесь метилового оранжевого и метиленового синего. Титруют до фиолетового окрашивания
 19 Соединения серы Натрия тиосульфат - Natrii thiosulfas Na2S2O3.5H2O Бесцветные прозрачные кристаллы. В сухой атмосфере выветриваются, образуя белые кристаллы безводной соли, во влажном воздухе – расплываются вследствие большой гигроскопичности. Препарат легко растворим в воде (1:1), практически нерастворим в этаноле. В водном растворе наблюдается слабый гидролиз по аниону: S2O32- + H2O HS2O3- + OH- pKb = 12.28 рН водного раствора 8.0-8.4. Поэтому при добавлении фенолфталеина раствор не должен принимать розовую окраску (интервал перехода окраски фенофталеина: рН 8.2-9.8).
19 Соединения серы Натрия тиосульфат - Natrii thiosulfas Na2S2O3.5H2O Бесцветные прозрачные кристаллы. В сухой атмосфере выветриваются, образуя белые кристаллы безводной соли, во влажном воздухе – расплываются вследствие большой гигроскопичности. Препарат легко растворим в воде (1:1), практически нерастворим в этаноле. В водном растворе наблюдается слабый гидролиз по аниону: S2O32- + H2O HS2O3- + OH- pKb = 12.28 рН водного раствора 8.0-8.4. Поэтому при добавлении фенолфталеина раствор не должен принимать розовую окраску (интервал перехода окраски фенофталеина: рН 8.2-9.8).
 20 Получение 1. Кипячением раствора сульфита натрия с серой: Na2SO3 + S Na2S2O3 Окончание процесса устанавливают по отрицательной реакции на сульфит-ионы с раствором хлорида кальция (отсутствие осадка СаSОз). Избыток серы отфильтровывают, а фильтрат выпаривают. При этом образуется кристаллогидрат Na2S2O3.5H2O. 2. Окислительно-восстановительной реакцией 2.а) сульфидов (Na2S, CaS) с диоксидом серы: 2Na2S + 3SO2 → 2Na2S2O3 + S 2.б) полисульфидов (CaS2) с кислородом: 2CaS2 + 3O2 → 2CaS2O3 3. сплавления кальция тиосульфата с сульфатом натрия: CaS2O3+ Na2SO4 → Na2S2O3 + CaSO4
20 Получение 1. Кипячением раствора сульфита натрия с серой: Na2SO3 + S Na2S2O3 Окончание процесса устанавливают по отрицательной реакции на сульфит-ионы с раствором хлорида кальция (отсутствие осадка СаSОз). Избыток серы отфильтровывают, а фильтрат выпаривают. При этом образуется кристаллогидрат Na2S2O3.5H2O. 2. Окислительно-восстановительной реакцией 2.а) сульфидов (Na2S, CaS) с диоксидом серы: 2Na2S + 3SO2 → 2Na2S2O3 + S 2.б) полисульфидов (CaS2) с кислородом: 2CaS2 + 3O2 → 2CaS2O3 3. сплавления кальция тиосульфата с сульфатом натрия: CaS2O3+ Na2SO4 → Na2S2O3 + CaSO4
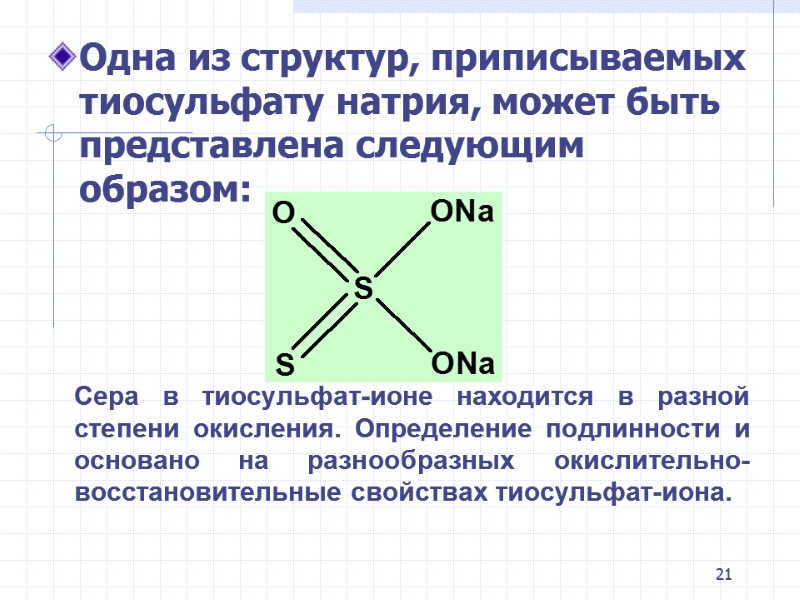
 21 Одна из структур, приписываемых тиосульфату натрия, может быть представлена следующим образом: Сера в тиосульфат-ионе находится в разной степени окисления. Определение подлинности и основано на разнообразных окислительно-восстановительные свойствах тиосульфат-иона.
21 Одна из структур, приписываемых тиосульфату натрия, может быть представлена следующим образом: Сера в тиосульфат-ионе находится в разной степени окисления. Определение подлинности и основано на разнообразных окислительно-восстановительные свойствах тиосульфат-иона.
 22 1.ГФ, ЕР: Тиосульфат-ион обнаруживают по опалесценции, вследствие выделения серы, и появлению запаха диоксида серы при добавлении к раствору препарата хлороводородной кислоты: Na2S2O3 + 2НСl SO2 + S+ 2NaCl + H2O ЕР: выделившийся SO2 окрашивает йодат –крахмальную бумагу в синий цвет 2. ГФ, ЕР: С избытком раствора нитрата серебра сначала образуется белый осадок тиосульфата серебра, который быстро разлагается: желтеет, буреет и, становится черным: Na2S2O3 + 2AgNO3 Ag2S2O3+ 2NaNO3 Ag2S2O3 Ag2SO3 + S Ag2S (белый) (желтый) (черный ) Определение подлинности
22 1.ГФ, ЕР: Тиосульфат-ион обнаруживают по опалесценции, вследствие выделения серы, и появлению запаха диоксида серы при добавлении к раствору препарата хлороводородной кислоты: Na2S2O3 + 2НСl SO2 + S+ 2NaCl + H2O ЕР: выделившийся SO2 окрашивает йодат –крахмальную бумагу в синий цвет 2. ГФ, ЕР: С избытком раствора нитрата серебра сначала образуется белый осадок тиосульфата серебра, который быстро разлагается: желтеет, буреет и, становится черным: Na2S2O3 + 2AgNO3 Ag2S2O3+ 2NaNO3 Ag2S2O3 Ag2SO3 + S Ag2S (белый) (желтый) (черный ) Определение подлинности
 23 3. ЕР: обесцвечивание раствора йода 2Na2S2O3 + I2 = 2NaI + Na2S4O6 4. ГФ, ЕР: Препарат дает характерные реакции на натрий-ион. ● В результате реакции с раствором хлорида железа (III) образуется фиолетовый осадок тиосульфата железа: 3Na2S2O3 + 2FeCl3 Fe2 (S2O3)3↓ + 6NaCl
23 3. ЕР: обесцвечивание раствора йода 2Na2S2O3 + I2 = 2NaI + Na2S4O6 4. ГФ, ЕР: Препарат дает характерные реакции на натрий-ион. ● В результате реакции с раствором хлорида железа (III) образуется фиолетовый осадок тиосульфата железа: 3Na2S2O3 + 2FeCl3 Fe2 (S2O3)3↓ + 6NaCl
 24 Оценка чистоты Допустимые примеси - хлориды, тяжелые металлы, железо. Недопустимые примеси - сульфиды, сульфиты, сульфаты, ионы кальция, а также мышьяк и селен. ЕР: сульфиды –недопустимая примесь Для определения примеси хлоридов необходимо сначала удалить из пробы сам тиосульфат-ион, который мешает определению (т.к. с нитратом серебра тиосульфат-ион дает белый осадок Ag2S2O3). Поэтому к пробе вначале прибавляют холодную разбавленную азотную куслоту: Na2S2O3 + 2HNO3 (разб. хол.) H2O + SO2+ S↓ + 2NaNO3 Осадок серы отфильтровывают и определяют хлорид-ионы с нитратом серебра.
24 Оценка чистоты Допустимые примеси - хлориды, тяжелые металлы, железо. Недопустимые примеси - сульфиды, сульфиты, сульфаты, ионы кальция, а также мышьяк и селен. ЕР: сульфиды –недопустимая примесь Для определения примеси хлоридов необходимо сначала удалить из пробы сам тиосульфат-ион, который мешает определению (т.к. с нитратом серебра тиосульфат-ион дает белый осадок Ag2S2O3). Поэтому к пробе вначале прибавляют холодную разбавленную азотную куслоту: Na2S2O3 + 2HNO3 (разб. хол.) H2O + SO2+ S↓ + 2NaNO3 Осадок серы отфильтровывают и определяют хлорид-ионы с нитратом серебра.
 25 При определении тяжелых металлов (≤ 0,001%). Разложение осуществляют разведенной HCl. После полной коагуляции серы и удалении SO2 (диоксида серы) при кипячении, раствор фильтруют и проводят испытание на тяжелые металлы. Этот же раствор - для определения допустимой примеси железа. Определение сульфитов и сульфатов На раствор препарата действуют избытком йода до светло-желтого цвета раствора 2Nа2S2O3 + I2 2 NaI + Na2S4O6 Na2SO3 +I2 + 2NaOH Na2SO4 + 2NaI + H2O После этого добавляют хлорид бария и обнаруживают сульфат-ион, который присутствует в препарате или образовался при окислении сульфит-иона йодом. Если не провести предварительную обработку раствора йодом, то тиосульфат-ион с ионом бария даст белый осадок: Na2S2O3 + BaCl2 BaS2O3↓ + 2NaCl
25 При определении тяжелых металлов (≤ 0,001%). Разложение осуществляют разведенной HCl. После полной коагуляции серы и удалении SO2 (диоксида серы) при кипячении, раствор фильтруют и проводят испытание на тяжелые металлы. Этот же раствор - для определения допустимой примеси железа. Определение сульфитов и сульфатов На раствор препарата действуют избытком йода до светло-желтого цвета раствора 2Nа2S2O3 + I2 2 NaI + Na2S4O6 Na2SO3 +I2 + 2NaOH Na2SO4 + 2NaI + H2O После этого добавляют хлорид бария и обнаруживают сульфат-ион, который присутствует в препарате или образовался при окислении сульфит-иона йодом. Если не провести предварительную обработку раствора йодом, то тиосульфат-ион с ионом бария даст белый осадок: Na2S2O3 + BaCl2 BaS2O3↓ + 2NaCl
![>26 Определение сульфидов проводят в аммиачном растворе с нитропруссидом натрия: Na2S + Na2[Fe(CN)5NO] >26 Определение сульфидов проводят в аммиачном растворе с нитропруссидом натрия: Na2S + Na2[Fe(CN)5NO]](https://present5.com/presentacii-2/20171208\18854-prod._vi_gr.___v_gr._2012.ppt\18854-prod_vi_gr___v_gr_2012_26.jpg) 26 Определение сульфидов проводят в аммиачном растворе с нитропруссидом натрия: Na2S + Na2[Fe(CN)5NO] Na4[Fe(CN)5NOS]. фиолетовая окраска Мышьяк и селен определяют из одной пробы препарата, сначала окисляя эти элементы азотной кислотой при нагревании. Осадок серы отфильтровывают. В фильтрате проводят определения мышьяка и селена по реакции с гипофосфитом натрия (восстанавливая определяемые элементы гипофосфитом натрия). устанавливают прозрачность и цветность 30% раствора ЛС, щелочность 10% раствора.
26 Определение сульфидов проводят в аммиачном растворе с нитропруссидом натрия: Na2S + Na2[Fe(CN)5NO] Na4[Fe(CN)5NOS]. фиолетовая окраска Мышьяк и селен определяют из одной пробы препарата, сначала окисляя эти элементы азотной кислотой при нагревании. Осадок серы отфильтровывают. В фильтрате проводят определения мышьяка и селена по реакции с гипофосфитом натрия (восстанавливая определяемые элементы гипофосфитом натрия). устанавливают прозрачность и цветность 30% раствора ЛС, щелочность 10% раствора.
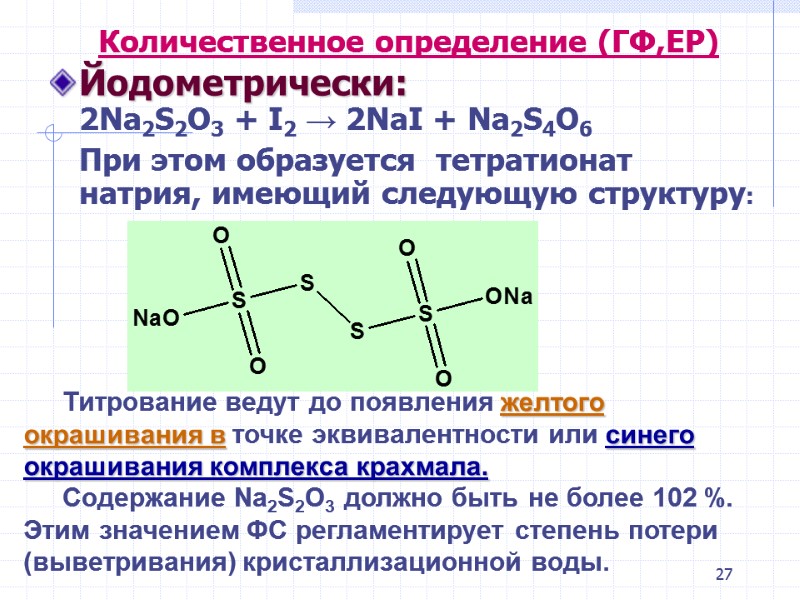
 27 Количественное определение (ГФ,ЕР) Йодометрически: 2Na2S2O3 + I2 → 2NaI + Na2S4O6 При этом образуется тетратионат натрия, имеющий следующую структуру: Титрование ведут до появления желтого окрашивания в точке эквивалентности или синего окрашивания комплекса крахмала. Содержание Na2S2O3 должно быть не более 102 %. Этим значением ФС регламентирует степень потери (выветривания) кристаллизационной воды.
27 Количественное определение (ГФ,ЕР) Йодометрически: 2Na2S2O3 + I2 → 2NaI + Na2S4O6 При этом образуется тетратионат натрия, имеющий следующую структуру: Титрование ведут до появления желтого окрашивания в точке эквивалентности или синего окрашивания комплекса крахмала. Содержание Na2S2O3 должно быть не более 102 %. Этим значением ФС регламентирует степень потери (выветривания) кристаллизационной воды.
 28 Хранение В хорошо закрытой таре. В сухом теплом воздухе препарат выветривается, во влажном слегка расплывается, а при 50°С плавится в кристаллизационной воде (эвтектический состав). Разлагается на воздухе (тиосульфат натрия является восстановителем и при хранении происходят следующие реакции): 2Na2S2O3 + O2 (воздух) →2Na2SO4 + 2S S2O32- [O] SO32- + S SO3 2- [O] SO42- В раствор тиосульфата натрия для инъекций (Solutio Natrii thiosulfatis 30% pro injectionibus) вводят стабилизатор гидрокарбонат натрия. NaHCO3 – стабилизатор – рН=7,8-8,4 Щелочность препарата регламентируется – по метилоранжу: NаНСО3 + HCI NaCI + Н2О + СО2
28 Хранение В хорошо закрытой таре. В сухом теплом воздухе препарат выветривается, во влажном слегка расплывается, а при 50°С плавится в кристаллизационной воде (эвтектический состав). Разлагается на воздухе (тиосульфат натрия является восстановителем и при хранении происходят следующие реакции): 2Na2S2O3 + O2 (воздух) →2Na2SO4 + 2S S2O32- [O] SO32- + S SO3 2- [O] SO42- В раствор тиосульфата натрия для инъекций (Solutio Natrii thiosulfatis 30% pro injectionibus) вводят стабилизатор гидрокарбонат натрия. NaHCO3 – стабилизатор – рН=7,8-8,4 Щелочность препарата регламентируется – по метилоранжу: NаНСО3 + HCI NaCI + Н2О + СО2
 29 Применение При отравлениях цианидами после приема внутрь тиосульфата натрия (20—30 мл 10 % раствора) образуются менее токсичные тиоцианаты: KCN + Na2S2O3 KNCS + Na2SO3 При отравлении солями тяжелых металлов (ртути, серебра, мышьяка, таллия, свинца) под воздействием тиосульфата натрия образуются малорастворимые тиосульфаты или прочные комплексные ионы: 2S2O32- + Ag + [Ag(S2O3)2]3-
29 Применение При отравлениях цианидами после приема внутрь тиосульфата натрия (20—30 мл 10 % раствора) образуются менее токсичные тиоцианаты: KCN + Na2S2O3 KNCS + Na2SO3 При отравлении солями тяжелых металлов (ртути, серебра, мышьяка, таллия, свинца) под воздействием тиосульфата натрия образуются малорастворимые тиосульфаты или прочные комплексные ионы: 2S2O32- + Ag + [Ag(S2O3)2]3-
 30 При аллергических заболеваниях тиосульфат натрия вводят внутривенно в виде 10-30% растворов. наружно при чесотке: 60% р-р Na2S2O3 + 6% р-р HCI выделяется сера – метод Демьяновича) Na2S2O3 + 2НСl SO2↓ + S ↓+ 2NaCl + H2O
30 При аллергических заболеваниях тиосульфат натрия вводят внутривенно в виде 10-30% растворов. наружно при чесотке: 60% р-р Na2S2O3 + 6% р-р HCI выделяется сера – метод Демьяновича) Na2S2O3 + 2НСl SO2↓ + S ↓+ 2NaCl + H2O
 31 Лекарственные средства на основе p-элементов V группы ПСЭ N, P, As, Sb, Bi
31 Лекарственные средства на основе p-элементов V группы ПСЭ N, P, As, Sb, Bi
 32 Общая характеристика группы N, P, As, Sb, Bi характеризуются меньшей относительной электроотрицательностью, чем галогены или халькогены, поэтому их неметаллические свойства выражены слабее, а с увеличением заряда ядра возрастают металлические свойства элементов. Висмут в лекарственных средствах присутствует в катионной форме. Все другие элементы находятся в виде аниона, за исключением азота, входящего в состав аммиака или иона аммония и имеющего степень окисления «-3» Все гидриды рассматриваемых элементов - фосфин PH3, арсин AsH3, стибин SbH3 и висмутин BiH3 - летучи и чрезвычайно токсичны.
32 Общая характеристика группы N, P, As, Sb, Bi характеризуются меньшей относительной электроотрицательностью, чем галогены или халькогены, поэтому их неметаллические свойства выражены слабее, а с увеличением заряда ядра возрастают металлические свойства элементов. Висмут в лекарственных средствах присутствует в катионной форме. Все другие элементы находятся в виде аниона, за исключением азота, входящего в состав аммиака или иона аммония и имеющего степень окисления «-3» Все гидриды рассматриваемых элементов - фосфин PH3, арсин AsH3, стибин SbH3 и висмутин BiH3 - летучи и чрезвычайно токсичны.
 33 Фосфор Является основной неорганической составляющей костной ткани (90% фосфора - в виде гидроксиапатита Са(ОН)2.3Са3(РО)2). Фосфаты принимают участие в образовании АТФ, ферментов, нуклеиновых кислот и фосфолипидов клеточных мембран. Входят в состав фосфатного буфера – одного из 4-х буферов крови. H2PO4-/HPO42- pH=pKa =7,25 В обычных условиях существует только три аллотропических модификации фосфора: белый, красный, черный, а в условиях сверхвысоких давлений — также металлическая форма.
33 Фосфор Является основной неорганической составляющей костной ткани (90% фосфора - в виде гидроксиапатита Са(ОН)2.3Са3(РО)2). Фосфаты принимают участие в образовании АТФ, ферментов, нуклеиновых кислот и фосфолипидов клеточных мембран. Входят в состав фосфатного буфера – одного из 4-х буферов крови. H2PO4-/HPO42- pH=pKa =7,25 В обычных условиях существует только три аллотропических модификации фосфора: белый, красный, черный, а в условиях сверхвысоких давлений — также металлическая форма.
 34 Белый фосфор очень токсичен. Это обусловлено его хорошей растворимостью в жирах и, следовательно, способностью проникать через мембраны клеток, а также высокой реакционной активностью. Остальные аллотропные модификации фосфора вследствие их нерастворимости не токсичны. Белый фосфор неустойчив: на свету или при нагревании медленно превращается в красный.
34 Белый фосфор очень токсичен. Это обусловлено его хорошей растворимостью в жирах и, следовательно, способностью проникать через мембраны клеток, а также высокой реакционной активностью. Остальные аллотропные модификации фосфора вследствие их нерастворимости не токсичны. Белый фосфор неустойчив: на свету или при нагревании медленно превращается в красный.
 35 В качестве ЛС используется: Натрия фосфат двузамещенный (кислая натриевая соль ортофосфорной кислоты) —— Natrii phosphas (Na2HPО4.12H2О) или «Динатрия фосфат додекагидрат». Применяется как компонент фосфатных клизм, при запорах, подготовки нижних отделов ЖКТ к эндоскопическому рентгенконтрастному исследованию, операциям, родам, ощищение кишечника после операций, рентгенконтрастных исследований.
35 В качестве ЛС используется: Натрия фосфат двузамещенный (кислая натриевая соль ортофосфорной кислоты) —— Natrii phosphas (Na2HPО4.12H2О) или «Динатрия фосфат додекагидрат». Применяется как компонент фосфатных клизм, при запорах, подготовки нижних отделов ЖКТ к эндоскопическому рентгенконтрастному исследованию, операциям, родам, ощищение кишечника после операций, рентгенконтрастных исследований.
 36 Натрия фосфат двузамещенный содержится в комплексном препарате Уродан, применяемый при подагре, почечнокаменной болезни для выведения избыточных солей из организма. В настоящее время натрия фосфат двузамещенный утрачивает свое значение ввиду появления других, более эффективных препаратов аналогичного фармакологического действия.
36 Натрия фосфат двузамещенный содержится в комплексном препарате Уродан, применяемый при подагре, почечнокаменной болезни для выведения избыточных солей из организма. В настоящее время натрия фосфат двузамещенный утрачивает свое значение ввиду появления других, более эффективных препаратов аналогичного фармакологического действия.
 37 Сурьма. Сурьма не является необходимым элементом для млекопитающих. Соединения сурьмы (SbO+) в малых дозах применялись как отхаркивающие средства, а в больших - как рвотные: Калия антимонилтартрат (калий сурьмяновиннокислый, рвотный камень) — комплексное соединение оксида сурьмы и калия виннокислого SbOKC4H4O6).
37 Сурьма. Сурьма не является необходимым элементом для млекопитающих. Соединения сурьмы (SbO+) в малых дозах применялись как отхаркивающие средства, а в больших - как рвотные: Калия антимонилтартрат (калий сурьмяновиннокислый, рвотный камень) — комплексное соединение оксида сурьмы и калия виннокислого SbOKC4H4O6).
 38 Мышьяк. Мышьяк As(III) в больших дозах является сильнейшим ядом, в малых дозах стимулирует эритропоэз и подавляет лейкопоэз. ЛС мышьяка: арсенат натрия, арсенит калия, мышьяковистый ангидрид ранее использовали при малокровии, истощении, неврастении и как противосифилитические средства. В настоящее время соединения мышьяка являются официально зарегистрированными гомеопатическими ЛС.
38 Мышьяк. Мышьяк As(III) в больших дозах является сильнейшим ядом, в малых дозах стимулирует эритропоэз и подавляет лейкопоэз. ЛС мышьяка: арсенат натрия, арсенит калия, мышьяковистый ангидрид ранее использовали при малокровии, истощении, неврастении и как противосифилитические средства. В настоящее время соединения мышьяка являются официально зарегистрированными гомеопатическими ЛС.
 39 Азот Азот составляет до 78% объема воздуха, является обязательной составной частью белка. В чистом виде он находится главным образом в атмосфере. В связанном состоянии встречается в виде нитратов NO3- и нитритов NO2-. Из неорганических соединений азота в медицине применяют: раствор аммиака в воде – NH3.H2O, соли аммония NH4+, оксид азота (I) N2O нитрит натрия NaNO2.
39 Азот Азот составляет до 78% объема воздуха, является обязательной составной частью белка. В чистом виде он находится главным образом в атмосфере. В связанном состоянии встречается в виде нитратов NO3- и нитритов NO2-. Из неорганических соединений азота в медицине применяют: раствор аммиака в воде – NH3.H2O, соли аммония NH4+, оксид азота (I) N2O нитрит натрия NaNO2.
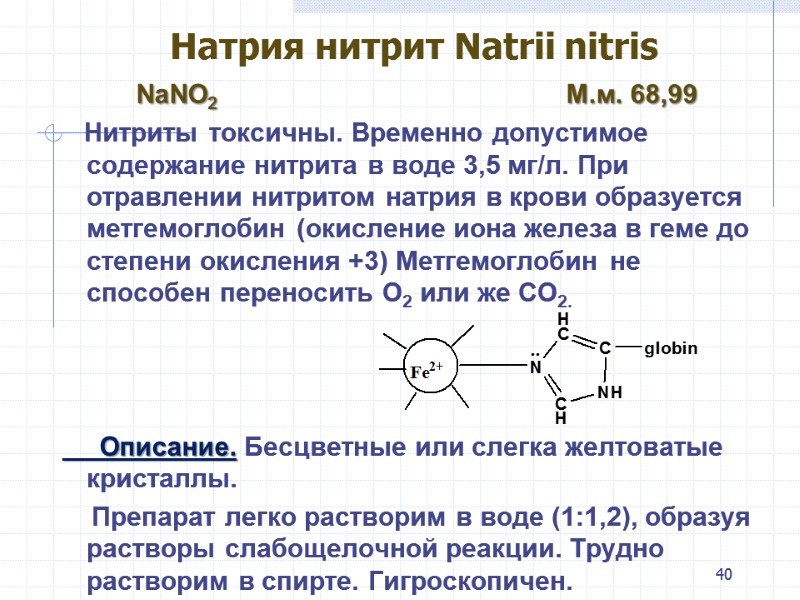
 40 Натрия нитрит Natrii nitris NaNO2 М.м. 68,99 Нитриты токсичны. Временно допустимое содержание нитрита в воде 3,5 мг/л. При отравлении нитритом натрия в крови образуется метгемоглобин (окисление иона железа в геме до степени окисления +3) Метгемоглобин не способен переносить О2 или же СО2. Описание. Бесцветные или слегка желтоватые кристаллы. Препарат легко растворим в воде (1:1,2), образуя растворы слабощелочной реакции. Трудно растворим в спирте. Гигроскопичен.
40 Натрия нитрит Natrii nitris NaNO2 М.м. 68,99 Нитриты токсичны. Временно допустимое содержание нитрита в воде 3,5 мг/л. При отравлении нитритом натрия в крови образуется метгемоглобин (окисление иона железа в геме до степени окисления +3) Метгемоглобин не способен переносить О2 или же СО2. Описание. Бесцветные или слегка желтоватые кристаллы. Препарат легко растворим в воде (1:1,2), образуя растворы слабощелочной реакции. Трудно растворим в спирте. Гигроскопичен.
 41 Получение Нитриты в природе образуются из аммиака гниющих органических веществ. Синтетически получают как побочный продукт при производстве азотной кислоты. Оксиды азота поглощаются щелочью или карбонатом натрия с образованием нитратов и нитритов. Полученную смесь солей разделяют фракционной перекристаллизацией. 2NO2 + 2NaOH NaNO3 + NaNO2 + H2O или: NO + NO2 + 2NaOH 2NaNO2 + H2O
41 Получение Нитриты в природе образуются из аммиака гниющих органических веществ. Синтетически получают как побочный продукт при производстве азотной кислоты. Оксиды азота поглощаются щелочью или карбонатом натрия с образованием нитратов и нитритов. Полученную смесь солей разделяют фракционной перекристаллизацией. 2NO2 + 2NaOH NaNO3 + NaNO2 + H2O или: NO + NO2 + 2NaOH 2NaNO2 + H2O
 42 Определение подлинности Степень окисления азота в натрия нитрите равна +3, поэтому он способен как восстанавливаться до NO, N2O, NH3, так и окисляться - до нитрата. Реакции на нитрит-ион: 1. При добавлении к раствору NaNO2 концентрированной серной кислоты образуется неустойчивая азотистая кислота, в результате разложения которой выделяются красно-бурые пары оксида азота (IV) NO2 - реакция диспропорционирования: NaNO2 + H2SO4 Na2SO4 + N+2O + N+4O2 + H2O
42 Определение подлинности Степень окисления азота в натрия нитрите равна +3, поэтому он способен как восстанавливаться до NO, N2O, NH3, так и окисляться - до нитрата. Реакции на нитрит-ион: 1. При добавлении к раствору NaNO2 концентрированной серной кислоты образуется неустойчивая азотистая кислота, в результате разложения которой выделяются красно-бурые пары оксида азота (IV) NO2 - реакция диспропорционирования: NaNO2 + H2SO4 Na2SO4 + N+2O + N+4O2 + H2O
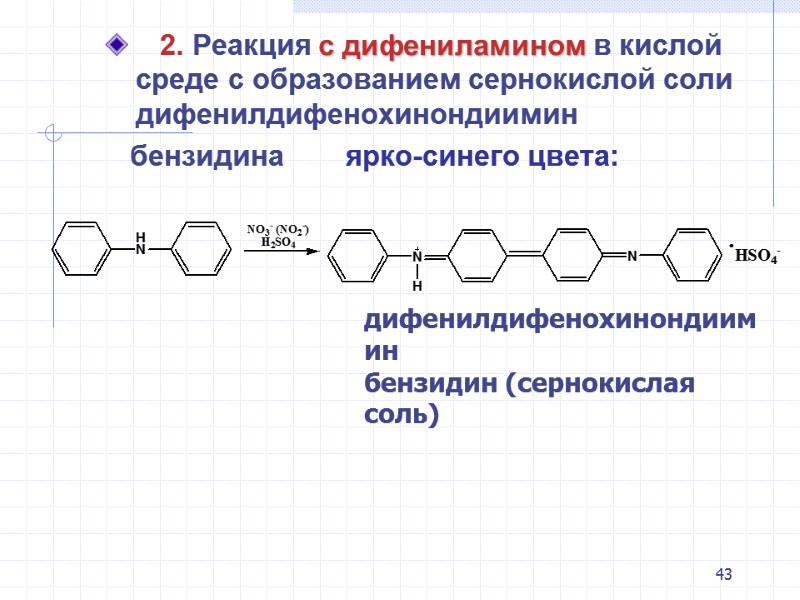
 43 2. Реакция с дифениламином в кислой среде с образованием сернокислой соли дифенилдифенохинондиимин бензидина ярко-синего цвета: дифенилдифенохинондиимин бензидин (сернокислая соль)
43 2. Реакция с дифениламином в кислой среде с образованием сернокислой соли дифенилдифенохинондиимин бензидина ярко-синего цвета: дифенилдифенохинондиимин бензидин (сернокислая соль)
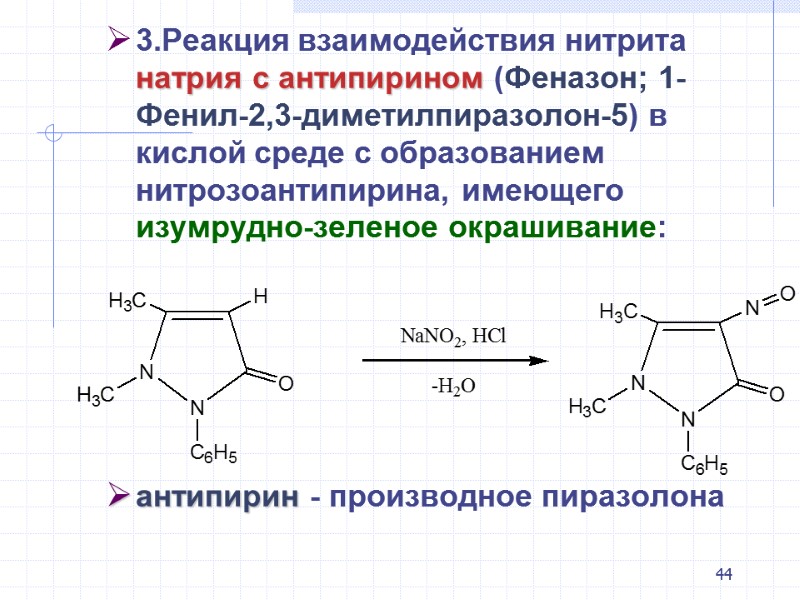
 44 3.Реакция взаимодействия нитрита натрия с антипирином (Феназон; 1-Фенил-2,3-диметилпиразолон-5) в кислой среде с образованием нитрозоантипирина, имеющего изумрудно-зеленое окрашивание: антипирин - производное пиразолона
44 3.Реакция взаимодействия нитрита натрия с антипирином (Феназон; 1-Фенил-2,3-диметилпиразолон-5) в кислой среде с образованием нитрозоантипирина, имеющего изумрудно-зеленое окрашивание: антипирин - производное пиразолона
 45 Антипирин оказывает болеутоляющее, жаропонижающее и противовоспалительное действие. По аналгезирующей и жаропонижающей активности препараты этой группы близки к производным салициловой кислоты. Производные пиразолона уменьшают проницаемость капилляров и препятствуют развитию воспалительной реакции.
45 Антипирин оказывает болеутоляющее, жаропонижающее и противовоспалительное действие. По аналгезирующей и жаропонижающей активности препараты этой группы близки к производным салициловой кислоты. Производные пиразолона уменьшают проницаемость капилляров и препятствуют развитию воспалительной реакции.
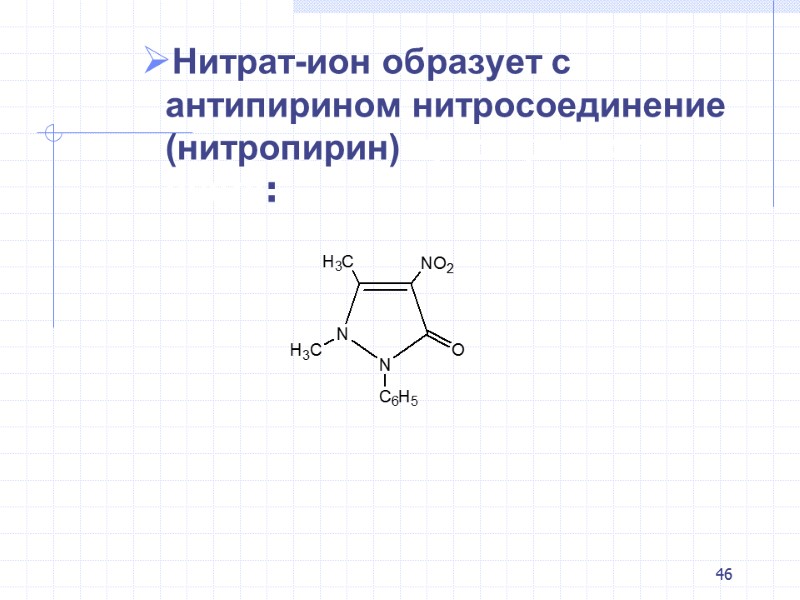
 46 Нитрат-ион образует с антипирином нитросоединение (нитропирин) ярко-красного цвета:
46 Нитрат-ион образует с антипирином нитросоединение (нитропирин) ярко-красного цвета:
 47 Не фармакопейные реакции: 1. Нитрит натрия, как восстановитель, обесцвечивает раствор перманганата калия: 2КМnО4 + 5NaNO2 + 3H2SО4 K2SO4 + 2MnSО4 + 5NaNO3 + 3Н2О 2. Как окислитель нитрит натрия взаимодействует с йодидами или бромидами в кислой среде, образуя молекулярные формы йода или брома: 2NaNO2 + 2 NaI + 2H2SО4 2NO + Na2SO4 + I2 + 2Н2О 3. Восстановление нитрит-иона может происходить до NH3, если применять еще более сильные восстановители: NaNO2 + 2Al + NaOH + 5H2O 2Na[Al(OH)4] + NH3
47 Не фармакопейные реакции: 1. Нитрит натрия, как восстановитель, обесцвечивает раствор перманганата калия: 2КМnО4 + 5NaNO2 + 3H2SО4 K2SO4 + 2MnSО4 + 5NaNO3 + 3Н2О 2. Как окислитель нитрит натрия взаимодействует с йодидами или бромидами в кислой среде, образуя молекулярные формы йода или брома: 2NaNO2 + 2 NaI + 2H2SО4 2NO + Na2SO4 + I2 + 2Н2О 3. Восстановление нитрит-иона может происходить до NH3, если применять еще более сильные восстановители: NaNO2 + 2Al + NaOH + 5H2O 2Na[Al(OH)4] + NH3
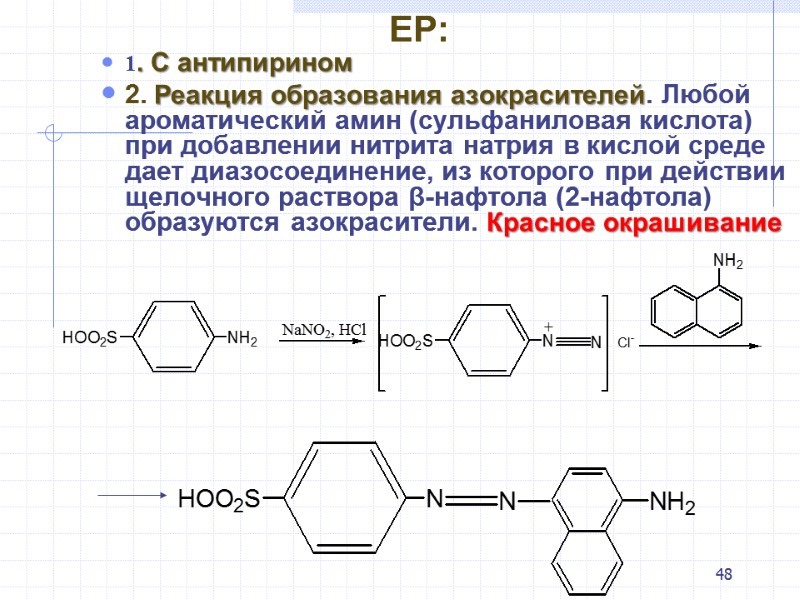
 48 EP: 1. С антипирином 2. Реакция образования азокрасителей. Любой ароматический амин (сульфаниловая кислота) при добавлении нитрита натрия в кислой среде дает диазосоединение, из которого при действии щелочного раствора β-нафтола (2-нафтола) образуются азокрасители. Красное окрашивание
48 EP: 1. С антипирином 2. Реакция образования азокрасителей. Любой ароматический амин (сульфаниловая кислота) при добавлении нитрита натрия в кислой среде дает диазосоединение, из которого при действии щелочного раствора β-нафтола (2-нафтола) образуются азокрасители. Красное окрашивание
 49 Реакция получения азокрасителя является специфичной для нитрит-ионов. Нитрат-ион этой реакции не дает. 3. Реакции на натрий.
49 Реакция получения азокрасителя является специфичной для нитрит-ионов. Нитрат-ион этой реакции не дает. 3. Реакции на натрий.
 50 Оценка чистоты (ЕР): Прозрачность и цветность: 5% раствор в воде – прозрачный и по окраске не превосходит эталон цветности B6. Допустимые примеси: хлориды (50 ppm), сульфаты (200 ppm), тяжелые металлы (20 ppm) - в пределах, оцениваемых эталонным методом. Потеря в весе при высушивании в вакууме -1%
50 Оценка чистоты (ЕР): Прозрачность и цветность: 5% раствор в воде – прозрачный и по окраске не превосходит эталон цветности B6. Допустимые примеси: хлориды (50 ppm), сульфаты (200 ppm), тяжелые металлы (20 ppm) - в пределах, оцениваемых эталонным методом. Потеря в весе при высушивании в вакууме -1%
 51 Количественное определение ГФ: Окисление перманганатом калия, избыток которого определяют йодометрически ( перманганатометрический метод обратного титрования, фармакопейный): 2КМnО4 + 5NaNO2 + 3H2SО4 K2SO4 + 2MnSО4 + + 5NaNO3 + 3Н2О 2KMnO4 + 10KIтв. + 8H2SО4 5I2+ 6K2SO4 + 2 MnSO4 + 8Н2О I2 + 2Na2S2O3 2NaI + Na2S4O6 Количество выделенного йода эквивалентно количеству перманганата калия, не вступившего в реакцию с нитритом натрия избыток
51 Количественное определение ГФ: Окисление перманганатом калия, избыток которого определяют йодометрически ( перманганатометрический метод обратного титрования, фармакопейный): 2КМnО4 + 5NaNO2 + 3H2SО4 K2SO4 + 2MnSО4 + + 5NaNO3 + 3Н2О 2KMnO4 + 10KIтв. + 8H2SО4 5I2+ 6K2SO4 + 2 MnSO4 + 8Н2О I2 + 2Na2S2O3 2NaI + Na2S4O6 Количество выделенного йода эквивалентно количеству перманганата калия, не вступившего в реакцию с нитритом натрия избыток
 52 ЕР: Ce(SO4)2: Изб. 2Ce(SO4)2 + NaNO2 + Н2О NaNO3 + Ce2 (SO4 )3 + H2SО4 Ce2 (SO4 )3 + 2KIтв. + H2SО4 I2+ K2SO4 + 2 Ce(SO4)2 + Н2О I2 + 2Na2S2O3 2NaI + Na2S4O6 Индикатор – крахмал. Титруют до исчезновения синий окраски.
52 ЕР: Ce(SO4)2: Изб. 2Ce(SO4)2 + NaNO2 + Н2О NaNO3 + Ce2 (SO4 )3 + H2SО4 Ce2 (SO4 )3 + 2KIтв. + H2SО4 I2+ K2SO4 + 2 Ce(SO4)2 + Н2О I2 + 2Na2S2O3 2NaI + Na2S4O6 Индикатор – крахмал. Титруют до исчезновения синий окраски.
 53 Хранение Препарат хранят в хорошо закрытых банках из оранжевого стекла в сухом темном месте, так как на воздухе он легко окисляется, а на свету частично разлагается (диспропорционирует) и желтеет: 2NaNO2 + H2O NO2+ NO+ 2NaOH В водных растворах НNО2 разлагается до NО + NО2
53 Хранение Препарат хранят в хорошо закрытых банках из оранжевого стекла в сухом темном месте, так как на воздухе он легко окисляется, а на свету частично разлагается (диспропорционирует) и желтеет: 2NaNO2 + H2O NO2+ NO+ 2NaOH В водных растворах НNО2 разлагается до NО + NО2
 54 Применение Редко как спазмолитическое (коронарнорасширяющее) средство при стенокардии, иногда при спазмах сосудов мозга. Препарат применяют внутрь или подкожно (О,1 - 0,2 г или 0,5 % раствор). нитрит натрия применяют как антидот при отравлениях цианидами (внутривенное ведение 10 - 20 мл 1 - 2 % раствора). NaCN + 7NaNO2 + 3H2O → 8NO + Na2CO3 + 6NaOH
54 Применение Редко как спазмолитическое (коронарнорасширяющее) средство при стенокардии, иногда при спазмах сосудов мозга. Препарат применяют внутрь или подкожно (О,1 - 0,2 г или 0,5 % раствор). нитрит натрия применяют как антидот при отравлениях цианидами (внутривенное ведение 10 - 20 мл 1 - 2 % раствора). NaCN + 7NaNO2 + 3H2O → 8NO + Na2CO3 + 6NaOH
 55 Аммиак и его соли В России в медицинской практике применяют раствор аммиака 10 %-ный в воде (Solutio Ammonii caustici), нашатырный спирт.
55 Аммиак и его соли В России в медицинской практике применяют раствор аммиака 10 %-ный в воде (Solutio Ammonii caustici), нашатырный спирт.
 56 Применение Как средство скорой помощи для возбуждения дыхания при обморочном состоянии. При больших концентрациях может вызвать рефлекторную остановку дыхания. При укусах насекомых раствор аммиака применяют наружно в виде примочек. Иногда используют как рвотное средство (по 5-10 капель на 100 мл воды). Только в разведенном виде. Прием неразведенного препарата вызывает ожоги пищевода и желудка Применяют внутрь — в виде нашатырно-анисовых капель (содержат 1,62—1,67 % аммиака), элексира грудного, линимента аммиачного для растираний при невралгиях и миозитах. Для мытья рук в хирургической практике по методу Спасокукоцкого и Кочергина (25 мл на 5 л теплой кипяченой воды) как антимикробное средство.
56 Применение Как средство скорой помощи для возбуждения дыхания при обморочном состоянии. При больших концентрациях может вызвать рефлекторную остановку дыхания. При укусах насекомых раствор аммиака применяют наружно в виде примочек. Иногда используют как рвотное средство (по 5-10 капель на 100 мл воды). Только в разведенном виде. Прием неразведенного препарата вызывает ожоги пищевода и желудка Применяют внутрь — в виде нашатырно-анисовых капель (содержат 1,62—1,67 % аммиака), элексира грудного, линимента аммиачного для растираний при невралгиях и миозитах. Для мытья рук в хирургической практике по методу Спасокукоцкого и Кочергина (25 мл на 5 л теплой кипяченой воды) как антимикробное средство.
 57 Хранение В прохладном месте в склянках с притертыми пробками или в бутылях с корковыми пробками, обернутыми станиолем, так как нашатырный спирт разъедает простую корковую пробку и жидкость буреет.
57 Хранение В прохладном месте в склянках с притертыми пробками или в бутылях с корковыми пробками, обернутыми станиолем, так как нашатырный спирт разъедает простую корковую пробку и жидкость буреет.
 58 В BP включены: гидрокарбонат аммония NH4НCO3 как отхаркивающее средство хлорид аммония NH4Cl как средство для коррекции метаболического алкалоза (Алкало́з — увеличение pH крови и др. тканей организма за счёт накопления щелочных веществ, т.е. нарушение кислотно-щелочного равновесия организма) Аммония бромид.
58 В BP включены: гидрокарбонат аммония NH4НCO3 как отхаркивающее средство хлорид аммония NH4Cl как средство для коррекции метаболического алкалоза (Алкало́з — увеличение pH крови и др. тканей организма за счёт накопления щелочных веществ, т.е. нарушение кислотно-щелочного равновесия организма) Аммония бромид.
 59 Большая фармакологическая группа лекарственных средств соединений азота – «Нитриты и нитритоподобные средства» (например, нитроглицерин).
59 Большая фармакологическая группа лекарственных средств соединений азота – «Нитриты и нитритоподобные средства» (например, нитроглицерин).
 60 Висмут Содержание висмута в земной коре 2×10−5 % по массе, в морской воде — 2×10−5 мг/л Из соединений висмута в медицинском направлении шире всего используют оксид висмута: для изготовления ЛС для лечения желудочно-кишечных заболеваний, антисептических и заживляющих средств, в последнее время на основе оксида висмута разрабатывается ряд противоопухолевых препаратов для лечения онкологических заболеваний.
60 Висмут Содержание висмута в земной коре 2×10−5 % по массе, в морской воде — 2×10−5 мг/л Из соединений висмута в медицинском направлении шире всего используют оксид висмута: для изготовления ЛС для лечения желудочно-кишечных заболеваний, антисептических и заживляющих средств, в последнее время на основе оксида висмута разрабатывается ряд противоопухолевых препаратов для лечения онкологических заболеваний.
 61 Оксохлорид висмута находит применение в медицине в качестве рентгеноконтрастного средства и в качестве наполнителя при изготовлении кровеносных сосудов. Соединения висмута - в качестве противоязвенных средств Раньше тартрат калия-висмута KBiC4H4O6 использовался при лечении сифилиса.
61 Оксохлорид висмута находит применение в медицине в качестве рентгеноконтрастного средства и в качестве наполнителя при изготовлении кровеносных сосудов. Соединения висмута - в качестве противоязвенных средств Раньше тартрат калия-висмута KBiC4H4O6 использовался при лечении сифилиса.
 62 Лекарственные средства висмута Соединения висмута, вводимые инъекционным путем высокотоксичны, так как образуют прочные химические связи с тиоловыми группами различных ферментов: Bi(SR)3. При попадании их в пищеварительный тракт, они практически безвредны из-за своей низкой растворимости. Препараты висмута применяются внутрь при желудочно-кишечных заболеваниях, связанных с накоплением соединений серы в кишечнике, которая, взаимодействуя с солями висмута, образует нерастворимый в кислотах и щелочах сульфид висмута Bi2S3.
62 Лекарственные средства висмута Соединения висмута, вводимые инъекционным путем высокотоксичны, так как образуют прочные химические связи с тиоловыми группами различных ферментов: Bi(SR)3. При попадании их в пищеварительный тракт, они практически безвредны из-за своей низкой растворимости. Препараты висмута применяются внутрь при желудочно-кишечных заболеваниях, связанных с накоплением соединений серы в кишечнике, которая, взаимодействуя с солями висмута, образует нерастворимый в кислотах и щелочах сульфид висмута Bi2S3.
 63 Висмута нитрат основный Висмута субнитрат Bismuthi subnitras BiO(NO3)•Н2О Мr 305,0 Описание. Аморфный или микрокристаллический порошок белого цвета, без запаха. Практически не растворим в воде и спирте. Легко растворим в минеральных кислотах (азотная, соляная).
63 Висмута нитрат основный Висмута субнитрат Bismuthi subnitras BiO(NO3)•Н2О Мr 305,0 Описание. Аморфный или микрокристаллический порошок белого цвета, без запаха. Практически не растворим в воде и спирте. Легко растворим в минеральных кислотах (азотная, соляная).
 64 Получение Из висмутовых руд. Восстановление висмута идет из оксохлорида (висмутил-хлорида) углем в щелочном расплаве: 4BiOСI + 2Nа2СО3 + 3C 4Bi + 4NаСI + 5CO2 Bi + 4HNO3 Bi(NO3)3 + NO + 2H2O При упаривании раствора средней соли выпадают бесцветные кристаллы Bi(NО3)3.5H2O, которые растворяются только в воде, сильно подкисленной азотной кислотой. При разбавлении водой полученного раствора этой соли в осадок выпадают малорастворимые основные соли переменного состава: Bi(NO3)3 + 2H2O Bi(OH)2(NO3) + 2HNO3
64 Получение Из висмутовых руд. Восстановление висмута идет из оксохлорида (висмутил-хлорида) углем в щелочном расплаве: 4BiOСI + 2Nа2СО3 + 3C 4Bi + 4NаСI + 5CO2 Bi + 4HNO3 Bi(NO3)3 + NO + 2H2O При упаривании раствора средней соли выпадают бесцветные кристаллы Bi(NО3)3.5H2O, которые растворяются только в воде, сильно подкисленной азотной кислотой. При разбавлении водой полученного раствора этой соли в осадок выпадают малорастворимые основные соли переменного состава: Bi(NO3)3 + 2H2O Bi(OH)2(NO3) + 2HNO3
 65 Состав основных солей зависит от условий получения (температуры и количества воды) и может быть представлен общей формулой: (5…10Bi 2О3)∙ (4…9 N2O5)∙ (7…9H2O) Это смесь солей различного состава: Bi(OH)2NO3, BiONO3, BiOOH. Иногда продукт гидролиза записывают в виде нитрата катиона висмутила BiO(NO3).
65 Состав основных солей зависит от условий получения (температуры и количества воды) и может быть представлен общей формулой: (5…10Bi 2О3)∙ (4…9 N2O5)∙ (7…9H2O) Это смесь солей различного состава: Bi(OH)2NO3, BiONO3, BiOOH. Иногда продукт гидролиза записывают в виде нитрата катиона висмутила BiO(NO3).
 66 Определение подлинности 1. При прокаливании препарата образуется желто-оранжевый оксид висмута Bi2O3 и выделяются красно-бурые пары диоксида азота (IV): 4BiONO3 2Bi2O3+ 4NO2 + O2
66 Определение подлинности 1. При прокаливании препарата образуется желто-оранжевый оксид висмута Bi2O3 и выделяются красно-бурые пары диоксида азота (IV): 4BiONO3 2Bi2O3+ 4NO2 + O2
 67 Общие реакции подлинности на ион висмута Bi3+ 2. Сульфиды щелочных металлов дают с растворами солей висмута темно-коричневый осадок сульфида висмута. Реакция идет в кислой среде – для перевода препарата в ионное состояние - висмутил 2BiONO3 + 3Na2S + 4HCI 2Bi2S3 + + 2NaNO3 + 4 NaCI + 2H2O Сульфид висмута растворяется в концентрированной азотной кислоте. Эта реакция позволяет обнаружить висмут в количестве 10 мкг/л (1:100000).
67 Общие реакции подлинности на ион висмута Bi3+ 2. Сульфиды щелочных металлов дают с растворами солей висмута темно-коричневый осадок сульфида висмута. Реакция идет в кислой среде – для перевода препарата в ионное состояние - висмутил 2BiONO3 + 3Na2S + 4HCI 2Bi2S3 + + 2NaNO3 + 4 NaCI + 2H2O Сульфид висмута растворяется в концентрированной азотной кислоте. Эта реакция позволяет обнаружить висмут в количестве 10 мкг/л (1:100000).
 68 3. Реакция с йодидом калия. При добавлении к концентрированному подкисленному раствору препарата раствора йодида калия выделяется бурый осадок йодида висмута, который растворяется в избытке реактива с образованием калия тетрайодовисмутата(III), окрашенного в темно-оранжевый цвет: Bi(NO3)3 + 3KI BiI3 + 3KNO3 BiI3 + KI K[BiI4] раствор йодида калия вначале добавляют по каплям
68 3. Реакция с йодидом калия. При добавлении к концентрированному подкисленному раствору препарата раствора йодида калия выделяется бурый осадок йодида висмута, который растворяется в избытке реактива с образованием калия тетрайодовисмутата(III), окрашенного в темно-оранжевый цвет: Bi(NO3)3 + 3KI BiI3 + 3KNO3 BiI3 + KI K[BiI4] раствор йодида калия вначале добавляют по каплям
 69 Реактив Драгендорфа - кислотный раствор калия йодвисмутата. 1.Классический реактив Драгендорфа - раствор иодвисмутата калия в азотной кислоте. Для его приготовления основной нитрат висмута (BiONO3) растворяют в азотной кислоте, затем прибавляют раствор иодида калия и после отстаивания в течение нескольких дней фильтруют и разбавляют водой. 2.Реактив Драгендорфа в модификации Мунье готовится на основе уксусной кислоты KBiI4 + CH3COOH.
69 Реактив Драгендорфа - кислотный раствор калия йодвисмутата. 1.Классический реактив Драгендорфа - раствор иодвисмутата калия в азотной кислоте. Для его приготовления основной нитрат висмута (BiONO3) растворяют в азотной кислоте, затем прибавляют раствор иодида калия и после отстаивания в течение нескольких дней фильтруют и разбавляют водой. 2.Реактив Драгендорфа в модификации Мунье готовится на основе уксусной кислоты KBiI4 + CH3COOH.
 70 Реактив Драгендорфа - общеалкалоидный реактив, который используют для определения подлинности аминов, алкалоидов, стероидов, с которыми реактив дает аморфные или кристаллические осадки. Некоторые соединения (никотин) дают с реактивом Драгендорфа кристаллические осадки с кристаллами характерной формы, видимой под микроскопом, что позволяет использовать эту реакцию для их качественного обнаружения.
70 Реактив Драгендорфа - общеалкалоидный реактив, который используют для определения подлинности аминов, алкалоидов, стероидов, с которыми реактив дает аморфные или кристаллические осадки. Некоторые соединения (никотин) дают с реактивом Драгендорфа кристаллические осадки с кристаллами характерной формы, видимой под микроскопом, что позволяет использовать эту реакцию для их качественного обнаружения.
 71 Неофицинальная реакция на ионы висмута: со щелочным раствором гидроксиламина гидрохлорида, который проявляет свойства восстановителя: 2Bi3+ + 6NH2OH 2Bi + 3N2+ 6H+ + 6H2O Подлинность (ВР): А. с калия йодида. B. Даёт реакцию (б) на висмут (Общие реакции). С. Даёт реакцию на нитраты. D. рН раствора 5% раствора, содержащего 10% азотной кислоты и 22% аммиака, не более 2.0
71 Неофицинальная реакция на ионы висмута: со щелочным раствором гидроксиламина гидрохлорида, который проявляет свойства восстановителя: 2Bi3+ + 6NH2OH 2Bi + 3N2+ 6H+ + 6H2O Подлинность (ВР): А. с калия йодида. B. Даёт реакцию (б) на висмут (Общие реакции). С. Даёт реакцию на нитраты. D. рН раствора 5% раствора, содержащего 10% азотной кислоты и 22% аммиака, не более 2.0
 72 Оценка чистоты (ГФ) Недопустимые примеси: медь, свинец, соли аммония, сульфаты, мышьяк и теллур. Допустимые примеси хлориды, соли щелочных и щелочноземельных металлов, карбонаты, серебро.
72 Оценка чистоты (ГФ) Недопустимые примеси: медь, свинец, соли аммония, сульфаты, мышьяк и теллур. Допустимые примеси хлориды, соли щелочных и щелочноземельных металлов, карбонаты, серебро.
 73 Оценка чистоты Недопустимые примеси Для обнаружения меди, свинца и сульфатов препарат растворяют в азотной кислоте, осаждают основные соли висмута, образовавшиеся в результате гидролиза при разбавлении и нагревании раствора. Для обнаружения меди в фильтрат добавляют аммиак. В присутствии меди фильтрат должен окрашиваться в ультрамариновый цвет, в результате образования аммиаката меди. 2Cu2+ + 4NH3.H2O 2[Сu(NН3)4]2+ + 4H2O комплекс ультрамаринового цвета
73 Оценка чистоты Недопустимые примеси Для обнаружения меди, свинца и сульфатов препарат растворяют в азотной кислоте, осаждают основные соли висмута, образовавшиеся в результате гидролиза при разбавлении и нагревании раствора. Для обнаружения меди в фильтрат добавляют аммиак. В присутствии меди фильтрат должен окрашиваться в ультрамариновый цвет, в результате образования аммиаката меди. 2Cu2+ + 4NH3.H2O 2[Сu(NН3)4]2+ + 4H2O комплекс ультрамаринового цвета
 74 Для обнаружения свинца в этот же фильтрат добавляют разведенной серной кислоты. Образуется сульфат свинца и появляется белый осадок или муть (PbSO4). Для обнаружения сульфатов в этот же фильтрат добавляют нитрат бария. Раствор должен оставаться прозрачным.
74 Для обнаружения свинца в этот же фильтрат добавляют разведенной серной кислоты. Образуется сульфат свинца и появляется белый осадок или муть (PbSO4). Для обнаружения сульфатов в этот же фильтрат добавляют нитрат бария. Раствор должен оставаться прозрачным.
 75 Определение мышьяка и теллура проводят по методу Буго и Тиле. Мышьяк и теллур восстанавливают до элементных форм. В качестве восстановителя используют гипофосфит натрия: 2Na(H2P+1O2) + Na2TeO3 Te + 2Na2(HP+3O3) + H2O При этом теллур дает черное окрашивание, а мышьяк – бурое, за счет выделения элементных форм. Соли аммония не должны обнаруживаться по запаху при кипячении 1 г препарата в 5 мл раствора натрия гидроксида.
75 Определение мышьяка и теллура проводят по методу Буго и Тиле. Мышьяк и теллур восстанавливают до элементных форм. В качестве восстановителя используют гипофосфит натрия: 2Na(H2P+1O2) + Na2TeO3 Te + 2Na2(HP+3O3) + H2O При этом теллур дает черное окрашивание, а мышьяк – бурое, за счет выделения элементных форм. Соли аммония не должны обнаруживаться по запаху при кипячении 1 г препарата в 5 мл раствора натрия гидроксида.
 76 Соли щелочных и щелочно-земельных металлов : препарат растворяют в соляной кислоте, пропускают сероводород до полного осаждения висмута (сульфид висмута), фильтруют. Фильтрат выпаривают досуха и остаток прокаливают до постоянной массы. Остаток оксидов и неразлагаюшихся солей не должен превышать 0,5 %.
76 Соли щелочных и щелочно-земельных металлов : препарат растворяют в соляной кислоте, пропускают сероводород до полного осаждения висмута (сульфид висмута), фильтруют. Фильтрат выпаривают досуха и остаток прокаливают до постоянной массы. Остаток оксидов и неразлагаюшихся солей не должен превышать 0,5 %.
 77 Содержание карбонатов не должно превышать количества, которое можно обнаружить по выделению углекислого газа, если на 1 г препарата подействовать 3 мл азотной кислоты. Определение хлоридов –эталонный метод Определение серебра –эталонный метод. Приготовление эталона описано в ФС
77 Содержание карбонатов не должно превышать количества, которое можно обнаружить по выделению углекислого газа, если на 1 г препарата подействовать 3 мл азотной кислоты. Определение хлоридов –эталонный метод Определение серебра –эталонный метод. Приготовление эталона описано в ФС
 78 Оценка чистоты (ЕР) Допустимые примеси медь, свинец, Вещества, осаждаемые аммиаком, хлориды, серебро.
78 Оценка чистоты (ЕР) Допустимые примеси медь, свинец, Вещества, осаждаемые аммиаком, хлориды, серебро.
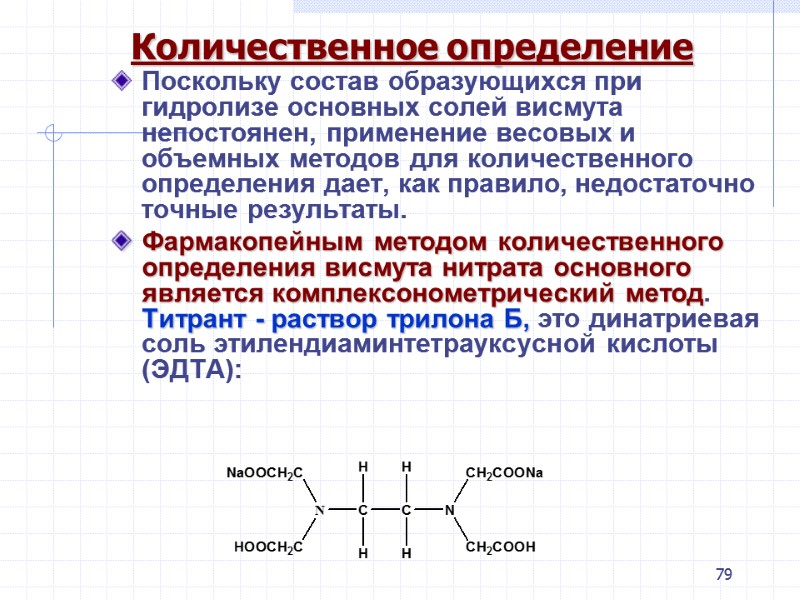
 79 Количественное определение Поскольку состав образующихся при гидролизе основных солей висмута непостоянен, применение весовых и объемных методов для количественного определения дает, как правило, недостаточно точные результаты. Фармакопейным методом количественного определения висмута нитрата основного является комплексонометрический метод. Титрант - раствор трилона Б, это динатриевая соль этилендиаминтетрауксусной кислоты (ЭДТА):
79 Количественное определение Поскольку состав образующихся при гидролизе основных солей висмута непостоянен, применение весовых и объемных методов для количественного определения дает, как правило, недостаточно точные результаты. Фармакопейным методом количественного определения висмута нитрата основного является комплексонометрический метод. Титрант - раствор трилона Б, это динатриевая соль этилендиаминтетрауксусной кислоты (ЭДТА):
 80 ЭДТА является шестидентатным лигандом, так как содержит 4 карбоксильные группы и два атома азота, имеющие каждый по неподеленной паре электронов. Хелаты ЭДТА с ионами металлов называют комплексонатами. ЭДТА- четырехосновная кислота и обозначается H4Y ЭДТА как титрант реагирует с ионами металла в соотношении 1:1 независимо от зарядов катиона, при этом происходит выделение двух ионов водорода: Bi3+ + H2Y2- → BiY- + 2H+. Для связывания ионов водорода в анализируемый раствор добавляют аммиачный буфер или щелочь. Если определение проводят в кислой среде, то ионы водорода не связываются. В качестве индикаторов используют металлоиндикаторы (органические красители, образующие с ионами титруемого металла интенсивно окрашенные комплексы, цвет которых отличается от окраски свободного индикатора).
80 ЭДТА является шестидентатным лигандом, так как содержит 4 карбоксильные группы и два атома азота, имеющие каждый по неподеленной паре электронов. Хелаты ЭДТА с ионами металлов называют комплексонатами. ЭДТА- четырехосновная кислота и обозначается H4Y ЭДТА как титрант реагирует с ионами металла в соотношении 1:1 независимо от зарядов катиона, при этом происходит выделение двух ионов водорода: Bi3+ + H2Y2- → BiY- + 2H+. Для связывания ионов водорода в анализируемый раствор добавляют аммиачный буфер или щелочь. Если определение проводят в кислой среде, то ионы водорода не связываются. В качестве индикаторов используют металлоиндикаторы (органические красители, образующие с ионами титруемого металла интенсивно окрашенные комплексы, цвет которых отличается от окраски свободного индикатора).
 81 Принцип комплексонометрического титрования К исследуемому раствору, содержащему определенный катион, при строго определенном значении рН прибавляют небольшое количество соответствующего индикатора (менее 1%). Если индикатор –шестиосновная кислота (ксиленовый оранжевый): Н6Ind=3H+ + Н3Ind3- (в свободном виде - желтого цвета) В результате образуется хорошо растворимое в воде окрашенное комплексное соединение индикатора с металлом. Bi3+ + Н3Ind3- = BiН3Ind3- Комплекс индикатора с ионом металла достаточно устойчив, но в 10 раз менее устойчив, чем комплекс металла с ЭДТА (изменение окраски индикатора должно быть четким, контрастным и быстрым).
81 Принцип комплексонометрического титрования К исследуемому раствору, содержащему определенный катион, при строго определенном значении рН прибавляют небольшое количество соответствующего индикатора (менее 1%). Если индикатор –шестиосновная кислота (ксиленовый оранжевый): Н6Ind=3H+ + Н3Ind3- (в свободном виде - желтого цвета) В результате образуется хорошо растворимое в воде окрашенное комплексное соединение индикатора с металлом. Bi3+ + Н3Ind3- = BiН3Ind3- Комплекс индикатора с ионом металла достаточно устойчив, но в 10 раз менее устойчив, чем комплекс металла с ЭДТА (изменение окраски индикатора должно быть четким, контрастным и быстрым).
 82 Проводят титрование раствором трилона Б свободных ионов металла. Более 99% ионов металла находится в свободном виде и в ходе титрования связывается комплексоном (Трилоном Б) в бесцветный растворимый комплекс ЭДТА с металлом. Bi3+ + H2Y2- → BiY- + 2H+. В процессе титрования титрант трилон Б (Na2ЭДТА) связывает ионы висмута, образовавшиеся при растворении препарата в азотной кислоте, в комплексное соединение: Na2ЭДТА + Bi(NO3)3 Na[BiЭДТА]+2HNO3+NaNO3
82 Проводят титрование раствором трилона Б свободных ионов металла. Более 99% ионов металла находится в свободном виде и в ходе титрования связывается комплексоном (Трилоном Б) в бесцветный растворимый комплекс ЭДТА с металлом. Bi3+ + H2Y2- → BiY- + 2H+. В процессе титрования титрант трилон Б (Na2ЭДТА) связывает ионы висмута, образовавшиеся при растворении препарата в азотной кислоте, в комплексное соединение: Na2ЭДТА + Bi(NO3)3 Na[BiЭДТА]+2HNO3+NaNO3
 83 В точке эквивалентности: происходит разрушение комплекса металл-индикатор, образование более устойчивого комплекса металла – ЭДТА и свободного индикатора. BiН3Ind3- + H2Y2- → BiY- + 3H+ +Ind3- При этом выделяется свободный индикатор, который окрашивает раствор в другой цвет, присущий свободному индикатору при данном значении рН.
83 В точке эквивалентности: происходит разрушение комплекса металл-индикатор, образование более устойчивого комплекса металла – ЭДТА и свободного индикатора. BiН3Ind3- + H2Y2- → BiY- + 3H+ +Ind3- При этом выделяется свободный индикатор, который окрашивает раствор в другой цвет, присущий свободному индикатору при данном значении рН.
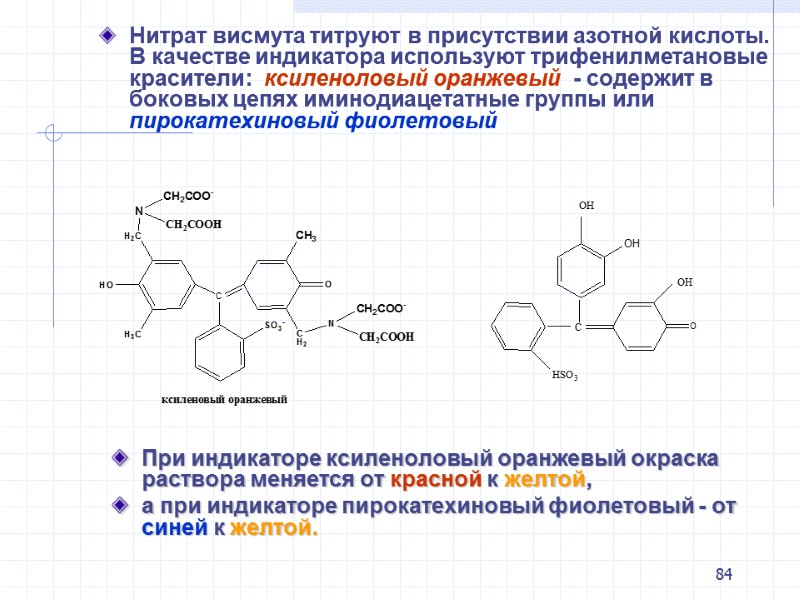
 84 Нитрат висмута титруют в присутствии азотной кислоты. В качестве индикатора используют трифенилметановые красители: ксиленоловый оранжевый - cодержит в боковых цепях иминодиацетатные группы или пирокатехиновый фиолетовый При индикаторе ксиленоловый оранжевый окраска раствора меняется от красной к желтой, а при индикаторе пирокатехиновый фиолетовый - от синей к желтой.
84 Нитрат висмута титруют в присутствии азотной кислоты. В качестве индикатора используют трифенилметановые красители: ксиленоловый оранжевый - cодержит в боковых цепях иминодиацетатные группы или пирокатехиновый фиолетовый При индикаторе ксиленоловый оранжевый окраска раствора меняется от красной к желтой, а при индикаторе пирокатехиновый фиолетовый - от синей к желтой.
 85 Применение Вяжущее, адсорбирующее, антацидное, противомикробное и противовоспалительное средство. Применяют при желудочно-кишечных заболеваниях. Выпускается в порошке и таблетках по 0,25 и 0,5 г. Входит в состав комбинированных антацидных препаратов (таблетки «Викалин», «Викаир» и др.). Применяют также наружно в виде мази и присыпки при воспалительных заболеваниях кожи и слизистых оболочек. В терапии вместо Bi(NO3)3 следует применять (BiO)2CO3, поскольку нитрат восстанавливается кишечными микробами до нитрита. Последний может вызывать отравления, ошибочно принимаемые за отравления висмутом.
85 Применение Вяжущее, адсорбирующее, антацидное, противомикробное и противовоспалительное средство. Применяют при желудочно-кишечных заболеваниях. Выпускается в порошке и таблетках по 0,25 и 0,5 г. Входит в состав комбинированных антацидных препаратов (таблетки «Викалин», «Викаир» и др.). Применяют также наружно в виде мази и присыпки при воспалительных заболеваниях кожи и слизистых оболочек. В терапии вместо Bi(NO3)3 следует применять (BiO)2CO3, поскольку нитрат восстанавливается кишечными микробами до нитрита. Последний может вызывать отравления, ошибочно принимаемые за отравления висмутом.
 86 Хранение В хорошо закрытых банках в сухом, защищенном от света месте без доступа воздуха.
86 Хранение В хорошо закрытых банках в сухом, защищенном от света месте без доступа воздуха.

