5.Презентация_Биофизика биополимеров.ppt
- Количество слайдов: 124

Лекция № 5 Физико-химические особенности строения и Функции биополимеров ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 1
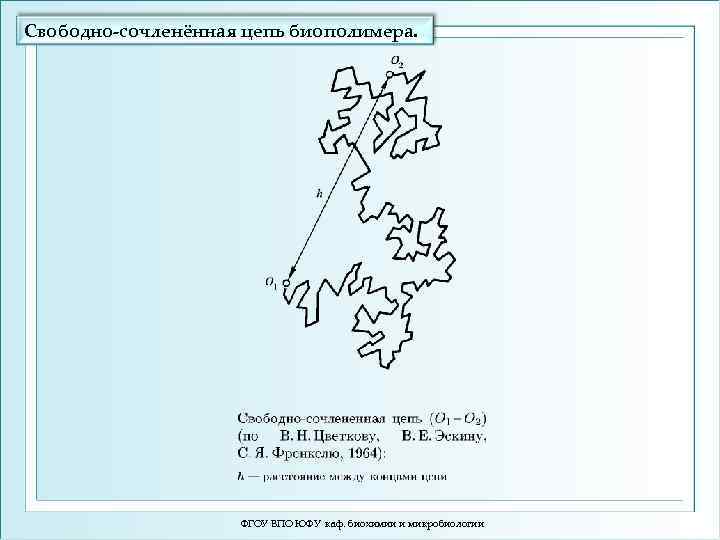
Свободно-сочленённая цепь биополимера. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Клубок и глобула. θ – температура, при которой отталкивание мономеров полностью компенсируется их взаимным притяжением, объёмные взаимодействия отсутствуют и макромолекула представляет собой клубок с размерами R = l N 1/2 Глобула – вид пространственной структуры полимера с компактной пространственной структурой, с малыми флуктуациями плотности, с однородной сердцевиной и постоянной концентрацией звеньев n 0. Клубок - вид пространственной структуры полимера, при котором взаимодействуют только соседние звенья, с большим количеством конформаций и отсутствует внутренняя структура. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Различия между клубком и глобулой Клубок Глобула Не имеет структуры Имеет структуру: в центре гидрофобное ядро, по периферии – гидрофильная «опушка» ; S→ 0 Нет объемных взаимодействий Имеются объемные взаимодействия Имеется корреляция плотности: Rкор= Rклубка Нет корреляции плотности: Rкор<<Rклубка Однофазная система Двухфазная система ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
![Внутреннее вращение и поворотная изомерия. [8] Внутреннее вращение и поворотная изомерия имеют важное значение Внутреннее вращение и поворотная изомерия. [8] Внутреннее вращение и поворотная изомерия имеют важное значение](https://present5.com/presentation/19930286_335801816/image-5.jpg)
Внутреннее вращение и поворотная изомерия. [8] Внутреннее вращение и поворотная изомерия имеют важное значение в конформационной структуре макромолекулы. Энергия ближних взаимодействий атомных групп зависит от расстояний между ними, которые в свою очередь меняются при вращении этих групп вокруг единичных связей. При близком расположении валентно не Молекула этана имеет минимум конформационной энергии в связанные атомы начинают отталкиваться, и возникает тран-сконформации и максимум - в цис-конформации. тормозящий энергетический Энергетический барьер, или тормозящий потенциал, для потенциал, препятствующий перехода одной транс-конформации в другую через цис вращению атомных групп. форму при повороте вокруг С-С связи на 120° равен Энергия вращения атомных групп вокруг единичных связей ~12, 5 к. Дж/моль. Зависимость потенциала внутреннего дает основной вклад в общую вращения от угла поворота φ задается выражением: конформационную энергию U (φ) = U 0/2 (1 - cos 3φ) полимерной цепи. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
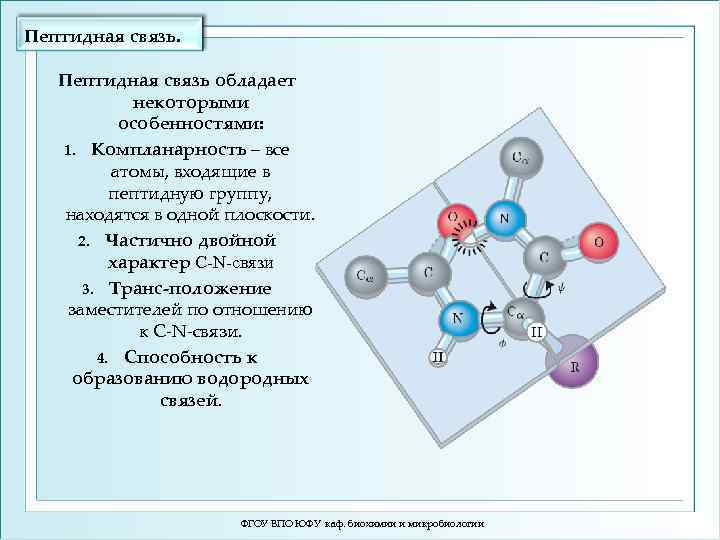
Пептидная связь обладает некоторыми особенностями: 1. Компланарность – все атомы, входящие в пептидную группу, находятся в одной плоскости. 2. Частично двойной характер С-N-связи 3. Транс-положение заместителей по отношению к С-N-связи. 4. Способность к образованию водородных связей. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
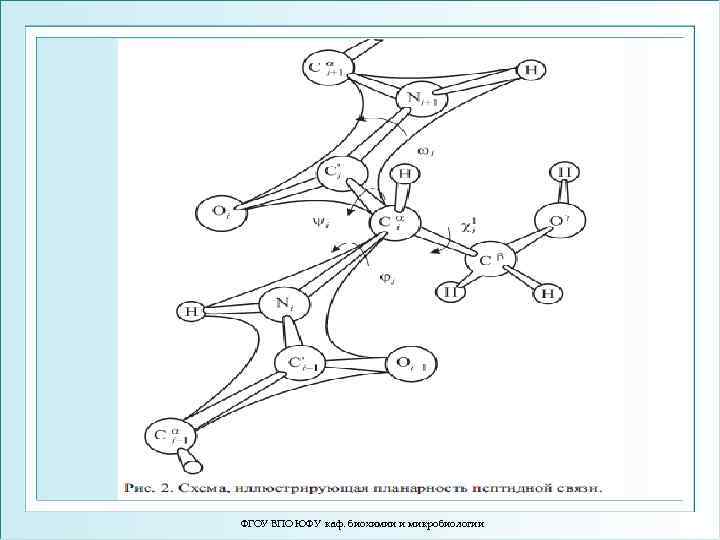
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
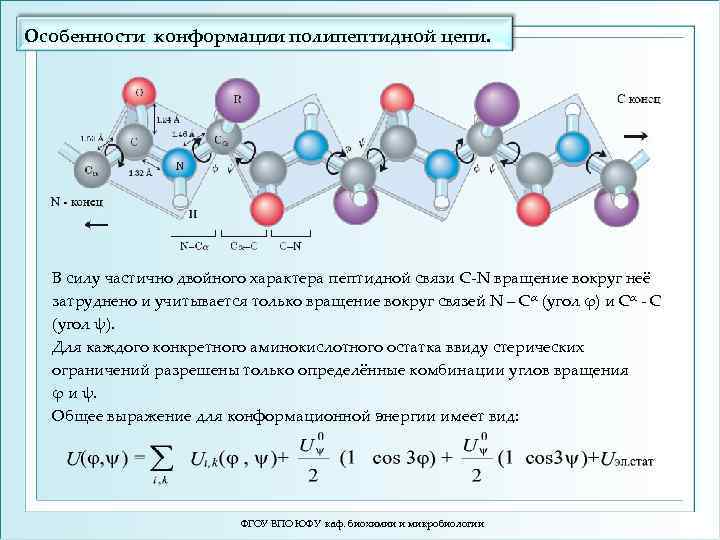
Особенности конформации полипептидной цепи. В силу частично двойного характера пептидной связи С-N вращение вокруг неё затруднено и учитывается только вращение вокруг связей N – Cα (угол φ) и Cα - C (угол ψ). Для каждого конкретного аминокислотного остатка ввиду стерических ограничений разрешены только определённые комбинации углов вращения φ и ψ. Общее выражение для конформационной энергии имеет вид: ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
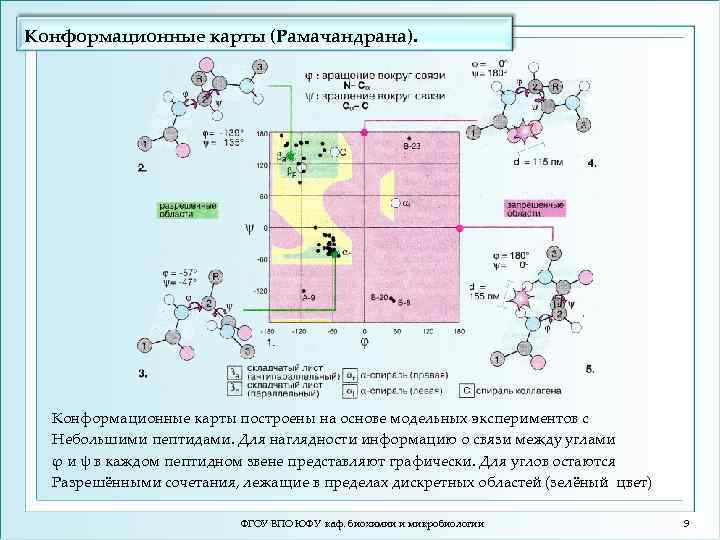
Конформационные карты (Рамачандрана). Конформационные карты построены на основе модельных экспериментов с Небольшими пептидами. Для наглядности информацию о связи между углами φ и ψ в каждом пептидном звене представляют графически. Для углов остаются Разрешёнными сочетания, лежащие в пределах дискретных областей (зелёный цвет) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 9

Уровни организации белков. α – спираль. Наиболее распространенным элементом вторичной структуры является правая α-спираль (αR). Пептидная цепь здесь изгибается винтообразно (ось выделена оранжевым цветом). Ha каждый виток приходится 3, 6 аминокислотного остатка, шаг винта (т. е. минимальное расстояние между двумя эквивалентными точками) составляет 0, 54 нм. α-Спираль стабилизирована почти линейными водородными связями (красный пунктир) между NH-группой и СО-группой четвертого по счету аминокислотного остатка. Таким образом, в протяженных спиральных участках каждый аминокислотный остаток принимает участие в формировании двух водородных связей. Неполярные или амфифильные α-спирали с 5 -6 витками часто обеспечивают заякоривание белков в биологических мембранах. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
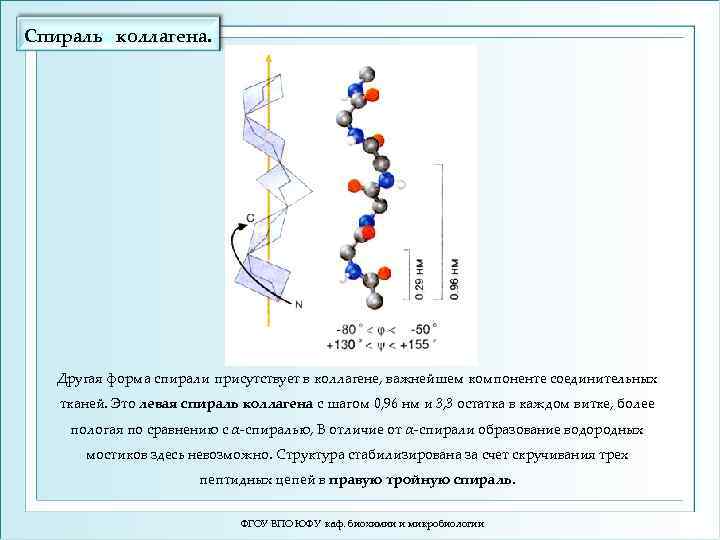
Спираль коллагена. Другая форма спирали присутствует в коллагене, важнейшем компоненте соединительных тканей. Это левая спираль коллагена с шагом 0, 96 нм и 3, 3 остатка в каждом витке, более пологая по сравнению с α-спиралью, В отличие от α-спирали образование водородных мостиков здесь невозможно. Структура стабилизирована за счет скручивания трех пептидных цепей в правую тройную спираль. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
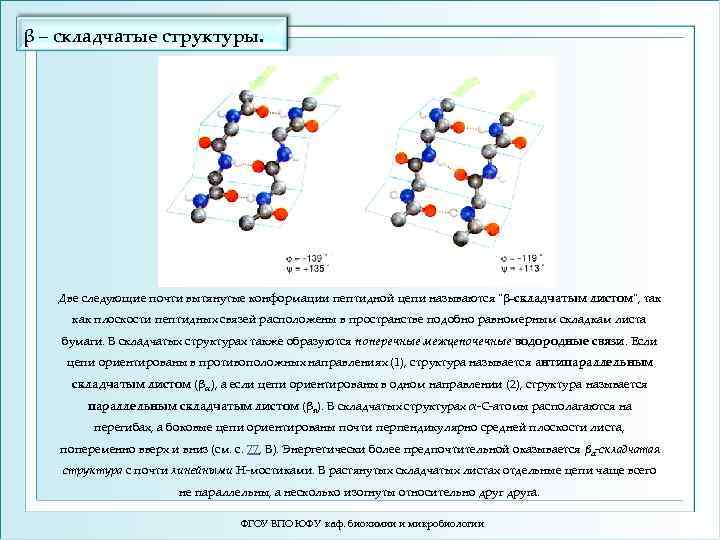
β – складчатые структуры. Две следующие почти вытянутые конформации пептидной цепи называются "β-складчатым листом", так как плоскости пептидных связей расположены в пространстве подобно равномерным складкам листа бумаги. B складчатых структурах также образуются поперечные межцепочечные водородные связи. Если цепи ориентированы в противоположных направлениях (1), структура называется антипараллельным складчатым листом (βα), а если цепи ориентированы в одном направлении (2), структура называется параллельным складчатым листом (βn). В складчатых структурах α-С-атомы располагаются на перегибах, а боковые цепи ориентированы почти перпендикулярно средней плоскости листа, попеременно вверх и вниз (см. с. 77, В). Энергетически более предпочтительной оказывается βα-складчатая структура с почти линейными H-мостиками. В растянутых складчатых листах отдельные цепи чаще всего не параллельны, а несколько изогнуты относительно друга. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

β - Петля. В тех участках, где пептидная цепь изгибается достаточно круто, часто находится β-петля. Это короткий фрагмент, в котором 4 аминокислотных остатка расположены таким образом, что цепь делает реверсивный поворот (на 180 о). Оба приведенных на схеме варианта петли (типы I и II) встречаются довольно часто. Обе структуры стабилизированы водородным мостиком между 1 и 4 остатками. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Типы объемных взаимодействий в биополимерах Тип взаимодействий Энергия взаимодействия 1. Электростатические 40 к. Дж/моль 2. Водородные 12 -40 к. Дж/моль 3. Ван-дер-ваальсовы 4 -8 к. Дж/моль 4. Гидрофобные 8 к. Дж/моль ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
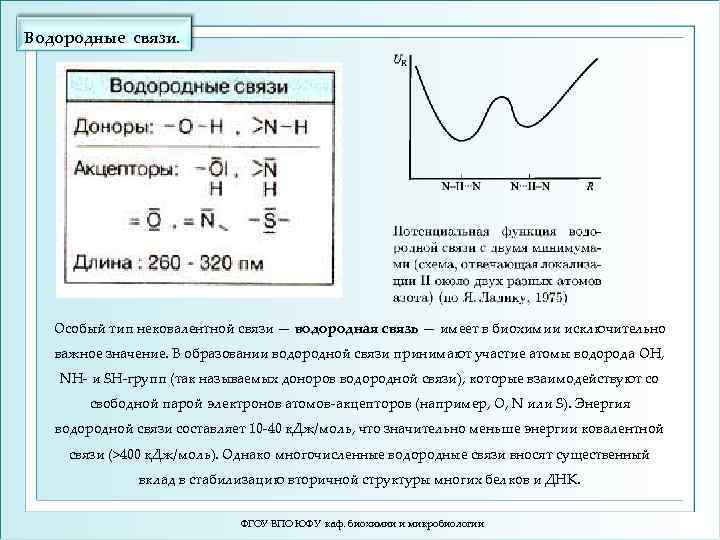
Водородные связи. Особый тип нековалентной связи — водородная связь — имеет в биохимии исключительно важное значение. В образовании водородной связи принимают участие атомы водорода ОН, NH- и SH-гpупп (так называемых доноров водородной связи), которые взаимодействуют со свободной парой электронов атомов-акцепторов (например, О, N или S). Энергия водородной связи составляет 10 -40 к. Дж/моль, что значительно меньше энергии ковалентной связи (>400 к. Дж/моль). Однако многочисленные водородные связи вносят существенный вклад в стабилизацию вторичной структуры многих белков и ДНК. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Ван-дер-ваальсовы взаимодействия – силы межмолекулярного взаимодействия, возникающие без передачи молекулами электронов и имеющие электромагнитную природу. В 1873 г. голландский ученый И. Ван-дер-Ваальс предположил, что существуют силы, обусловливающие притяжение между молекулами. Эти силы позднее получили название ван-дер-ваальсовых сил. Они включают в себя три составляющие: ориентационное, индукционное и дисперсионное взаимодействия. а – ориентационное взаимодействие; б - индукционное взаимодействие; в – дисперсионное взаимодействие ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Зависимость энергии ван-дер-ваальсова взаимодействия Wв от расстояния между молекулами R Wв сил притяжения обратно пропорциональна расстоянию в шестой степени (знак «минус» указывает, что соответствующая энергия падает при сближении) Wв = -А/R 6 + B/R 12 Wв сил отталкивания обратно пропорциональна расстоянию в двенадцатой степени (знак «плюс» указывает, что соответствующая энергия возрастает при сближении) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
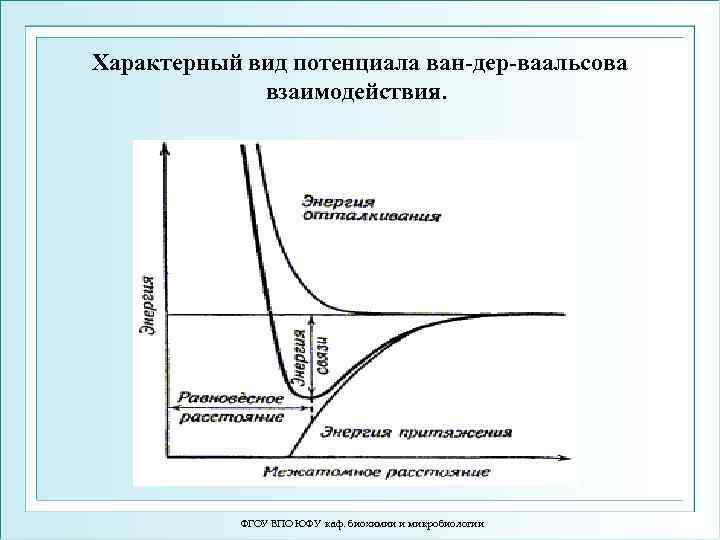
Характерный вид потенциала ван-дер-ваальсова взаимодействия. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
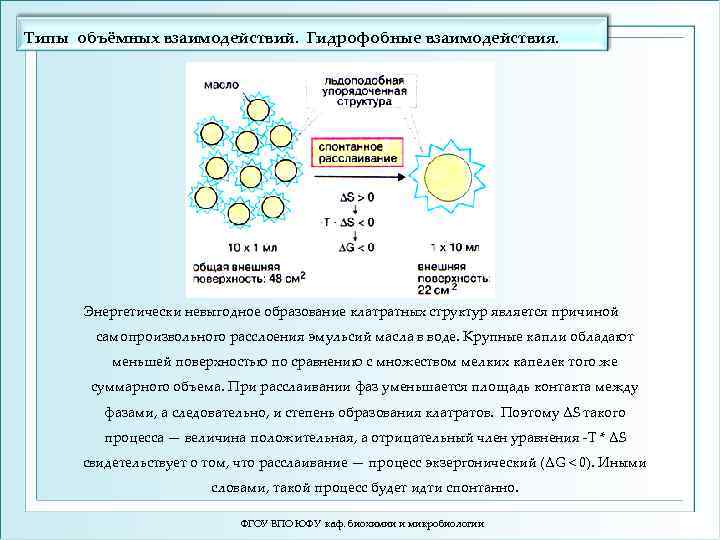
Типы объёмных взаимодействий. Гидрофобные взаимодействия. Энергетически невыгодное образование клатратных структур является причиной самопроизвольного расслоения эмульсий масла в воде. Крупные капли обладают меньшей поверхностью по сравнению с множеством мелких капелек того же суммарного объема. При расслаивании фаз уменьшается площадь контакта между фазами, а следовательно, и степень образования клатратов. Поэтому ΔS такого процесса — величина положительная, а отрицательный член уравнения -T * ΔS свидетельствует о том, что расслаивание — процесс экзергонический (ΔG < 0). Иными словами, такой процесс будет идти спонтанно. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Гидрофобные взаимодействия Это термодинамическая, точнее, энтропийная форма взаимодействий между молекулами воды и гидрофобными радикалами любой природы, в общем – между молекулами воды и гидрофобной поверхностью. - Гидрофобные взаимодействия не являются какими-то особыми связями. Это неспецифические взаимодействия, обусловленные изменением структуры воды при внедрении в нее неполярных молекул. - ∆G = ∆H - T∆S - ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
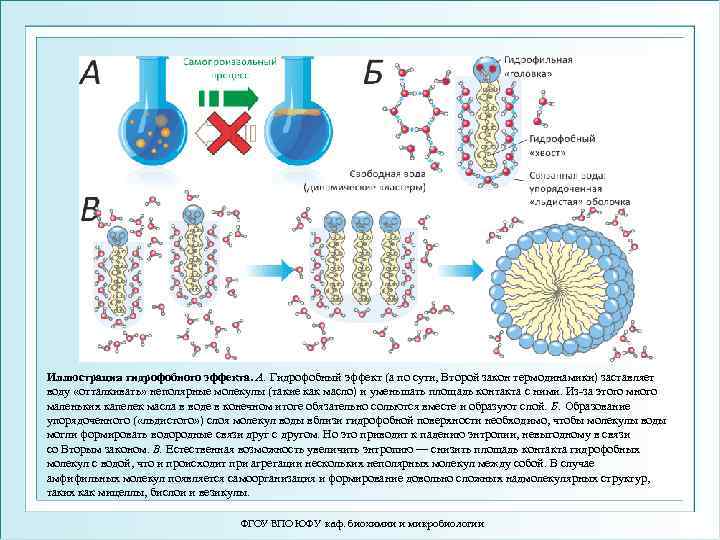
Иллюстрация гидрофобного эффекта. А. Гидрофобный эффект (а по сути, Второй закон термодинамики) заставляет воду «отталкивать» неполярные молекулы (такие как масло) и уменьшать площадь контакта с ними. Из-за этого много маленьких капелек масла в воде в конечном итоге обязательно сольются вместе и образуют слой. Б. Образование упорядоченного ( «льдистого» ) слоя молекул воды вблизи гидрофобной поверхности необходимо, чтобы молекулы воды могли формировать водородные связи друг с другом. Но это приводит к падению энтропии, невыгодному в связи со Вторым законом. В. Естественная возможность увеличить энтропию — снизить площадь контакта гидрофобных молекул с водой, что и происходит при агрегации нескольких неполярных молекул между собой. В случае амфифильных молекул появляется самоорганизация и формирование довольно сложных надмолекулярных структур, таких как мицеллы, бислои и везикулы. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Молекула воды полярна, является выраженным диполем. Это значит, что на ее атомах есть небольшие ("парциальные") электрические заряды: на электроотрицательном О — отрицательный, на Н — положительный. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Различная конфигурация молекул воды вблизи гидрофобных частиц ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

• Гидрофобный эффект берет на себя, грубо говоря, три четверти работы по созданию белковой глобулы. Но он сам по себе не может создать нативный твердый белок. Он создает лишь расплавленную белковую глобулу. Отвердевает белок, как и все органические жидкости, под действием Ван-дер-ваальсовых сил, а также водородных и ионных связей — взаимодействий более специфичных и более чувствительных к деталям атомной структуры, чем простая водобоязнь. Но это — окончательная огранка, а большая часть работы, вся черновая работа падает на гидрофобный эффект (Финкельштейн А. В. , 2000). ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

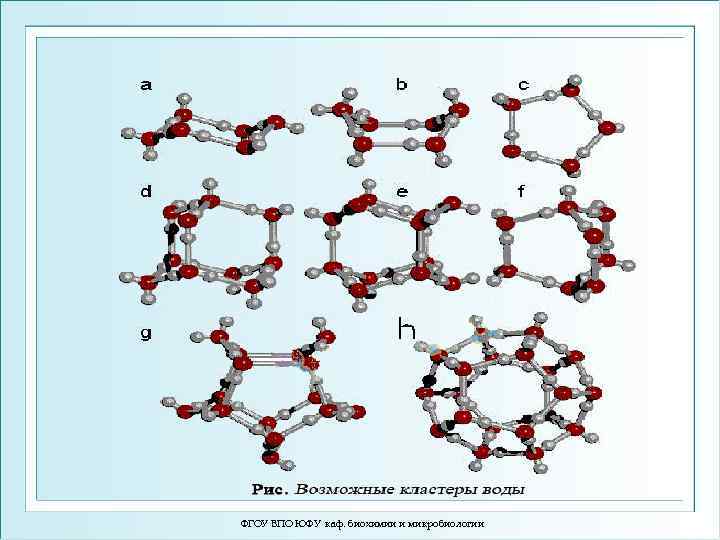
Структура кластеров воды ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Типы структурной укладки полипептидных цепей 1) α-белки – содержат только α-спирали + бесструктурные участки (глобины) 2) β-белки – содержат только β-конформации + бесструктурные участки (порины) 3) α+β-белки– в белке перемешаны α-спирали и β-слои (РНК-аза, лизоцим) 4) α/β-белки – послойное расположение α- и β-структур, своеобразный сэндвич (НАД+-зависимые дегидрогеназы) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
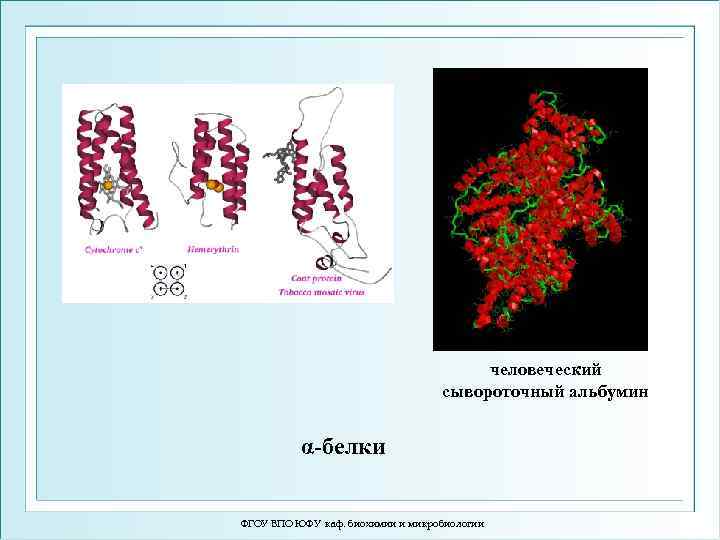
человеческий сывороточный альбумин α-белки ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Порин – длинный бета-лист, свернутый в цилиндр β-белки ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
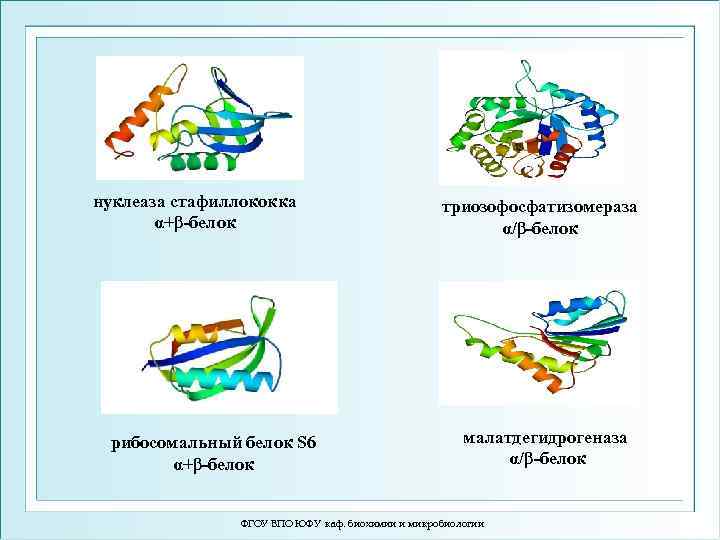
нуклеаза стафиллококка α+β-белок рибосомальный белок S 6 α+β-белок триозофосфатизомераза α/β-белок малатдегидрогеназа α/β-белок ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
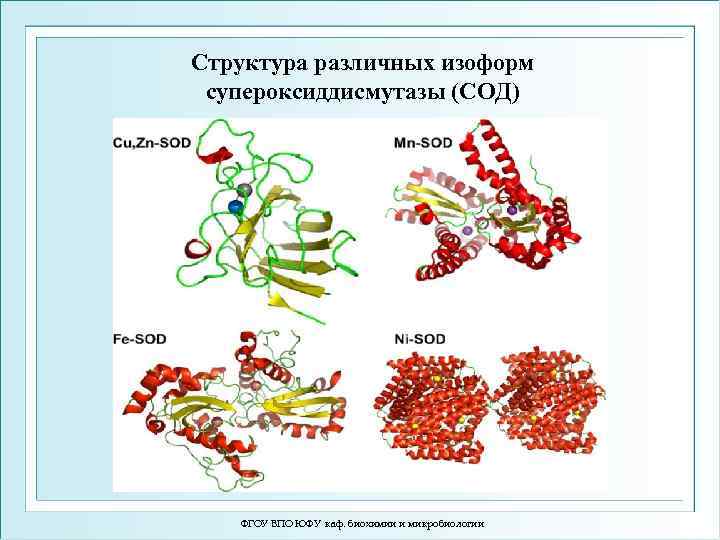
Структура различных изоформ супероксиддисмутазы (СОД) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
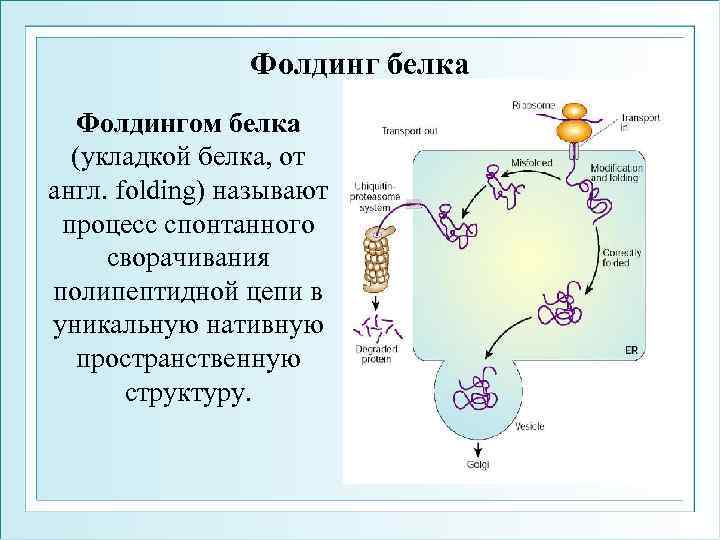
Фолдинг белка Фолдингом белка (укладкой белка, от англ. folding) называют процесс спонтанного сворачивания полипептидной цепи в уникальную нативную пространственную структуру.

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Парадокс Левинталя • сформулирован в 1968 г. С. Левинталем: «промежуток времени, за который полипептид приходит к своему скрученному состоянию, на много порядков меньше, чем если бы полипептид просто перебирал все возможные конфигурации» Чтобы разрешить данный парадокс, необходимо ответить на вопрос: «Как белок выбирает свою нативную структуру среди бесчисленного множества возможных? » . Для цепи из 100 остатков число возможных конформаций ~10100 , и их полный перебор занял бы ~1080 лет, если один переход осуществлять за ~10− 13 секунды. Поэтому сложность проблемы заключается в том, что данный вопрос нельзя решить экспериментально, так как придется ждать ~1080 лет! • • ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

В 1972 г. К. Анфинсен получил Нобелевскую премию по химии «за работы по рибонуклеазе, в частности, за установление связи между последовательностью аминокислот и конформацией биологически активной молекулы» , а его статья в Science стала классикой в теории фолдинга белка. Главный принцип фолдинга – код фолдинга белка заложен в его аминокислотной последовательности. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Самосборка полипептидной цепи идет поэтапно, элементы более низкой структурной организации являются фундаментом для формирования более высоких уровней структуры. Число термодинамических стабильных укладок полипептидной цепи резко лимитировано. Структурный каркас практически всегда должен состоять из α-спиральных или β-структурных слоев, а лишенные вторичной структуры петли должны проходить по поверхности. Небольшие белки (до 100 аминокислотных остатков) принимают одну из нескольких наиболее компактных структур. Для более крупных белков стабильной становится доменная структура. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Домены – участки молекулы белка, имеющие вид глобулы, которые могут сохранять характерную для них трехмерную структуру даже после отделения от всей остальной молекулы. Домены: -Сворачиваются самостоятельно -Один и тот же домен может встречаться в разных белках (белках, которые выполняют разную функцию) -Белки часто состоят из нескольких доменов

Как располагаются различные аминокислоты в разных структурных участках полипептидной цепи? 1)В α-спиралях располагаются преимущественно гидрофобные аминокислоты. На поверхности αспиралей формируются гребни из гидрофобных радикалов аминокислот, что дает возможность образования доменной, шпилечной организации белков. • 2)На концах α-спиралей, в местах их прерывания располагаются заряженные аминокислоты, они дестабилизируют α-спираль и β-структуру. • 3)В углах поворота полипептидной цепи располагаются короткие полярные аминокислоты, а также глицин и пролин. • • ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Иерархия структуры белка. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
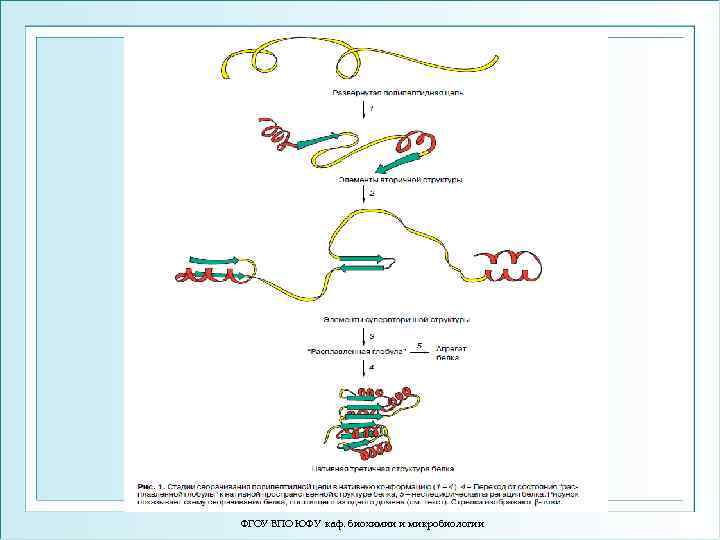
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Механизмы фолдинга 1) Гипотеза нуклеации и роста. Лимитирующий этап – формирование «ядра сворачивания» . Фолдинг идет по принципу «все или ничего» : молекула белка скачком переходит в свернутое состояние. 2) Гипотеза формирования кинетических интермедиатов с последующим возрастанием упорядоченности. Особенность – формирование «расплавленной глобулы» . В этом состоянии молекула белка сохраняет многие особенности нативной топологии, т. е. взаимного расположения α-спиралей и β -тяжей, но при этом значительно ослаблена жесткая упаковка боковых радикалов. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
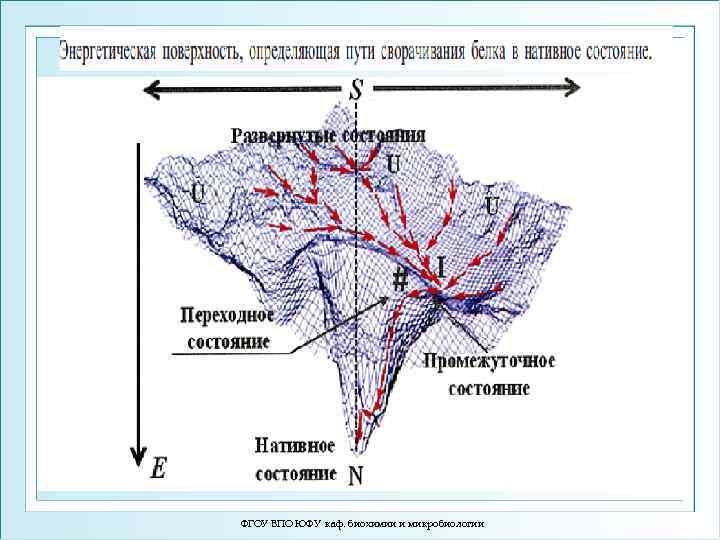
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
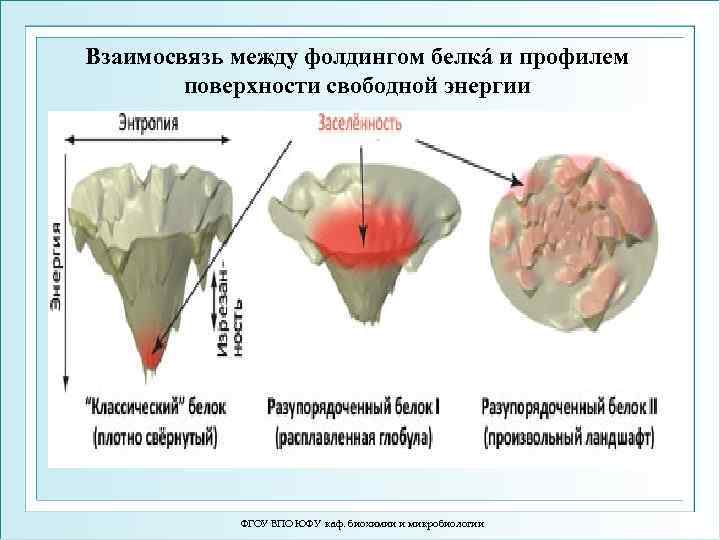
Взаимосвязь между фолдингом белкá и профилем поверхности свободной энергии ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
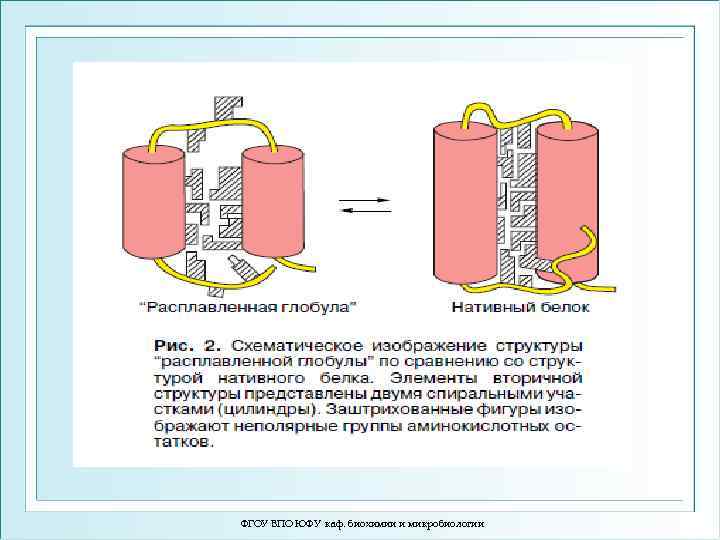
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

В расплавленной глобуле гидрофобные боковые группы обретают свободу движений, выигрывают энтропию, но теряют энергию плотного контакта. Так в глобуле возникают пoры, куда проникает вода, не разваливая расплавленную глобулу, но приводит к ее набуханию. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Ососбенности расплавленной глобулы Нативная глобула Расправленная глобула 1. Компактность 1. Нет уникальной упаковки боковых групп 2. Наличие ядра 2. Флуктуации молекулы 3. Снижение подвижности части ароматических боковых групп 3. Повышение подвижности алифатических боковых групп 4. Часть остатков Триптофана скрыты от воды 4. Часть остатков Триптофана выходит в воду 5. Сохранение объемных взаимодействий 5. Нарушение большинства объемных взаимодействий 6. Усиленное связывание неполярных молекул ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Факторы фолдинга 1) Ферменты фолдинга, или фолдазы, ускоряющие процесс сворачивания белка. 2) Молекулярные шапероны. Способствуют правильной укладке белка, предотвращают денатурацию и агрегацию; направляют необратимо денатурированные белки в систему пртеасомной деградации. 3) Котрансляционное сворачивание – укладка в процессе синтеза на рибосоме (1. образуется туннель, где располагается синтезирующийся белкок, что защищает его от денатурации и деградации; 2. большая субъединица рибосомы может работать как шаперон).
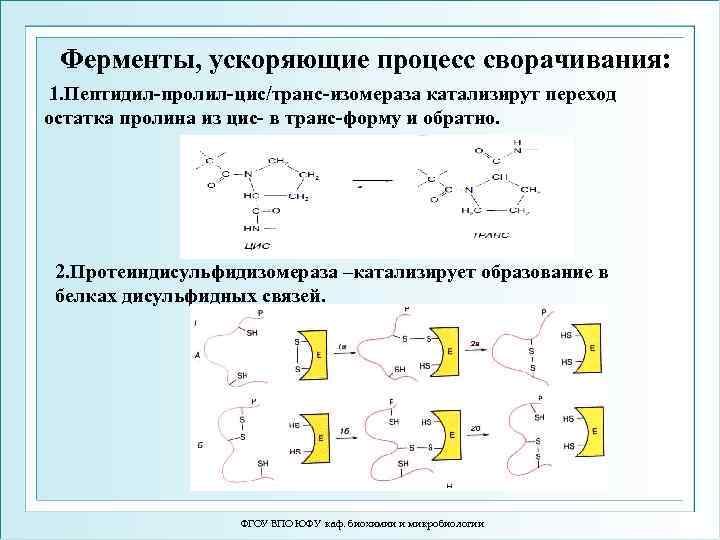
Ферменты, ускоряющие процесс сворачивания: 1. Пептидил-пролил-цис/транс-изомераза катализирут переход остатка пролина из цис- в транс-форму и обратно. 2. Протеиндисульфидизомераза –катализирует образование в белках дисульфидных связей. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Конформационные патологии (КБ) КБ - это заболевания, характеризующиеся нарушнием механизмов, обеспечивающих нативную укладку клеточных белков (фолдинг) в процессе их созревания и выполнения ими физиологических функций. • При КБ наблюдается агрегация аномальных белков, что приводит к формированию амилоидных отложений. • К КБ относятся: нейродегенеративные заболевания (болезнь Паркинсона, болезнь Альцгеймера, боковой амиотрофический склероз, болезнь Гентингтона); • трансмиссивные спонгиозные энцефалопатии (куру, болезнь Крецфельда-Якоба, семейная инсомния) • ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
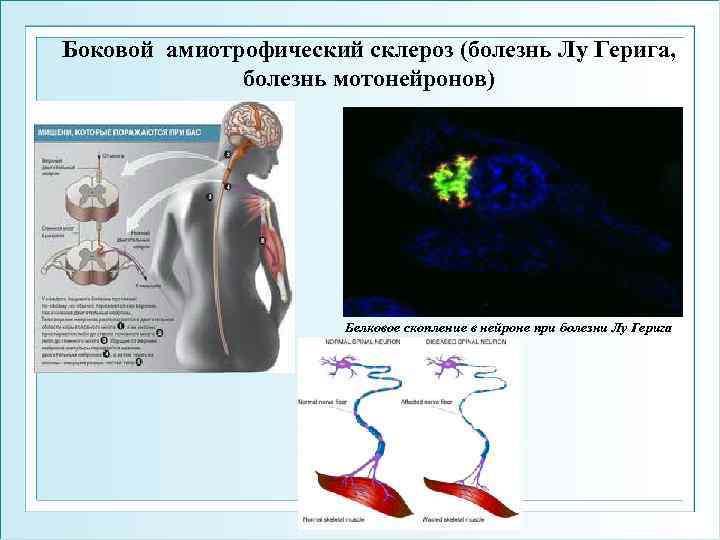
Боковой амиотрофический склероз (болезнь Лу Герига, болезнь мотонейронов) Белковое скопление в нейроне при болезни Лу Герига

Генри Луи Гериг, прозванный за выносливость «Железный конь» — выдающийся бейсболист. В возрасте 36 лет он заболел боковым амитрофическим склерозом, который широко известен в США и Канаде как «болезнь Лу Герига» . Эксперт по черным дырам, Стивен Хокинг – один из самых выдающихся астрофизиков. Его достижения еще более значимы потому, что ученый страдает дегенеративным генетическим заболеванием, которое диагностировали, когда Стивену был 21 год; тогда будущему ученому врачи обещали всего несколько лет. Но Хокинг не только прожил полвека, но и сделал множество фундаментальных открытий в области теоретической астрофизики.

Папуасы, больные куру. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
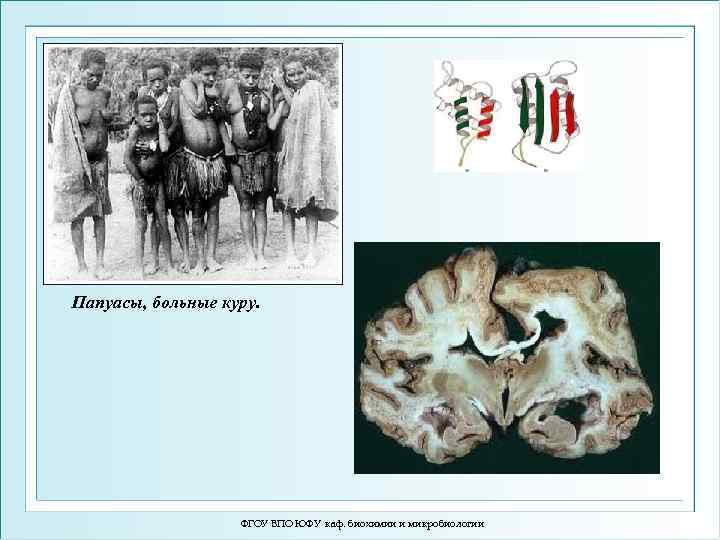
Папуасы, больные куру. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Туннельный эффект. Туннельный эффект, туннелирование — преодоление микрочастицей потенциального барьера в случае, когда её полная энергия (остающаяся при туннелировании неизменной) меньше высоты барьера. U Если высота барьера U больше, чем энергия U 0 частицы, то, с точки зрения классической механики, прохождение этой частицей барьера абсолютно невозможно, W но тем не менее она его преодолевает. Объяснение этому эффекту даёт квантовая теория. Вероятность прохождения частицы сквозь барьер характеризуется величиной D – коэффициент прозрачности барьера. X L ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
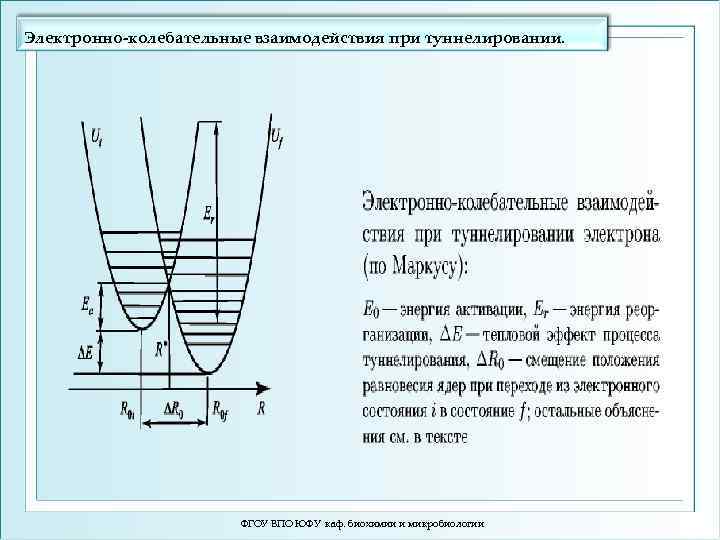
Электронно-колебательные взаимодействия при туннелировании. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Для макроскопических частиц массой 1 г при высоте барьера 1 эрг и его длине 1 см вероятность туннелирования столь ничтожна, что даже если частица будет сталкиваться с барьером 1015 раз в сек. , то за время жизни Вселенной вероятность туннельного прохождения барьера будет исчезающее мала. Для частиц с массой 10 -27 г при высоте барьера 1 э. В, длине барьера 1 ангстрем прозрачность потенциального барьера становится порядка 1. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

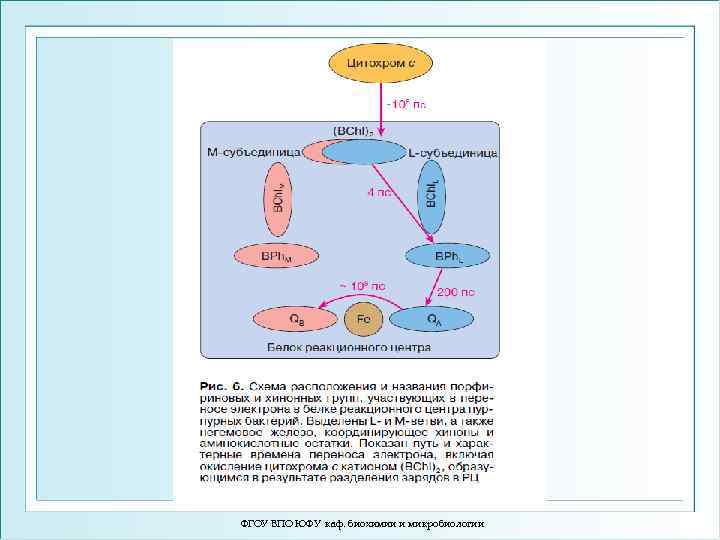
Особенности туннельного эффекта в белках: 1) структурное туннелирование; 2) электрон-конформационные взаимодействия (ЭКВ): - образование «электронной тропы» , вдоль которой происходят поэтапный перенос электронов от донорной группы к акцепторной; - участие виртуальных уровней промежуточных звеньев (аминокислотные последовательности, которые играют роль электронных мостиков – π-мостиков). ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 59

Туннельные трубы, по которым идет транспорт электронов в цитохромоксидазе. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 60
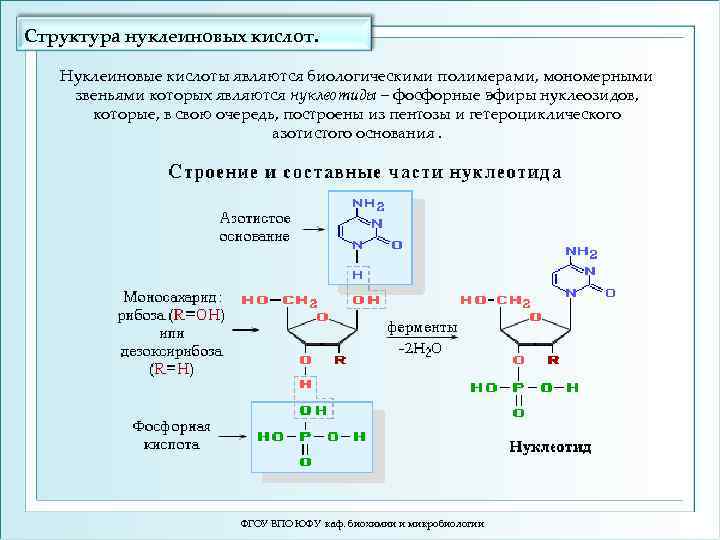
Структура нуклеиновых кислот. Нуклеиновые кислоты являются биологическими полимерами, мономерными звеньями которых являются нуклеотиды – фосфорные эфиры нуклеозидов, которые, в свою очередь, построены из пентозы и гетероциклического азотистого основания. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
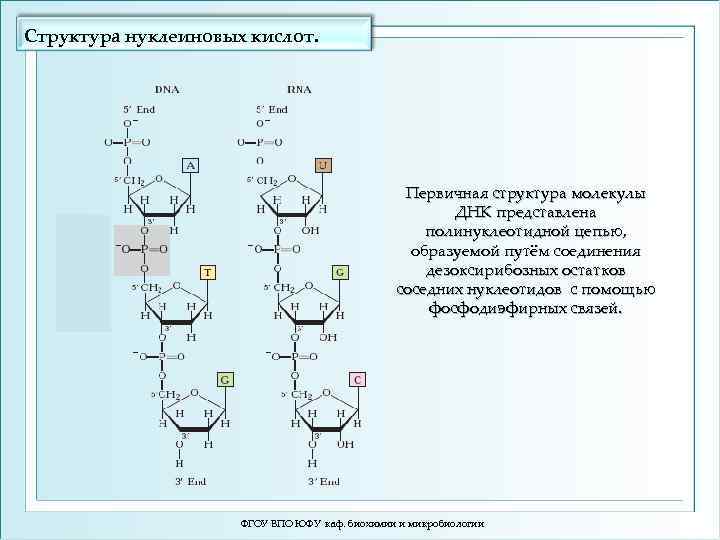
Структура нуклеиновых кислот. Первичная структура молекулы ДНК представлена полинуклеотидной цепью, образуемой путём соединения дезоксирибозных остатков соседних нуклеотидов с помощью фосфодиэфирных связей. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
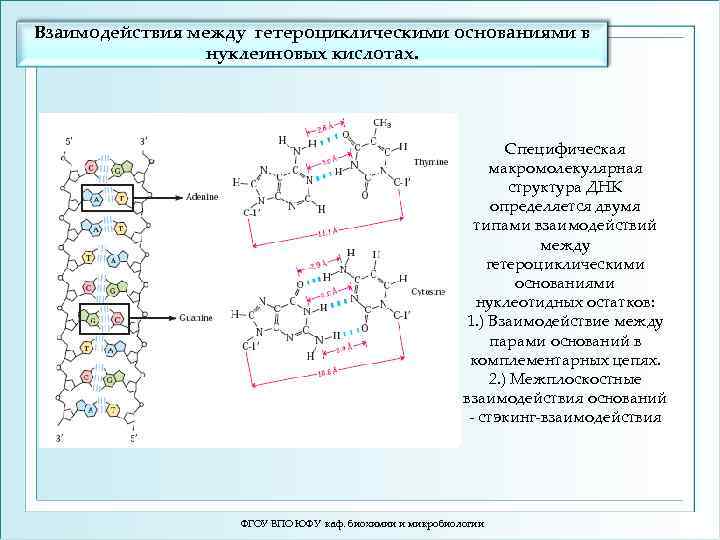
Взаимодействия между гетероциклическими основаниями в нуклеиновых кислотах. Специфическая макромолекулярная структура ДНК определяется двумя типами взаимодействий между гетероциклическими основаниями нуклеотидных остатков: 1. ) Взаимодействие между парами оснований в комплементарных цепях. 2. ) Межплоскостные взаимодействия оснований - стэкинг-взаимодействия ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Двойная спираль молекулы ДНК. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
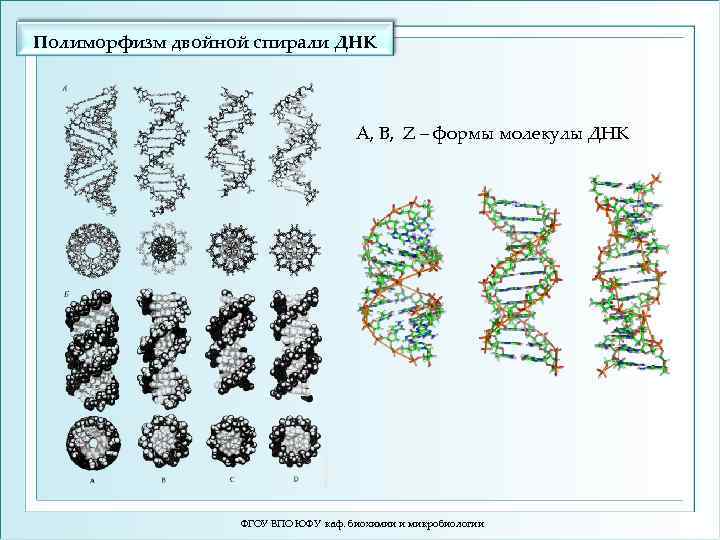
Полиморфизм двойной спирали ДНК А, В, Z – формы молекулы ДНК ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Лекция № 6 Биофизика мембранных процессов ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Структурно-молекулярная организация биомембраны. Структурной основой биомембраны служит липидный бимолекулярный слой. В состав мембраны входят белки, которые подразделяются на интегральные, полуинтегральные и периферические. Кроме того в состав мембраны входят углеводы, которые образуют сложные соединения с белками. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
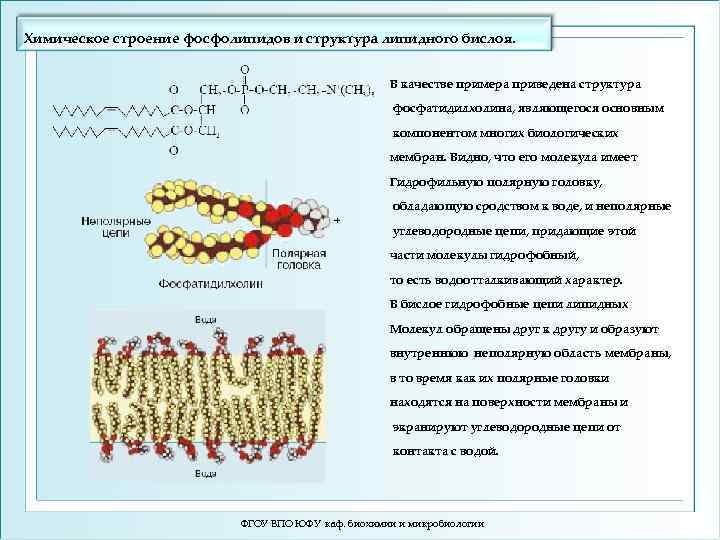
Химическое строение фосфолипидов и структура липидного бислоя. В качестве примера приведена структура фосфатидилхолина, являющегося основным компонентом многих биологических мембран. Видно, что его молекула имеет Гидрофильную полярную головку, обладающую сродством к воде, и неполярные углеводородные цепи, придающие этой части молекулы гидрофобный, то есть водоотталкивающий характер. В бислое гидрофобные цепи липидных Молекул обращены друг к другу и образуют внутреннюю неполярную область мембраны, в то время как их полярные головки находятся на поверхности мембраны и экранируют углеводородные цепи от контакта с водой. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
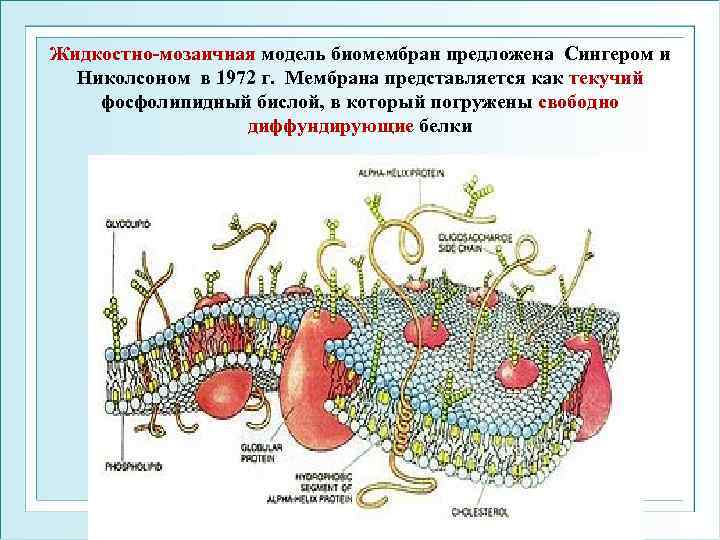
Жидкостно-мозаичная модель биомембран предложена Сингером и Николсоном в 1972 г. Мембрана представляется как текучий фосфолипидный бислой, в который погружены свободно диффундирующие белки ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Жидкостно-мозаичная модель строения мембран названа «последней классической» теорией потому, что, с одной стороны, она явно устарела, а с другой – современные представления не достигли еще той лаконичной изящности, чтобы их начала можно было бы легко изложить в школьном учебнике (Bagatolli et al. , 2010). ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Недостатки жидкостно-мозаичной модели 1. Не все белки свободно диффундируют в жидком липидном бислое. 2. Имеются отличия от классического липидного бислоя за счет липидного полиморфизма. 3. Наблюдается неоднородность мембраны за счет явления латеральной гетерогенности бислоя. 4. Наблюдается сложная динамическая структура биомембран, для которой характерны: - вариации толщины, - образование небислойных структур ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Липидный состав клеточных мембран ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Принципы организации липидного бислоя 1. Амфифильность фосфолипидов. 2. Полиморфизм липидов – способность образовывать агрегаты различных типов, которые могут переходить друг в друга. 3. Текучесть (микровязкость) биомембран. 4. Фазовые переходы мембранных липидов. 5. Латеральная гетерогенность мембранных липидов. 6. Подвижность мембранных липидов. 7. Трансбислойная асимметрия липидов. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
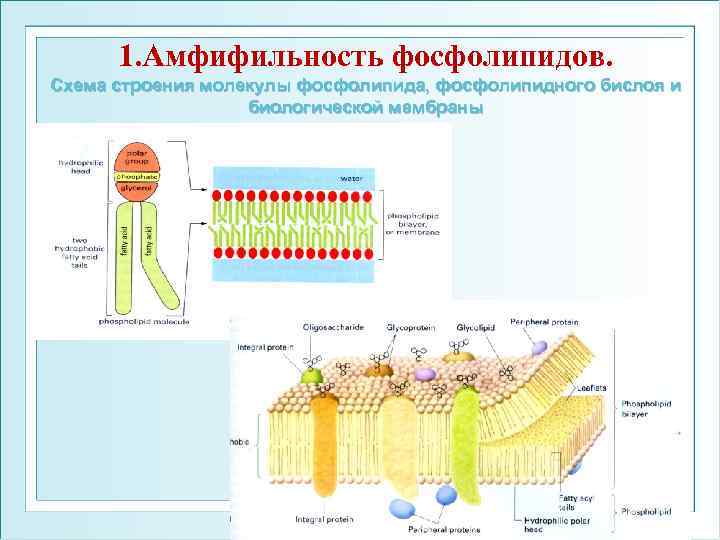
1. Амфифильность фосфолипидов. Схема строения молекулы фосфолипида, фосфолипидного бислоя и биологической мембраны ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 75
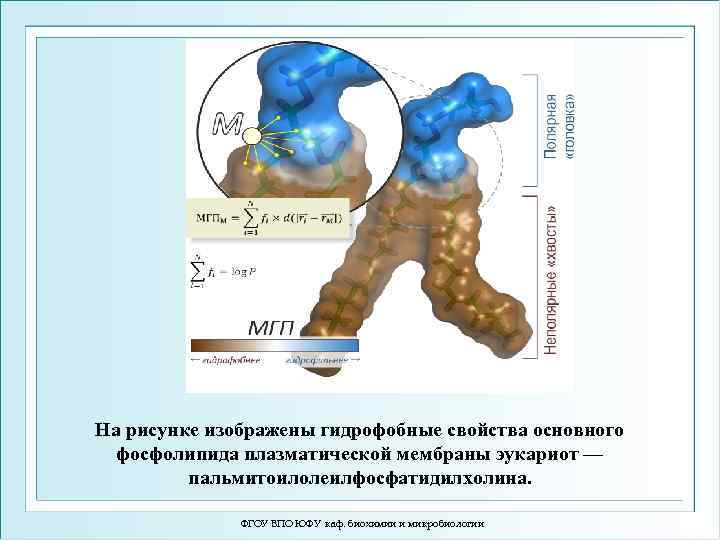
На рисунке изображены гидрофобные свойства основного фосфолипида плазматической мембраны эукариот — пальмитоилолеилфосфатидилхолина. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
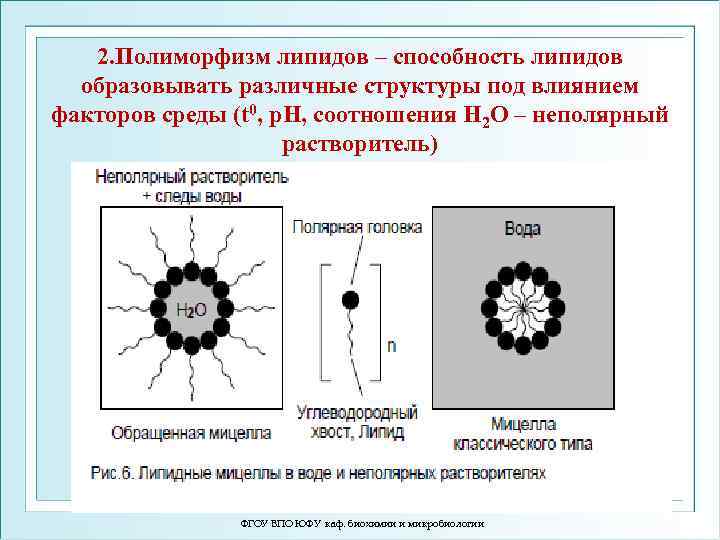
2. Полиморфизм липидов – способность липидов образовывать различные структуры под влиянием факторов среды (t 0, p. H, соотношения H 2 O – неполярный растворитель) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
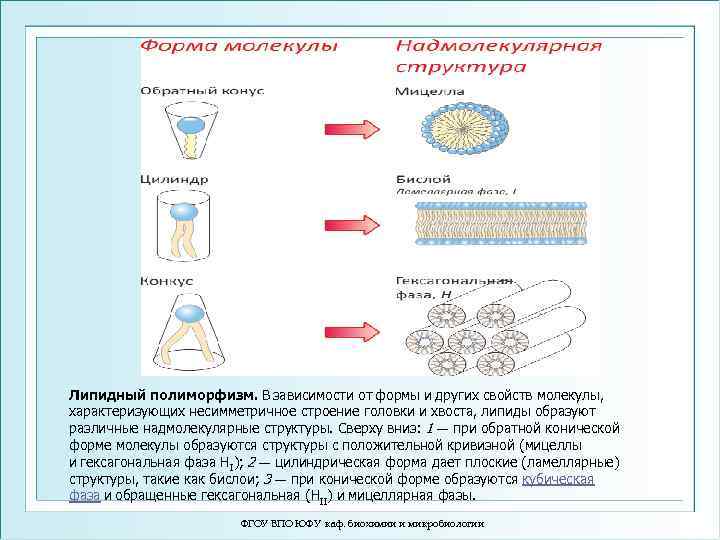
Липидный полиморфизм. В зависимости от формы и других свойств молекулы, характеризующих несимметричное строение головки и хвоста, липиды образуют различные надмолекулярные структуры. Сверху вниз: 1 — при обратной конической форме молекулы образуются структуры с положительной кривизной (мицеллы и гексагональная фаза HI); 2 — цилиндрическая форма дает плоские (ламеллярные) структуры, такие как бислои; 3 — при конической форме образуются кубическая фаза и обращенные гексагональная (HII) и мицеллярная фазы. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Основные типы структурной организации водно -липидных систем ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

3. Текучесть (микровязкость) липидной фазы биомембран регулирует мембранные процессы. В физиологических условиях липиды мембран имеют жидко-кристаллическую структуру, что необходимо для нормального функционирования. 2. Степень текучести мембран зависит от: - длины жирнокислотных цепей и степени их ненасыщенности; - соотношения фосфолипиды/стерины; - физических факторов (to , р, р. Н, потенциала) 1.

Взаимосвязь степени ненасыщенности липидных молекул и текучести мембран 1. При постоянной длине ацильной цепи и температуре, увеличение количества двойных связей повышает текучесть мембраны. 2. При постоянном количестве двойных связей и постоянной температуре, удлинение ацильной цепи уменьшает текучесть мембраны. 3. При любой комбинации длины цепей и двойных связей, увеличение температуры повышает текучесть мембраны

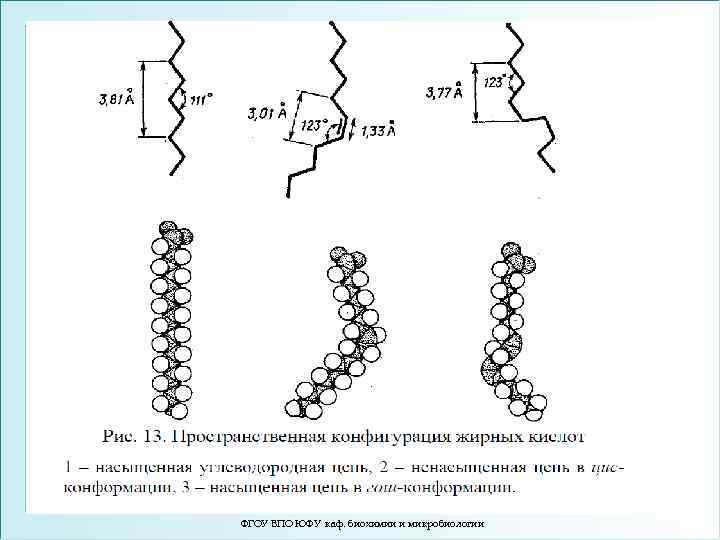
4. Фазовые переходы мембранных липидов. В жидко-кристаллической фазе наблюдается конформационное плавление – транс-конформация ацилов жирных кислот переходит в гош-конформацию, что приводит к образованию кинков (кинк – петля). ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
![[9] Гипотеза кинков. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии [9] Гипотеза кинков. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии](https://present5.com/presentation/19930286_335801816/image-84.jpg)
[9] Гипотеза кинков. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
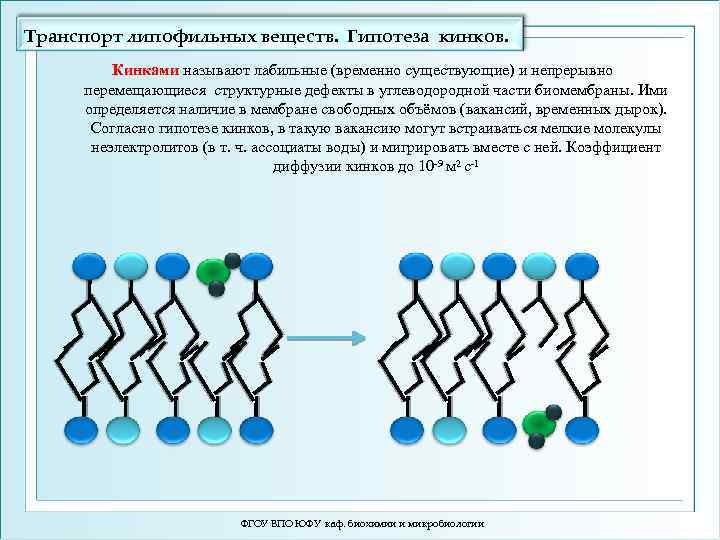
Транспорт липофильных веществ. Гипотеза кинков. Кинками называют лабильные (временно существующие) и непрерывно перемещающиеся структурные дефекты в углеводородной части биомембраны. Ими определяется наличие в мембране свободных объёмов (вакансий, временных дырок). Согласно гипотезе кинков, в такую вакансию могут встраиваться мелкие молекулы неэлектролитов (в т. ч. ассоциаты воды) и мигрировать вместе с ней. Коэффициент диффузии кинков до 10 -9 м 2 с-1 ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Расположение молекул в аморфном (а) и жидкокристаллическом состояниях (б, в, г) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
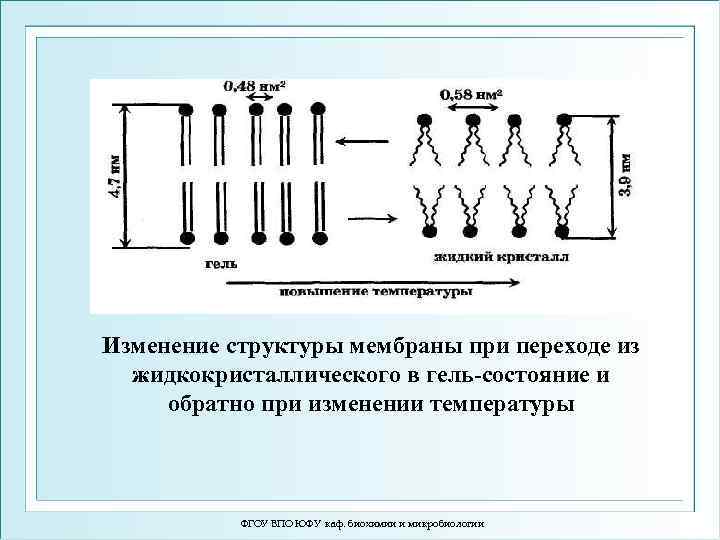
Изменение структуры мембраны при переходе из жидкокристаллического в гель-состояние и обратно при изменении температуры ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

5. Латеральная гетерогенность мембранных липидов. Латеральная гетерогенность мембраны – это свойство бислойной мембраны сложного липидного состава образовывать неоднородности (несмешиваемые микрофазы, микродомены или рафты). Мембранные рафты – это маленькие (10 -200 нм), гетерогенные и очень динамичные липидные домены, обогащенные холестеролом, сфинголипидами, специфическими белками, более структурированные и упорядоченные, чем окружающая «жидкая» фаза. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
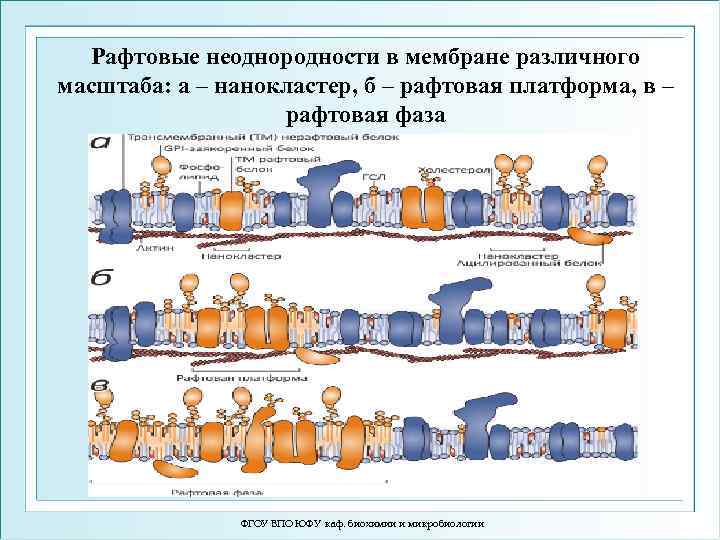
Рафтовые неоднородности в мембране различного масштаба: а – нанокластер, б – рафтовая платформа, в – рафтовая фаза ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Взаимодействие лейкоцитов с липидными рафтами ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

6. Трансбислойная асимметрия мембранных липидов – это различное распределение липидов между внутренним и наружным монослоями. 1. Во внешнем монослое локализуются холинсодержащие липиды – фосфатидилхолин, сфингомиелин, а также стероид холестерол. 2. Во внутреннем монослое локализуются аминосодержащие ФЛ – фосфатидилэтаноламин, фосфатидилсерин. 3. Во внешнем монослое – 1/3 двойных связей, во внутреннем – 2/3 двойных связей. 4. Известны 2 механизма, обеспечивающие асимметрию липидного бислоя: - различия конформационных размеров полярных «головок» липидов; - транслокация с помощью белков-переносчиков. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
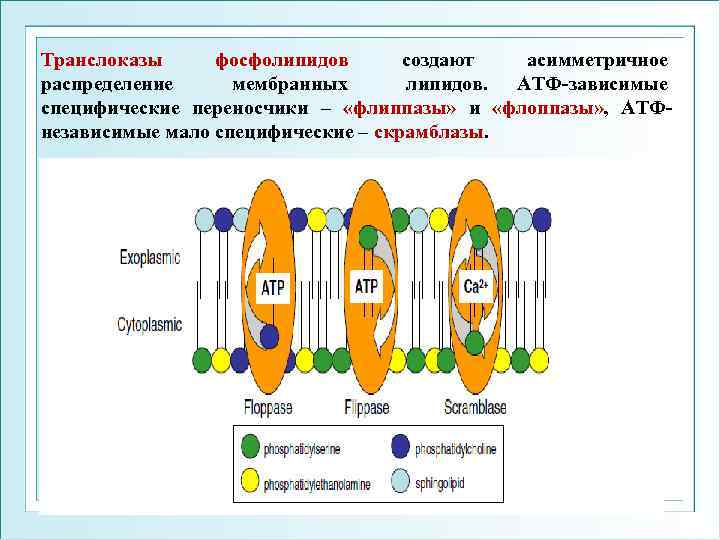
Транслоказы фосфолипидов создают асимметричное распределение мембранных липидов. АТФ-зависимые специфические переносчики – «флиппазы» и «флоппазы» , АТФнезависимые мало специфические – скрамблазы.

Различные виды подвижности мембранных липидов 1. Изменение ориентации полярных голов. 2. Латеральная подвижность. 3. Сегментарная подвижность – колебания ацильный цепей. 4. Образование кинков и их миграция вдоль ацильных цепей. 5. Ротационная подвижность. 6. Флип-флоп переходы. 7. Выход из бислоя.

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
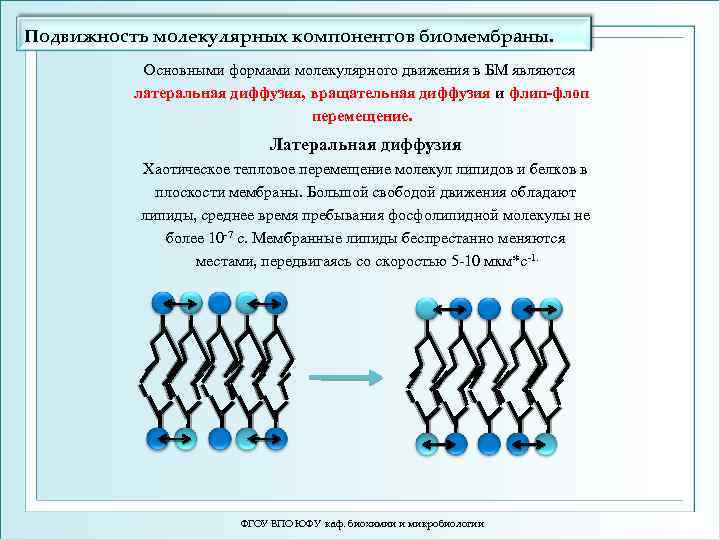
Подвижность молекулярных компонентов биомембраны. Основными формами молекулярного движения в БМ являются латеральная диффузия, вращательная диффузия и флип-флоп перемещение. Латеральная диффузия Хаотическое тепловое перемещение молекул липидов и белков в плоскости мембраны. Большой свободой движения обладают липиды, среднее время пребывания фосфолипидной молекулы не более 10 -7 с. Мембранные липиды беспрестанно меняются местами, передвигаясь со скоростью 5 -10 мкм*с-1. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
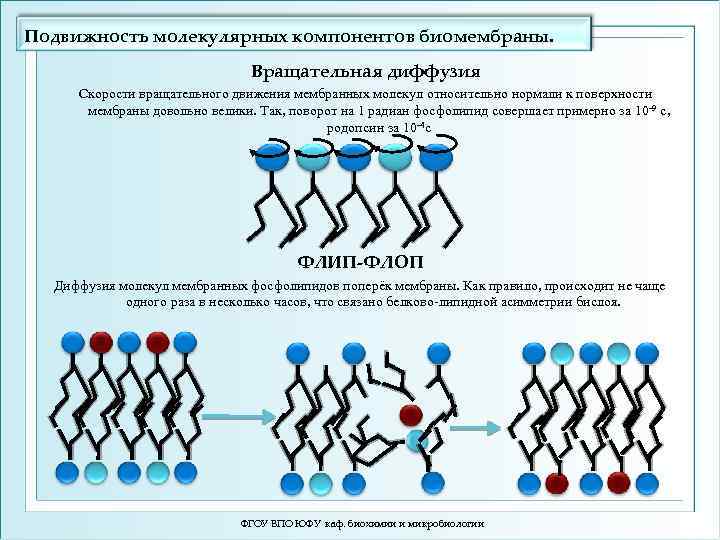
Подвижность молекулярных компонентов биомембраны. Вращательная диффузия Скорости вращательного движения мембранных молекул относительно нормали к поверхности мембраны довольно велики. Так, поворот на 1 радиан фосфолипид совершает примерно за 10 -9 с, родопсин за 10 -4 с ФЛИП-ФЛОП Диффузия молекул мембранных фосфолипидов поперёк мембраны. Как правило, происходит не чаще одного раза в несколько часов, что связано белково-липидной асимметрии бислоя. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
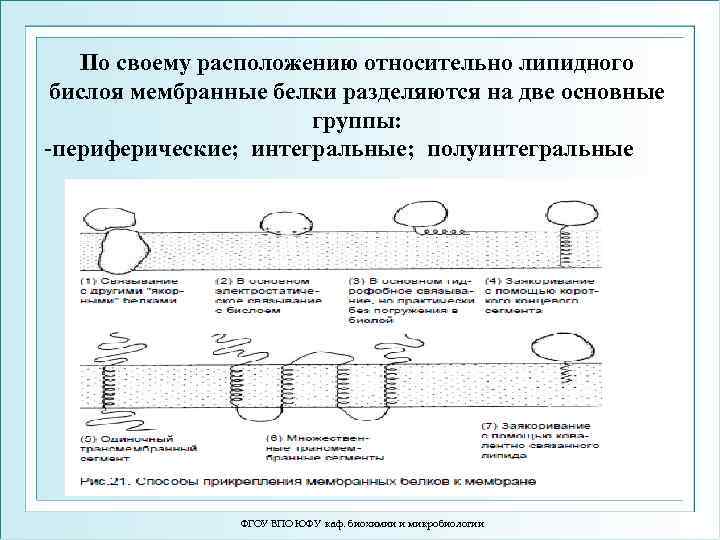
По своему расположению относительно липидного бислоя мембранные белки разделяются на две основные группы: -периферические; интегральные; полуинтегральные ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

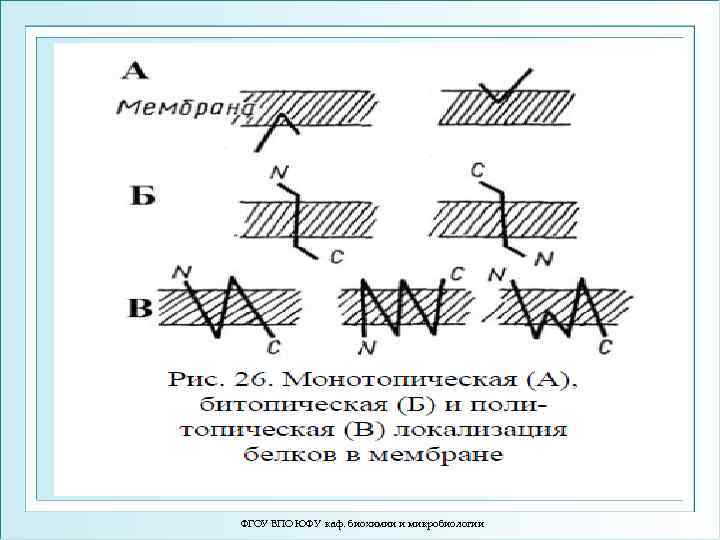
Топологическая классификация мембранных белков: 1. Монотопические – являются периферическими белками и не пронизывают мембрану (цит b 5) 2. Битопические – пронизывают мембрану один раз (гликофорин) 3. Политопические - пронизывают мембрану два и более раз (рецепторы, сопряженные с Gбелками; Na, K- АТФ-аза; АТФ-синтаза) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Расположение белков в мембране ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
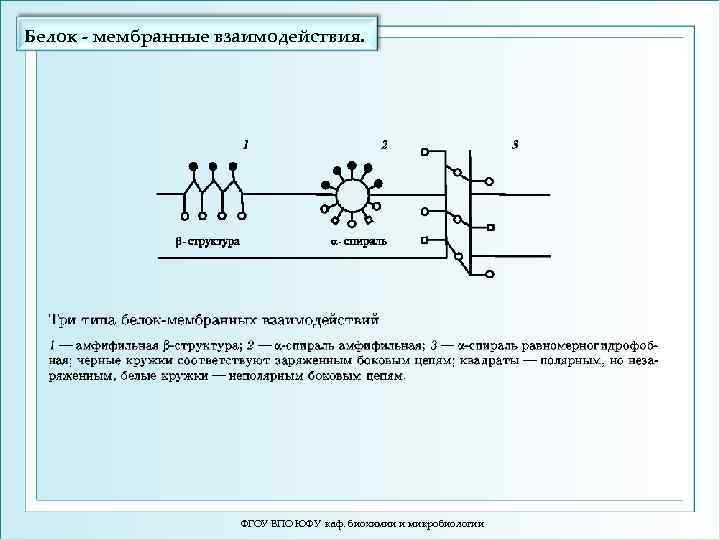
Белок - мембранные взаимодействия. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Функции мембранных белков • • • Мембранные белки по биологической роли делятся на 3 группы: 1)белки-ферменты, обладающие каталитической активностью 2)рецепторные белки, специфически связывающие лиганды 3) белки-ионные каналы 4)структурные белки
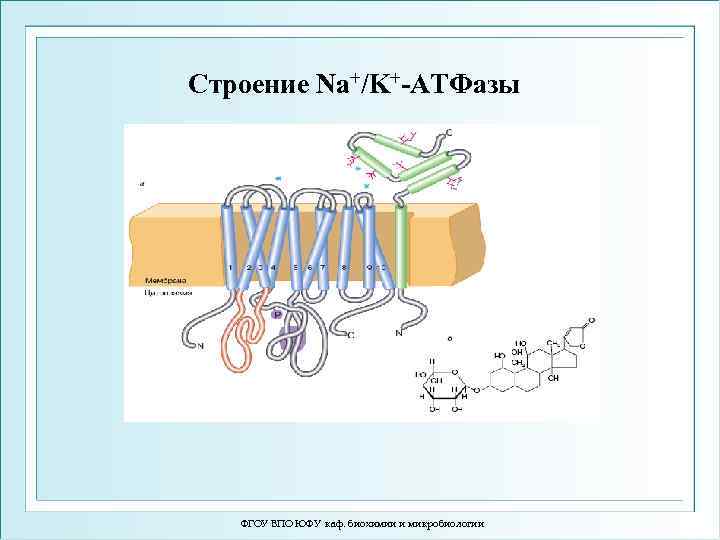
Строение Na+/K+-ATФазы ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
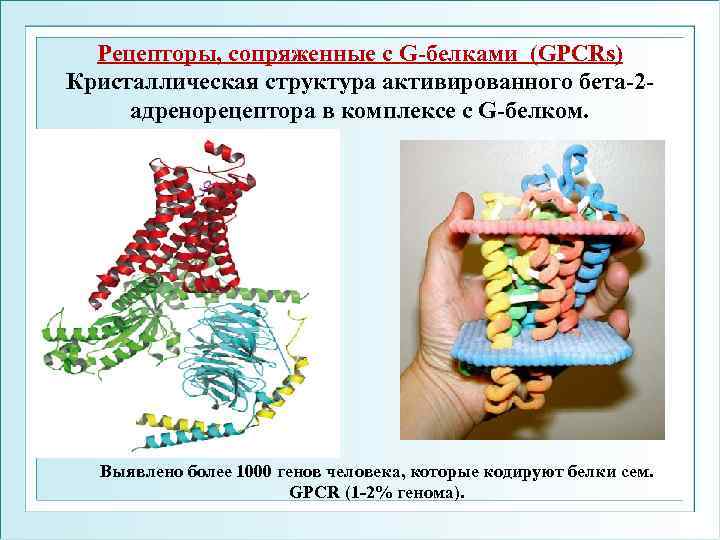
Рецепторы, сопряженные с G-белками (GPCRs) Кристаллическая структура активированного бета-2 адренорецептора в комплексе с G-белком. Выявлено более 1000 генов человека, которые кодируют белки сем. GPCR (1 -2% генома).
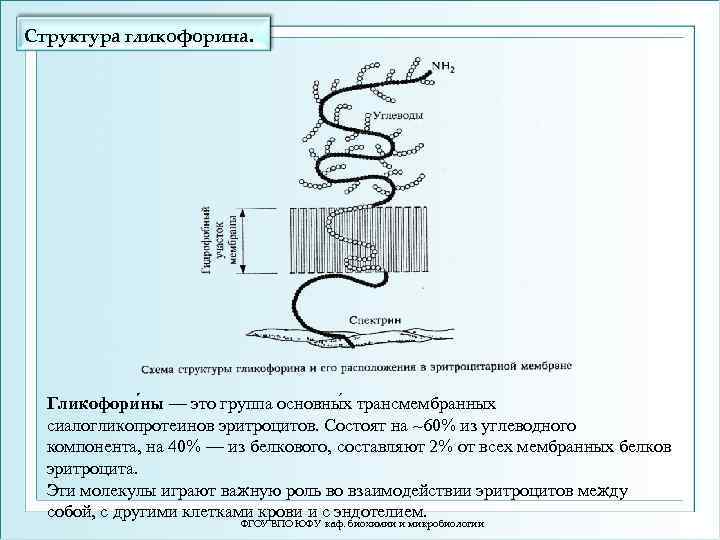
Структура гликофорина. Гликофори ны — это группа основны х трансмембранных сиалогликопротеинов эритроцитов. Состоят на ~60% из углеводного компонента, на 40% — из белкового, составляют 2% от всех мембранных белков эритроцита. Эти молекулы играют важную роль во взаимодействии эритроцитов между собой, с другими клетками крови и с эндотелием. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
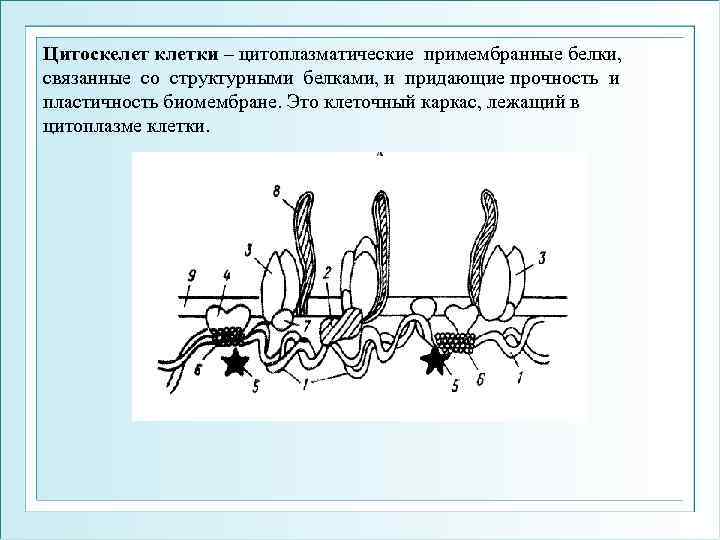
Цитоскелет клетки – цитоплазматические примембранные белки, связанные со структурными белками, и придающие прочность и пластичность биомембране. Это клеточный каркас, лежащий в цитоплазме клетки.

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 107
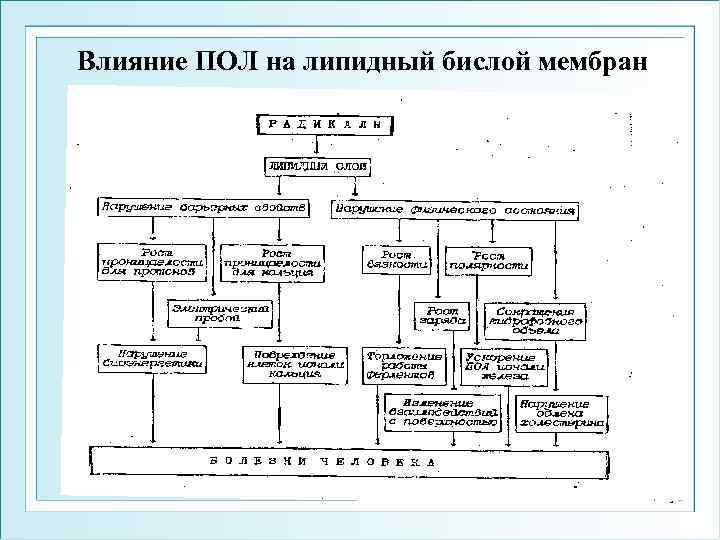
Влияние ПОЛ на липидный бислой мембран
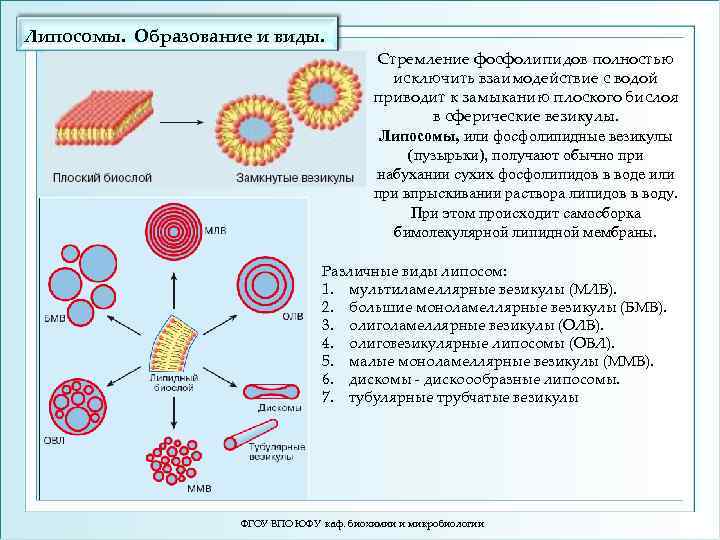
Липосомы. Образование и виды. Стремление фосфолипидов полностью исключить взаимодействие с водой приводит к замыканию плоского бислоя в сферические везикулы. Липосомы, или фосфолипидные везикулы (пузырьки), получают обычно при набухании сухих фосфолипидов в воде или при впрыскивании раствора липидов в воду. При этом происходит самосборка бимолекулярной липидной мембраны. Различные виды липосом: 1. мультиламеллярные везикулы (МЛВ). 2. большие моноламеллярные везикулы (БМВ). 3. олиголамеллярные везикулы (ОЛВ). 4. олиговезикулярные липосомы (ОВЛ). 5. малые моноламеллярные везикулы (ММВ). 6. дискомы - дискоообразные липосомы. 7. тубулярные трубчатые везикулы ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
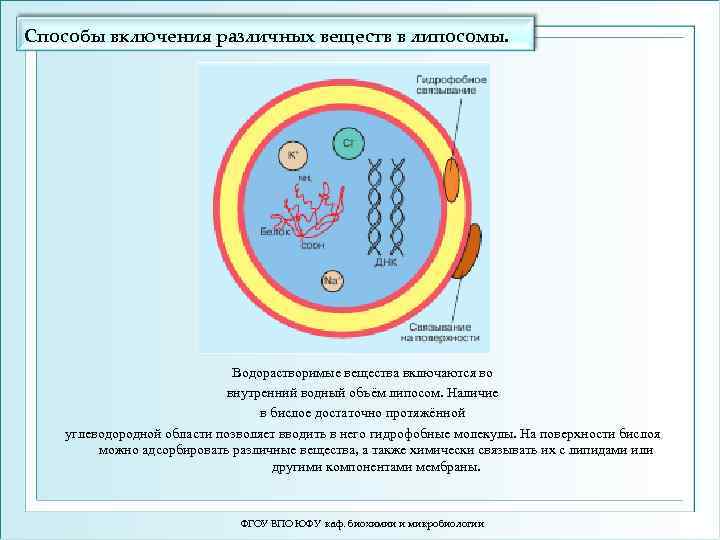
Способы включения различных веществ в липосомы. Водорастворимые вещества включаются во внутренний водный объём липосом. Наличие в бислое достаточно протяжённой углеводородной области позволяет вводить в него гидрофобные молекулы. На поверхности бислоя можно адсорбировать различные вещества, а также химически связывать их с липидами или другими компонентами мембраны. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Применение липосом. Применение липосом и везикул В фундаментальных научных исследованиях В фармакологии и медицине В косметологии ФГОУ ВПО ЮФУ каф. биохимии и микробиологии В пищевой индустрии

Липосомы-невидимки. Полиэтиленгликоль с молекулярной массой 1500 -5000 дальтон ковалентно связывали с фосфатидилэтаноламином и такой коньюгированный липид в количестве не более 10% включали в липосомы. Полагают, что сильно гидратированная полимерная "шуба" затрудняет адсорбцию антител (А) и других защитных белков (Р) на поверхности таких липосом, в результате чего макрофаги не воспринимают их как подлежащие удалению чужеродные частицы. Эксперименты на животных показали, что терапевтическое действие противоопухолевых препаратов в результате включения в "липосомыневидимки" необычайно усиливается и в некоторых случаях приводит к полной ремиссии опухоли. При злокачественных опухолях наблюдалось стойкое снижение размера метастазов ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
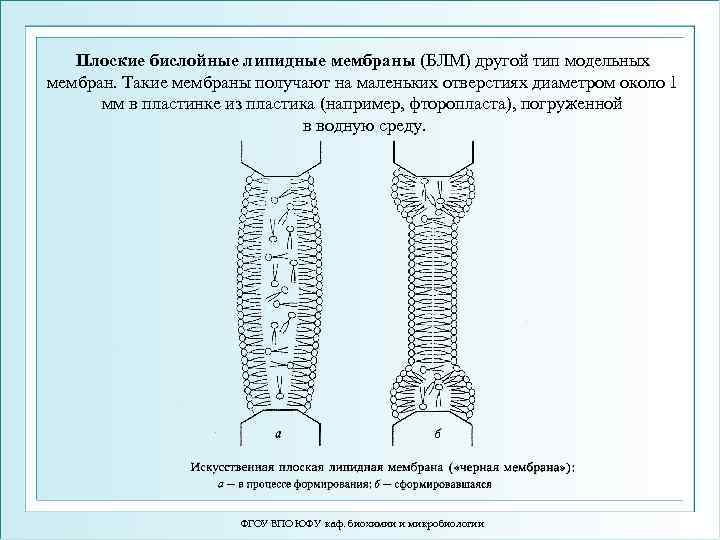
Плоские бислойные липидные мембраны (БЛМ) другой тип модельных мембран. Такие мембраны получают на маленьких отверстиях диаметром около 1 мм в пластинке из пластика (например, фторопласта), погруженной в водную среду. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
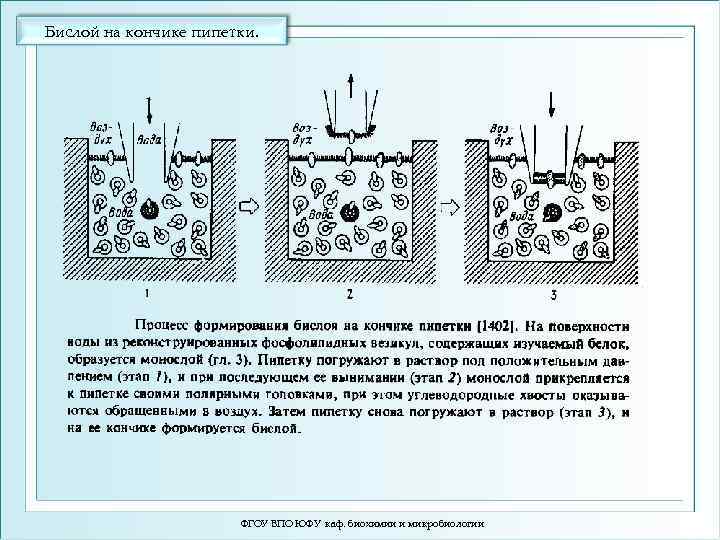
Бислой на кончике пипетки. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
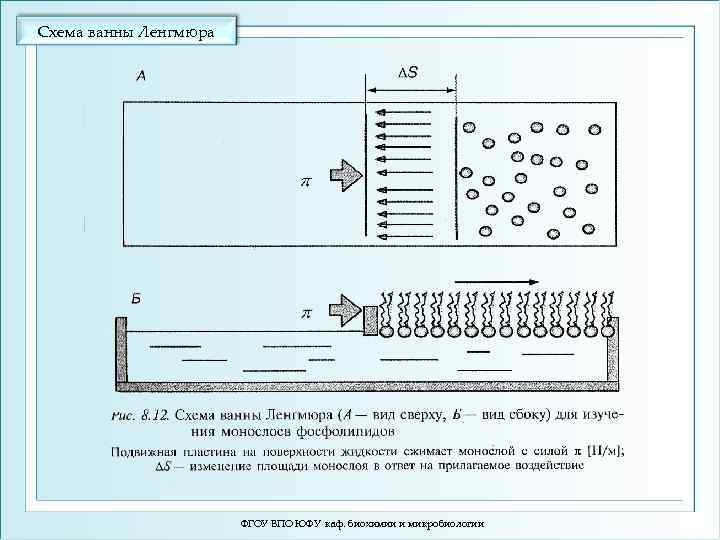
Схема ванны Ленгмюра ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
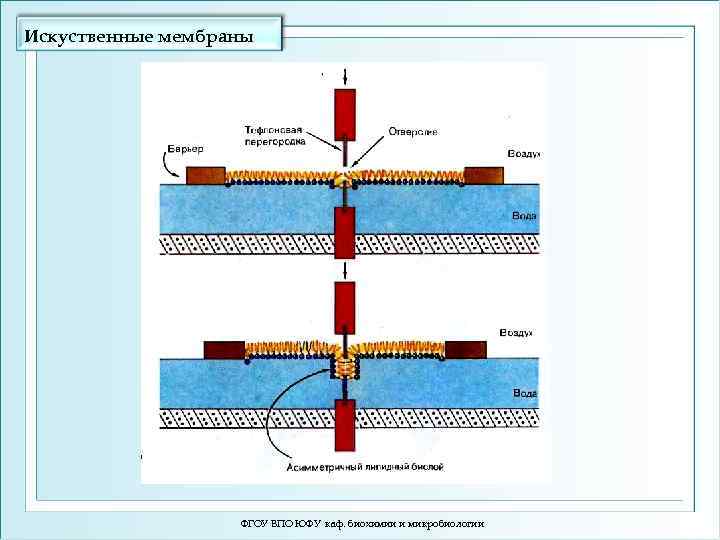
Искуственные мембраны ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Образование бислойной липидной мембраны. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Электрокинетические явления (ЭКЯ) • • • ЭКЯ – движение фаз гетерогенной среды под влиянием постоянного электрического поля, а также образование разности потенциалов в системе при механическом движении фаз. Электрофорез – движение частиц дисперсной фазы в постоянном электрическом поле к противоположно заряженному электроду. Электроосмос – движение дисперсионной среды в постоянном электрическом поле к противоположно заряженному электроду. Потенциалы течения - появление электрической разности потенциалов на концах капилляра или мембраны при протекании жидкости в результате градиента гидростатического давления. Потенциалы течения противоположны электроосмосу. Потенциалы оседания (седиментации) - появление электрической разности потенциалов в гетерогенной среде под влиянием сил гравитации между верхними и нижними слоями системы. Потенциалы оседания противоположны электрофорезу. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Схема опытов Ф. Рейсса (1808) по электроосмосу и электрофорезу В мокрую глину помещаются две заполненные водой стеклянные трубки, в которых расположены электроды, и прикладывается внешнее электрическое поле. В анодном пространстве появляется взвесь частиц, движущихся к аноду. Это указывает на то, что частицы глины заряжены отрицательно. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
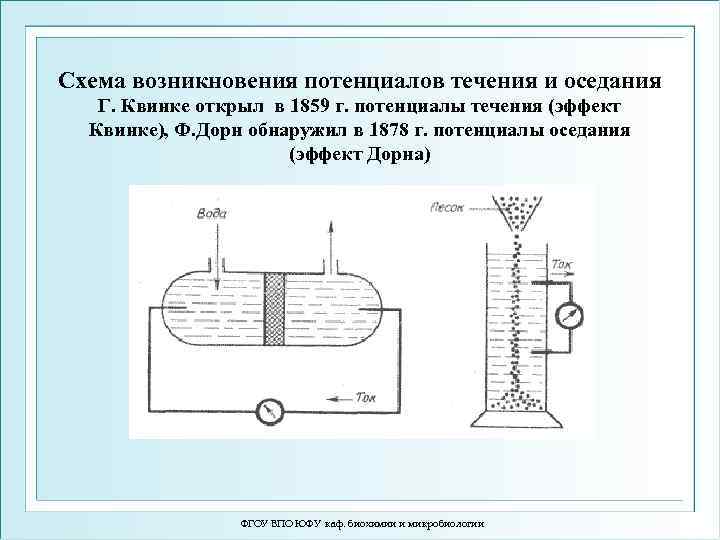
Схема возникновения потенциалов течения и оседания Г. Квинке открыл в 1859 г. потенциалы течения (эффект Квинке), Ф. Дорн обнаружил в 1878 г. потенциалы оседания (эффект Дорна) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
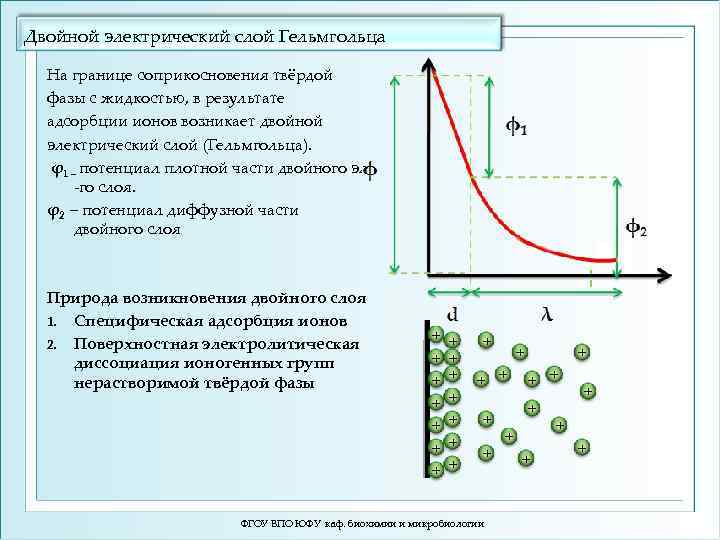
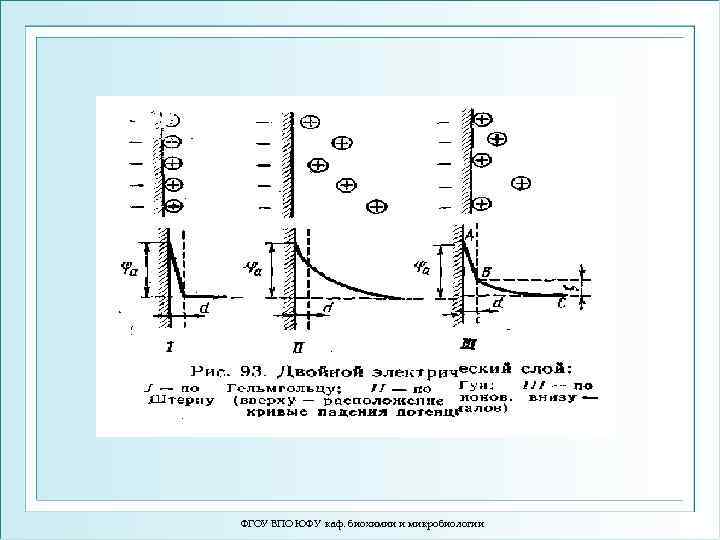
Двойной электрический слой Гельмгольца На границе соприкосновения твёрдой фазы с жидкостью, в результате адсорбции ионов возникает двойной электрический слой (Гельмгольца). φ1 – потенциал плотной части двойного эл -го слоя. φ2 – потенциал диффузной части двойного слоя Природа возникновения двойного слоя 1. Специфическая адсорбция ионов 2. Поверхностная электролитическая диссоциация ионогенных групп нерастворимой твёрдой фазы + + + + + ФГОУ ВПО ЮФУ каф. биохимии и микробиологии + + + + +
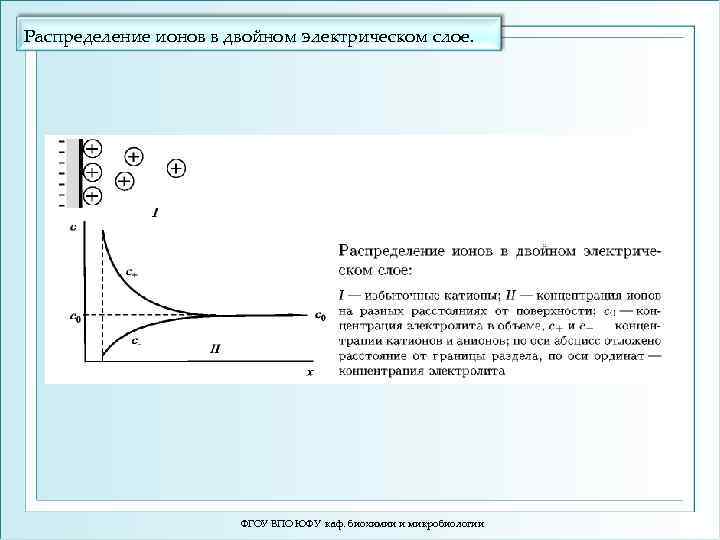
Распределение ионов в двойном электрическом слое. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Электрокинетический потенциал. Потенциал, связанный с электрокинетическими явлениями называется электрокинетическим потенциалом. ζ = Кπηu/ εЕ K – постоянная, зависящая от формы частиц η – коэффициент вязкости ε– диэлектрическая проницаемость раствора v – скорость электрофореза Е – градиент потенциала приложенного электрического поля Электрокинетический потенциал существует только в связи с движением и очень чувствителен к изменению распределения ионов в двойном слое. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
5.Презентация_Биофизика биополимеров.ppt