Лекція № 5 Дисперсні Системи Коагуляція.
Лекція № 5 Дисперсні Системи Коагуляція.
 l Біологічні рідини (кров, плазма, спинно-мозкова рідина, деякі лікарські препарати) є дисперсними системами. l Колоїдна хімія – розділ хімії, що вивчає фізико-хімічні властивості гетерогенних високодисперсних і високомолекулярних сполук. l З грецького kola- клей - Грем (1861 р. )
l Біологічні рідини (кров, плазма, спинно-мозкова рідина, деякі лікарські препарати) є дисперсними системами. l Колоїдна хімія – розділ хімії, що вивчає фізико-хімічні властивості гетерогенних високодисперсних і високомолекулярних сполук. l З грецького kola- клей - Грем (1861 р. )
 l Дисперсні системи -в якій речовина знаходиться в стані більш-менш високої подрібненості (дисперсності) частинок, які рівномірно розподілені в дисперсному середовищі. l Дисперсні системи – два компоненти: l Дисперсна фаза –подрібнена речовина l Дисперсійне середовище- де розміщена фаза
l Дисперсні системи -в якій речовина знаходиться в стані більш-менш високої подрібненості (дисперсності) частинок, які рівномірно розподілені в дисперсному середовищі. l Дисперсні системи – два компоненти: l Дисперсна фаза –подрібнена речовина l Дисперсійне середовище- де розміщена фаза
 l Колоїдно-дисперсні системи є гетерогенними, термодинамічно нестійкими. l Між частинками і середовищем є поверхня розділу, що володіє надлишком поверхневої енергії. l Характерні самодовільні процеси, що знижують надлишок енергії шляхом зменшення ступеня дисперсності.
l Колоїдно-дисперсні системи є гетерогенними, термодинамічно нестійкими. l Між частинками і середовищем є поверхня розділу, що володіє надлишком поверхневої енергії. l Характерні самодовільні процеси, що знижують надлишок енергії шляхом зменшення ступеня дисперсності.
 l. Ступінь подрібненості, чи ступінь дисперсності, системи D = 1/d.
l. Ступінь подрібненості, чи ступінь дисперсності, системи D = 1/d.
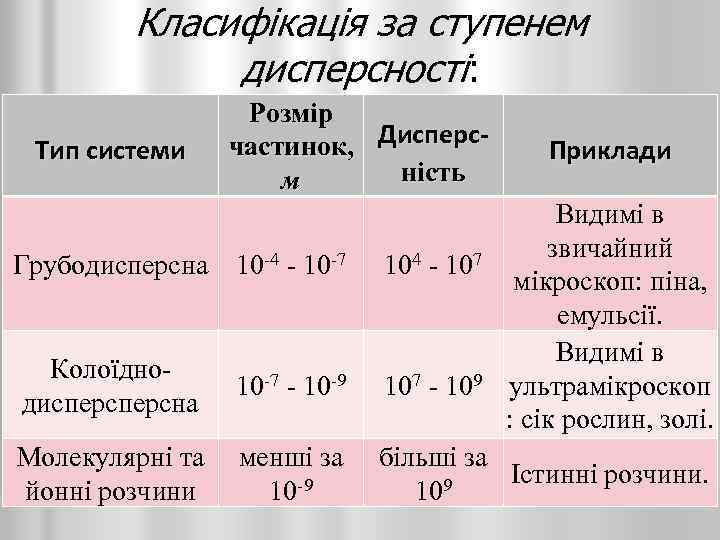 Класифікація за ступенем дисперсності: Тип системи Розмір частинок, Дисперсність м Грубодисперсна 10 -4 - 10 -7 104 - 107 Приклади Видимі в звичайний мікроскоп: піна, емульсії. Видимі в ультрамікроскоп : сік рослин, золі. Колоїднодисперсна 10 -7 - 10 -9 107 - 109 Молекулярні та йонні розчини менші за 10 -9 більші за Істинні розчини. 9 10
Класифікація за ступенем дисперсності: Тип системи Розмір частинок, Дисперсність м Грубодисперсна 10 -4 - 10 -7 104 - 107 Приклади Видимі в звичайний мікроскоп: піна, емульсії. Видимі в ультрамікроскоп : сік рослин, золі. Колоїднодисперсна 10 -7 - 10 -9 107 - 109 Молекулярні та йонні розчини менші за 10 -9 більші за Істинні розчини. 9 10
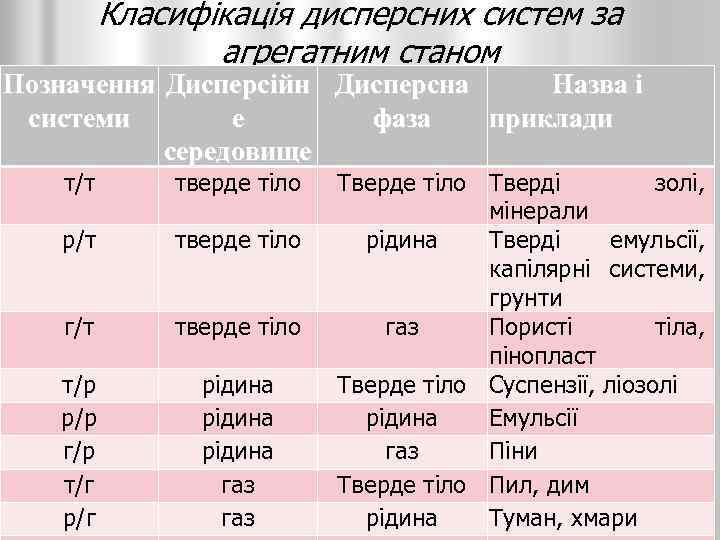 Класифікація дисперсних систем за агрегатним станом Позначення Дисперсійн Дисперсна Назва і системи е фаза приклади середовище т/т тверде тіло р/т тверде тіло г/т тверде тіло т/р р/р г/р т/г рідина газ Тверде тіло Тверді золі, мінерали рідина Тверді емульсії, капілярні системи, грунти газ Пористі тіла, пінопласт Тверде тіло Суспензії, ліозолі рідина Емульсії газ Піни Тверде тіло Пил, дим рідина Туман, хмари
Класифікація дисперсних систем за агрегатним станом Позначення Дисперсійн Дисперсна Назва і системи е фаза приклади середовище т/т тверде тіло р/т тверде тіло г/т тверде тіло т/р р/р г/р т/г рідина газ Тверде тіло Тверді золі, мінерали рідина Тверді емульсії, капілярні системи, грунти газ Пористі тіла, пінопласт Тверде тіло Суспензії, ліозолі рідина Емульсії газ Піни Тверде тіло Пил, дим рідина Туман, хмари
 l Системи поділяються на: ліофільні(гідрофільні) ліофобні (гідрофобні). l Ліофільні - взаємодія частинок дисперсної фази із середовищем досить сильна. l Ліофобні - взаємодія фази із середовищем слабка. l Одержання колоїдних систем передбачає виконання двох операцій: l а) довести розміри колоїдних частинокк до величини 1 - 100 нм; l б) стабілізувати ці частинки в дисперсному середовищі.
l Системи поділяються на: ліофільні(гідрофільні) ліофобні (гідрофобні). l Ліофільні - взаємодія частинок дисперсної фази із середовищем досить сильна. l Ліофобні - взаємодія фази із середовищем слабка. l Одержання колоїдних систем передбачає виконання двох операцій: l а) довести розміри колоїдних частинокк до величини 1 - 100 нм; l б) стабілізувати ці частинки в дисперсному середовищі.
 Дисперсійні методи l Механічні методи (колоїдні млини). l Ультразвуковий метод. l Метод пептизації. l Метод розчинення (для полімерів). l Метод заміни розчинника. l Електричний метод.
Дисперсійні методи l Механічні методи (колоїдні млини). l Ультразвуковий метод. l Метод пептизації. l Метод розчинення (для полімерів). l Метод заміни розчинника. l Електричний метод.
 Конденсаційні методи – хімічні реакції: 1. Метод окиснення. l 2 H 2 S + SO 2 2 Н 2 О + 3 S↓ 2. Метод відновлення. l [Ag(NH 3)2]2 O + CH 2 O 2 Ag↓ + H 2 O + CO 2 + 2 NH 3↑ 3. Метод гідролізу. l Fe. Cl 3 + H 2 O HCl + Fe(OH)CI 2 l Fe(OH)CI 2 + Н 2 О Fe(OH)2 CI + НСІ l Fe(OH)2 CI = Fe(OH)3 + Н 2 О l Fe(OH)2 CI = Fe. OCI + Н 2 О l Fe. OCI = Fe. O+ + СІl при стабілізаторі колоїдних частинок Fe. O+ l {[(m. Fe(OH)3) n. Fe. О+]n+ (n-x)Cl-}x+ x. Cl-.
Конденсаційні методи – хімічні реакції: 1. Метод окиснення. l 2 H 2 S + SO 2 2 Н 2 О + 3 S↓ 2. Метод відновлення. l [Ag(NH 3)2]2 O + CH 2 O 2 Ag↓ + H 2 O + CO 2 + 2 NH 3↑ 3. Метод гідролізу. l Fe. Cl 3 + H 2 O HCl + Fe(OH)CI 2 l Fe(OH)CI 2 + Н 2 О Fe(OH)2 CI + НСІ l Fe(OH)2 CI = Fe(OH)3 + Н 2 О l Fe(OH)2 CI = Fe. OCI + Н 2 О l Fe. OCI = Fe. O+ + СІl при стабілізаторі колоїдних частинок Fe. O+ l {[(m. Fe(OH)3) n. Fe. О+]n+ (n-x)Cl-}x+ x. Cl-.
 4. Метод подвійного обміну : l Ag. NO 3 + КJ → Ag. J↓ + KNO 3 l Будова міцели Ag. J в надлишку нітрату срібла l Ag. J m: - агрегат l Ag. J m n Ag+ - ядро l Ag. J m n Ag+ n-x NO 3 - x+ - гранула l адсорбційний шар l Ag. J m n Ag+ n-x NO 3 - x+ x. NO 3 - -
4. Метод подвійного обміну : l Ag. NO 3 + КJ → Ag. J↓ + KNO 3 l Будова міцели Ag. J в надлишку нітрату срібла l Ag. J m: - агрегат l Ag. J m n Ag+ - ядро l Ag. J m n Ag+ n-x NO 3 - x+ - гранула l адсорбційний шар l Ag. J m n Ag+ n-x NO 3 - x+ x. NO 3 - -
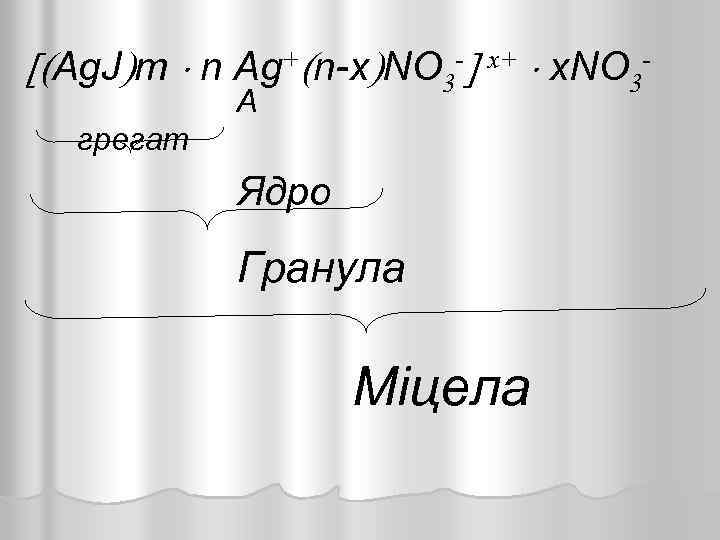 Ag. J m n Ag+ n-x NO 3 - x+ x. NO 3 А грегат Ядро Гранула Міцела
Ag. J m n Ag+ n-x NO 3 - x+ x. NO 3 А грегат Ядро Гранула Міцела
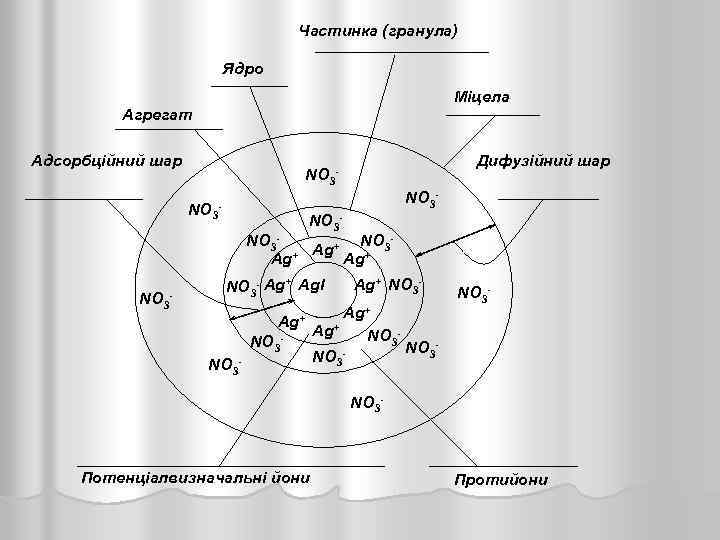 Частинка (гранула) Ядро Міцела Агрегат Адсорбційний шар NO 3 Дифузійний шар - NO 3 - NO 3 Ag+ Ag+ NO 3 - NO 3 - Ag+ Ag. I Ag+ NO 3 - Ag+ NO 3 NO 3 - Потенціалвизначальні йони Протийони
Частинка (гранула) Ядро Міцела Агрегат Адсорбційний шар NO 3 Дифузійний шар - NO 3 - NO 3 Ag+ Ag+ NO 3 - NO 3 - Ag+ Ag. I Ag+ NO 3 - Ag+ NO 3 NO 3 - Потенціалвизначальні йони Протийони
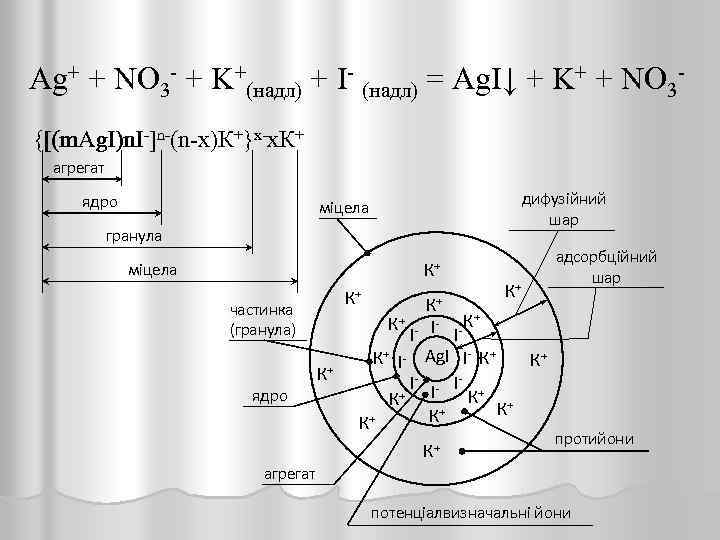 Ag+ + NO 3 - + K+(надл) + I- (надл) = Ag. I↓ + K+ + NO 3{[(m. Аg. I)nІ-]n-(n-х)К+}х-х. К+ [(m. Аg. I)nІ (m. Аg. I) агрегат ядро дифузійний шар міцела гранула К+ міцела К+ частинка (гранула) ядро К+ К+ - І- - К+ І І К+ І- Ag. I І- К+ К+ І- І- І- + К К+ К+ + К К+ адсорбційний шар протийони агрегат потенціалвизначальні йони
Ag+ + NO 3 - + K+(надл) + I- (надл) = Ag. I↓ + K+ + NO 3{[(m. Аg. I)nІ-]n-(n-х)К+}х-х. К+ [(m. Аg. I)nІ (m. Аg. I) агрегат ядро дифузійний шар міцела гранула К+ міцела К+ частинка (гранула) ядро К+ К+ - І- - К+ І І К+ І- Ag. I І- К+ К+ І- І- І- + К К+ К+ + К К+ адсорбційний шар протийони агрегат потенціалвизначальні йони
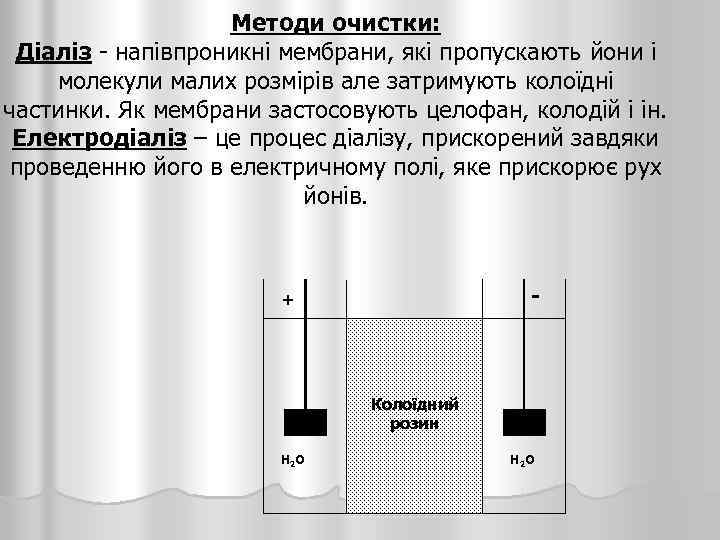 Методи очистки: Діаліз - напівпроникні мембрани, які пропускають йони і молекули малих розмірів але затримують колоїдні частинки. Як мембрани застосовують целофан, колодій і ін. Електродіаліз – це процес діалізу, прискорений завдяки проведенню його в електричному полі, яке прискорює рух йонів. - + Колоїдний розин Н 2 О
Методи очистки: Діаліз - напівпроникні мембрани, які пропускають йони і молекули малих розмірів але затримують колоїдні частинки. Як мембрани застосовують целофан, колодій і ін. Електродіаліз – це процес діалізу, прискорений завдяки проведенню його в електричному полі, яке прискорює рух йонів. - + Колоїдний розин Н 2 О
 Компенсаційний діаліз - діалізатор обмивається не чистим розчинником, а розчином із певною концентрацією вівідіаліз - перерізану кров’яну судину приєднують до трубок із напівпрониклого матеріалу і занурюють в посудину з фізіологічним розчином
Компенсаційний діаліз - діалізатор обмивається не чистим розчинником, а розчином із певною концентрацією вівідіаліз - перерізану кров’яну судину приєднують до трубок із напівпрониклого матеріалу і занурюють в посудину з фізіологічним розчином
 l Молекулярно-кінетичні властивості колоїдних систем як і для істинних характерні дифузія і осмотичний тиск. l Осмотичний тиск ультрамікрогетерогенних дисперсних систем можна визначити за рівнянням: l , l де mд. ф. – маса дисперсної фази, m 0 – маса однієї частинки, V – об'єм системи, v – частинкова концентрація, кількість частинок в одиниці об’єму, l k – константа Больцмана. l l
l Молекулярно-кінетичні властивості колоїдних систем як і для істинних характерні дифузія і осмотичний тиск. l Осмотичний тиск ультрамікрогетерогенних дисперсних систем можна визначити за рівнянням: l , l де mд. ф. – маса дисперсної фази, m 0 – маса однієї частинки, V – об'єм системи, v – частинкова концентрація, кількість частинок в одиниці об’єму, l k – константа Больцмана. l l
 Осмотичний тиск ліозолів має мале значення і несталість. Мале значення зумовлене низькою частинковою концентрацією розчинів. несталість пов'язана із спонтанною зміною розмірів. осмотичний тиск ліозолів маскується або спотворюється присутніми електролітами. Броунівський рух – це хаотичний рух частинок у мікрогетерогенних системах. Седиментація – процес осідання колоїдних частинок під дією сил земного тяжіння. седиментаційний аналіз.
Осмотичний тиск ліозолів має мале значення і несталість. Мале значення зумовлене низькою частинковою концентрацією розчинів. несталість пов'язана із спонтанною зміною розмірів. осмотичний тиск ліозолів маскується або спотворюється присутніми електролітами. Броунівський рух – це хаотичний рух частинок у мікрогетерогенних системах. Седиментація – процес осідання колоїдних частинок під дією сил земного тяжіння. седиментаційний аналіз.
 l Оптичні властивості колоїдних систем. l здатність розсіювання світла - явище Тіндаля. l закон Релея, згідно якого інтенсивність розсіяного світла (І) прямо пропорційне числу частинок (n), квадрату об’єму частинок (V 2) і обернено пропорційне четвертій степені від довжини хвилі (λ 4) падаючого світла:
l Оптичні властивості колоїдних систем. l здатність розсіювання світла - явище Тіндаля. l закон Релея, згідно якого інтенсивність розсіяного світла (І) прямо пропорційне числу частинок (n), квадрату об’єму частинок (V 2) і обернено пропорційне четвертій степені від довжини хвилі (λ 4) падаючого світла:
 l К – константа, що залежить від показника заломлення дисперсного середовища. l Рівняння Релея лежить в основі оптичних методів визначення розмірів частинок і концентрації дисперсної фази ультрамікрогетерогенних систем: ультрамікроскопії, нефелометрії і турбідиметрії.
l К – константа, що залежить від показника заломлення дисперсного середовища. l Рівняння Релея лежить в основі оптичних методів визначення розмірів частинок і концентрації дисперсної фази ультрамікрогетерогенних систем: ультрамікроскопії, нефелометрії і турбідиметрії.
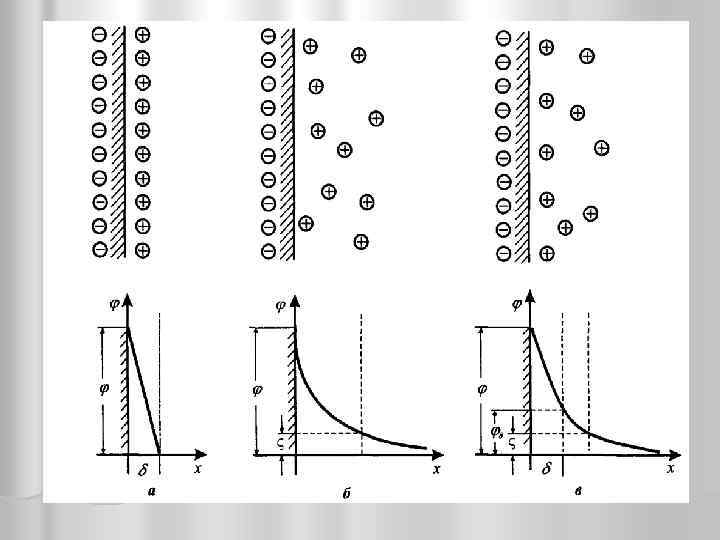
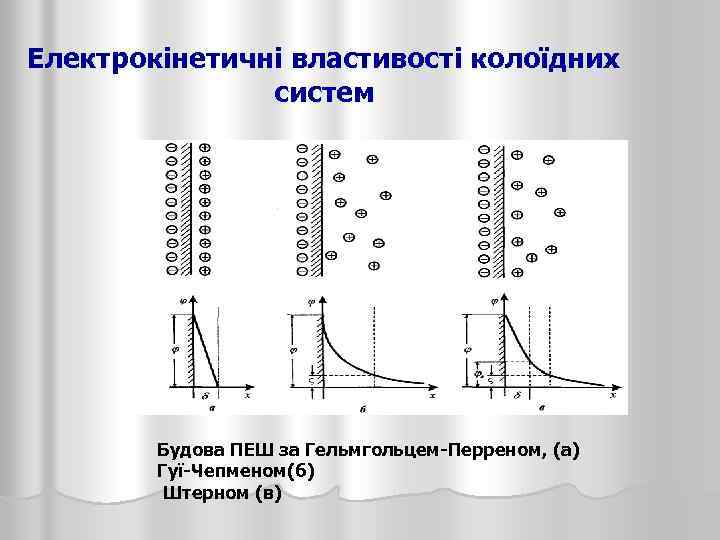 Електрокінетичні властивості колоїдних систем Будова ПЕШ за Гельмгольцем-Перреном, (а) Гуї-Чепменом(б) Штерном (в)
Електрокінетичні властивості колоїдних систем Будова ПЕШ за Гельмгольцем-Перреном, (а) Гуї-Чепменом(б) Штерном (в)
 l Стійкість дисперсної системи – це здатність зберігати склад і основні властивості системи. l Кінетична стійкість – збереження рівномірного розподілу частинок у всьому об’ємі системи (протидія силам тяжіння). l Агрегативна стійкість – це здатність протидіяти злипанню. l На стійкість впливає: l різка зміна температури l інтенсивне струшування l перемішування, центрифугування
l Стійкість дисперсної системи – це здатність зберігати склад і основні властивості системи. l Кінетична стійкість – збереження рівномірного розподілу частинок у всьому об’ємі системи (протидія силам тяжіння). l Агрегативна стійкість – це здатність протидіяти злипанню. l На стійкість впливає: l різка зміна температури l інтенсивне струшування l перемішування, центрифугування
 l Коагуляція – процес зменшення дисперсності системи за рахунок укрупнення. l Поріг коагуляції (Спор) або критична концентрація (Ск) - мінімальна концентрація, яка здатна спричинити коагуляцію 1 л золю. l Мінімальне значення ζ-потенціалу, за якого золь стійкий, називають критичним (ζ = 30 м. В).
l Коагуляція – процес зменшення дисперсності системи за рахунок укрупнення. l Поріг коагуляції (Спор) або критична концентрація (Ск) - мінімальна концентрація, яка здатна спричинити коагуляцію 1 л золю. l Мінімальне значення ζ-потенціалу, за якого золь стійкий, називають критичним (ζ = 30 м. В).
 l помітною швидкість коагуляції відбувається лише за певної кількості введеного електроліту. Мінімальну концентрацію електроліту в ммоль, яка здатна спричинити коагуляцію 1 л золю, називають порогом коагуляції (Спор) або критичною концентрацією (Ск). l Початок явної коагуляції визначають за ознаками: зміною забарвлення системи, виникненням каламуті.
l помітною швидкість коагуляції відбувається лише за певної кількості введеного електроліту. Мінімальну концентрацію електроліту в ммоль, яка здатна спричинити коагуляцію 1 л золю, називають порогом коагуляції (Спор) або критичною концентрацією (Ск). l Початок явної коагуляції визначають за ознаками: зміною забарвлення системи, виникненням каламуті.
 l. Поріг коагуляції обчислюють за формулою: l , де Vел – об'єм електроліту (мл), що спричинив коагуляцію; Сел – концентрація електроліту, ммоль/л; Vзолю – об'єм золю, мл. l Величину, обернену до порогу коагуляції, називають коагулюючою здатністю (Vк): Vк=1C
l. Поріг коагуляції обчислюють за формулою: l , де Vел – об'єм електроліту (мл), що спричинив коагуляцію; Сел – концентрація електроліту, ммоль/л; Vзолю – об'єм золю, мл. l Величину, обернену до порогу коагуляції, називають коагулюючою здатністю (Vк): Vк=1C
 l Коагулююча здатність – це об'єм золю, для коагуляції якого потрібно 1 ммоль електроліту l Правила коагуляції l 1 правило Гарді l Коагулюючу дію виявляє не вся молекула електроліту, а лише той його йон, знак якого протилежний до заряду гранули. Ці йони електроліту називають коагулюючими або йонами- коагуляторами
l Коагулююча здатність – це об'єм золю, для коагуляції якого потрібно 1 ммоль електроліту l Правила коагуляції l 1 правило Гарді l Коагулюючу дію виявляє не вся молекула електроліту, а лише той його йон, знак якого протилежний до заряду гранули. Ці йони електроліту називають коагулюючими або йонами- коагуляторами
 2 правило Шульце коагулююча здатність йона тим більша, чим більший його заряд. Тому найменший поріг коагуляції будуть мати електроліти, що містять багатозарядний йонкоагулятор. Спор(K+) > Спор(Ca 2+) > Спор(Al 3+) Поріг коагуляції (Спор) є оберненим до заряду йона (z) в шостому степені: . Тому значення порогів коагуляції для одно-, дво- і тризарядних йонів відносяться як: . 2
2 правило Шульце коагулююча здатність йона тим більша, чим більший його заряд. Тому найменший поріг коагуляції будуть мати електроліти, що містять багатозарядний йонкоагулятор. Спор(K+) > Спор(Ca 2+) > Спор(Al 3+) Поріг коагуляції (Спор) є оберненим до заряду йона (z) в шостому степені: . Тому значення порогів коагуляції для одно-, дво- і тризарядних йонів відносяться як: . 2
 Грубодисперсні системи Аерозолі т/г d>10 -5 м-пил d=10 -9 - 10 -5 м-дим р/г d близько 10 -5 м-туман У медицині застосовуються у вигляді аерозолів, спреїв, інгаляцій для лікування захворювань легень, бронхів, носа, горла.
Грубодисперсні системи Аерозолі т/г d>10 -5 м-пил d=10 -9 - 10 -5 м-дим р/г d близько 10 -5 м-туман У медицині застосовуються у вигляді аерозолів, спреїв, інгаляцій для лікування захворювань легень, бронхів, носа, горла.
 Суспензії т/р d=10 -6 - 10 -4 м Стабілізаторами суспензій виступають ліофільні полімери, електроліти, ПАР. Пасти - висококонцентровані суспензії.
Суспензії т/р d=10 -6 - 10 -4 м Стабілізаторами суспензій виступають ліофільні полімери, електроліти, ПАР. Пасти - висококонцентровані суспензії.
 Колоїдні ПАР Поділяються на: 1) за розчинністю: гідрофільні, олеофільні. 2)За здатністю до іонізації: іоногенні, неіоногенні. Іоногенні аніоноактивні амфоліти катіоноактивні
Колоїдні ПАР Поділяються на: 1) за розчинністю: гідрофільні, олеофільні. 2)За здатністю до іонізації: іоногенні, неіоногенні. Іоногенні аніоноактивні амфоліти катіоноактивні
 Колоїдні ПАР Аніоноактивні ПАР: мило, олеат натрію, алкілсульфати, жовчні кислоти С 17 Н 35 СООNa С 17 Н 35 СОО- +Na+ Катіоноактивні: солі амінів, четвертинні азотисті основи, алкілпірідинієві солі [R-N+ (CH 3)3]Cl[R-N+ (CH 3)3]+ + Cl. Неіоногенні: не дисоціюють R(OCH 2 – CH 2)n-OH
Колоїдні ПАР Аніоноактивні ПАР: мило, олеат натрію, алкілсульфати, жовчні кислоти С 17 Н 35 СООNa С 17 Н 35 СОО- +Na+ Катіоноактивні: солі амінів, четвертинні азотисті основи, алкілпірідинієві солі [R-N+ (CH 3)3]Cl[R-N+ (CH 3)3]+ + Cl. Неіоногенні: не дисоціюють R(OCH 2 – CH 2)n-OH
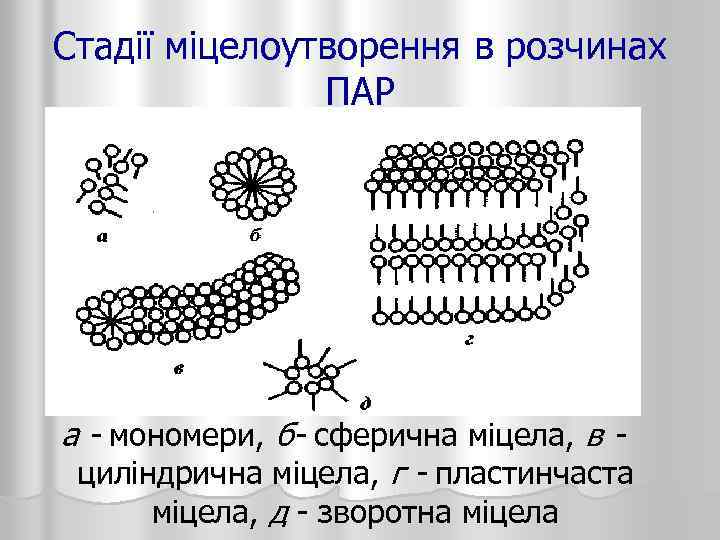 Стадії міцелоутворення в розчинах ПАР а - мономери, б- сферична міцела, в - циліндрична міцела, г - пластинчаста міцела, д - зворотна міцела
Стадії міцелоутворення в розчинах ПАР а - мономери, б- сферична міцела, в - циліндрична міцела, г - пластинчаста міцела, д - зворотна міцела

 Солюбілізація –процес переходу нерозчинних у чистих рідинах сполук у колоїдний стан в присутності ПАР Солюбілізована система Солюбілізат ПАР Солюбілізатор(речовина що розчиняється)
Солюбілізація –процес переходу нерозчинних у чистих рідинах сполук у колоїдний стан в присутності ПАР Солюбілізована система Солюбілізат ПАР Солюбілізатор(речовина що розчиняється)
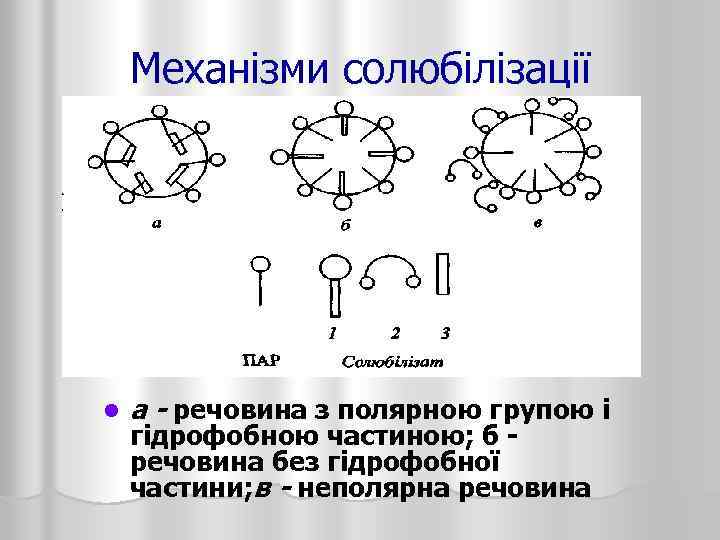 Механізми солюбілізації l а - речовина з полярною групою і гідрофобною частиною; б речовина без гідрофобної частини; в - неполярна речовина
Механізми солюбілізації l а - речовина з полярною групою і гідрофобною частиною; б речовина без гідрофобної частини; в - неполярна речовина

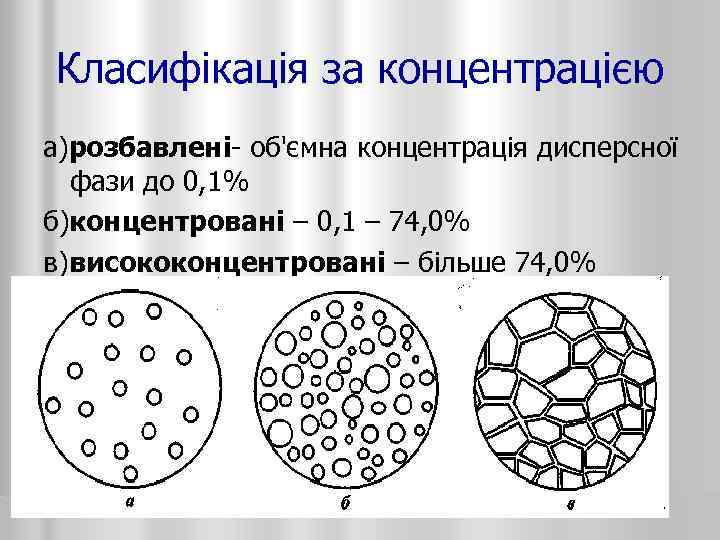 Класифікація за концентрацією а)розбавлені- об'ємна концентрація дисперсної фази до 0, 1% б)концентровані – 0, 1 – 74, 0% в)висококонцентровані – більше 74, 0%
Класифікація за концентрацією а)розбавлені- об'ємна концентрація дисперсної фази до 0, 1% б)концентровані – 0, 1 – 74, 0% в)висококонцентровані – більше 74, 0%