 Лекция № 4 Химическая термодинамика
Лекция № 4 Химическая термодинамика
 Лекция № 5 Химическая кинетика и равновесие
Лекция № 5 Химическая кинетика и равновесие
 Порядок реакции Показатель степени при концентрации каждого из реагирующих веществ в кинетическом уравнении химической реакции есть частный порядок реакции по данному компоненту. Сумма показателей степени в кинетическом уравнении химической реакции представляет собой общий порядок реакции. Порядок реакции определяется экспериментально.
Порядок реакции Показатель степени при концентрации каждого из реагирующих веществ в кинетическом уравнении химической реакции есть частный порядок реакции по данному компоненту. Сумма показателей степени в кинетическом уравнении химической реакции представляет собой общий порядок реакции. Порядок реакции определяется экспериментально.
 Молекулярность реакций • Молекулярность элементарной реакции – число частиц, которые, согласно экспериментально установленному механизму реакции, участвуют в элементарном акте химического взаимодействия.
Молекулярность реакций • Молекулярность элементарной реакции – число частиц, которые, согласно экспериментально установленному механизму реакции, участвуют в элементарном акте химического взаимодействия.
 Мономолекулярные – реакции, в которых происходит химическое превращение одной молекулы (изомеризация, диссоциация и т. д. ): I 2 ––> I • + I •
Мономолекулярные – реакции, в которых происходит химическое превращение одной молекулы (изомеризация, диссоциация и т. д. ): I 2 ––> I • + I •
 Бимолекулярные – реакции, элементарный акт которых осуществляется при столкновении двух частиц (одинаковых или различных): СН 3 Вr + КОН ––> СН 3 ОН + КВr
Бимолекулярные – реакции, элементарный акт которых осуществляется при столкновении двух частиц (одинаковых или различных): СН 3 Вr + КОН ––> СН 3 ОН + КВr
 Тримолекулярные – реакции, элементарный акт которых осуществляется при столкновении трех частиц: О 2 + NО ––> 2 NО 2 Реакции с молекулярностью более трёх неизвестны.
Тримолекулярные – реакции, элементарный акт которых осуществляется при столкновении трех частиц: О 2 + NО ––> 2 NО 2 Реакции с молекулярностью более трёх неизвестны.
 Сложные реакции химические реакции, протекающие более чем в одну стадию. 2 НI + Н 2 О 2 ––> I 2 + 2 Н 2 О 1) НI + Н 2 О 2 ––> НIО + Н 2 О (медленная) V = k [HI] [H 2 O 2] 2) НIО + НI ––> I 2 + Н 2 О (быстрая)
Сложные реакции химические реакции, протекающие более чем в одну стадию. 2 НI + Н 2 О 2 ––> I 2 + 2 Н 2 О 1) НI + Н 2 О 2 ––> НIО + Н 2 О (медленная) V = k [HI] [H 2 O 2] 2) НIО + НI ––> I 2 + Н 2 О (быстрая)
 Сложные реакции Последовательные реакции А ––> В ––> С ––>. . . Параллельные реакции (одни и те же исходные вещества одновременно могут образовывать различные продукты реакции) Сопряжённые реакции 1) А + В ––> С 2) А + D ––> Е
Сложные реакции Последовательные реакции А ––> В ––> С ––>. . . Параллельные реакции (одни и те же исходные вещества одновременно могут образовывать различные продукты реакции) Сопряжённые реакции 1) А + В ––> С 2) А + D ––> Е
 Неразветвлённые цепные реакции Н 2 + Cl 2 = 2 HCl 1. Зарождение цепи (инициация): Сl 2 + hν ––> 2 Сl • 2. Развитие цепи: Н 2 + Сl • ––> НСl + Н • + Сl 2 ––> НСl + Сl • 3. Обрыв цепи: Н • + Н • ––> Н 2 Сl • + Сl • ––> Сl 2 Н • + Сl • ––> НСl
Неразветвлённые цепные реакции Н 2 + Cl 2 = 2 HCl 1. Зарождение цепи (инициация): Сl 2 + hν ––> 2 Сl • 2. Развитие цепи: Н 2 + Сl • ––> НСl + Н • + Сl 2 ––> НСl + Сl • 3. Обрыв цепи: Н • + Н • ––> Н 2 Сl • + Сl • ––> Сl 2 Н • + Сl • ––> НСl
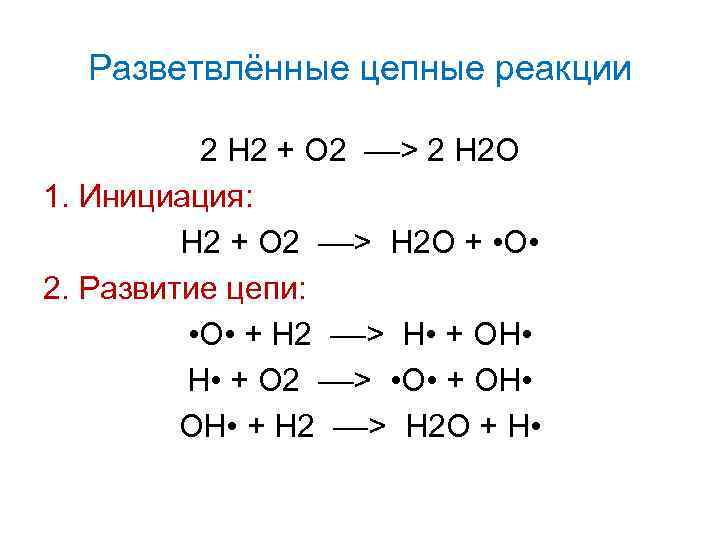 Разветвлённые цепные реакции 2 Н 2 + О 2 ––> 2 Н 2 О 1. Инициация: Н 2 + О 2 ––> Н 2 О + • О • 2. Развитие цепи: • О • + Н 2 ––> Н • + ОН • + О 2 ––> • О • + ОН • + Н 2 ––> Н 2 О + Н •
Разветвлённые цепные реакции 2 Н 2 + О 2 ––> 2 Н 2 О 1. Инициация: Н 2 + О 2 ––> Н 2 О + • О • 2. Развитие цепи: • О • + Н 2 ––> Н • + ОН • + О 2 ––> • О • + ОН • + Н 2 ––> Н 2 О + Н •