Lektsia__4_2011.ppt
- Количество слайдов: 22
 Лекция № 4 Химическая связь и строение молекул Метод молекулярных орбиталей (продолжение)
Лекция № 4 Химическая связь и строение молекул Метод молекулярных орбиталей (продолжение)
 • Каждый электрон находится в поле всех ядер. • При этом связь не обязательно образована парой электронов. Например: ион Н 2+ состоит из двух протонов и одного электрона. • Для молекулы H 2 1) c. A 2 + c. B 2 = 1; c. A = c. B = 1 Ψ+ = ϕA + ϕB - связывающая МО 2) c. A 2 + c. B 2 = 1; c. A = 1; c. B = – 1 Ψ - = ϕA – ϕB - разрыхляющая МО
• Каждый электрон находится в поле всех ядер. • При этом связь не обязательно образована парой электронов. Например: ион Н 2+ состоит из двух протонов и одного электрона. • Для молекулы H 2 1) c. A 2 + c. B 2 = 1; c. A = c. B = 1 Ψ+ = ϕA + ϕB - связывающая МО 2) c. A 2 + c. B 2 = 1; c. A = 1; c. B = – 1 Ψ - = ϕA – ϕB - разрыхляющая МО
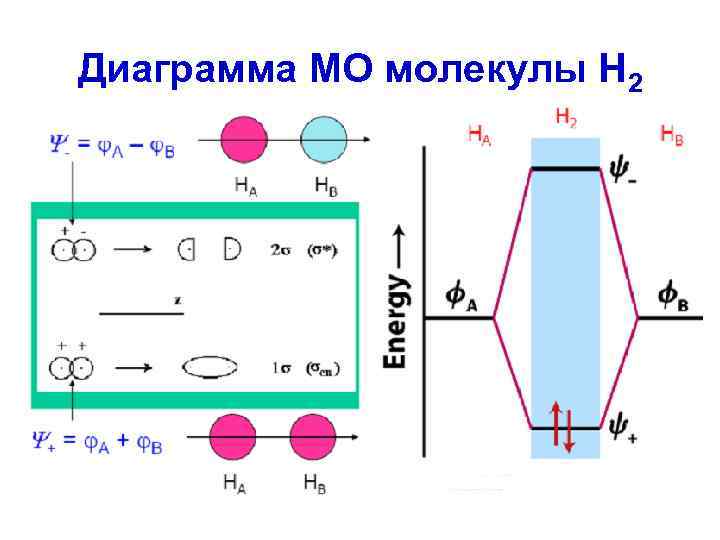 Диаграмма МО молекулы Н 2
Диаграмма МО молекулы Н 2
 Порядок связи: ω = [N 1(число e− на МО св) − N 2(число e− на МО раз)] / 2
Порядок связи: ω = [N 1(число e− на МО св) − N 2(число e− на МО раз)] / 2
 Сравнительная характеристика ММО и МВС 1. Оба подхода к описанию химической связи – ММО и МВС – приближенны, ММО придает преувеличенное значение делокализации электрона в молекуле и основывается на одноэлектронных волновых функциях – молекулярных орбиталях. 2. МВС преувеличивает роль локализации электронной плотности и основывается на том, что элементарная связь осуществляется только парой электронов между двумя атомами.
Сравнительная характеристика ММО и МВС 1. Оба подхода к описанию химической связи – ММО и МВС – приближенны, ММО придает преувеличенное значение делокализации электрона в молекуле и основывается на одноэлектронных волновых функциях – молекулярных орбиталях. 2. МВС преувеличивает роль локализации электронной плотности и основывается на том, что элементарная связь осуществляется только парой электронов между двумя атомами.
 3. Достоинством МВС является его наглядность: насыщаемость связи объясняется как максимальная ковалентность, направленность вытекает из направленности атомных и гибридных орбиталей; дипольный момент молекулы складывается из дипольных моментов связей, разности ОЭО атомов, образующих молекулу, и наличия неподеленных электронных пар. 4. Существование некоторых соединений невозможно объяснить с позиций МВС.
3. Достоинством МВС является его наглядность: насыщаемость связи объясняется как максимальная ковалентность, направленность вытекает из направленности атомных и гибридных орбиталей; дипольный момент молекулы складывается из дипольных моментов связей, разности ОЭО атомов, образующих молекулу, и наличия неподеленных электронных пар. 4. Существование некоторых соединений невозможно объяснить с позиций МВС.
 5. Устойчивость молекулярных ионов и атомов в сравнении с молекулами легко предсказывается с позиции ММО. Магнетизм и окраска вещества также легко объясняются ММО. 6. Количественные расчеты в ММО проще, чем в МВС. 7. В то же время качественно выводы МВС гораздо нагляднее.
5. Устойчивость молекулярных ионов и атомов в сравнении с молекулами легко предсказывается с позиции ММО. Магнетизм и окраска вещества также легко объясняются ММО. 6. Количественные расчеты в ММО проще, чем в МВС. 7. В то же время качественно выводы МВС гораздо нагляднее.
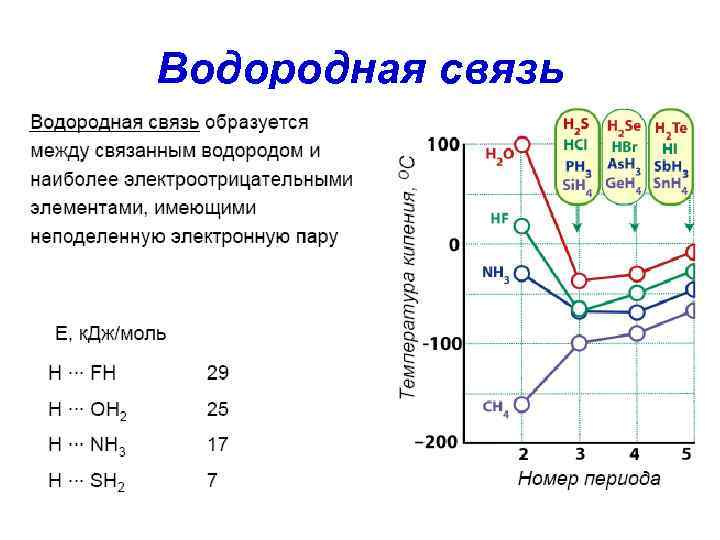 Водородная связь
Водородная связь
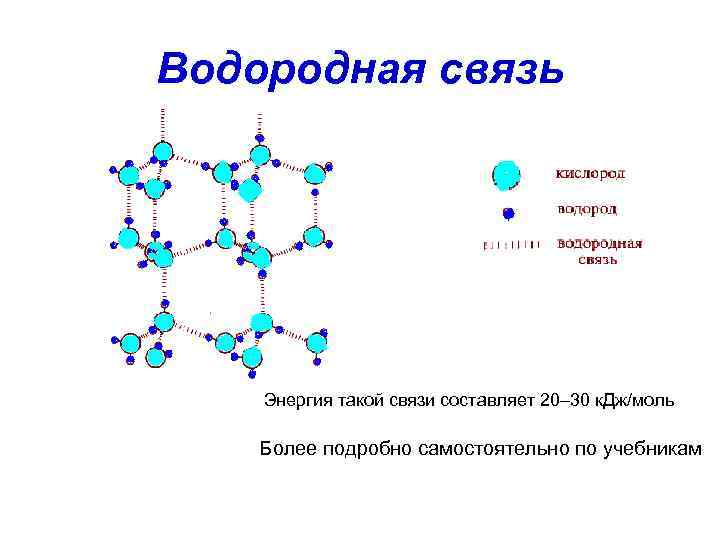 Водородная связь Энергия такой связи составляет 20– 30 к. Дж/моль Более подробно самостоятельно по учебникам
Водородная связь Энергия такой связи составляет 20– 30 к. Дж/моль Более подробно самостоятельно по учебникам
 Ван-дер-ваальсовы силы Силы Ван-дер-Ваальса включают все виды межмолекулярного притяжения и отталкивания. Три типа Ван-дер-Ваальсовых сил: • • • Диполь-дипольное притяжение - взаимодействие постоянных диполей Индукционное притяжение - взаимодействие постоянного и наведенного диполей Дисперсионное притяжение - взаимодействие мгновенных диполей
Ван-дер-ваальсовы силы Силы Ван-дер-Ваальса включают все виды межмолекулярного притяжения и отталкивания. Три типа Ван-дер-Ваальсовых сил: • • • Диполь-дипольное притяжение - взаимодействие постоянных диполей Индукционное притяжение - взаимодействие постоянного и наведенного диполей Дисперсионное притяжение - взаимодействие мгновенных диполей
 • Уравнение Леннарда-Джонсона: EM = − a / r 6 + b / r 12 Диполь-дипольное притяжение Индукционное притяжение Дисперсионное притяжение
• Уравнение Леннарда-Джонсона: EM = − a / r 6 + b / r 12 Диполь-дипольное притяжение Индукционное притяжение Дисперсионное притяжение
 Химическая связь и типы кристаллов. Связь в металлах, полупроводниках и диэлектриках • Жидкое и твердое состояния веществ объединяются под общим названием конденсированное. • Tвердое агрегатное состояние: кристаллическое (истинно твердое) и аморфное. • В кристаллах реализуется дальний порядок – упорядоченность в расположении частиц, повторяющаяся на неограниченно больших расстоя-ниях. • Характерным признаком кристаллического состояния является наличие постоянной температуры плавления или кристаллизации
Химическая связь и типы кристаллов. Связь в металлах, полупроводниках и диэлектриках • Жидкое и твердое состояния веществ объединяются под общим названием конденсированное. • Tвердое агрегатное состояние: кристаллическое (истинно твердое) и аморфное. • В кристаллах реализуется дальний порядок – упорядоченность в расположении частиц, повторяющаяся на неограниченно больших расстоя-ниях. • Характерным признаком кристаллического состояния является наличие постоянной температуры плавления или кристаллизации
 • Регулярное расположение образующих кристалл частиц (атомов, ионов, молекул) может быть изображено в виде так называемой кристаллической решетки, в узлах которой располагаются центры частиц, формирующих данный кристалл. • кристаллы делятся на: ионные, ковалентные, металлические, молекулярные. • кристаллические решетки характеризуются: координационным числом, параметрами и энергией решетки
• Регулярное расположение образующих кристалл частиц (атомов, ионов, молекул) может быть изображено в виде так называемой кристаллической решетки, в узлах которой располагаются центры частиц, формирующих данный кристалл. • кристаллы делятся на: ионные, ковалентные, металлические, молекулярные. • кристаллические решетки характеризуются: координационным числом, параметрами и энергией решетки
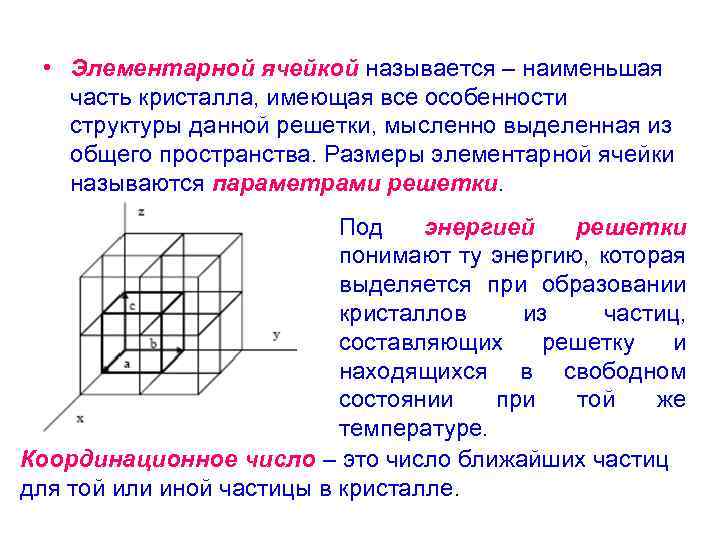 • Элементарной ячейкой называется – наименьшая часть кристалла, имеющая все особенности структуры данной решетки, мысленно выделенная из общего пространства. Размеры элементарной ячейки называются параметрами решетки. Под энергией решетки понимают ту энергию, которая выделяется при образовании кристаллов из частиц, составляющих решетку и находящихся в свободном состоянии при той же температуре. Координационное число – это число ближайших частиц для той или иной частицы в кристалле.
• Элементарной ячейкой называется – наименьшая часть кристалла, имеющая все особенности структуры данной решетки, мысленно выделенная из общего пространства. Размеры элементарной ячейки называются параметрами решетки. Под энергией решетки понимают ту энергию, которая выделяется при образовании кристаллов из частиц, составляющих решетку и находящихся в свободном состоянии при той же температуре. Координационное число – это число ближайших частиц для той или иной частицы в кристалле.
 • Ионные кристаллы – кристаллические решетки этого типа состоят из чередующихся положительно и отрицательно заряженных ионов, соединенных силами электростатического притяжения, т. е. в них реализуется ионный тип связи. Большинство ионных кристаллов – диэлектрики и некоторые сложные полупроводниковые соединения Энергия ионных кристаллов достигает больших значений (к. Дж/моль): Be. O – 4530, Na. Cl – 770
• Ионные кристаллы – кристаллические решетки этого типа состоят из чередующихся положительно и отрицательно заряженных ионов, соединенных силами электростатического притяжения, т. е. в них реализуется ионный тип связи. Большинство ионных кристаллов – диэлектрики и некоторые сложные полупроводниковые соединения Энергия ионных кристаллов достигает больших значений (к. Дж/моль): Be. O – 4530, Na. Cl – 770
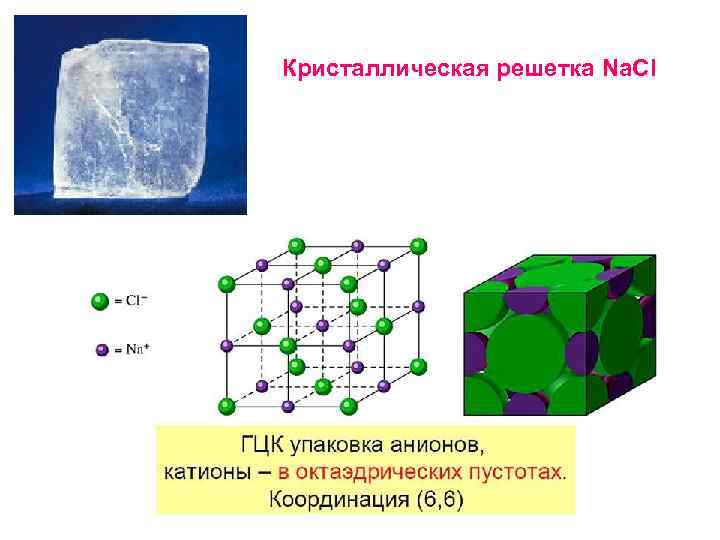 Кристаллическая решетка Na. Cl
Кристаллическая решетка Na. Cl
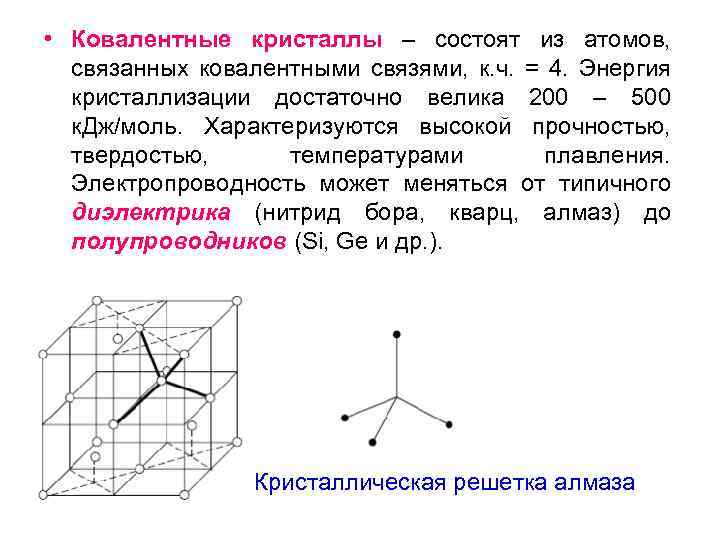 • Ковалентные кристаллы – состоят из атомов, связанных ковалентными связями, к. ч. = 4. Энергия кристаллизации достаточно велика 200 – 500 к. Дж/моль. Характеризуются высокой прочностью, твердостью, температурами плавления. Электропроводность может меняться от типичного диэлектрика (нитрид бора, кварц, алмаз) до полупроводников (Si, Ge и др. ). Кристаллическая решетка алмаза
• Ковалентные кристаллы – состоят из атомов, связанных ковалентными связями, к. ч. = 4. Энергия кристаллизации достаточно велика 200 – 500 к. Дж/моль. Характеризуются высокой прочностью, твердостью, температурами плавления. Электропроводность может меняться от типичного диэлектрика (нитрид бора, кварц, алмаз) до полупроводников (Si, Ge и др. ). Кристаллическая решетка алмаза
 • Вещества различные по химическому составу, но имеющие одинаковый структурный тип решетки, называются изоморфными, они могут совместно кристаллизовываться, образуя твердые растворы. Например: Au – Ag, Si– Ge. Металлические кристаллы – в узлах кристаллической решетки расположены ионы, в междоузлиях – свободные электроны (электронный газ). Устойчивость кристалла обеспечивается силами притяжения между положительными ионами и электронным газом (металлическая связь). Координационные числа (8 – 12), свидетельствующие о большой плотности упаковки в кристаллических решетках. Энергия решетки занимает промежуточное положение между ковалентными и молекулярными кристаллами.
• Вещества различные по химическому составу, но имеющие одинаковый структурный тип решетки, называются изоморфными, они могут совместно кристаллизовываться, образуя твердые растворы. Например: Au – Ag, Si– Ge. Металлические кристаллы – в узлах кристаллической решетки расположены ионы, в междоузлиях – свободные электроны (электронный газ). Устойчивость кристалла обеспечивается силами притяжения между положительными ионами и электронным газом (металлическая связь). Координационные числа (8 – 12), свидетельствующие о большой плотности упаковки в кристаллических решетках. Энергия решетки занимает промежуточное положение между ковалентными и молекулярными кристаллами.
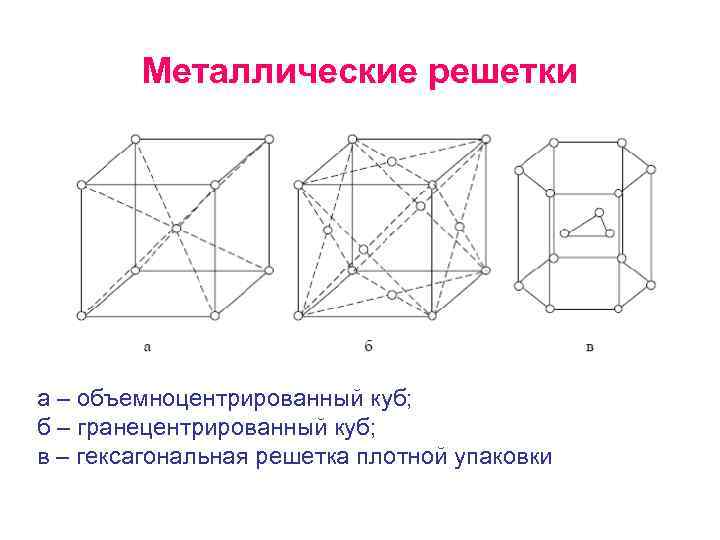 Металлические решетки а – объемноцентрированный куб; б – гранецентрированный куб; в – гексагональная решетка плотной упаковки
Металлические решетки а – объемноцентрированный куб; б – гранецентрированный куб; в – гексагональная решетка плотной упаковки
 • Молекулярные кристаллы. Структурными единицами служат молекулы, связанными друг с другом силами Ван–дер–Ваальса или силами водородной связи. Характерна низкая энергия решетки и связанная с этим малая механическая прочность, низкие температуры плавления и высокая летучесть. М. к. не проводят электрический ток и обладают низкой теплопроводностью. • для М. к. с близкими к сферическим молекулами характерна структура кубическая (Ne, Ar, Kr) или гексагональная (He, N 2) плотнейшей упаковки. Для молекул несферической формы наблюдается некоторое искажение плотнейшей упаковки, например, HCl, H 2 O.
• Молекулярные кристаллы. Структурными единицами служат молекулы, связанными друг с другом силами Ван–дер–Ваальса или силами водородной связи. Характерна низкая энергия решетки и связанная с этим малая механическая прочность, низкие температуры плавления и высокая летучесть. М. к. не проводят электрический ток и обладают низкой теплопроводностью. • для М. к. с близкими к сферическим молекулами характерна структура кубическая (Ne, Ar, Kr) или гексагональная (He, N 2) плотнейшей упаковки. Для молекул несферической формы наблюдается некоторое искажение плотнейшей упаковки, например, HCl, H 2 O.
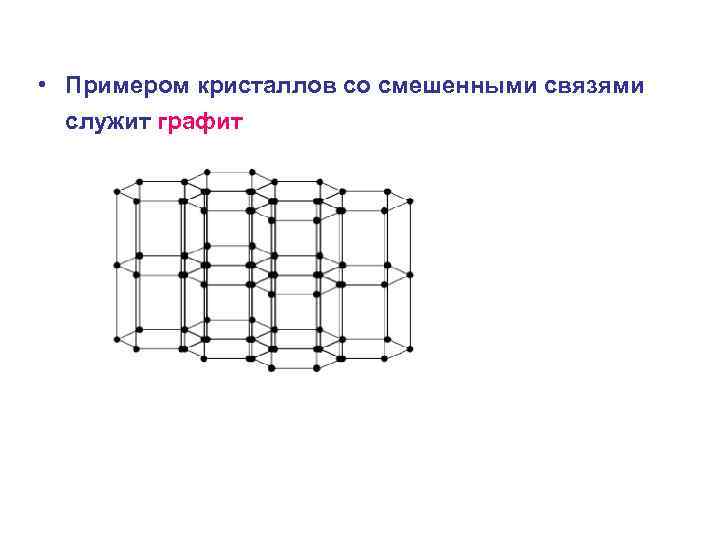 • Примером кристаллов со смешенными связями служит графит
• Примером кристаллов со смешенными связями служит графит
 Структура льда
Структура льда


