 ЛЕКЦИЯ 4 ХИМИЧЕСКАЯ КИНЕТИКА И КАТАЛИЗ
ЛЕКЦИЯ 4 ХИМИЧЕСКАЯ КИНЕТИКА И КАТАЛИЗ
 Последовательные реакции: А→В→С→D Параллельные реакции: В D А С Е KCl + 3 KCl. O 4 ← 4 KCl. O 3 → 4 KCl + 6 O 2
Последовательные реакции: А→В→С→D Параллельные реакции: В D А С Е KCl + 3 KCl. O 4 ← 4 KCl. O 3 → 4 KCl + 6 O 2
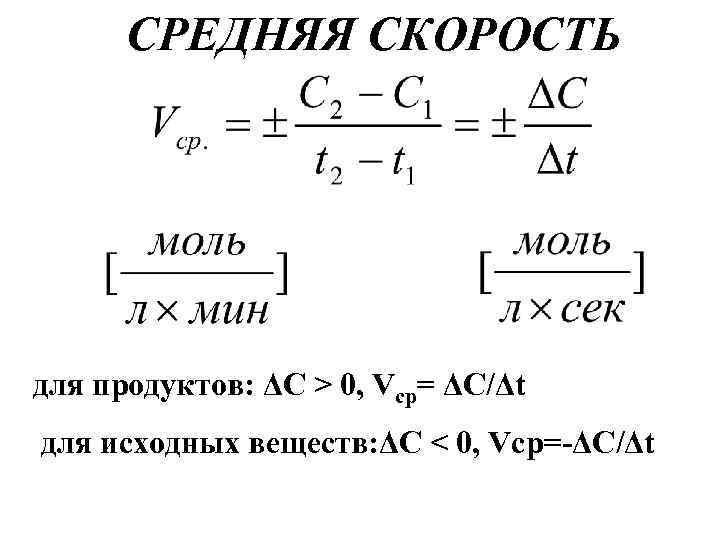 СРЕДНЯЯ СКОРОСТЬ для продуктов: ΔС > 0, Vcр= ΔС/Δt для исходных веществ: ΔС < 0, Vcр=-ΔС/Δt
СРЕДНЯЯ СКОРОСТЬ для продуктов: ΔС > 0, Vcр= ΔС/Δt для исходных веществ: ΔС < 0, Vcр=-ΔС/Δt
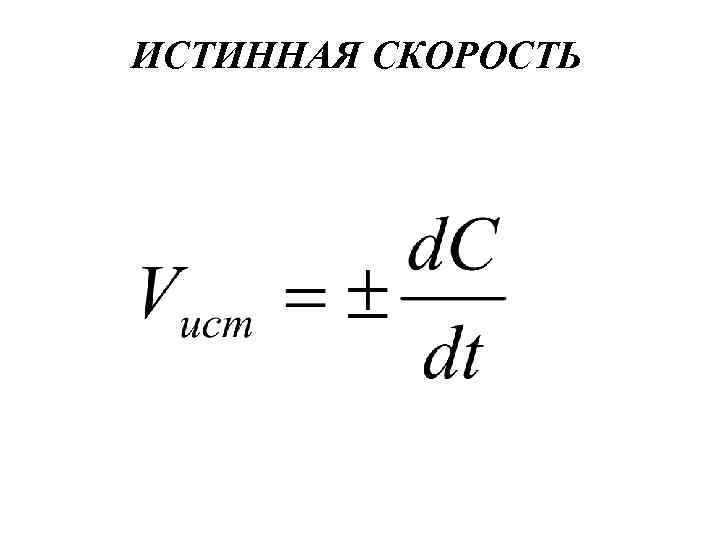 ИСТИННАЯ СКОРОСТЬ
ИСТИННАЯ СКОРОСТЬ
 ВЛИЯНИЕ КОНЦЕНТРАЦИИ НА СКОРОСТЬ РЕАКЦИИ ЗАКОН ГУЛЬДБЕРГА и ВААГЕ а. А +b. В ↔ с. С + d. D V = k×[A]a × [B]b [A] и [B] – молярные концентрации реагентов, моль/л a и b – степени концентраций, равные стехиометрическим коэффициентам, только для простых реакций
ВЛИЯНИЕ КОНЦЕНТРАЦИИ НА СКОРОСТЬ РЕАКЦИИ ЗАКОН ГУЛЬДБЕРГА и ВААГЕ а. А +b. В ↔ с. С + d. D V = k×[A]a × [B]b [A] и [B] – молярные концентрации реагентов, моль/л a и b – степени концентраций, равные стехиометрическим коэффициентам, только для простых реакций
 В СЛУЧАЕ МНОГОСТАДИЙНЫХ РЕАКЦИЙ СКОРОСТЬ ПО ЗДМ РАВНА na и nb – постоянные, не зависящие от концентрации числа, называемые показателями порядка реакций по реагентам А и В, определяются экспериментально и имеют значения от 0 до 2
В СЛУЧАЕ МНОГОСТАДИЙНЫХ РЕАКЦИЙ СКОРОСТЬ ПО ЗДМ РАВНА na и nb – постоянные, не зависящие от концентрации числа, называемые показателями порядка реакций по реагентам А и В, определяются экспериментально и имеют значения от 0 до 2
 ОБЩИЙ ПОРЯДОК РЕАКЦИИ – величина равная сумме показателей степени концентрации реагентов в кинетическом уравнении реакции n = na + nb
ОБЩИЙ ПОРЯДОК РЕАКЦИИ – величина равная сумме показателей степени концентрации реагентов в кинетическом уравнении реакции n = na + nb
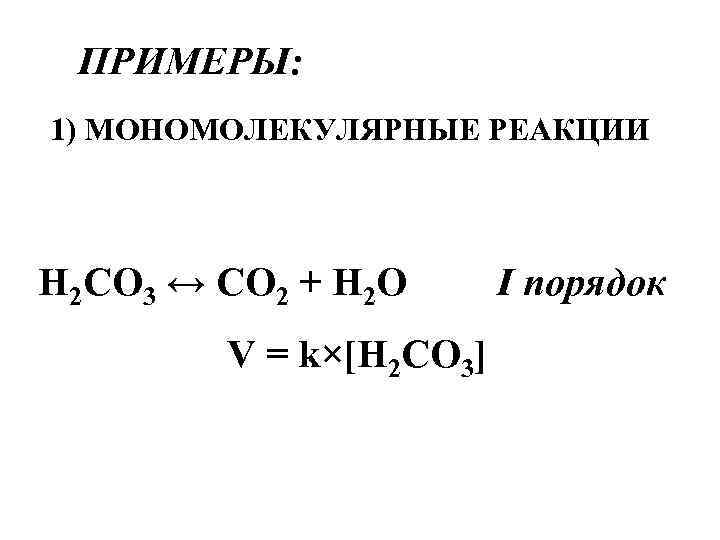 ПРИМЕРЫ: 1) МОНОМОЛЕКУЛЯРНЫЕ РЕАКЦИИ H 2 CO 3 ↔ CO 2 + H 2 O V = k×[H 2 CO 3] I порядок
ПРИМЕРЫ: 1) МОНОМОЛЕКУЛЯРНЫЕ РЕАКЦИИ H 2 CO 3 ↔ CO 2 + H 2 O V = k×[H 2 CO 3] I порядок
 2) БИМОЛЕКУЛЯРНЫЕ РЕАКЦИИ СО + Сl 2 ↔ CОCl 2 II порядок V = k×[CO]×[Сl 2] Hb + O 2 ↔ Hb. O 2 II порядок V = k×[Hb]×[O 2]
2) БИМОЛЕКУЛЯРНЫЕ РЕАКЦИИ СО + Сl 2 ↔ CОCl 2 II порядок V = k×[CO]×[Сl 2] Hb + O 2 ↔ Hb. O 2 II порядок V = k×[Hb]×[O 2]
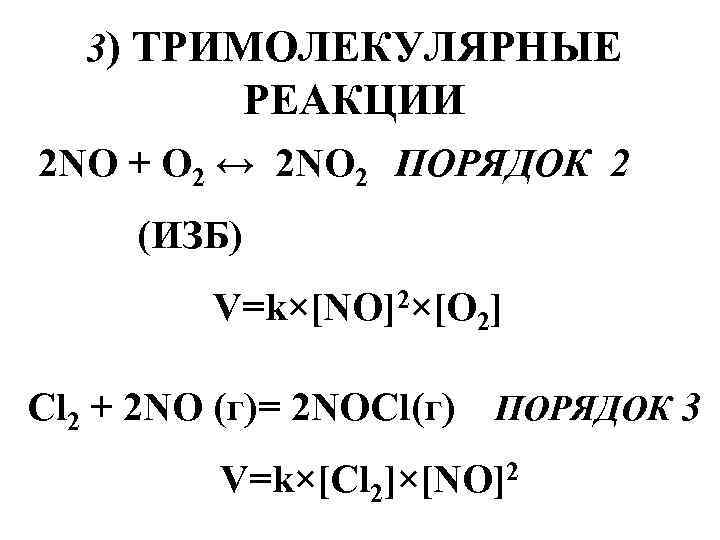 3) ТРИМОЛЕКУЛЯРНЫЕ РЕАКЦИИ 2 NO + O 2 ↔ 2 NO 2 ПОРЯДОК 2 (ИЗБ) V=k×[NO]2×[O 2] Cl 2 + 2 NO (г)= 2 NOCl(г) ПОРЯДОК 3 V=k×[Cl 2]×[NO]2
3) ТРИМОЛЕКУЛЯРНЫЕ РЕАКЦИИ 2 NO + O 2 ↔ 2 NO 2 ПОРЯДОК 2 (ИЗБ) V=k×[NO]2×[O 2] Cl 2 + 2 NO (г)= 2 NOCl(г) ПОРЯДОК 3 V=k×[Cl 2]×[NO]2
 КИНЕТИЧЕСКОЕ УРАВНЕНИЕ I ПОРЯДКА
КИНЕТИЧЕСКОЕ УРАВНЕНИЕ I ПОРЯДКА
 С 0 – начальная концентрация (С 0 -Х) = С – концентрация конечная Х – количество прореагированного вещества [k] = c-1, мин-1, час-1
С 0 – начальная концентрация (С 0 -Х) = С – концентрация конечная Х – количество прореагированного вещества [k] = c-1, мин-1, час-1
 ПОЛУПЕРИОД РЕАКЦИИ
ПОЛУПЕРИОД РЕАКЦИИ
 КИНЕТИЧЕСКОЕ УРАВНЕНИЕ ДЛЯ РЕАКЦИЙ II ПОРЯДКА
КИНЕТИЧЕСКОЕ УРАВНЕНИЕ ДЛЯ РЕАКЦИЙ II ПОРЯДКА
![Размерность константы реакций II порядка [k. II ] - л/моль×сек; -1×сек-1] [л×моль Размерность константы реакций II порядка [k. II ] - л/моль×сек; -1×сек-1] [л×моль](https://present5.com/presentation/3/86093824_131816707.pdf-img/86093824_131816707.pdf-15.jpg) Размерность константы реакций II порядка [k. II ] - л/моль×сек; -1×сек-1] [л×моль
Размерность константы реакций II порядка [k. II ] - л/моль×сек; -1×сек-1] [л×моль
 ПЕРИОД ПОЛУРАСПАДА ДЛЯ РЕАКЦИЙ II ПОРЯДКА
ПЕРИОД ПОЛУРАСПАДА ДЛЯ РЕАКЦИЙ II ПОРЯДКА
 Кинетическое уравнение реакций нулевого порядка
Кинетическое уравнение реакций нулевого порядка
 ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРТУРЫ УРАВНЕНИЕ ВАНТ-ГОФФА
ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРТУРЫ УРАВНЕНИЕ ВАНТ-ГОФФА
 γ – температурный коэффициент константы скорости реакции (2 -4) Vt и kt - скорость и константа при температуре t, (Vt + 100) и (kt +100) – при температуре (t+100)
γ – температурный коэффициент константы скорости реакции (2 -4) Vt и kt - скорость и константа при температуре t, (Vt + 100) и (kt +100) – при температуре (t+100)
 УРАВНЕНИЕ АРРЕНИУСА Еа и А – постоянные не зависящие от температуры величины; R – универсальная Дж/моль×К) газовая постоянная (8, 31 Т – абсолютная температура; А – предэкспонента, зависит от суммарного порядка реакции, размерность совпадает с размерностью константы скорости
УРАВНЕНИЕ АРРЕНИУСА Еа и А – постоянные не зависящие от температуры величины; R – универсальная Дж/моль×К) газовая постоянная (8, 31 Т – абсолютная температура; А – предэкспонента, зависит от суммарного порядка реакции, размерность совпадает с размерностью константы скорости
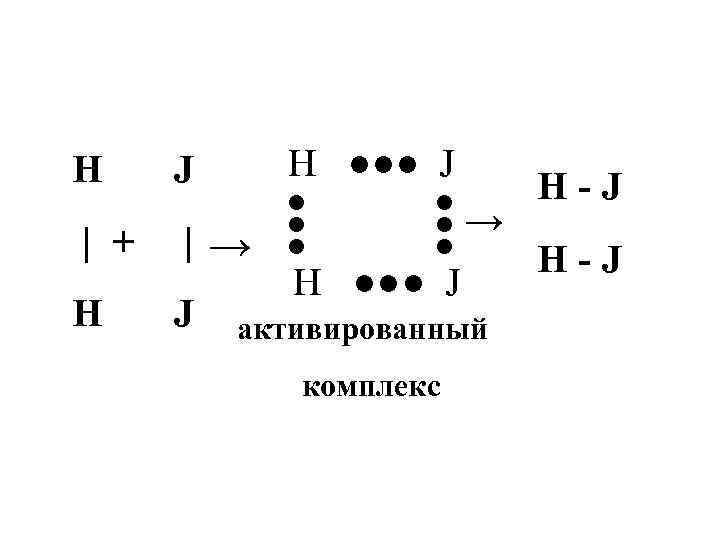 H ●●● J | + |→ ●●● H J ●●● J H → H ●●● J активированный комплекс H-J
H ●●● J | + |→ ●●● H J ●●● J H → H ●●● J активированный комплекс H-J
 РАСЧЁТ ЭНЕРГИИ АКТИВАЦИИ ПО УРАВНЕНИЮ АРРЕНИУСА
РАСЧЁТ ЭНЕРГИИ АКТИВАЦИИ ПО УРАВНЕНИЮ АРРЕНИУСА
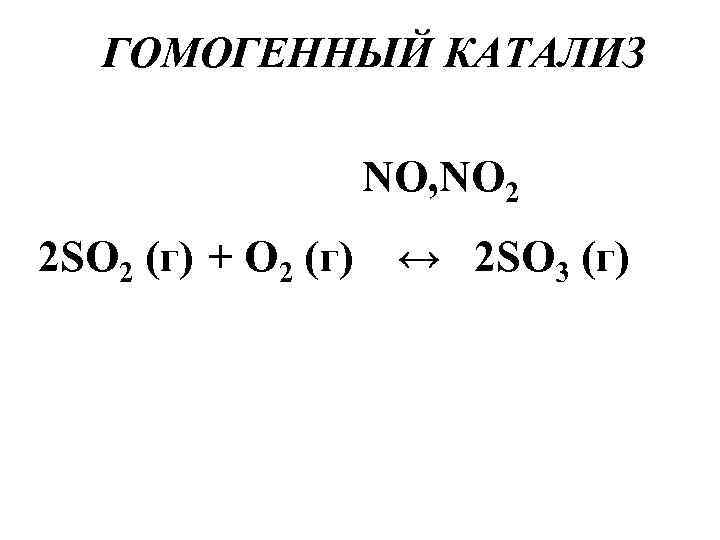 ГОМОГЕННЫЙ КАТАЛИЗ NO, NO 2 2 SO 2 (г) + O 2 (г) ↔ 2 SO 3 (г)
ГОМОГЕННЫЙ КАТАЛИЗ NO, NO 2 2 SO 2 (г) + O 2 (г) ↔ 2 SO 3 (г)
 ГЕТЕРОГЕННЫЙ АНАЛИЗ Fe N 2 (г) + 3 H 2 (г) ↔ 2 NH 3 (г)
ГЕТЕРОГЕННЫЙ АНАЛИЗ Fe N 2 (г) + 3 H 2 (г) ↔ 2 NH 3 (г)
 ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ СУБСТРАТА k 1 Е + S ↔ Е – S - фермент-субстратный k 2 комплекс k 3 Е – S ↔ Е + Р - где Р - продукт реакции
ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ СУБСТРАТА k 1 Е + S ↔ Е – S - фермент-субстратный k 2 комплекс k 3 Е – S ↔ Е + Р - где Р - продукт реакции
 УРАВНЕНИЕ МИХАЭЛИСА-МЕНТЕНА Vmax – максимальная скорость реакции в условиях насыщения фермента; kм – константа Михаэлиса, размерность концентрации; [S] – концентрация субстрата имеющая
УРАВНЕНИЕ МИХАЭЛИСА-МЕНТЕНА Vmax – максимальная скорость реакции в условиях насыщения фермента; kм – константа Михаэлиса, размерность концентрации; [S] – концентрация субстрата имеющая
 КОНСТАНТА МИХАЭЛИСА
КОНСТАНТА МИХАЭЛИСА
![ЗАВИСИМОСТЬ ИЗМЕНЕНИЯ СКОРОСТИ ОТ КОНЦЕНТРАЦИИ СУБСТРАТА VСТ [S] << KМ Vmax [S]>>KМ КМ [S] ЗАВИСИМОСТЬ ИЗМЕНЕНИЯ СКОРОСТИ ОТ КОНЦЕНТРАЦИИ СУБСТРАТА VСТ [S] << KМ Vmax [S]>>KМ КМ [S]](https://present5.com/presentation/3/86093824_131816707.pdf-img/86093824_131816707.pdf-28.jpg) ЗАВИСИМОСТЬ ИЗМЕНЕНИЯ СКОРОСТИ ОТ КОНЦЕНТРАЦИИ СУБСТРАТА VСТ [S] << KМ Vmax [S]>>KМ КМ [S] VСТ = VMAX
ЗАВИСИМОСТЬ ИЗМЕНЕНИЯ СКОРОСТИ ОТ КОНЦЕНТРАЦИИ СУБСТРАТА VСТ [S] << KМ Vmax [S]>>KМ КМ [S] VСТ = VMAX