Л.4.Теория цепных реакций.ppt
- Количество слайдов: 19
 Лекция 4 ВОЗНИКНОВЕНИЕ ПРОЦЕССОВ ГОРЕНИЯ ТГВ Основные механизмы самоускорения реакции 1. Тепловое самоускорение происходит вследствие саморазогрева системы за счет выделяющегося при реакции тепла. 2. Автокаталитическое, или, точнее, автокаталитически-тепловое, самоускорение происходит в результате накопления продуктов реакции, катализирующих превращение исходного вещества. Когда достигается перевес теплоприхода над теплоотводом, наступает тепловое ускорение, заканчивающееся взрывом. Сюда же относится самоускорение реакции в результате накопления промежуточного продукта при протекании распада в несколько последовательных стадий. 3. Цепное самоускорение реакции при постоянной температуре происходит в результате превышения разветвления над обрывом цепей.
Лекция 4 ВОЗНИКНОВЕНИЕ ПРОЦЕССОВ ГОРЕНИЯ ТГВ Основные механизмы самоускорения реакции 1. Тепловое самоускорение происходит вследствие саморазогрева системы за счет выделяющегося при реакции тепла. 2. Автокаталитическое, или, точнее, автокаталитически-тепловое, самоускорение происходит в результате накопления продуктов реакции, катализирующих превращение исходного вещества. Когда достигается перевес теплоприхода над теплоотводом, наступает тепловое ускорение, заканчивающееся взрывом. Сюда же относится самоускорение реакции в результате накопления промежуточного продукта при протекании распада в несколько последовательных стадий. 3. Цепное самоускорение реакции при постоянной температуре происходит в результате превышения разветвления над обрывом цепей.
 Лекция 4 Кинетика самоускоряющихся реакций ТГВ Каталитическое ускорение реакции Одним из наиболее широко известных примеров автокатализа является окисление щавелевой кислоты перманганатом калия 5 H 2 C 2 O 4 + 2 KMn. O 4 + 3 H 2 SO 4® 2 Mn. SO 4 + K 2 SO 4 + 10 CO 2 + 8 H 2 O. Катализатором этой реакции являются ионы Mn 2+. При комнатной температуре эта реакция вначале протекает медленно, но по мере накопления в растворе продуктакатализатора, она ускоряется.
Лекция 4 Кинетика самоускоряющихся реакций ТГВ Каталитическое ускорение реакции Одним из наиболее широко известных примеров автокатализа является окисление щавелевой кислоты перманганатом калия 5 H 2 C 2 O 4 + 2 KMn. O 4 + 3 H 2 SO 4® 2 Mn. SO 4 + K 2 SO 4 + 10 CO 2 + 8 H 2 O. Катализатором этой реакции являются ионы Mn 2+. При комнатной температуре эта реакция вначале протекает медленно, но по мере накопления в растворе продуктакатализатора, она ускоряется.
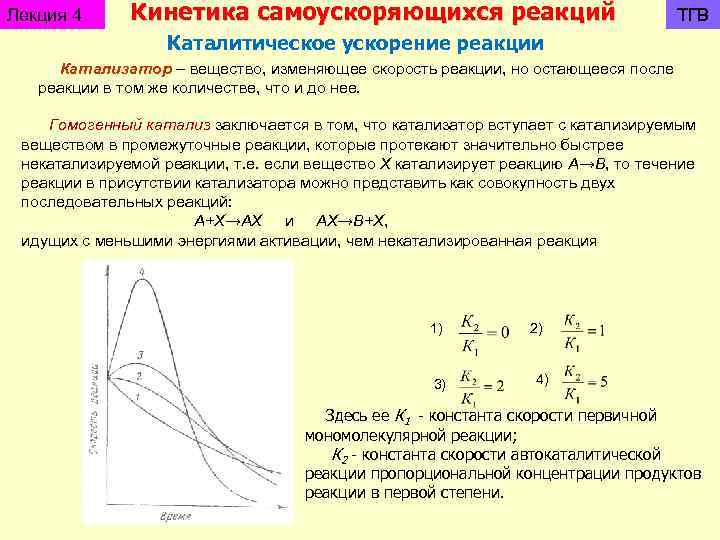 Лекция 4 Кинетика самоускоряющихся реакций ТГВ Каталитическое ускорение реакции Катализатор – вещество, изменяющее скорость реакции, но остающееся после реакции в том же количестве, что и до нее. Гомогенный катализ заключается в том, что катализатор вступает с катализируемым веществом в промежуточные реакции, которые протекают значительно быстрее некатализируемой реакции, т. е. если вещество X катализирует реакцию А→В, то течение реакции в присутствии катализатора можно представить как совокупность двух последовательных реакций: А+Х→АХ и АХ→В+Х, идущих с меньшими энергиями активации, чем некатализированная реакция 1) 3) 2) 4) Здесь ее К 1 - константа скорости первичной мономолекулярной реакции; К 2 - константа скорости автокаталитической реакции пропорциональной концентрации продуктов реакции в первой степени.
Лекция 4 Кинетика самоускоряющихся реакций ТГВ Каталитическое ускорение реакции Катализатор – вещество, изменяющее скорость реакции, но остающееся после реакции в том же количестве, что и до нее. Гомогенный катализ заключается в том, что катализатор вступает с катализируемым веществом в промежуточные реакции, которые протекают значительно быстрее некатализируемой реакции, т. е. если вещество X катализирует реакцию А→В, то течение реакции в присутствии катализатора можно представить как совокупность двух последовательных реакций: А+Х→АХ и АХ→В+Х, идущих с меньшими энергиями активации, чем некатализированная реакция 1) 3) 2) 4) Здесь ее К 1 - константа скорости первичной мономолекулярной реакции; К 2 - константа скорости автокаталитической реакции пропорциональной концентрации продуктов реакции в первой степени.
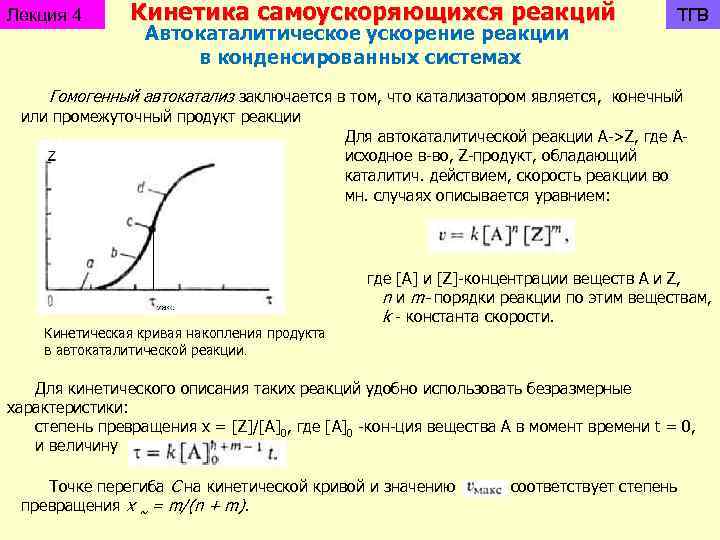 Лекция 4 Кинетика самоускоряющихся реакций Автокаталитическое ускорение реакции в конденсированных системах ТГВ Гомогенный автокатализ заключается в том, что катализатором является, конечный или промежуточный продукт реакции Для автокаталитической реакции A->Z, где Аисходное в-во, Z-продукт, обладающий каталитич. действием, скорость реакции во мн. случаях описывается уравнием: Кинетическая кривая накопления продукта в автокаталитической реакции. где [А] и [Z]-концентрации веществ А и Z, n и m- порядки реакции по этим веществам, k - константа скорости. Для кинетического описания таких реакций удобно использовать безразмерные характеристики: степень превращения x = [Z]/[A]0, где [А]0 -кон-ция вещества А в момент времени t = 0, и величину Точке перегиба C на кинетической кривой и значению соответствует степень превращения х ~ = m/(n + m).
Лекция 4 Кинетика самоускоряющихся реакций Автокаталитическое ускорение реакции в конденсированных системах ТГВ Гомогенный автокатализ заключается в том, что катализатором является, конечный или промежуточный продукт реакции Для автокаталитической реакции A->Z, где Аисходное в-во, Z-продукт, обладающий каталитич. действием, скорость реакции во мн. случаях описывается уравнием: Кинетическая кривая накопления продукта в автокаталитической реакции. где [А] и [Z]-концентрации веществ А и Z, n и m- порядки реакции по этим веществам, k - константа скорости. Для кинетического описания таких реакций удобно использовать безразмерные характеристики: степень превращения x = [Z]/[A]0, где [А]0 -кон-ция вещества А в момент времени t = 0, и величину Точке перегиба C на кинетической кривой и значению соответствует степень превращения х ~ = m/(n + m).
 Кинетика самоускоряющихся реакций Лекция 4 Автокаталитическое ускорение реакции в конденсированных системах Степень превращения вещества х и максимальная скорость реакции для автокаталитической реакции А -> Z - Помимо автокаталитических реакций, с самоускорением протекают: - Цепные реакции, если в исходной смеси присутствует ингибитор. Цепные разветвленные реакции в условиях нестационарного режима. - и др. ТГВ
Кинетика самоускоряющихся реакций Лекция 4 Автокаталитическое ускорение реакции в конденсированных системах Степень превращения вещества х и максимальная скорость реакции для автокаталитической реакции А -> Z - Помимо автокаталитических реакций, с самоускорением протекают: - Цепные реакции, если в исходной смеси присутствует ингибитор. Цепные разветвленные реакции в условиях нестационарного режима. - и др. ТГВ
 Лекция 4 ТГВ Теория цепной разветвленной реакции Кинетика цепных реакций водорода с кислородом Здесь М - любая молекула. 4. ОН + Н 2 = Н 2 О + Н продолжение цепи обрыв цепей на стенке 9. Н + О 2 + М = НО 2 + M 10. обрыв цепей в объеме
Лекция 4 ТГВ Теория цепной разветвленной реакции Кинетика цепных реакций водорода с кислородом Здесь М - любая молекула. 4. ОН + Н 2 = Н 2 О + Н продолжение цепи обрыв цепей на стенке 9. Н + О 2 + М = НО 2 + M 10. обрыв цепей в объеме
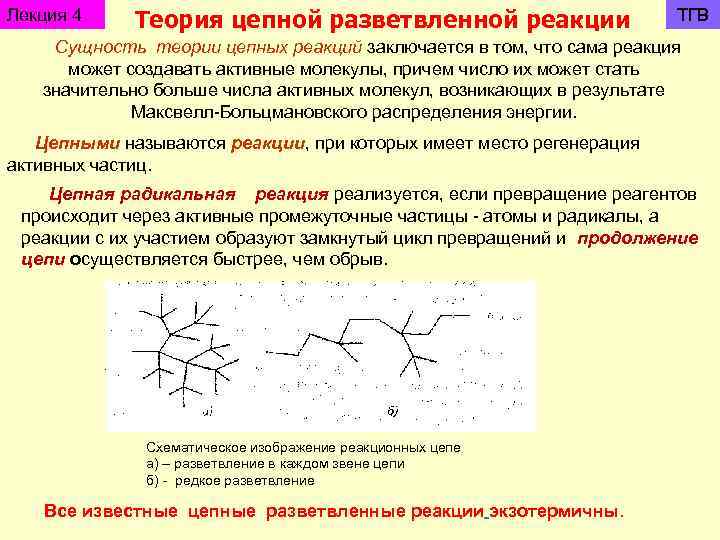 Лекция 4 Теория цепной разветвленной реакции ТГВ Сущность теории цепных реакций заключается в том, что сама реакция может создавать активные молекулы, причем число их может стать значительно больше числа активных молекул, возникающих в результате Максвелл-Больцмановского распределения энергии. Цепными называются реакции, при которых имеет место регенерация активных частиц. Цепная радикальная реакция реализуется, если превращение реагентов происходит через активные промежуточные частицы - атомы и радикалы, а реакции с их участием образуют замкнутый цикл превращений и продолжение цепи осуществляется быстрее, чем обрыв. Схематическое изображение реакционных цепе а) – разветвление в каждом звене цепи б) - редкое разветвление Все известные цепные разветвленные реакции экзотермичны.
Лекция 4 Теория цепной разветвленной реакции ТГВ Сущность теории цепных реакций заключается в том, что сама реакция может создавать активные молекулы, причем число их может стать значительно больше числа активных молекул, возникающих в результате Максвелл-Больцмановского распределения энергии. Цепными называются реакции, при которых имеет место регенерация активных частиц. Цепная радикальная реакция реализуется, если превращение реагентов происходит через активные промежуточные частицы - атомы и радикалы, а реакции с их участием образуют замкнутый цикл превращений и продолжение цепи осуществляется быстрее, чем обрыв. Схематическое изображение реакционных цепе а) – разветвление в каждом звене цепи б) - редкое разветвление Все известные цепные разветвленные реакции экзотермичны.
 Лекция 4 Теория цепной разветвленной реакции ТГВ В цепной неразветвленной реакции концентрация активных центров n зависит только от скоростей инициирования vi и обрыва vt = gn, где g -удельная скорость обрыва цепей в присутствии ингибитора In. H, g = k. In. H[In. H], в квазистационарном режиме n = vi/g. В цепной разветвленной реакции акты разветвления обеспечивают возможность прогрессивного увеличения концентрации активных центров во времени. При обрыве и разветвлении цепей по реакции 1 -го порядка с удельными скоростями g и f, соответственно, скорость изменения концентрации активных центров n описывается уравнением: dn/dt = vi - (g - f)n. При квазистационарном режиме протекания реакции (g > f) n = vi/(g -f) = const, начиная с t > (g - f)-1 При нестационарном режиме (f > g) концентрация активных центров непрерывно нарастает во времени, и если не принимать во внимание расходования реагентов и изменения во времени vi, g и f, то n = vi (f -g)-1(e(f -g)t-1). Критическим условием перехода системы из одного состояния в другое является равенство f = g. Таким образом, цепная реакция с разветвлением протекает как самоускоряющийся процесс только тогда, когда активные центры быстрее вступают в акты разветвления, чем в акты обрыва.
Лекция 4 Теория цепной разветвленной реакции ТГВ В цепной неразветвленной реакции концентрация активных центров n зависит только от скоростей инициирования vi и обрыва vt = gn, где g -удельная скорость обрыва цепей в присутствии ингибитора In. H, g = k. In. H[In. H], в квазистационарном режиме n = vi/g. В цепной разветвленной реакции акты разветвления обеспечивают возможность прогрессивного увеличения концентрации активных центров во времени. При обрыве и разветвлении цепей по реакции 1 -го порядка с удельными скоростями g и f, соответственно, скорость изменения концентрации активных центров n описывается уравнением: dn/dt = vi - (g - f)n. При квазистационарном режиме протекания реакции (g > f) n = vi/(g -f) = const, начиная с t > (g - f)-1 При нестационарном режиме (f > g) концентрация активных центров непрерывно нарастает во времени, и если не принимать во внимание расходования реагентов и изменения во времени vi, g и f, то n = vi (f -g)-1(e(f -g)t-1). Критическим условием перехода системы из одного состояния в другое является равенство f = g. Таким образом, цепная реакция с разветвлением протекает как самоускоряющийся процесс только тогда, когда активные центры быстрее вступают в акты разветвления, чем в акты обрыва.
 Теория цепной разветвленной реакции Лекция 4 ТГВ Пределы воспламенения по давлению При низком давлении газа в реакторе активные центры быстро достигают стенки реактора, адсорбируются на ней и рекомбинируют: происходит обрыв цепей на стенке. При малой вероятности рекомбинации на стенке обрыв цепи происходит после многократных столкновений активного центра с поверхностью и не лимитируется их диффузией к поверхности. Скорость обрыва цепей равна vt = gn = 250(S/V) где S и V -поверхность и объем реактора; -средняя тепловая скорость движения частиц. Разветвление цепи происходит со скоростью, равной vf = kf [реагент]n = 10 -3 kf (RT )-1 n где -парциальное давление реагента. Критический переход наблюдается при выполнении равенства f = g или vf = vt, откуда следует выражение для нижнего критического давления p 1 = 103 g. RT/ kf. Этого давления можно достичь как путем изменения концентрации реагентов, так и путем введения инертного газа
Теория цепной разветвленной реакции Лекция 4 ТГВ Пределы воспламенения по давлению При низком давлении газа в реакторе активные центры быстро достигают стенки реактора, адсорбируются на ней и рекомбинируют: происходит обрыв цепей на стенке. При малой вероятности рекомбинации на стенке обрыв цепи происходит после многократных столкновений активного центра с поверхностью и не лимитируется их диффузией к поверхности. Скорость обрыва цепей равна vt = gn = 250(S/V) где S и V -поверхность и объем реактора; -средняя тепловая скорость движения частиц. Разветвление цепи происходит со скоростью, равной vf = kf [реагент]n = 10 -3 kf (RT )-1 n где -парциальное давление реагента. Критический переход наблюдается при выполнении равенства f = g или vf = vt, откуда следует выражение для нижнего критического давления p 1 = 103 g. RT/ kf. Этого давления можно достичь как путем изменения концентрации реагентов, так и путем введения инертного газа
 Лекция 4 Теория цепной разветвленной реакции Пределы воспламенения по давлению (продолжение) Повышение давления приводит к тому, что все чаще происходит гибель активных центров при тройном столкновении активного центра с двумя частицами, в результате чего происходит обрыв цепи. Скорость обрыва цепей в таком случае vt = 2 x 103 kt p 2(RT )-2 n. Критическое условие vf = vt приводит к верхнему пределу по давлению: p 2 = 10 -3 kf RT/2 kt. ТГВ
Лекция 4 Теория цепной разветвленной реакции Пределы воспламенения по давлению (продолжение) Повышение давления приводит к тому, что все чаще происходит гибель активных центров при тройном столкновении активного центра с двумя частицами, в результате чего происходит обрыв цепи. Скорость обрыва цепей в таком случае vt = 2 x 103 kt p 2(RT )-2 n. Критическое условие vf = vt приводит к верхнему пределу по давлению: p 2 = 10 -3 kf RT/2 kt. ТГВ
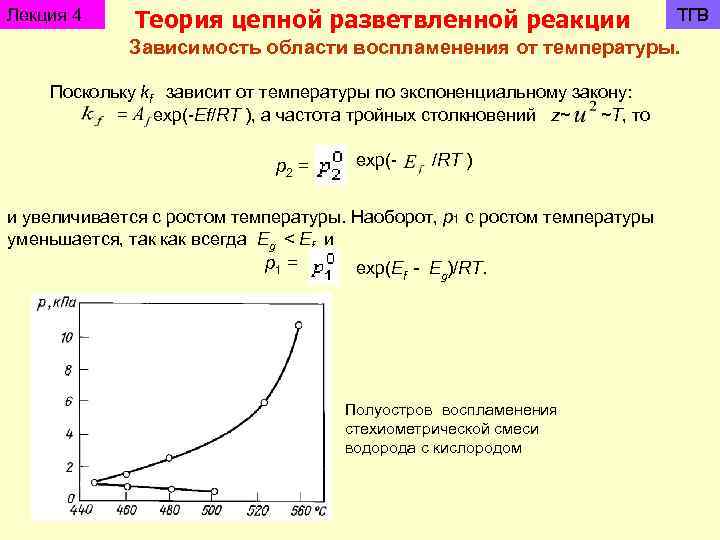 Лекция 4 Теория цепной разветвленной реакции ТГВ Зависимость области воспламенения от температуры. kf Поскольку зависит от температуры по экспоненциальному закону: = exp(-Ef/RT ), а частота тройных столкновений z~ ~T, то exp(- /RT ) p = 2 и увеличивается с ростом температуры. Наоборот, р1 с ростом температуры уменьшается, так как всегда Eg < Ef и p 1 = exp(E - E )/RT. f g Полуостров воспламенения стехиометрической смеси водорода с кислородом
Лекция 4 Теория цепной разветвленной реакции ТГВ Зависимость области воспламенения от температуры. kf Поскольку зависит от температуры по экспоненциальному закону: = exp(-Ef/RT ), а частота тройных столкновений z~ ~T, то exp(- /RT ) p = 2 и увеличивается с ростом температуры. Наоборот, р1 с ростом температуры уменьшается, так как всегда Eg < Ef и p 1 = exp(E - E )/RT. f g Полуостров воспламенения стехиометрической смеси водорода с кислородом
 Лекция 4 Теория цепной разветвленной реакции ТГВ Зависимость области воспламенения от температуры (продолжение) Оба предела сходятся при температуре ТМ (“мыс полуострова воспламенения”), когда р1 = р2. Эта температура определяется равенством ТМ = (2 Ef-Eg)/[Rln При Т < ТМ цепная разветвленная реакция не реализуется, т. е. ТМ -это критическая температура, ниже которой цепное воспламенение невозможно. Контур этого полуострова может изменяться при изменении условий опыта: - при увеличении отношения S/V (введение в сосуд стержней, уменьшении диаметра сосуда и т. п. ) g возрастает и происходит повышение нижнего предела р1 как функции Т; - разбавление смеси инертным газом затрудняет диффузию активных частиц к стенке и одновременно повышает долю тримолекулярных столкновений из-за роста общего давления. В результате происходят уменьшение g в области нижнего предела самовоспламенения и рост g в области верхнего предела; - при введении ингибитора контур полуострова воспламенения изменяется, нижний предел повышается, верхний - понижается.
Лекция 4 Теория цепной разветвленной реакции ТГВ Зависимость области воспламенения от температуры (продолжение) Оба предела сходятся при температуре ТМ (“мыс полуострова воспламенения”), когда р1 = р2. Эта температура определяется равенством ТМ = (2 Ef-Eg)/[Rln При Т < ТМ цепная разветвленная реакция не реализуется, т. е. ТМ -это критическая температура, ниже которой цепное воспламенение невозможно. Контур этого полуострова может изменяться при изменении условий опыта: - при увеличении отношения S/V (введение в сосуд стержней, уменьшении диаметра сосуда и т. п. ) g возрастает и происходит повышение нижнего предела р1 как функции Т; - разбавление смеси инертным газом затрудняет диффузию активных частиц к стенке и одновременно повышает долю тримолекулярных столкновений из-за роста общего давления. В результате происходят уменьшение g в области нижнего предела самовоспламенения и рост g в области верхнего предела; - при введении ингибитора контур полуострова воспламенения изменяется, нижний предел повышается, верхний - понижается.
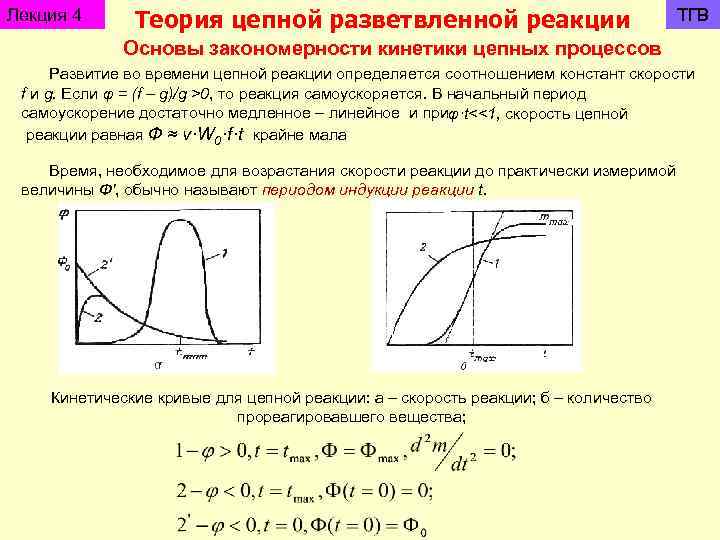 Лекция 4 Теория цепной разветвленной реакции ТГВ Основы закономерности кинетики цепных процессов Развитие во времени цепной реакции определяется соотношением констант скорости f и g. Если φ = (f – g)/g >0, то реакция самоускоряется. В начальный период самоускорение достаточно медленное – линейное и при φ·t<<1, скорость цепной реакции равная Ф ≈ v·W 0·f·t крайне мала Время, необходимое для возрастания скорости реакции до практически измеримой величины Ф', обычно называют периодом индукции реакции t. Кинетические кривые для цепной реакции: а – скорость реакции; б – количество прореагировавшего вещества;
Лекция 4 Теория цепной разветвленной реакции ТГВ Основы закономерности кинетики цепных процессов Развитие во времени цепной реакции определяется соотношением констант скорости f и g. Если φ = (f – g)/g >0, то реакция самоускоряется. В начальный период самоускорение достаточно медленное – линейное и при φ·t<<1, скорость цепной реакции равная Ф ≈ v·W 0·f·t крайне мала Время, необходимое для возрастания скорости реакции до практически измеримой величины Ф', обычно называют периодом индукции реакции t. Кинетические кривые для цепной реакции: а – скорость реакции; б – количество прореагировавшего вещества;
 Лекция 4 ТГВ Теория цепной разветвленной реакции Кинетика цепных реакций водорода с кислородом При воспламенении и горении в области между нижним и верхним пределом основную роль играют реакции разветвления цепи 5 и 6. Обрыв цепи идет главным образом на стенке по реакции 7. При повышении давления увеличивается число тройных соударений, ведущих к обрыву цепи по реакции 9 с образованием малоактивного радикала НО 2, который разлагается на стенке по реакциям 10. Для медленного окисления при давлениях выше верхнего предела значение отдельных реакций уже иное, чем в пламени. Роль реакции 5, протекающей через двойные соударения, уменьшается по сравнению с реакцией 9. Концентрация атомарного водорода уменьшается потому, что реакция 6 становится относительно редкой. Разветвления цепи начинают играть второстепенную роль, и вместо воспламенения происходит медленная реакция. Повышение общего давления затрудняет диффузию и гибель на стенке радикала НО 2, который теперь может реагировать в объеме, в частности, по реакции 11 (образование перекиси водорода при медленном окислении водорода в этой области давлений). Ведущей при достаточно больших давлениях (выше верхнего предела) становится последовательность реакций 9, 11 и 10. Концентрация атомов водорода в начальной стадии процесса самовоспламенения составляет незначительную часть от начального содержания водорода. При развитии цепной реакции скорость превращения молекулярного водорода становится столь высокой, что он расходуется за сотые доли секунды.
Лекция 4 ТГВ Теория цепной разветвленной реакции Кинетика цепных реакций водорода с кислородом При воспламенении и горении в области между нижним и верхним пределом основную роль играют реакции разветвления цепи 5 и 6. Обрыв цепи идет главным образом на стенке по реакции 7. При повышении давления увеличивается число тройных соударений, ведущих к обрыву цепи по реакции 9 с образованием малоактивного радикала НО 2, который разлагается на стенке по реакциям 10. Для медленного окисления при давлениях выше верхнего предела значение отдельных реакций уже иное, чем в пламени. Роль реакции 5, протекающей через двойные соударения, уменьшается по сравнению с реакцией 9. Концентрация атомарного водорода уменьшается потому, что реакция 6 становится относительно редкой. Разветвления цепи начинают играть второстепенную роль, и вместо воспламенения происходит медленная реакция. Повышение общего давления затрудняет диффузию и гибель на стенке радикала НО 2, который теперь может реагировать в объеме, в частности, по реакции 11 (образование перекиси водорода при медленном окислении водорода в этой области давлений). Ведущей при достаточно больших давлениях (выше верхнего предела) становится последовательность реакций 9, 11 и 10. Концентрация атомов водорода в начальной стадии процесса самовоспламенения составляет незначительную часть от начального содержания водорода. При развитии цепной реакции скорость превращения молекулярного водорода становится столь высокой, что он расходуется за сотые доли секунды.
 Лекция 4 Теория цепной разветвленной реакции ТГВ Взаимодействие окиси углерода с кислородом Окисление окиси углерода кислородом – сложная разветвленная цепная реакция. Ее специфическая особенность заключается в том, что она катализируется водородом, водой либо другими водородсодержащими веществами. Тщательно высушенные смеси СО+О 2 не горят и не реагируют при умеренном нагревании, а при Т>700°С в них начинается медленное гетерогенное взаимодействие. 1. ОН+СО→СO 2+Н 2. Н+О 2→OH+O 3. О+СО+М→СО 2+М 4. Н 2 О+СО↔CО 2+H 2 5. НО 2+СО→СО 2+ОН 6. О+Н 2→ОН+Н 7. ОН+Н 2→Н 2 О+Н Главные активные центры в реакционной цепи – гидроксил и атомарный водород. Условие горения оксида углерода в воздухе в значительной степени определяется присутствием и закономерностями горения водорода. Окисление СО по реакции (1) зависит от концентрации радикалов ОН, образующихся в реакциях с участием водорода.
Лекция 4 Теория цепной разветвленной реакции ТГВ Взаимодействие окиси углерода с кислородом Окисление окиси углерода кислородом – сложная разветвленная цепная реакция. Ее специфическая особенность заключается в том, что она катализируется водородом, водой либо другими водородсодержащими веществами. Тщательно высушенные смеси СО+О 2 не горят и не реагируют при умеренном нагревании, а при Т>700°С в них начинается медленное гетерогенное взаимодействие. 1. ОН+СО→СO 2+Н 2. Н+О 2→OH+O 3. О+СО+М→СО 2+М 4. Н 2 О+СО↔CО 2+H 2 5. НО 2+СО→СО 2+ОН 6. О+Н 2→ОН+Н 7. ОН+Н 2→Н 2 О+Н Главные активные центры в реакционной цепи – гидроксил и атомарный водород. Условие горения оксида углерода в воздухе в значительной степени определяется присутствием и закономерностями горения водорода. Окисление СО по реакции (1) зависит от концентрации радикалов ОН, образующихся в реакциях с участием водорода.
 Лекция 4 Теория цепной разветвленной реакции ТГВ Взаимодействие окиси углерода с кислородом (продолжение) Реакция (6) и реакция, обратная (7) (оба процесса обратимы), также способствуют быстрому расщеплению воды на радикалы. В результате этих процессов действие любых водородсодержащих катализаторов оказывается эквивалентным, независимо от того, в каком виде водород попадает в реакционную среду, если концентрация катализатора мала по сравнению с концентрацией недостающего компонента смеси Особенность реакции горения оксида углерода заключается в ее резком торможении при введении в реагирующую систему малых добавок веществ, обладающих высоким сродством к атомам водорода. Такими веществами, ингибирующими горение СО, являются галоиды и галоидироизводные углеводородов. Их ингибирующее действие обусловлено обрывом реакционных цепей при взаимодействии с атомами водорода по реакции CCl 4 - четыреххлористый углерод (тетрахлорметан)
Лекция 4 Теория цепной разветвленной реакции ТГВ Взаимодействие окиси углерода с кислородом (продолжение) Реакция (6) и реакция, обратная (7) (оба процесса обратимы), также способствуют быстрому расщеплению воды на радикалы. В результате этих процессов действие любых водородсодержащих катализаторов оказывается эквивалентным, независимо от того, в каком виде водород попадает в реакционную среду, если концентрация катализатора мала по сравнению с концентрацией недостающего компонента смеси Особенность реакции горения оксида углерода заключается в ее резком торможении при введении в реагирующую систему малых добавок веществ, обладающих высоким сродством к атомам водорода. Такими веществами, ингибирующими горение СО, являются галоиды и галоидироизводные углеводородов. Их ингибирующее действие обусловлено обрывом реакционных цепей при взаимодействии с атомами водорода по реакции CCl 4 - четыреххлористый углерод (тетрахлорметан)
 Лекция 4 Теория цепной разветвленной реакции ТГВ Окисление углеводородов В углеводородных пламенах, наряду с уже известными активными частицами присутствует большое количество промежуточных продуктов более сложного строения. В ряде случаев они становятся источниками зарождения новых цепей. Основную роль в процессах воспламенения и горения углеводородов играют следующие типы промежуточных соединений: 1. Углеводородные радикалы, представляющие собой молекулу углеводорода, у которой удалены один или несколько атомов водорода. Эти остатки называются алкилами (СНз - метил; С 2 Н 5 - этил; С 3 Н 7 - пропил и т. д. ). Из-за высокой реакционной способности алкилы в свободном виде длительно не существуют. Присутствуют в пламенах в виде промежуточных продуктов. При взаимодействии с другими молекулами ведут себя как самостоятельная структурная группа. Углеводородные радикалы обычно изображают буквой R. 2. Перекиси - соединения общей формулы R-00 -R'. 3. Альдегиды - соединения типа Простейшими альдегидами являются муравьиный (формальдегид) и уксусный (ацетальдегид). Эти вещества всегда присутствуют в продуктах неполного сгорания углеводородов.
Лекция 4 Теория цепной разветвленной реакции ТГВ Окисление углеводородов В углеводородных пламенах, наряду с уже известными активными частицами присутствует большое количество промежуточных продуктов более сложного строения. В ряде случаев они становятся источниками зарождения новых цепей. Основную роль в процессах воспламенения и горения углеводородов играют следующие типы промежуточных соединений: 1. Углеводородные радикалы, представляющие собой молекулу углеводорода, у которой удалены один или несколько атомов водорода. Эти остатки называются алкилами (СНз - метил; С 2 Н 5 - этил; С 3 Н 7 - пропил и т. д. ). Из-за высокой реакционной способности алкилы в свободном виде длительно не существуют. Присутствуют в пламенах в виде промежуточных продуктов. При взаимодействии с другими молекулами ведут себя как самостоятельная структурная группа. Углеводородные радикалы обычно изображают буквой R. 2. Перекиси - соединения общей формулы R-00 -R'. 3. Альдегиды - соединения типа Простейшими альдегидами являются муравьиный (формальдегид) и уксусный (ацетальдегид). Эти вещества всегда присутствуют в продуктах неполного сгорания углеводородов.
 Лекция 4 Теория цепной разветвленной реакции ТГВ Окисление углеводородов Зарождением цепи при горении углеводородов может стать любая реакция, в которой образуются углеводородные радикалы. Это может быть реакция разложения молекулы этана с образованием двух свободных метальных групп: или реакция углеводорода с кислородом: Продолжение цепей происходит в результате реакций образования | перекисей или гидроперекиси: Разветвление цепей осуществляется при разложении гидроперекиси: Одновременно с накоплением перекисей, радикалов начинают идти параллельные реакции: и
Лекция 4 Теория цепной разветвленной реакции ТГВ Окисление углеводородов Зарождением цепи при горении углеводородов может стать любая реакция, в которой образуются углеводородные радикалы. Это может быть реакция разложения молекулы этана с образованием двух свободных метальных групп: или реакция углеводорода с кислородом: Продолжение цепей происходит в результате реакций образования | перекисей или гидроперекиси: Разветвление цепей осуществляется при разложении гидроперекиси: Одновременно с накоплением перекисей, радикалов начинают идти параллельные реакции: и
 Лекция 4 Теория цепной разветвленной реакции ТГВ Окисление углеводородов 1. ОН+RH→Н 2 О + R˙ 2. O+RH→OH+R˙ 3. О 2+R˙→RO+O Общие черты: для всех горючих суммарный процесс – автокаталитический, он протекает по разветвленному цепному механизму, обнаруживая склонность к замедленному развитию во времени после определенного периода индукции. Как и для водорода, концентрации активных центров значительно превосходят равновесные. 4. R˙+О 2→RO 2 5. RO 2+RH→RO 2 H+R˙ При высоких температурах в пламенах смесей, содержащих избыток горючего, образуются в заметных 6. R'CH 2 O 2→R'CHO+ОН количествах радикалы С 2 и СН. ˙ 7. R'CH 2 O 2→HCHO+RO˙ 8. HCHO+RH→H 3 CO˙+R˙ или H 2 C˙OH+R˙ При повышении температуры реагирующей смеси роль активных центров переходит от одних промежуточных продуктов к другим в следующем порядке: • гидроперекиси алкилов, • ацильные гидроперекиси, • формальдегиды.
Лекция 4 Теория цепной разветвленной реакции ТГВ Окисление углеводородов 1. ОН+RH→Н 2 О + R˙ 2. O+RH→OH+R˙ 3. О 2+R˙→RO+O Общие черты: для всех горючих суммарный процесс – автокаталитический, он протекает по разветвленному цепному механизму, обнаруживая склонность к замедленному развитию во времени после определенного периода индукции. Как и для водорода, концентрации активных центров значительно превосходят равновесные. 4. R˙+О 2→RO 2 5. RO 2+RH→RO 2 H+R˙ При высоких температурах в пламенах смесей, содержащих избыток горючего, образуются в заметных 6. R'CH 2 O 2→R'CHO+ОН количествах радикалы С 2 и СН. ˙ 7. R'CH 2 O 2→HCHO+RO˙ 8. HCHO+RH→H 3 CO˙+R˙ или H 2 C˙OH+R˙ При повышении температуры реагирующей смеси роль активных центров переходит от одних промежуточных продуктов к другим в следующем порядке: • гидроперекиси алкилов, • ацильные гидроперекиси, • формальдегиды.


