Лекция 4,5 ЭМ.ppt
- Количество слайдов: 40
 Лекция № 4 «Влияние химических факторов на микроорганизмы. Водная активность. Механизмы осмотолерантности. Микроорганизмы и р. Н» по дисциплине «Экология микроорганизмов»
Лекция № 4 «Влияние химических факторов на микроорганизмы. Водная активность. Механизмы осмотолерантности. Микроорганизмы и р. Н» по дисциплине «Экология микроорганизмов»
 План лекции: n n Механизмы осмотолерантности: – Понятие водной активности и водного потенциала. – Молекулярные механизмы осмотолерантности. Микроорганизмы и р. Н. – Отношение микроорганизмов к р. Н. Ацидофилы, нейтрофилы и алкалофилы. – Влияние р. Н среды на формирование трансмембранного электрохимического потенциала в бактериальной клетке. 2
План лекции: n n Механизмы осмотолерантности: – Понятие водной активности и водного потенциала. – Молекулярные механизмы осмотолерантности. Микроорганизмы и р. Н. – Отношение микроорганизмов к р. Н. Ацидофилы, нейтрофилы и алкалофилы. – Влияние р. Н среды на формирование трансмембранного электрохимического потенциала в бактериальной клетке. 2
 Активность воды Активности воды (аw) - степень доступности воды для химических реакций и микроорганизмов аw =Р/Р 0=ОВ/100=П 2/П 1 -П 2 , где Р - давления пара жидкости, Р 0 - давление пара дистиллированной воды, ОВ – относительная влажность, П 1 - число молей растворителя, П 2 – число молей растворённого вещества. 3
Активность воды Активности воды (аw) - степень доступности воды для химических реакций и микроорганизмов аw =Р/Р 0=ОВ/100=П 2/П 1 -П 2 , где Р - давления пара жидкости, Р 0 - давление пара дистиллированной воды, ОВ – относительная влажность, П 1 - число молей растворителя, П 2 – число молей растворённого вещества. 3
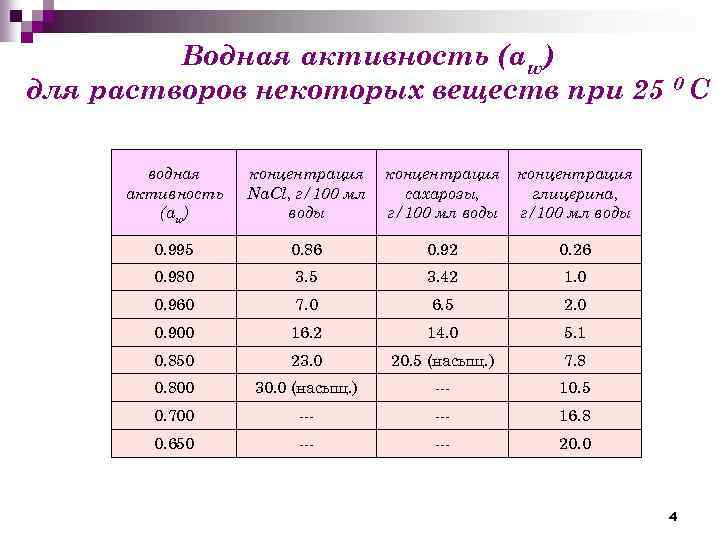 Водная активность (аw) для растворов некоторых веществ при 25 0 С водная активность (аw) концентрация Na. Cl, г/100 мл воды концентрация сахарозы, г/100 мл воды концентрация глицерина, г/100 мл воды 0. 995 0. 86 0. 92 0. 26 0. 980 3. 5 3. 42 1. 0 0. 960 7. 0 6. 5 2. 0 0. 900 16. 2 14. 0 5. 1 0. 850 23. 0 20. 5 (насыщ. ) 7. 8 0. 800 30. 0 (насыщ. ) --- 10. 5 0. 700 --- 16. 8 0. 650 --- 20. 0 4
Водная активность (аw) для растворов некоторых веществ при 25 0 С водная активность (аw) концентрация Na. Cl, г/100 мл воды концентрация сахарозы, г/100 мл воды концентрация глицерина, г/100 мл воды 0. 995 0. 86 0. 92 0. 26 0. 980 3. 5 3. 42 1. 0 0. 960 7. 0 6. 5 2. 0 0. 900 16. 2 14. 0 5. 1 0. 850 23. 0 20. 5 (насыщ. ) 7. 8 0. 800 30. 0 (насыщ. ) --- 10. 5 0. 700 --- 16. 8 0. 650 --- 20. 0 4
 Значения водной активности аw, лимитирующие рост некоторых микроорганизмов аw Бактерии 1. 00 Многие грамположительные палочки Мицелиальные грибы Водоросли Caulobacter Spirillum 0. 95 Дрожжи 0. 90 Многие кокки Lactobacillus Bacillus 0. 85. Staphyllococcus Basidiomycetes Ascomycetes Debariomyces Saccharomyces bailii 0. 80 0. 75 0. 65 Большинство групп Penicillum Halobacterium Halococcus Wallemia Aspergillus Chrysosporum Saccharomyces rouxii Dunaliella Xeromyces bisporus 5
Значения водной активности аw, лимитирующие рост некоторых микроорганизмов аw Бактерии 1. 00 Многие грамположительные палочки Мицелиальные грибы Водоросли Caulobacter Spirillum 0. 95 Дрожжи 0. 90 Многие кокки Lactobacillus Bacillus 0. 85. Staphyllococcus Basidiomycetes Ascomycetes Debariomyces Saccharomyces bailii 0. 80 0. 75 0. 65 Большинство групп Penicillum Halobacterium Halococcus Wallemia Aspergillus Chrysosporum Saccharomyces rouxii Dunaliella Xeromyces bisporus 5
 Активность воды § § § Зависит от температуры Активность чистой воды равна единице. При взаимодействии воды с поверхностями , анионами и катионами, любыми гидрофильными группами aw становится меньше единице. Значение водной активности снижается при повышении концентрации растворенных веществ. Активность воды может изменяться двумя путями: Осмотическое изменение – происходит в результате взаимодействия молекул воды с растворенными веществами Матричное изменение – обусловлено адсорбцией молекул воды на поверхностях твердых субстратов 6
Активность воды § § § Зависит от температуры Активность чистой воды равна единице. При взаимодействии воды с поверхностями , анионами и катионами, любыми гидрофильными группами aw становится меньше единице. Значение водной активности снижается при повышении концентрации растворенных веществ. Активность воды может изменяться двумя путями: Осмотическое изменение – происходит в результате взаимодействия молекул воды с растворенными веществами Матричное изменение – обусловлено адсорбцией молекул воды на поверхностях твердых субстратов 6
 Активность воды и микроорганизмы МО могут расти на средах со значениями aw =0, 99 -0, 60. n Большинство МО не может расти при aw ниже 0, 95, и не обнаружены МО, растущие при aw ниже 0, 60. n Лучше всех МО при низкой aw растут мицелиальные грибы и дрожжи. n Потребность в воде у МО и толерантность к ее дефициту зависит от сопутствующих экологических факторов и, в частности, от температуры. n Наибольшая устойчивость МО к низким значениям aw наблюдается в условиях температурного оптимума, при отклонении от которого нижний уровень aw повышается. n 7
Активность воды и микроорганизмы МО могут расти на средах со значениями aw =0, 99 -0, 60. n Большинство МО не может расти при aw ниже 0, 95, и не обнаружены МО, растущие при aw ниже 0, 60. n Лучше всех МО при низкой aw растут мицелиальные грибы и дрожжи. n Потребность в воде у МО и толерантность к ее дефициту зависит от сопутствующих экологических факторов и, в частности, от температуры. n Наибольшая устойчивость МО к низким значениям aw наблюдается в условиях температурного оптимума, при отклонении от которого нижний уровень aw повышается. n 7
 На рост МО влияет концентрация растворов, опосредованная влиянием осмотического давления, которое, в свою очередь, изменяет водную активность. В действительности оно складывается на изменении водной активности как меры доступной для организма воды. ЦПМ – полупроницаемая перегородка, через которую вода свободно переходит по градиенту концентрации солей. И если содержание солей вне клетки окажется выше их концентрации в клетке, то вода будет выходить из клетки. n Для того чтобы вода поступала в клетку, цитоплазма должна содержать низкомолекулярные вещества и ионы в более высокой концентрации, чем окружающая клетку среда, ее осмомолярность должна быть выше осмолярности окружающей среды. n 8
На рост МО влияет концентрация растворов, опосредованная влиянием осмотического давления, которое, в свою очередь, изменяет водную активность. В действительности оно складывается на изменении водной активности как меры доступной для организма воды. ЦПМ – полупроницаемая перегородка, через которую вода свободно переходит по градиенту концентрации солей. И если содержание солей вне клетки окажется выше их концентрации в клетке, то вода будет выходить из клетки. n Для того чтобы вода поступала в клетку, цитоплазма должна содержать низкомолекулярные вещества и ионы в более высокой концентрации, чем окружающая клетку среда, ее осмомолярность должна быть выше осмолярности окружающей среды. n 8
 Осмотические свойства растворов Осмолярным называют раствор, содержащий один осмоль вещества в 1 л растворителя. Осмотическое давление осмолярного раствора равно 22, 4 атм при 0 0 С, а температура замерзания раствора при этом снижена на 1, 86 0 С. Способность МО развиваться в средах с широко варьирующей осмолярностью называют осмотолерантностью. Обычно МО растут лучше при значениях аw = 0, 95 -0, 99. Осмофилы проявляют оптимальный рост в условиях пониженной водной активности. Осмофильными обычно называют МО, развивающиеся в средах с высокой концентрацией сахара (мицелиальные грибы, дрожжи, спироплазмы). 9
Осмотические свойства растворов Осмолярным называют раствор, содержащий один осмоль вещества в 1 л растворителя. Осмотическое давление осмолярного раствора равно 22, 4 атм при 0 0 С, а температура замерзания раствора при этом снижена на 1, 86 0 С. Способность МО развиваться в средах с широко варьирующей осмолярностью называют осмотолерантностью. Обычно МО растут лучше при значениях аw = 0, 95 -0, 99. Осмофилы проявляют оптимальный рост в условиях пониженной водной активности. Осмофильными обычно называют МО, развивающиеся в средах с высокой концентрацией сахара (мицелиальные грибы, дрожжи, спироплазмы). 9
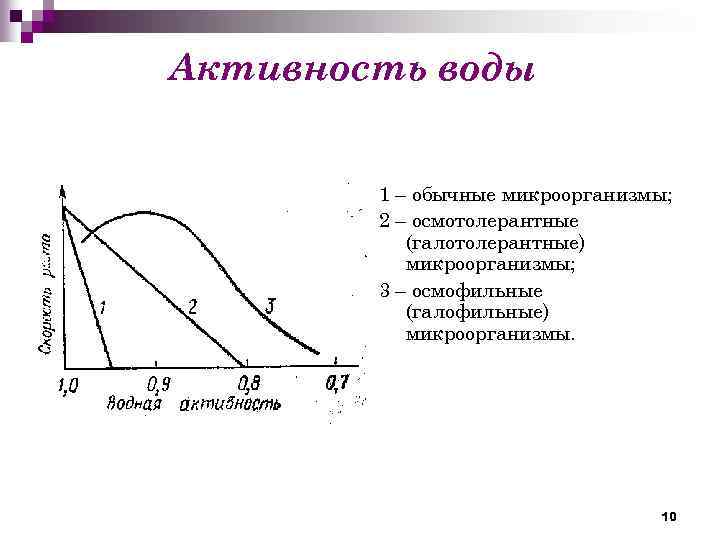 Активность воды 1 – обычные микроорганизмы; 2 – осмотолерантные (галотолерантные) микроорганизмы; 3 – осмофильные (галофильные) микроорганизмы. 10
Активность воды 1 – обычные микроорганизмы; 2 – осмотолерантные (галотолерантные) микроорганизмы; 3 – осмофильные (галофильные) микроорганизмы. 10
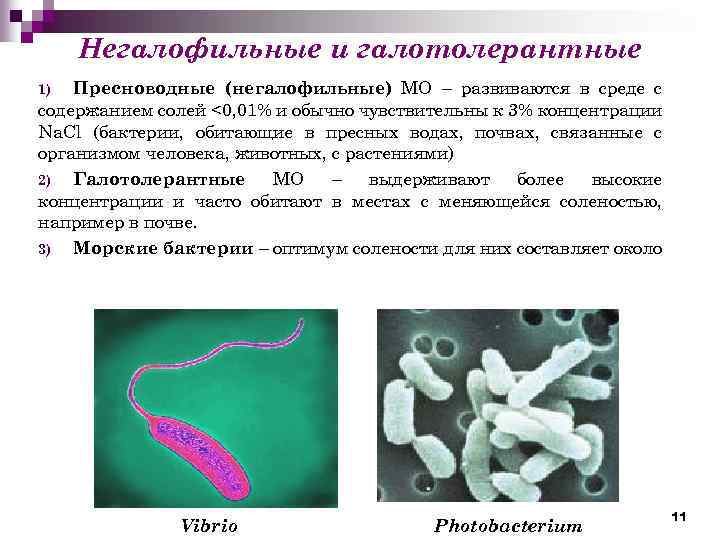 Негалофильные и галотолерантные Пресноводные (негалофильные) МО – развиваются в среде с содержанием солей <0, 01% и обычно чувствительны к 3% концентрации Na. Cl (бактерии, обитающие в пресных водах, почвах, связанные с организмом человека, животных, с растениями) 2) Галотолерантные МО – выдерживают более высокие концентрации и часто обитают в местах с меняющейся соленостью, например в почве. 3) Морские бактерии – оптимум солености для них составляет около 1) Vibrio Photobacterium 11
Негалофильные и галотолерантные Пресноводные (негалофильные) МО – развиваются в среде с содержанием солей <0, 01% и обычно чувствительны к 3% концентрации Na. Cl (бактерии, обитающие в пресных водах, почвах, связанные с организмом человека, животных, с растениями) 2) Галотолерантные МО – выдерживают более высокие концентрации и часто обитают в местах с меняющейся соленостью, например в почве. 3) Морские бактерии – оптимум солености для них составляет около 1) Vibrio Photobacterium 11
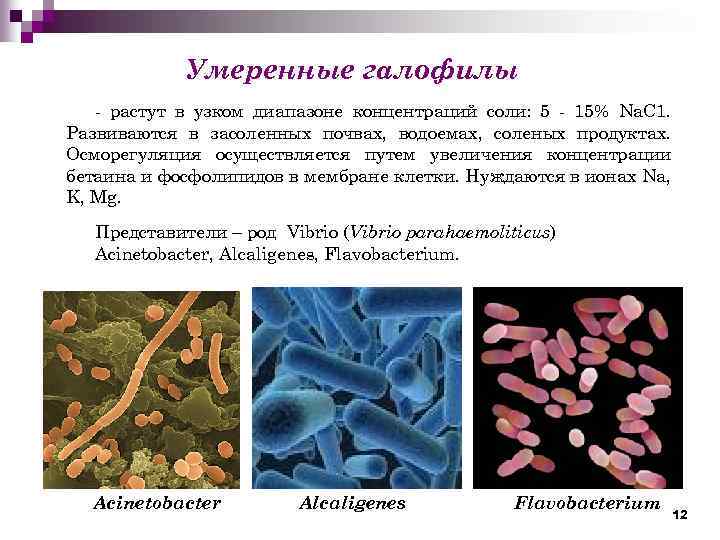 Умеренные галофилы - растут в узком диапазоне концентраций соли: 5 - 15% Na. С 1. Развиваются в засоленных почвах, водоемах, соленых продуктах. Осморегуляция осуществляется путем увеличения концентрации бетаина и фосфолипидов в мембране клетки. Нуждаются в ионах Na, K, Mg. Представители – род Vibrio (Vibrio parahaemoliticus) Acinetobacter, Alcaligenes, Flavobacterium. Acinetobacter Alcaligenes Flavobacterium 12
Умеренные галофилы - растут в узком диапазоне концентраций соли: 5 - 15% Na. С 1. Развиваются в засоленных почвах, водоемах, соленых продуктах. Осморегуляция осуществляется путем увеличения концентрации бетаина и фосфолипидов в мембране клетки. Нуждаются в ионах Na, K, Mg. Представители – род Vibrio (Vibrio parahaemoliticus) Acinetobacter, Alcaligenes, Flavobacterium. Acinetobacter Alcaligenes Flavobacterium 12
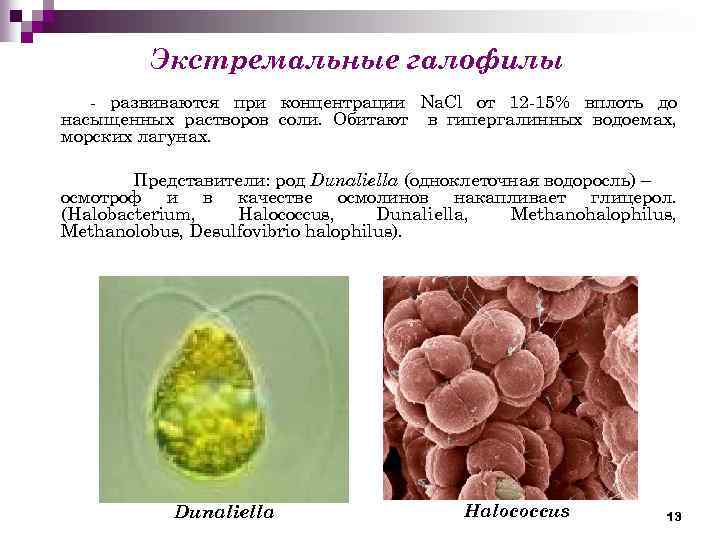 Экстремальные галофилы - развиваются при концентрации Na. Сl от 12 -15% вплоть до насыщенных растворов соли. Обитают в гипергалинных водоемах, морских лагунах. Представители: род Dunaliella (одноклеточная водоросль) – осмотроф и в качестве осмолинов накапливает глицерол. (Halobacterium, Halococcus, Dunaliella, Methanohalophilus, Methanolobus, Desulfovibrio halophilus). Dunaliella Halococcus 13
Экстремальные галофилы - развиваются при концентрации Na. Сl от 12 -15% вплоть до насыщенных растворов соли. Обитают в гипергалинных водоемах, морских лагунах. Представители: род Dunaliella (одноклеточная водоросль) – осмотроф и в качестве осмолинов накапливает глицерол. (Halobacterium, Halococcus, Dunaliella, Methanohalophilus, Methanolobus, Desulfovibrio halophilus). Dunaliella Halococcus 13
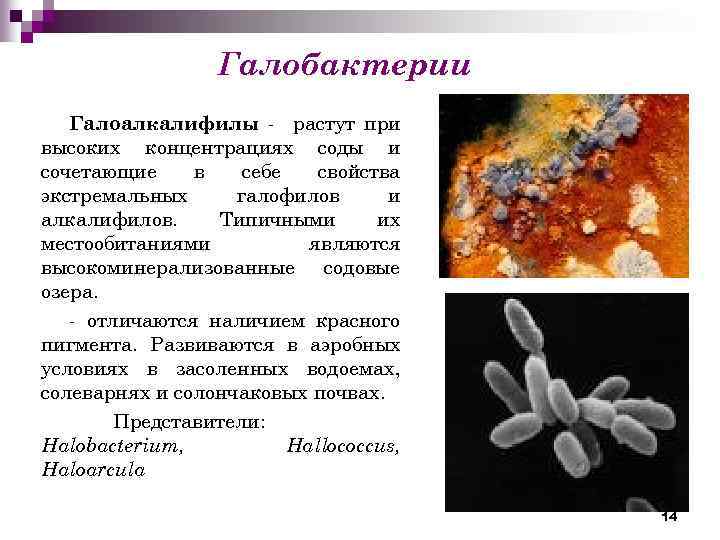 Галобактерии Галоалкалифилы - растут при высоких концентрациях соды и сочетающие в себе свойства экстремальных галофилов и алкалифилов. Типичными их местообитаниями являются высокоминерализованные содовые озера. - отличаются наличием красного пигмента. Развиваются в аэробных условиях в засоленных водоемах, солеварнях и солончаковых почвах. Представители: Halobacterium, Hallococcus, Haloarcula 14
Галобактерии Галоалкалифилы - растут при высоких концентрациях соды и сочетающие в себе свойства экстремальных галофилов и алкалифилов. Типичными их местообитаниями являются высокоминерализованные содовые озера. - отличаются наличием красного пигмента. Развиваются в аэробных условиях в засоленных водоемах, солеварнях и солончаковых почвах. Представители: Halobacterium, Hallococcus, Haloarcula 14
 Осморегуляция микроорганизмов Влияние концентрации раствора на рост опосредовано влиянием осмотического давления. n Для поступления воды в клетку цитоплазма должна содержать низкомолекулярные вещества осмопротекторы (осмолиты) – (это некоторые аминокислоты и их производные, сахара, гетерогликозиды) - и ионы в более высокой концентрации, чем окружающая среда. n Второй распространенной системой осморегуляции в живой природе является система избирательного накопления в клетках ионов К+. n 15
Осморегуляция микроорганизмов Влияние концентрации раствора на рост опосредовано влиянием осмотического давления. n Для поступления воды в клетку цитоплазма должна содержать низкомолекулярные вещества осмопротекторы (осмолиты) – (это некоторые аминокислоты и их производные, сахара, гетерогликозиды) - и ионы в более высокой концентрации, чем окружающая среда. n Второй распространенной системой осморегуляции в живой природе является система избирательного накопления в клетках ионов К+. n 15
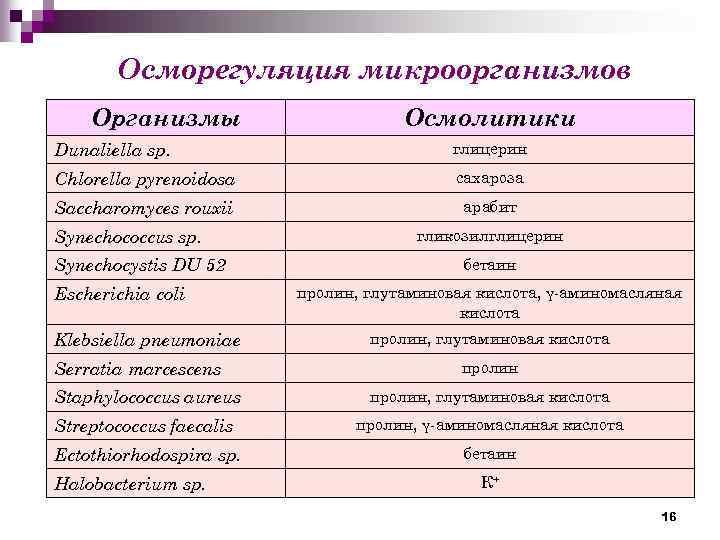 Осморегуляция микроорганизмов Организмы Осмолитики Dunaliella sp. глицерин Chlorella pyrenoidosa сахароза Saccharomyces rouxii арабит Synechococcus sp. Synechocystis DU 52 Escherichia coli Klebsiella pneumoniae Serratia marcescens гликозилглицерин бетаин пролин, глутаминовая кислота, γ-аминомасляная кислота пролин, глутаминовая кислота пролин Staphylococcus aureus пролин, глутаминовая кислота Streptococcus faecalis пролин, γ-аминомасляная кислота Ectothiorhodospira sp. бетаин Halobacterium sp. К+ 16
Осморегуляция микроорганизмов Организмы Осмолитики Dunaliella sp. глицерин Chlorella pyrenoidosa сахароза Saccharomyces rouxii арабит Synechococcus sp. Synechocystis DU 52 Escherichia coli Klebsiella pneumoniae Serratia marcescens гликозилглицерин бетаин пролин, глутаминовая кислота, γ-аминомасляная кислота пролин, глутаминовая кислота пролин Staphylococcus aureus пролин, глутаминовая кислота Streptococcus faecalis пролин, γ-аминомасляная кислота Ectothiorhodospira sp. бетаин Halobacterium sp. К+ 16
 Матричное изменение активности воды В естественных условиях микроорганизмы подвергаются высушиванию, т. е. водному стрессу. постоянно Обычно МО проявляют более высокую чувствительность к матричному стрессу, чем к осмотическому. Бактерии в основном гигрофилы. Для того, чтобы клетка находилась в состоянии тургора и не подвергалась коллапсу, осмолярность в ней должна поддерживаться на достаточно высоком уровне, а водная активность должна быть ниже, чем в среде. Если клетка подвергается осмотическому стрессу, она может поглотить какое-то количество растворенных веществ из окружающей среды и тем самым повысить концентрацию внутренней среды. 17
Матричное изменение активности воды В естественных условиях микроорганизмы подвергаются высушиванию, т. е. водному стрессу. постоянно Обычно МО проявляют более высокую чувствительность к матричному стрессу, чем к осмотическому. Бактерии в основном гигрофилы. Для того, чтобы клетка находилась в состоянии тургора и не подвергалась коллапсу, осмолярность в ней должна поддерживаться на достаточно высоком уровне, а водная активность должна быть ниже, чем в среде. Если клетка подвергается осмотическому стрессу, она может поглотить какое-то количество растворенных веществ из окружающей среды и тем самым повысить концентрацию внутренней среды. 17
 Матричное изменение активности воды МО, которые подвергаются матричному стрессу в среде с низкой концентрацией растворенных веществ, не имеют возможности поглощать осмотически активные вещества. Такие МО должны либо сами синтезировать растворимые вещества de novo, либо осуществлять деструкцию некотороых внутриклеточных макромолекул. На поверхности субстрата удерживается плёночная вода (ОВ>94%). 18
Матричное изменение активности воды МО, которые подвергаются матричному стрессу в среде с низкой концентрацией растворенных веществ, не имеют возможности поглощать осмотически активные вещества. Такие МО должны либо сами синтезировать растворимые вещества de novo, либо осуществлять деструкцию некотороых внутриклеточных макромолекул. На поверхности субстрата удерживается плёночная вода (ОВ>94%). 18
 Матричное изменение активности воды Основными механизмами защиты от высыхания служит образование слизистых капсул или переживающих клеток (спор, конидий, цист). Так, бактерии, живущие на корнях пустынных растений, выделяют значительное колическтво гигроскорической слизи, что способствует обеспечению водой не только самих бактерий, но и растений. Возможность сохранения бактериями жизнеспособности при высушивании определяется множеством факторов, в том числе температуры, соленого состава среды и т. д. Обычно формы с мелкими клетками устойчивее, чем крупноклеточные, кокки устойчивее палочек. Высокую устойчивость на воздухе обнаруживают многие микобактерии с высоким содержанием липидов в клеточной стенке. Бактериальные цисты и споры устойчивее к высушиванию, чем вегетативные клетки. 19
Матричное изменение активности воды Основными механизмами защиты от высыхания служит образование слизистых капсул или переживающих клеток (спор, конидий, цист). Так, бактерии, живущие на корнях пустынных растений, выделяют значительное колическтво гигроскорической слизи, что способствует обеспечению водой не только самих бактерий, но и растений. Возможность сохранения бактериями жизнеспособности при высушивании определяется множеством факторов, в том числе температуры, соленого состава среды и т. д. Обычно формы с мелкими клетками устойчивее, чем крупноклеточные, кокки устойчивее палочек. Высокую устойчивость на воздухе обнаруживают многие микобактерии с высоким содержанием липидов в клеточной стенке. Бактериальные цисты и споры устойчивее к высушиванию, чем вегетативные клетки. 19
 Воздействие р. Н на микроорганизмы Значение р. Н представляет собой отрицательный логарифм концентрации ионов водорода. Кислотность среды является важным фактором, определяющим существование в ней прокариот. Концентрация ионов водорода в окружающей среде действует на организм n прямо (непосредственное воздействие H+ на заряд мембраны и протекание окислительновосстановительных реакций) или n косвенно (через влияние на ионное состояние и доступность многих неорганических ионов и метаболитов, стабильность макромолекул, равновесие электрических зарядов на поверхности клетки). 20
Воздействие р. Н на микроорганизмы Значение р. Н представляет собой отрицательный логарифм концентрации ионов водорода. Кислотность среды является важным фактором, определяющим существование в ней прокариот. Концентрация ионов водорода в окружающей среде действует на организм n прямо (непосредственное воздействие H+ на заряд мембраны и протекание окислительновосстановительных реакций) или n косвенно (через влияние на ионное состояние и доступность многих неорганических ионов и метаболитов, стабильность макромолекул, равновесие электрических зарядов на поверхности клетки). 20
 Воздействие р. Н на микроорганизмы при низких значениях р. Н понижается растворимость углекислоты – источника углерода для автотрофов, а растворимость таких катионов как Сu 2+, Mo 2+, Mg 2+ возрастает и достигает токсичных уровней. n Наоборот, при высоких значениях р. Н растворимость многих катионов, необходимых клетке (Fe 2+, Ca 2+, Mg 2+, Mn 2+), резко понижается, и они становятся недоступными для организма. n От значений р. Н зависит состояние веществ в окружающей среде. Многие органические кислоты в кислой среде находятся в недиссоциированной форме и легко проникают в клетку, становясь токсичными для нее. n Концентрация H+ внешней среды влияет и на равновесие электрических зарядов на поверхности клетки: при низких значениях p. H увеличивается суммарный положительный заряд, при высоких — суммарный отрицательный заряд. n 21
Воздействие р. Н на микроорганизмы при низких значениях р. Н понижается растворимость углекислоты – источника углерода для автотрофов, а растворимость таких катионов как Сu 2+, Mo 2+, Mg 2+ возрастает и достигает токсичных уровней. n Наоборот, при высоких значениях р. Н растворимость многих катионов, необходимых клетке (Fe 2+, Ca 2+, Mg 2+, Mn 2+), резко понижается, и они становятся недоступными для организма. n От значений р. Н зависит состояние веществ в окружающей среде. Многие органические кислоты в кислой среде находятся в недиссоциированной форме и легко проникают в клетку, становясь токсичными для нее. n Концентрация H+ внешней среды влияет и на равновесие электрических зарядов на поверхности клетки: при низких значениях p. H увеличивается суммарный положительный заряд, при высоких — суммарный отрицательный заряд. n 21
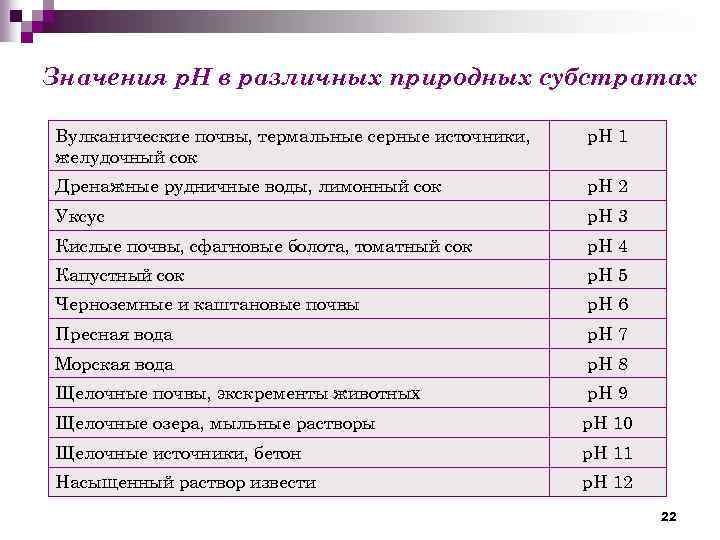 Значения р. Н в различных природных субстратах Вулканические почвы, термальные серные источники, желудочный сок р. Н 1 Дренажные рудничные воды, лимонный сок р. Н 2 Уксус р. Н 3 Кислые почвы, сфагновые болота, томатный сок р. Н 4 Капустный сок р. Н 5 Черноземные и каштановые почвы р. Н 6 Пресная вода р. Н 7 Морская вода р. Н 8 Щелочные почвы, экскременты животных р. Н 9 Щелочные озера, мыльные растворы р. Н 10 Щелочные источники, бетон р. Н 11 Насыщенный раствор извести р. Н 12 22
Значения р. Н в различных природных субстратах Вулканические почвы, термальные серные источники, желудочный сок р. Н 1 Дренажные рудничные воды, лимонный сок р. Н 2 Уксус р. Н 3 Кислые почвы, сфагновые болота, томатный сок р. Н 4 Капустный сок р. Н 5 Черноземные и каштановые почвы р. Н 6 Пресная вода р. Н 7 Морская вода р. Н 8 Щелочные почвы, экскременты животных р. Н 9 Щелочные озера, мыльные растворы р. Н 10 Щелочные источники, бетон р. Н 11 Насыщенный раствор извести р. Н 12 22
 Активная кислотность среды как экологический фактор оказывает сильное влияние на характер и распределение гидробионтов. В морской воде р. Н близок к нейтральному значению. В период максимального фотосинтеза в обычных пресных озерах наблюдаются колебания р. Н от 6, 3 (ночью) до 10, 1 (днем). Водородный показатель может варьироваться в водоемах в очень широких пределах: от р. Н 2 - в вулканических озерах до р. Н 12 - в степных и пустынных содовых озерах. При крайних значениях р. Н формируются ацидофильные или алкалофильные сообщества микроорганизмов. ) 23
Активная кислотность среды как экологический фактор оказывает сильное влияние на характер и распределение гидробионтов. В морской воде р. Н близок к нейтральному значению. В период максимального фотосинтеза в обычных пресных озерах наблюдаются колебания р. Н от 6, 3 (ночью) до 10, 1 (днем). Водородный показатель может варьироваться в водоемах в очень широких пределах: от р. Н 2 - в вулканических озерах до р. Н 12 - в степных и пустынных содовых озерах. При крайних значениях р. Н формируются ацидофильные или алкалофильные сообщества микроорганизмов. ) 23
 Активная кислотность среды как экологический фактор Способность к росту при низких или высоких значениях р. Н обеспечивает организму определенные преимущества, так как в этих условиях мала конкуренция со стороны большинства других организмов. n Однако некоторые бактерии - облигатные формы - не просто переносят высокие концентрации Н+ или ОН-, но и нуждаются в этих ионах для роста и стабильности, т. е. это результат эволюционной адаптации. Так, Thermoplasma acidophilum лизируется при р. Н выше 5, 0. n 24
Активная кислотность среды как экологический фактор Способность к росту при низких или высоких значениях р. Н обеспечивает организму определенные преимущества, так как в этих условиях мала конкуренция со стороны большинства других организмов. n Однако некоторые бактерии - облигатные формы - не просто переносят высокие концентрации Н+ или ОН-, но и нуждаются в этих ионах для роста и стабильности, т. е. это результат эволюционной адаптации. Так, Thermoplasma acidophilum лизируется при р. Н выше 5, 0. n 24
 Кислотность природных субстратов Нейтральные условия – мировой океан и большая часть суши, где концентрация водородных ионов поддерживается в довольно узком диапазоне, оптимальном для роста большинства прокариот. n Умеренно кислые условия ( p. H около 3 – 4) – многие озера, кислые болота, некоторые истощенные почвы. n Экстремально кислые условия – горячие кислые источники и окружающие их горячие кислые почвы, p. H которых может достигать 1. Из этих мест были выделены бактерии, являющиеся одновременно термофилами и ацидофилами (Sulfolobus acidocaldarius). n Щелочные условия обычно связаны с почвами (почвы, обогащенные щелочными минералами, экскрементами животных, разлагающимися белками). Обнаружены также щелочные озера и источники, p. H которых 8 – 11. Из таких мест выделены представители родов Bacillus, Pseudomonas, Flavobacterium, Streptococcus и др. Некоторые из нитрати сульфатвосстанавливающих бактерий могут существовать при p. H выше 11. Цианобактерии обильно растут в природных средах с p. H до 10. n 25
Кислотность природных субстратов Нейтральные условия – мировой океан и большая часть суши, где концентрация водородных ионов поддерживается в довольно узком диапазоне, оптимальном для роста большинства прокариот. n Умеренно кислые условия ( p. H около 3 – 4) – многие озера, кислые болота, некоторые истощенные почвы. n Экстремально кислые условия – горячие кислые источники и окружающие их горячие кислые почвы, p. H которых может достигать 1. Из этих мест были выделены бактерии, являющиеся одновременно термофилами и ацидофилами (Sulfolobus acidocaldarius). n Щелочные условия обычно связаны с почвами (почвы, обогащенные щелочными минералами, экскрементами животных, разлагающимися белками). Обнаружены также щелочные озера и источники, p. H которых 8 – 11. Из таких мест выделены представители родов Bacillus, Pseudomonas, Flavobacterium, Streptococcus и др. Некоторые из нитрати сульфатвосстанавливающих бактерий могут существовать при p. H выше 11. Цианобактерии обильно растут в природных средах с p. H до 10. n 25
 Классификация Границы и оптимальные зоны роста прокариот в зависимости от р. Н 1 -нейтрофилы, 2 -группа кислотоустойчивых и 3 -группа щелочеустойчивых прокариот, 4 -ацидофилы, 5 -алкалофилы. А-облигатные и Б-факультативные формы. Жирной линией выделен оптимальный р. Н роста. 26
Классификация Границы и оптимальные зоны роста прокариот в зависимости от р. Н 1 -нейтрофилы, 2 -группа кислотоустойчивых и 3 -группа щелочеустойчивых прокариот, 4 -ацидофилы, 5 -алкалофилы. А-облигатные и Б-факультативные формы. Жирной линией выделен оптимальный р. Н роста. 26
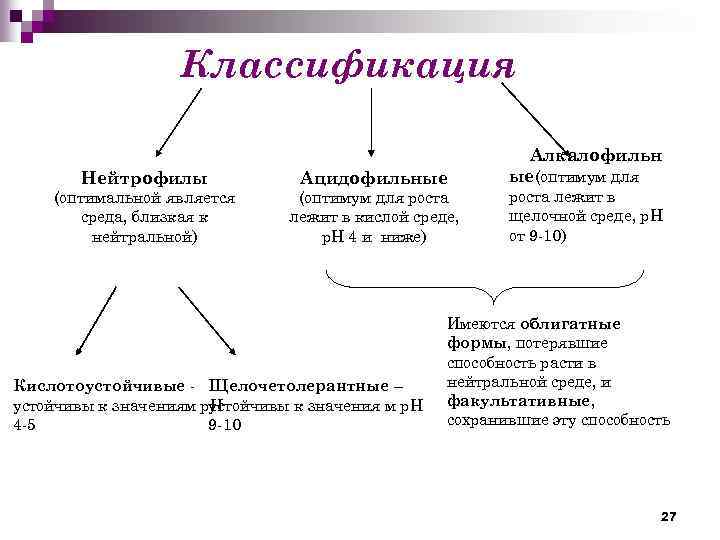 Классификация Нейтрофилы Ацидофильные (оптимальной является среда, близкая к нейтральной) (оптимум для роста лежит в кислой среде, р. Н 4 и ниже) Кислотоустойчивые - Щелочетолерантные – устойчивы к значениям р. Н устойчивы к значения м р. Н 4 -5 9 -10 Алкалофильн ые(оптимум для роста лежит в щелочной среде, р. Н от 9 -10) Имеются облигатные формы, потерявшие способность расти в нейтральной среде, и факультативные, сохранившие эту способность 27
Классификация Нейтрофилы Ацидофильные (оптимальной является среда, близкая к нейтральной) (оптимум для роста лежит в кислой среде, р. Н 4 и ниже) Кислотоустойчивые - Щелочетолерантные – устойчивы к значениям р. Н устойчивы к значения м р. Н 4 -5 9 -10 Алкалофильн ые(оптимум для роста лежит в щелочной среде, р. Н от 9 -10) Имеются облигатные формы, потерявшие способность расти в нейтральной среде, и факультативные, сохранившие эту способность 27
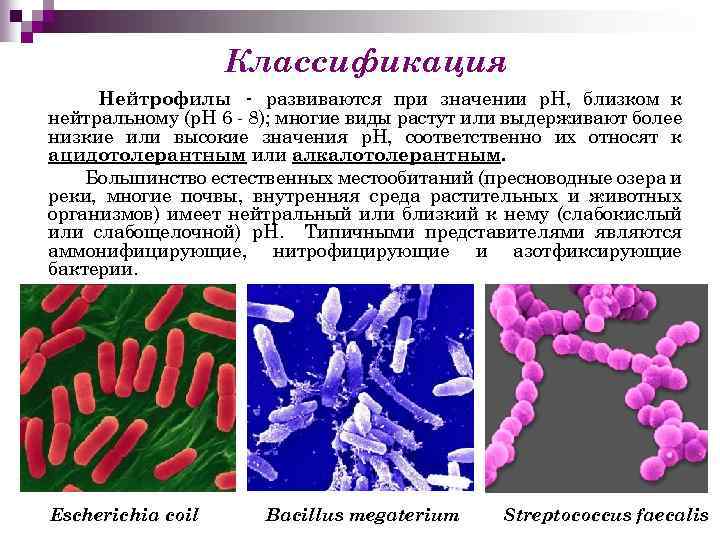 Классификация Нейтрофилы - развиваются при значении р. Н, близком к нейтральному (р. Н 6 - 8); многие виды растут или выдерживают более низкие или высокие значения р. Н, соответственно их относят к ацидотолерантным или алкалотолерантным. Большинство естественных местообитаний (пресноводные озера и реки, многие почвы, внутренняя среда растительных и животных организмов) имеет нейтральный или близкий к нему (слабокислый или слабощелочной) р. Н. Типичными представителями являются аммонифицирующие, нитрофицирующие и азотфиксирующие бактерии. Escherichia coil Bacillus megaterium Streptococcus faecalis
Классификация Нейтрофилы - развиваются при значении р. Н, близком к нейтральному (р. Н 6 - 8); многие виды растут или выдерживают более низкие или высокие значения р. Н, соответственно их относят к ацидотолерантным или алкалотолерантным. Большинство естественных местообитаний (пресноводные озера и реки, многие почвы, внутренняя среда растительных и животных организмов) имеет нейтральный или близкий к нему (слабокислый или слабощелочной) р. Н. Типичными представителями являются аммонифицирующие, нитрофицирующие и азотфиксирующие бактерии. Escherichia coil Bacillus megaterium Streptococcus faecalis
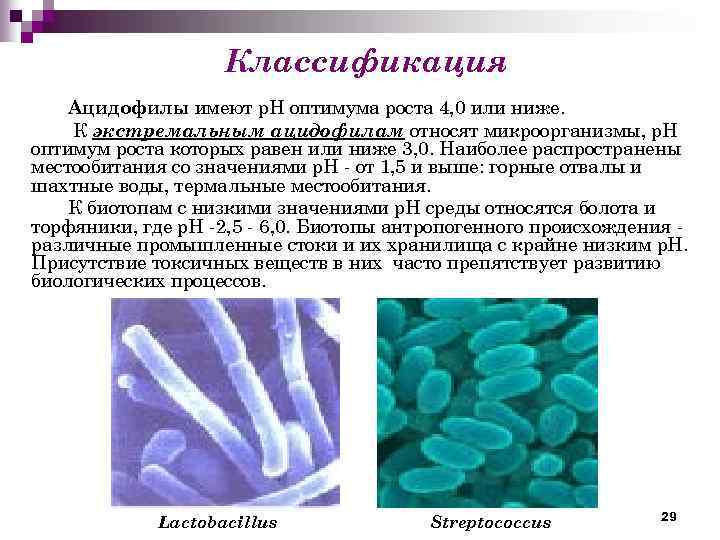 Классификация Ацидофилы имеют р. Н оптимума роста 4, 0 или ниже. К экстремальным ацидофилам относят микроорганизмы, р. Н оптимум роста которых равен или ниже 3, 0. Наиболее распространены местообитания со значениями р. Н - от 1, 5 и выше: горные отвалы и шахтные воды, термальные местообитания. К биотопам с низкими значениями р. Н среды относятся болота и торфяники, где р. Н -2, 5 - 6, 0. Биотопы антропогенного происхождения различные промышленные стоки и их хранилища с крайне низким р. Н. Присутствие токсичных веществ в них часто препятствует развитию биологических процессов. Lactobacillus Streptococcus 29
Классификация Ацидофилы имеют р. Н оптимума роста 4, 0 или ниже. К экстремальным ацидофилам относят микроорганизмы, р. Н оптимум роста которых равен или ниже 3, 0. Наиболее распространены местообитания со значениями р. Н - от 1, 5 и выше: горные отвалы и шахтные воды, термальные местообитания. К биотопам с низкими значениями р. Н среды относятся болота и торфяники, где р. Н -2, 5 - 6, 0. Биотопы антропогенного происхождения различные промышленные стоки и их хранилища с крайне низким р. Н. Присутствие токсичных веществ в них часто препятствует развитию биологических процессов. Lactobacillus Streptococcus 29
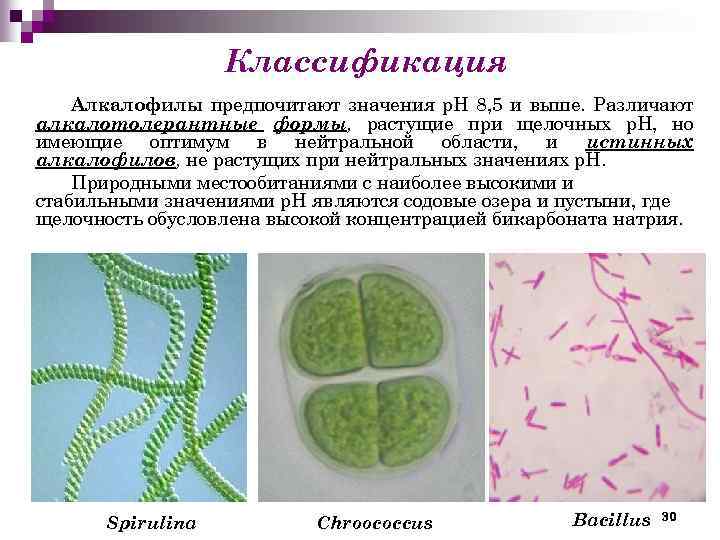 Классификация Алкалофилы предпочитают значения р. Н 8, 5 и выше. Различают алкалотолерантные формы, растущие при щелочных р. Н, но имеющие оптимум в нейтральной области, и истинных алкалофилов, не растущих при нейтральных значениях р. Н. Природными местообитаниями с наиболее высокими и стабильными значениями р. Н являются содовые озера и пустыни, где щелочность обусловлена высокой концентрацией бикарбоната натрия. Spirulina Chroococcus Bacillus 30
Классификация Алкалофилы предпочитают значения р. Н 8, 5 и выше. Различают алкалотолерантные формы, растущие при щелочных р. Н, но имеющие оптимум в нейтральной области, и истинных алкалофилов, не растущих при нейтральных значениях р. Н. Природными местообитаниями с наиболее высокими и стабильными значениями р. Н являются содовые озера и пустыни, где щелочность обусловлена высокой концентрацией бикарбоната натрия. Spirulina Chroococcus Bacillus 30
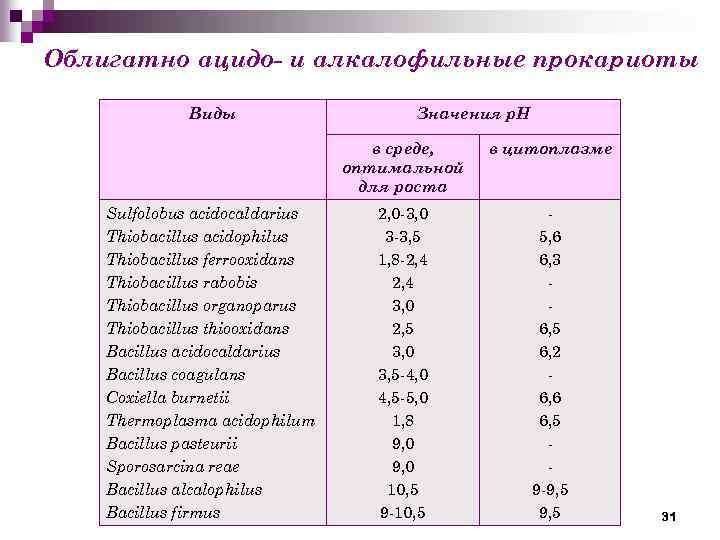 Облигатно ацидо- и алкалофильные прокариоты Виды Значения р. Н в среде, оптимальной для роста Sulfolobus acidocaldarius Thiobacillus acidophilus Thiobacillus ferrooxidans Thiobacillus rabobis Thiobacillus organoparus Thiobacillus thiooxidans Bacillus acidocaldarius Bacillus coagulans Coxiella burnetii Thermoplasma acidophilum Bacillus pasteurii Sporosarcina reae Bacillus alcalophilus Bacillus firmus в цитоплазме 2, 0 -3, 0 3 -3, 5 1, 8 -2, 4 3, 0 2, 5 3, 0 3, 5 -4, 0 4, 5 -5, 0 1, 8 9, 0 10, 5 9 -10, 5 5, 6 6, 3 6, 5 6, 2 6, 6 6, 5 9 -9, 5 31
Облигатно ацидо- и алкалофильные прокариоты Виды Значения р. Н в среде, оптимальной для роста Sulfolobus acidocaldarius Thiobacillus acidophilus Thiobacillus ferrooxidans Thiobacillus rabobis Thiobacillus organoparus Thiobacillus thiooxidans Bacillus acidocaldarius Bacillus coagulans Coxiella burnetii Thermoplasma acidophilum Bacillus pasteurii Sporosarcina reae Bacillus alcalophilus Bacillus firmus в цитоплазме 2, 0 -3, 0 3 -3, 5 1, 8 -2, 4 3, 0 2, 5 3, 0 3, 5 -4, 0 4, 5 -5, 0 1, 8 9, 0 10, 5 9 -10, 5 5, 6 6, 3 6, 5 6, 2 6, 6 6, 5 9 -9, 5 31
 Внутриклеточный р. Н В природе можно наблюдать развитие бактерий при р. Н от 1 до 11, тогда как диапазон значений р. Н их цитоплазмы варьирует в гораздо более узких пределах. У всех известных ацидофилов значение р. Н поддерживается около 6, 5, у нейтрофилов – 7, 5 у алкалофилов – 9, 5. р. Н-гомеостаз – поддержание определенного значения р. Н в цитоплазме клеток Обеспечивается совместным действием n пассивных (низкая проницаемость мембраны для ионов, высокая буферная емкость цитоплазмы) и n активных механизмов (транспорт ионов Н+, К+, Nа+) 32
Внутриклеточный р. Н В природе можно наблюдать развитие бактерий при р. Н от 1 до 11, тогда как диапазон значений р. Н их цитоплазмы варьирует в гораздо более узких пределах. У всех известных ацидофилов значение р. Н поддерживается около 6, 5, у нейтрофилов – 7, 5 у алкалофилов – 9, 5. р. Н-гомеостаз – поддержание определенного значения р. Н в цитоплазме клеток Обеспечивается совместным действием n пассивных (низкая проницаемость мембраны для ионов, высокая буферная емкость цитоплазмы) и n активных механизмов (транспорт ионов Н+, К+, Nа+) 32
 Алкалофильные бактерии растут с наибольшей скоростью при р. Н 8 -11 и в связи с этим обладают тремя особенностями. Первая особенность – это свойство поддержания р. Н цитоплазмы на физиологическом уровне в щелочной среде. Это достигается благодаря наличию в цитоплазме буферных систем, которая обеспечивает содержание в ней нуклеиновых кислот и белков, а также пулов глутамата и полиаминов. В основном буферную емкость обеспечивают фосфатные группы в составе РНК и ДНК (в нейтральном диапазоне) и основные или кислые боковые цепи аминокислот в составе белков при крайних значениях р. Н. n 33
Алкалофильные бактерии растут с наибольшей скоростью при р. Н 8 -11 и в связи с этим обладают тремя особенностями. Первая особенность – это свойство поддержания р. Н цитоплазмы на физиологическом уровне в щелочной среде. Это достигается благодаря наличию в цитоплазме буферных систем, которая обеспечивает содержание в ней нуклеиновых кислот и белков, а также пулов глутамата и полиаминов. В основном буферную емкость обеспечивают фосфатные группы в составе РНК и ДНК (в нейтральном диапазоне) и основные или кислые боковые цепи аминокислот в составе белков при крайних значениях р. Н. n 33
 Вторая особенность алкалофилов ферменты, находящиеся на поверхности клетки или секретируемые в окружающую среду, устойчивы к денатурирующему влиянию щелочной среды. Так, большее содержание остатков аргинина во внеклеточной сериновой протеазе может сдвинуть оптимум р. Н в более щелочную сторону. Убедительно доказано наличие у алкалофилов ферментов, устойчивых к высоким значениям р. Н; эти ферменты используются при производстве детергентов. n 34
Вторая особенность алкалофилов ферменты, находящиеся на поверхности клетки или секретируемые в окружающую среду, устойчивы к денатурирующему влиянию щелочной среды. Так, большее содержание остатков аргинина во внеклеточной сериновой протеазе может сдвинуть оптимум р. Н в более щелочную сторону. Убедительно доказано наличие у алкалофилов ферментов, устойчивых к высоким значениям р. Н; эти ферменты используются при производстве детергентов. n 34
 Третья особенность алкалофилов образование на мембране градиента р. Н с кислым полюсом внутри клетки нейтрализует мембранный потенциал последовательно, снижает протондвижущую силу, которая обеспечивает синтез АТР при дыхании. У ацидофильных и нейтрофильных бактерий внутренний р. Н выше и градиент р. Н термодинамически дополняет протондвижущую силу. Низкая проницаемость цитоплазматической мембраны для протонов и других ионов обеспечивает адаптацию при высоких значениях р. Н среды. Na+/H+антипорт является универсальным механизмом для создания ионных градиентов и поддержания р. Нгомеостаза у алкалофилов. n 35
Третья особенность алкалофилов образование на мембране градиента р. Н с кислым полюсом внутри клетки нейтрализует мембранный потенциал последовательно, снижает протондвижущую силу, которая обеспечивает синтез АТР при дыхании. У ацидофильных и нейтрофильных бактерий внутренний р. Н выше и градиент р. Н термодинамически дополняет протондвижущую силу. Низкая проницаемость цитоплазматической мембраны для протонов и других ионов обеспечивает адаптацию при высоких значениях р. Н среды. Na+/H+антипорт является универсальным механизмом для создания ионных градиентов и поддержания р. Нгомеостаза у алкалофилов. n 35
 Третья особенность алкалофилов Протонная помпа и системы транспорта Nа+ служат основными механизмами регуляции р. Н у бактерий, обитающих в щелочных средах; они согласованно действуют для понижения р. Н цитоплазмы. Это обеспечивается транспортом ионов натрия, в котором участвуют по меньшей мере три системы. У алкалофильных бактерий образование обратного градиента р. Н на мембране компенсируется высокой величиной мембранного потенциала или сопряжением транспорта электронов с выделением из клеток Na+ для поддержания гомеостаза р. Н и запасания энергии. 36
Третья особенность алкалофилов Протонная помпа и системы транспорта Nа+ служат основными механизмами регуляции р. Н у бактерий, обитающих в щелочных средах; они согласованно действуют для понижения р. Н цитоплазмы. Это обеспечивается транспортом ионов натрия, в котором участвуют по меньшей мере три системы. У алкалофильных бактерий образование обратного градиента р. Н на мембране компенсируется высокой величиной мембранного потенциала или сопряжением транспорта электронов с выделением из клеток Na+ для поддержания гомеостаза р. Н и запасания энергии. 36
 Регуляция р. Н среды Жизнедеятельность МО часто может приводить к изменению р. Н среды. n Так, к подкислению среды ведут окисление сульфидов до серной кислоты тионовыми бактериями, процессы нитрификации, многие брожения. n В некоторых случаях бактерии могут регулировать р. Н среды за счет изменения метаболизма. Наиболее известным примером является двухфазность брожения, подробно изученная на примере ацетоно-бутилового брожения (Clostridium acetobutilicum): при снижении р. Н до критическоо уровня в результате выделения масляной кислоты бактерия переключаеься на образование нейтральных продуктов, ацетона и бутанола. n 37
Регуляция р. Н среды Жизнедеятельность МО часто может приводить к изменению р. Н среды. n Так, к подкислению среды ведут окисление сульфидов до серной кислоты тионовыми бактериями, процессы нитрификации, многие брожения. n В некоторых случаях бактерии могут регулировать р. Н среды за счет изменения метаболизма. Наиболее известным примером является двухфазность брожения, подробно изученная на примере ацетоно-бутилового брожения (Clostridium acetobutilicum): при снижении р. Н до критическоо уровня в результате выделения масляной кислоты бактерия переключаеься на образование нейтральных продуктов, ацетона и бутанола. n 37
 Трансмембранный электрохимический потенциал Ведущую роль в поддержании р. Н-гомеостаза играют протонные помпы. Работа протонных помп связана с образованием трансмембранного электрохимическоо потенциала, который состоит из электрического (∆ψ) и химического (∆р. Н) компонентов: ∆μн+ = ∆ψ - Z∆р. Н n n ∆μн+ - трансмембранный электрохимический потенциал ∆ψ - трансмембранная разность электрического потенциала ∆р. Н - градиент концентрации Н+ Z – коэффициент для перевода единиц р. Н в милливольты, Z=2, 303 RT/F=-60 м. В при 25 °С (R – газовая константа, T – абсолютная температура, F – число Фарадея). 38
Трансмембранный электрохимический потенциал Ведущую роль в поддержании р. Н-гомеостаза играют протонные помпы. Работа протонных помп связана с образованием трансмембранного электрохимическоо потенциала, который состоит из электрического (∆ψ) и химического (∆р. Н) компонентов: ∆μн+ = ∆ψ - Z∆р. Н n n ∆μн+ - трансмембранный электрохимический потенциал ∆ψ - трансмембранная разность электрического потенциала ∆р. Н - градиент концентрации Н+ Z – коэффициент для перевода единиц р. Н в милливольты, Z=2, 303 RT/F=-60 м. В при 25 °С (R – газовая константа, T – абсолютная температура, F – число Фарадея). 38
 Трансмембранный электрохимический потенциал Значения ∆µн+ и его составляющих ∆ψ и ∆р. Н различаются у нейтрофилов, ацидофилов и алкалофилов. n У нейтрофилов ∆˜µн+ в среднем равен - 170 м. В и представлен обеими компонентами-∆ψ и ∆р. Н. n У ацидофилов ∆˜µН+ имеет высокие значения 270 м. В. Однако протондвижущая сила представлена главным образом одной своей составляющей - ∆р. Н; ∆ψ имеет низкие значения, а внутренняя поверхность цитоплазматической мембраны заряжена положительно. n У алкалофильных бактерий - ∆µн+ равен -50 м. В. Протондвижущая сила представлена главным образом одной своей составляющей ∆ψ, а ∆р. Н имеет очень низкие значения и обратный знак, т. е. концентрация Н+ в цитоплазме выше, чем в окружающей клетку среде. . n Таким образом, биоэнергетика прокариот зависит от экологического фактора -р. Н окружающей среды n Биоэнергетика ацидофилов (а), нейтрофилов (б), алкалофилов (в). 39
Трансмембранный электрохимический потенциал Значения ∆µн+ и его составляющих ∆ψ и ∆р. Н различаются у нейтрофилов, ацидофилов и алкалофилов. n У нейтрофилов ∆˜µн+ в среднем равен - 170 м. В и представлен обеими компонентами-∆ψ и ∆р. Н. n У ацидофилов ∆˜µН+ имеет высокие значения 270 м. В. Однако протондвижущая сила представлена главным образом одной своей составляющей - ∆р. Н; ∆ψ имеет низкие значения, а внутренняя поверхность цитоплазматической мембраны заряжена положительно. n У алкалофильных бактерий - ∆µн+ равен -50 м. В. Протондвижущая сила представлена главным образом одной своей составляющей ∆ψ, а ∆р. Н имеет очень низкие значения и обратный знак, т. е. концентрация Н+ в цитоплазме выше, чем в окружающей клетку среде. . n Таким образом, биоэнергетика прокариот зависит от экологического фактора -р. Н окружающей среды n Биоэнергетика ацидофилов (а), нейтрофилов (б), алкалофилов (в). 39
 Трансмембранный электрохимический потенциал Оптимальный рост E. coli наблюдается в диапазоне р. Н 6 -8, в котором ∆µн+ также мало зависит от р. Н среды, как и интенсивность дыхания клеток, что подтверждает постоянство работы протонных помп. Значение ∆˜µн+ при р. Н 6 и 8 равно -200 и -140 м. В соответственно. Однако составляющие ∆˜µн+ сильно зависят от р. Н среды. Для обеспечения клеток энергией протонные помпы ориентированы на выброс Н+ в среду. Одновременно с ним функционируют помпы, переносящие Н+ в клетку и скорость работы этих насосов зависит от изменения р. Н в среде. Это катион Н+помпы: Na+/H+- и К+/Н+-антипорт. 40
Трансмембранный электрохимический потенциал Оптимальный рост E. coli наблюдается в диапазоне р. Н 6 -8, в котором ∆µн+ также мало зависит от р. Н среды, как и интенсивность дыхания клеток, что подтверждает постоянство работы протонных помп. Значение ∆˜µн+ при р. Н 6 и 8 равно -200 и -140 м. В соответственно. Однако составляющие ∆˜µн+ сильно зависят от р. Н среды. Для обеспечения клеток энергией протонные помпы ориентированы на выброс Н+ в среду. Одновременно с ним функционируют помпы, переносящие Н+ в клетку и скорость работы этих насосов зависит от изменения р. Н в среде. Это катион Н+помпы: Na+/H+- и К+/Н+-антипорт. 40


