лекция 4 -Т лф - копия.ppt
- Количество слайдов: 70
 Лекция 4 Т-ЛИМФОЦИТЫ
Лекция 4 Т-ЛИМФОЦИТЫ
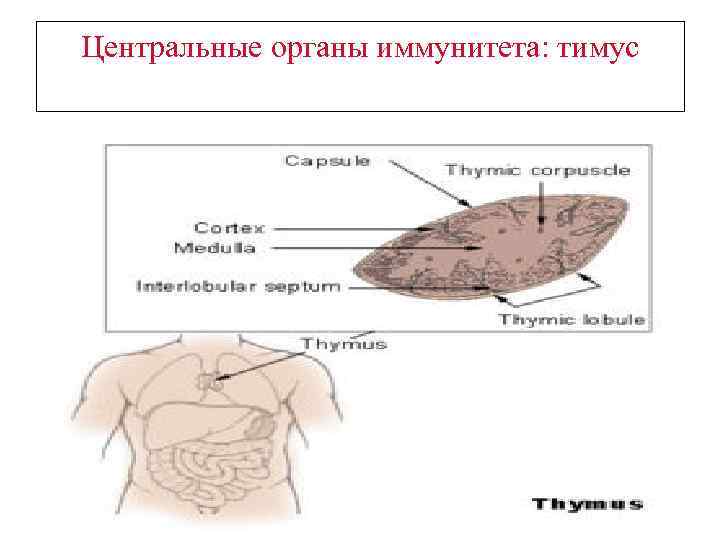 Центральные органы иммунитета: тимус
Центральные органы иммунитета: тимус
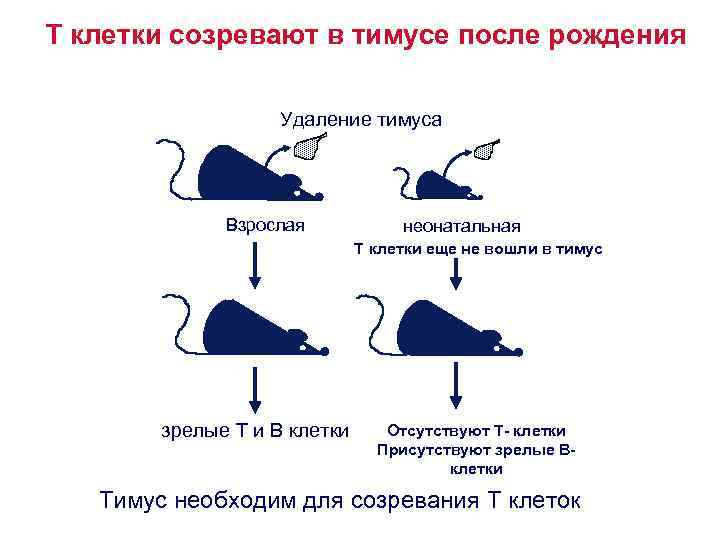 Т клетки созревают в тимусе после рождения Удаление тимуса Взрослая неонатальная T клетки еще не вошли в тимус зрелые T и B клетки Отсутствуют Т- клетки Присутствуют зрелые Вклетки Тимус необходим для созревания T клеток
Т клетки созревают в тимусе после рождения Удаление тимуса Взрослая неонатальная T клетки еще не вошли в тимус зрелые T и B клетки Отсутствуют Т- клетки Присутствуют зрелые Вклетки Тимус необходим для созревания T клеток
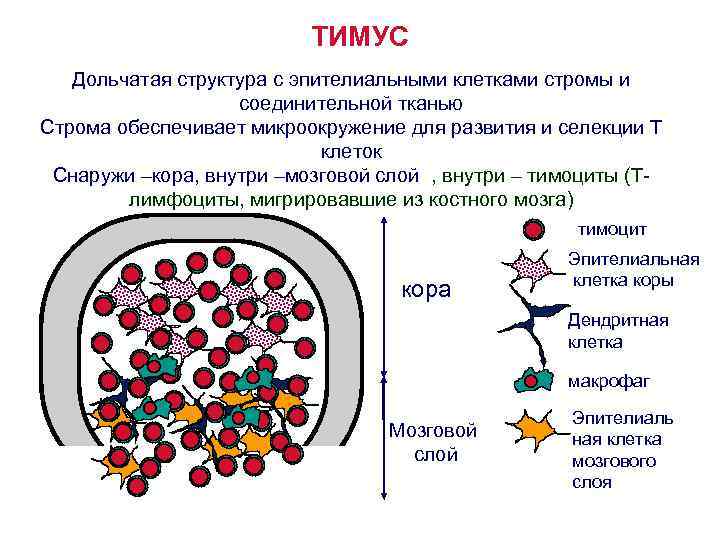 ТИМУС Дольчатая структура с эпителиальными клетками стромы и соединительной тканью Строма обеспечивает микроокружение для развития и селекции Т клеток Снаружи –кора, внутри –мозговой слой , внутри – тимоциты (Тлимфоциты, мигрировавшие из костного мозга) тимоцит кора Эпителиальная клетка коры Дендритная клетка макрофаг Мозговой слой Эпителиаль ная клетка мозгового слоя
ТИМУС Дольчатая структура с эпителиальными клетками стромы и соединительной тканью Строма обеспечивает микроокружение для развития и селекции Т клеток Снаружи –кора, внутри –мозговой слой , внутри – тимоциты (Тлимфоциты, мигрировавшие из костного мозга) тимоцит кора Эпителиальная клетка коры Дендритная клетка макрофаг Мозговой слой Эпителиаль ная клетка мозгового слоя
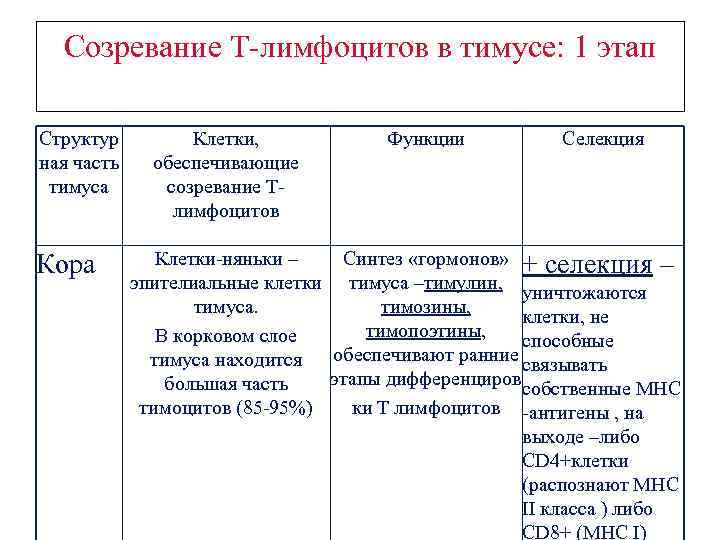 Созревание Т-лимфоцитов в тимусе: 1 этап Структур ная часть тимуса Кора Клетки, обеспечивающие созревание Тлимфоцитов Функции Селекция Клетки-няньки – Синтез «гормонов» + селекция – эпителиальные клетки тимуса –тимулин, уничтожаются тимуса. тимозины, клетки, не тимопоэтины, В корковом слое способные обеспечивают ранние связывать тимуса находится этапы дифференцировсобственные МНС большая часть тимоцитов (85 -95%) ки Т лимфоцитов -антигены , на выходе –либо CD 4+клетки (распознают МНС II класса ) либо CD 8+ (МНС I)
Созревание Т-лимфоцитов в тимусе: 1 этап Структур ная часть тимуса Кора Клетки, обеспечивающие созревание Тлимфоцитов Функции Селекция Клетки-няньки – Синтез «гормонов» + селекция – эпителиальные клетки тимуса –тимулин, уничтожаются тимуса. тимозины, клетки, не тимопоэтины, В корковом слое способные обеспечивают ранние связывать тимуса находится этапы дифференцировсобственные МНС большая часть тимоцитов (85 -95%) ки Т лимфоцитов -антигены , на выходе –либо CD 4+клетки (распознают МНС II класса ) либо CD 8+ (МНС I)
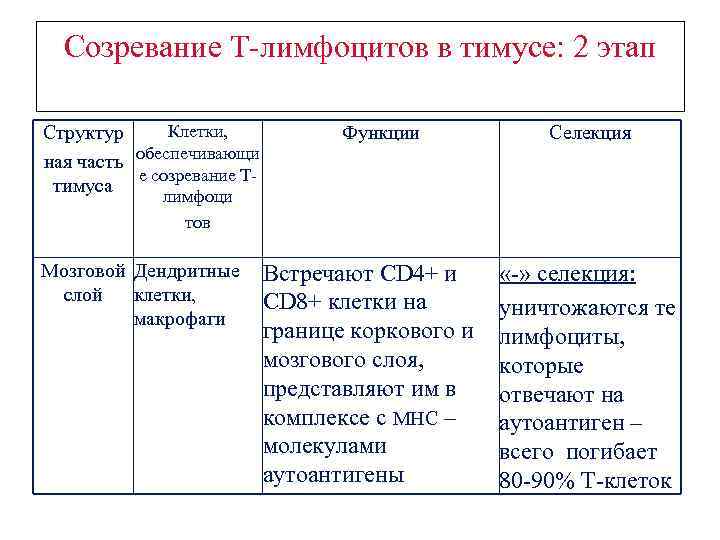 Созревание Т-лимфоцитов в тимусе: 2 этап Клетки, Структур ная часть обеспечивающи е созревание Ттимуса Функции Селекция лимфоци тов Мозговой Дендритные слой клетки, макрофаги Встречают CD 4+ и CD 8+ клетки на границе коркового и мозгового слоя, представляют им в комплексе с МНС – молекулами аутоантигены «-» селекция: уничтожаются те лимфоциты, которые отвечают на аутоантиген – всего погибает 80 -90% Т-клеток
Созревание Т-лимфоцитов в тимусе: 2 этап Клетки, Структур ная часть обеспечивающи е созревание Ттимуса Функции Селекция лимфоци тов Мозговой Дендритные слой клетки, макрофаги Встречают CD 4+ и CD 8+ клетки на границе коркового и мозгового слоя, представляют им в комплексе с МНС – молекулами аутоантигены «-» селекция: уничтожаются те лимфоциты, которые отвечают на аутоантиген – всего погибает 80 -90% Т-клеток
 Интенсивность отбора тимоцитов • T клетки созревают в тимусе, но гораздо больше Т- клеток погибает в тимусе. • 98% клеток погибает в тимусе без развития воспаления и изменения размеров тимуса. • Макрофаги тимуса фагоцитируют апоптозные тимоциты.
Интенсивность отбора тимоцитов • T клетки созревают в тимусе, но гораздо больше Т- клеток погибает в тимусе. • 98% клеток погибает в тимусе без развития воспаления и изменения размеров тимуса. • Макрофаги тимуса фагоцитируют апоптозные тимоциты.
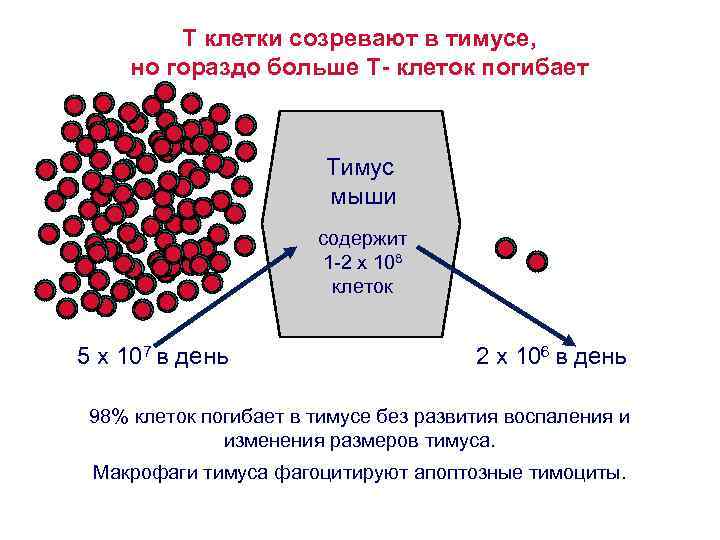 T клетки созревают в тимусе, но гораздо больше Т- клеток погибает Тимус мыши содержит 1 -2 x 108 клеток 5 x 107 в день 2 x 106 в день 98% клеток погибает в тимусе без развития воспаления и изменения размеров тимуса. Макрофаги тимуса фагоцитируют апоптозные тимоциты.
T клетки созревают в тимусе, но гораздо больше Т- клеток погибает Тимус мыши содержит 1 -2 x 108 клеток 5 x 107 в день 2 x 106 в день 98% клеток погибает в тимусе без развития воспаления и изменения размеров тимуса. Макрофаги тимуса фагоцитируют апоптозные тимоциты.
 Двойное распознавание – «свое» и «чужое» • T клетки способны развиваться только в том случае, если их Tc. R распознают часть собственных молекул MHC. • Tc. R способны распознавать собственные антигены – молекулы главного комплекса гистосовместимости (МНС), ассоциированные с фрагментами чужеродных АГ. • MHC молекулы участвуют в активации Т клеток.
Двойное распознавание – «свое» и «чужое» • T клетки способны развиваться только в том случае, если их Tc. R распознают часть собственных молекул MHC. • Tc. R способны распознавать собственные антигены – молекулы главного комплекса гистосовместимости (МНС), ассоциированные с фрагментами чужеродных АГ. • MHC молекулы участвуют в активации Т клеток.
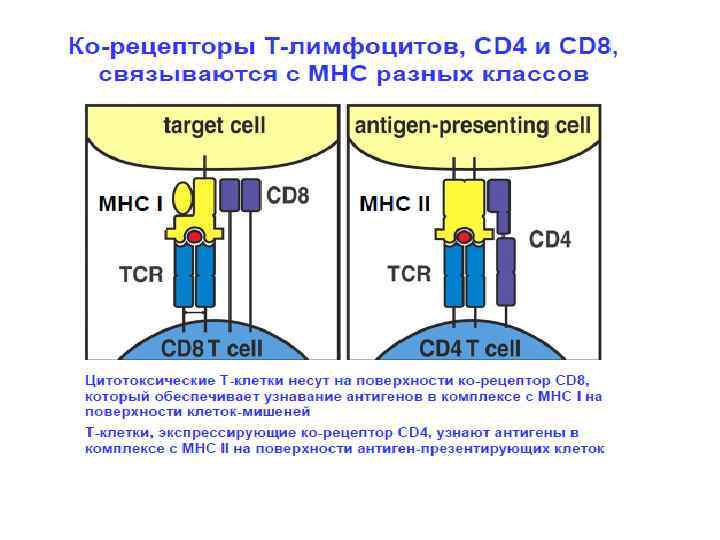
 Процесс созревания тимоцитов: этапы формирования корецепторов • • Корецепторы: CD 4 – распознает молекулы МНС 2 класса CD 8 – распознает молекулы МНС 1 класса В коре находятся незрелые двойные негативные (CD 3/Tc. R-CD 4 - 8 -) и двойные позитивные тимоциты (CD 3/Tc. R- CD 4+ 8+), при переходе в мозговой слой клетки теряют либо CD 4, либо CD 8 молекулы и становятся однопозитивными • В мозговом слое - зрелые однопозитивные тимоциты, их 2 типа: • либо (CD 3+ Tc. R CD 4+) –Т –хелперы • либо (CD 3+ Tc. R CD 8+) –Т –цитотоксические клетки
Процесс созревания тимоцитов: этапы формирования корецепторов • • Корецепторы: CD 4 – распознает молекулы МНС 2 класса CD 8 – распознает молекулы МНС 1 класса В коре находятся незрелые двойные негативные (CD 3/Tc. R-CD 4 - 8 -) и двойные позитивные тимоциты (CD 3/Tc. R- CD 4+ 8+), при переходе в мозговой слой клетки теряют либо CD 4, либо CD 8 молекулы и становятся однопозитивными • В мозговом слое - зрелые однопозитивные тимоциты, их 2 типа: • либо (CD 3+ Tc. R CD 4+) –Т –хелперы • либо (CD 3+ Tc. R CD 8+) –Т –цитотоксические клетки
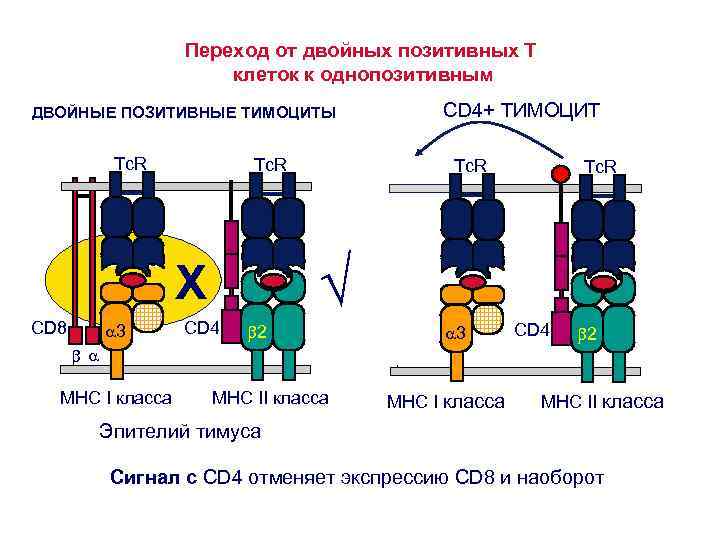 Переход от двойных позитивных Т клеток к однопозитивным CD 4+ ТИМОЦИТ ДВОЙНЫЕ ПОЗИТИВНЫЕ ТИМОЦИТЫ Tc. R 3 Tc. R √ X CD 8 Tc. R CD 4 2 CD 8 3 CD 4 2 MHC I класса MHC II класса Эпителий тимуса Сигнал с CD 4 отменяет экспрессию CD 8 и наоборот
Переход от двойных позитивных Т клеток к однопозитивным CD 4+ ТИМОЦИТ ДВОЙНЫЕ ПОЗИТИВНЫЕ ТИМОЦИТЫ Tc. R 3 Tc. R √ X CD 8 Tc. R CD 4 2 CD 8 3 CD 4 2 MHC I класса MHC II класса Эпителий тимуса Сигнал с CD 4 отменяет экспрессию CD 8 и наоборот
 Строение Т рецепторов • Т клеточный рецептор имеет и -цепи (есть альтернативные рецепторы, которые имеют и цепи- обеспечивают иммунитет слизистых оболочек, первичный ответ при инфекции). • Каждая и цепь в составе Т рецептора имеет: • 1 наружный вариабельный Vдомен и и 1 наружный константный Cдомен • Трансмембранный сегмент • Цитоплазматический хвостик (короткий)
Строение Т рецепторов • Т клеточный рецептор имеет и -цепи (есть альтернативные рецепторы, которые имеют и цепи- обеспечивают иммунитет слизистых оболочек, первичный ответ при инфекции). • Каждая и цепь в составе Т рецептора имеет: • 1 наружный вариабельный Vдомен и и 1 наружный константный Cдомен • Трансмембранный сегмент • Цитоплазматический хвостик (короткий)
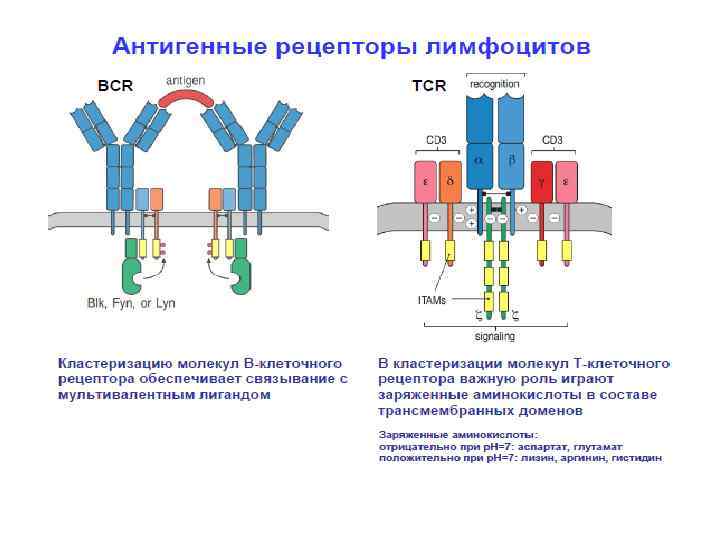
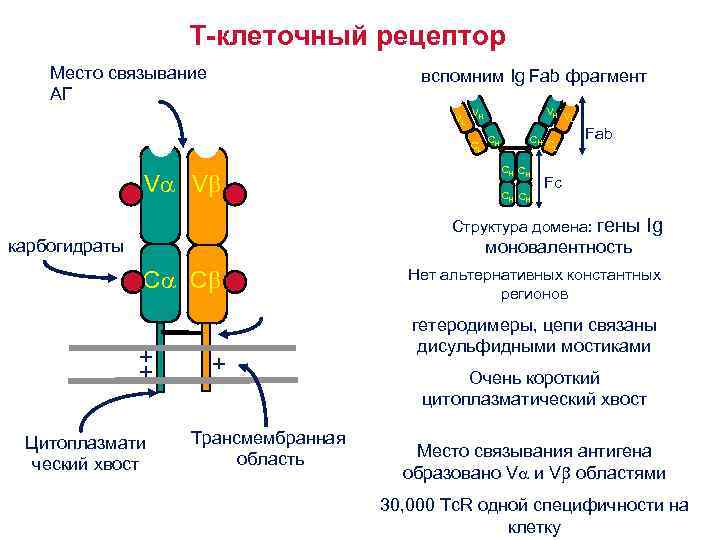 Т-клеточный рецептор Место связывание АГ вспомним Ig Fab фрагмент VL CL V V VH V L VH CH CH CH CL Fab Fc Структура домена: гены карбогидраты моновалентность C C + + Цитоплазмати ческий хвост + Трансмембранная область Ig Нет альтернативных константных регионов гетеродимеры, цепи связаны дисульфидными мостиками Очень короткий цитоплазматический хвост Место связывания антигена образовано V и V областями 30, 000 Tc. R одной специфичности на клетку
Т-клеточный рецептор Место связывание АГ вспомним Ig Fab фрагмент VL CL V V VH V L VH CH CH CH CL Fab Fc Структура домена: гены карбогидраты моновалентность C C + + Цитоплазмати ческий хвост + Трансмембранная область Ig Нет альтернативных константных регионов гетеродимеры, цепи связаны дисульфидными мостиками Очень короткий цитоплазматический хвост Место связывания антигена образовано V и V областями 30, 000 Tc. R одной специфичности на клетку
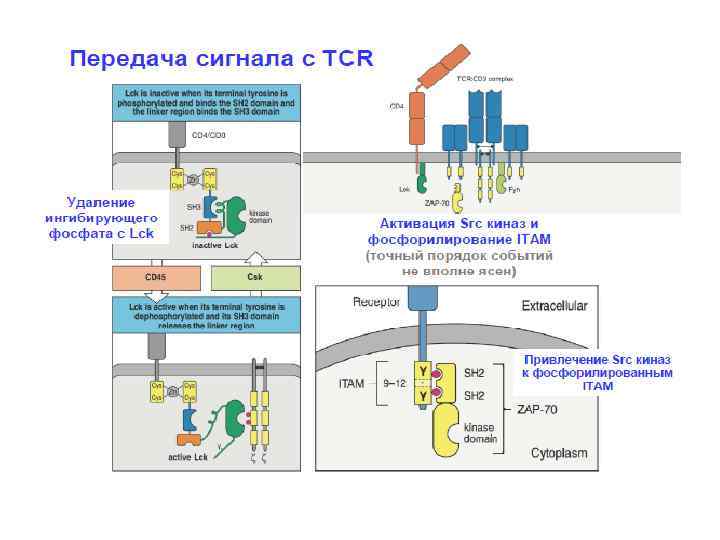
 Строение Т рецепторного комплекса • На клеточной поверхности -Т клеточный рецептор (или ) расположен в непосредственной близости к комплексу, называемому CD 3. • Через комплекс CD 3 происходит передача сигнала с Т клеточного рецептора в клетку.
Строение Т рецепторного комплекса • На клеточной поверхности -Т клеточный рецептор (или ) расположен в непосредственной близости к комплексу, называемому CD 3. • Через комплекс CD 3 происходит передача сигнала с Т клеточного рецептора в клетку.
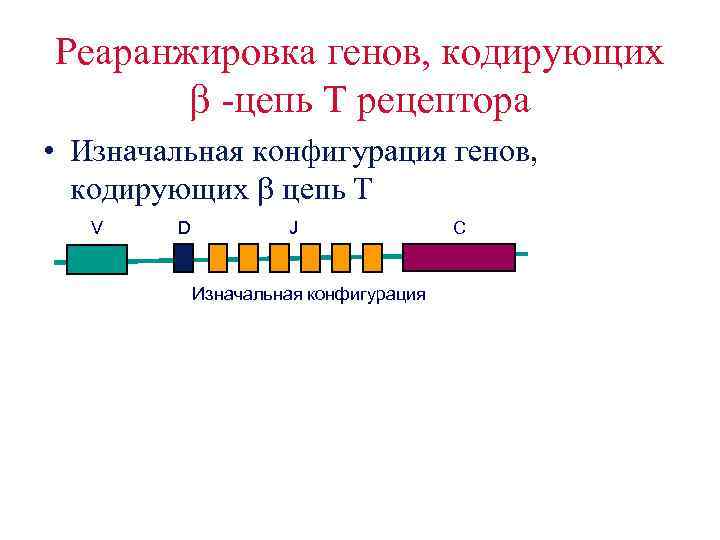 Реаранжировка генов, кодирующих -цепь Т рецептора • Изначальная конфигурация генов, кодирующих цепь Т V D J Изначальная конфигурация C
Реаранжировка генов, кодирующих -цепь Т рецептора • Изначальная конфигурация генов, кодирующих цепь Т V D J Изначальная конфигурация C
 Реаранжировка генов, кодирующих Т рецептор, путем соматической рекомбинации • 1 этап – слияние генов D-J • 2 этап - слияние генов V-DJ • 3 этап – сборка цепи V D J C V DJ C V-DJ слияние D-J слияние
Реаранжировка генов, кодирующих Т рецептор, путем соматической рекомбинации • 1 этап – слияние генов D-J • 2 этап - слияние генов V-DJ • 3 этап – сборка цепи V D J C V DJ C V-DJ слияние D-J слияние
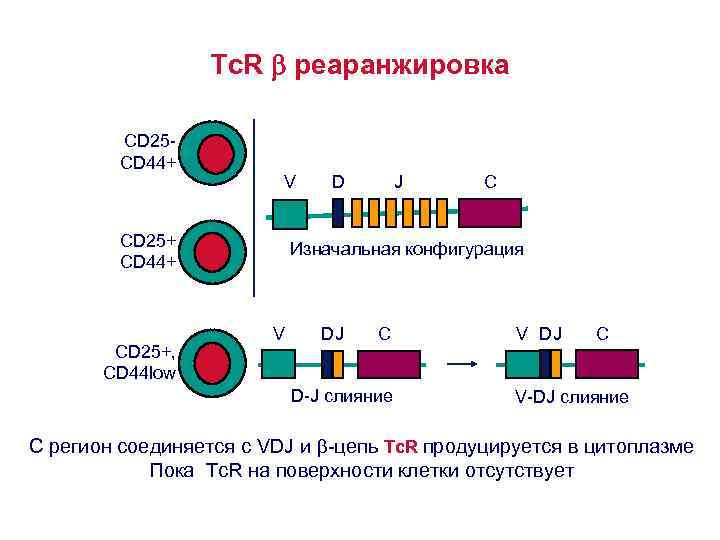 Tc. R реаранжировка CD 25 CD 44+ V CD 25+ CD 44+ CD 25+, CD 44 low D J C Изначальная конфигурация V DJ C D-J слияние V DJ C V-DJ слияние C регион соединяется с VDJ и -цепь Tc. R продуцируется в цитоплазме Пока Tc. R на поверхности клетки отсутствует
Tc. R реаранжировка CD 25 CD 44+ V CD 25+ CD 44+ CD 25+, CD 44 low D J C Изначальная конфигурация V DJ C D-J слияние V DJ C V-DJ слияние C регион соединяется с VDJ и -цепь Tc. R продуцируется в цитоплазме Пока Tc. R на поверхности клетки отсутствует
 Реаранжировка генов, кодирующих -цепь Т рецептора, сборка Т рецептора • Те же этапы, что и при перестройке генов -цепи. • По окончании реаранжировки генов цепи происходит считывание м РНК , построение белков, совместная сборка и цепей, экспрессия на поверхностную мембрану Т- рецепторного комплекса. • T клетки уже могут распознать антиген и взаимодействовать с молекулами MHC I и II классов через корецепторы - CD 4 и CD 8. • После этого начинается селекция
Реаранжировка генов, кодирующих -цепь Т рецептора, сборка Т рецептора • Те же этапы, что и при перестройке генов -цепи. • По окончании реаранжировки генов цепи происходит считывание м РНК , построение белков, совместная сборка и цепей, экспрессия на поверхностную мембрану Т- рецепторного комплекса. • T клетки уже могут распознать антиген и взаимодействовать с молекулами MHC I и II классов через корецепторы - CD 4 и CD 8. • После этого начинается селекция
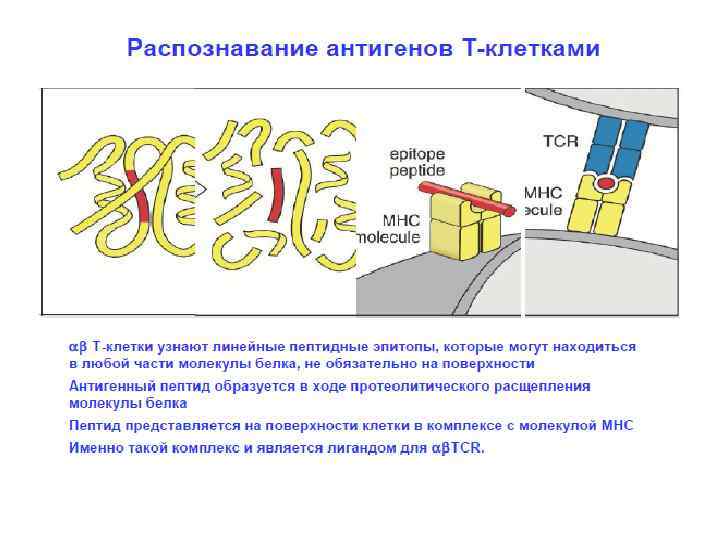
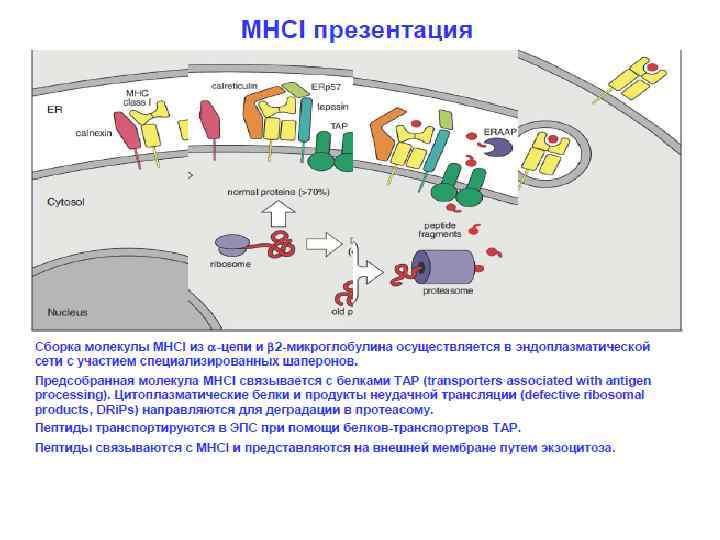
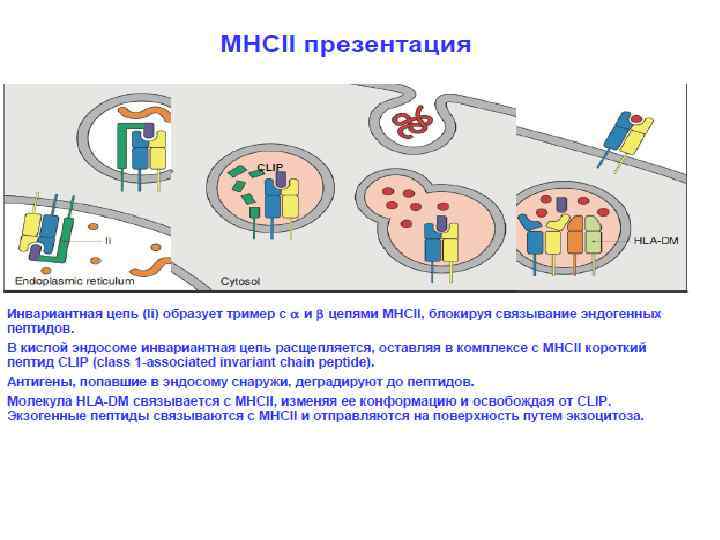
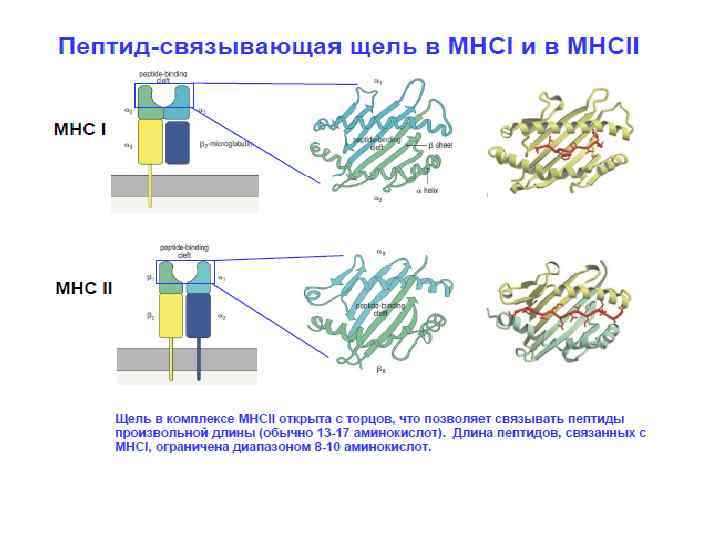

 Антигены и суперантигены: различные механизмы презентации и распознавания антигены суперантигены Требуется процессинг до пептидов Не процессируются Tc. R и цепи участвуют в распознавании презентируются молекулами MHC I или. II класса Большинство белков антигены только Tc. R цепь участвует в распознавании Презентируются в основном молекулами MHC II класса Очень небольшое число антигенов суперантигены
Антигены и суперантигены: различные механизмы презентации и распознавания антигены суперантигены Требуется процессинг до пептидов Не процессируются Tc. R и цепи участвуют в распознавании презентируются молекулами MHC I или. II класса Большинство белков антигены только Tc. R цепь участвует в распознавании Презентируются в основном молекулами MHC II класса Очень небольшое число антигенов суперантигены
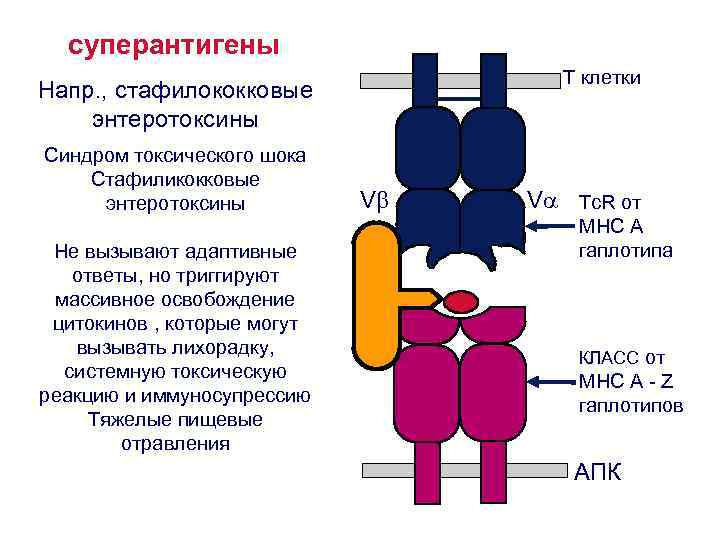 суперантигены T клетки Напр. , стафилококковые энтеротоксины Синдром токсического шока Стафиликокковые энтеротоксины Не вызывают адаптивные ответы, но триггируют массивное освобождение цитокинов , которые могут вызывать лихорадку, системную токсическую реакцию и иммуносупрессию Тяжелые пищевые отравления V V Tc. R от MHC A гаплотипа КЛАСС от MHC A - Z гаплотипов АПК
суперантигены T клетки Напр. , стафилококковые энтеротоксины Синдром токсического шока Стафиликокковые энтеротоксины Не вызывают адаптивные ответы, но триггируют массивное освобождение цитокинов , которые могут вызывать лихорадку, системную токсическую реакцию и иммуносупрессию Тяжелые пищевые отравления V V Tc. R от MHC A гаплотипа КЛАСС от MHC A - Z гаплотипов АПК

 Каким образом развивается аутотолерантность к антигенам, отсутствующим в тимусе? • T клетки, несущие Tc. R , и вступающие во взаимодействие с антигенами тимуса, уничтожаются (отрицательная селекция). • Но! Некоторые аутоантигены не экспрессируются в тимусе – т. е. с ними тимоцит встретится впервые, когда он выйдет на периферию. • Вывод: клеточная толерантность должна развиваться и вне тимуса.
Каким образом развивается аутотолерантность к антигенам, отсутствующим в тимусе? • T клетки, несущие Tc. R , и вступающие во взаимодействие с антигенами тимуса, уничтожаются (отрицательная селекция). • Но! Некоторые аутоантигены не экспрессируются в тимусе – т. е. с ними тимоцит встретится впервые, когда он выйдет на периферию. • Вывод: клеточная толерантность должна развиваться и вне тимуса.
 Механизмы формирования периферической толерантность или анергии Антигенпрезентирующие клетки не выполняют функцию костимуляции, т. е. не передают сигналы активации Т клеткам, вступившим в контакт с антигеном.
Механизмы формирования периферической толерантность или анергии Антигенпрезентирующие клетки не выполняют функцию костимуляции, т. е. не передают сигналы активации Т клеткам, вступившим в контакт с антигеном.
 Костимуляция: АПК – Т лимфоцит 1. Костимулирующие молекулы- члены семейства B 7 (CD 80 и CD 86) экспрессируются на большинстве АПК, включая, клетки Лангерганса, моноциты/макрофаги, В клетки и др. , но не клетками, которые не обладают функциями иммунорегуляции – такими, как мышечные, нервные клетки , гепатоциты, эпителиальные клетки и др. 2. Молекулы семейства B 7 (CD 80 и CD 86) на АПК связываются с молекулой CD 28 на поверхности Т клетки.
Костимуляция: АПК – Т лимфоцит 1. Костимулирующие молекулы- члены семейства B 7 (CD 80 и CD 86) экспрессируются на большинстве АПК, включая, клетки Лангерганса, моноциты/макрофаги, В клетки и др. , но не клетками, которые не обладают функциями иммунорегуляции – такими, как мышечные, нервные клетки , гепатоциты, эпителиальные клетки и др. 2. Молекулы семейства B 7 (CD 80 и CD 86) на АПК связываются с молекулой CD 28 на поверхности Т клетки.
 Механизм костимуляции Т клеток • На покоящихся Т клетках экспрессируются низкоаффинные рецепторы к интерлейкину -2 (IL 2 R) – его и цепи, но не -цепь. • После стимуляции Т лимфоцита, активируются гены, кодирующие -цепь. • Экспрессия -цепи IL 2 R превращает IL 2 рецептор в высокоаффинную форму. • Костимулирующие сигналы активируют ядерные факторы транскрипции , это приводит к повышению продукции интерлейкина -2 более, чем в 100 раз. • Связывание IL 2 R с IL 2 запускает процесс пролиферации Т лимфоцитов, т. е. клональную экспансию.
Механизм костимуляции Т клеток • На покоящихся Т клетках экспрессируются низкоаффинные рецепторы к интерлейкину -2 (IL 2 R) – его и цепи, но не -цепь. • После стимуляции Т лимфоцита, активируются гены, кодирующие -цепь. • Экспрессия -цепи IL 2 R превращает IL 2 рецептор в высокоаффинную форму. • Костимулирующие сигналы активируют ядерные факторы транскрипции , это приводит к повышению продукции интерлейкина -2 более, чем в 100 раз. • Связывание IL 2 R с IL 2 запускает процесс пролиферации Т лимфоцитов, т. е. клональную экспансию.
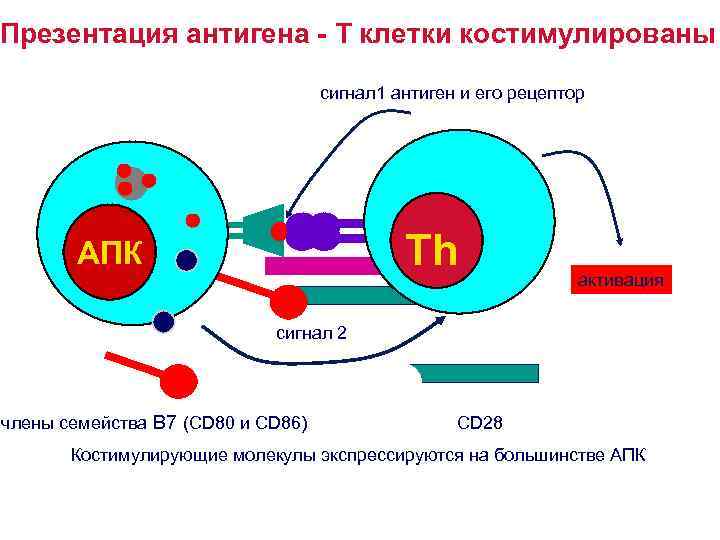 Презентация антигена - T клетки костимулированы сигнал 1 антиген и его рецептор Th АПК активация сигнал 2 члены семейства B 7 (CD 80 и CD 86) CD 28 Костимулирующие молекулы экспрессируются на большинстве АПК
Презентация антигена - T клетки костимулированы сигнал 1 антиген и его рецептор Th АПК активация сигнал 2 члены семейства B 7 (CD 80 и CD 86) CD 28 Костимулирующие молекулы экспрессируются на большинстве АПК
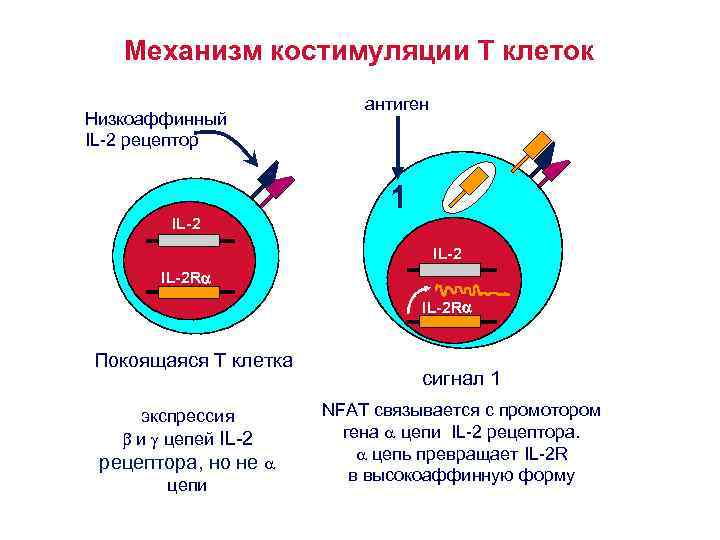 Механизм костимуляции Т клеток Низкоаффинный IL-2 рецептор антиген 1 IL-2 R Покоящаяся Т клетка экспрессия и цепей IL-2 рецептора, но не цепи сигнал 1 NFAT связывается с промотором гена цепи IL-2 рецептора. цепь превращает IL-2 R в высокоаффинную форму
Механизм костимуляции Т клеток Низкоаффинный IL-2 рецептор антиген 1 IL-2 R Покоящаяся Т клетка экспрессия и цепей IL-2 рецептора, но не цепи сигнал 1 NFAT связывается с промотором гена цепи IL-2 рецептора. цепь превращает IL-2 R в высокоаффинную форму
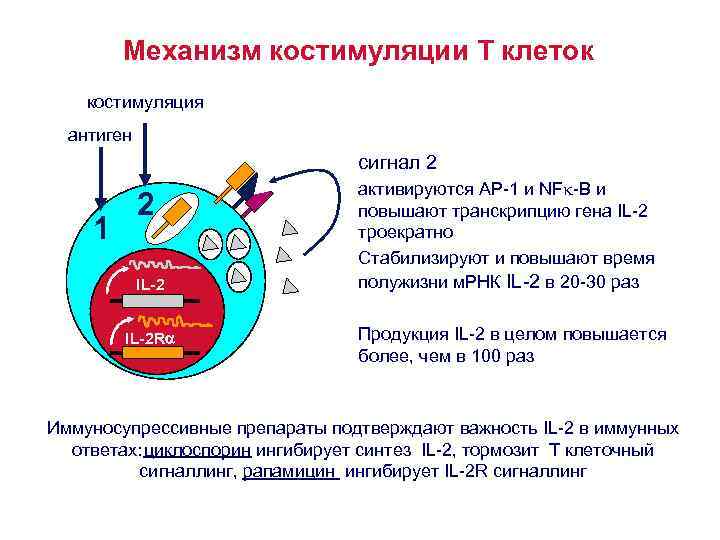 Механизм костимуляции Т клеток костимуляция антиген сигнал 2 1 2 IL-2 R активируются AP-1 и NFk-B и повышают транскрипцию гена IL-2 троекратно Стабилизируют и повышают время полужизни м. РНК IL-2 в 20 -30 раз Продукция IL-2 в целом повышается более, чем в 100 раз Иммуносупрессивные препараты подтверждают важность IL-2 в иммунных ответах: циклоспорин ингибирует синтез IL-2, тормозит Т клеточный сигналлинг, рапамицин ингибирует IL-2 R сигналлинг
Механизм костимуляции Т клеток костимуляция антиген сигнал 2 1 2 IL-2 R активируются AP-1 и NFk-B и повышают транскрипцию гена IL-2 троекратно Стабилизируют и повышают время полужизни м. РНК IL-2 в 20 -30 раз Продукция IL-2 в целом повышается более, чем в 100 раз Иммуносупрессивные препараты подтверждают важность IL-2 в иммунных ответах: циклоспорин ингибирует синтез IL-2, тормозит Т клеточный сигналлинг, рапамицин ингибирует IL-2 R сигналлинг
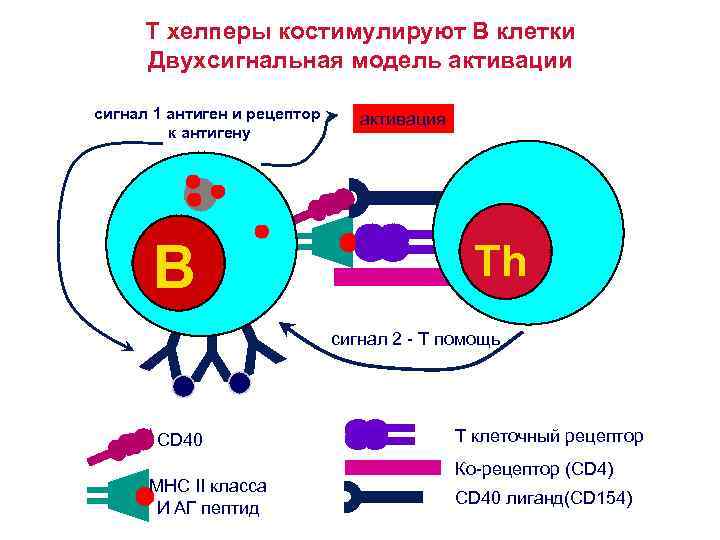 T хелперы костимулируют В клетки Двухсигнальная модель активации сигнал 1 антиген и рецептор к антигену B Y YY CD 40 MHC II класса И АГ пептид активация Th сигнал 2 - T помощь T клеточный рецептор Ко-рецептор (CD 4) CD 40 лиганд(CD 154)
T хелперы костимулируют В клетки Двухсигнальная модель активации сигнал 1 антиген и рецептор к антигену B Y YY CD 40 MHC II класса И АГ пептид активация Th сигнал 2 - T помощь T клеточный рецептор Ко-рецептор (CD 4) CD 40 лиганд(CD 154)
 Анергия (неотвечаемость) развивается при отсутствии сигналов костимуляции • Если Т клетка получает только 1 сигнал – антиген+МНС, который распознается Т клеточным рецептором, но при этом не получает костимулирующих сигналов, она не способна к активации. • В этом случае Т-клетка не способна продуцировать IL-2 и поэтому не способна пролиферировать и подвергаться клональной селекции.
Анергия (неотвечаемость) развивается при отсутствии сигналов костимуляции • Если Т клетка получает только 1 сигнал – антиген+МНС, который распознается Т клеточным рецептором, но при этом не получает костимулирующих сигналов, она не способна к активации. • В этом случае Т-клетка не способна продуцировать IL-2 и поэтому не способна пролиферировать и подвергаться клональной селекции.
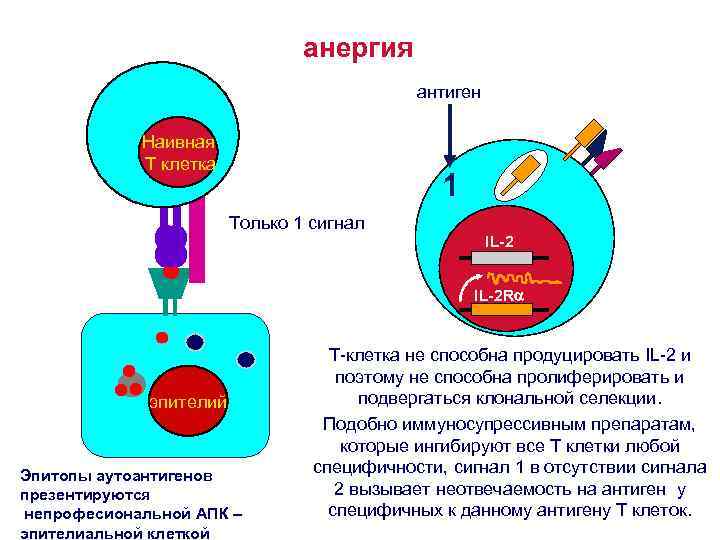 анергия антиген Наивная Т клетка 1 Только 1 сигнал IL-2 R эпителий Эпитопы аутоантигенов презентируются непрофесиональной АПК – эпителиальной клеткой Т-клетка не способна продуцировать IL-2 и поэтому не способна пролиферировать и подвергаться клональной селекции. Подобно иммуносупрессивным препаратам, которые ингибируют все Т клетки любой специфичности, сигнал 1 в отсутствии сигнала 2 вызывает неотвечаемость на антиген у специфичных к данному антигену Т клеток.
анергия антиген Наивная Т клетка 1 Только 1 сигнал IL-2 R эпителий Эпитопы аутоантигенов презентируются непрофесиональной АПК – эпителиальной клеткой Т-клетка не способна продуцировать IL-2 и поэтому не способна пролиферировать и подвергаться клональной селекции. Подобно иммуносупрессивным препаратам, которые ингибируют все Т клетки любой специфичности, сигнал 1 в отсутствии сигнала 2 вызывает неотвечаемость на антиген у специфичных к данному антигену Т клеток.
 Гипотеза угрозы • Выполнение эффекторных функций Т клеток, либо их толерантность зависят от того, когда и где экспрессируются костимулирующие молекулы. • Если нет сигналов тревоги, Т клетки остаются толерантными.
Гипотеза угрозы • Выполнение эффекторных функций Т клеток, либо их толерантность зависят от того, когда и где экспрессируются костимулирующие молекулы. • Если нет сигналов тревоги, Т клетки остаются толерантными.
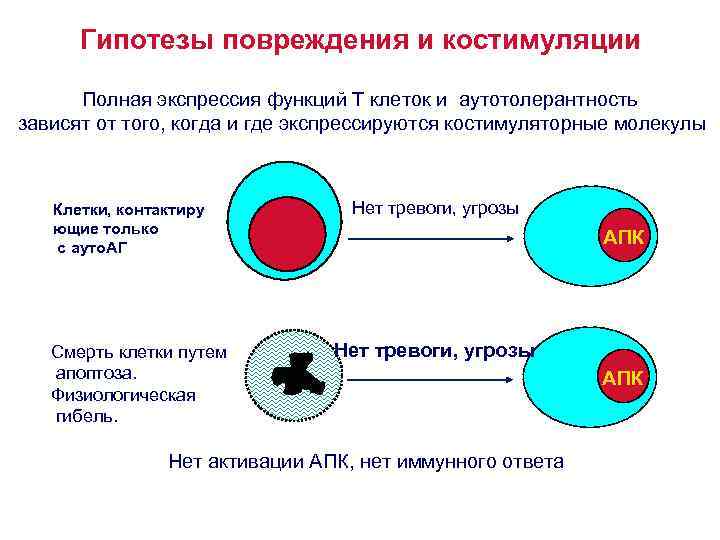 Гипотезы повреждения и костимуляции Полная экспрессия функций Т клеток и аутотолерантность зависят от того, когда и где экспрессируются костимуляторные молекулы Клетки, контактиру ющие только с ауто. АГ Смерть клетки путем апоптоза. Физиологическая гибель. Нет тревоги, угрозы АПК Нет тревоги, угрозы Нет активации АПК, нет иммунного ответа АПК
Гипотезы повреждения и костимуляции Полная экспрессия функций Т клеток и аутотолерантность зависят от того, когда и где экспрессируются костимуляторные молекулы Клетки, контактиру ющие только с ауто. АГ Смерть клетки путем апоптоза. Физиологическая гибель. Нет тревоги, угрозы АПК Нет тревоги, угрозы Нет активации АПК, нет иммунного ответа АПК
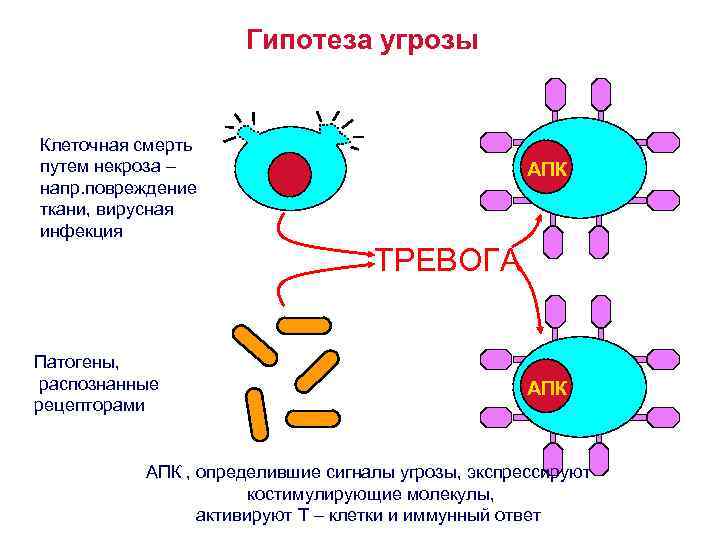 Гипотеза угрозы Клеточная смерть путем некроза – напр. повреждение ткани, вирусная инфекция АПК ТРЕВОГА Патогены, распознанные рецепторами АПК , определившие сигналы угрозы, экспрессируют костимулирующие молекулы, активируют Т – клетки и иммунный ответ
Гипотеза угрозы Клеточная смерть путем некроза – напр. повреждение ткани, вирусная инфекция АПК ТРЕВОГА Патогены, распознанные рецепторами АПК , определившие сигналы угрозы, экспрессируют костимулирующие молекулы, активируют Т – клетки и иммунный ответ
 Соотношение гипотезы сигналов тревоги, угрозы, опасности, повреждения с иммунологической догмой распознавания «свое –не свое» • Антигены вызывают толерантность или иммунный ответ в зависимости от того, способна ли иммунная система воспринимать их как тревожные, угрожающие , а не как «свои они или не свои» ЭТО НЕ ИСКЛЮЧАЕТ ВАЖНОСТИ РАСПОЗНАВАНИЯ «Свое –несвое» , НО ГИПОТЕЗА СИГНАЛОВ ТРЕВОГИ, ПОВРЕЖДЕНИЯ, УГРОЗЫ, ОПАСНОСТИ, пока не подтверждена экспериментально
Соотношение гипотезы сигналов тревоги, угрозы, опасности, повреждения с иммунологической догмой распознавания «свое –не свое» • Антигены вызывают толерантность или иммунный ответ в зависимости от того, способна ли иммунная система воспринимать их как тревожные, угрожающие , а не как «свои они или не свои» ЭТО НЕ ИСКЛЮЧАЕТ ВАЖНОСТИ РАСПОЗНАВАНИЯ «Свое –несвое» , НО ГИПОТЕЗА СИГНАЛОВ ТРЕВОГИ, ПОВРЕЖДЕНИЯ, УГРОЗЫ, ОПАСНОСТИ, пока не подтверждена экспериментально
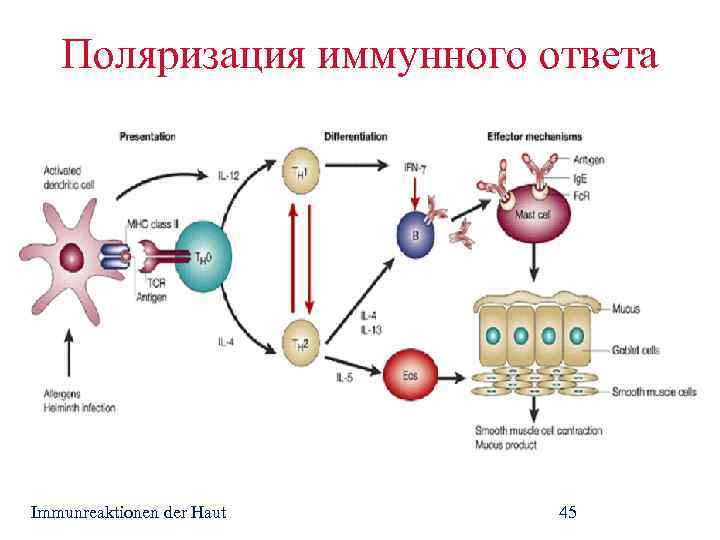 Поляризация иммунного ответа Immunreaktionen der Haut 45
Поляризация иммунного ответа Immunreaktionen der Haut 45
 2. Усиление реакций адаптивного иммунного ответа: активация, пролиферация и дифференцировка лимфоцитов цитокин эффект ИЛ-2 Пролиферация и созревание Т-клеток, повышение уровня экспрессии рецептора к ИЛ-2 ИЛ-4 Повышение уровня экспрессии молекул МНС II класса, Fc-рецепторов и рецепторов к ИЛ-2 на поверхности Т- и В-лимфоцитов. Способствует переключению классов Ig на Ig. Eизотип. ИЛ-6 Созревание и дифференцировка Т- и В-лимфоцитов
2. Усиление реакций адаптивного иммунного ответа: активация, пролиферация и дифференцировка лимфоцитов цитокин эффект ИЛ-2 Пролиферация и созревание Т-клеток, повышение уровня экспрессии рецептора к ИЛ-2 ИЛ-4 Повышение уровня экспрессии молекул МНС II класса, Fc-рецепторов и рецепторов к ИЛ-2 на поверхности Т- и В-лимфоцитов. Способствует переключению классов Ig на Ig. Eизотип. ИЛ-6 Созревание и дифференцировка Т- и В-лимфоцитов
 Цитокины с регуляторной функцией цитокин ИЛ-10 эффект Подавляет продукцию цитокинов, подавляет активацию Т-хелперов 1 типа ТРФ - бета 1 (трансформирующий ростовый фактор) Подавляет активацию Тхелперов 1 и 2 типа, стимулирует рост фибробластов
Цитокины с регуляторной функцией цитокин ИЛ-10 эффект Подавляет продукцию цитокинов, подавляет активацию Т-хелперов 1 типа ТРФ - бета 1 (трансформирующий ростовый фактор) Подавляет активацию Тхелперов 1 и 2 типа, стимулирует рост фибробластов
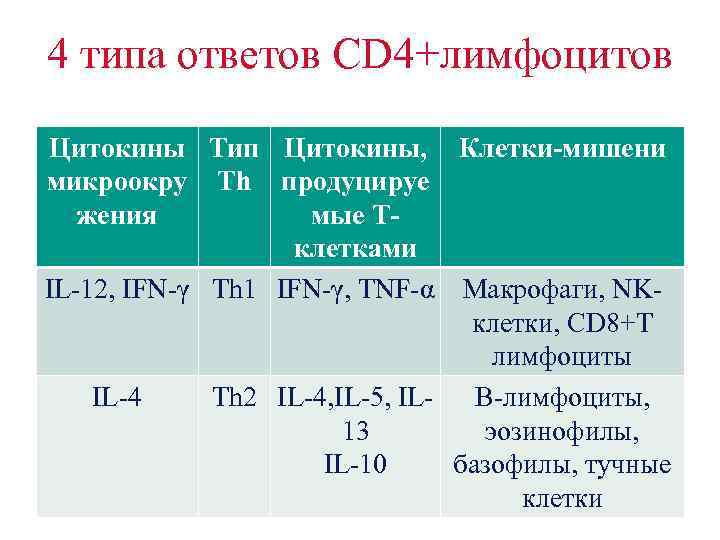 4 типа ответов CD 4+лимфоцитов Цитокины Тип Цитокины, Клетки-мишени микроокру Th продуцируе жения мые Тклетками IL-12, IFN-γ Th 1 IFN-γ, TNF-α Макрофаги, NKклетки, CD 8+Т лимфоциты IL-4 Th 2 IL-4, IL-5, IL- В-лимфоциты, 13 эозинофилы, IL-10 базофилы, тучные клетки
4 типа ответов CD 4+лимфоцитов Цитокины Тип Цитокины, Клетки-мишени микроокру Th продуцируе жения мые Тклетками IL-12, IFN-γ Th 1 IFN-γ, TNF-α Макрофаги, NKклетки, CD 8+Т лимфоциты IL-4 Th 2 IL-4, IL-5, IL- В-лимфоциты, 13 эозинофилы, IL-10 базофилы, тучные клетки
 4 типа ответов CD 4+лимфоцитов Цитокины микроокруже ния Тип Th Цитокины, продуцируемые Тклетками Клетки-мишени IL-6, TGF-β 1 Th 17 IL-17, IL -22 Нейтрофилы, эпителиальные клетки (защита слизистых) TGF-β 1, IL-10 Т-reg TGF-β 1, IL-10 Клетки врожденного и приобретенного иммунитета (все типы ответа)
4 типа ответов CD 4+лимфоцитов Цитокины микроокруже ния Тип Th Цитокины, продуцируемые Тклетками Клетки-мишени IL-6, TGF-β 1 Th 17 IL-17, IL -22 Нейтрофилы, эпителиальные клетки (защита слизистых) TGF-β 1, IL-10 Т-reg TGF-β 1, IL-10 Клетки врожденного и приобретенного иммунитета (все типы ответа)
 Апоптоз –физиологическая смерть клеток • Fas – рецептор (CD 95)- рецептор готовности клетки к апоптозу • Fas L или CD 95 L –лиганды Fas - рецептора. • Лигандами для таких рецепторов могут служить либо растворимые факторы, либо молекулы, экспрессирующиеся на поверхности клеток –таких, как цитотоксические Т лимфоциты. • При связывании Fas – рецептора Fas –лигандом, происходит запуск программируемой гибели клеток организма.
Апоптоз –физиологическая смерть клеток • Fas – рецептор (CD 95)- рецептор готовности клетки к апоптозу • Fas L или CD 95 L –лиганды Fas - рецептора. • Лигандами для таких рецепторов могут служить либо растворимые факторы, либо молекулы, экспрессирующиеся на поверхности клеток –таких, как цитотоксические Т лимфоциты. • При связывании Fas – рецептора Fas –лигандом, происходит запуск программируемой гибели клеток организма.
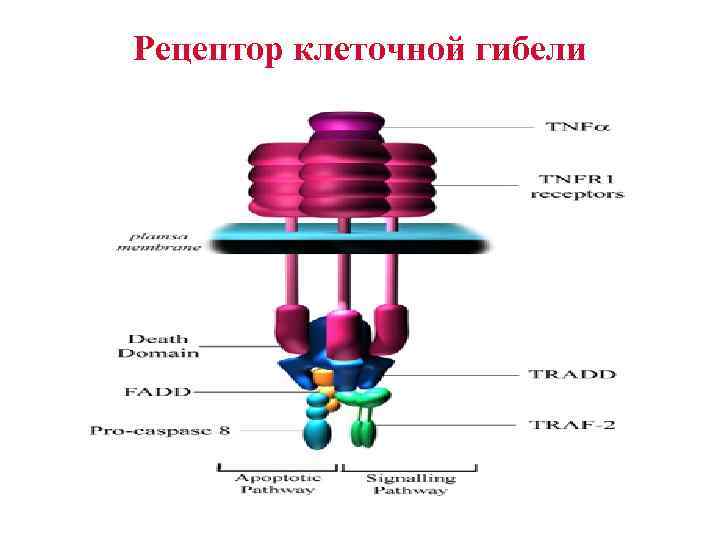 Рецептор клеточной гибели
Рецептор клеточной гибели
 механизмы запуска апоптоза • Цитотоксические Т лимфоциты распознают поврежденные , вирустрансформированные или малигнизированные клетки организма –хозяина и запускают в них программу апоптоза. • Цитотоксические Т лимфоциты также могут вызывать апоптоз клеток –мишеней с помощью специальных ферментов –гранзимов, которые они впрыскивают в отверстия клеточной мембраны клетки –мишени, созданные перфоринами – полимеризующимися в мембране мишени протеинами.
механизмы запуска апоптоза • Цитотоксические Т лимфоциты распознают поврежденные , вирустрансформированные или малигнизированные клетки организма –хозяина и запускают в них программу апоптоза. • Цитотоксические Т лимфоциты также могут вызывать апоптоз клеток –мишеней с помощью специальных ферментов –гранзимов, которые они впрыскивают в отверстия клеточной мембраны клетки –мишени, созданные перфоринами – полимеризующимися в мембране мишени протеинами.
 механизмы запуска апоптоза • Гранзим B может быть введен в клетку-мишень цитотоксическим Т лимфоцитом с помощью отверстий в мембране мишени, созданных перфоринами. Гранзим B способен прямо активировать каспазы 3, 7, 8 и 10. • Митохондрия – также является ключевым регулятором каспазного каскада и апоптоза: • Освобождение цитохрома C из митохондрии прямо активирует сначала каспазу 9, потом каспазу 3.
механизмы запуска апоптоза • Гранзим B может быть введен в клетку-мишень цитотоксическим Т лимфоцитом с помощью отверстий в мембране мишени, созданных перфоринами. Гранзим B способен прямо активировать каспазы 3, 7, 8 и 10. • Митохондрия – также является ключевым регулятором каспазного каскада и апоптоза: • Освобождение цитохрома C из митохондрии прямо активирует сначала каспазу 9, потом каспазу 3.
 Каспазы и разрушение хроматина Основной механизм запрограммированной гибели клеток – разрушение хромосомальной ДНК до нуклеосом. • Каспазы (ферменты с каскадным принципом действия) играют основную роль в этом процессе: • Активируют ДНКазы • Ингибируют ферменты, участвующие в репарации ДНК • Разрушают структурные протеины ядра
Каспазы и разрушение хроматина Основной механизм запрограммированной гибели клеток – разрушение хромосомальной ДНК до нуклеосом. • Каспазы (ферменты с каскадным принципом действия) играют основную роль в этом процессе: • Активируют ДНКазы • Ингибируют ферменты, участвующие в репарации ДНК • Разрушают структурные протеины ядра
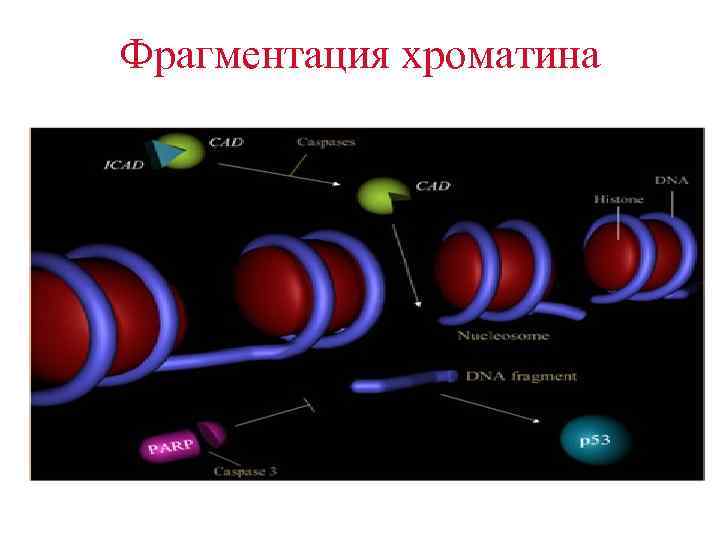 Фрагментация хроматина
Фрагментация хроматина
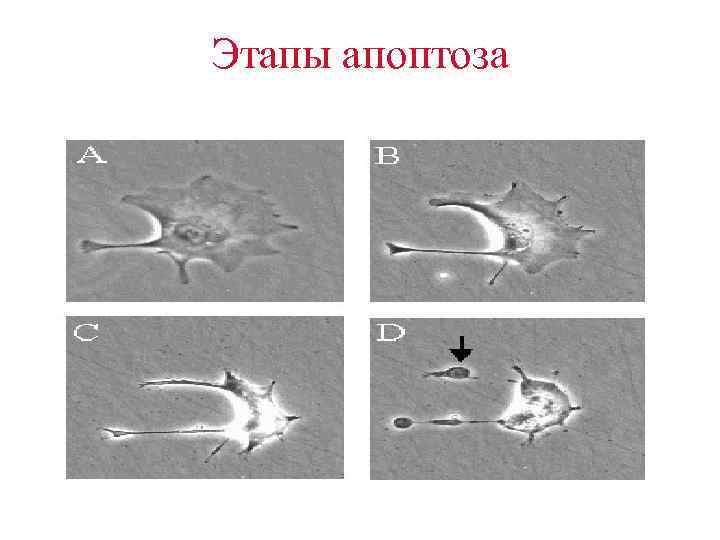
 Этапы апоптоза • (A) Разрыв ламинов (ядерных белков) и актинов – белков цитоскелета. • (B) Повреждение хроматина в ядре , конденсация хроматина. Ядро как бы «сморщивается» .
Этапы апоптоза • (A) Разрыв ламинов (ядерных белков) и актинов – белков цитоскелета. • (B) Повреждение хроматина в ядре , конденсация хроматина. Ядро как бы «сморщивается» .
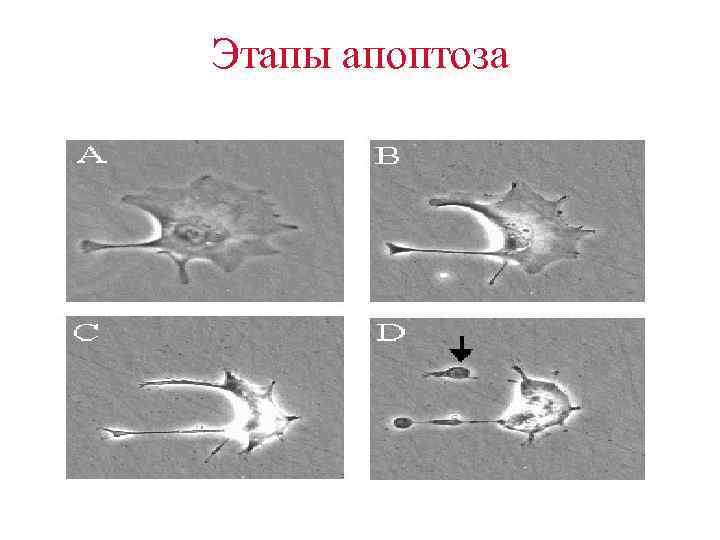 Этапы апоптоза
Этапы апоптоза
 Этапы апоптоза • (C) клетка уменьшается в размерах, как бы упаковывается в форму, удобную для ее поглощения макрофагом. • Макрофаги ответственны за клиренс апоптозных клеток из организма, причем при физиологической смерти клеток , в отличие от патологической гибели клеток путем некроза, воспаление не развивается вообще.
Этапы апоптоза • (C) клетка уменьшается в размерах, как бы упаковывается в форму, удобную для ее поглощения макрофагом. • Макрофаги ответственны за клиренс апоптозных клеток из организма, причем при физиологической смерти клеток , в отличие от патологической гибели клеток путем некроза, воспаление не развивается вообще.
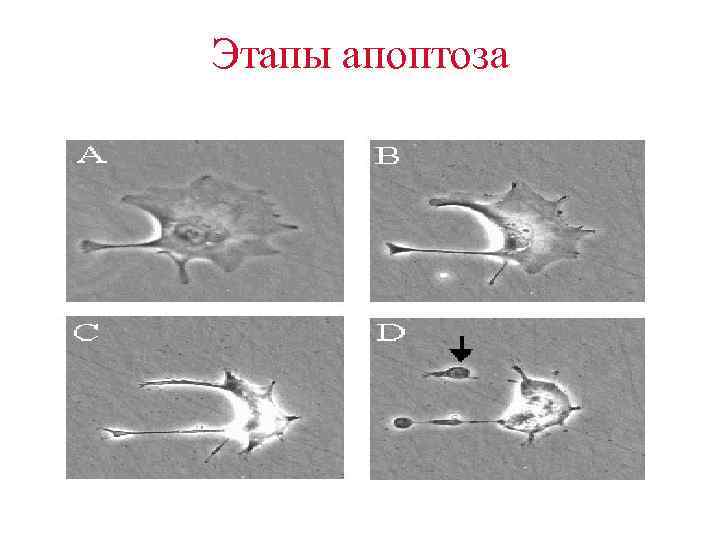 Этапы апоптоза
Этапы апоптоза
 Этапы апоптоза • Апоптозная клетка как бы «помогает» макрофагу поглотить себя, для этого в цитоплазиатическую мембрану апоптозной клетки транслоцируется фосфатидилсерин из клетки, он запускает активацию фагоцитоза макрофагов – т. е. триггирует макрофагальный ответ.
Этапы апоптоза • Апоптозная клетка как бы «помогает» макрофагу поглотить себя, для этого в цитоплазиатическую мембрану апоптозной клетки транслоцируется фосфатидилсерин из клетки, он запускает активацию фагоцитоза макрофагов – т. е. триггирует макрофагальный ответ.
 Этапы апоптоза • (D) маленькие везикулы – все, что остается от клетки на последнем этапе ее физиологической гибели - апоптозные тела, легко поглощаются макрофагами. • Так происходит физиологическая смена поколений клеток в организме повсеместно на протяжении всей жизни макроорганизма.
Этапы апоптоза • (D) маленькие везикулы – все, что остается от клетки на последнем этапе ее физиологической гибели - апоптозные тела, легко поглощаются макрофагами. • Так происходит физиологическая смена поколений клеток в организме повсеместно на протяжении всей жизни макроорганизма.
 Этапы апоптоза
Этапы апоптоза
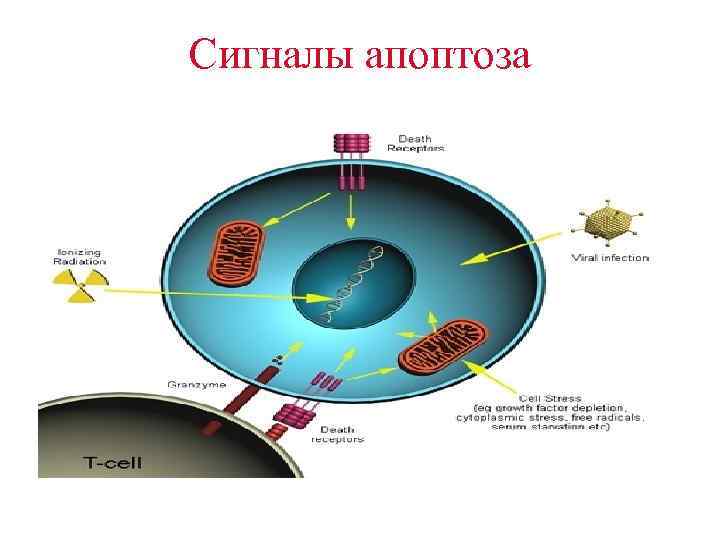
 Сигналы, вызывающие запуск апоптоза • Существует несколько типов сигналов, запускающих апоптоз. • Чувствительность клетки к таким сигналам зависит от многих факторов : • От экспрессии про- и противоапоптических протеинов (семейства Bcl-2 ) • От выраженности (силы) апоптозных стимулов • От стадии клеточного цикла
Сигналы, вызывающие запуск апоптоза • Существует несколько типов сигналов, запускающих апоптоз. • Чувствительность клетки к таким сигналам зависит от многих факторов : • От экспрессии про- и противоапоптических протеинов (семейства Bcl-2 ) • От выраженности (силы) апоптозных стимулов • От стадии клеточного цикла
 Сигналы апоптоза
Сигналы апоптоза
 Внутренние сигналы апоптоза • В других случаях апоптоз клетки может запускаться внутренними сигналами –сигналами стресса. • клеточный стресс может вызываться при экспозиции клетки к радиации, химическим веществам, либо при вирусной инфекции. • Стресс может быть также оксидативным - в клетке скапливается слишком больное число оксидантов. • В генерацию внутренних сигналов апоптоза вовлечены митохондрии. • Относительное количество антиапоптозных белков - bcl-2 определяет – насколько интенсивность клеточного стресса достаточна для входа клетки в апоптоз.
Внутренние сигналы апоптоза • В других случаях апоптоз клетки может запускаться внутренними сигналами –сигналами стресса. • клеточный стресс может вызываться при экспозиции клетки к радиации, химическим веществам, либо при вирусной инфекции. • Стресс может быть также оксидативным - в клетке скапливается слишком больное число оксидантов. • В генерацию внутренних сигналов апоптоза вовлечены митохондрии. • Относительное количество антиапоптозных белков - bcl-2 определяет – насколько интенсивность клеточного стресса достаточна для входа клетки в апоптоз.
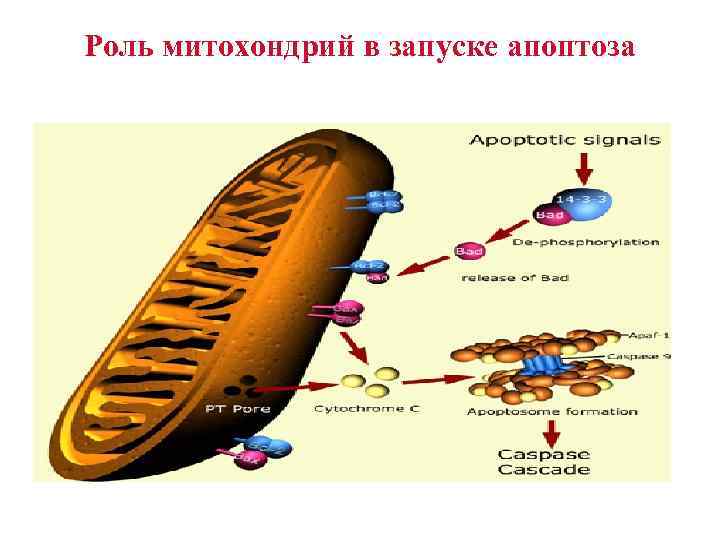
 Роль Bcl-2 протеинов • Проапоптозные bcl-2 часто обнаруживаются и в цитозоле клетки, где они выполняют роль сенсоров клеточного повреждения или стресса. • Вслед за развившимся клеточным стрессом они встраиваются в мембрану митохондрии, где локализуются противоапоптозные белки. • Такое взаимодействие между про- и противоапоптозными bcl-2 белками в мембране митохондрий приводит к образованию пори к освобождению цитохрома С и других проапоптозных молекул из внутримембранного пространства. • Это, в свою очередь, приводит к образованию апоптосом и активации каспазного каскада.
Роль Bcl-2 протеинов • Проапоптозные bcl-2 часто обнаруживаются и в цитозоле клетки, где они выполняют роль сенсоров клеточного повреждения или стресса. • Вслед за развившимся клеточным стрессом они встраиваются в мембрану митохондрии, где локализуются противоапоптозные белки. • Такое взаимодействие между про- и противоапоптозными bcl-2 белками в мембране митохондрий приводит к образованию пори к освобождению цитохрома С и других проапоптозных молекул из внутримембранного пространства. • Это, в свою очередь, приводит к образованию апоптосом и активации каспазного каскада.
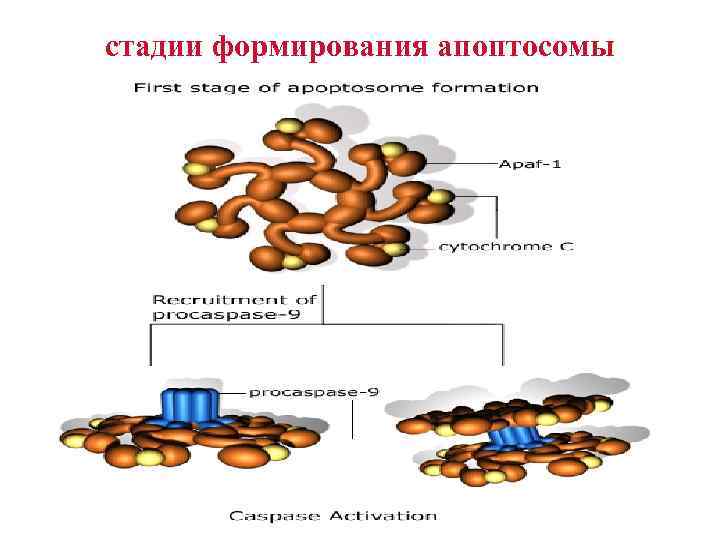
 Формирование апоптосом • Освобождение цитохрома С в цитозоль приводит также к взаимодействию цитохрома С с белком, названным Apaf-1. • Это приводит к привлечению прокаспазы 9 в формирование многобелкового комплекса –с цитохромом С и белком Apaf-1, весь комплекс таких белков называется апоптосомой. • Формирование апоптосом приводит к активации каспазы 9 и к запуску апоптоза.
Формирование апоптосом • Освобождение цитохрома С в цитозоль приводит также к взаимодействию цитохрома С с белком, названным Apaf-1. • Это приводит к привлечению прокаспазы 9 в формирование многобелкового комплекса –с цитохромом С и белком Apaf-1, весь комплекс таких белков называется апоптосомой. • Формирование апоптосом приводит к активации каспазы 9 и к запуску апоптоза.
 Роль митохондрий в запуске апоптоза
Роль митохондрий в запуске апоптоза
 стадии формирования апоптосомы
стадии формирования апоптосомы
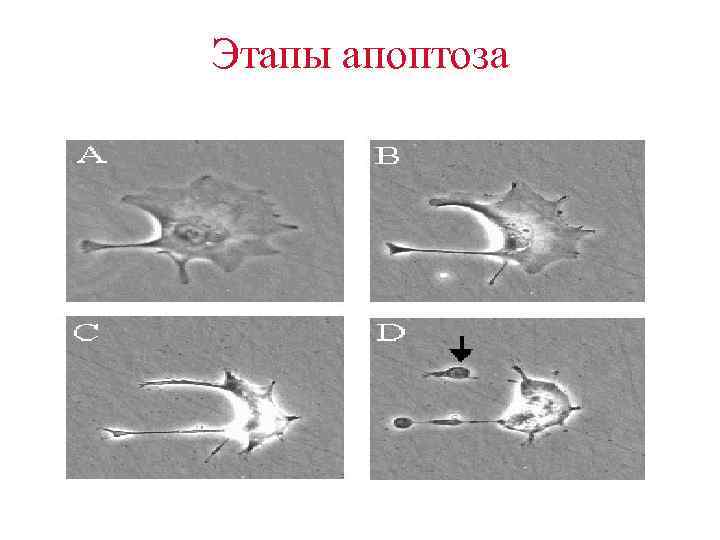 Этапы апоптоза
Этапы апоптоза


