Презентация растворы . Лекция 4.ppt
- Количество слайдов: 49
 Лекция 4 Растворы и дисперсные системы 1
Лекция 4 Растворы и дисперсные системы 1
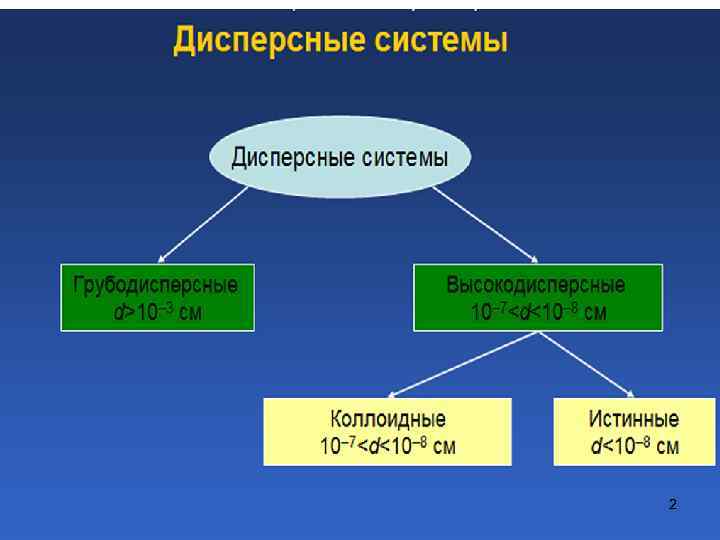 2
2
 3
3
 4
4
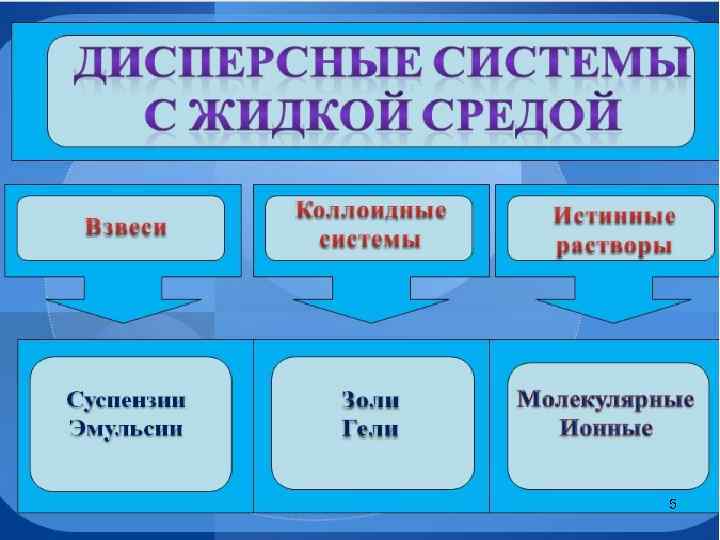 5
5
 6
6
 7
7
 8
8
 9
9
 Растворы занимают промежуточное положение между химическими соединениями и механическими смесями 10
Растворы занимают промежуточное положение между химическими соединениями и механическими смесями 10
 11
11
 При наличии одного растворенного вещества(газообразного, жидкого или твердого) в жидкости – индивидуальный раствор, двух – бинарный, более - моногокомпонентный • Растворимость веществ в растворителе может быть ограниченной и неограниченной, т. е. полная смешиваемость ингредиентов в любых соотношениях, например этанол-вода • Растворители делят на неводные (органические), воду и смешанные • Растворяемые компоненты могут быть электролитами и неэлектролитами. Растворы неэлектролитов с водой и между собой содержат нейтральные молекулы и не обладают заметной электропроводностью 12
При наличии одного растворенного вещества(газообразного, жидкого или твердого) в жидкости – индивидуальный раствор, двух – бинарный, более - моногокомпонентный • Растворимость веществ в растворителе может быть ограниченной и неограниченной, т. е. полная смешиваемость ингредиентов в любых соотношениях, например этанол-вода • Растворители делят на неводные (органические), воду и смешанные • Растворяемые компоненты могут быть электролитами и неэлектролитами. Растворы неэлектролитов с водой и между собой содержат нейтральные молекулы и не обладают заметной электропроводностью 12
 13
13
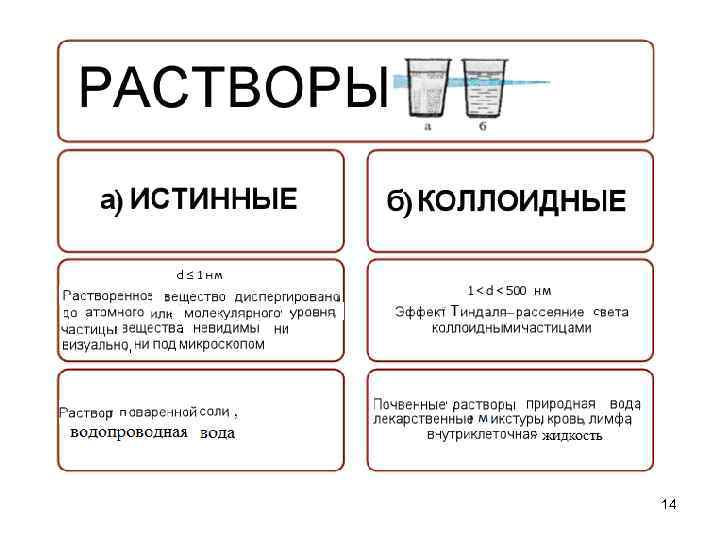 14
14
 СОСТАВ РАСТВОРА • Растворенное вещество распределено в растворителе в виде молекул, атомов или ионов • Растворитель среда, в которой равномерно распределены растворенные вещества в виде молекул, атомов или ионов. • Растворителем считают тот компонент, который существует в том же агрегатном состоянии, что и раствор, или тот компонент, который находится в большем количестве 15
СОСТАВ РАСТВОРА • Растворенное вещество распределено в растворителе в виде молекул, атомов или ионов • Растворитель среда, в которой равномерно распределены растворенные вещества в виде молекул, атомов или ионов. • Растворителем считают тот компонент, который существует в том же агрегатном состоянии, что и раствор, или тот компонент, который находится в большем количестве 15
 Растворение – физико-химический процесс • Растворы образуются при взаимодействии растворителя и растворенного вещества • Процесс взаимодействия растворителя и растворенного вещества называется сольватацией (если растворителем является вода - гидратацией) • Растворение протекает с образованием различных по форме и прочности продуктов – гидратов • Энергетической характеристикой растворения является теплота образования раствора, рассматриваемая как алгебраическая сумма тепловых эффектов всех эндо-и экзо-термических стадий процесса. 16
Растворение – физико-химический процесс • Растворы образуются при взаимодействии растворителя и растворенного вещества • Процесс взаимодействия растворителя и растворенного вещества называется сольватацией (если растворителем является вода - гидратацией) • Растворение протекает с образованием различных по форме и прочности продуктов – гидратов • Энергетической характеристикой растворения является теплота образования раствора, рассматриваемая как алгебраическая сумма тепловых эффектов всех эндо-и экзо-термических стадий процесса. 16
 Поглощающие тепло процессы – разрушение кристаллической решетки, разрывы химических связей в молекулах (эндотермический процесс) • Выделяющие тепло процессы – образование продуктов взаимодействия растворенного вещества с растворителем (экзотермический процесс) • Если энергия разрушения кристаллической решетки меньше энергии гидратации растворенного вещества, то растворение идет с выделением теплоты (Q > 0 ) • Если энергия кристаллической решетки больше энергии гидратации, то растворение протекает с поглощением теплоты (Q < 0) 17
Поглощающие тепло процессы – разрушение кристаллической решетки, разрывы химических связей в молекулах (эндотермический процесс) • Выделяющие тепло процессы – образование продуктов взаимодействия растворенного вещества с растворителем (экзотермический процесс) • Если энергия разрушения кристаллической решетки меньше энергии гидратации растворенного вещества, то растворение идет с выделением теплоты (Q > 0 ) • Если энергия кристаллической решетки больше энергии гидратации, то растворение протекает с поглощением теплоты (Q < 0) 17
 Ненасыщенный раствор, в котором данное вещество при данной температуре еще растворяется • Насыщенный раствор: • – раствор, в котором данное вещество при данной температуре больше не растворяется. • содержит максимальное количество растворенного вещества при данной температуре. • находится в равновесии с избытком растворенного вещества • Пересыщенный раствор – раствор , который содержится растворенного вещества больше, чем его содержится в насыщенном растворе при данной температуре 18
Ненасыщенный раствор, в котором данное вещество при данной температуре еще растворяется • Насыщенный раствор: • – раствор, в котором данное вещество при данной температуре больше не растворяется. • содержит максимальное количество растворенного вещества при данной температуре. • находится в равновесии с избытком растворенного вещества • Пересыщенный раствор – раствор , который содержится растворенного вещества больше, чем его содержится в насыщенном растворе при данной температуре 18
 19
19
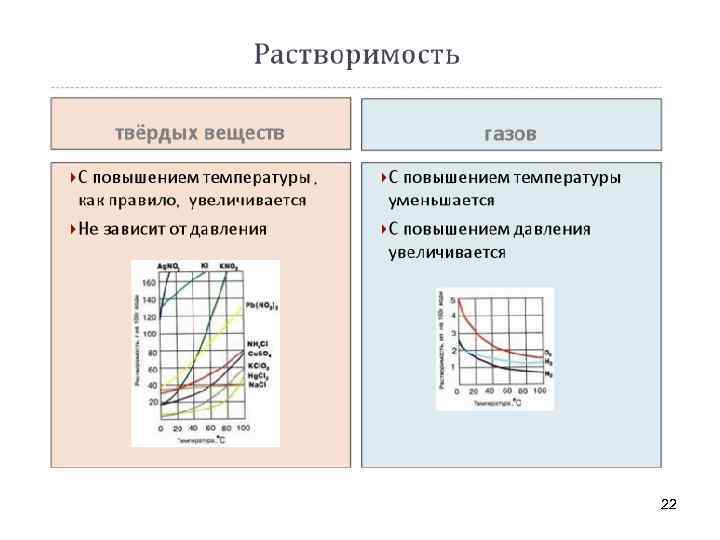
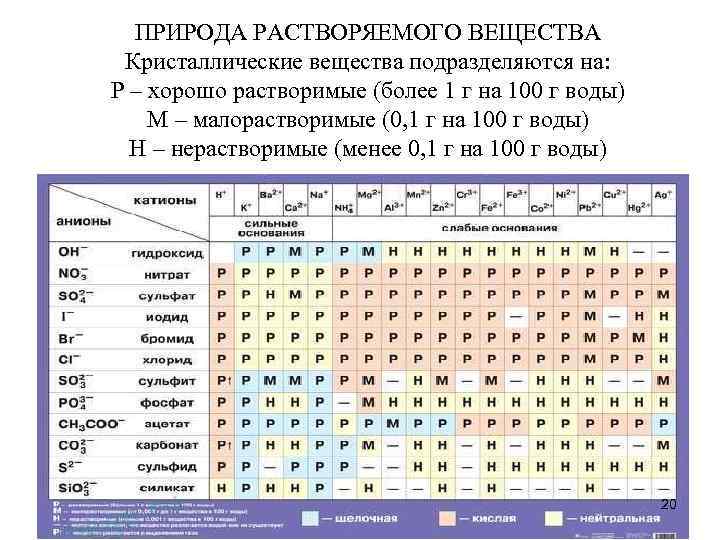 ПРИРОДА РАСТВОРЯЕМОГО ВЕЩЕСТВА Кристаллические вещества подразделяются на: Р – хорошо растворимые (более 1 г на 100 г воды) М – малорастворимые (0, 1 г на 100 г воды) Н – нерастворимые (менее 0, 1 г на 100 г воды) 20
ПРИРОДА РАСТВОРЯЕМОГО ВЕЩЕСТВА Кристаллические вещества подразделяются на: Р – хорошо растворимые (более 1 г на 100 г воды) М – малорастворимые (0, 1 г на 100 г воды) Н – нерастворимые (менее 0, 1 г на 100 г воды) 20
 21
21
 22
22
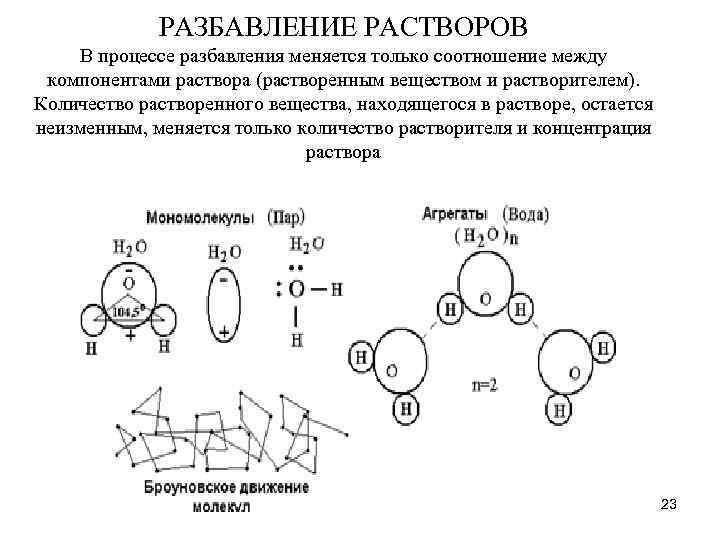 РАЗБАВЛЕНИЕ РАСТВОРОВ В процессе разбавления меняется только соотношение между компонентами раствора (растворенным веществом и растворителем). Количество растворенного вещества, находящегося в растворе, остается неизменным, меняется только количество растворителя и концентрация раствора 23
РАЗБАВЛЕНИЕ РАСТВОРОВ В процессе разбавления меняется только соотношение между компонентами раствора (растворенным веществом и растворителем). Количество растворенного вещества, находящегося в растворе, остается неизменным, меняется только количество растворителя и концентрация раствора 23
 СВОЙСТВА ВОДЫ • Молекула воды имеет ассиметричное строение • Существует в трех агрегатных состояниях • Теплоемкость воды достигает минимальных значений при 37°С • Аномально изменяется плотность воды при нагреванииохлаждении (при понижении температуры от 100 °С до 3, 98 °С) вода непрерывно сокращается в объеме • Вода обладает самым высоким поверхностным натяжением среди всех жидкостей (исключение ртуть) 24
СВОЙСТВА ВОДЫ • Молекула воды имеет ассиметричное строение • Существует в трех агрегатных состояниях • Теплоемкость воды достигает минимальных значений при 37°С • Аномально изменяется плотность воды при нагреванииохлаждении (при понижении температуры от 100 °С до 3, 98 °С) вода непрерывно сокращается в объеме • Вода обладает самым высоким поверхностным натяжением среди всех жидкостей (исключение ртуть) 24
 Химические свойства воды • Вода обладает амфотерными свойствами: NH 3 + H 2 O NH 3·H 2 O NH 4++HOP 2 O 5 + H 2 O 2 H 3 PO 4 • Вода реагирует с солями, образуя гидраты: Ca. Cl 2 + 6 H 2 O Ca. Cl 2· 6 H 2 O либо продукты гидролиза: Al 2 S 3 + 6 H 2 O 2 Al(OH)3 +3 H 2 S Вода окисляет металлы, расположенные в ряду напряжений до олова 2 K + H 2 O 2 KOH + H 2 25
Химические свойства воды • Вода обладает амфотерными свойствами: NH 3 + H 2 O NH 3·H 2 O NH 4++HOP 2 O 5 + H 2 O 2 H 3 PO 4 • Вода реагирует с солями, образуя гидраты: Ca. Cl 2 + 6 H 2 O Ca. Cl 2· 6 H 2 O либо продукты гидролиза: Al 2 S 3 + 6 H 2 O 2 Al(OH)3 +3 H 2 S Вода окисляет металлы, расположенные в ряду напряжений до олова 2 K + H 2 O 2 KOH + H 2 25
 26
26
 27
27
 28
28
 Массовая доля компонента в растворе • Задача № 1: Какую массу фосфата калия и воды нужно взять для приготовления 250 г раствора с массовой долей фосфата 8%? • Задача № 2: В воде объемом 200 мл растворили соль массой 40 г. Определите массовую долю соли в полученном растворе? 29
Массовая доля компонента в растворе • Задача № 1: Какую массу фосфата калия и воды нужно взять для приготовления 250 г раствора с массовой долей фосфата 8%? • Задача № 2: В воде объемом 200 мл растворили соль массой 40 г. Определите массовую долю соли в полученном растворе? 29
 ОПРЕДЕЛЕНИЕ ПЛОТНОСТИ РАСТВОРОВ • Применение ареометра основано на том, что плавающее тело погружается в жидкость до тех пор, пока масса вытесненной им жидкости не станет, равна массе самого тела (закон Архимеда). В расширенной нижней части ареометра помещен груз, на узкой верхней части – шейке - нанесены деления, указывающие плотность жидкости, в которой плавает ареометр. Для этого раствор перелить в мерный цилиндр. Уровень жидкости должен быть ниже края цилиндра на 3 -4 см. Осторожно опустить ареометр в раствор. Ареометр не должен касаться стенок цилиндра. Отсчет плотности по уровню жидкости производите сверху вниз. 30
ОПРЕДЕЛЕНИЕ ПЛОТНОСТИ РАСТВОРОВ • Применение ареометра основано на том, что плавающее тело погружается в жидкость до тех пор, пока масса вытесненной им жидкости не станет, равна массе самого тела (закон Архимеда). В расширенной нижней части ареометра помещен груз, на узкой верхней части – шейке - нанесены деления, указывающие плотность жидкости, в которой плавает ареометр. Для этого раствор перелить в мерный цилиндр. Уровень жидкости должен быть ниже края цилиндра на 3 -4 см. Осторожно опустить ареометр в раствор. Ареометр не должен касаться стенок цилиндра. Отсчет плотности по уровню жидкости производите сверху вниз. 30
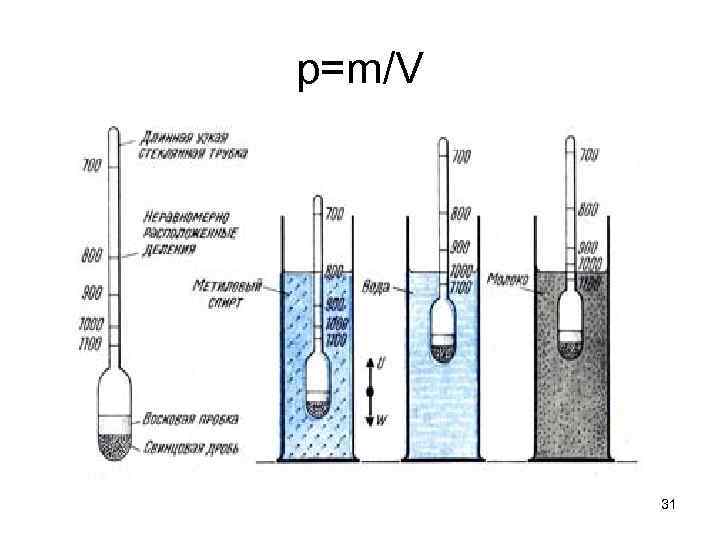 p=m/V 31
p=m/V 31
 32
32
 ОБЪЕМНАЯ ДОЛЯ РАСТВОРЕННОГО ВЕЩЕСТВА • Задача № 1: К метанолу массой 32 г и плотностью 0, 8 г/мл добавили воду до объема 80 мл. Определите объемную долю спирта в растворе • Задача № 2: При смешении веществ объемом 50 мл и метанола объемом 70 мл и плотностью 0, 8 г/мл получим раствор с плотностью 0, 9 г/мл. Определите объемную долю метанола в растворе 33
ОБЪЕМНАЯ ДОЛЯ РАСТВОРЕННОГО ВЕЩЕСТВА • Задача № 1: К метанолу массой 32 г и плотностью 0, 8 г/мл добавили воду до объема 80 мл. Определите объемную долю спирта в растворе • Задача № 2: При смешении веществ объемом 50 мл и метанола объемом 70 мл и плотностью 0, 8 г/мл получим раствор с плотностью 0, 9 г/мл. Определите объемную долю метанола в растворе 33
 34
34
 35
35
 36
36
 МОЛЯРНАЯ КОНЦЕНТРАЦИЯ • Задача № 1 В воде растворили гидроксид калия 11, 2 г, объем раствора довели до 200 мл. Определите молярную концентрацию полученного раствора. • Задача № 2 Определите молярную концентрацию раствора, полученного при растворении сульфата натрия массой 42, 6 г в воде массой 300 г, если плотность полученного раствора равна 1, 12 г/мл 37
МОЛЯРНАЯ КОНЦЕНТРАЦИЯ • Задача № 1 В воде растворили гидроксид калия 11, 2 г, объем раствора довели до 200 мл. Определите молярную концентрацию полученного раствора. • Задача № 2 Определите молярную концентрацию раствора, полученного при растворении сульфата натрия массой 42, 6 г в воде массой 300 г, если плотность полученного раствора равна 1, 12 г/мл 37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49


