Лекция 4 Периодический закон.ppt
- Количество слайдов: 50
 Лекция 4
Лекция 4
 После утверждения атомно-молекулярной теории важнейшим событием в химии было открытие Периодического закона.
После утверждения атомно-молекулярной теории важнейшим событием в химии было открытие Периодического закона.
 «ШАГИ» в направлении классификации элементов Существование триад (Дёберейнер, 1817 г. ) Расположение элементов на витках спирали (А. Э. Б. Де Шанкуртуа, 1862 г. ) Закон октав (Дж. Ньюлендс, 1863 г. ) Периодический закон (Д. И. Менделеев, 1869 г. ) Таблица из 8 колонок (Л. Мейер, 1871 г. ) Открытие инертных газов (Релей, Рамзай, 1894 г. ) Заряд ядра равен порядковому номеру (А. ван ден Брук, 1911 г. )
«ШАГИ» в направлении классификации элементов Существование триад (Дёберейнер, 1817 г. ) Расположение элементов на витках спирали (А. Э. Б. Де Шанкуртуа, 1862 г. ) Закон октав (Дж. Ньюлендс, 1863 г. ) Периодический закон (Д. И. Менделеев, 1869 г. ) Таблица из 8 колонок (Л. Мейер, 1871 г. ) Открытие инертных газов (Релей, Рамзай, 1894 г. ) Заряд ядра равен порядковому номеру (А. ван ден Брук, 1911 г. )
 В 1817 году немецкий химик Дёберейнер (1780 -1849) показал, что атомный вес стронция Sr имеет среднее значение между атомными весами двух родственных элементов – кальция Ca и бария Ba. Позже он установил существование других триад подобных элементов (Cl, Br, I; Li, Na, K).
В 1817 году немецкий химик Дёберейнер (1780 -1849) показал, что атомный вес стронция Sr имеет среднее значение между атомными весами двух родственных элементов – кальция Ca и бария Ba. Позже он установил существование других триад подобных элементов (Cl, Br, I; Li, Na, K).
 «ШАГИ» в направлении классификации элементов Существование триад (Дёберейнер, 1817 г. ) Расположение элементов на витках спирали (А. Э. Б. Де Шанкуртуа, 1862 г. ) Закон октав (Дж. Ньюлендс, 1863 г. ) Периодический закон (Д. И. Менделеев, 1869 г. ) Таблица из 8 колонок (Л. Мейер, 1871 г. ) Открытие инертных газов (Релей, Рамзай, 1894 г. ) Заряд ядра равен порядковому номеру (А. ван ден Брук, 1911 г. )
«ШАГИ» в направлении классификации элементов Существование триад (Дёберейнер, 1817 г. ) Расположение элементов на витках спирали (А. Э. Б. Де Шанкуртуа, 1862 г. ) Закон октав (Дж. Ньюлендс, 1863 г. ) Периодический закон (Д. И. Менделеев, 1869 г. ) Таблица из 8 колонок (Л. Мейер, 1871 г. ) Открытие инертных газов (Релей, Рамзай, 1894 г. ) Заряд ядра равен порядковому номеру (А. ван ден Брук, 1911 г. )
 В 1862 году французский химик А. Э. Б. де Шанкуртуа расположил элементы в порядке возрастания атомных весов на пространственной спиральной кривой с соответствующими точками на последовательных витках спирали (разница в 16 единиц).
В 1862 году французский химик А. Э. Б. де Шанкуртуа расположил элементы в порядке возрастания атомных весов на пространственной спиральной кривой с соответствующими точками на последовательных витках спирали (разница в 16 единиц).
 «ШАГИ» в направлении классификации элементов Существование триад (Дёберейнер, 1817 г. ) Расположение элементов на витках спирали (А. Э. Б. Де Шанкуртуа, 1862 г. ) Закон октав (Дж. Ньюлендс, 1863 г. ) Периодический закон (Д. И. Менделеев, 1869 г. ) Таблица из 8 колонок (Л. Мейер, 1871 г. ) Открытие инертных газов (Релей, Рамзай, 1894 г. ) Заряд ядра равен порядковому номеру (А. ван ден Брук, 1911 г. )
«ШАГИ» в направлении классификации элементов Существование триад (Дёберейнер, 1817 г. ) Расположение элементов на витках спирали (А. Э. Б. Де Шанкуртуа, 1862 г. ) Закон октав (Дж. Ньюлендс, 1863 г. ) Периодический закон (Д. И. Менделеев, 1869 г. ) Таблица из 8 колонок (Л. Мейер, 1871 г. ) Открытие инертных газов (Релей, Рамзай, 1894 г. ) Заряд ядра равен порядковому номеру (А. ван ден Брук, 1911 г. )
 В 1863 году Дж. Ньюлендс разделил элементы на 7 групп по 7 элементов и назвал такую зависимость «законом октав» по аналогии с семью интервалами музыкальной гаммы.
В 1863 году Дж. Ньюлендс разделил элементы на 7 групп по 7 элементов и назвал такую зависимость «законом октав» по аналогии с семью интервалами музыкальной гаммы.
 «ШАГИ» в направлении классификации элементов Существование триад (Дёберейнер, 1817 г. ) Расположение элементов на витках спирали (А. Э. Б. Де Шанкуртуа, 1862 г. ) Закон октав (Дж. Ньюлендс, 1863 г. ) Периодический закон (Д. И. Менделеев, 1869 г. ) Таблица из 8 колонок (Л. Мейер, 1871 г. ) Открытие инертных газов (Релей, Рамзай, 1894 г. ) Заряд ядра равен порядковому номеру (А. ван ден Брук, 1911 г. )
«ШАГИ» в направлении классификации элементов Существование триад (Дёберейнер, 1817 г. ) Расположение элементов на витках спирали (А. Э. Б. Де Шанкуртуа, 1862 г. ) Закон октав (Дж. Ньюлендс, 1863 г. ) Периодический закон (Д. И. Менделеев, 1869 г. ) Таблица из 8 колонок (Л. Мейер, 1871 г. ) Открытие инертных газов (Релей, Рамзай, 1894 г. ) Заряд ядра равен порядковому номеру (А. ван ден Брук, 1911 г. )
 Д. И. Менделеев (1834 -1907) В 1869 году Д. И. Менделеев предложил периодическую систему из 17 колонок. В 1871 году он пересмотрел эту таблицу и передвинул некоторые элементы на другие места, соответствующие уточненным значениям атомных весов.
Д. И. Менделеев (1834 -1907) В 1869 году Д. И. Менделеев предложил периодическую систему из 17 колонок. В 1871 году он пересмотрел эту таблицу и передвинул некоторые элементы на другие места, соответствующие уточненным значениям атомных весов.
 Таблица Д. И. Менделеева, 1871 г
Таблица Д. И. Менделеева, 1871 г
 Meyer’s Periodic Table (1870) Julius L. Meyer 1830 -1895 Julius Meyer was a contemporary and competitor of Mendeleev. He constructed an Periodic table but unfortunately published it one year after Mendeleev’s table was published!
Meyer’s Periodic Table (1870) Julius L. Meyer 1830 -1895 Julius Meyer was a contemporary and competitor of Mendeleev. He constructed an Periodic table but unfortunately published it one year after Mendeleev’s table was published!
 В том же 1871 году Лотар Мейер предложил таблицу из 8 колонок. Он разделил каждый длинный период на период из 7 элементов, на восьмую группу, содержащую триады элементов (подобных Fe, Co, Ni) и на второй период из 7 элементов.
В том же 1871 году Лотар Мейер предложил таблицу из 8 колонок. Он разделил каждый длинный период на период из 7 элементов, на восьмую группу, содержащую триады элементов (подобных Fe, Co, Ni) и на второй период из 7 элементов.
 «ШАГИ» в направлении классификации элементов Существование триад (Дёберейнер, 1817 г. ) Расположение элементов на витках спирали (А. Э. Б. Де Шанкуртуа, 1862 г. ) Закон октав (Дж. Ньюлендс, 1863 г. ) Периодический закон (Д. И. Менделеев, 1869 г. ) Таблица из 8 колонок (Л. Мейер, 1871 г. ) Открытие инертных газов (Релей, Рамзай, 1894 г. ) Заряд ядра равен порядковому номеру (А. ван ден Брук, 1911 г. )
«ШАГИ» в направлении классификации элементов Существование триад (Дёберейнер, 1817 г. ) Расположение элементов на витках спирали (А. Э. Б. Де Шанкуртуа, 1862 г. ) Закон октав (Дж. Ньюлендс, 1863 г. ) Периодический закон (Д. И. Менделеев, 1869 г. ) Таблица из 8 колонок (Л. Мейер, 1871 г. ) Открытие инертных газов (Релей, Рамзай, 1894 г. ) Заряд ядра равен порядковому номеру (А. ван ден Брук, 1911 г. )
 В 1894 году Релеем и Рамзаем были открыты аргоноиды (благородные газы – He, Ne, Ar, Kr, Xe). В последующие годы к периодической таблице была добавлена «нулевая группа»
В 1894 году Релеем и Рамзаем были открыты аргоноиды (благородные газы – He, Ne, Ar, Kr, Xe). В последующие годы к периодической таблице была добавлена «нулевая группа»
 «ШАГИ» в направлении классификации элементов Существование триад (Дёберейнер, 1817 г. ) Расположение элементов на витках спирали (А. Э. Б. Де Шанкуртуа, 1862 г. ) Закон октав (Дж. Ньюлендс, 1863 г. ) Периодический закон (Д. И. Менделеев, 1869 г. ) Таблица из 8 колонок (Л. Мейер, 1871 г. ) Открытие инертных газов (Релей, Рамзай, 1894 г. ) Заряд ядра равен порядковому номеру (А. ван ден Брук, 1911 г. )
«ШАГИ» в направлении классификации элементов Существование триад (Дёберейнер, 1817 г. ) Расположение элементов на витках спирали (А. Э. Б. Де Шанкуртуа, 1862 г. ) Закон октав (Дж. Ньюлендс, 1863 г. ) Периодический закон (Д. И. Менделеев, 1869 г. ) Таблица из 8 колонок (Л. Мейер, 1871 г. ) Открытие инертных газов (Релей, Рамзай, 1894 г. ) Заряд ядра равен порядковому номеру (А. ван ден Брук, 1911 г. )
 После открытия электрона и разработки теории ядра атома голландский физик А. ван ден Брук в 1911 году предположил, что заряд ядра атома того или иного элемента может быть равен порядковому номеру в периодической системе.
После открытия электрона и разработки теории ядра атома голландский физик А. ван ден Брук в 1911 году предположил, что заряд ядра атома того или иного элемента может быть равен порядковому номеру в периодической системе.
 Группы – вертикальные колонки периодической таблицы. Элементы, входящие в одну и ту же группу – родственные элементы – обладают весьма близкими физическими и химическими свойствами.
Группы – вертикальные колонки периодической таблицы. Элементы, входящие в одну и ту же группу – родственные элементы – обладают весьма близкими физическими и химическими свойствами.
 Периодический закон Свойства химических элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины заряда ядра их атомов
Периодический закон Свойства химических элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины заряда ядра их атомов
 Д. И. Менделееву удалось предсказать существование шести элементов, которые в то время еще не были открыты и которые должны были занять незаполненные места в его таблице. экабор экаалюминий экасилиций экамарганец двимарганец экатантал скандий галлий германий технеций рений полоний Sc Ga Ge Tc Re Po
Д. И. Менделееву удалось предсказать существование шести элементов, которые в то время еще не были открыты и которые должны были занять незаполненные места в его таблице. экабор экаалюминий экасилиций экамарганец двимарганец экатантал скандий галлий германий технеций рений полоний Sc Ga Ge Tc Re Po
 После того как были открыты гелий He и аргон Ar, вывод о существовании неона Ne, криптона Kr, ксенона Xe и радона Rn ясно следовал из периодического закона. Первые три были открыты в воздухе, радон открыли при исследовании свойств радия и других радиоактивных веществ.
После того как были открыты гелий He и аргон Ar, вывод о существовании неона Ne, криптона Kr, ксенона Xe и радона Rn ясно следовал из периодического закона. Первые три были открыты в воздухе, радон открыли при исследовании свойств радия и других радиоактивных веществ.
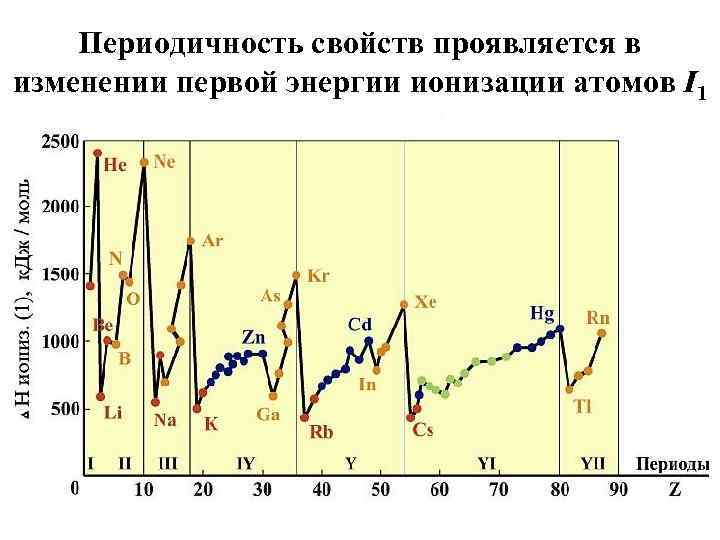 Периодичность свойств проявляется в изменении первой энергии ионизации атомов I 1
Периодичность свойств проявляется в изменении первой энергии ионизации атомов I 1
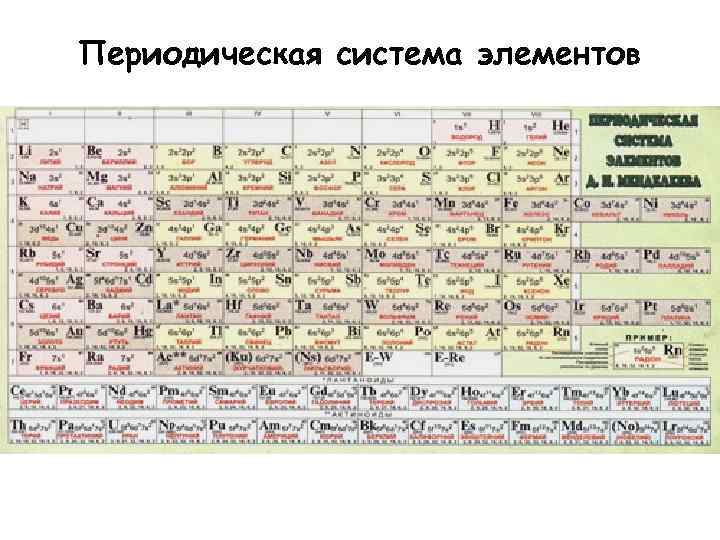 Периодическая система элементов
Периодическая система элементов
 Периоды - горизонтальные ряды периодической таблицы: 1 короткий из двух элементов (Н и Не), 2 коротких периода по восемь элементов, 2 длинных периода из 18 элементов, 1 очень длинный из 32 элементов и 1 незаконченный период.
Периоды - горизонтальные ряды периодической таблицы: 1 короткий из двух элементов (Н и Не), 2 коротких периода по восемь элементов, 2 длинных периода из 18 элементов, 1 очень длинный из 32 элементов и 1 незаконченный период.
 Металлы, неметаллы и металлоиды Металлоиды Неметаллы
Металлы, неметаллы и металлоиды Металлоиды Неметаллы
 üАтомный радиус üЭнергия ионизации üИонный радиус üСродство к электрону üЭлектроотрицательность
üАтомный радиус üЭнергия ионизации üИонный радиус üСродство к электрону üЭлектроотрицательность
 Атомный радиус – величина расчетная и относительная.
Атомный радиус – величина расчетная и относительная.
 Атомный объем химического элемента – объем 1 моля его атомов. Атомный радиус Зная атомный объем можно вычислить объем одного атома, так как в 1 моле вещества содержится 6· 1023 атомов. Исходя из этих данных вычислим атомный радиус. v Объем и радиус атома зависят от того, как связан он с другими атомами
Атомный объем химического элемента – объем 1 моля его атомов. Атомный радиус Зная атомный объем можно вычислить объем одного атома, так как в 1 моле вещества содержится 6· 1023 атомов. Исходя из этих данных вычислим атомный радиус. v Объем и радиус атома зависят от того, как связан он с другими атомами
 Å= -10 10 м нм = -9 м 10 пм = -12 м 10
Å= -10 10 м нм = -9 м 10 пм = -12 м 10
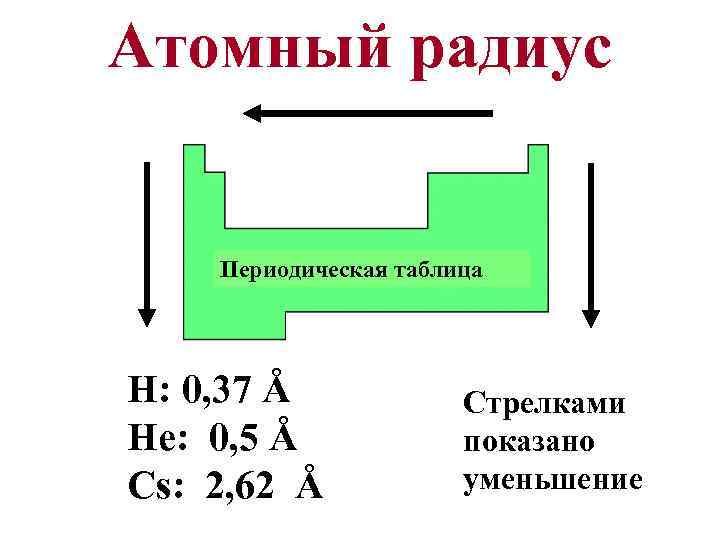 Атомный радиус Периодическая таблица H: 0, 37 Å He: 0, 5 Å Cs: 2, 62 Å Стрелками показано уменьшение
Атомный радиус Периодическая таблица H: 0, 37 Å He: 0, 5 Å Cs: 2, 62 Å Стрелками показано уменьшение
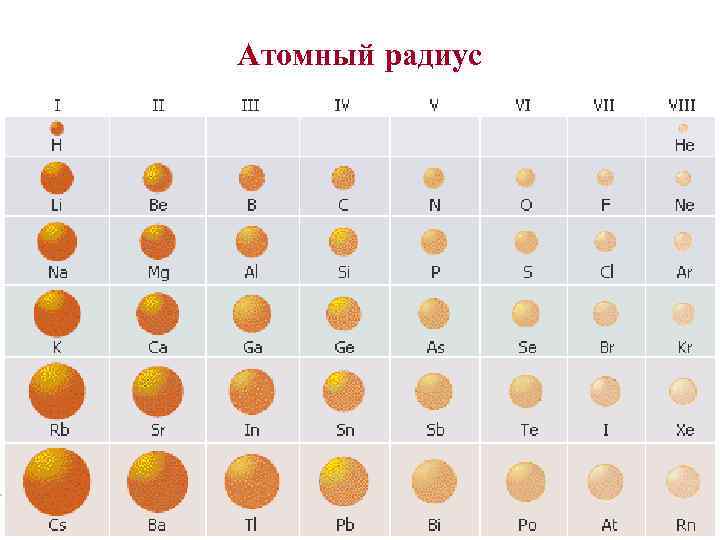 Атомный радиус
Атомный радиус
 Энергия ионизации – количество энергии, затрачиваемое при превращении атома в положительно заряженный ион. Первая и вторая энергии ионизации Na (г) Na+ (г) + e- ΔH° 1, m= + 495 к. Дж/моль Na+ (г) Na 2+ (г) + e- ΔH° 1, m= + 4563 к. Дж/моль
Энергия ионизации – количество энергии, затрачиваемое при превращении атома в положительно заряженный ион. Первая и вторая энергии ионизации Na (г) Na+ (г) + e- ΔH° 1, m= + 495 к. Дж/моль Na+ (г) Na 2+ (г) + e- ΔH° 1, m= + 4563 к. Дж/моль
 1. Элементы с низкой энергией ионизации образуют ионные соединения к. Дж/моль Ø Li Ø Na Ø Cs 520 497 376
1. Элементы с низкой энергией ионизации образуют ионные соединения к. Дж/моль Ø Li Ø Na Ø Cs 520 497 376
 2. Элементы с промежуточной энергией ионизации образуют ковалентные (молекулярные) соединения за счет спаривания электронов с другими атомами. к. Дж/моль Ø B ØC ØP 801 1086 1012
2. Элементы с промежуточной энергией ионизации образуют ковалентные (молекулярные) соединения за счет спаривания электронов с другими атомами. к. Дж/моль Ø B ØC ØP 801 1086 1012
 3. Элементы с очень высокой энергией ионизации часто присоединяют электрон с образованием отрицательных ионов. к. Дж/моль Ø O ØF Ø Cl 1314 1681 1251
3. Элементы с очень высокой энергией ионизации часто присоединяют электрон с образованием отрицательных ионов. к. Дж/моль Ø O ØF Ø Cl 1314 1681 1251
 Ио нный ра диус — характерный размер шарообразных ионов, применяемый для вычисления межатомных расстояний в ионных соединениях. Понятие ионный радиус основано на предположении, что размеры ионов не зависят от состава молекул, в которые они входят. На него влияет количество электронных оболочек и плотность упаковки атомов и ионов в кристаллической решётке.
Ио нный ра диус — характерный размер шарообразных ионов, применяемый для вычисления межатомных расстояний в ионных соединениях. Понятие ионный радиус основано на предположении, что размеры ионов не зависят от состава молекул, в которые они входят. На него влияет количество электронных оболочек и плотность упаковки атомов и ионов в кристаллической решётке.
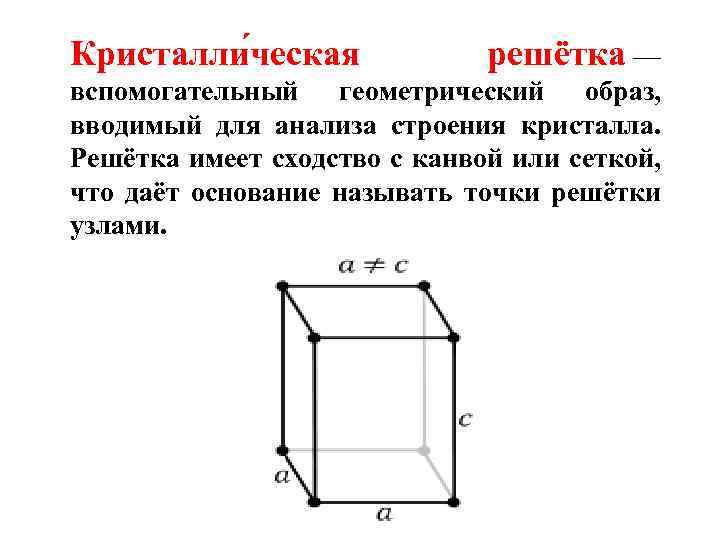 Кристалли ческая решётка — вспомогательный геометрический образ, вводимый для анализа строения кристалла. Решётка имеет сходство с канвой или сеткой, что даёт основание называть точки решётки узлами.
Кристалли ческая решётка — вспомогательный геометрический образ, вводимый для анализа строения кристалла. Решётка имеет сходство с канвой или сеткой, что даёт основание называть точки решётки узлами.
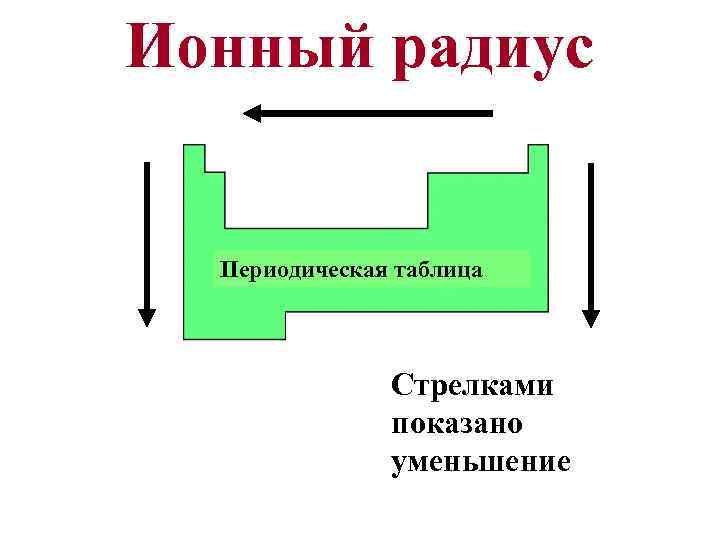 Ионный радиус Периодическая таблица Стрелками показано уменьшение
Ионный радиус Периодическая таблица Стрелками показано уменьшение
 Ионы, имеющие одинаковое количество электронов – изоэлектронные. Внутри изоэлектронных серий ионов ионный радиус уменьшается с увеличением атомного номера.
Ионы, имеющие одинаковое количество электронов – изоэлектронные. Внутри изоэлектронных серий ионов ионный радиус уменьшается с увеличением атомного номера.
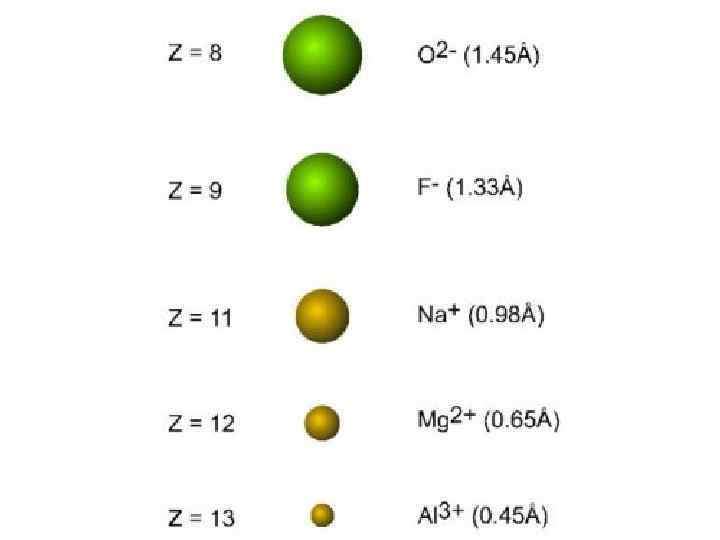
 Сродство к электрону - энергия абсорбции электрона присоединении к изолированному атому в газовой фазе с образованием однозарядного отрицательного иона.
Сродство к электрону - энергия абсорбции электрона присоединении к изолированному атому в газовой фазе с образованием однозарядного отрицательного иона.
 Абсо рбция (лат. absorptio от absorbere — поглощать) — поглощение сорбата всем объёмом сорбента. В технике и химической технологии чаще всего встречается абсорбция (поглощение, растворение) газов жидкостями. Но известны и процессы абсорбции газов и жидкостей кристаллическими и аморфными телами (например, абсорбция водорода металлами, абсорбция низкомолекулярных жидкостей и газов цеолитами, абсорбция нефтепродуктов резинотехническими изделиями и т. п. ).
Абсо рбция (лат. absorptio от absorbere — поглощать) — поглощение сорбата всем объёмом сорбента. В технике и химической технологии чаще всего встречается абсорбция (поглощение, растворение) газов жидкостями. Но известны и процессы абсорбции газов и жидкостей кристаллическими и аморфными телами (например, абсорбция водорода металлами, абсорбция низкомолекулярных жидкостей и газов цеолитами, абсорбция нефтепродуктов резинотехническими изделиями и т. п. ).
 Адсорбция (лат. ad — на, при; sorbeo — поглощаю) — это, в широком смысле, процесс изменения концентрации у поверхности раздела двух фаз, а в более узком и употребительном — это повышение концентрации одного вещества (газ, жидкость) у поверхности другого вещества (жидкость, твердое тело). Поглощаемое вещество, ещё находящееся в объёме фазы, называют адсорбтив, поглощённое — адсорбат. В более узком смысле под адсорбцией часто понимают поглощение примеси из газа или жидкости твёрдым веществом (в случае газа и жидкости) или жидкостью (в случае газа) — адсорбентом. При этом, как и в общем случае адсорбции, происходит концентрирование примеси на границе раздела адсорбентжидкость либо адсорбент-газ. Процесс, обратный адсорбции, то есть перенос вещества с поверхности раздела фаз в объём фазы, называется десорбция.
Адсорбция (лат. ad — на, при; sorbeo — поглощаю) — это, в широком смысле, процесс изменения концентрации у поверхности раздела двух фаз, а в более узком и употребительном — это повышение концентрации одного вещества (газ, жидкость) у поверхности другого вещества (жидкость, твердое тело). Поглощаемое вещество, ещё находящееся в объёме фазы, называют адсорбтив, поглощённое — адсорбат. В более узком смысле под адсорбцией часто понимают поглощение примеси из газа или жидкости твёрдым веществом (в случае газа и жидкости) или жидкостью (в случае газа) — адсорбентом. При этом, как и в общем случае адсорбции, происходит концентрирование примеси на границе раздела адсорбентжидкость либо адсорбент-газ. Процесс, обратный адсорбции, то есть перенос вещества с поверхности раздела фаз в объём фазы, называется десорбция.
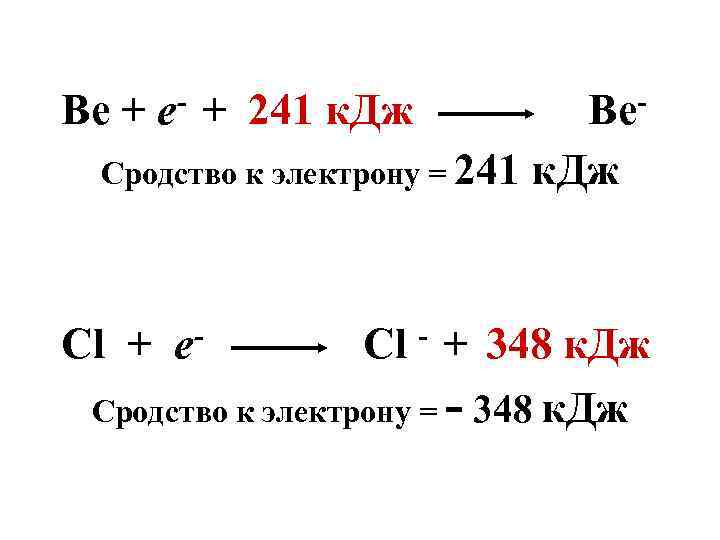 Be + 241 к. Дж Be Сродство к электрону = 241 к. Дж Cl + e- Cl - + 348 к. Дж Сродство к электрону = - 348 к. Дж
Be + 241 к. Дж Be Сродство к электрону = 241 к. Дж Cl + e- Cl - + 348 к. Дж Сродство к электрону = - 348 к. Дж
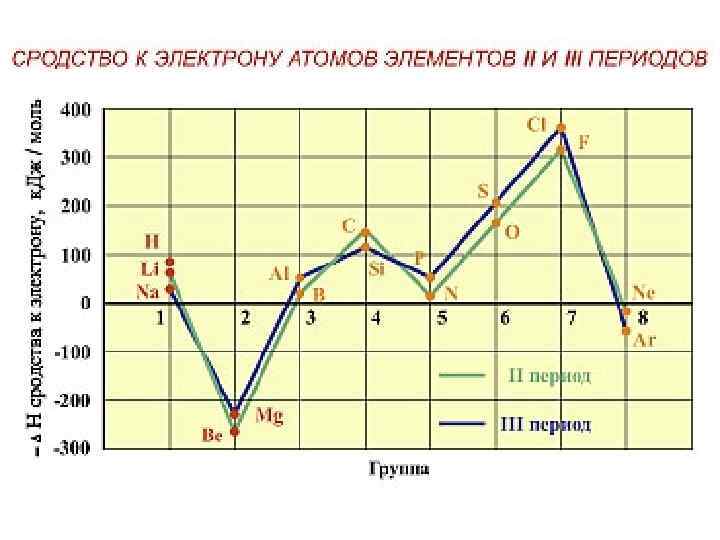
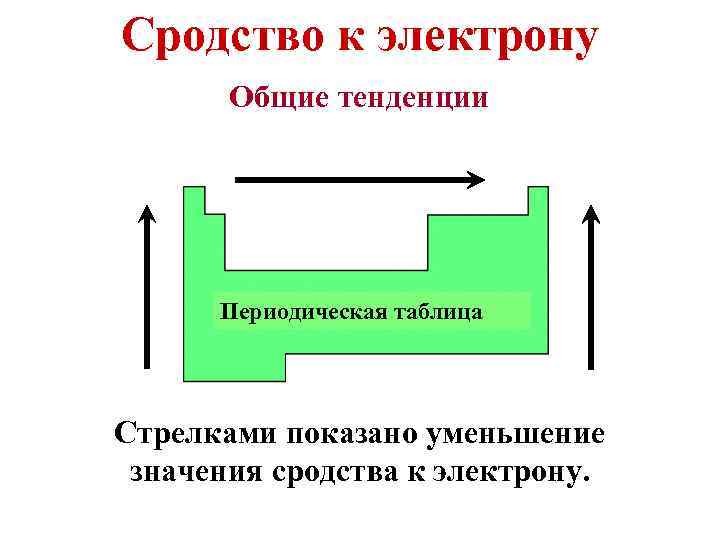 Сродство к электрону Общие тенденции Периодическая таблица Стрелками показано уменьшение значения сродства к электрону.
Сродство к электрону Общие тенденции Периодическая таблица Стрелками показано уменьшение значения сродства к электрону.
 Электроотрицательность - способность атомов притягивать(присоединять) электроны в химических соединениях с другими элементами.
Электроотрицательность - способность атомов притягивать(присоединять) электроны в химических соединениях с другими элементами.
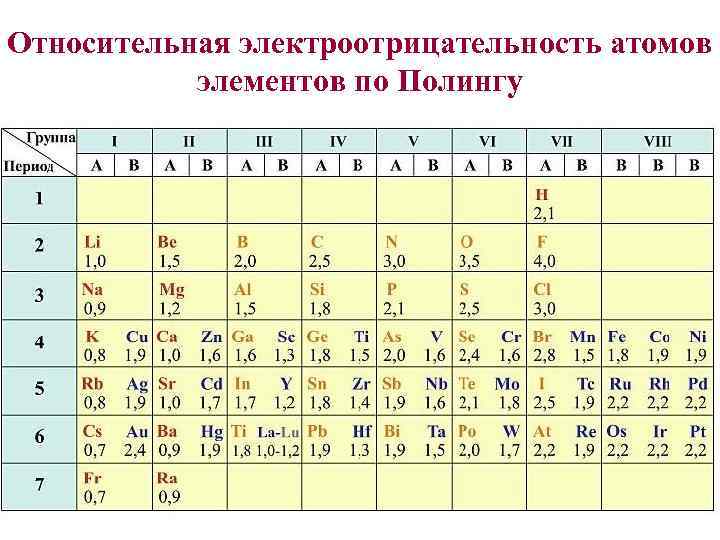 Относительная электроотрицательность атомов элементов по Полингу
Относительная электроотрицательность атомов элементов по Полингу
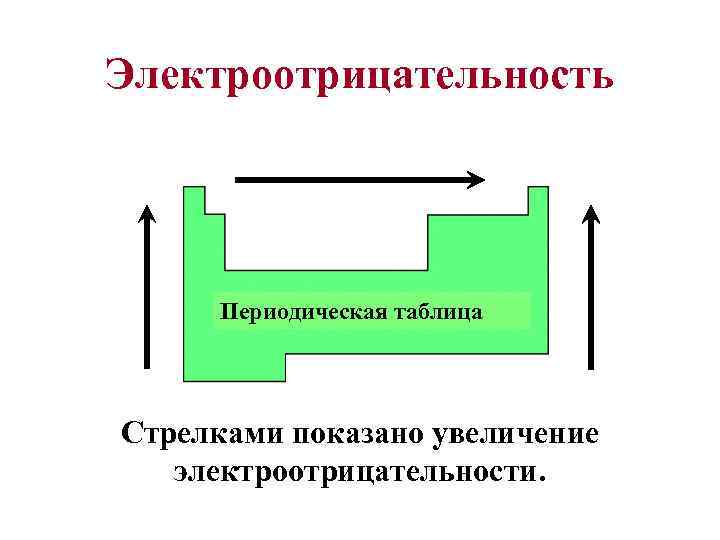 Электроотрицательность Периодическая таблица Стрелками показано увеличение электроотрицательности.
Электроотрицательность Периодическая таблица Стрелками показано увеличение электроотрицательности.
 Спасибо за внимание!
Спасибо за внимание!


