Lecture_04_2017.ppt
- Количество слайдов: 156
 ЛЕКЦИЯ № 4 ПАТОЛОГИЯ РЕАКТИВНОСТИ НАРУШЕНИЯ ИММУННОЙ СИСТЕМЫ АЛЛЕРГИЯ Зав. кафедрой – проф. Вастьянов Р. С. https: //www. facebook. com/groups/1931771850426027/ vastyanov@odmu. edu
ЛЕКЦИЯ № 4 ПАТОЛОГИЯ РЕАКТИВНОСТИ НАРУШЕНИЯ ИММУННОЙ СИСТЕМЫ АЛЛЕРГИЯ Зав. кафедрой – проф. Вастьянов Р. С. https: //www. facebook. com/groups/1931771850426027/ vastyanov@odmu. edu
 УБЕДИТЕЛЬНАЯ ПРОСЬБА!
УБЕДИТЕЛЬНАЯ ПРОСЬБА!
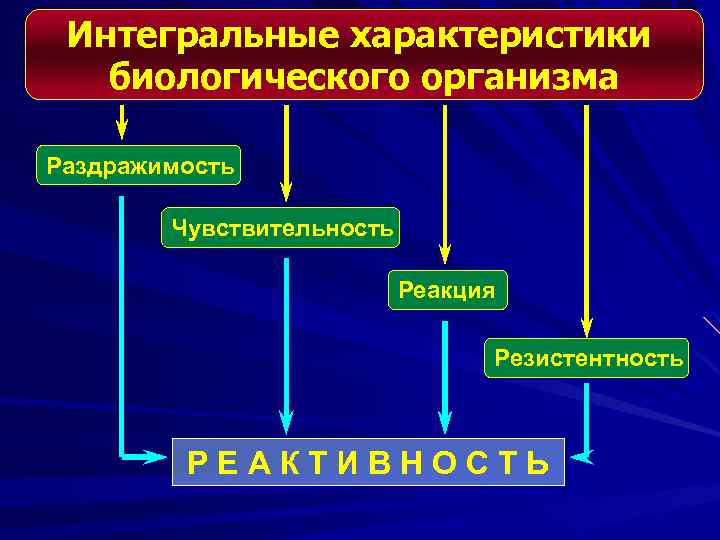 Интегральные характеристики биологического организма Раздражимость Чувствительность Реакция Резистентность Р Е А К Т И В Н О С Т Ь
Интегральные характеристики биологического организма Раздражимость Чувствительность Реакция Резистентность Р Е А К Т И В Н О С Т Ь
 Р Е А К Т И В Н О С Т Ь - это • свойство целостного организма • ДИФФЕРЕНЦИРОВАННО: качественно и количественно, определенным образом • реагировать изменением жизнедеятельности • на воздействия факторов внешней и внутренней среды
Р Е А К Т И В Н О С Т Ь - это • свойство целостного организма • ДИФФЕРЕНЦИРОВАННО: качественно и количественно, определенным образом • реагировать изменением жизнедеятельности • на воздействия факторов внешней и внутренней среды
 Критерии оценки и виды реактивности организма #1 Критерии Биологические факторы, определяющие реактивность: Виды реактивности • видовая • групповая: - возрастная, - половая, - конституциональная • индивидуальная Степень специфичности реакции организма на воздействие: • специфическая • неспецифическая
Критерии оценки и виды реактивности организма #1 Критерии Биологические факторы, определяющие реактивность: Виды реактивности • видовая • групповая: - возрастная, - половая, - конституциональная • индивидуальная Степень специфичности реакции организма на воздействие: • специфическая • неспецифическая
 Критерии оценки и виды реактивности организма #2 Критерии Выраженность реакции на воздействие: Виды реактивности • нормергическая • гиперергическая • гипоергическая Природа фактора, вызывающего ответ организма • иммуногенная Природа фактора, вызывающего ответ организма • физиологическая • неиммуногенная • патологическая
Критерии оценки и виды реактивности организма #2 Критерии Выраженность реакции на воздействие: Виды реактивности • нормергическая • гиперергическая • гипоергическая Природа фактора, вызывающего ответ организма • иммуногенная Природа фактора, вызывающего ответ организма • физиологическая • неиммуногенная • патологическая
 ТИПОВЫЕ НАРУШЕНИЯ РЕАКТИВНОСТИ ОРГАНИЗМА Неиммуногенной природы • диатезы • экстремальные состояния • фобии • фазовые состояния • другие Иммуногенной природы Иммунопатологические состояния и реакции
ТИПОВЫЕ НАРУШЕНИЯ РЕАКТИВНОСТИ ОРГАНИЗМА Неиммуногенной природы • диатезы • экстремальные состояния • фобии • фазовые состояния • другие Иммуногенной природы Иммунопатологические состояния и реакции
 Гисто-гематические барьеры #1 … комплекс физиологических механизмов, регулирующих обменные процессы между кровью и тканями, обеспечивающих тем самым постоянство состава и физико-химических свойств тканевой жидкости, а также задерживающих переход в нее чужеродных веществ из крови … внутренние барьерные структуры между кровью и органами, между кровью и тканевыми жидкостями … благодаря не только избирательной, но и меняющейся проницаемости, регулируют поступление к клеткам из крови необходимых пластических и энергетических материалов и своевременный отток продуктов клеточного обмена
Гисто-гематические барьеры #1 … комплекс физиологических механизмов, регулирующих обменные процессы между кровью и тканями, обеспечивающих тем самым постоянство состава и физико-химических свойств тканевой жидкости, а также задерживающих переход в нее чужеродных веществ из крови … внутренние барьерные структуры между кровью и органами, между кровью и тканевыми жидкостями … благодаря не только избирательной, но и меняющейся проницаемости, регулируют поступление к клеткам из крови необходимых пластических и энергетических материалов и своевременный отток продуктов клеточного обмена
 Гисто-гематические барьеры #2 Изолирующие: • гематоплацентарный Не изолирующие: • гемато-энцефалический • гематоликворный • гематонейрональный (ПНС) • существуют в миокарде, ске летных мышцах, мозговом • гематотестикулярный слое надпочечников, паращи товидных железах • барьер хрусталика глаза • желчные капилляры печени • позволяют белку проникать из крови в интерстициальную • кора надпочечников жидкость, однако ограничивают его транспорт в микроокружение • пигментный эпителий глаза (между сосудистой и сетчатой оболочками) и цитоплазму паренхиматозных клеток • гематоофтальмический (на уровне цилиарных отростков глаза) Частично изолирующие: • барьер щитовидной железы • барьер концевых долек поджелудочной железы
Гисто-гематические барьеры #2 Изолирующие: • гематоплацентарный Не изолирующие: • гемато-энцефалический • гематоликворный • гематонейрональный (ПНС) • существуют в миокарде, ске летных мышцах, мозговом • гематотестикулярный слое надпочечников, паращи товидных железах • барьер хрусталика глаза • желчные капилляры печени • позволяют белку проникать из крови в интерстициальную • кора надпочечников жидкость, однако ограничивают его транспорт в микроокружение • пигментный эпителий глаза (между сосудистой и сетчатой оболочками) и цитоплазму паренхиматозных клеток • гематоофтальмический (на уровне цилиарных отростков глаза) Частично изолирующие: • барьер щитовидной железы • барьер концевых долек поджелудочной железы
 Гисто-гематические барьеры #3 Функции: 1. Защитная 2. Поддержание/регуляция реактивности 3. Регуляторная
Гисто-гематические барьеры #3 Функции: 1. Защитная 2. Поддержание/регуляция реактивности 3. Регуляторная
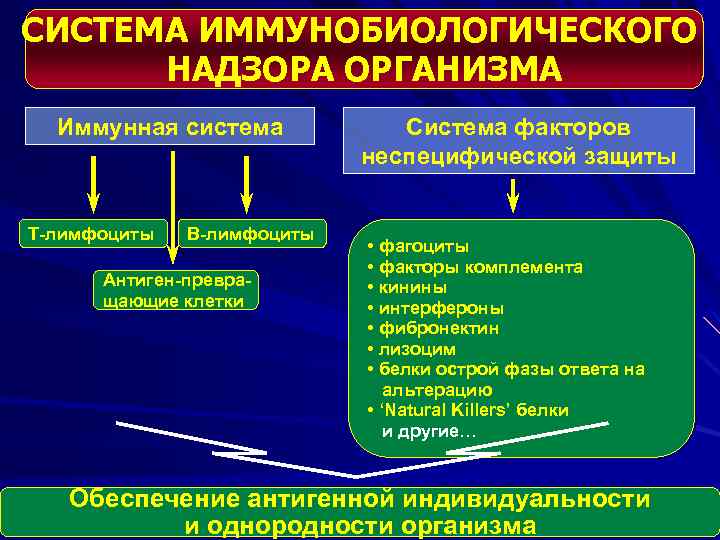 СИСТЕМА ИММУНОБИОЛОГИЧЕСКОГО НАДЗОРА ОРГАНИЗМА Иммунная система Т-лимфоциты В-лимфоциты Антиген-превращающие клетки Система факторов неспецифической защиты • фагоциты • факторы комплемента • кинины • интерфероны • фибронектин • лизоцим • белки острой фазы ответа на альтерацию • ‘Natural Killers’ белки и другие… Обеспечение антигенной индивидуальности и однородности организма
СИСТЕМА ИММУНОБИОЛОГИЧЕСКОГО НАДЗОРА ОРГАНИЗМА Иммунная система Т-лимфоциты В-лимфоциты Антиген-превращающие клетки Система факторов неспецифической защиты • фагоциты • факторы комплемента • кинины • интерфероны • фибронектин • лизоцим • белки острой фазы ответа на альтерацию • ‘Natural Killers’ белки и другие… Обеспечение антигенной индивидуальности и однородности организма
 И М М У Н И Т Е Т - это • Физиологическая форма иммуногенной реактивности • Формируется в результате реализации наследуемой генетической программы и/или при контакте клеток иммунной системы с чужеродным антигеном • Обеспечивает постоянный и однородный антигенный состав организма • Реализуется путем обнаружения и, как правило, деструкции, инактивации и элиминации чужеродного антигена • Характеризуется повышенной резистентностью организма к нему
И М М У Н И Т Е Т - это • Физиологическая форма иммуногенной реактивности • Формируется в результате реализации наследуемой генетической программы и/или при контакте клеток иммунной системы с чужеродным антигеном • Обеспечивает постоянный и однородный антигенный состав организма • Реализуется путем обнаружения и, как правило, деструкции, инактивации и элиминации чужеродного антигена • Характеризуется повышенной резистентностью организма к нему
 ВОЗМОЖНЫЕ ЭФФЕКТЫ АНТИГЕНА В ОРГАНИЗМЕ АНТИГЕН иммуноген И М М У Н И Т Е Т аллерген толероген А Л Л Е Р Г И Я ТОЛЕРАНТНОСТЬ Антиген - вещество экзо- или эндогенного происхождения, как правило, вызывающее иммунную реакцию
ВОЗМОЖНЫЕ ЭФФЕКТЫ АНТИГЕНА В ОРГАНИЗМЕ АНТИГЕН иммуноген И М М У Н И Т Е Т аллерген толероген А Л Л Е Р Г И Я ТОЛЕРАНТНОСТЬ Антиген - вещество экзо- или эндогенного происхождения, как правило, вызывающее иммунную реакцию
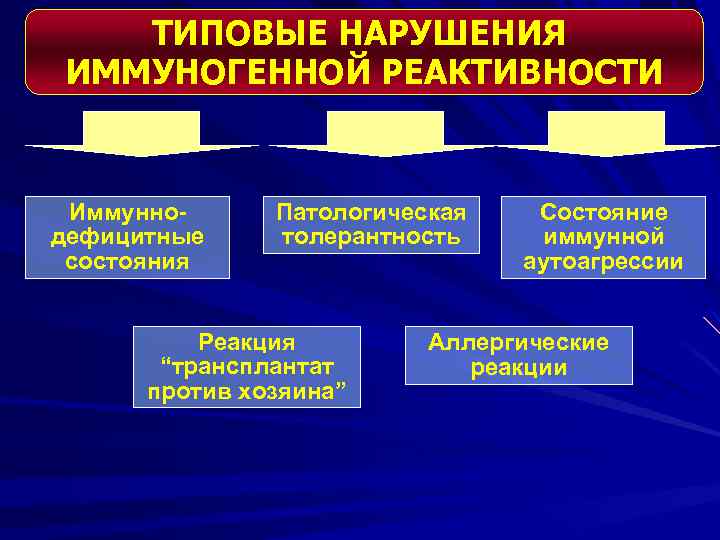 ТИПОВЫЕ НАРУШЕНИЯ ИММУНОГЕННОЙ РЕАКТИВНОСТИ Иммуннодефицитные состояния Патологическая толерантность Реакция “трансплантат против хозяина” Состояние иммунной аутоагрессии Аллергические реакции
ТИПОВЫЕ НАРУШЕНИЯ ИММУНОГЕННОЙ РЕАКТИВНОСТИ Иммуннодефицитные состояния Патологическая толерантность Реакция “трансплантат против хозяина” Состояние иммунной аутоагрессии Аллергические реакции
 ИММУНОДЕФИЦИТНЫЕ СОСТОЯНИЯ • Типовая форма патологии системы иммуно биологического надзора • Характеризуется снижением эффективности или полной её неспособностью осуществлять реакции обнаружения, деструкции и элиминации чужеродного антигена
ИММУНОДЕФИЦИТНЫЕ СОСТОЯНИЯ • Типовая форма патологии системы иммуно биологического надзора • Характеризуется снижением эффективности или полной её неспособностью осуществлять реакции обнаружения, деструкции и элиминации чужеродного антигена
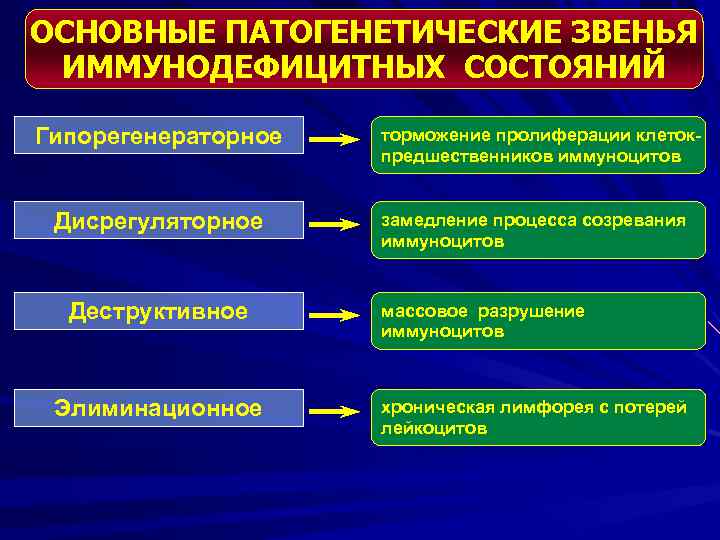 ОСНОВНЫЕ ПАТОГЕНЕТИЧЕСКИЕ ЗВЕНЬЯ ИММУНОДЕФИЦИТНЫХ СОСТОЯНИЙ Гипорегенераторное Дисрегуляторное Деструктивное Элиминационное торможение пролиферации клетокпредшественников иммуноцитов замедление процесса созревания иммуноцитов массовое разрушение иммуноцитов хроническая лимфорея с потерей лейкоцитов
ОСНОВНЫЕ ПАТОГЕНЕТИЧЕСКИЕ ЗВЕНЬЯ ИММУНОДЕФИЦИТНЫХ СОСТОЯНИЙ Гипорегенераторное Дисрегуляторное Деструктивное Элиминационное торможение пролиферации клетокпредшественников иммуноцитов замедление процесса созревания иммуноцитов массовое разрушение иммуноцитов хроническая лимфорея с потерей лейкоцитов
 ВАРИАНТЫ ПАТОГЕНЕЗА ИММУНОДЕФИЦИТНЫХ СОСТОЯНИЙ Лейкопенический Дисфункциональный Дисрегуляторный
ВАРИАНТЫ ПАТОГЕНЕЗА ИММУНОДЕФИЦИТНЫХ СОСТОЯНИЙ Лейкопенический Дисфункциональный Дисрегуляторный
 ВИДЫ ТОЛЕРАНТНОСТИ Физиологическая Патологическая Индуцированная (медицинская)
ВИДЫ ТОЛЕРАНТНОСТИ Физиологическая Патологическая Индуцированная (медицинская)
 Механизмы физиологической толерантности Клональная анергия Тлимфоцитов, не подвергшихся ко -стимуляции Клональная делеция апоптоз лимфоцитов, активированных эндогенными антигенами Центральная селекция Клональноселекционный Изоляционный Депрессия Т-киллеров Т-супрессорами ликвидация аутоагрессивных Т-лимфоцитов в тимусе
Механизмы физиологической толерантности Клональная анергия Тлимфоцитов, не подвергшихся ко -стимуляции Клональная делеция апоптоз лимфоцитов, активированных эндогенными антигенами Центральная селекция Клональноселекционный Изоляционный Депрессия Т-киллеров Т-супрессорами ликвидация аутоагрессивных Т-лимфоцитов в тимусе
 ПАТОЛОГИЧЕСКАЯ ТОЛЕРАНТНОСТЬ (лат. tolerantia - терпимость, переносимость) • Типовая форма патологии системы иммуно биологического надзора • Характеризуется отсутствием или низкой эффективностью её реакций по обнаружению, деструкции и элиминации из организма носителя чужеродного антигена
ПАТОЛОГИЧЕСКАЯ ТОЛЕРАНТНОСТЬ (лат. tolerantia - терпимость, переносимость) • Типовая форма патологии системы иммуно биологического надзора • Характеризуется отсутствием или низкой эффективностью её реакций по обнаружению, деструкции и элиминации из организма носителя чужеродного антигена
 Механизмы патологической толерантности Активация Т- и В-лимфоцитов – супрессоров Экранирование чужеродных антигенных детерминант иммуноглобулинами Антигенная “перегрузка” иммунной системы Недостаточна ко-стимуляция Т-лимфоцитов Иммунодефицитные состояния Апоптоз цитотоксических Т-лимфоцитов
Механизмы патологической толерантности Активация Т- и В-лимфоцитов – супрессоров Экранирование чужеродных антигенных детерминант иммуноглобулинами Антигенная “перегрузка” иммунной системы Недостаточна ко-стимуляция Т-лимфоцитов Иммунодефицитные состояния Апоптоз цитотоксических Т-лимфоцитов
 РЕАКЦИЯ “ТРАНСПЛАНТАТ ПРОТИВ ХОЗЯИНА” #1 • Типовая форма патологии иммунитета и жизнедея тельности организма • Развивается в результате трансплантации реципиенту (“хозяину”) тканей, содержащих иммуноциты • Характеризуется повреждением тканей и органов с развитием иммунодефицттного состояния
РЕАКЦИЯ “ТРАНСПЛАНТАТ ПРОТИВ ХОЗЯИНА” #1 • Типовая форма патологии иммунитета и жизнедея тельности организма • Развивается в результате трансплантации реципиенту (“хозяину”) тканей, содержащих иммуноциты • Характеризуется повреждением тканей и органов с развитием иммунодефицттного состояния
 РЕАКЦИЯ “ТРАНСПЛАНТАТ ПРОТИВ ХОЗЯИНА” #2 Причина • иммуноциты трансплан тата (костного мозга, селезенки, крови, фрагментов тонкого кишечника, печени, лейкоцитарной массы) Условия • генетическая (антигенная) чужеродность донора и реципиента • наличие в трансплантате клеток, способных к актив ному иммунному ответу • неспособность реципиента уничтожить или отторгнуть трансплантат Патогенез - повреждение органов и тканей реципиента иммунными клетками донора
РЕАКЦИЯ “ТРАНСПЛАНТАТ ПРОТИВ ХОЗЯИНА” #2 Причина • иммуноциты трансплан тата (костного мозга, селезенки, крови, фрагментов тонкого кишечника, печени, лейкоцитарной массы) Условия • генетическая (антигенная) чужеродность донора и реципиента • наличие в трансплантате клеток, способных к актив ному иммунному ответу • неспособность реципиента уничтожить или отторгнуть трансплантат Патогенез - повреждение органов и тканей реципиента иммунными клетками донора
 АЛЛЕРГИЯ - это • ПАТОЛОГИЧЕСКАЯ ФОРМА ИММУНОГЕННОЙ РЕАКТИВНОСТИ • ТИПОВОЙ ПАТОЛОГИЧЕСКИЙ ПРОЦЕСС • Формируется, как правило, в результате повторного контакта клеток иммунной системы с чужеродным антигеном • Сопровождается изменением (обычно - повышением) чувствительности к данному антигену • Характеризуется обнаружением и часто (но не всегда!) деструкцией и элиминацией чужеродного антигена, повреждением собственных структур организма, снижением его адаптивных возможностей и нарушением жизнедеятельности
АЛЛЕРГИЯ - это • ПАТОЛОГИЧЕСКАЯ ФОРМА ИММУНОГЕННОЙ РЕАКТИВНОСТИ • ТИПОВОЙ ПАТОЛОГИЧЕСКИЙ ПРОЦЕСС • Формируется, как правило, в результате повторного контакта клеток иммунной системы с чужеродным антигеном • Сопровождается изменением (обычно - повышением) чувствительности к данному антигену • Характеризуется обнаружением и часто (но не всегда!) деструкцией и элиминацией чужеродного антигена, повреждением собственных структур организма, снижением его адаптивных возможностей и нарушением жизнедеятельности
 АЛЛЕРГИЯ – это проявление иммунологической реактивности, как и иммунитет. Это пример повышенной реактивности и сниженной резистентности Аллергия и иммунитет имеют защитный характер и направлены на поддержание гомеостаза организма (защищают от генетически чужеродной информации) Аллергия и иммунитет имеют общие механизмы развития
АЛЛЕРГИЯ – это проявление иммунологической реактивности, как и иммунитет. Это пример повышенной реактивности и сниженной резистентности Аллергия и иммунитет имеют защитный характер и направлены на поддержание гомеостаза организма (защищают от генетически чужеродной информации) Аллергия и иммунитет имеют общие механизмы развития
 Отличие аллергии от иммунитета: • Аллергия является патологической формой иммунологической реактивности, это патологическое течение иммунного ответа, которое сопровождается повреждением тканей организма
Отличие аллергии от иммунитета: • Аллергия является патологической формой иммунологической реактивности, это патологическое течение иммунного ответа, которое сопровождается повреждением тканей организма
 Этиология аллергии Вещества антигенной природы, вызывающие аллергию, называются аллергенами. Аллерген - главный этиологический фактор аллергии. Свойства аллергена: – генетическая чужеродность – макромолекулярность – белковая природа – иммуногенность
Этиология аллергии Вещества антигенной природы, вызывающие аллергию, называются аллергенами. Аллерген - главный этиологический фактор аллергии. Свойства аллергена: – генетическая чужеродность – макромолекулярность – белковая природа – иммуногенность
 Гаптены (неполные антигены) приобретают антигенные свойства в соединении с белками организма. Например, простые химические вещества (йод, бром), низкомолекулярные лекарственные препараты
Гаптены (неполные антигены) приобретают антигенные свойства в соединении с белками организма. Например, простые химические вещества (йод, бром), низкомолекулярные лекарственные препараты
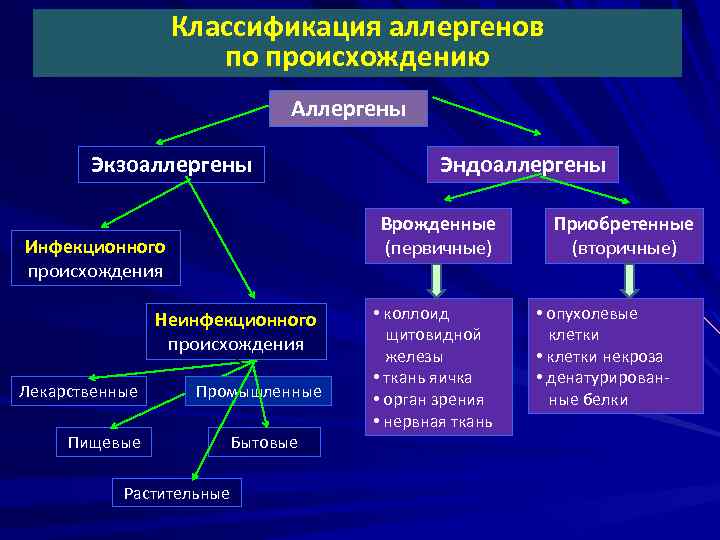 Классификация аллергенов по происхождению Аллергены Экзоаллергены Врожденные (первичные) Инфекционного происхождения Неинфекционного происхождения Лекарственные Эндоаллергены Промышленные Пищевые Растительные Бытовые • коллоид щитовидной железы • ткань яичка • орган зрения • нервная ткань Приобретенные (вторичные) • опухолевые клетки • клетки некроза • денатурированные белки
Классификация аллергенов по происхождению Аллергены Экзоаллергены Врожденные (первичные) Инфекционного происхождения Неинфекционного происхождения Лекарственные Эндоаллергены Промышленные Пищевые Растительные Бытовые • коллоид щитовидной железы • ткань яичка • орган зрения • нервная ткань Приобретенные (вторичные) • опухолевые клетки • клетки некроза • денатурированные белки
 Наиболее распространенные экзоаллергены Пыльца луговых трав и деревьев Перхоть домашних животных Плесневые грибки Бытовые клещи
Наиболее распространенные экзоаллергены Пыльца луговых трав и деревьев Перхоть домашних животных Плесневые грибки Бытовые клещи
 Пыльцевые аллергены. Поллиноз – классическое аллергическое заболевание. Развивается при повторном контакте сенсибилизированного организма с пыльцой растений. Характеризуется острым аллергическим воспалением слизистых оболочек дыхательных путей, глаз, кожи.
Пыльцевые аллергены. Поллиноз – классическое аллергическое заболевание. Развивается при повторном контакте сенсибилизированного организма с пыльцой растений. Характеризуется острым аллергическим воспалением слизистых оболочек дыхательных путей, глаз, кожи.
 Бытовые аллергены. Клещ домашней пыли § Симптомы аллергии проявляются круглый год при нахождении внутри помещений § Высокая концентрация антигена § Часто ассоциируется с аллергенами домашних животных ØВ 70% - 80% случаев БА связана с бытовыми клещами § Клещи имеют размер 10 -24 мкм § 1 гр домашней пыли содержит 240 тыс. клещей
Бытовые аллергены. Клещ домашней пыли § Симптомы аллергии проявляются круглый год при нахождении внутри помещений § Высокая концентрация антигена § Часто ассоциируется с аллергенами домашних животных ØВ 70% - 80% случаев БА связана с бытовыми клещами § Клещи имеют размер 10 -24 мкм § 1 гр домашней пыли содержит 240 тыс. клещей
 Эпидермальные аллергены. Шерсть и перхоть домашних животных
Эпидермальные аллергены. Шерсть и перхоть домашних животных
 Пищевые аллергены
Пищевые аллергены
 Классификация аллергических реакций 1. Согласно классификации, предложенной Cooke (1930 г. ), по скорости и механизмам развития аллергические реакции подразделяются на 2 типа: гиперчувствительность немедленного типа гиперчувствительность замедленного типа
Классификация аллергических реакций 1. Согласно классификации, предложенной Cooke (1930 г. ), по скорости и механизмам развития аллергические реакции подразделяются на 2 типа: гиперчувствительность немедленного типа гиперчувствительность замедленного типа
 2. По классифкации Gell и Coombs (1969 г. ) в зависимости от характера иммунного повреждения тканей и органов аллергические реакции подразделяются на 4 типа: реагиновый (анафилактический) ГНТ цитотоксический иммунокомплексный клеточноопосредованный (ГЗТ)
2. По классифкации Gell и Coombs (1969 г. ) в зависимости от характера иммунного повреждения тканей и органов аллергические реакции подразделяются на 4 типа: реагиновый (анафилактический) ГНТ цитотоксический иммунокомплексный клеточноопосредованный (ГЗТ)
 3. Андрей Дмитриевич Адо (1963 г. ) по механизмам развития разделял аллергические реакции на 2 типа: истинные ложные (псевдоаллергические) Псевдоаллергические реакции имеют только 2 стадии – патохимическую и патофизиологическую. Главная – иммунологическая стадия – отсутствует. Нет антител, нет иммунных комплексов, болезнетворный фактор самостоятельно стимулирует образование медиаторов повреждения.
3. Андрей Дмитриевич Адо (1963 г. ) по механизмам развития разделял аллергические реакции на 2 типа: истинные ложные (псевдоаллергические) Псевдоаллергические реакции имеют только 2 стадии – патохимическую и патофизиологическую. Главная – иммунологическая стадия – отсутствует. Нет антител, нет иммунных комплексов, болезнетворный фактор самостоятельно стимулирует образование медиаторов повреждения.
 Общий патогенез аллергических реакций В развитии аллергических реакций выделяют 3 стадии: • иммунологическую • патохимическую • патофизиологическую
Общий патогенез аллергических реакций В развитии аллергических реакций выделяют 3 стадии: • иммунологическую • патохимическую • патофизиологическую
 1. Иммунологическая стадия (стадия иммунных реакций) с момента первичного попадания аллергена в организм до повторной встречи с ним. Итог – образование иммунного комплекса. 1. Период сенсибилизации → образуются антитела или сенсибилизированные Тлимфоциты 2. Период повторного поступления аллергена в сенсибилизированный организм → образуется иммунный комплекс антиген+антитело антиген+сенсибилизированный Т-лимфоцит
1. Иммунологическая стадия (стадия иммунных реакций) с момента первичного попадания аллергена в организм до повторной встречи с ним. Итог – образование иммунного комплекса. 1. Период сенсибилизации → образуются антитела или сенсибилизированные Тлимфоциты 2. Период повторного поступления аллергена в сенсибилизированный организм → образуется иммунный комплекс антиген+антитело антиген+сенсибилизированный Т-лимфоцит
 2. Патохимическая стадия (стадия биохимических реакций) характеризуется образованием и выделением биологически активных веществ (медиаторов аллергии), поступающих в кровь и ткани. Пусковым стимулом для этих процессов служат иммунные комплексы. 3. Патофизиологическая стадия (стадия клинических проявлений) характеризуется повреждающим действием медиаторов на клетки, ткани и органы. Эта стадия включает в себя клинические проявление возникающих в организме нарушений в виде аллергических реакций и заболеваний
2. Патохимическая стадия (стадия биохимических реакций) характеризуется образованием и выделением биологически активных веществ (медиаторов аллергии), поступающих в кровь и ткани. Пусковым стимулом для этих процессов служат иммунные комплексы. 3. Патофизиологическая стадия (стадия клинических проявлений) характеризуется повреждающим действием медиаторов на клетки, ткани и органы. Эта стадия включает в себя клинические проявление возникающих в организме нарушений в виде аллергических реакций и заболеваний
 Иммунопатологические реакции I типа (синонимы: реагиновый тип, немедленная аллергия, анафилаксия, атопия)
Иммунопатологические реакции I типа (синонимы: реагиновый тип, немедленная аллергия, анафилаксия, атопия)
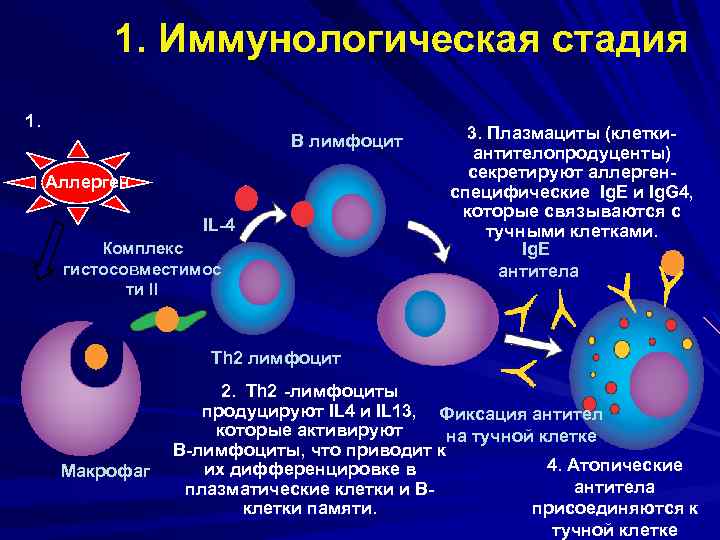 1. Иммунологическая стадия 1. B лимфоцит Аллерген IL-4 Комплекс гистосовместимос ти II 3. Плазмациты (клеткиантителопродуценты) секретируют аллергенспецифические Ig. E и Ig. G 4, которые связываются с тучными клетками. Ig. E антитела Тh 2 лимфоцит Макрофаг 2. Th 2 -лимфоциты продуцируют IL 4 и IL 13, Фиксация антител которые активируют на тучной клетке B-лимфоциты, что приводит к 4. Атопические их дифференцировке в антитела плазматические клетки и Вклетки памяти. присоединяются к тучной клетке
1. Иммунологическая стадия 1. B лимфоцит Аллерген IL-4 Комплекс гистосовместимос ти II 3. Плазмациты (клеткиантителопродуценты) секретируют аллергенспецифические Ig. E и Ig. G 4, которые связываются с тучными клетками. Ig. E антитела Тh 2 лимфоцит Макрофаг 2. Th 2 -лимфоциты продуцируют IL 4 и IL 13, Фиксация антител которые активируют на тучной клетке B-лимфоциты, что приводит к 4. Атопические их дифференцировке в антитела плазматические клетки и Вклетки памяти. присоединяются к тучной клетке
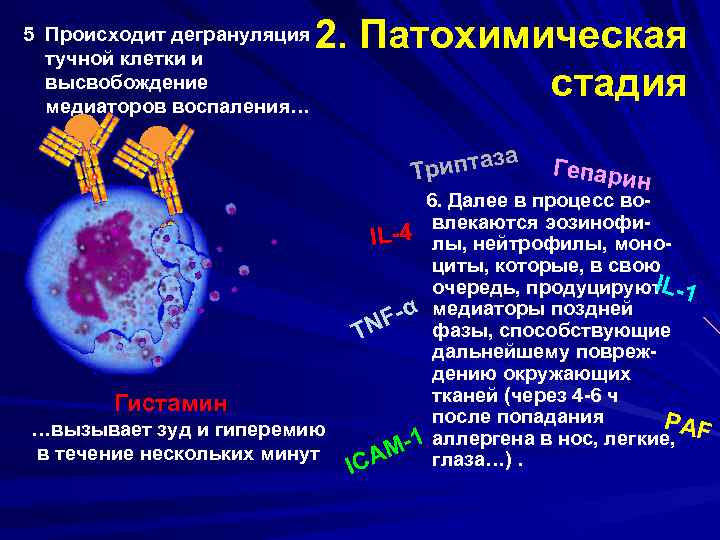 2. Патохимическая стадия 5. Происходит дегрануляция тучной клетки и высвобождение медиаторов воспаления… иптаза Tр Гепари н 6. Далее в процесс вовлекаются эозинофи. L-4 лы, нейтрофилы, моно. I циты, которые, в свою IL очередь, продуцируют -1 F-α медиаторы поздней фазы, способствующие TN дальнейшему повреждению окружающих тканей (через 4 -6 ч Гистамин после попадания PAF …вызывает зуд и гиперемию аллергена в нос, легкие, M-1 глаза…). в течение нескольких минут ICA
2. Патохимическая стадия 5. Происходит дегрануляция тучной клетки и высвобождение медиаторов воспаления… иптаза Tр Гепари н 6. Далее в процесс вовлекаются эозинофи. L-4 лы, нейтрофилы, моно. I циты, которые, в свою IL очередь, продуцируют -1 F-α медиаторы поздней фазы, способствующие TN дальнейшему повреждению окружающих тканей (через 4 -6 ч Гистамин после попадания PAF …вызывает зуд и гиперемию аллергена в нос, легкие, M-1 глаза…). в течение нескольких минут ICA
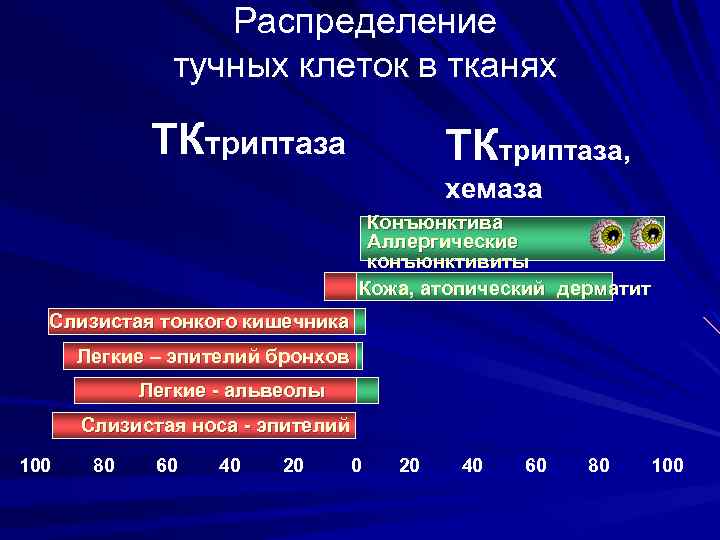 Распределение тучных клеток в тканях ТКтриптаза, хемаза Конъюнктива Аллергические конъюнктивиты Кожа, атопический дерматит Слизистая тонкого кишечника Легкие – эпителий бронхов Легкие - альвеолы Слизистая носа - эпителий 100 80 60 40 20 40 60 80 100
Распределение тучных клеток в тканях ТКтриптаза, хемаза Конъюнктива Аллергические конъюнктивиты Кожа, атопический дерматит Слизистая тонкого кишечника Легкие – эпителий бронхов Легкие - альвеолы Слизистая носа - эпителий 100 80 60 40 20 40 60 80 100
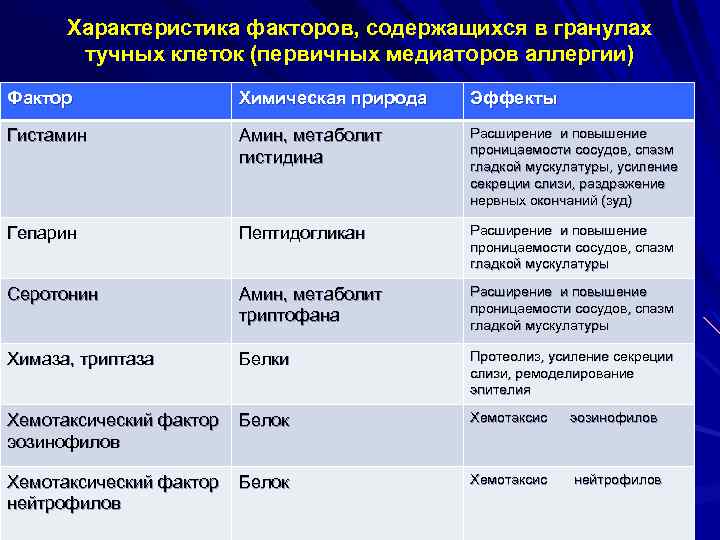 Характеристика факторов, содержащихся в гранулах тучных клеток (первичных медиаторов аллергии) Фактор Химическая природа Эффекты Гистамин Амин, метаболит гистидина Расширение и повышение проницаемости сосудов, спазм гладкой мускулатуры, усиление секреции слизи, раздражение нервных окончаний (зуд) Гепарин Пептидогликан Расширение и повышение проницаемости сосудов, спазм гладкой мускулатуры Серотонин Амин, метаболит триптофана Расширение и повышение проницаемости сосудов, спазм гладкой мускулатуры Химаза, триптаза Белки Протеолиз, усиление секреции слизи, ремоделирование эпителия Хемотаксический фактор эозинофилов Белок Хемотаксис эозинофилов Хемотаксический фактор нейтрофилов Белок Хемотаксис нейтрофилов
Характеристика факторов, содержащихся в гранулах тучных клеток (первичных медиаторов аллергии) Фактор Химическая природа Эффекты Гистамин Амин, метаболит гистидина Расширение и повышение проницаемости сосудов, спазм гладкой мускулатуры, усиление секреции слизи, раздражение нервных окончаний (зуд) Гепарин Пептидогликан Расширение и повышение проницаемости сосудов, спазм гладкой мускулатуры Серотонин Амин, метаболит триптофана Расширение и повышение проницаемости сосудов, спазм гладкой мускулатуры Химаза, триптаза Белки Протеолиз, усиление секреции слизи, ремоделирование эпителия Хемотаксический фактор эозинофилов Белок Хемотаксис эозинофилов Хемотаксический фактор нейтрофилов Белок Хемотаксис нейтрофилов
 Гуморальные факторы, высвобождаемые эффекторными клетками аллергии Группа факторов Тучные клетки Эозинофилы Предобразованные факторы Гистамин, гепарин, хондроитинсульфат, серотонин, протеазы Главный основной белок(MBP), катионный белок эозинофилов(ЕCP), пероксидаза эозинофилов (EPO), нейротоксин эозинофилов (EDT) Быстро синтезируемые факторы Лейкотриены (LTC 4, LTD 4), простагландины (D 2), тромбоксаны, фактор, активирующий тромбоциты (PAF) Лейкотриены (LTC 4, LTD 4) - SASR, простагландины (E, F), фактор, активирующий тромбоциты (PAF) Медленно синтезируемые IL-5, GM-CSF, TNFα, IL-8 факторы IL-3, IL-5, GM-CSF, TGFβ
Гуморальные факторы, высвобождаемые эффекторными клетками аллергии Группа факторов Тучные клетки Эозинофилы Предобразованные факторы Гистамин, гепарин, хондроитинсульфат, серотонин, протеазы Главный основной белок(MBP), катионный белок эозинофилов(ЕCP), пероксидаза эозинофилов (EPO), нейротоксин эозинофилов (EDT) Быстро синтезируемые факторы Лейкотриены (LTC 4, LTD 4), простагландины (D 2), тромбоксаны, фактор, активирующий тромбоциты (PAF) Лейкотриены (LTC 4, LTD 4) - SASR, простагландины (E, F), фактор, активирующий тромбоциты (PAF) Медленно синтезируемые IL-5, GM-CSF, TNFα, IL-8 факторы IL-3, IL-5, GM-CSF, TGFβ
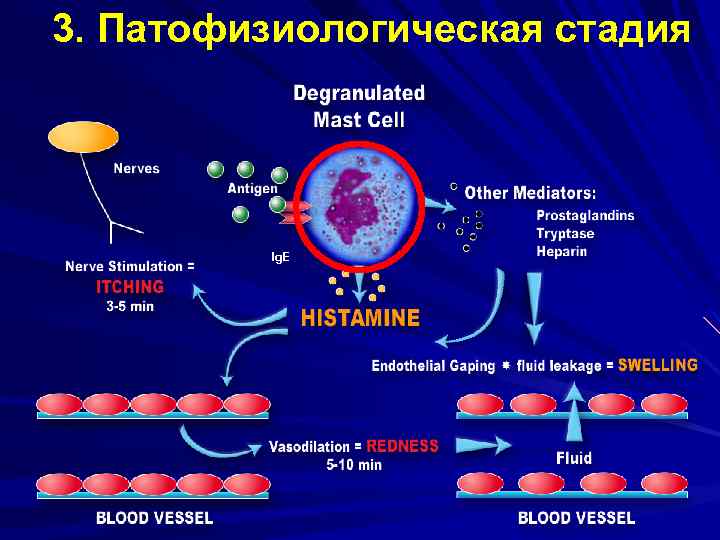 3. Патофизиологическая стадия Ig. E
3. Патофизиологическая стадия Ig. E
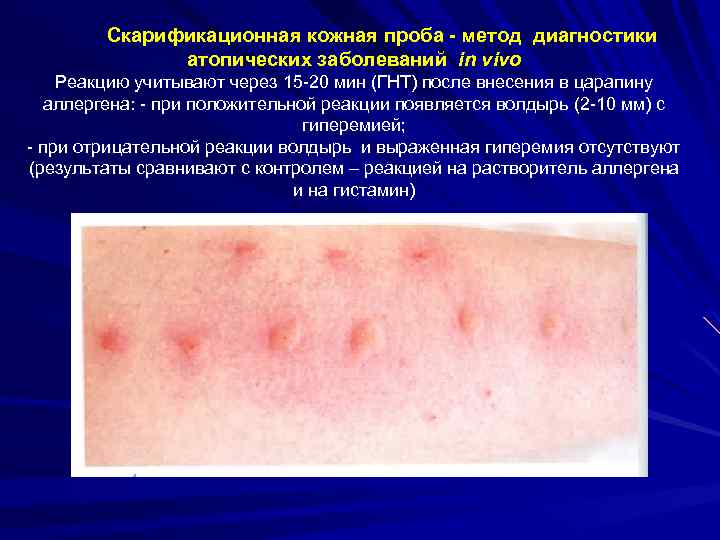 Скарификационная кожная проба - метод диагностики атопических заболеваний in vivo Реакцию учитывают через 15 -20 мин (ГНТ) после внесения в царапину аллергена: - при положительной реакции появляется волдырь (2 -10 мм) с гиперемией; - при отрицательной реакции волдырь и выраженная гиперемия отсутствуют (результаты сравнивают с контролем – реакцией на растворитель аллергена и на гистамин)
Скарификационная кожная проба - метод диагностики атопических заболеваний in vivo Реакцию учитывают через 15 -20 мин (ГНТ) после внесения в царапину аллергена: - при положительной реакции появляется волдырь (2 -10 мм) с гиперемией; - при отрицательной реакции волдырь и выраженная гиперемия отсутствуют (результаты сравнивают с контролем – реакцией на растворитель аллергена и на гистамин)
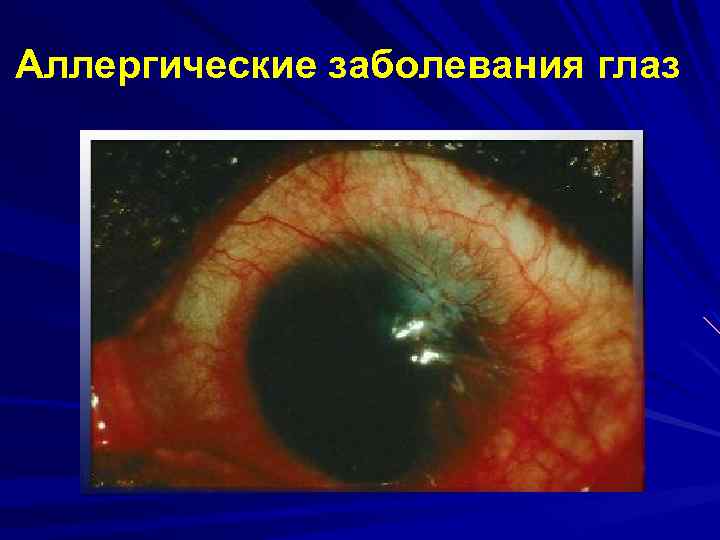 Аллергические заболевания глаз
Аллергические заболевания глаз
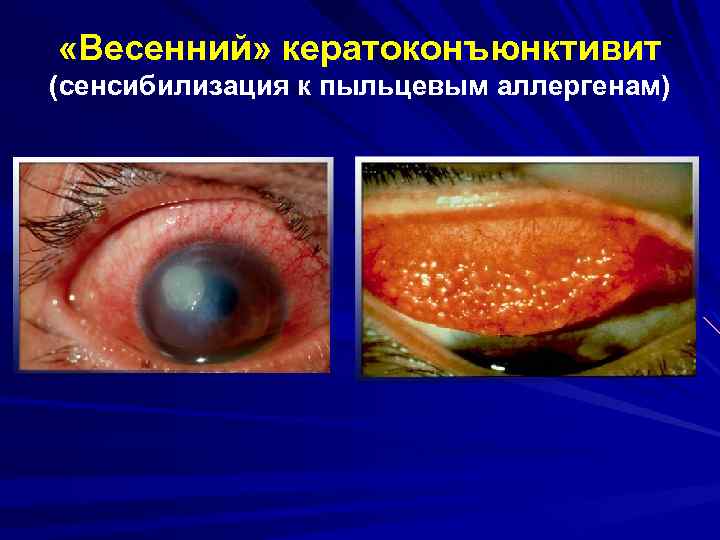 «Весенний» кератоконъюнктивит (сенсибилизация к пыльцевым аллергенам)
«Весенний» кератоконъюнктивит (сенсибилизация к пыльцевым аллергенам)
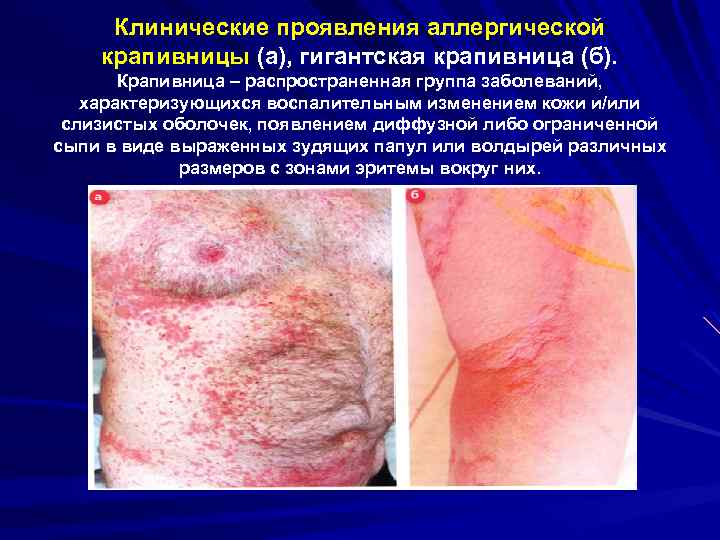 Клинические проявления аллергической крапивницы (а), гигантская крапивница (б). Крапивница – распространенная группа заболеваний, характеризующихся воспалительным изменением кожи и/или слизистых оболочек, появлением диффузной либо ограниченной сыпи в виде выраженных зудящих папул или волдырей различных размеров с зонами эритемы вокруг них.
Клинические проявления аллергической крапивницы (а), гигантская крапивница (б). Крапивница – распространенная группа заболеваний, характеризующихся воспалительным изменением кожи и/или слизистых оболочек, появлением диффузной либо ограниченной сыпи в виде выраженных зудящих папул или волдырей различных размеров с зонами эритемы вокруг них.
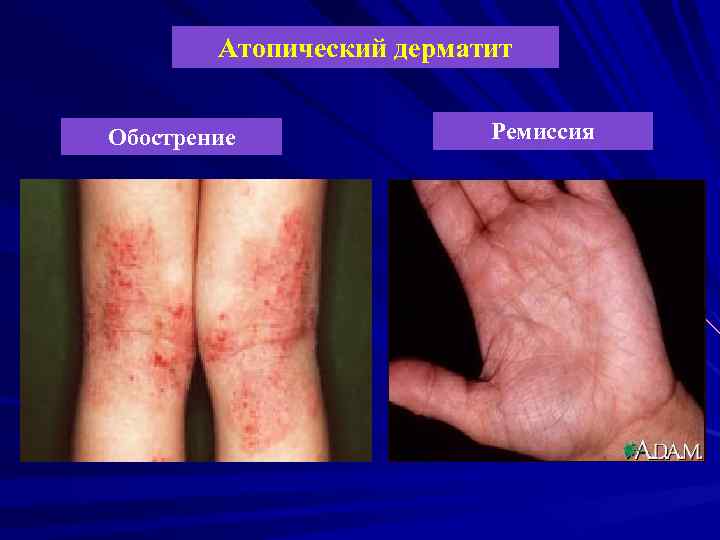 Атопический дерматит Обострение Ремиссия
Атопический дерматит Обострение Ремиссия
 Иммунопатологические реакции II типа (синонимы: цитотоксический тип, антителозависимая цитотоксичность)
Иммунопатологические реакции II типа (синонимы: цитотоксический тип, антителозависимая цитотоксичность)
 Аллерген - собственные клетки организма с измененной антигенной структурой. К ним образуются аутоантитела. Аутоантитела соединяются с антигенами, связанными с мембранами клеток и вызывают их повреждение – цитотоксическое действие
Аллерген - собственные клетки организма с измененной антигенной структурой. К ним образуются аутоантитела. Аутоантитела соединяются с антигенами, связанными с мембранами клеток и вызывают их повреждение – цитотоксическое действие
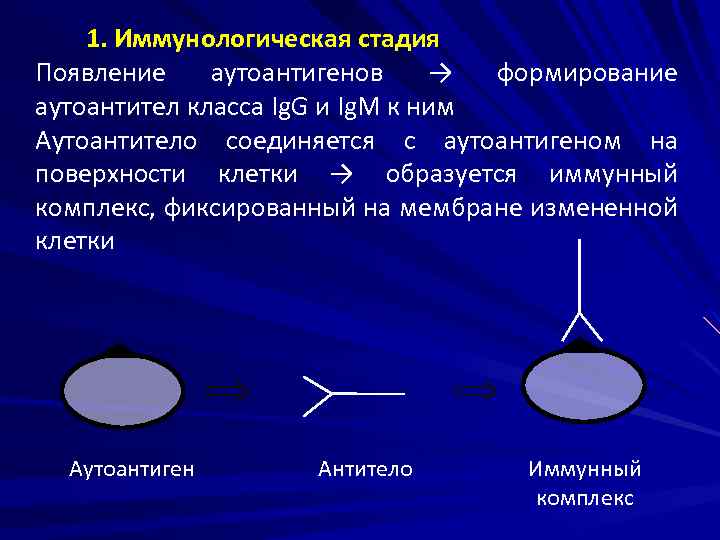 1. Иммунологическая стадия Появление аутоантигенов → формирование аутоантител класса Ig. G и Ig. M к ним Аутоантитело соединяется с аутоантигеном на поверхности клетки → образуется иммунный комплекс, фиксированный на мембране измененной клетки Аутоантиген Антитело Иммунный комплекс
1. Иммунологическая стадия Появление аутоантигенов → формирование аутоантител класса Ig. G и Ig. M к ним Аутоантитело соединяется с аутоантигеном на поверхности клетки → образуется иммунный комплекс, фиксированный на мембране измененной клетки Аутоантиген Антитело Иммунный комплекс
 2. Патохимическая стадия. Выделяют 3 механизма реализации: 1. Комплемент-зависимый цитолиз (активируется комплемент → образуется мембрано-атакующий комплекс С 5 -С 9 → повреждение клеточных мембран → гибель клетки) 2. Фагоцитоз (фиксированные на клетках Ig. M и Ig. G активируют фагоциты → фагоциты поглощают и разрушают эти клетки при помощи лизосомальных ферментов)
2. Патохимическая стадия. Выделяют 3 механизма реализации: 1. Комплемент-зависимый цитолиз (активируется комплемент → образуется мембрано-атакующий комплекс С 5 -С 9 → повреждение клеточных мембран → гибель клетки) 2. Фагоцитоз (фиксированные на клетках Ig. M и Ig. G активируют фагоциты → фагоциты поглощают и разрушают эти клетки при помощи лизосомальных ферментов)
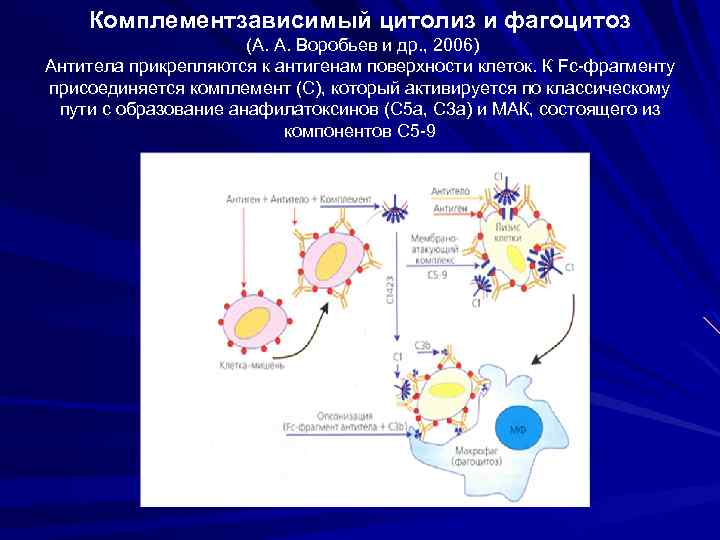 Комплементзависимый цитолиз и фагоцитоз (А. А. Воробьев и др. , 2006) Антитела прикрепляются к антигенам поверхности клеток. К Fc-фрагменту присоединяется комплемент (С), который активируется по классическому пути с образование анафилатоксинов (С 5 а, С 3 а) и МАК, состоящего из компонентов С 5 -9
Комплементзависимый цитолиз и фагоцитоз (А. А. Воробьев и др. , 2006) Антитела прикрепляются к антигенам поверхности клеток. К Fc-фрагменту присоединяется комплемент (С), который активируется по классическому пути с образование анафилатоксинов (С 5 а, С 3 а) и МАК, состоящего из компонентов С 5 -9
 3. Антителозависимая клеточная цитотоксичность - клетка-киллер (NK, NKT-клетка, γδТ-клетка, моноцит/макрофаг) присоединяется к Fc-фрагменту Ig. M и Ig. G на измененных клетках → лизис этих клеток с помощью перфоринов и гранзимов
3. Антителозависимая клеточная цитотоксичность - клетка-киллер (NK, NKT-клетка, γδТ-клетка, моноцит/макрофаг) присоединяется к Fc-фрагменту Ig. M и Ig. G на измененных клетках → лизис этих клеток с помощью перфоринов и гранзимов
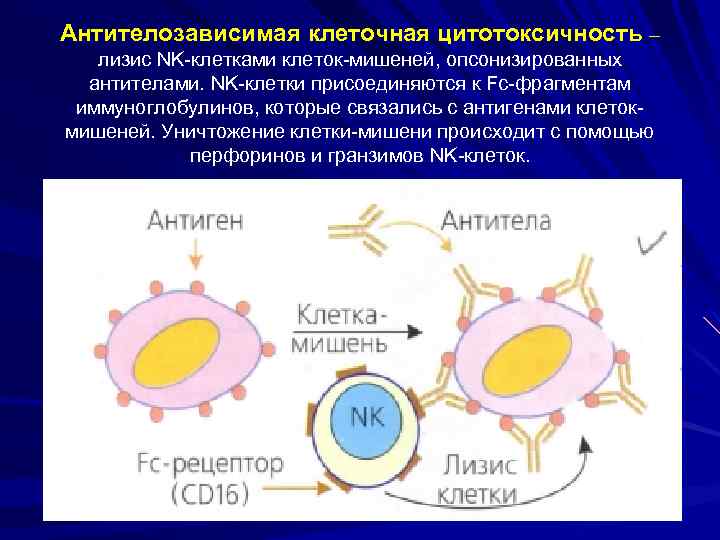 Антителозависимая клеточная цитотоксичность – лизис NK-клетками клеток-мишеней, опсонизированных антителами. NK-клетки присоединяются к Fc-фрагментам иммуноглобулинов, которые связались с антигенами клетокмишеней. Уничтожение клетки-мишени происходит с помощью перфоринов и гранзимов NK-клеток.
Антителозависимая клеточная цитотоксичность – лизис NK-клетками клеток-мишеней, опсонизированных антителами. NK-клетки присоединяются к Fc-фрагментам иммуноглобулинов, которые связались с антигенами клетокмишеней. Уничтожение клетки-мишени происходит с помощью перфоринов и гранзимов NK-клеток.
 3. Патофизиологическая стадия Аллергические реакции 2 -го типа могут иметь место при переливании разногруппной крови, при резус-конфликте, трансплантации органов; при лекарственной аллергии (с развитием лейкопении, тромбоцитопении, гемолитической анемии); после перенесенных вирусных, бактериальных и паразитарных инфекций; при аутоиммунных заболеваниях
3. Патофизиологическая стадия Аллергические реакции 2 -го типа могут иметь место при переливании разногруппной крови, при резус-конфликте, трансплантации органов; при лекарственной аллергии (с развитием лейкопении, тромбоцитопении, гемолитической анемии); после перенесенных вирусных, бактериальных и паразитарных инфекций; при аутоиммунных заболеваниях
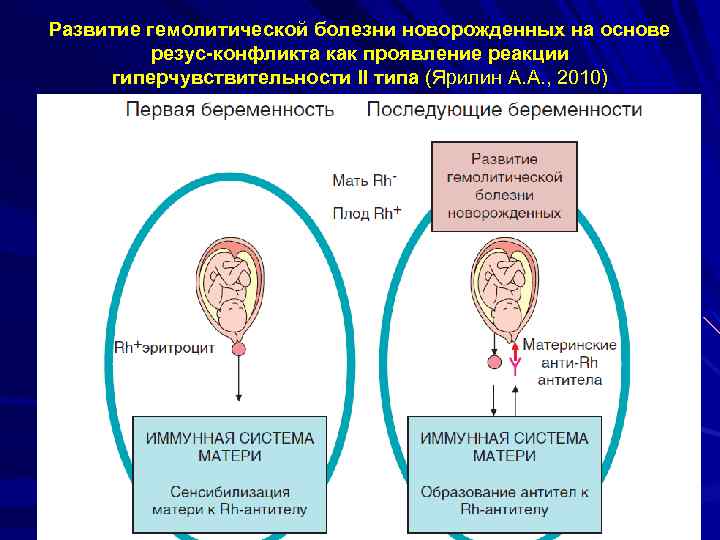 Развитие гемолитической болезни новорожденных на основе резус-конфликта как проявление реакции гиперчувствительности II типа (Ярилин А. А. , 2010)
Развитие гемолитической болезни новорожденных на основе резус-конфликта как проявление реакции гиперчувствительности II типа (Ярилин А. А. , 2010)
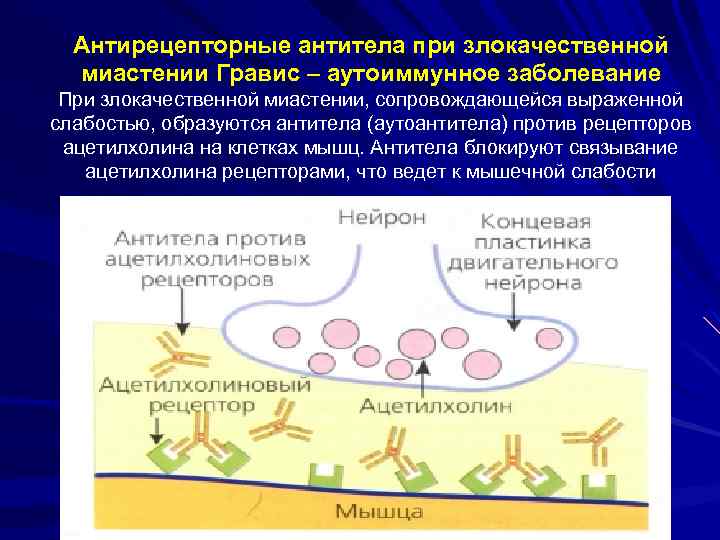 Антирецепторные антитела при злокачественной миастении Гравис – аутоиммунное заболевание При злокачественной миастении, сопровождающейся выраженной слабостью, образуются антитела (аутоантитела) против рецепторов ацетилхолина на клетках мышц. Антитела блокируют связывание ацетилхолина рецепторами, что ведет к мышечной слабости
Антирецепторные антитела при злокачественной миастении Гравис – аутоиммунное заболевание При злокачественной миастении, сопровождающейся выраженной слабостью, образуются антитела (аутоантитела) против рецепторов ацетилхолина на клетках мышц. Антитела блокируют связывание ацетилхолина рецепторами, что ведет к мышечной слабости
 Иммунопатологические реакции III типа (иммунокомплексная патология)
Иммунопатологические реакции III типа (иммунокомплексная патология)
 Аллергены (эндо- и экзоаллергены) свободные, не связаны с тканями «хозяина» , растворены в плазме, лимфе, тканевой жидкости Иммунное повреждение осуществляется циркулирующими иммунными комплексами (ЦИК) - аллерген+антитело. В норме иммунные комплексы удаляются из организма с помощью системы комплемента (компонентов С 1 -С 5), эритроцитов и макрофагов ретикуло-эндотелиальной системы печени.
Аллергены (эндо- и экзоаллергены) свободные, не связаны с тканями «хозяина» , растворены в плазме, лимфе, тканевой жидкости Иммунное повреждение осуществляется циркулирующими иммунными комплексами (ЦИК) - аллерген+антитело. В норме иммунные комплексы удаляются из организма с помощью системы комплемента (компонентов С 1 -С 5), эритроцитов и макрофагов ретикуло-эндотелиальной системы печени.
 1. Иммунологическая стадия В ответ на появление аллергена в организме синтезируются Ig. M и Ig. G, они соединяются с аллергенами с образованием иммунных комплексов. При нарушении процессов элиминации иммунные комплексы накапливаются и начинают циркулировать в организме. Они осаждаются на сосудистой стенке (васкулит), на мембранах почечных клубочков (гломерулонефрит) или в тканях (местная воспалительная реакция по типу феномена Артюса) + Аллерген Антитело Циркулирующий иммунный комплекс
1. Иммунологическая стадия В ответ на появление аллергена в организме синтезируются Ig. M и Ig. G, они соединяются с аллергенами с образованием иммунных комплексов. При нарушении процессов элиминации иммунные комплексы накапливаются и начинают циркулировать в организме. Они осаждаются на сосудистой стенке (васкулит), на мембранах почечных клубочков (гломерулонефрит) или в тканях (местная воспалительная реакция по типу феномена Артюса) + Аллерген Антитело Циркулирующий иммунный комплекс
 2. Патохимическая стадия. Под влиянием иммунных комплексов образуются медиаторы воспаления 1. Фиксированные в тканях иммунные комплексы активируют систему комплемента (С 1 -С 5 компоненты) - анафилатоксины (С 3 а и С 5 а) активируют тучные клетки к продукции БАВ - макрофаги продуцируют TNFα и др. провоспалительные цитокины - нейтрофилы 2. Фиксированные в тканях иммунные комплексы активируют калликреин-кининовую систему (брадикинин)
2. Патохимическая стадия. Под влиянием иммунных комплексов образуются медиаторы воспаления 1. Фиксированные в тканях иммунные комплексы активируют систему комплемента (С 1 -С 5 компоненты) - анафилатоксины (С 3 а и С 5 а) активируют тучные клетки к продукции БАВ - макрофаги продуцируют TNFα и др. провоспалительные цитокины - нейтрофилы 2. Фиксированные в тканях иммунные комплексы активируют калликреин-кининовую систему (брадикинин)
 3. Патофизиологическая стадия В местах отложения иммунных комплексов развивается экссудативное воспаление. Происходит альтерация клеток и тканей Клинически это проявляется дерматитами, альвеолитами , генерализованными васкулитами, гломерулонефритами, системной красной волчанкой
3. Патофизиологическая стадия В местах отложения иммунных комплексов развивается экссудативное воспаление. Происходит альтерация клеток и тканей Клинически это проявляется дерматитами, альвеолитами , генерализованными васкулитами, гломерулонефритами, системной красной волчанкой
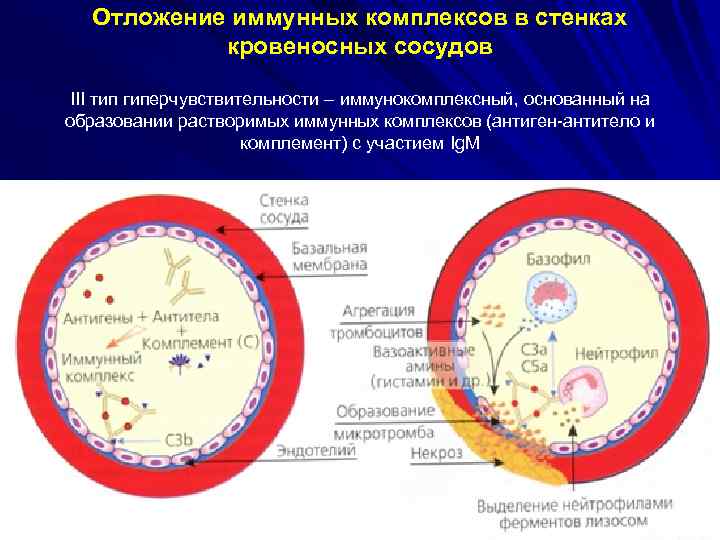 Отложение иммунных комплексов в стенках кровеносных сосудов III тип гиперчувствительности – иммунокомплексный, основанный на образовании растворимых иммунных комплексов (антиген-антитело и комплемент) с участием Ig. M
Отложение иммунных комплексов в стенках кровеносных сосудов III тип гиперчувствительности – иммунокомплексный, основанный на образовании растворимых иммунных комплексов (антиген-антитело и комплемент) с участием Ig. M
 Иммунопатологические реакции IV типа (гиперчувствительность замедленного типа)
Иммунопатологические реакции IV типа (гиперчувствительность замедленного типа)
 Общая характеристика Реакции этого типа не зависят от антител и комплемента, - они являются клеточноопосредованными. Их течение определяют сенсибилизированные Т-лимфоциты, т. е. Т-клетки памяти, индуцированные антигеном и нацеленные на его элиминацию. ГЗТ составляет патогенетическую основу контактной гиперчувствительности, некоторых аутоиммунных заболеваний, развивается при внутриклеточных бактериальных, грибковых и протозойных инфекциях, участвует в реакциях отторжения трансплантата.
Общая характеристика Реакции этого типа не зависят от антител и комплемента, - они являются клеточноопосредованными. Их течение определяют сенсибилизированные Т-лимфоциты, т. е. Т-клетки памяти, индуцированные антигеном и нацеленные на его элиминацию. ГЗТ составляет патогенетическую основу контактной гиперчувствительности, некоторых аутоиммунных заболеваний, развивается при внутриклеточных бактериальных, грибковых и протозойных инфекциях, участвует в реакциях отторжения трансплантата.
 1. Иммунологическая стадия ГЗТ-реакция протекает по Th 1 -зависимому типу Аллерген фагоцитируется, процессируется макрофагом и представляется Т-хелперам (Th). АПК секретируют интерлейкин-12, который способствует дифференцировке Th 0, распознавшего аллерген, в Th 1 -го типа с фенотипом CD 4+ - сенсибилизированный лимфоцит. При повторном поступлении аллергена Th 1 с фенотипом CD 4+ продуцируют цитокины, опосредующие воспалительный ответ
1. Иммунологическая стадия ГЗТ-реакция протекает по Th 1 -зависимому типу Аллерген фагоцитируется, процессируется макрофагом и представляется Т-хелперам (Th). АПК секретируют интерлейкин-12, который способствует дифференцировке Th 0, распознавшего аллерген, в Th 1 -го типа с фенотипом CD 4+ - сенсибилизированный лимфоцит. При повторном поступлении аллергена Th 1 с фенотипом CD 4+ продуцируют цитокины, опосредующие воспалительный ответ
 2. Патохимическая стадия Обусловлена либо активирующим, либо ингибирующим действием цитокинов (они могут быть провоспалительными, - IL-1, IL-2, IL-6, TNFα и противовоспалительными с иммуносупрессорной активностью, - IL 10, TGFβ) на: лимфоциты макрофаги и нейтрофилы клетки-мишени
2. Патохимическая стадия Обусловлена либо активирующим, либо ингибирующим действием цитокинов (они могут быть провоспалительными, - IL-1, IL-2, IL-6, TNFα и противовоспалительными с иммуносупрессорной активностью, - IL 10, TGFβ) на: лимфоциты макрофаги и нейтрофилы клетки-мишени
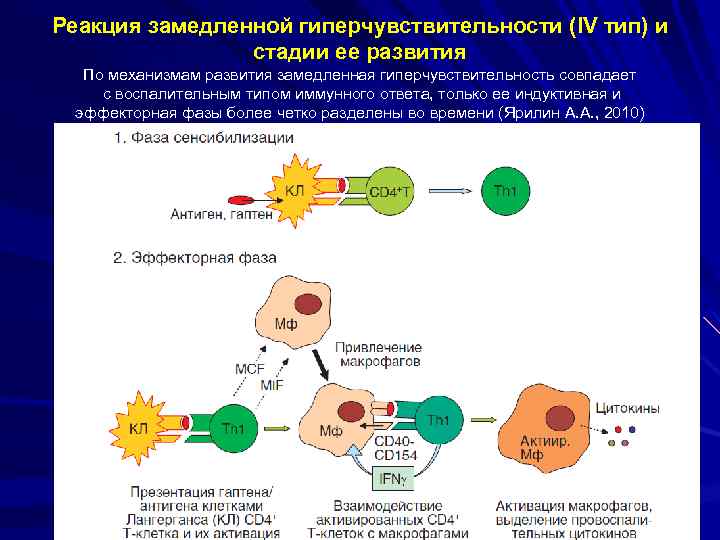 Реакция замедленной гиперчувствительности (IV тип) и стадии ее развития По механизмам развития замедленная гиперчувствительность совпадает с воспалительным типом иммунного ответа, только ее индуктивная и эффекторная фазы более четко разделены во времени (Ярилин А. А. , 2010)
Реакция замедленной гиперчувствительности (IV тип) и стадии ее развития По механизмам развития замедленная гиперчувствительность совпадает с воспалительным типом иммунного ответа, только ее индуктивная и эффекторная фазы более четко разделены во времени (Ярилин А. А. , 2010)
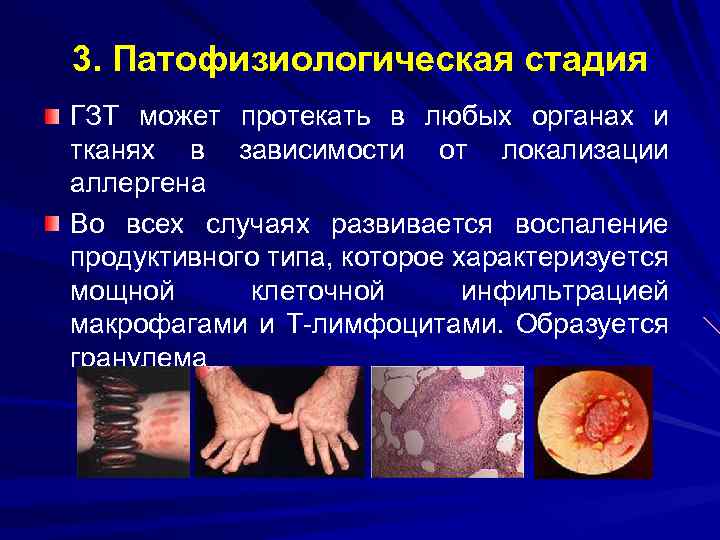 3. Патофизиологическая стадия ГЗТ может протекать в любых органах и тканях в зависимости от локализации аллергена Во всех случаях развивается воспаление продуктивного типа, которое характеризуется мощной клеточной инфильтрацией макрофагами и Т-лимфоцитами. Образуется гранулема
3. Патофизиологическая стадия ГЗТ может протекать в любых органах и тканях в зависимости от локализации аллергена Во всех случаях развивается воспаление продуктивного типа, которое характеризуется мощной клеточной инфильтрацией макрофагами и Т-лимфоцитами. Образуется гранулема
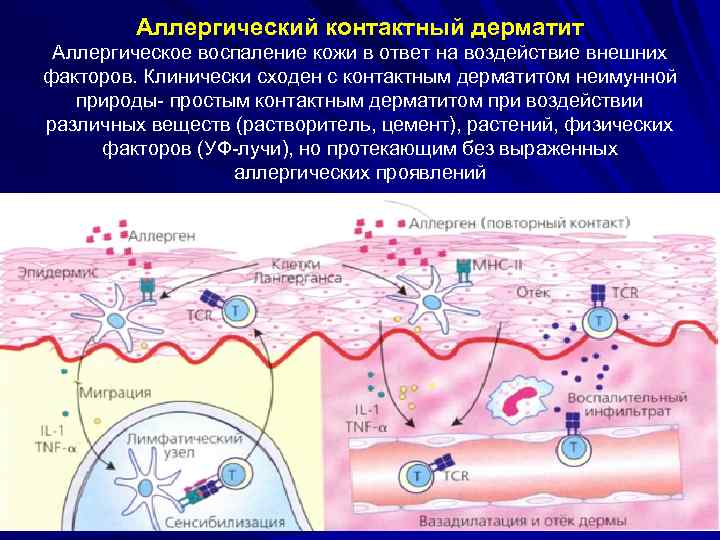 Аллергический контактный дерматит Аллергическое воспаление кожи в ответ на воздействие внешних факторов. Клинически сходен с контактным дерматитом неимунной природы- простым контактным дерматитом при воздействии различных веществ (растворитель, цемент), растений, физических факторов (УФ-лучи), но протекающим без выраженных аллергических проявлений
Аллергический контактный дерматит Аллергическое воспаление кожи в ответ на воздействие внешних факторов. Клинически сходен с контактным дерматитом неимунной природы- простым контактным дерматитом при воздействии различных веществ (растворитель, цемент), растений, физических факторов (УФ-лучи), но протекающим без выраженных аллергических проявлений
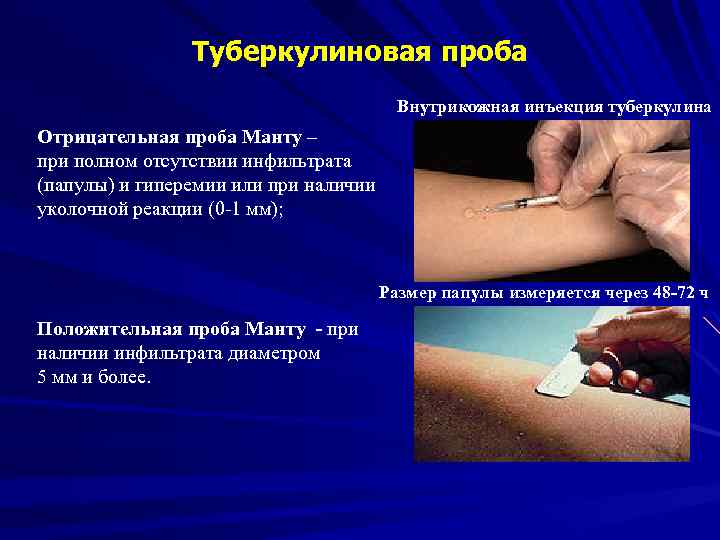 Туберкулиновая проба Внутрикожная инъекция туберкулина Отрицательная проба Манту – при полном отсутствии инфильтрата (папулы) и гиперемии или при наличии уколочной реакции (0 -1 мм); Размер папулы измеряется через 48 -72 ч Положительная проба Манту - при наличии инфильтрата диаметром 5 мм и более.
Туберкулиновая проба Внутрикожная инъекция туберкулина Отрицательная проба Манту – при полном отсутствии инфильтрата (папулы) и гиперемии или при наличии уколочной реакции (0 -1 мм); Размер папулы измеряется через 48 -72 ч Положительная проба Манту - при наличии инфильтрата диаметром 5 мм и более.
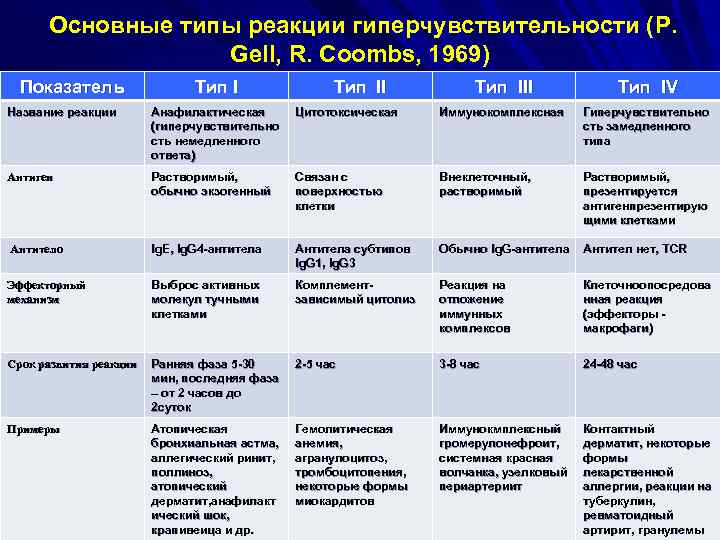 Основные типы реакции гиперчувствительности (P. Gell, R. Coombs, 1969) Показатель Тип III Тип IV Название реакции Анафилактическая (гиперчувствительно сть немедленного ответа) Цитотоксическая Иммунокомплексная Гиперчувствительно сть замедленного типа Антиген Растворимый, обычно экзогенный Связан с поверхностью клетки Внеклеточный, растворимый Растворимый, презентируется антигенпрезентирую щими клетками Антитело Ig. E, Ig. G 4 -антитела Антитела субтипов Ig. G 1, Ig. G 3 Обычно Ig. G-антитела Антител нет, TCR Эффекторный механизм Выброс активных молекул тучными клетками Комплементзависимый цитолиз Реакция на отложение иммунных комплексов Клеточноопосредова нная реакция (эффекторы - макрофаги) Срок развития реакции Ранняя фаза 5 -30 мин, последняя фаза – от 2 часов до 2 суток 2 -5 час 3 -8 час 24 -48 час Примеры Атопическая бронхиальная астма, аллегический ринит, поллиноз, атопический дерматит, анафилакт ический шок, крапивеица и др. Гемолитическая анемия, агранулоцитоз, тромбоцитопения, некоторые формы миокардитов Иммунокмплексный громерулонефроит, системная красная волчанка, узелковый периартериит Контактный дерматит, некоторые формы лекарственной аллергии, реакции на туберкулин, ревматоидный артирит, гранулемы
Основные типы реакции гиперчувствительности (P. Gell, R. Coombs, 1969) Показатель Тип III Тип IV Название реакции Анафилактическая (гиперчувствительно сть немедленного ответа) Цитотоксическая Иммунокомплексная Гиперчувствительно сть замедленного типа Антиген Растворимый, обычно экзогенный Связан с поверхностью клетки Внеклеточный, растворимый Растворимый, презентируется антигенпрезентирую щими клетками Антитело Ig. E, Ig. G 4 -антитела Антитела субтипов Ig. G 1, Ig. G 3 Обычно Ig. G-антитела Антител нет, TCR Эффекторный механизм Выброс активных молекул тучными клетками Комплементзависимый цитолиз Реакция на отложение иммунных комплексов Клеточноопосредова нная реакция (эффекторы - макрофаги) Срок развития реакции Ранняя фаза 5 -30 мин, последняя фаза – от 2 часов до 2 суток 2 -5 час 3 -8 час 24 -48 час Примеры Атопическая бронхиальная астма, аллегический ринит, поллиноз, атопический дерматит, анафилакт ический шок, крапивеица и др. Гемолитическая анемия, агранулоцитоз, тромбоцитопения, некоторые формы миокардитов Иммунокмплексный громерулонефроит, системная красная волчанка, узелковый периартериит Контактный дерматит, некоторые формы лекарственной аллергии, реакции на туберкулин, ревматоидный артирит, гранулемы
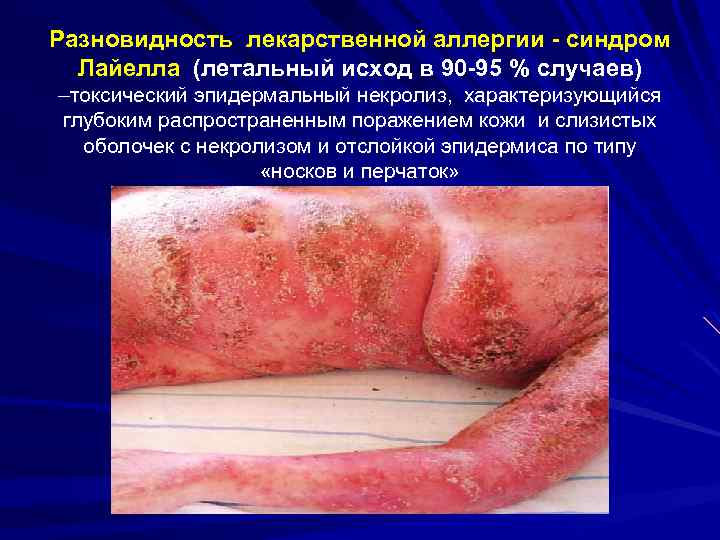 Разновидность лекарственной аллергии - синдром Лайелла (летальный исход в 90 -95 % случаев) –токсический эпидермальный некролиз, характеризующийся глубоким распространенным поражением кожи и слизистых оболочек с некролизом и отслойкой эпидермиса по типу «носков и перчаток»
Разновидность лекарственной аллергии - синдром Лайелла (летальный исход в 90 -95 % случаев) –токсический эпидермальный некролиз, характеризующийся глубоким распространенным поражением кожи и слизистых оболочек с некролизом и отслойкой эпидермиса по типу «носков и перчаток»
 ПСЕВДОАЛЛЕРГИЯ – отсутствует иммунологическая стадия Реакции, связанные с высвобождением медиаторов из тучных клеток Анафилактоидные псевдоаллергические реакции: нарушение метаболизма арахидоновой кислоты нарушения системы комплемента: - наследственный дефицит ингибитора С 1 - активация альтернативного пути
ПСЕВДОАЛЛЕРГИЯ – отсутствует иммунологическая стадия Реакции, связанные с высвобождением медиаторов из тучных клеток Анафилактоидные псевдоаллергические реакции: нарушение метаболизма арахидоновой кислоты нарушения системы комплемента: - наследственный дефицит ингибитора С 1 - активация альтернативного пути

 МАТЕРИАЛ для самостоятельной подготовки
МАТЕРИАЛ для самостоятельной подготовки
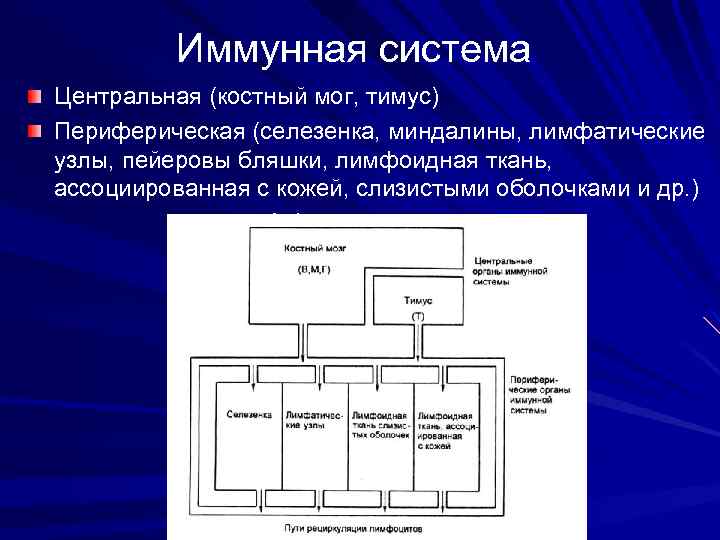 Иммунная система Центральная (костный мог, тимус) Периферическая (селезенка, миндалины, лимфатические узлы, пейеровы бляшки, лимфоидная ткань, ассоциированная с кожей, слизистыми оболочками и др. )
Иммунная система Центральная (костный мог, тимус) Периферическая (селезенка, миндалины, лимфатические узлы, пейеровы бляшки, лимфоидная ткань, ассоциированная с кожей, слизистыми оболочками и др. )
 Функции иммунной системы Функция иммунной системы - иммунная защита от биологической агрессии, которая достигается за счет: 1. Распознавания чужеродных и собственных измененных макромолекул (антигенов); 2. Удаление из организма антигенов и несущих их клеток; 3. Запоминание контакта с конкретными антигенами, определяющее их быстрое удаление при повторном поступлении в организм. Антиген-распознающие рецепторы лимфоцитов различают антигены, отличающиеся по 1 -2 аминокислотным остаткам
Функции иммунной системы Функция иммунной системы - иммунная защита от биологической агрессии, которая достигается за счет: 1. Распознавания чужеродных и собственных измененных макромолекул (антигенов); 2. Удаление из организма антигенов и несущих их клеток; 3. Запоминание контакта с конкретными антигенами, определяющее их быстрое удаление при повторном поступлении в организм. Антиген-распознающие рецепторы лимфоцитов различают антигены, отличающиеся по 1 -2 аминокислотным остаткам
 Лейкоциты – иммунные клетки крови Лейкоциты: 5 -10 тыс. Нейтрофилы: 40 -60% Фагоцитоз и лизис бактерий и паразитов, выработка лейкотриенов, лизоцима, радикалов О 2 Эозинофилы: 1 -3% Защита от глистных инвазий, синергичное действие с тучными клетками и базофилами при аллергическом воспалении Базофилы: 0 -1% Выделение гепарина и гистамина обеспечение гистамин-зависимых аллергических симптомов Моноциты: 4 -8% фагоцитоз, презентация антигена, освобождение радикалов О 2 и интерлейкинов Лимфоциты: 20 -40% В- и Т-лимфоциты, гуморальный и клеточный иммунитет, природные киллеры (NK-клетки)
Лейкоциты – иммунные клетки крови Лейкоциты: 5 -10 тыс. Нейтрофилы: 40 -60% Фагоцитоз и лизис бактерий и паразитов, выработка лейкотриенов, лизоцима, радикалов О 2 Эозинофилы: 1 -3% Защита от глистных инвазий, синергичное действие с тучными клетками и базофилами при аллергическом воспалении Базофилы: 0 -1% Выделение гепарина и гистамина обеспечение гистамин-зависимых аллергических симптомов Моноциты: 4 -8% фагоцитоз, презентация антигена, освобождение радикалов О 2 и интерлейкинов Лимфоциты: 20 -40% В- и Т-лимфоциты, гуморальный и клеточный иммунитет, природные киллеры (NK-клетки)
 Клетки иммунной системы Большинство клеток иммунной системы происходит из кроветворных тканей и некоторое время находится в кровотоке (в этом смысле иммунная система является дочерней по отношению к кроветворной). Это относится как к лимфоцитам, моноцитам и нейтрофилам, так и к дендритным и тучным клеткам, которые формально не отноcятся к клеткам крови из-за их малой численности в крови и непродолжительности пребывания там
Клетки иммунной системы Большинство клеток иммунной системы происходит из кроветворных тканей и некоторое время находится в кровотоке (в этом смысле иммунная система является дочерней по отношению к кроветворной). Это относится как к лимфоцитам, моноцитам и нейтрофилам, так и к дендритным и тучным клеткам, которые формально не отноcятся к клеткам крови из-за их малой численности в крови и непродолжительности пребывания там
 Нейтрофилы и их функция Нейтрофилы (полиморфноядерные лейкоциты). неделящиеся клетки с сегментированным ядром и набором гранул, не окрашивающихся гематоксилином и эозином. Нейтрофилы живут 2 -3 суток Дисфункции нейтрофилов, такие как различные формы нейтропении, дефицит адгезии нейтрофилов или хронический грануломатоз, приводят к тяжелым формам подверженности бактериальным инфекциям, т. е нейтрофилы играют ключевую роль в обеспечении врожденной формы иммунитета. Гиперактивация нейтрофилов приводит к возникновению таких патологий, как повреждение при реперфузии, васкулит, синдром дыхательной недостаточности взрослых и гломерулонефрит. Нейтрофилы обеспечивают основную защиту от пиогенных (гноеродных) бактерий и могут существовать в анаэробных условиях. Находятся главным образом в крови, за исключением случаев острого воспаления. Нехватка нейтрофилов приводит к хроническим инфекциям.
Нейтрофилы и их функция Нейтрофилы (полиморфноядерные лейкоциты). неделящиеся клетки с сегментированным ядром и набором гранул, не окрашивающихся гематоксилином и эозином. Нейтрофилы живут 2 -3 суток Дисфункции нейтрофилов, такие как различные формы нейтропении, дефицит адгезии нейтрофилов или хронический грануломатоз, приводят к тяжелым формам подверженности бактериальным инфекциям, т. е нейтрофилы играют ключевую роль в обеспечении врожденной формы иммунитета. Гиперактивация нейтрофилов приводит к возникновению таких патологий, как повреждение при реперфузии, васкулит, синдром дыхательной недостаточности взрослых и гломерулонефрит. Нейтрофилы обеспечивают основную защиту от пиогенных (гноеродных) бактерий и могут существовать в анаэробных условиях. Находятся главным образом в крови, за исключением случаев острого воспаления. Нехватка нейтрофилов приводит к хроническим инфекциям.
 Функция нейтрофилов Основная функция нейтрофилов - фагоцитоз. Действие нейтрофилов, как и макрофагов, неспецифично. Время их нахождения в кровеносном русле в среднем составляет 6 - 8 ч, они быстро мигрируют в слизистые оболочки. При острых инфекционных заболеваниях число нейтрофилов быстро нарастает. Они способны получать энергию путем анаэробного гликолиза и поэтому существуют даже в тканях, бедных кислородом: воспаленных тканях, отечных тканях или тканях с плохим кровоснабжением. Нейтрофилы фагоцитируют бактерии и продукты распада тканей и разрушают их своими лизосомными ферментами (протеазами, пептидазами, оксидазами , дезоксирибонуклеазами и липазами). Гной состоит главным образом из нейтрофилов и их остатков. Лизосомные ферменты, высвобождающиеся при распаде нейтрофилов, вызывают размягчение окружающих тканей, т. е. формирование гнойного очага.
Функция нейтрофилов Основная функция нейтрофилов - фагоцитоз. Действие нейтрофилов, как и макрофагов, неспецифично. Время их нахождения в кровеносном русле в среднем составляет 6 - 8 ч, они быстро мигрируют в слизистые оболочки. При острых инфекционных заболеваниях число нейтрофилов быстро нарастает. Они способны получать энергию путем анаэробного гликолиза и поэтому существуют даже в тканях, бедных кислородом: воспаленных тканях, отечных тканях или тканях с плохим кровоснабжением. Нейтрофилы фагоцитируют бактерии и продукты распада тканей и разрушают их своими лизосомными ферментами (протеазами, пептидазами, оксидазами , дезоксирибонуклеазами и липазами). Гной состоит главным образом из нейтрофилов и их остатков. Лизосомные ферменты, высвобождающиеся при распаде нейтрофилов, вызывают размягчение окружающих тканей, т. е. формирование гнойного очага.
 Эозинофилы и их функция Эозинофилы (полиморфноядерные гранулоциты) - поражают крупные паразитические организмы (гельминты). Активированные эозинофилы выделяют содержимое внутриклеточных гранул и другие вещества, не находящиеся в гранулах. По свойствам эозинофилы сходны с нейтрофилами, но имеют меньшую фагоцитарную активность. Живут намного дольше нейтрофилов и, в отличие от них, способны к возвращению из тканей в кровь Способны к фагоцитозу и образованию активных форм кислорода , реагируют на специфический хемокин - эотоксин и обладают рецепторами к нему. Среди освобождаемых белков гранул MBP (главный основный белок) и катионный белок, которые повреждают оболочку паразита. MBP обладает свойствами гистаминазы. Один из белков, находящихся в гранулах, может "протыкать" мембрану клетки-мишени подобно C 9 или перфорину NK
Эозинофилы и их функция Эозинофилы (полиморфноядерные гранулоциты) - поражают крупные паразитические организмы (гельминты). Активированные эозинофилы выделяют содержимое внутриклеточных гранул и другие вещества, не находящиеся в гранулах. По свойствам эозинофилы сходны с нейтрофилами, но имеют меньшую фагоцитарную активность. Живут намного дольше нейтрофилов и, в отличие от них, способны к возвращению из тканей в кровь Способны к фагоцитозу и образованию активных форм кислорода , реагируют на специфический хемокин - эотоксин и обладают рецепторами к нему. Среди освобождаемых белков гранул MBP (главный основный белок) и катионный белок, которые повреждают оболочку паразита. MBP обладает свойствами гистаминазы. Один из белков, находящихся в гранулах, может "протыкать" мембрану клетки-мишени подобно C 9 или перфорину NK
 Эозинофилы и их функция Эозинофилы имеют рецептор для C 3 b (компонент системы комплемента), при активации C 3 b происходит усиление дыхания, сопровождающееся выработкой активных форм кислорода. В норме эозинофилы угнетают воспаление. Но при бронхиальной астме они начинают вырабатывать медиаторы воспаления- главный основный белок , нейротоксин эозинофилов , катионный белок эозинофилов , лизофосфолипазу, которые повреждают эпителий дыхательных путей. Гранулы эозинофилов содержат специфичную пероксидазу эозинофилов, катализирующую окисление различных веществ до перекиси водорода. В присутствии перекиси водорода и галогенидов пероксидаза эозинофилов стимулирует секреторную активность тучных клеток, способствуя развитию воспаления. Выделяемый тучными клетками анафилактический фактор хемотаксиса эозинофилов увеличивает количество рецепторов к компонентам комплемента на поверхности эозинофилов, стимулируя уничтожение эозинофилами простейших и гельминтов
Эозинофилы и их функция Эозинофилы имеют рецептор для C 3 b (компонент системы комплемента), при активации C 3 b происходит усиление дыхания, сопровождающееся выработкой активных форм кислорода. В норме эозинофилы угнетают воспаление. Но при бронхиальной астме они начинают вырабатывать медиаторы воспаления- главный основный белок , нейротоксин эозинофилов , катионный белок эозинофилов , лизофосфолипазу, которые повреждают эпителий дыхательных путей. Гранулы эозинофилов содержат специфичную пероксидазу эозинофилов, катализирующую окисление различных веществ до перекиси водорода. В присутствии перекиси водорода и галогенидов пероксидаза эозинофилов стимулирует секреторную активность тучных клеток, способствуя развитию воспаления. Выделяемый тучными клетками анафилактический фактор хемотаксиса эозинофилов увеличивает количество рецепторов к компонентам комплемента на поверхности эозинофилов, стимулируя уничтожение эозинофилами простейших и гельминтов
 Базофилы и их функция Базофилы (базофильные сегментоядерные гранулоциты) живут несколько суток). Гранулы базофилов окрашиваются основными красителями и содержат гепарин и гистамин. Базофилы (как и тучные клетки) секретируют медиаторы - гистамин, гепарин, лейкотриены , простагландины, фактор активации тромбоцитов, фактор анафилаксии, фактор хемотаксиса. Большая часть этих соединений повышает проницаемость сосудов и участвует в воспалении. Выделяя гепарин, базофилы активируют липолиз и уменьшают свертываемость крови Базофилы и тучные клетки несут на своей поверхности рецепторы Ig. E и играют важнейшую роль в аллергических реакциях немедленного типа. Аллергены служат стимулом дегрануляции базофилов. Они перекрестно "сшивают" соседние молекулы Ig. E , связанные высокоафинными рецепторами для Ig. E на плазматической мембране базофила. В результате дегрануляции происходит быстрое освобождение всего содержимого гранул. Секретируемые базофилами медиаторы (гистамин) ответственны за проявления аллергии, но играют
Базофилы и их функция Базофилы (базофильные сегментоядерные гранулоциты) живут несколько суток). Гранулы базофилов окрашиваются основными красителями и содержат гепарин и гистамин. Базофилы (как и тучные клетки) секретируют медиаторы - гистамин, гепарин, лейкотриены , простагландины, фактор активации тромбоцитов, фактор анафилаксии, фактор хемотаксиса. Большая часть этих соединений повышает проницаемость сосудов и участвует в воспалении. Выделяя гепарин, базофилы активируют липолиз и уменьшают свертываемость крови Базофилы и тучные клетки несут на своей поверхности рецепторы Ig. E и играют важнейшую роль в аллергических реакциях немедленного типа. Аллергены служат стимулом дегрануляции базофилов. Они перекрестно "сшивают" соседние молекулы Ig. E , связанные высокоафинными рецепторами для Ig. E на плазматической мембране базофила. В результате дегрануляции происходит быстрое освобождение всего содержимого гранул. Секретируемые базофилами медиаторы (гистамин) ответственны за проявления аллергии, но играют
 Тучные клетки — высокоспециализированные иммунные клетки соединительной ткани позвоночных животных, аналоги базофилов крови. Участвуют в адаптивном иммунитете. Рассеяны по соединительной ткани организма, особенно под кожей, вокруг лимфатических узлов и кровеносных сосудов; содержатся в селезенке и костном мозге. Тучные клетки играют важную роль в воспалительных реакциях, в частности, аллергических реакциях. Так же как и у базофилов поверхность тучных клеток имеет рецепторы для иммуноглобулинов Ig. E. Тучные клетки содержат большое количество цитоплазматических гранул, окрашиваемых катионными красителями. Гранулы включают гепарин, гистамин, серотонин, интерлейкины и нейтральные протеазы. Как и базофилы секретируют, лейкотриены , простагландины , фактор активации тромбоцитов. При активации (например, при аллергической реакции) тучные клетки высвобождают содержимое гранул в окружающую ткань (дегрануляция). Тучные клетки играют важнейшую роль в аллергических реакциях немедленного типа. Дегрануляцию тучных клеток вызывают и физические факторы, например, холод, ультрафиолетовое излучение, причем функциональные изменения тучных клеток и гистологическая картина при этом также неодинаковы. В зависимости от стимулятора реакция тучных клеток может быть одно- или двухфазной. Так, при стимуляции тучных клеток, опосредованной рецепторами к Ig. E , наблюдаются ранняя и поздняя реакции, а при стимуляции опиоидами и холодом -
Тучные клетки — высокоспециализированные иммунные клетки соединительной ткани позвоночных животных, аналоги базофилов крови. Участвуют в адаптивном иммунитете. Рассеяны по соединительной ткани организма, особенно под кожей, вокруг лимфатических узлов и кровеносных сосудов; содержатся в селезенке и костном мозге. Тучные клетки играют важную роль в воспалительных реакциях, в частности, аллергических реакциях. Так же как и у базофилов поверхность тучных клеток имеет рецепторы для иммуноглобулинов Ig. E. Тучные клетки содержат большое количество цитоплазматических гранул, окрашиваемых катионными красителями. Гранулы включают гепарин, гистамин, серотонин, интерлейкины и нейтральные протеазы. Как и базофилы секретируют, лейкотриены , простагландины , фактор активации тромбоцитов. При активации (например, при аллергической реакции) тучные клетки высвобождают содержимое гранул в окружающую ткань (дегрануляция). Тучные клетки играют важнейшую роль в аллергических реакциях немедленного типа. Дегрануляцию тучных клеток вызывают и физические факторы, например, холод, ультрафиолетовое излучение, причем функциональные изменения тучных клеток и гистологическая картина при этом также неодинаковы. В зависимости от стимулятора реакция тучных клеток может быть одно- или двухфазной. Так, при стимуляции тучных клеток, опосредованной рецепторами к Ig. E , наблюдаются ранняя и поздняя реакции, а при стимуляции опиоидами и холодом -
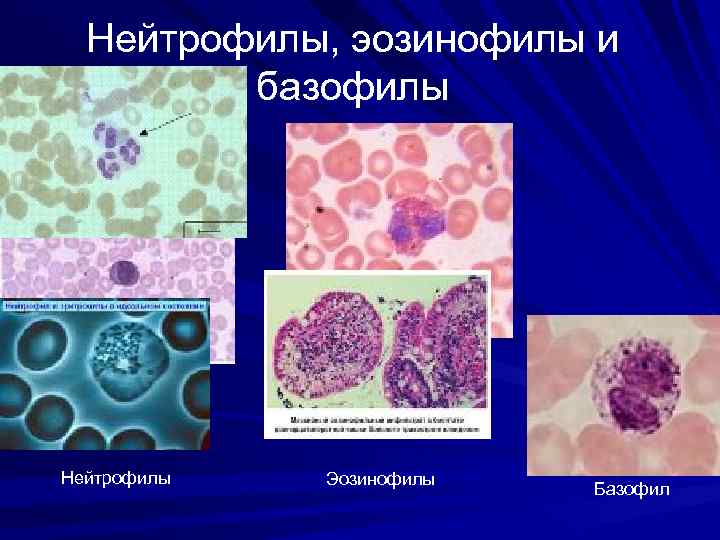 Нейтрофилы, эозинофилы и базофилы Эозинофилы Нейтрофилы Эозинофилы Базофил
Нейтрофилы, эозинофилы и базофилы Эозинофилы Нейтрофилы Эозинофилы Базофил
 Моноциты - это лейкоциты, не содержащие гранул (4 - 8% лейкоцитов крови). Образуются в костном мозге, откуда в кровь поступают не совсем созревшие клетки с самой высокой способностью к фагоцитозу. Живут месяцы и годы Несколько суток моноциты циркулируют в крови, затем мигрируют в ткани и растут, превращаясь в макрофаги, которые вместе нейтрофилами являются основными фагоцитами. Достигнув зрелости, моноциты превращаются в неподвижные клетки – гистоциты (тканевые макрофаги). Вблизи очага воспаления они могут размножаться делением, образуя изолирующий слой вокруг инородных тел, которые не могут разрушить. Эти клетки присутствуют в больших количествах в лимфатических узлах, стенках альвеол и синусах печени, селезенки и костного мозга. Моноциты также являются предшественниками клеток Лангерганса, микроглии и других клеток, способных к переработке и презентации антигена. Но макрофаги и моноциты не способны к специфическому распознаванию антигена.
Моноциты - это лейкоциты, не содержащие гранул (4 - 8% лейкоцитов крови). Образуются в костном мозге, откуда в кровь поступают не совсем созревшие клетки с самой высокой способностью к фагоцитозу. Живут месяцы и годы Несколько суток моноциты циркулируют в крови, затем мигрируют в ткани и растут, превращаясь в макрофаги, которые вместе нейтрофилами являются основными фагоцитами. Достигнув зрелости, моноциты превращаются в неподвижные клетки – гистоциты (тканевые макрофаги). Вблизи очага воспаления они могут размножаться делением, образуя изолирующий слой вокруг инородных тел, которые не могут разрушить. Эти клетки присутствуют в больших количествах в лимфатических узлах, стенках альвеол и синусах печени, селезенки и костного мозга. Моноциты также являются предшественниками клеток Лангерганса, микроглии и других клеток, способных к переработке и презентации антигена. Но макрофаги и моноциты не способны к специфическому распознаванию антигена.
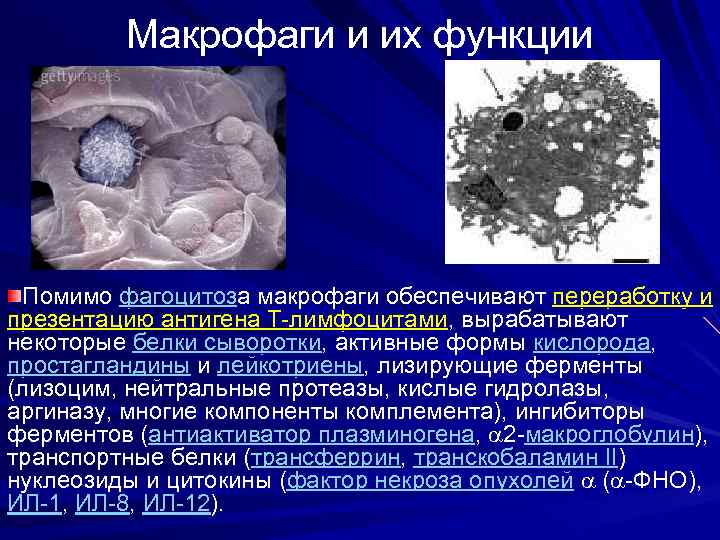 Макрофаги и их функции Помимо фагоцитоза макрофаги обеспечивают переработку и презентацию антигена T-лимфоцитами, вырабатывают некоторые белки сыворотки, активные формы кислорода, простагландины и лейкотриены, лизирующие ферменты (лизоцим, нейтральные протеазы, кислые гидролазы, аргиназу, многие компоненты комплемента), ингибиторы ферментов (антиактиватор плазминогена, 2 -макроглобулин), транспортные белки (трансферрин, транскобаламин II) нуклеозиды и цитокины (фактор некроза опухолей ( -ФНО), ИЛ-1, ИЛ-8, ИЛ-12).
Макрофаги и их функции Помимо фагоцитоза макрофаги обеспечивают переработку и презентацию антигена T-лимфоцитами, вырабатывают некоторые белки сыворотки, активные формы кислорода, простагландины и лейкотриены, лизирующие ферменты (лизоцим, нейтральные протеазы, кислые гидролазы, аргиназу, многие компоненты комплемента), ингибиторы ферментов (антиактиватор плазминогена, 2 -макроглобулин), транспортные белки (трансферрин, транскобаламин II) нуклеозиды и цитокины (фактор некроза опухолей ( -ФНО), ИЛ-1, ИЛ-8, ИЛ-12).
 Макрофаги и их функции ИЛ-1 действует на гипоталамус, вызывая лихорадку, стимулирует выход нейтрофилов в кровь, активирует лимфоциты и нейтрофилы. -ФНО также является пирогеном, частично дублируя эффекты ИЛ-1, он играет важную роль в патогенезе септического шока, вызванного грамотрицательными бактериями. Под влиянием -ФНО увеличивается образование макрофагами и нейтрофилами перекиси водорода и других свободных радикалов. Макрофаги продуцируют также фактор активации тромбоцитов, колониестимулирующие факторы, стимулирующие пролиферацию фибробластов и разрастание мелких сосудов. Макрофаги разрушают опухолевые клетки, вирусы и некоторые бактерий (Mycobacterium tuberculosis , Listeria monocytogenes). Для уничтожении внутриклеточных паразитов макрофаги сливаются в гигантские клетки, которые под влиянием цитокинов объединяются в гранулемы. Важная функция макрофагов сводится к борьбе с бактериями, вирусами и простейшими, которые могут существовать вне- и внутри клетки-хозяина, при помощи мощных бактерицидных механизмов.
Макрофаги и их функции ИЛ-1 действует на гипоталамус, вызывая лихорадку, стимулирует выход нейтрофилов в кровь, активирует лимфоциты и нейтрофилы. -ФНО также является пирогеном, частично дублируя эффекты ИЛ-1, он играет важную роль в патогенезе септического шока, вызванного грамотрицательными бактериями. Под влиянием -ФНО увеличивается образование макрофагами и нейтрофилами перекиси водорода и других свободных радикалов. Макрофаги продуцируют также фактор активации тромбоцитов, колониестимулирующие факторы, стимулирующие пролиферацию фибробластов и разрастание мелких сосудов. Макрофаги разрушают опухолевые клетки, вирусы и некоторые бактерий (Mycobacterium tuberculosis , Listeria monocytogenes). Для уничтожении внутриклеточных паразитов макрофаги сливаются в гигантские клетки, которые под влиянием цитокинов объединяются в гранулемы. Важная функция макрофагов сводится к борьбе с бактериями, вирусами и простейшими, которые могут существовать вне- и внутри клетки-хозяина, при помощи мощных бактерицидных механизмов.
 Лимфоциты - клетки иммунной системы, представляющие собой разновидность лейкоцитов, и отвечающие за приобретённый иммунитет. Лимфоциты подразделяются на B-клетки, T-клетки, K-клетки и NК-клетки. В-лимфоциты распознают чужеродные структуры (антигены) вырабатывая при этом специфические антитела (белковые молекулы, направленные против чужеродных структур). Т-лимфоциты выполняют функцию регуляции иммунитета. Тпомощники (Th) стимулируют выработку антител, а Тсупрессоры (Ts) тормозят ее. NК-лимфоциты способны разрушать чужеродные структуры, помеченные антителами. Под влиянием этих клеток могут быть разрушены различные бактерии, раковые клетки или клетки, инфицированные вирусами. NK-лимфоциты осуществляют контроль над качеством клеток организма. При этом NK-лимфоциты способны разрушать клетки, которые по своим свойствам отличаются от нормальных клеток, например, раковые клетки.
Лимфоциты - клетки иммунной системы, представляющие собой разновидность лейкоцитов, и отвечающие за приобретённый иммунитет. Лимфоциты подразделяются на B-клетки, T-клетки, K-клетки и NК-клетки. В-лимфоциты распознают чужеродные структуры (антигены) вырабатывая при этом специфические антитела (белковые молекулы, направленные против чужеродных структур). Т-лимфоциты выполняют функцию регуляции иммунитета. Тпомощники (Th) стимулируют выработку антител, а Тсупрессоры (Ts) тормозят ее. NК-лимфоциты способны разрушать чужеродные структуры, помеченные антителами. Под влиянием этих клеток могут быть разрушены различные бактерии, раковые клетки или клетки, инфицированные вирусами. NK-лимфоциты осуществляют контроль над качеством клеток организма. При этом NK-лимфоциты способны разрушать клетки, которые по своим свойствам отличаются от нормальных клеток, например, раковые клетки.
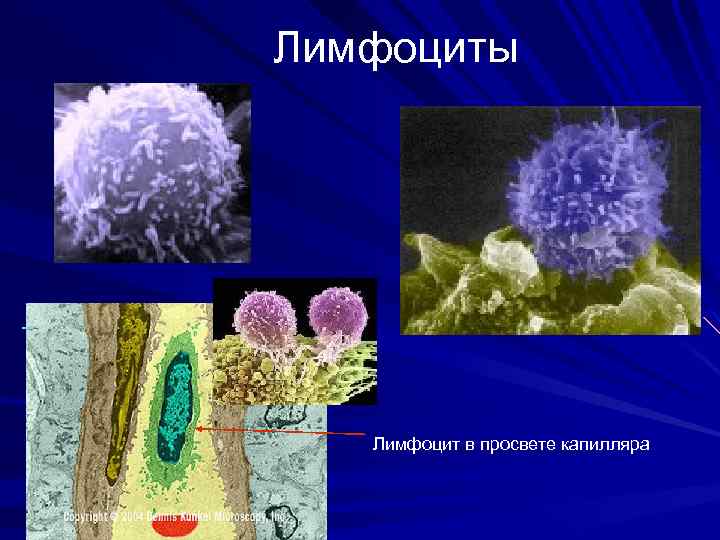 Лимфоциты Лимфоцит в просвете капилляра
Лимфоциты Лимфоцит в просвете капилляра
 Антиген-презентующие клетки В процессе активации T-лимфоцитов, клетки, представляющие антиген в иммуногенной форме на своей поверхности (антигенпрезентирующие клетки), должны обладать, по крайней мере, двумя основными свойствами: - способностью образовывать комплекс антигенного пептида с молекулами I или II классов МНС, что является первым сигналом к пролиферации и дифференцировке наивных T-клеток , и - экспрессировать костимуляторы, обеспечивающие прохождение второго сигнала активации Т-клеток. Макрофаги в состоянии покоя обладают очень незначительным количеством молекул MHC II класса и полностью лишены костимулятора В 7 на своей поверхности. Выраженное представительство этих молекул на мембране макрофага начинается после захвата и внутриклеточного переваривания микроорганизмов. Один из способов поглощения бактерий связан с рецепторами к маннозе, которые способны взаимодействовать с углеводами бактериальной стенки. Захваченные микроорганизмы деградируют в фаголизосомах, образуя отдельные пептиды, которые выносятся на клеточную поверхность в комплексе с молекулами MHC.
Антиген-презентующие клетки В процессе активации T-лимфоцитов, клетки, представляющие антиген в иммуногенной форме на своей поверхности (антигенпрезентирующие клетки), должны обладать, по крайней мере, двумя основными свойствами: - способностью образовывать комплекс антигенного пептида с молекулами I или II классов МНС, что является первым сигналом к пролиферации и дифференцировке наивных T-клеток , и - экспрессировать костимуляторы, обеспечивающие прохождение второго сигнала активации Т-клеток. Макрофаги в состоянии покоя обладают очень незначительным количеством молекул MHC II класса и полностью лишены костимулятора В 7 на своей поверхности. Выраженное представительство этих молекул на мембране макрофага начинается после захвата и внутриклеточного переваривания микроорганизмов. Один из способов поглощения бактерий связан с рецепторами к маннозе, которые способны взаимодействовать с углеводами бактериальной стенки. Захваченные микроорганизмы деградируют в фаголизосомах, образуя отдельные пептиды, которые выносятся на клеточную поверхность в комплексе с молекулами MHC.
 Дендритные клетки -это гетерогенная популяция антигенпрезентирующих клеток, происходящих из костного мозга. Существует несколько разновидностей дендритных клеток: Обыкновенные дендритные клетки названы за их способность иметь изначально фенотип свойственный дендритным клеткам. Эти дендритные клетки также называются миелоидные дендритные клетки, потому что происходят из общего миелоидного гемопоэтического предшественника. Кроме того, выделяют несколько субтипов внутри миелоидных дендритных клеток: клетки Лангерганса - эпителиальные дендритные клетки дермальные дендритные клетки плазмоцитоидные дендритные клетки, характеризуемые тем, что при вирусной инфекции эти клетки активно продуцируют интерферон альфа (IFN-alpha). Основная информация о субтипах дендритных клеток была получена из исследований иммунной системы мышей, о человеческих дендритных клетках известно значительно меньше.
Дендритные клетки -это гетерогенная популяция антигенпрезентирующих клеток, происходящих из костного мозга. Существует несколько разновидностей дендритных клеток: Обыкновенные дендритные клетки названы за их способность иметь изначально фенотип свойственный дендритным клеткам. Эти дендритные клетки также называются миелоидные дендритные клетки, потому что происходят из общего миелоидного гемопоэтического предшественника. Кроме того, выделяют несколько субтипов внутри миелоидных дендритных клеток: клетки Лангерганса - эпителиальные дендритные клетки дермальные дендритные клетки плазмоцитоидные дендритные клетки, характеризуемые тем, что при вирусной инфекции эти клетки активно продуцируют интерферон альфа (IFN-alpha). Основная информация о субтипах дендритных клеток была получена из исследований иммунной системы мышей, о человеческих дендритных клетках известно значительно меньше.
 Дендритные клетки и их функции Основной функцией дендритных клеток является презентация антигенов Т-клеткам. Дендритные клетки также выполняют важные иммунорегуляторные функции, такие как контроль за дифференцировкой Т-лимфоцитов, регуляция активации и супрессии иммунного ответа. Важной особенностью дендритных клеток является способность захватывать из окружающей среды различные антигены при помощи фагоцитоза, пиноцитоза и рецептор-опосредованного эндоцитоза. Больше всего дендритных клеток находиться в тканях, которые соприкасаются с внешней средой, например в толще эпителиального слоя слизистой оболочки кишечника, в подслизистой респираторного, желудочно-кишечного и урогенитального трактов. Дендритные клетки поглощают антигены, процессируют и представляют на своей поверхности в комплексе с MHC I или MHC II классов. Только в таком виде Т-клетки способны распознать антиген и вслед за этим активироваться и развивать иммунный ответ. В зависимости от типа патогена дендритные клетки способны направлять дифференцировку наивных Тхелперов (Th 0) в сторону Т-хелперов 1 типа, Т-хелперов -2 типа, регуляторных Т-клеток или же Т-хелперов 17.
Дендритные клетки и их функции Основной функцией дендритных клеток является презентация антигенов Т-клеткам. Дендритные клетки также выполняют важные иммунорегуляторные функции, такие как контроль за дифференцировкой Т-лимфоцитов, регуляция активации и супрессии иммунного ответа. Важной особенностью дендритных клеток является способность захватывать из окружающей среды различные антигены при помощи фагоцитоза, пиноцитоза и рецептор-опосредованного эндоцитоза. Больше всего дендритных клеток находиться в тканях, которые соприкасаются с внешней средой, например в толще эпителиального слоя слизистой оболочки кишечника, в подслизистой респираторного, желудочно-кишечного и урогенитального трактов. Дендритные клетки поглощают антигены, процессируют и представляют на своей поверхности в комплексе с MHC I или MHC II классов. Только в таком виде Т-клетки способны распознать антиген и вслед за этим активироваться и развивать иммунный ответ. В зависимости от типа патогена дендритные клетки способны направлять дифференцировку наивных Тхелперов (Th 0) в сторону Т-хелперов 1 типа, Т-хелперов -2 типа, регуляторных Т-клеток или же Т-хелперов 17.
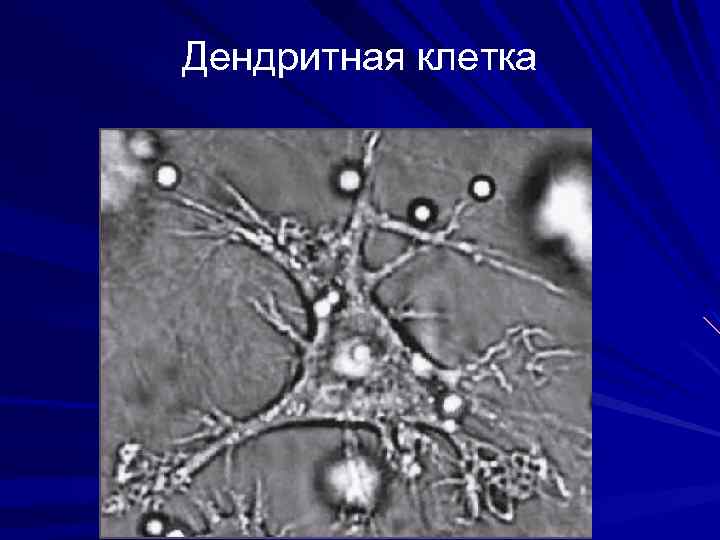 Дендритная клетка
Дендритная клетка
 Дендритные клетки и их функции На поверхности дендритных клеток представлен широкий набор рецепторов, способных распознавать и связывать разнообразные антигены, как экзогенные, так и эндогенные. Типы рецепторов дендритных клеток: Толл-подобные рецепторы (англ. Toll-like receptors) — рецепторы к различным компонентам патогенов, включая бактерии, грибы и вирусы. Эти рецепторы распознают набор (паттерн) молекул, ассоциированных с патогенами ("pathogenassociated molecular patterns" (PAMPs), включая липополисахариды (LPS), флагеллины, нуклеиновые кислоты (ДНК и одно- и дву-цепочечные РНК) Лектины С типа - рецепторы к углеводной части гликопротеинов. Например, DC-SIGN — является одним из рецепторов к ВИЧ (HIV-1) NLRs — внутриклеточные цитоплазматические рецепторы PAMPs.
Дендритные клетки и их функции На поверхности дендритных клеток представлен широкий набор рецепторов, способных распознавать и связывать разнообразные антигены, как экзогенные, так и эндогенные. Типы рецепторов дендритных клеток: Толл-подобные рецепторы (англ. Toll-like receptors) — рецепторы к различным компонентам патогенов, включая бактерии, грибы и вирусы. Эти рецепторы распознают набор (паттерн) молекул, ассоциированных с патогенами ("pathogenassociated molecular patterns" (PAMPs), включая липополисахариды (LPS), флагеллины, нуклеиновые кислоты (ДНК и одно- и дву-цепочечные РНК) Лектины С типа - рецепторы к углеводной части гликопротеинов. Например, DC-SIGN — является одним из рецепторов к ВИЧ (HIV-1) NLRs — внутриклеточные цитоплазматические рецепторы PAMPs.
 Взаимодействие Т-лимфоцитов и антигенпрезентующих клеток T-лимфоциты распознают инфицированный макрофаг по экспонированию на его поверхности микробного антигена, находящегося в комплексе с гликопротеином MHC класса II , который в данном случае служит сигналом макрофага. В результате распознавания T-клетки выделяют лимфокины , стимулирующие внутриклеточное уничтожение возбудителя макрофагом При внутриклеточном переваривания корпускулярого антигена внутри антиген-презентующей клетки происходит индукция синтеза и экспрессии на клеточной поверхности молекул MHC класса II и костимулятора В 7. Факторами индукции, возможно, являются рецепторы клеточной поверхности, взаимодействующие с микроорганизмами, поскольку синтез В 7 можно индуцировать инкубацией макрофагов с компонентами (липополисахаридами) бактериальной стенки. Индукция костимулирующей активности к общим микробным компонентам позволяет иммунной системе отличать бактериальные антигены от собственных антигенов или безвредных чужеродных белков. Получение иммунного ответа к некоторым белкам возможно только с использованием адъювантов, включающих убитые микроорганизмы или продукты их бактериальной стенки.
Взаимодействие Т-лимфоцитов и антигенпрезентующих клеток T-лимфоциты распознают инфицированный макрофаг по экспонированию на его поверхности микробного антигена, находящегося в комплексе с гликопротеином MHC класса II , который в данном случае служит сигналом макрофага. В результате распознавания T-клетки выделяют лимфокины , стимулирующие внутриклеточное уничтожение возбудителя макрофагом При внутриклеточном переваривания корпускулярого антигена внутри антиген-презентующей клетки происходит индукция синтеза и экспрессии на клеточной поверхности молекул MHC класса II и костимулятора В 7. Факторами индукции, возможно, являются рецепторы клеточной поверхности, взаимодействующие с микроорганизмами, поскольку синтез В 7 можно индуцировать инкубацией макрофагов с компонентами (липополисахаридами) бактериальной стенки. Индукция костимулирующей активности к общим микробным компонентам позволяет иммунной системе отличать бактериальные антигены от собственных антигенов или безвредных чужеродных белков. Получение иммунного ответа к некоторым белкам возможно только с использованием адъювантов, включающих убитые микроорганизмы или продукты их бактериальной стенки.
 Презентация антигена Если белковые антигены захватываются и презентуются макрофагами в отсутствие бактериальных компонентов, которые инициируют синтез В 7 , то Т-клетка специфически распознает антиген, однако остается рефрактерной, так как отсутствует второй сигнал для запуска пролиферации и дифференцировки клеток. Внесение в систему бактериальных компонентов - индукторов костимулятора В 7 - обеспечивает полноценное включение в иммунный ответ Т-клеток. В эксперименте аутоиммунное заболевание легко индуцируется смесью собственных тканевых антигенов с компонентами бактериальной стенки, иллюстрируя значение костимуляции в процессе разграничения "своего" и "чужого". Запуск Т-клеточного ответа, связанного с двухсигнальной системой активации, объясняет работу макрофагов в качестве "мусорщиков". Купферовские клетки печени, макрофаги селезенки постоянно захватывают и разрушают отжившие клетки этих органов. При этом в отсутствие бактериальных стимуляторов экспрессируемых на поверхности фагоцитирующих клеток собственные антигены, появившиеся в результате деградации отживших клеток, не в состоянии развить аутоиммунный ответ.
Презентация антигена Если белковые антигены захватываются и презентуются макрофагами в отсутствие бактериальных компонентов, которые инициируют синтез В 7 , то Т-клетка специфически распознает антиген, однако остается рефрактерной, так как отсутствует второй сигнал для запуска пролиферации и дифференцировки клеток. Внесение в систему бактериальных компонентов - индукторов костимулятора В 7 - обеспечивает полноценное включение в иммунный ответ Т-клеток. В эксперименте аутоиммунное заболевание легко индуцируется смесью собственных тканевых антигенов с компонентами бактериальной стенки, иллюстрируя значение костимуляции в процессе разграничения "своего" и "чужого". Запуск Т-клеточного ответа, связанного с двухсигнальной системой активации, объясняет работу макрофагов в качестве "мусорщиков". Купферовские клетки печени, макрофаги селезенки постоянно захватывают и разрушают отжившие клетки этих органов. При этом в отсутствие бактериальных стимуляторов экспрессируемых на поверхности фагоцитирующих клеток собственные антигены, появившиеся в результате деградации отживших клеток, не в состоянии развить аутоиммунный ответ.
 Классификация иммунных ответов Врожденный иммунитет реализуется через клеточные (макрофаги, дендритные клетки, нейтрофилы, киллеры) и гуморальные (естественные антитела, комплемент, белки острой фазы, цитокины, лизоцим и др. ). Клетки врожденной системы не создают клонов, не подвергаются негативной и позитивной селекции. Это готовые клетки, которые действуют благодаря реакциям фагоцитоза, цитолиза и др.
Классификация иммунных ответов Врожденный иммунитет реализуется через клеточные (макрофаги, дендритные клетки, нейтрофилы, киллеры) и гуморальные (естественные антитела, комплемент, белки острой фазы, цитокины, лизоцим и др. ). Клетки врожденной системы не создают клонов, не подвергаются негативной и позитивной селекции. Это готовые клетки, которые действуют благодаря реакциям фагоцитоза, цитолиза и др.
 Система комплемента – семья, состоящая примерно из 20 протеаз (С 1 -С 9, факторы В, D), действующих вместе со специфическими антителами и вместе с ними убивающих клетки путем лизиса. Белки системы комплемента образуют два связанных друг с другом ферментативных каскада, которые начинаются расщеплением первого компонента, в результате чего возникают протеазы, расщепляющие следующий компонент комплекса. Многие из активированных компонентов прочно связываются с мембранами, большинство этих событий происходит на поверхностях клеток Далее образуется атакующий мембрану комплекс, состоящий из компонентов С 5 -С 9, который нарушает целостность мембраны бактерии, вызывая ее гибель. Система комплемента запускается посредством взаимодействия С 1 с IGg , Ig. M – это классический путь активации В альтернативном варианте сигнал запускают полисахариды мембран некоторых бактерий или С-реактивный белок, маркирующий (опсонизирующий) поверхность мембраны для системы комплемента.
Система комплемента – семья, состоящая примерно из 20 протеаз (С 1 -С 9, факторы В, D), действующих вместе со специфическими антителами и вместе с ними убивающих клетки путем лизиса. Белки системы комплемента образуют два связанных друг с другом ферментативных каскада, которые начинаются расщеплением первого компонента, в результате чего возникают протеазы, расщепляющие следующий компонент комплекса. Многие из активированных компонентов прочно связываются с мембранами, большинство этих событий происходит на поверхностях клеток Далее образуется атакующий мембрану комплекс, состоящий из компонентов С 5 -С 9, который нарушает целостность мембраны бактерии, вызывая ее гибель. Система комплемента запускается посредством взаимодействия С 1 с IGg , Ig. M – это классический путь активации В альтернативном варианте сигнал запускают полисахариды мембран некоторых бактерий или С-реактивный белок, маркирующий (опсонизирующий) поверхность мембраны для системы комплемента.
 Активация системы комплемента и С 1 белок, взаимодействующий с антителами C 1 белок (С 1 r, C 1 s, C 1 q), связывающийся с антителом Главная реакция –активация С 3 Атакующий мембрану комплекс
Активация системы комплемента и С 1 белок, взаимодействующий с антителами C 1 белок (С 1 r, C 1 s, C 1 q), связывающийся с антителом Главная реакция –активация С 3 Атакующий мембрану комплекс
 Заболевания, связанные с дефектами системы комплемента Дефицит С 1: сыворотка утрачивает бактерицидность. Повторяющиеся инфекции верхних дыхательных путей, отит, поражение суставов, хронический гломерулонефрит, нередко приводящие к смерти. Наследуется по аутосомному признаку. При наследственном дефиците ингибитора компонента С 1 -ангионевротический отек Квинке. Дефицит С 2: снижение бактерицидности сыворотки, вирусные инфекции, диффузные болезни соединительной ткани, гломерулонефрит и тромбоцитопении. Компонент С 3. Синтез С 3 определяется двумя аллельными генами как кодоминантный признак; при отсутствии одного из генов количество С 3 в крови снижается в 2 раза. При дефиците С 3 наблюдается высокая смертность. Дефицит С 5: тяжелые кишечные инфекции, вызванные грамотрицательными возбудителями. Поражается также кожа. При наследственной недостаточности С 5 в раннем детском возрасте дерматиты и понос, нарушается развитие ребенка. Дефиците С 6: заболевания суставов (специфический артрит), нарушение свертываемости крови Дефицит С 7: диффузные заболеваний соединительной ткани.
Заболевания, связанные с дефектами системы комплемента Дефицит С 1: сыворотка утрачивает бактерицидность. Повторяющиеся инфекции верхних дыхательных путей, отит, поражение суставов, хронический гломерулонефрит, нередко приводящие к смерти. Наследуется по аутосомному признаку. При наследственном дефиците ингибитора компонента С 1 -ангионевротический отек Квинке. Дефицит С 2: снижение бактерицидности сыворотки, вирусные инфекции, диффузные болезни соединительной ткани, гломерулонефрит и тромбоцитопении. Компонент С 3. Синтез С 3 определяется двумя аллельными генами как кодоминантный признак; при отсутствии одного из генов количество С 3 в крови снижается в 2 раза. При дефиците С 3 наблюдается высокая смертность. Дефицит С 5: тяжелые кишечные инфекции, вызванные грамотрицательными возбудителями. Поражается также кожа. При наследственной недостаточности С 5 в раннем детском возрасте дерматиты и понос, нарушается развитие ребенка. Дефиците С 6: заболевания суставов (специфический артрит), нарушение свертываемости крови Дефицит С 7: диффузные заболеваний соединительной ткани.
 Заболевания, связанные с дефектами системы комплемента Приобретенная недостаточность системы комплемента отмечена при развитии у человека эндокардита, сепсиса, малярии, некоторых вирусных инфекций, осложняющихся развитием гломерулонефрита, возможно, вследствие накопления в организме неразрушенных комплексов антиген-антитело. Активность комплемента снижается также при красной волчанке, ревматоидном артрите и других аутоиммуных заболеваниях.
Заболевания, связанные с дефектами системы комплемента Приобретенная недостаточность системы комплемента отмечена при развитии у человека эндокардита, сепсиса, малярии, некоторых вирусных инфекций, осложняющихся развитием гломерулонефрита, возможно, вследствие накопления в организме неразрушенных комплексов антиген-антитело. Активность комплемента снижается также при красной волчанке, ревматоидном артрите и других аутоиммуных заболеваниях.
 Механизм фагоцитоза Способность к связыванию и фагоцитоз облегчается маркированием мембраны патогена (опсонизацией). Частицы бактерий, нагруженные антителами или С 3, связываются с мембраной фагоцитов через С 3 или Fcрецепторы Затем происходит образование псевдоподий, которые окружают инородное тело (образование фагосом) Разрушение происходит после слияния фагосомы с лизосомами Некоторые микроорганизмы проявляют устойчивость к фагоцитозу или к перевариванию в макрофагах. Это возбудители туберкулеза, тифа, гонореи, проказы. Для защиты от этих бактерий необходимо сотрудничество с Тклетками хелперами. Подтип Th 1 выделяет цитокины, в частности, интерферон , которые максимально активируют макрофаги. При этом индуцируется синтез NO, который может взаимодейтвовать с супероксид анионом, образуя пероксинитрит.
Механизм фагоцитоза Способность к связыванию и фагоцитоз облегчается маркированием мембраны патогена (опсонизацией). Частицы бактерий, нагруженные антителами или С 3, связываются с мембраной фагоцитов через С 3 или Fcрецепторы Затем происходит образование псевдоподий, которые окружают инородное тело (образование фагосом) Разрушение происходит после слияния фагосомы с лизосомами Некоторые микроорганизмы проявляют устойчивость к фагоцитозу или к перевариванию в макрофагах. Это возбудители туберкулеза, тифа, гонореи, проказы. Для защиты от этих бактерий необходимо сотрудничество с Тклетками хелперами. Подтип Th 1 выделяет цитокины, в частности, интерферон , которые максимально активируют макрофаги. При этом индуцируется синтез NO, который может взаимодейтвовать с супероксид анионом, образуя пероксинитрит.
 Лимфоциты Главный структурный элемент иммунной системы: лимфоциты В-лимфоциты и Т-лимфоциты. Иммунокомпетентная клетка, способная распознавать чужеродный антиген, развивать иммунный ответ, создавать клоны подобных себе клеток, формировать иммунную толерантность и клетки памяти, подвергаться позитивному и негативному отбору. Для выполнения этих функций лимфоциты проходят через серию преобразований и взаимодействий с другими клетками (моноциты, макрофаги, дендритные клетки природные киллеры (NK-клетки), нейтрофилы, базофилы, тучные клетки, эозинофилы, которые не обладают свойствами Т- и В-лимфоцитов) антиген представляет собой продукт чужеродной генетической информации, способный при введении в организм вызывать развитие специфических иммунных реакций
Лимфоциты Главный структурный элемент иммунной системы: лимфоциты В-лимфоциты и Т-лимфоциты. Иммунокомпетентная клетка, способная распознавать чужеродный антиген, развивать иммунный ответ, создавать клоны подобных себе клеток, формировать иммунную толерантность и клетки памяти, подвергаться позитивному и негативному отбору. Для выполнения этих функций лимфоциты проходят через серию преобразований и взаимодействий с другими клетками (моноциты, макрофаги, дендритные клетки природные киллеры (NK-клетки), нейтрофилы, базофилы, тучные клетки, эозинофилы, которые не обладают свойствами Т- и В-лимфоцитов) антиген представляет собой продукт чужеродной генетической информации, способный при введении в организм вызывать развитие специфических иммунных реакций
 Приобретенный иммунный ответ возникает благодаря уникальному процессу соматической перегруппировки генных сегментов (V, D, J, C) иммуноглобулинов и рецепторов Т-клеток, ответственных за синтез молекул антител или рецепторов Тклеток, в результате чего создается разнообразие распознающих элементов, перекрывающих все существующие в природе антигены
Приобретенный иммунный ответ возникает благодаря уникальному процессу соматической перегруппировки генных сегментов (V, D, J, C) иммуноглобулинов и рецепторов Т-клеток, ответственных за синтез молекул антител или рецепторов Тклеток, в результате чего создается разнообразие распознающих элементов, перекрывающих все существующие в природе антигены
 Антитела В основе триады реакций иммунного ответа лежат механизмы, специфичные в отношении конкретных антигенов, которые распознаются белковыми структурами, комплементарными к антигенам, а именно, антителами
Антитела В основе триады реакций иммунного ответа лежат механизмы, специфичные в отношении конкретных антигенов, которые распознаются белковыми структурами, комплементарными к антигенам, а именно, антителами
 Структура мономерного иммуноглобулина
Структура мономерного иммуноглобулина
 Класификация антител Ig. G – циркулируют в крови (80% всех антител). Проходят через плаценту. Молекулярная масса 160000. Обезвреживают антиген путем его корпускуляризации (преципитации, осаждения, агглютинации), что облегчает фагоцитоз, лизис, нейтрализацию. Ig. G синтезируется со скоростью около 30 мг/кг в день. В составе тяжелой цепи иммуноглобулина G имеются четыре отличных друг от друга типа молекул, которые определяют соответствующие подклассы. Поэтому он разделяется на подклассы Ig. G 1, Ig. G 2, Ig. G 3 и Ig. G 4. Больше всего – до 60– 70% от общего количества иммуноглобулинов - приходится на долю Ig. G 1.
Класификация антител Ig. G – циркулируют в крови (80% всех антител). Проходят через плаценту. Молекулярная масса 160000. Обезвреживают антиген путем его корпускуляризации (преципитации, осаждения, агглютинации), что облегчает фагоцитоз, лизис, нейтрализацию. Ig. G синтезируется со скоростью около 30 мг/кг в день. В составе тяжелой цепи иммуноглобулина G имеются четыре отличных друг от друга типа молекул, которые определяют соответствующие подклассы. Поэтому он разделяется на подклассы Ig. G 1, Ig. G 2, Ig. G 3 и Ig. G 4. Больше всего – до 60– 70% от общего количества иммуноглобулинов - приходится на долю Ig. G 1.
 Класификация антител Ig М - циркулируют в крови, составляют 5 -10% всех антител. Молекулярная масса 950000, функционально пятивалентен, первым появляется после заражения или вакцинации. Не проходит через плаценту. Значение Ig. M определяется участием в механизме агглютинации и фиксации комплемента, а также в предохранении внутрисосудистой среды от микробной инвазии. Белок часто называют макроглобулином , Ig. М первым из иммуноглобулинов реагирует на появление антигена. Ig. D - концентрация в сыворотке крови не более 1%, молекулярная масса 160000, обладает активируемой активностью, не связывается с тканями. Отмечено увеличение его содержания при миеломной болезни. Он действует как рецептор на поверхности незрелых В-лимфоцитов. По-видимому, Ig. D может играть роль в дифференциации этих клеток.
Класификация антител Ig М - циркулируют в крови, составляют 5 -10% всех антител. Молекулярная масса 950000, функционально пятивалентен, первым появляется после заражения или вакцинации. Не проходит через плаценту. Значение Ig. M определяется участием в механизме агглютинации и фиксации комплемента, а также в предохранении внутрисосудистой среды от микробной инвазии. Белок часто называют макроглобулином , Ig. М первым из иммуноглобулинов реагирует на появление антигена. Ig. D - концентрация в сыворотке крови не более 1%, молекулярная масса 160000, обладает активируемой активностью, не связывается с тканями. Отмечено увеличение его содержания при миеломной болезни. Он действует как рецептор на поверхности незрелых В-лимфоцитов. По-видимому, Ig. D может играть роль в дифференциации этих клеток.
 Класификация антител Ig А – включает два вида : сывороточный и секреторный. Сывороточный Ig A имеет молекулярную массу 170000, не обладает способностью преципитировать растворимые антигены, принимает участие в реакции нейтрализации токсинов. Термоустойчив, синтезируется в селезенке, лимфатических узлах и в слизистых оболочках и поступает в секреты – слюну, слезную жидкость, бронхиальный секрет, молозиво. Секреторный Ig A характеризуется наличием структурного добавочного компонента, представляет собой полимер с молекулярной массой 380000, синтезируется в слизистых оболочках. Биологическая функция заключается в местной защите слизистых оболочек, например, при заболеваниях желудочно-кишечного или дыхательного тракта. Обладает бактерицидностью и опсоническим эффектом. Ig. E - молекулярная масса 190000, прочно связывается с клетками тканей, с тканевыми базофилами, принимает участие в реакции гиперчувствительности немедленного типа. Ig. E играет защитную роль при гельминтозах и протозойных болезнях, способствует усилению фагоцитарной активности макрофагов и эозинофилов. Увеличение содержания этого иммуноглобулина при аллергических заболеваниях и миеломной болезни используется в качестве диагностического теста. У здоровых взрослых людей уровень Ig. Е в крови составляет в среднем 0, 0003 г/л
Класификация антител Ig А – включает два вида : сывороточный и секреторный. Сывороточный Ig A имеет молекулярную массу 170000, не обладает способностью преципитировать растворимые антигены, принимает участие в реакции нейтрализации токсинов. Термоустойчив, синтезируется в селезенке, лимфатических узлах и в слизистых оболочках и поступает в секреты – слюну, слезную жидкость, бронхиальный секрет, молозиво. Секреторный Ig A характеризуется наличием структурного добавочного компонента, представляет собой полимер с молекулярной массой 380000, синтезируется в слизистых оболочках. Биологическая функция заключается в местной защите слизистых оболочек, например, при заболеваниях желудочно-кишечного или дыхательного тракта. Обладает бактерицидностью и опсоническим эффектом. Ig. E - молекулярная масса 190000, прочно связывается с клетками тканей, с тканевыми базофилами, принимает участие в реакции гиперчувствительности немедленного типа. Ig. E играет защитную роль при гельминтозах и протозойных болезнях, способствует усилению фагоцитарной активности макрофагов и эозинофилов. Увеличение содержания этого иммуноглобулина при аллергических заболеваниях и миеломной болезни используется в качестве диагностического теста. У здоровых взрослых людей уровень Ig. Е в крови составляет в среднем 0, 0003 г/л
 Рецепторы лимфоцитов Лимфоциты при своем формировании проходят особый, только им присущий этап, который имеет прямое отношение к иммунной специфике: на определенной стадии развития на поверхности лимфоцитов появляются рецепторы для антигена. При этом одна клетка может иметь рецептор лишь для одного антигена, т. е. каждый лимфоцит способен распознать только одну пространственную конфигурацию чужеродных макромолекул.
Рецепторы лимфоцитов Лимфоциты при своем формировании проходят особый, только им присущий этап, который имеет прямое отношение к иммунной специфике: на определенной стадии развития на поверхности лимфоцитов появляются рецепторы для антигена. При этом одна клетка может иметь рецептор лишь для одного антигена, т. е. каждый лимфоцит способен распознать только одну пространственную конфигурацию чужеродных макромолекул.
 Рецепторы лимфоцитов На уровне генов, содержащихся в зародышевых клетках, обеспечивается лишь грубое распознавание за счет существования нескольких сотен так называемых вариабельных генов, и для достижения более тонкого распознавания эти «зародышевые» гены должны подвергнуться перестройке в процессе дифференцировки клеток. В итоге на поверхности как Т-лимфоцитов, так и Вдимфоцитов), появляются продукты перестроенных вариабельных, а также неизменных константных генов, которые формируют мембранный рецептор.
Рецепторы лимфоцитов На уровне генов, содержащихся в зародышевых клетках, обеспечивается лишь грубое распознавание за счет существования нескольких сотен так называемых вариабельных генов, и для достижения более тонкого распознавания эти «зародышевые» гены должны подвергнуться перестройке в процессе дифференцировки клеток. В итоге на поверхности как Т-лимфоцитов, так и Вдимфоцитов), появляются продукты перестроенных вариабельных, а также неизменных константных генов, которые формируют мембранный рецептор.
 Рецепторы лимфоцитов Основу антиген-распознающего рецептора В-лимфоцита составляет молекула иммуноглобулина, Ig (иммуноглобулиновые рецепторы памяти на поверхности В -лимфоцитов принадлежат к разным изотипам, за исключением Ig. M и Ig. D). Рецептор T- лимфоцита (TCR , от англ. Т cell receptor) представляет собой гетеродимер, состоящий из двух (альфа- и бета-) цепей (молекулярная масса каждой - 4050 к. Да), которые не являются продуктами иммуноглобулиновых генов. Существует два типа TCR, каждый из которых связан с разными типами T-лимфоцитов. TCR 1 , состоящий из гамма- и дельта-цепей, появляется на ранних стадиях онтогенеза. TCR 2 состоит из альфа- и бета-цепей. Каждая цепь альфа-бета-TСR имеет по одному наружному вариабельному V- и константному С-домену, гомологичных соответствующим доменам иммуноглобулинов. Вариабельный участок связывается с антигеном и молекулами MHC.
Рецепторы лимфоцитов Основу антиген-распознающего рецептора В-лимфоцита составляет молекула иммуноглобулина, Ig (иммуноглобулиновые рецепторы памяти на поверхности В -лимфоцитов принадлежат к разным изотипам, за исключением Ig. M и Ig. D). Рецептор T- лимфоцита (TCR , от англ. Т cell receptor) представляет собой гетеродимер, состоящий из двух (альфа- и бета-) цепей (молекулярная масса каждой - 4050 к. Да), которые не являются продуктами иммуноглобулиновых генов. Существует два типа TCR, каждый из которых связан с разными типами T-лимфоцитов. TCR 1 , состоящий из гамма- и дельта-цепей, появляется на ранних стадиях онтогенеза. TCR 2 состоит из альфа- и бета-цепей. Каждая цепь альфа-бета-TСR имеет по одному наружному вариабельному V- и константному С-домену, гомологичных соответствующим доменам иммуноглобулинов. Вариабельный участок связывается с антигеном и молекулами MHC.
 Структура рецепторов Т-клеток Альфа и бета-цепи совместно обуславливают распознавание специфичности антигена. У всех иммунокомпетентных T-лимфоцитов антигенный рецептор нековалентно, но прочно связан в комплекс с молекулой CD 3, которая состоит из пяти пептидных цепей (CD 3 -гамма, -дельта, -эпсилон, -зета и -зета-ню) и участвует в передаче сигнала от узнающего антиген альфа, бета-гетеродимера внутрь клетки. Кроме того, этот рецептор взаимодействует с определенным набором СD-молекул (далее).
Структура рецепторов Т-клеток Альфа и бета-цепи совместно обуславливают распознавание специфичности антигена. У всех иммунокомпетентных T-лимфоцитов антигенный рецептор нековалентно, но прочно связан в комплекс с молекулой CD 3, которая состоит из пяти пептидных цепей (CD 3 -гамма, -дельта, -эпсилон, -зета и -зета-ню) и участвует в передаче сигнала от узнающего антиген альфа, бета-гетеродимера внутрь клетки. Кроме того, этот рецептор взаимодействует с определенным набором СD-молекул (далее).
 Дифференцировка Влимфоцитов Связывание антигена с рецептором В-лимфоцита ведет к активации этих клеток и к их пролиферации, в результате чего образуются дочерние клетки –клон, его клетки называются плазматическими клетками, продуцирующими антитела. Для превращения Влимфоцитов в плазматические необходимо взаимодействие с антиген-презентующими клетками и Т-лимфоцитами хелперами Наряду с плазматическими клетками при контакте с антигеном возникают клетки памяти, которые после контакта с антигеном не производят антитела, а сохраняют информацию о структуре антигена
Дифференцировка Влимфоцитов Связывание антигена с рецептором В-лимфоцита ведет к активации этих клеток и к их пролиферации, в результате чего образуются дочерние клетки –клон, его клетки называются плазматическими клетками, продуцирующими антитела. Для превращения Влимфоцитов в плазматические необходимо взаимодействие с антиген-презентующими клетками и Т-лимфоцитами хелперами Наряду с плазматическими клетками при контакте с антигеном возникают клетки памяти, которые после контакта с антигеном не производят антитела, а сохраняют информацию о структуре антигена
 Дифференцировка Тлимфоцитов Дифференцировка лимфоцитов приводит к разделению на функциональные субпопуляции, т. е. на типы клеток, которые могут выполнять определенную работу, различную для каждого из этих типов. В случае развития Т-лимфоцитов их единая линия уже в тимусе разделяется на две основные ветви — Т-хелперы и Т-киллеры (цитотоксические Т-лимфоциты). Созревшие клетки со сформированными функциями и сложившимся репертуаром для распознавания антигенов расселяются в лимфоидных органах и скоплениях, причем не только в глубине организма, но и на его границах с окружающей средой — в барьерных тканях (кожа, слизистые оболочки).
Дифференцировка Тлимфоцитов Дифференцировка лимфоцитов приводит к разделению на функциональные субпопуляции, т. е. на типы клеток, которые могут выполнять определенную работу, различную для каждого из этих типов. В случае развития Т-лимфоцитов их единая линия уже в тимусе разделяется на две основные ветви — Т-хелперы и Т-киллеры (цитотоксические Т-лимфоциты). Созревшие клетки со сформированными функциями и сложившимся репертуаром для распознавания антигенов расселяются в лимфоидных органах и скоплениях, причем не только в глубине организма, но и на его границах с окружающей средой — в барьерных тканях (кожа, слизистые оболочки).
 Функции Т-хелперов Функция Т-хелперов состоит в оказании «помощи» (отсюда обозначение этих клеток — от англ. help) Влимфоцитам и Т-киллерам, которые распознали антиген. Для В-лимфоцитов недостаточно одного антигенного стимула, поскольку он лишь определяет выбор клеток, включаемых в ответную реакцию. Для вступления в реакцию требуется активация, они должны получить дополнительно сигналы стимуляции от контакта с клетками (на этот раз с Тхелперами) и от цитокинов. Активация приводит к размножению клеток соответствующих клонов и их дифференцировке в клетки-эффекторы, т. е. в «исполнители» конечных эффектов иммунного ответа
Функции Т-хелперов Функция Т-хелперов состоит в оказании «помощи» (отсюда обозначение этих клеток — от англ. help) Влимфоцитам и Т-киллерам, которые распознали антиген. Для В-лимфоцитов недостаточно одного антигенного стимула, поскольку он лишь определяет выбор клеток, включаемых в ответную реакцию. Для вступления в реакцию требуется активация, они должны получить дополнительно сигналы стимуляции от контакта с клетками (на этот раз с Тхелперами) и от цитокинов. Активация приводит к размножению клеток соответствующих клонов и их дифференцировке в клетки-эффекторы, т. е. в «исполнители» конечных эффектов иммунного ответа
 Участие клеток иммунной системы в иммунном ответе 1. Антиген (АГ) обрабатывается антиген-представляющими клетками (АПК) и презентуется T-лимфоцитам с участием молекул МНС АПК и рецепторов CD 4 и CD 8 T-клеток. 1 5 4 2. Рецепторы В-лимфоцитов связывают свободный АГ и презентуют его Т-хелперам 2 3. Дополнительная стимуляция осуществляется в процессе контактных взаимодействий с АПК (в случае В-клеток с Т-хелперами), а также при действии цитокинов. 4. Активированные лимфоциты пролиферируют и дифференцируются в эффекторные клетки. CD 4+-T-клeтки дифференцируются в два типа хелперов - Th 1 и Th 2, которые секретируют разные наборы цитокинов
Участие клеток иммунной системы в иммунном ответе 1. Антиген (АГ) обрабатывается антиген-представляющими клетками (АПК) и презентуется T-лимфоцитам с участием молекул МНС АПК и рецепторов CD 4 и CD 8 T-клеток. 1 5 4 2. Рецепторы В-лимфоцитов связывают свободный АГ и презентуют его Т-хелперам 2 3. Дополнительная стимуляция осуществляется в процессе контактных взаимодействий с АПК (в случае В-клеток с Т-хелперами), а также при действии цитокинов. 4. Активированные лимфоциты пролиферируют и дифференцируются в эффекторные клетки. CD 4+-T-клeтки дифференцируются в два типа хелперов - Th 1 и Th 2, которые секретируют разные наборы цитокинов
 Субпопуляции Т-хелперов Th 1 активируют макрофаги, что проявляется в усилении фагоцитоза бактерий, разрушении измененных клеток организма, секреции цитокинов Th 2 способствуют дифференцировке В-лимфоцитов в плазматические клетки, секретирующие антитела. Антитела связывают свободные и связанные с мембранами AГ, способствуя их расщеплению. СD 8+ Т-клетки при участии ИЛ-2 пролиферируют и дифференцируются в цитотоксические Т-лимфоциты, которые разрушают клетки, несущие на поверхности антиген.
Субпопуляции Т-хелперов Th 1 активируют макрофаги, что проявляется в усилении фагоцитоза бактерий, разрушении измененных клеток организма, секреции цитокинов Th 2 способствуют дифференцировке В-лимфоцитов в плазматические клетки, секретирующие антитела. Антитела связывают свободные и связанные с мембранами AГ, способствуя их расщеплению. СD 8+ Т-клетки при участии ИЛ-2 пролиферируют и дифференцируются в цитотоксические Т-лимфоциты, которые разрушают клетки, несущие на поверхности антиген.
 Субпопуляции Т-лимфоцитов хелперов Тh 1 связаны с развитием преимущественно клеточного, а Th 2 - с развитием гуморального иммунного ответа. При индукции иммунного ответа аллергенами чаще формируются клоны Th 2 -клеток Микроокружение лимфатических узлов благоприятствует развитию Thl-клеток, а микроокружение слизистых оболочек — Тh 2 -клеток При отсутствии вмешательства ИЛ-12 и интерферона γ СD 4+-клетки дифференцируются в Тh 2 -клетки. Развитию последних способствует ИЛ-4. Вероятнее всего продуцируют тучные клетки Под действием ИЛ-4 происходит переключение Влимфоцитов на синтез Ig. E и Ig. G 1. ИЛ-4 повышает экспрессию на В-лимфоцитах и тучных клетках CD 23 — низкоаффинного рецептора для Ig. E, который потенцирует выработку Ig. E. Эти эффекты, а также способность ИЛ-4 поддерживать пролиферацию тучных клеток имеют прямое отношение к развитию аллергических
Субпопуляции Т-лимфоцитов хелперов Тh 1 связаны с развитием преимущественно клеточного, а Th 2 - с развитием гуморального иммунного ответа. При индукции иммунного ответа аллергенами чаще формируются клоны Th 2 -клеток Микроокружение лимфатических узлов благоприятствует развитию Thl-клеток, а микроокружение слизистых оболочек — Тh 2 -клеток При отсутствии вмешательства ИЛ-12 и интерферона γ СD 4+-клетки дифференцируются в Тh 2 -клетки. Развитию последних способствует ИЛ-4. Вероятнее всего продуцируют тучные клетки Под действием ИЛ-4 происходит переключение Влимфоцитов на синтез Ig. E и Ig. G 1. ИЛ-4 повышает экспрессию на В-лимфоцитах и тучных клетках CD 23 — низкоаффинного рецептора для Ig. E, который потенцирует выработку Ig. E. Эти эффекты, а также способность ИЛ-4 поддерживать пролиферацию тучных клеток имеют прямое отношение к развитию аллергических
 Участие Т-хелперов в обеспечении иммунного ответа Клеточные формы иммунного ответа (Th 1) c участием соответствующих цитокинов Гуморалльные формы иммунного ответа с участием соответствующих цитокинов
Участие Т-хелперов в обеспечении иммунного ответа Клеточные формы иммунного ответа (Th 1) c участием соответствующих цитокинов Гуморалльные формы иммунного ответа с участием соответствующих цитокинов
 Распознавание антигена Нативный антиген, в частности, растворимый, распознается только иммуноглобулиновыми рецепторами В-лимфоцитов. Т-лимфоциты способны распознавать не антиген как таковой, а «измененное свое» — фрагменты антигена, встроенные в специализированные молекулы поверхности клеток организма — молекулы главного комплекса гистосовместимости. Это связано с особенностями специфичности рецептора Т-клеток: он распознает только антигенные детерминанты, встроенные в молекулы МНС. Молекула МНС служит как бы эталоном «своего» , и все отклонения от эталона распознаются рецепторами Т-лимфоцитов.
Распознавание антигена Нативный антиген, в частности, растворимый, распознается только иммуноглобулиновыми рецепторами В-лимфоцитов. Т-лимфоциты способны распознавать не антиген как таковой, а «измененное свое» — фрагменты антигена, встроенные в специализированные молекулы поверхности клеток организма — молекулы главного комплекса гистосовместимости. Это связано с особенностями специфичности рецептора Т-клеток: он распознает только антигенные детерминанты, встроенные в молекулы МНС. Молекула МНС служит как бы эталоном «своего» , и все отклонения от эталона распознаются рецепторами Т-лимфоцитов.
 Супрессорные Т-клетки В результате иммунного ответа малочисленная группа неактивных лимфоцитов, специфически распознавая чужеродный антиген, активируется, размножается и дифференцирует в эффекторные клетки, способные с помощью различных механизмов убивать клетки, несущие антиген По мере успешного выполнения задачи на уровне организма включаются и срабатывают механизмы, которые ограничивают иммунные процессы и приводят к устранению видимых последствий иммунного ответа. В этом участвуют антитела и лимфоциты благодаря проявлению ими супрессорной функции. Эту функцию осуществляет субпопуляция Т-лимфоцитов супрессоров. Они распознают «свои» и «чужие» антигеноыи посредством своих медиаторов регулируют иммунный ответ. Их супрессивное действие осуществляется в основном путем регуляции пролиферативной способности иммунокомпетентных клеток и торможения производства антител
Супрессорные Т-клетки В результате иммунного ответа малочисленная группа неактивных лимфоцитов, специфически распознавая чужеродный антиген, активируется, размножается и дифференцирует в эффекторные клетки, способные с помощью различных механизмов убивать клетки, несущие антиген По мере успешного выполнения задачи на уровне организма включаются и срабатывают механизмы, которые ограничивают иммунные процессы и приводят к устранению видимых последствий иммунного ответа. В этом участвуют антитела и лимфоциты благодаря проявлению ими супрессорной функции. Эту функцию осуществляет субпопуляция Т-лимфоцитов супрессоров. Они распознают «свои» и «чужие» антигеноыи посредством своих медиаторов регулируют иммунный ответ. Их супрессивное действие осуществляется в основном путем регуляции пролиферативной способности иммунокомпетентных клеток и торможения производства антител
 Характеристика основных популяций лимфоцитов человека Признак В-лимфоциты Т-лимфоциты NК-клетки Органы, где Костный мозг Костный мозг, Костный мозг развиваются вилочковая железа селезенка Рецептор для Иммуноглобулин Два типа димеров отсутствует антигена TCR (αβ или γδ) Основные CD 19, 20, 21, 72 CD 3, 2, 5, 7 CD 16, 57 мембранные CD 5 CD 4 и CD 8 маркеры Содержание в крови 8 -20% 65 -80% 5 -20% Функции Синтез антител Клеточный природные иммунитет киллеры Антигены CD имеют белковую природу и играют важную роль в иммунном ответе. Дифференцировочным антигенам по номенклатуре ВОЗ дается название CD плюс порядковый номер. Аббревитатура CD, расшифровывается как кластер дифференцировки и обозначает группу антител, распознающих одну и ту же или близкие антигенные детерминанты, но может использоваться и для обозначения самого антигена - молекулы, распознаваемой соответствующей группой антител.
Характеристика основных популяций лимфоцитов человека Признак В-лимфоциты Т-лимфоциты NК-клетки Органы, где Костный мозг Костный мозг, Костный мозг развиваются вилочковая железа селезенка Рецептор для Иммуноглобулин Два типа димеров отсутствует антигена TCR (αβ или γδ) Основные CD 19, 20, 21, 72 CD 3, 2, 5, 7 CD 16, 57 мембранные CD 5 CD 4 и CD 8 маркеры Содержание в крови 8 -20% 65 -80% 5 -20% Функции Синтез антител Клеточный природные иммунитет киллеры Антигены CD имеют белковую природу и играют важную роль в иммунном ответе. Дифференцировочным антигенам по номенклатуре ВОЗ дается название CD плюс порядковый номер. Аббревитатура CD, расшифровывается как кластер дифференцировки и обозначает группу антител, распознающих одну и ту же или близкие антигенные детерминанты, но может использоваться и для обозначения самого антигена - молекулы, распознаваемой соответствующей группой антител.
 Антиген-распознающий рецептор В-лимфоцита
Антиген-распознающий рецептор В-лимфоцита
 Рецептор Т-лимофцитов. αβ-рецептор CD 4+ Т-лимфоцитов
Рецептор Т-лимофцитов. αβ-рецептор CD 4+ Т-лимфоцитов
 Другие молекулы адгезии, участвующие в иммунном ответе Другие адгезивные молекулы важны для осуществления контактов с межклеточным матриксом и клетками стромы при миграции Тлимфоцитов, а также с вспомогательными клетками иммунной системы и с клетками-мишенями в процессе индукции иммунного ответа и при осуществлении реакций иммунитета. К ним относятся L-селектины — тканевые лектины, которые распознают углеводные остатки (сиалированную фукозу) мембранных гликопротеинов других клеток, а также интегрины. Среди β 1 -интегринов для Тлимфоцитов свойственны молекулы VLA-4 (α 4β 1) и VLA-5 (α 5β 1), среди β 2 -интегринов - LFA-1.
Другие молекулы адгезии, участвующие в иммунном ответе Другие адгезивные молекулы важны для осуществления контактов с межклеточным матриксом и клетками стромы при миграции Тлимфоцитов, а также с вспомогательными клетками иммунной системы и с клетками-мишенями в процессе индукции иммунного ответа и при осуществлении реакций иммунитета. К ним относятся L-селектины — тканевые лектины, которые распознают углеводные остатки (сиалированную фукозу) мембранных гликопротеинов других клеток, а также интегрины. Среди β 1 -интегринов для Тлимфоцитов свойственны молекулы VLA-4 (α 4β 1) и VLA-5 (α 5β 1), среди β 2 -интегринов - LFA-1.
 Иммунодефицитные заболевания, связанные с изменениями в системе Т-лимфоцитов. Генетическая блокада размножения и дифференцировки возможна на любом из этапов генеза Т-лимфоцитов. В генезе Т-лимфоцитов, по отношению к вилочковой железе, можно выделить три периода: дотимический, тимический и посттимический. В дотимическом периоде на I этапе стволовая кроветворная клетка превращается в полустволовую лимфоидную клетку-предшественник, общую для Т- и В-лимфоцитов. Блок на этом уровне приводит к полному нарушению выработки лимфоцитов обеих линий при сохраненном генезе других клеток крови — гранулоцитов, эритроцитов и др. Это вызывает такую степень иммунной беззащитности, которая приводит к гибели в раннем возрасте. На II этапе образуется полустволовая клетка-предшественник Тлимфоцитов. Блок на этом уровне приводит к отсутствию Тлимфоцитов при наличии В-лимфоцитов. При этом развивается тяжелое иммунодефицитное заболевание, обусловленное отсутствием иммунных реакций клеточного типа и выпадением других функций Тлимфоцитов. Генетический блок в период внутривилочковой дифференцировки клеток (IV этап) вызывает нарушения дифференцировки Тлимфоцитов, но не всегда приводит к их полному отсутствию в крови. При блоке посттимической дифференцировки клеток может нарушаться образование соответствующих субпопуляций Тлимфоцитов (V и VI этапы) — хелперов, супрессоров, киллеров.
Иммунодефицитные заболевания, связанные с изменениями в системе Т-лимфоцитов. Генетическая блокада размножения и дифференцировки возможна на любом из этапов генеза Т-лимфоцитов. В генезе Т-лимфоцитов, по отношению к вилочковой железе, можно выделить три периода: дотимический, тимический и посттимический. В дотимическом периоде на I этапе стволовая кроветворная клетка превращается в полустволовую лимфоидную клетку-предшественник, общую для Т- и В-лимфоцитов. Блок на этом уровне приводит к полному нарушению выработки лимфоцитов обеих линий при сохраненном генезе других клеток крови — гранулоцитов, эритроцитов и др. Это вызывает такую степень иммунной беззащитности, которая приводит к гибели в раннем возрасте. На II этапе образуется полустволовая клетка-предшественник Тлимфоцитов. Блок на этом уровне приводит к отсутствию Тлимфоцитов при наличии В-лимфоцитов. При этом развивается тяжелое иммунодефицитное заболевание, обусловленное отсутствием иммунных реакций клеточного типа и выпадением других функций Тлимфоцитов. Генетический блок в период внутривилочковой дифференцировки клеток (IV этап) вызывает нарушения дифференцировки Тлимфоцитов, но не всегда приводит к их полному отсутствию в крови. При блоке посттимической дифференцировки клеток может нарушаться образование соответствующих субпопуляций Тлимфоцитов (V и VI этапы) — хелперов, супрессоров, киллеров.
 Заболевания, при которых нарушено образование Т-лимфоцитов Первичная недостаточность T-клеток. Блокада ранних этапов образования Т-лимфоцитов или нарушение образования Т-хелперов. Гипоплазия вилочковой железы (синдром Ди Джорджи). Заболевание развивается в результате нарушения формирования третьего и четвертого окологлоточных жаберных карманов в эмбриональном периоде. В результате наряду с отсутствием вилочковой железы и Тлимфоцитов возникают дефекты лица, щитовидной и паращитовидной желез, пороки системы кровообращения. Не развиваются иммунные реакции клеточного типа, не происходит или сильно задерживается отторжение трансплантатов. Иммунодефицит Т-лимфоцитов, вызванный генетически обусловленным дефектом пуриннуклеотидфосфорилазы, приводит к снижению функции Т-лимфоцитов
Заболевания, при которых нарушено образование Т-лимфоцитов Первичная недостаточность T-клеток. Блокада ранних этапов образования Т-лимфоцитов или нарушение образования Т-хелперов. Гипоплазия вилочковой железы (синдром Ди Джорджи). Заболевание развивается в результате нарушения формирования третьего и четвертого окологлоточных жаберных карманов в эмбриональном периоде. В результате наряду с отсутствием вилочковой железы и Тлимфоцитов возникают дефекты лица, щитовидной и паращитовидной желез, пороки системы кровообращения. Не развиваются иммунные реакции клеточного типа, не происходит или сильно задерживается отторжение трансплантатов. Иммунодефицит Т-лимфоцитов, вызванный генетически обусловленным дефектом пуриннуклеотидфосфорилазы, приводит к снижению функции Т-лимфоцитов
 Заболевания, при которых нарушено образование В-лимфоцитов Возможны генетически обусловленные нарушения формирования В-лимфоцитов на всех этапах их созревания. Как указывалось выше, если генетический блок имеет место на уровне образования общего предшественника Т- и В-лимфоцитов (I этап), то может возникнуть сочетанный дефицит обеих линий лимфоцитов. Если наследственно обусловленный дефект будет препятствовать дифференцировке Влимфоцитов на II, IV этапах, то разовьется недостаточность В-лимфоцитов различных субпопуляций, а формирование системы Т-лимфоцитов может осуществляться обычным путем. При дефектах окончательной дифференцировки Влимфоцитов и клеток памяти на V, VII, VIII этапах может прекращаться синтез отдельных классов иммуноглобулинов
Заболевания, при которых нарушено образование В-лимфоцитов Возможны генетически обусловленные нарушения формирования В-лимфоцитов на всех этапах их созревания. Как указывалось выше, если генетический блок имеет место на уровне образования общего предшественника Т- и В-лимфоцитов (I этап), то может возникнуть сочетанный дефицит обеих линий лимфоцитов. Если наследственно обусловленный дефект будет препятствовать дифференцировке Влимфоцитов на II, IV этапах, то разовьется недостаточность В-лимфоцитов различных субпопуляций, а формирование системы Т-лимфоцитов может осуществляться обычным путем. При дефектах окончательной дифференцировки Влимфоцитов и клеток памяти на V, VII, VIII этапах может прекращаться синтез отдельных классов иммуноглобулинов
 Виды иммунодефицитов с нарушениями в системе В-лимфоцитов Гипогаммаглобулинемия Брутона. Блокируется образование всех типов плазматических клеток так, что количество Ig. G снижено в 10, а Ig. A и Ig. M — в 100 раз. Генетический дефект имеет место, вероятно, на уровне клеткипредшественника В-лимфоцитов. В крови и лимфатических узлах отсутствуют В-лимфоциты и плазматические клетки. Заболевание сцеплено с полом и проявляется у мальчиков. Реакции Т-лимфоцитов сохранены. Поздняя гипогаммаглобулинемия развивается в возрасте 25 — 30 лет, а иногда между 40 и 50 годами. При этом снижение количества иммуноглобулинов умеренное, но уменьшается и синтез изогемагглютининов групп крови. Иммунодефицит Ig. A развивается при генетическом блоке на конечном этапе трансформации В-лимфоцитов в плазматические клетки, синтезирующие Ig. A. Передается как аутосомный, рецессивный, а иногда доминантный признак. В некоторых случаях у больных обнаруживается делеция 18 -й хромосомы. Синтез других классов иммуноглобулинов обычно сохраняется. Кроме блока дифференцировки В-лимфоцитов дефицит иммуноглобулинов А развивается при генетически обусловленном дефекте синтеза секреторного компонента S в эпителии железистых органов. В результате содержание Ig. A в секрете уменьшается. Полипептид S необходим для превращения Ig. A в секретируемую форму.
Виды иммунодефицитов с нарушениями в системе В-лимфоцитов Гипогаммаглобулинемия Брутона. Блокируется образование всех типов плазматических клеток так, что количество Ig. G снижено в 10, а Ig. A и Ig. M — в 100 раз. Генетический дефект имеет место, вероятно, на уровне клеткипредшественника В-лимфоцитов. В крови и лимфатических узлах отсутствуют В-лимфоциты и плазматические клетки. Заболевание сцеплено с полом и проявляется у мальчиков. Реакции Т-лимфоцитов сохранены. Поздняя гипогаммаглобулинемия развивается в возрасте 25 — 30 лет, а иногда между 40 и 50 годами. При этом снижение количества иммуноглобулинов умеренное, но уменьшается и синтез изогемагглютининов групп крови. Иммунодефицит Ig. A развивается при генетическом блоке на конечном этапе трансформации В-лимфоцитов в плазматические клетки, синтезирующие Ig. A. Передается как аутосомный, рецессивный, а иногда доминантный признак. В некоторых случаях у больных обнаруживается делеция 18 -й хромосомы. Синтез других классов иммуноглобулинов обычно сохраняется. Кроме блока дифференцировки В-лимфоцитов дефицит иммуноглобулинов А развивается при генетически обусловленном дефекте синтеза секреторного компонента S в эпителии железистых органов. В результате содержание Ig. A в секрете уменьшается. Полипептид S необходим для превращения Ig. A в секретируемую форму.
 Иммунодефицитные заболевания (нарушения в системе В-лимфоцитов) Иммунодефицитное заболевание, связанное с блоком синтеза Ig. G и Ig. A при сохранении синтеза Ig. M. Генетический блок может быть на уровне конечных этапов превращения В-лимфоцитов в плазматические клетки, а также при переключении синтеза Ig. M на синтез Ig. G и Ig. A в одной и той же плазматической клетке. Иммунодефицит, связанный с генетическим блоком синтеза легких цепей иммуноглобулинов, в результате чего нарушается синтез полноцепочечных иммуноглобулинов. Иммунодефициты, связанные с дисфункцией иммуноцитов. При этом наряду со снижением продукции одних иммуноглобулинов возрастает синтез других. К таким болезням относится дефицит Ig. G (нередко с дефицитом Ig. A), который сопровождается увеличением синтеза Ig. M. Передается по наследству как сцепленный с полом или аутосомно-рецессивный признак. Комбинированные иммунодефицитные заболевания. Наибольшее число обнаруженных иммунодефицитных заболеваний являются комбинированными — с одновременным дефектом Т- и В-лимфоцитов.
Иммунодефицитные заболевания (нарушения в системе В-лимфоцитов) Иммунодефицитное заболевание, связанное с блоком синтеза Ig. G и Ig. A при сохранении синтеза Ig. M. Генетический блок может быть на уровне конечных этапов превращения В-лимфоцитов в плазматические клетки, а также при переключении синтеза Ig. M на синтез Ig. G и Ig. A в одной и той же плазматической клетке. Иммунодефицит, связанный с генетическим блоком синтеза легких цепей иммуноглобулинов, в результате чего нарушается синтез полноцепочечных иммуноглобулинов. Иммунодефициты, связанные с дисфункцией иммуноцитов. При этом наряду со снижением продукции одних иммуноглобулинов возрастает синтез других. К таким болезням относится дефицит Ig. G (нередко с дефицитом Ig. A), который сопровождается увеличением синтеза Ig. M. Передается по наследству как сцепленный с полом или аутосомно-рецессивный признак. Комбинированные иммунодефицитные заболевания. Наибольшее число обнаруженных иммунодефицитных заболеваний являются комбинированными — с одновременным дефектом Т- и В-лимфоцитов.
 Иммунодефицитные заболевания Швейцарский тип иммунодефицита. Передается как аутосомнорецессивный признак, проявляется в виде лимфоцитопении и гипогаммаглобулинемии (дефицита Т- и В-линий лимфоцитов одновременно), обнаруживается в первые недели жизни. Вилочковая железа зачаточной формы, кора и мозговое вещество ее не дифференцированы. В периферических лимфоидных органах (селезенке, лимфатических узлах) наблюдается резкое уменьшение количества лимфоцитов и плазматических клеток. Трансплантаты тканей не отторгаются, реакция замедленной гиперчувствительности отсутствует. Определяются следы Ig. G, отсутствуют Ig. M и Ig. A. У некоторых больных из-за отсутствия в клетках аденозиндезаминазы накапливается аденозин, который токсичен для лимфоцитов. Иммунодефицит с телеангиэктазией и атаксией (синдром Луи-Бар). Наследуется как аутосомно-рецессивное заболевание. Нарушена функция системы Т- и В-лимфоцитов, дифференцировка Т-лимфоцитов на ранних этапах генеза. Вилочковая железа находится в зачаточном состоянии, количество Т-лимфоцитов снижено, отсутствуют Ig. A, понижен или остается нормальным уровень Ig. G при нормальном содержании Ig. M. Нарушены конечные этапы дифференцировки В-лимфоцитов. Иммунодефицит с тромбоцитопенией и экземой (синдром Вискотта. Олдрича). Наследование заболевания сцеплено с полом, оно проявляется у мальчиков в возрасте старше 10 лет. Прогрессивно нарушается функция системы Т-лимфоцитов, опустошаются Т-зоны в лимфатических узлах. Одновременно нарушаются гуморальные иммунные реакции в связи с поражением В-системы: снижается количество Ig. M при нормальном содержании Ig. A и Ig. G.
Иммунодефицитные заболевания Швейцарский тип иммунодефицита. Передается как аутосомнорецессивный признак, проявляется в виде лимфоцитопении и гипогаммаглобулинемии (дефицита Т- и В-линий лимфоцитов одновременно), обнаруживается в первые недели жизни. Вилочковая железа зачаточной формы, кора и мозговое вещество ее не дифференцированы. В периферических лимфоидных органах (селезенке, лимфатических узлах) наблюдается резкое уменьшение количества лимфоцитов и плазматических клеток. Трансплантаты тканей не отторгаются, реакция замедленной гиперчувствительности отсутствует. Определяются следы Ig. G, отсутствуют Ig. M и Ig. A. У некоторых больных из-за отсутствия в клетках аденозиндезаминазы накапливается аденозин, который токсичен для лимфоцитов. Иммунодефицит с телеангиэктазией и атаксией (синдром Луи-Бар). Наследуется как аутосомно-рецессивное заболевание. Нарушена функция системы Т- и В-лимфоцитов, дифференцировка Т-лимфоцитов на ранних этапах генеза. Вилочковая железа находится в зачаточном состоянии, количество Т-лимфоцитов снижено, отсутствуют Ig. A, понижен или остается нормальным уровень Ig. G при нормальном содержании Ig. M. Нарушены конечные этапы дифференцировки В-лимфоцитов. Иммунодефицит с тромбоцитопенией и экземой (синдром Вискотта. Олдрича). Наследование заболевания сцеплено с полом, оно проявляется у мальчиков в возрасте старше 10 лет. Прогрессивно нарушается функция системы Т-лимфоцитов, опустошаются Т-зоны в лимфатических узлах. Одновременно нарушаются гуморальные иммунные реакции в связи с поражением В-системы: снижается количество Ig. M при нормальном содержании Ig. A и Ig. G.
 Иммунодефицитные заболевания Дефицит Т-лимфоцитов приводит к значительному снижению устойчивости к вирусным и грибковым заболеваниям, в меньшей степени — к гноеродной и пневмококковой инфекции. При недостаточности Т-лимфоцитов снижается способность организма отторгать трансплантаты, а при тяжелых формах ее эта способность утрачивается. Иммунодефициты системы В-лимфоцитов выражаются отсутствием или снижением гуморальных реакций в связи с дефицитом иммуноглобулинов одного или многих классов. Наблюдается значительное снижение устойчивости к стрептококковой, пневмококковой, кишечной инфекциям, что обусловливает развитие респираторных инфекций, пневмонии. При этом сохраняется устойчивость к вирусной и грибковой инфекции. Вид дефицита иммуноглобулинов определяет снижение устойчивости организма к той или иной инфекции: при дефиците Ig. M снижается устойчивость к грамотрицательным микробам; при дефиците Ig. A ослабляется защита слизистой оболочки пищеварительной системы, глаз и др.
Иммунодефицитные заболевания Дефицит Т-лимфоцитов приводит к значительному снижению устойчивости к вирусным и грибковым заболеваниям, в меньшей степени — к гноеродной и пневмококковой инфекции. При недостаточности Т-лимфоцитов снижается способность организма отторгать трансплантаты, а при тяжелых формах ее эта способность утрачивается. Иммунодефициты системы В-лимфоцитов выражаются отсутствием или снижением гуморальных реакций в связи с дефицитом иммуноглобулинов одного или многих классов. Наблюдается значительное снижение устойчивости к стрептококковой, пневмококковой, кишечной инфекциям, что обусловливает развитие респираторных инфекций, пневмонии. При этом сохраняется устойчивость к вирусной и грибковой инфекции. Вид дефицита иммуноглобулинов определяет снижение устойчивости организма к той или иной инфекции: при дефиците Ig. M снижается устойчивость к грамотрицательным микробам; при дефиците Ig. A ослабляется защита слизистой оболочки пищеварительной системы, глаз и др.
 © П. Ф. Литвицкий, 2004 ГЭОТАР-МЕД, 2004 © С П И Д * ПРИЧИНА: · ВИРУС ИММУНОДЕФИЦИТА ЧЕЛОВЕКА (ВИЧ), * ФАКТОРЫ РИСКА: · СПИД У РОДИТЕЛЕЙ (для детей) · БЕСПОРЯДОЧНЫЕ ГОМО- И БИСЕКСУАЛЬНЫЕ КОНТАКТЫ · ИСПОЛЬЗОВАНИЕ “КОЛЛЕКТИВНЫХ ” ШПРИЦЕВ ретровирус (разновидность лентивирусов). · ЧАСТЫЕ ГЕМОТРАНСФУЗИИ
© П. Ф. Литвицкий, 2004 ГЭОТАР-МЕД, 2004 © С П И Д * ПРИЧИНА: · ВИРУС ИММУНОДЕФИЦИТА ЧЕЛОВЕКА (ВИЧ), * ФАКТОРЫ РИСКА: · СПИД У РОДИТЕЛЕЙ (для детей) · БЕСПОРЯДОЧНЫЕ ГОМО- И БИСЕКСУАЛЬНЫЕ КОНТАКТЫ · ИСПОЛЬЗОВАНИЕ “КОЛЛЕКТИВНЫХ ” ШПРИЦЕВ ретровирус (разновидность лентивирусов). · ЧАСТЫЕ ГЕМОТРАНСФУЗИИ
 © П. Ф. Литвицкий, 2004 ГЭОТАР-МЕД, 2004 © КЛЕТКИ – “МИШЕНИ ” ДЛЯ ВИРУСА СПИД`а Т– лимфоциты хелперы моноциты В – лимфоциты тканевые макрофаги нейроны естественные киллеры клетки глии
© П. Ф. Литвицкий, 2004 ГЭОТАР-МЕД, 2004 © КЛЕТКИ – “МИШЕНИ ” ДЛЯ ВИРУСА СПИД`а Т– лимфоциты хелперы моноциты В – лимфоциты тканевые макрофаги нейроны естественные киллеры клетки глии
 © П. Ф. Литвицкий, 2004 ГЭОТАР-МЕД, 2004 © +
© П. Ф. Литвицкий, 2004 ГЭОТАР-МЕД, 2004 © +
 Иммунодефициты, связанные с недостаточностью ферментов В лейкоцитах также могут образовываться наследственные дефекты ферментов, необходимых для внутриклеточного разрушения бактерий) в частности дефицит НАДФН-оксидазы и недостаточное образование перекиси водорода, без которой процесс фагоцитоза нарушается и становится незавершенным. Этот дефект отмечается при хроническом гранулематозе. Больные устойчивы к пневмо-, стрепто-менингококковой инфекции, в то время как стафилококки, кишечная палочка — условно патогенная флора — вызывают тяжелые заболевания. Это показывает, что основную функцию защиты от сапрофитных инфекций, возможно, выполняет фагоцитоз. К сходным нарушениям приводит дефект миелопероксидазы. Отмечены также наследственные дефекты сократительного белка — актина, в отсутствие которого нарушается смыкание цитоплазматической мембраны над фагосомой.
Иммунодефициты, связанные с недостаточностью ферментов В лейкоцитах также могут образовываться наследственные дефекты ферментов, необходимых для внутриклеточного разрушения бактерий) в частности дефицит НАДФН-оксидазы и недостаточное образование перекиси водорода, без которой процесс фагоцитоза нарушается и становится незавершенным. Этот дефект отмечается при хроническом гранулематозе. Больные устойчивы к пневмо-, стрепто-менингококковой инфекции, в то время как стафилококки, кишечная палочка — условно патогенная флора — вызывают тяжелые заболевания. Это показывает, что основную функцию защиты от сапрофитных инфекций, возможно, выполняет фагоцитоз. К сходным нарушениям приводит дефект миелопероксидазы. Отмечены также наследственные дефекты сократительного белка — актина, в отсутствие которого нарушается смыкание цитоплазматической мембраны над фагосомой.
 Корреляция между иммунной системой и антигенным составом организма Антигенный состав организма может обусловливать и повышение иммунитета. Так, у лиц с группой крови В (III) в несколько раз ниже заболеваемость чумой. Благодаря иммунологическим методам исследования в организме обнаружены различные антигены, функция которых до настоящего времени остается неизвестной. Тем не менее установлена связь между этими антигенами и заболеваниями. Так, у лиц, гомозиготных по антигенам I группы крови 0 (I), в 3 раза чаще встречается язвенная болезнь желудка. Возможно, что антигены А- и В-групп крови необходимы мембранам клеток слизистой оболочки желудка в обеспечении их устойчивости к действию соляной кислоты, и именно эти антигены отсутствуют у лиц группы крови 0 (I), либо их присутствие мешает заселению желудка Helicobacter pylori. У людей, имеющих трансплантационный антиген HLA-B 8 главной системы гистосовместимости МНС (кодируется тремя генами, расположенными у людей в хромосоме 6 -й пары), существенно увеличена частота аутоиммунных повреждений мышц, надпочечных желез, печени, кожи, щитовидной железы, кишок. У людей, имеющих трансплантационные антигены HLA-B 8 и HLA-B 15, чаще всего наблюдается юношеский диабет, у носителей HLA-B 27 — поражение мочеполовой системы (болезнь Рейтера) и юношеский ревматоидный полиартрит, у носителей HLA-B 13, HLA-17 и HLA-B 28 — псориаз. Инсулин-зависимый диабет четко ассоциирован с наследованием главного локуса гистосовместимости HLA-DR 4.
Корреляция между иммунной системой и антигенным составом организма Антигенный состав организма может обусловливать и повышение иммунитета. Так, у лиц с группой крови В (III) в несколько раз ниже заболеваемость чумой. Благодаря иммунологическим методам исследования в организме обнаружены различные антигены, функция которых до настоящего времени остается неизвестной. Тем не менее установлена связь между этими антигенами и заболеваниями. Так, у лиц, гомозиготных по антигенам I группы крови 0 (I), в 3 раза чаще встречается язвенная болезнь желудка. Возможно, что антигены А- и В-групп крови необходимы мембранам клеток слизистой оболочки желудка в обеспечении их устойчивости к действию соляной кислоты, и именно эти антигены отсутствуют у лиц группы крови 0 (I), либо их присутствие мешает заселению желудка Helicobacter pylori. У людей, имеющих трансплантационный антиген HLA-B 8 главной системы гистосовместимости МНС (кодируется тремя генами, расположенными у людей в хромосоме 6 -й пары), существенно увеличена частота аутоиммунных повреждений мышц, надпочечных желез, печени, кожи, щитовидной железы, кишок. У людей, имеющих трансплантационные антигены HLA-B 8 и HLA-B 15, чаще всего наблюдается юношеский диабет, у носителей HLA-B 27 — поражение мочеполовой системы (болезнь Рейтера) и юношеский ревматоидный полиартрит, у носителей HLA-B 13, HLA-17 и HLA-B 28 — псориаз. Инсулин-зависимый диабет четко ассоциирован с наследованием главного локуса гистосовместимости HLA-DR 4.
 Аллергия АЛЛЕРГИЯ (allergia; греч. allos другой + ergon действие) — повышенная чувствительность организма к воздействию некоторых факторов окружающей среды (химических веществ, микроорганизмов и продуктов их жизнедеятельности, пищевых продуктов и др. ), называемых аллергенами. Аллергия – это реакция гиперчувствительности, запускаемая иммунологическими механизмами. Аллергия может быть антитело- или клеточно-опосредованной. У большинства пациентов антитело, типично отвечающее за аллергическую реакцию, принадлежит к Ig. E-изотипу, и про этих пациентов можно сказать, что они страдают от Ig. E-опосредованной аллергии или атопии Выявлено более 20 генов-кандидатов, вызывающих возникновение гиперчувствительности атопического типа. С практической точки зрения, важен факт, что гены, определяющие бронхиальную гиперреактивность и механизмы атопических реакций различны, следовательно, даже тяжелое течение атопического дерматита (АД) не всегда приводит к развитию бронхиальной астмы (БА). Отмечают также, что существуют отдельные геныкандидаты, ответственные только за назальные симптомы при аллергическом рините (АР). Возникновение аллергии в первую очередь связано с нарушением баланса между Th 1 и Th 2 хелперами
Аллергия АЛЛЕРГИЯ (allergia; греч. allos другой + ergon действие) — повышенная чувствительность организма к воздействию некоторых факторов окружающей среды (химических веществ, микроорганизмов и продуктов их жизнедеятельности, пищевых продуктов и др. ), называемых аллергенами. Аллергия – это реакция гиперчувствительности, запускаемая иммунологическими механизмами. Аллергия может быть антитело- или клеточно-опосредованной. У большинства пациентов антитело, типично отвечающее за аллергическую реакцию, принадлежит к Ig. E-изотипу, и про этих пациентов можно сказать, что они страдают от Ig. E-опосредованной аллергии или атопии Выявлено более 20 генов-кандидатов, вызывающих возникновение гиперчувствительности атопического типа. С практической точки зрения, важен факт, что гены, определяющие бронхиальную гиперреактивность и механизмы атопических реакций различны, следовательно, даже тяжелое течение атопического дерматита (АД) не всегда приводит к развитию бронхиальной астмы (БА). Отмечают также, что существуют отдельные геныкандидаты, ответственные только за назальные симптомы при аллергическом рините (АР). Возникновение аллергии в первую очередь связано с нарушением баланса между Th 1 и Th 2 хелперами
 Проявления аллергии Аллергический ринит — наиболее распространенное в этом ряду заболевание. Он бывает как сезонным, возникающим во время цветения растений, так и круглогодичным, в качестве реакции на бытовые аллергены. Заложенность носа, насморк, сопровождающийся раздражением глаз и слезотечением, является к тому же и первопричиной заболеваний нервной системы. Бронхиальная астма (от греч. asthma — тяжелое дыхание) — это хроническое заболевание дыхательных путей, сопровождающееся приступообразным кашлем, выделением мокроты, приступами удушья. Как и другие аллергические болезни, астма часто передается по наследству. Крапивница — это аллергическая реакция, встречающаяся не менее часто, чем ринит и бронхиальная астма. При крапивнице на коже появляются зудящие волдыри, похожие на ожоги от крапивы. Отек Квинке — вид аллергической реакции, длящийся от нескольких часов до нескольких суток. Для него характерно внезапное появление отека кожи, подкожной клетчатки и слизистых оболочек. Обычно отек поражает губы, щеки, веки, половые органы. При отеке Квинке в области гортани возникает удушье. Анафилактический шок (греч. ana — обратный и philaxis — защита) — самая тяжелая аллергическая реакция, возникающая при повторном попадании аллергена в организм. Ее характерные проявления заключаются во внезапном появлении острого зуда, за которым следуют затруднение дыхания и шок. В тяжелых случаях возможен также отек легких и головного мозга. Чаще всего такая форма аллергической реакции возникает при проникновении в организм различных сильнодействующих веществ, а также при укусах насекомых.
Проявления аллергии Аллергический ринит — наиболее распространенное в этом ряду заболевание. Он бывает как сезонным, возникающим во время цветения растений, так и круглогодичным, в качестве реакции на бытовые аллергены. Заложенность носа, насморк, сопровождающийся раздражением глаз и слезотечением, является к тому же и первопричиной заболеваний нервной системы. Бронхиальная астма (от греч. asthma — тяжелое дыхание) — это хроническое заболевание дыхательных путей, сопровождающееся приступообразным кашлем, выделением мокроты, приступами удушья. Как и другие аллергические болезни, астма часто передается по наследству. Крапивница — это аллергическая реакция, встречающаяся не менее часто, чем ринит и бронхиальная астма. При крапивнице на коже появляются зудящие волдыри, похожие на ожоги от крапивы. Отек Квинке — вид аллергической реакции, длящийся от нескольких часов до нескольких суток. Для него характерно внезапное появление отека кожи, подкожной клетчатки и слизистых оболочек. Обычно отек поражает губы, щеки, веки, половые органы. При отеке Квинке в области гортани возникает удушье. Анафилактический шок (греч. ana — обратный и philaxis — защита) — самая тяжелая аллергическая реакция, возникающая при повторном попадании аллергена в организм. Ее характерные проявления заключаются во внезапном появлении острого зуда, за которым следуют затруднение дыхания и шок. В тяжелых случаях возможен также отек легких и головного мозга. Чаще всего такая форма аллергической реакции возникает при проникновении в организм различных сильнодействующих веществ, а также при укусах насекомых.
 Классификация Аллергическая реакция I типа (реакция немедленного типа, реагиновый, анафилактический, атопический тип). Она развивается с образованием АТ, относящихся к классу Ig. E и lg. G 4, которые фиксируются на тучных клетках и базофилах. При их соединении с аллергеном из этих клеток выделяются медиаторы: гистамин, гепарин, серотонин, тромбоцитактивирующий фактор, простагландины, лейкотриены и др. , определяющие клинику аллергической реакции немедленного типа. После контакта со специфическим аллергеном клинические проявления реакции возникают через 15 -20 мин. Аллергическая реакция II типа (цитотоксический тип). Тип характеризуется тем, что AT образуются к клеткам тканей и представлены Ig. G и Ig. M. Этот тип реакции вызывается только AT, способными активизировать комплемент. AT соединяются с видоизмененными клетками организма, что приводит к реакции активации комплемента, который также вызывает повреждение и разрушение клеток с последующим фагоцитозом и удалением их. Именно по цитотоксическому типу происходит развитие лекарственной аллергии. Аллергическая реакция III типа (повреждение тканей иммунными комплексами - тип Артюса, иммунокомплексный тип). Возникает в результате образования циркулирующих иммунных комплексов, в состав которых входят Ig. G и Ig. M. AT этого класса называют преципитирующими, так как они образуют преципитат при соединении с АГ. Этот тип реакции является ведущим в развитии сывороточной болезни, аллергических альвеолитов, лекарственной и пищевой аллергии, при ряде аутоаллергических заболеваний (СКВ,
Классификация Аллергическая реакция I типа (реакция немедленного типа, реагиновый, анафилактический, атопический тип). Она развивается с образованием АТ, относящихся к классу Ig. E и lg. G 4, которые фиксируются на тучных клетках и базофилах. При их соединении с аллергеном из этих клеток выделяются медиаторы: гистамин, гепарин, серотонин, тромбоцитактивирующий фактор, простагландины, лейкотриены и др. , определяющие клинику аллергической реакции немедленного типа. После контакта со специфическим аллергеном клинические проявления реакции возникают через 15 -20 мин. Аллергическая реакция II типа (цитотоксический тип). Тип характеризуется тем, что AT образуются к клеткам тканей и представлены Ig. G и Ig. M. Этот тип реакции вызывается только AT, способными активизировать комплемент. AT соединяются с видоизмененными клетками организма, что приводит к реакции активации комплемента, который также вызывает повреждение и разрушение клеток с последующим фагоцитозом и удалением их. Именно по цитотоксическому типу происходит развитие лекарственной аллергии. Аллергическая реакция III типа (повреждение тканей иммунными комплексами - тип Артюса, иммунокомплексный тип). Возникает в результате образования циркулирующих иммунных комплексов, в состав которых входят Ig. G и Ig. M. AT этого класса называют преципитирующими, так как они образуют преципитат при соединении с АГ. Этот тип реакции является ведущим в развитии сывороточной болезни, аллергических альвеолитов, лекарственной и пищевой аллергии, при ряде аутоаллергических заболеваний (СКВ,
 Развитие аллергической реакции В течении специфических аллергических реакций различают три стадии: I стадию — иммунологическую; II стадию — патохимическую, или образования медиаторов; III стадию — патофизиологическую, или стадию клинического проявления повреждения. В I стадии отмечается повышенная чувствительность к впервые попавшему в организм аллергену — сенсибилизация. Происходит это в результате выработки антител, образующихся в ответ на введение только данного аллергена, или появления лимфоцитов, способных взаимодействовать с данным аллергеном. Если к моменту их возникновения аллерген удален из организма, никаких болезненных проявлений не наблюдается. При повторном воздействии на уже сенсибилизированный к нему организм аллерген соединяется с образовавшимися антителами или лимфоцитами. С этого момента начинается II стадия — происходит ряд биохимических процессов с выделением гистамина и других медиаторов. Если количество медиаторов и их соотношение оказываются неоптимальными, то это приводит к повреждению клеток, тканей, органов — развивается III стадия, т. е. собственно клиническое проявления аллергической реакции. Повышенная чувствительность организма в таких случаях специфична: она проявляется по отношению к аллергену, который ранее вызвал состояние сенсибилизации
Развитие аллергической реакции В течении специфических аллергических реакций различают три стадии: I стадию — иммунологическую; II стадию — патохимическую, или образования медиаторов; III стадию — патофизиологическую, или стадию клинического проявления повреждения. В I стадии отмечается повышенная чувствительность к впервые попавшему в организм аллергену — сенсибилизация. Происходит это в результате выработки антител, образующихся в ответ на введение только данного аллергена, или появления лимфоцитов, способных взаимодействовать с данным аллергеном. Если к моменту их возникновения аллерген удален из организма, никаких болезненных проявлений не наблюдается. При повторном воздействии на уже сенсибилизированный к нему организм аллерген соединяется с образовавшимися антителами или лимфоцитами. С этого момента начинается II стадия — происходит ряд биохимических процессов с выделением гистамина и других медиаторов. Если количество медиаторов и их соотношение оказываются неоптимальными, то это приводит к повреждению клеток, тканей, органов — развивается III стадия, т. е. собственно клиническое проявления аллергической реакции. Повышенная чувствительность организма в таких случаях специфична: она проявляется по отношению к аллергену, который ранее вызвал состояние сенсибилизации
 Наиболее распространенные аллергены Пыльцевые аллергены. Поллинозы (от pollen - пыльца) характеризуются строгой сезонностью, поражением дыхательных путей, конъюнктивы глаз, реже - кожи. Аллергенность пыльцы зависит от сенсибилизирующих свойств ее собственных частей, количества в воздухе и т. п. Выделяют несколько групп аллергоопасных растений. В средней полосе России это - ряд деревьев (береза, ольха, орешник и др. ), злаковые (тимофеевка, ежа, овсяница), культурные злаки (рожь, пшеница, ячмень и др. ), сорные травы (полынь). При постановке кожных тестов с пыльцевыми аллергенами возможны так называемые перекрестные реакции: например, при аллергии на пыльцу березы - на аллергены орешника и ольхи. Бытовые аллергены. К категории бытовых аллергенов относят домашнюю пыль, в состав которой входят аллергены микроклещей, тараканов и других внутрижилищных насекомых, споры грибов, эпидермис и слюна домашних животных, частицы отделочных материалов и т. д. В последнее время значимыми признаны не только клещевые, но и другие инсектные аллергены - тараканов, моли, оконных муравьев и др. Эпидермальные аллергены. Наиболее значимыми источниками эпидермальных аллергенов являются домашние животные - кошки, собаки. Грибковые аллергены. Аллергия к вдыхаемым грибковым аллергенам жилища (споры плесневых грибов, ржавчинный, головневый, дрожжевой грибы) является причиной респираторных аллергических заболеваний. Концентрация грибковых аэроаллергенов особенно высока в квартирах с высокой влажностью. Грибы заселяют бумажные изделия, обои, кожу, комнатные растения, землю в цветочных горшках (здесь создаются условия для их интенсивного размножения).
Наиболее распространенные аллергены Пыльцевые аллергены. Поллинозы (от pollen - пыльца) характеризуются строгой сезонностью, поражением дыхательных путей, конъюнктивы глаз, реже - кожи. Аллергенность пыльцы зависит от сенсибилизирующих свойств ее собственных частей, количества в воздухе и т. п. Выделяют несколько групп аллергоопасных растений. В средней полосе России это - ряд деревьев (береза, ольха, орешник и др. ), злаковые (тимофеевка, ежа, овсяница), культурные злаки (рожь, пшеница, ячмень и др. ), сорные травы (полынь). При постановке кожных тестов с пыльцевыми аллергенами возможны так называемые перекрестные реакции: например, при аллергии на пыльцу березы - на аллергены орешника и ольхи. Бытовые аллергены. К категории бытовых аллергенов относят домашнюю пыль, в состав которой входят аллергены микроклещей, тараканов и других внутрижилищных насекомых, споры грибов, эпидермис и слюна домашних животных, частицы отделочных материалов и т. д. В последнее время значимыми признаны не только клещевые, но и другие инсектные аллергены - тараканов, моли, оконных муравьев и др. Эпидермальные аллергены. Наиболее значимыми источниками эпидермальных аллергенов являются домашние животные - кошки, собаки. Грибковые аллергены. Аллергия к вдыхаемым грибковым аллергенам жилища (споры плесневых грибов, ржавчинный, головневый, дрожжевой грибы) является причиной респираторных аллергических заболеваний. Концентрация грибковых аэроаллергенов особенно высока в квартирах с высокой влажностью. Грибы заселяют бумажные изделия, обои, кожу, комнатные растения, землю в цветочных горшках (здесь создаются условия для их интенсивного размножения).
 Наиболее распространенные аллергены Инфекционные аллергены. Группу инфекционных аллергенов представляют аллергены микробные (бактериальные), грибковые и вирусные. Инфекционно-аллергические заболевания- одни из самых сложных для лечения. Особое значение в последние годы придают аллергенам условно-патогенных микроорганизмов - активным сенсибилизаторам тканей бронхолегочного аппарата человека. Следует указать и на выраженную активность патогенных микробов, заселяющих бронхи больных инфекционной бронхиальной астмой. Активным сенсибилизатором является дрожжеподобный гриб рода Candida - С. albicans. Пищевые аллергены. Основные аллергены этой группы - коровье молоко, куриные яйца, рыба, цитрусовые, шоколад. Аллергенные свойства пищевого продукта зависят от его химической структуры и концентрации в нем белка. Пищевые добавки и красители, широко используемые при изготовлении консервов и кондитерских изделий, способны провоцировать псевдоаллергические реакции. Промышленные аллергены. Это химические и биологические загрязнители среды - выбросы различных производств, отходы, образующиеся при внедрении неудачных технологий. С проблемой антропогенных аллергенов тесно связаны проблемы защиты окружающей среды.
Наиболее распространенные аллергены Инфекционные аллергены. Группу инфекционных аллергенов представляют аллергены микробные (бактериальные), грибковые и вирусные. Инфекционно-аллергические заболевания- одни из самых сложных для лечения. Особое значение в последние годы придают аллергенам условно-патогенных микроорганизмов - активным сенсибилизаторам тканей бронхолегочного аппарата человека. Следует указать и на выраженную активность патогенных микробов, заселяющих бронхи больных инфекционной бронхиальной астмой. Активным сенсибилизатором является дрожжеподобный гриб рода Candida - С. albicans. Пищевые аллергены. Основные аллергены этой группы - коровье молоко, куриные яйца, рыба, цитрусовые, шоколад. Аллергенные свойства пищевого продукта зависят от его химической структуры и концентрации в нем белка. Пищевые добавки и красители, широко используемые при изготовлении консервов и кондитерских изделий, способны провоцировать псевдоаллергические реакции. Промышленные аллергены. Это химические и биологические загрязнители среды - выбросы различных производств, отходы, образующиеся при внедрении неудачных технологий. С проблемой антропогенных аллергенов тесно связаны проблемы защиты окружающей среды.
 Механизмы, запускающие аллергические реакции При недостаточной активности определенной субпопуляции Тсупрессоров, либо при повышенной активности Th 2 хелперов происходит переключение В-лимфоцитов на синтез Ig. E, что может привести к возникновению сенсибилизации атопического типа. Дефицит секреторного Ig. A способствует проникновению через слизистые оболочки дыхательных путей или желудочнокишечного тракта аллергенов и развитию аллергических реакций как атопического, так и других типов. В крови здоровых людей lg. E содержится в незначительных количествах — всего 20— 120 едмл, а в крови аллергиков с атопическими проявлениями этот уровень повышается до нескольких тысяч единиц, в зависимости от длительности и тяжести заболевания. Причем повышение этого иммуноглобулина у таких больных фиксируется как во время приступов, так и между ними.
Механизмы, запускающие аллергические реакции При недостаточной активности определенной субпопуляции Тсупрессоров, либо при повышенной активности Th 2 хелперов происходит переключение В-лимфоцитов на синтез Ig. E, что может привести к возникновению сенсибилизации атопического типа. Дефицит секреторного Ig. A способствует проникновению через слизистые оболочки дыхательных путей или желудочнокишечного тракта аллергенов и развитию аллергических реакций как атопического, так и других типов. В крови здоровых людей lg. E содержится в незначительных количествах — всего 20— 120 едмл, а в крови аллергиков с атопическими проявлениями этот уровень повышается до нескольких тысяч единиц, в зависимости от длительности и тяжести заболевания. Причем повышение этого иммуноглобулина у таких больных фиксируется как во время приступов, так и между ними.
 Антагонисты Н 1 -рецепторов Антигистаминовая структура (Н 1) Хлорфенирамин антагонист Н 1 Доксиламин антагонист Н 1
Антагонисты Н 1 -рецепторов Антигистаминовая структура (Н 1) Хлорфенирамин антагонист Н 1 Доксиламин антагонист Н 1
 Лечение аллергии Наиболее известны препараты т. н. первого поколения, к которым относятся димедрол, тавегил, супрастин, фенкарол, кетотифен и др. Однако, несмотря на эффективность этих лекарств, у них есть ряд недостатков. Они обладают снотворным эффектом, многие вызывают сухость слизистых оболочек, нарушают зрение, повышают аппетит (а соответственно увеличивается и вес тела). Многие из них способны снижать артериальное давление и даже извращать действие некоторых лекарств; к ним быстро развивается привыкание, и необходима смена препарата уже через 7 -10 дней. Кроме того, при длительном применении препараты первого поколения нарушают психоэмоциональное развитие ребенка, а у мужчин могут вызвать импотенцию. Препараты второго поколения более совершенны: большинство из них не оказывает угнетающего действия на центральную нервную систему, не влияет на умственную и физическую работоспособность, не обладает снотворным эффектом и не вызывает привыкания. К числу таких препаратов относятся кларитин (лоратадин), трексил, гисманал, гисталонг, аллергодил и др. Однако некоторые препараты второго поколения (в частности, терфенадин, астемизол) при передозировке или в сочетании с другими лекарствами способны оказывать кардиотоксический эффект, проявляющийся в развитии тяжелых аритмий. Прием антигистаминных средств второго поколения зачастую противопоказан при заболеваниях печени и почек. В последние годы появились препараты, лишенные целого ряда недостатков своих предшественников. Это т. н. антигистаминные препараты третьего поколения (хотя такого деления придерживаются не все специалисты). Они обладают рядом преимуществ: у них отсутствует кардиотоксический эффект, возможен прием при заболевании печени, почек, они сочетаются с другими медикаментами и не зависят от приема пищи. Одним из наиболее удачных представителей новых антигистаминных средств является дезлоратадин (эриус). Эриус создан на основе лоратадина (кларитина), который многие годы успешно применялся для лечения многих аллергических заболеваний и реакций, в т. ч. атопического дерматита и крапивницы.
Лечение аллергии Наиболее известны препараты т. н. первого поколения, к которым относятся димедрол, тавегил, супрастин, фенкарол, кетотифен и др. Однако, несмотря на эффективность этих лекарств, у них есть ряд недостатков. Они обладают снотворным эффектом, многие вызывают сухость слизистых оболочек, нарушают зрение, повышают аппетит (а соответственно увеличивается и вес тела). Многие из них способны снижать артериальное давление и даже извращать действие некоторых лекарств; к ним быстро развивается привыкание, и необходима смена препарата уже через 7 -10 дней. Кроме того, при длительном применении препараты первого поколения нарушают психоэмоциональное развитие ребенка, а у мужчин могут вызвать импотенцию. Препараты второго поколения более совершенны: большинство из них не оказывает угнетающего действия на центральную нервную систему, не влияет на умственную и физическую работоспособность, не обладает снотворным эффектом и не вызывает привыкания. К числу таких препаратов относятся кларитин (лоратадин), трексил, гисманал, гисталонг, аллергодил и др. Однако некоторые препараты второго поколения (в частности, терфенадин, астемизол) при передозировке или в сочетании с другими лекарствами способны оказывать кардиотоксический эффект, проявляющийся в развитии тяжелых аритмий. Прием антигистаминных средств второго поколения зачастую противопоказан при заболеваниях печени и почек. В последние годы появились препараты, лишенные целого ряда недостатков своих предшественников. Это т. н. антигистаминные препараты третьего поколения (хотя такого деления придерживаются не все специалисты). Они обладают рядом преимуществ: у них отсутствует кардиотоксический эффект, возможен прием при заболевании печени, почек, они сочетаются с другими медикаментами и не зависят от приема пищи. Одним из наиболее удачных представителей новых антигистаминных средств является дезлоратадин (эриус). Эриус создан на основе лоратадина (кларитина), который многие годы успешно применялся для лечения многих аллергических заболеваний и реакций, в т. ч. атопического дерматита и крапивницы.
 Специфическая иммунотерапия Наиболее эффективным способом лечения аллергических заболеваний является специфическая иммунотерапия (СИТ) специально созданными препаратами аллергенов. СИТ, заключающаяся в многократном введении больным субклинических доз специфических аллергенов с целью снижения гиперреактивности, используется уже более 80 лет, однако ее механизмы до конца не изучены. Главный принцип СИТ - введение малых доз аллергена при сниженном риске провокации реакций анафилактического типа - определяет и основные требования к лечебным формам аллергенов. Лечебные аллергены обладают меньшей активностью, чем диагностические, сохраняют исходную специфичность. Обычная схема предусматривает 24 -54 инъекций. Курс предсезонной терапии продолжается 2 -4 мес. Для СИТ выбирают аллергены, элиминация которых невозможна (аллергены деревьев, трав, цветов, клещей, спор грибов, яда насекомых), причем те, которые, несомненно, провоцируют у пациента аллергические реакции.
Специфическая иммунотерапия Наиболее эффективным способом лечения аллергических заболеваний является специфическая иммунотерапия (СИТ) специально созданными препаратами аллергенов. СИТ, заключающаяся в многократном введении больным субклинических доз специфических аллергенов с целью снижения гиперреактивности, используется уже более 80 лет, однако ее механизмы до конца не изучены. Главный принцип СИТ - введение малых доз аллергена при сниженном риске провокации реакций анафилактического типа - определяет и основные требования к лечебным формам аллергенов. Лечебные аллергены обладают меньшей активностью, чем диагностические, сохраняют исходную специфичность. Обычная схема предусматривает 24 -54 инъекций. Курс предсезонной терапии продолжается 2 -4 мес. Для СИТ выбирают аллергены, элиминация которых невозможна (аллергены деревьев, трав, цветов, клещей, спор грибов, яда насекомых), причем те, которые, несомненно, провоцируют у пациента аллергические реакции.


