Лекция 4.ppt
- Количество слайдов: 31
 Лекция № 4 Основы химической кинетики. Химическое равновесие 1. Некоторые основные понятия. 2. Основные факторы, определяющие скорость химической реакции. 3. Молекулярность реакции. Понятие о механизме реакции. 4. Теория скоростей реакций (теория переходного состояния). 5. Катализ. Каталитические реакции. Понятие о механизме катализа. 6. Химическое равновесие. 1
Лекция № 4 Основы химической кинетики. Химическое равновесие 1. Некоторые основные понятия. 2. Основные факторы, определяющие скорость химической реакции. 3. Молекулярность реакции. Понятие о механизме реакции. 4. Теория скоростей реакций (теория переходного состояния). 5. Катализ. Каталитические реакции. Понятие о механизме катализа. 6. Химическое равновесие. 1
 ХИМИЧЕСКАЯ КИНЕТИКА Химическая кинетика – раздел физической химии, в котором химические превращения веществ изучаются как процессы, протекающие во времени, исследуются закономерности, определяющие скорости этих превращений, а также их механизмы Формальная (феноменологическая) или макрокинетика – описание химического превращения проводится на основании экспериментальных данных о текущих концентрациях (парциальных давлениях) реагентов Теория скоростей или микрокинетика – описание процессов производится на микроуровне с учетом свойств реагирующих частиц 2
ХИМИЧЕСКАЯ КИНЕТИКА Химическая кинетика – раздел физической химии, в котором химические превращения веществ изучаются как процессы, протекающие во времени, исследуются закономерности, определяющие скорости этих превращений, а также их механизмы Формальная (феноменологическая) или макрокинетика – описание химического превращения проводится на основании экспериментальных данных о текущих концентрациях (парциальных давлениях) реагентов Теория скоростей или микрокинетика – описание процессов производится на микроуровне с учетом свойств реагирующих частиц 2
 ХИМИЧЕСКАЯ КИНЕТИКА Прямая задача – определение скоростей химических реакций и концентраций участников этих реакций в любой момент времени начальные условия (начальные концентрации участников реакции) вид кинетического уравнения (определяется механизмом химической реакции) Обратная задача – определение вида кинетического уравнения, описывающего реакцию кинетические данные (зависимости концентраций участников реакции от времени Ci = f(t)) механизм реакции • константа скорости химической реакции • порядок химической реакции 3
ХИМИЧЕСКАЯ КИНЕТИКА Прямая задача – определение скоростей химических реакций и концентраций участников этих реакций в любой момент времени начальные условия (начальные концентрации участников реакции) вид кинетического уравнения (определяется механизмом химической реакции) Обратная задача – определение вида кинетического уравнения, описывающего реакцию кинетические данные (зависимости концентраций участников реакции от времени Ci = f(t)) механизм реакции • константа скорости химической реакции • порядок химической реакции 3
 ХИМИЧЕСКАЯ КИНЕТИКА • столкновение реагирующих частиц • наличие у этих частиц достаточного запаса энергии • оптимальное расположение частиц друг относительно друга в пространстве Скорость химической реакции определяется числом соударений (элементарных актов химической реакции), приводящих к химическому превращению в единице объема в единицу времени На практике скорость гомогенных реакций определяется изменением концентрации реагирующих веществ в единицу времени Скорость гетерогенной реакции определяется числом молей веществ, вступивших в или образующихся в результате реакции в единицу времени на единице поверхности 4
ХИМИЧЕСКАЯ КИНЕТИКА • столкновение реагирующих частиц • наличие у этих частиц достаточного запаса энергии • оптимальное расположение частиц друг относительно друга в пространстве Скорость химической реакции определяется числом соударений (элементарных актов химической реакции), приводящих к химическому превращению в единице объема в единицу времени На практике скорость гомогенных реакций определяется изменением концентрации реагирующих веществ в единицу времени Скорость гетерогенной реакции определяется числом молей веществ, вступивших в или образующихся в результате реакции в единицу времени на единице поверхности 4

 ХИМИЧЕСКАЯ КИНЕТИКА ОСНОВНЫЕ ФАКТОРЫ, ОПРЕДЕЛЯЮЩИЕ СКОРОСТЬ ХИМИЧЕСКОЙ РЕАКЦИИ • • • Природы реагирующих веществ Концентрации реагирующих веществ Температуры Наличия катализатора Величины поверхности раздела (для гетерогенных реакций) Прочих энергетических воздействий (светового, радиационного и др. ) 6
ХИМИЧЕСКАЯ КИНЕТИКА ОСНОВНЫЕ ФАКТОРЫ, ОПРЕДЕЛЯЮЩИЕ СКОРОСТЬ ХИМИЧЕСКОЙ РЕАКЦИИ • • • Природы реагирующих веществ Концентрации реагирующих веществ Температуры Наличия катализатора Величины поверхности раздела (для гетерогенных реакций) Прочих энергетических воздействий (светового, радиационного и др. ) 6
 ХИМИЧЕСКАЯ КИНЕТИКА Скорость химической реакции зависит от • • • Природы реагирующих веществ Концентрации реагирующих веществ Температуры Наличия катализатора Величины поверхности раздела (для гетерогенных реакций) Прочих энергетических воздействий (светового, радиационного и др. ) Закон действующих масс скорость химической реакции при постоянной температуре прямо пропорциональна произведению мольных концентраций реагирующих веществ, возведенных в определенные степени (К. Гульдберг, П. Вааге, 1867 г. Норвегия) - молярные концентрации, моль/л - порядок реакции - константа скорости реакции (скорость химической реакции при концентрации реагирующих веществ, равных 1 моль/л) 7
ХИМИЧЕСКАЯ КИНЕТИКА Скорость химической реакции зависит от • • • Природы реагирующих веществ Концентрации реагирующих веществ Температуры Наличия катализатора Величины поверхности раздела (для гетерогенных реакций) Прочих энергетических воздействий (светового, радиационного и др. ) Закон действующих масс скорость химической реакции при постоянной температуре прямо пропорциональна произведению мольных концентраций реагирующих веществ, возведенных в определенные степени (К. Гульдберг, П. Вааге, 1867 г. Норвегия) - молярные концентрации, моль/л - порядок реакции - константа скорости реакции (скорость химической реакции при концентрации реагирующих веществ, равных 1 моль/л) 7
 ХИМИЧЕСКАЯ КИНЕТИКА - молярные концентрации, моль/л - порядок реакции - константа скорости реакции (скорость химической реакции при концентрации реагирующих веществ, равных 1 моль/л) Константа скорости химической реакции НЕ ЗАВИСИТ от концентраций (парциальных давлений) участников реакции и ЗАВИСИТ от: • температуры • давления (для газофазных реакций, для жидкофазных выражено слабо, т. к. сжимаемость жидкостей очень мала) • наличия катализатора (или ингибитора) • ряда других факторов (например, природы растворителя – для реакций, протекающих в растворах)… 8
ХИМИЧЕСКАЯ КИНЕТИКА - молярные концентрации, моль/л - порядок реакции - константа скорости реакции (скорость химической реакции при концентрации реагирующих веществ, равных 1 моль/л) Константа скорости химической реакции НЕ ЗАВИСИТ от концентраций (парциальных давлений) участников реакции и ЗАВИСИТ от: • температуры • давления (для газофазных реакций, для жидкофазных выражено слабо, т. к. сжимаемость жидкостей очень мала) • наличия катализатора (или ингибитора) • ряда других факторов (например, природы растворителя – для реакций, протекающих в растворах)… 8
 ХИМИЧЕСКАЯ КИНЕТИКА Порядок реакции устанавливается экспериментально при обработке данных кинетических исследований и основан на решении кинетического уравнения А→В 9
ХИМИЧЕСКАЯ КИНЕТИКА Порядок реакции устанавливается экспериментально при обработке данных кинетических исследований и основан на решении кинетического уравнения А→В 9
 ХИМИЧЕСКАЯ КИНЕТИКА Некоторые примеры реакций различного порядка Теоретическое уравнение V=k С (N 2) С 3 (Н 2); р = 4. Найденная экспериментально зависимость скорости реакции от концентраций реагентов Для гетерогенных систем 10
ХИМИЧЕСКАЯ КИНЕТИКА Некоторые примеры реакций различного порядка Теоретическое уравнение V=k С (N 2) С 3 (Н 2); р = 4. Найденная экспериментально зависимость скорости реакции от концентраций реагентов Для гетерогенных систем 10
 ХИМИЧЕСКАЯ КИНЕТИКА А→В n=0 Необратимые реакции 0 -ого порядка где k - константа скорости необратимой реакции 0 -го порядка • концентрация реагента автоматически поддерживается постоянной (например, в насыщенном растворе вещества, контактирующем с избытком этого не растворившегося вещества); • скорость реакции определяется не концентрацией реагирующего вещества, которая очень велика и практически не изменяется (или изменяется незначительно) в ходе реакции, а иными факторами – концентрацией катализатора (при гомогенном катализе) или фермента (при ферментативном катализе), количеством поглощенного света (для фотохимических реакций) и др. 11
ХИМИЧЕСКАЯ КИНЕТИКА А→В n=0 Необратимые реакции 0 -ого порядка где k - константа скорости необратимой реакции 0 -го порядка • концентрация реагента автоматически поддерживается постоянной (например, в насыщенном растворе вещества, контактирующем с избытком этого не растворившегося вещества); • скорость реакции определяется не концентрацией реагирующего вещества, которая очень велика и практически не изменяется (или изменяется незначительно) в ходе реакции, а иными факторами – концентрацией катализатора (при гомогенном катализе) или фермента (при ферментативном катализе), количеством поглощенного света (для фотохимических реакций) и др. 11
 ХИМИЧЕСКАЯ КИНЕТИКА Необратимые реакции 0 -ого порядка А→В Графическое определение константы скорости необратимой реакции 0 -го порядка k τ, c 12
ХИМИЧЕСКАЯ КИНЕТИКА Необратимые реакции 0 -ого порядка А→В Графическое определение константы скорости необратимой реакции 0 -го порядка k τ, c 12
 ХИМИЧЕСКАЯ КИНЕТИКА Необратимые реакции 0 -ого порядка А→В Время (период) полупревращения (полураспада) - время, в течение которого концентрация исходного вещества уменьшается в два раза т. е. если то Время полупревращения 13
ХИМИЧЕСКАЯ КИНЕТИКА Необратимые реакции 0 -ого порядка А→В Время (период) полупревращения (полураспада) - время, в течение которого концентрация исходного вещества уменьшается в два раза т. е. если то Время полупревращения 13
 ХИМИЧЕСКАЯ КИНЕТИКА n=1 Необратимые реакции 1 -ого порядка А→В интегрируем k τ, c 14
ХИМИЧЕСКАЯ КИНЕТИКА n=1 Необратимые реакции 1 -ого порядка А→В интегрируем k τ, c 14
 ХИМИЧЕСКАЯ КИНЕТИКА Порядок реакции устанавливается экспериментально при обработке данных кинетических исследований и основан на решении кинетического уравнения Порядок реакции Кинетическое уравнение Координаты, в которых график зависимости С(τ) линеен 0 1 2 n 15
ХИМИЧЕСКАЯ КИНЕТИКА Порядок реакции устанавливается экспериментально при обработке данных кинетических исследований и основан на решении кинетического уравнения Порядок реакции Кинетическое уравнение Координаты, в которых график зависимости С(τ) линеен 0 1 2 n 15
 ХИМИЧЕСКАЯ КИНЕТИКА Скорость химической реакции зависит от • • • Природы реагирующих веществ Концентрации реагирующих веществ Температуры Наличия катализатора Величины поверхности раздела (для гетерогенных реакций) Прочих энергетических воздействий (светового, радиационного и др. ) правило Вант-Гоффа γ - температурный коэффициент скорости реакции При повышении температуры на каждые 10 градусов константа скорости гомогенной элементарной реакции увеличивается в два – четыре раза Якоб Хендрик Вант-Гофф 16
ХИМИЧЕСКАЯ КИНЕТИКА Скорость химической реакции зависит от • • • Природы реагирующих веществ Концентрации реагирующих веществ Температуры Наличия катализатора Величины поверхности раздела (для гетерогенных реакций) Прочих энергетических воздействий (светового, радиационного и др. ) правило Вант-Гоффа γ - температурный коэффициент скорости реакции При повышении температуры на каждые 10 градусов константа скорости гомогенной элементарной реакции увеличивается в два – четыре раза Якоб Хендрик Вант-Гофф 16
 ХИМИЧЕСКАЯ КИНЕТИКА Зависимость скорости химической реакции от температуры Допущения Аррениуса Изобара химической реакции Изохора химической реакции - реагировать могут не все молекулы, а лишь находящиеся в особой таутомерной форме или активной модификации - образование активной модификации рассматривается как обратимая реакция, а концентрация этой модификации всегда соответствует термодинамическому равновесию и в принципе ее можно выразить через константу равновесия - концентрация активной модификации всегда мала и ее образование практически не влияет на концентрацию исходных молекул - образовавшаяся активная модификация превращается в продукт со скоростью, независящей от температуры Сванте Август Аррениус 17
ХИМИЧЕСКАЯ КИНЕТИКА Зависимость скорости химической реакции от температуры Допущения Аррениуса Изобара химической реакции Изохора химической реакции - реагировать могут не все молекулы, а лишь находящиеся в особой таутомерной форме или активной модификации - образование активной модификации рассматривается как обратимая реакция, а концентрация этой модификации всегда соответствует термодинамическому равновесию и в принципе ее можно выразить через константу равновесия - концентрация активной модификации всегда мала и ее образование практически не влияет на концентрацию исходных молекул - образовавшаяся активная модификация превращается в продукт со скоростью, независящей от температуры Сванте Август Аррениус 17
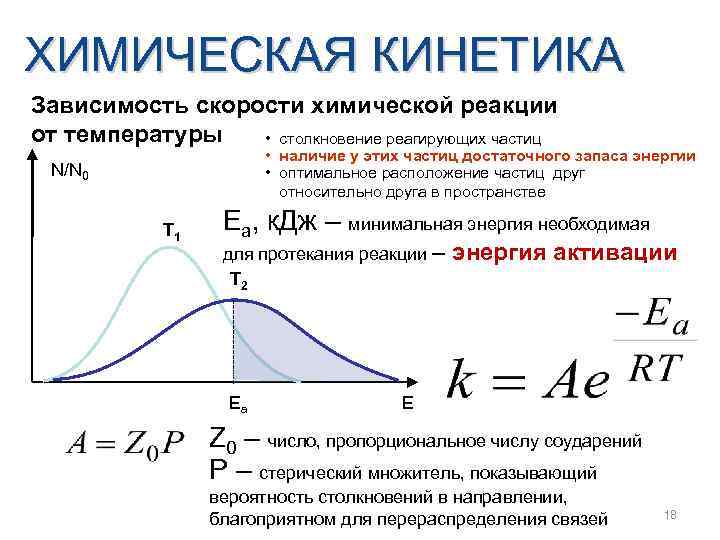 ХИМИЧЕСКАЯ КИНЕТИКА Зависимость скорости химической реакции от температуры • столкновение реагирующих частиц • наличие у этих частиц достаточного запаса энергии • оптимальное расположение частиц друг относительно друга в пространстве N/N 0 T 1 Eа, к. Дж – минимальная энергия необходимая для протекания реакции – энергия T 2 Ea активации E Z 0 – число, пропорциональное числу соударений P – стерический множитель, показывающий вероятность столкновений в направлении, благоприятном для перераспределения связей 18
ХИМИЧЕСКАЯ КИНЕТИКА Зависимость скорости химической реакции от температуры • столкновение реагирующих частиц • наличие у этих частиц достаточного запаса энергии • оптимальное расположение частиц друг относительно друга в пространстве N/N 0 T 1 Eа, к. Дж – минимальная энергия необходимая для протекания реакции – энергия T 2 Ea активации E Z 0 – число, пропорциональное числу соударений P – стерический множитель, показывающий вероятность столкновений в направлении, благоприятном для перераспределения связей 18
 ХИМИЧЕСКАЯ КИНЕТИКА Определение энергии активации Аналитический метод 19
ХИМИЧЕСКАЯ КИНЕТИКА Определение энергии активации Аналитический метод 19
 ХИМИЧЕСКАЯ КИНЕТИКА Определение энергии активации Графический метод 20
ХИМИЧЕСКАЯ КИНЕТИКА Определение энергии активации Графический метод 20
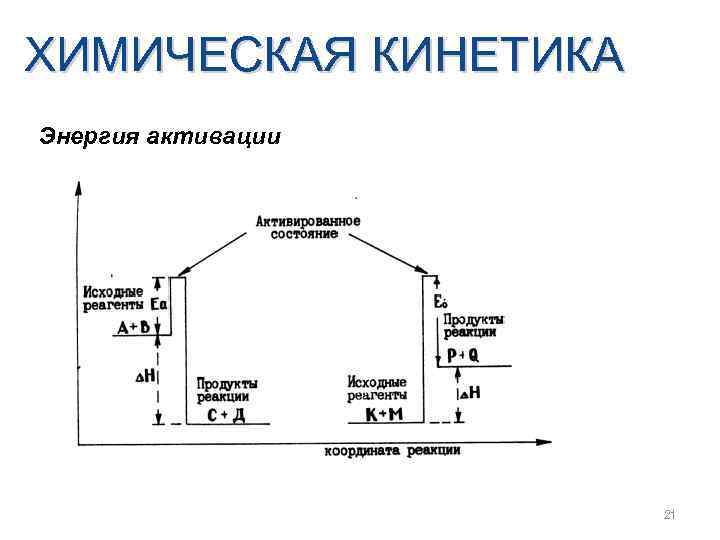 ХИМИЧЕСКАЯ КИНЕТИКА Энергия активации 21
ХИМИЧЕСКАЯ КИНЕТИКА Энергия активации 21
 ХИМИЧЕСКАЯ КИНЕТИКА Другие факторы влияющие на скорость реакции Молекулярность определяется по числу молекул одновременное соударение которых приводит к химическому взаимодействию 22
ХИМИЧЕСКАЯ КИНЕТИКА Другие факторы влияющие на скорость реакции Молекулярность определяется по числу молекул одновременное соударение которых приводит к химическому взаимодействию 22
 ХИМИЧЕСКАЯ КИНЕТИКА 23
ХИМИЧЕСКАЯ КИНЕТИКА 23
 ХИМИЧЕСКАЯ КИНЕТИКА 24
ХИМИЧЕСКАЯ КИНЕТИКА 24
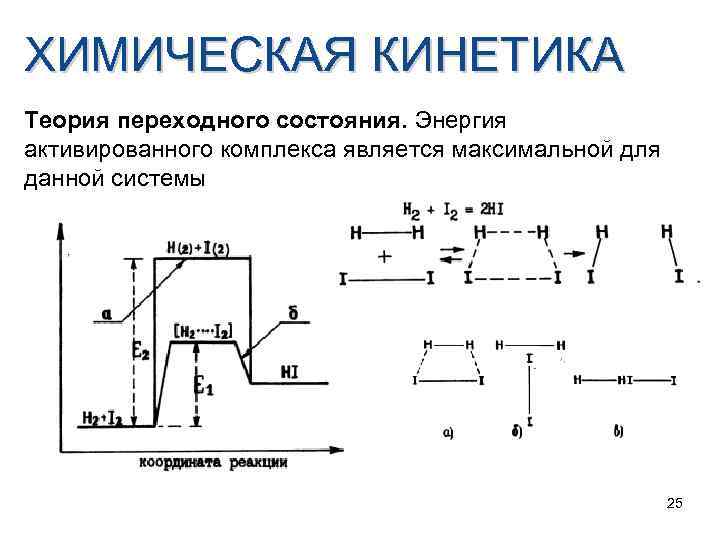 ХИМИЧЕСКАЯ КИНЕТИКА Теория переходного состояния. Энергия активированного комплекса является максимальной для данной системы 25
ХИМИЧЕСКАЯ КИНЕТИКА Теория переходного состояния. Энергия активированного комплекса является максимальной для данной системы 25
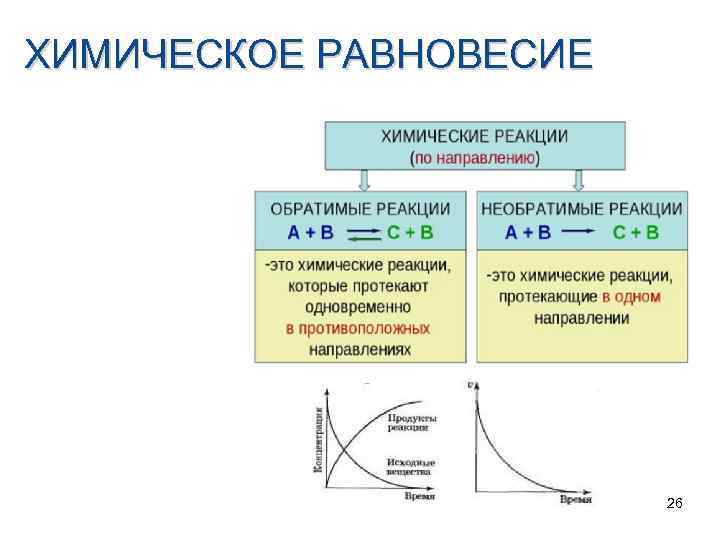 ХИМИЧЕСКОЕ РАВНОВЕСИЕ 26
ХИМИЧЕСКОЕ РАВНОВЕСИЕ 26
 ХИМИЧЕСКОЕ РАВНОВЕСИЕ 1) Равновесие является динамическим процессом. Это означает, что в положении равновесия протекают химические реакции, но это не отражается на свойствах системы. Так, в равновесной системе N 2 О 4(г) = 2 NО 2(г) димер оксида азота диссоциирует с образованием оксида азота и одновременно оксид азота димеризуется (обратный процесс). Эти процессы не прекращаются во времени. 2) Для любой реакции характерно стремление самопроизвольно смещаться к положению равновесия, движущей силой в этом случае является изменение энергии Гиббса. 3) Равновесие достигается тогда, когда энергия системы будет наименьшей, а изменение энергии Гиббса становится равным 0. 27
ХИМИЧЕСКОЕ РАВНОВЕСИЕ 1) Равновесие является динамическим процессом. Это означает, что в положении равновесия протекают химические реакции, но это не отражается на свойствах системы. Так, в равновесной системе N 2 О 4(г) = 2 NО 2(г) димер оксида азота диссоциирует с образованием оксида азота и одновременно оксид азота димеризуется (обратный процесс). Эти процессы не прекращаются во времени. 2) Для любой реакции характерно стремление самопроизвольно смещаться к положению равновесия, движущей силой в этом случае является изменение энергии Гиббса. 3) Равновесие достигается тогда, когда энергия системы будет наименьшей, а изменение энергии Гиббса становится равным 0. 27
 ХИМИЧЕСКОЕ РАВНОВЕСИЕ Принцип Ле Шателье: «Если на систему, находящуюся в состоянии химического равновесия, оказать внешнее воздействие (изменив температуру, давление или концентрации веществ), то положение равновесия сместится таким образом, чтобы ослабить внешнее воздействие» . 28
ХИМИЧЕСКОЕ РАВНОВЕСИЕ Принцип Ле Шателье: «Если на систему, находящуюся в состоянии химического равновесия, оказать внешнее воздействие (изменив температуру, давление или концентрации веществ), то положение равновесия сместится таким образом, чтобы ослабить внешнее воздействие» . 28
 ХИМИЧЕСКОЕ РАВНОВЕСИЕ Константа равновесия G 0 = -R · T · ln K = -2, 3 · R · T · lg K при 298 К(250 С) это уравнение преобразуется к виду G 0 = -5, 69 · lg K Константа равновесия связана с энтальпией системы: Из уравнения Аррениуса k = A · e-Eа /R ·T Кравн = А · е - Н /R·T –уравнение Вант - Гоффа, или в логарифмической форме ln. K = ln. A - H/R · T 29
ХИМИЧЕСКОЕ РАВНОВЕСИЕ Константа равновесия G 0 = -R · T · ln K = -2, 3 · R · T · lg K при 298 К(250 С) это уравнение преобразуется к виду G 0 = -5, 69 · lg K Константа равновесия связана с энтальпией системы: Из уравнения Аррениуса k = A · e-Eа /R ·T Кравн = А · е - Н /R·T –уравнение Вант - Гоффа, или в логарифмической форме ln. K = ln. A - H/R · T 29
 ХИМИЧЕСКОЕ РАВНОВЕСИЕ Правило фаз Гиббса: в равновесной многофазной системе число степеней свободы равно числу компонентов плюс два, минус число фаз. С = К + 2 - Ф или Ф + С = К + 2, где С – число степеней свободы К – число компонентов Ф – число фаз в системе инвариантная система, если (С = 0). моновариантная, если (С = 1), бивариантная, если (С = 2) В физических системах число компонентов равно числу составляющих систему веществ В химических системах число компонентов меньше числа составляющих веществ на число уравнений, по которым вещества, образующие систему, обратимо реагируют между собой: Ca. CO (тв) Ca. O(тв) + СО (г) 3 2 30
ХИМИЧЕСКОЕ РАВНОВЕСИЕ Правило фаз Гиббса: в равновесной многофазной системе число степеней свободы равно числу компонентов плюс два, минус число фаз. С = К + 2 - Ф или Ф + С = К + 2, где С – число степеней свободы К – число компонентов Ф – число фаз в системе инвариантная система, если (С = 0). моновариантная, если (С = 1), бивариантная, если (С = 2) В физических системах число компонентов равно числу составляющих систему веществ В химических системах число компонентов меньше числа составляющих веществ на число уравнений, по которым вещества, образующие систему, обратимо реагируют между собой: Ca. CO (тв) Ca. O(тв) + СО (г) 3 2 30
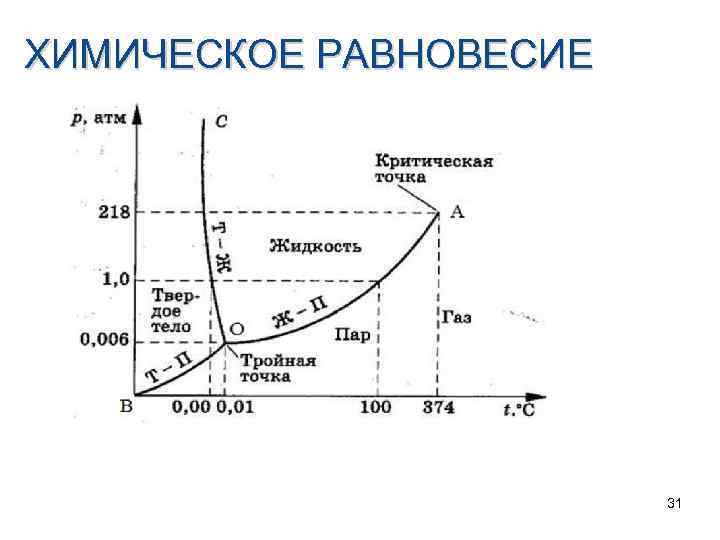 ХИМИЧЕСКОЕ РАВНОВЕСИЕ 31
ХИМИЧЕСКОЕ РАВНОВЕСИЕ 31


