Лек_4_прод.ppt
- Количество слайдов: 21
 Лекция 4. Ферменты (продолжение). • • • Классификация ферментов Кинетика ферментативных реакций Уравнение Михаэлиса-Ментен Специфичность действия ферментов Основные этапы каталитического акта Действие факторов внешней среды на активность ферментов
Лекция 4. Ферменты (продолжение). • • • Классификация ферментов Кинетика ферментативных реакций Уравнение Михаэлиса-Ментен Специфичность действия ферментов Основные этапы каталитического акта Действие факторов внешней среды на активность ферментов
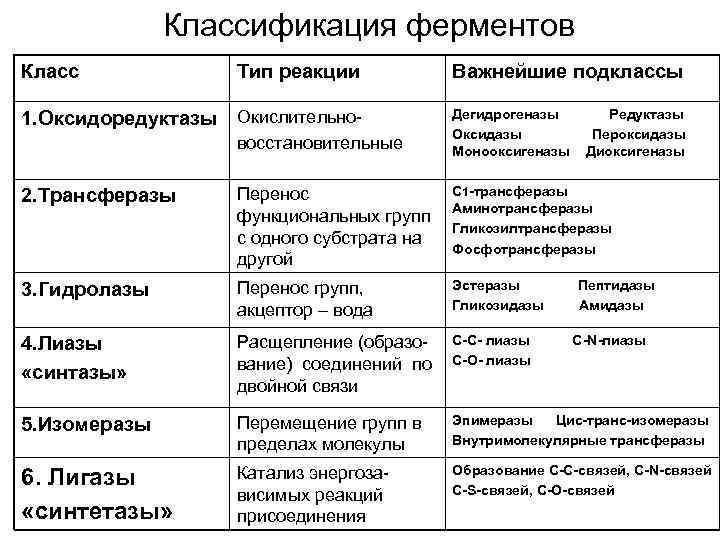 Классификация ферментов Класс Тип реакции 1. Оксидоредуктазы Окислительновосстановительные Важнейшие подклассы Дегидрогеназы Оксидазы Монооксигеназы Редуктазы Пероксидазы Диоксигеназы 2. Трансферазы Перенос функциональных групп с одного субстрата на другой С 1 -трансферазы Аминотрансферазы Гликозилтрансферазы Фосфотрансферазы 3. Гидролазы Перенос групп, акцептор – вода Эстеразы Гликозидазы 4. Лиазы «синтазы» Расщепление (образование) соединений по двойной связи С-С- лиазы С-О- лиазы 5. Изомеразы Перемещение групп в пределах молекулы Эпимеразы Цис-транс-изомеразы Внутримолекулярные трансферазы 6. Лигазы «синтетазы» Катализ энергозависимых реакций присоединения Образование С-С-связей, С-N-связей С-S-связей, С-О-связей Пептидазы Амидазы С-N-лиазы
Классификация ферментов Класс Тип реакции 1. Оксидоредуктазы Окислительновосстановительные Важнейшие подклассы Дегидрогеназы Оксидазы Монооксигеназы Редуктазы Пероксидазы Диоксигеназы 2. Трансферазы Перенос функциональных групп с одного субстрата на другой С 1 -трансферазы Аминотрансферазы Гликозилтрансферазы Фосфотрансферазы 3. Гидролазы Перенос групп, акцептор – вода Эстеразы Гликозидазы 4. Лиазы «синтазы» Расщепление (образование) соединений по двойной связи С-С- лиазы С-О- лиазы 5. Изомеразы Перемещение групп в пределах молекулы Эпимеразы Цис-транс-изомеразы Внутримолекулярные трансферазы 6. Лигазы «синтетазы» Катализ энергозависимых реакций присоединения Образование С-С-связей, С-N-связей С-S-связей, С-О-связей Пептидазы Амидазы С-N-лиазы
 Номенклатура ферментов (Класификация ферментов, 1992) КФ. 1. 1. (Класс, подкласс, подподкласс, номер фермента) Алкоголь: НАД-оксидоредуктаза (алкогольдегидрогеназа) Этанол+НАД → Ацетальдегид +НАД Н 2 КФ. 2. 7. 1. 1. АТФ: D-гексоза-6 -фосфотрансфераза (гексокиназа) АТФ+D-гексоза → АДФ+D-гексозо-6 -фосфат
Номенклатура ферментов (Класификация ферментов, 1992) КФ. 1. 1. (Класс, подкласс, подподкласс, номер фермента) Алкоголь: НАД-оксидоредуктаза (алкогольдегидрогеназа) Этанол+НАД → Ацетальдегид +НАД Н 2 КФ. 2. 7. 1. 1. АТФ: D-гексоза-6 -фосфотрансфераза (гексокиназа) АТФ+D-гексоза → АДФ+D-гексозо-6 -фосфат
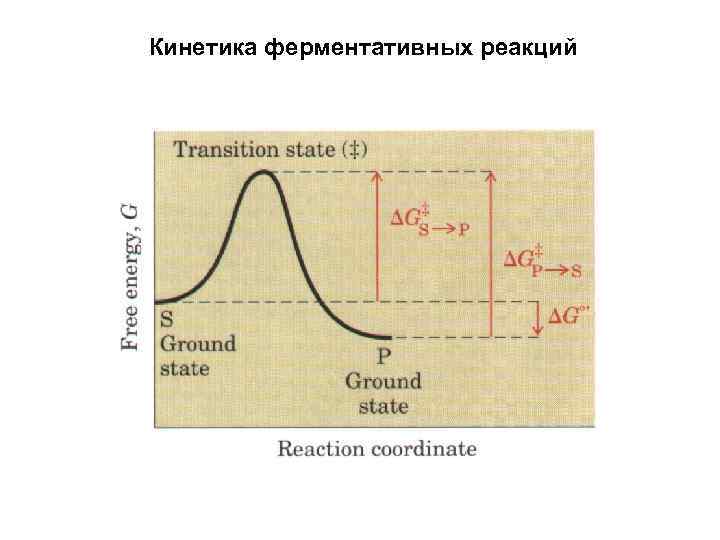 Кинетика ферментативных реакций
Кинетика ферментативных реакций
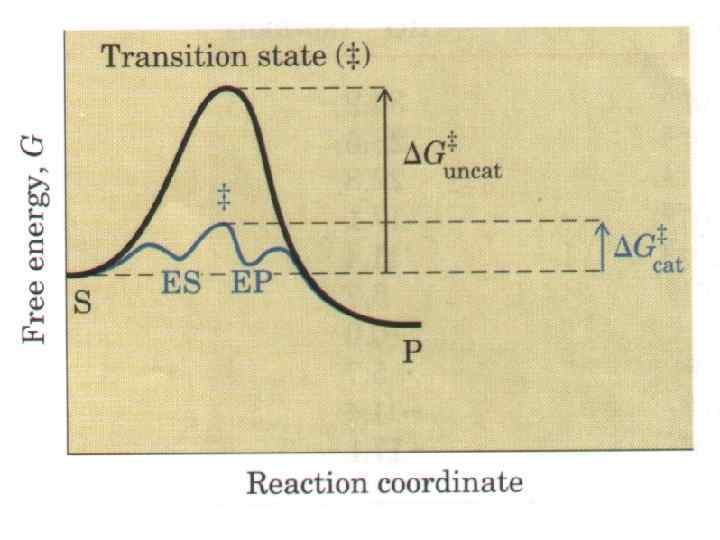
 Общее уравнение ферментативной реакции
Общее уравнение ферментативной реакции
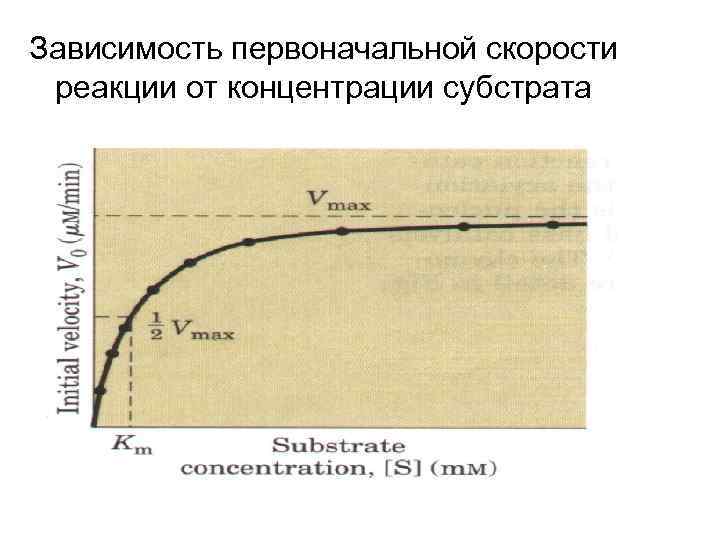 Зависимость первоначальной скорости реакции от концентрации субстрата
Зависимость первоначальной скорости реакции от концентрации субстрата
 Уравнение Михаэлиса-Ментен
Уравнение Михаэлиса-Ментен
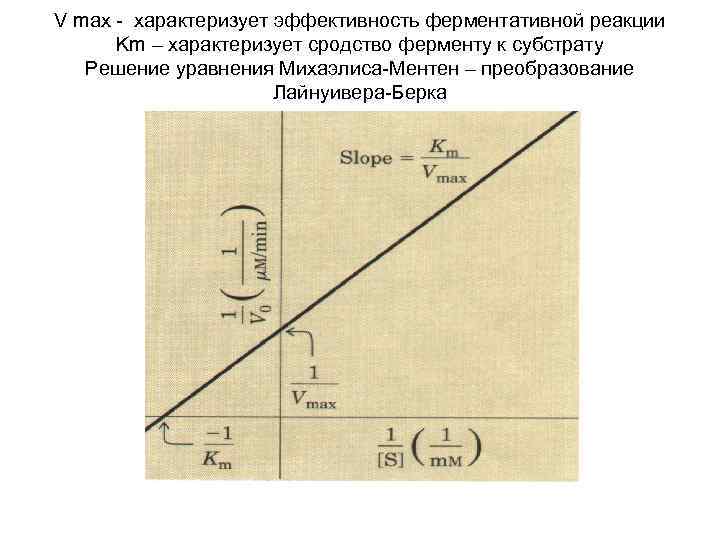 V max - характеризует эффективность ферментативной реакции Km – характеризует сродство ферменту к субстрату Решение уравнения Михаэлиса-Ментен – преобразование Лайнуивера-Берка
V max - характеризует эффективность ферментативной реакции Km – характеризует сродство ферменту к субстрату Решение уравнения Михаэлиса-Ментен – преобразование Лайнуивера-Берка
 Важные константы ферментативных реакций • V max - характеризует эффективность ферментативной реакции • Km – характеризует сродство ферменту к субстрату
Важные константы ферментативных реакций • V max - характеризует эффективность ферментативной реакции • Km – характеризует сродство ферменту к субстрату
 Специфичность 1. Абсолютная специфичность: уреаза CO(NH 2)2 CO(NH 2)(NHOH) CO(NHOH)2 cукцинатдегидрогеназа – допускает замену только одного атома Н в СН 2 -группе на атом Cl аспартаза: фумарат+NH 3 → L-аспартат 2. Групповая специфичность: оксидаза D-аминокислот химотрипсин, фосфатаза 3. Высокая специфичность: способность ферментов отбирать «легкие» изотопы Р, S, P Степень специфичности ферментов оценивают на основании их способности катализировать превращения аналогов главного субстрата Комплементарность молекулы субстрата и специфического участка на поверхности фермента – «ключ к замку»
Специфичность 1. Абсолютная специфичность: уреаза CO(NH 2)2 CO(NH 2)(NHOH) CO(NHOH)2 cукцинатдегидрогеназа – допускает замену только одного атома Н в СН 2 -группе на атом Cl аспартаза: фумарат+NH 3 → L-аспартат 2. Групповая специфичность: оксидаза D-аминокислот химотрипсин, фосфатаза 3. Высокая специфичность: способность ферментов отбирать «легкие» изотопы Р, S, P Степень специфичности ферментов оценивают на основании их способности катализировать превращения аналогов главного субстрата Комплементарность молекулы субстрата и специфического участка на поверхности фермента – «ключ к замку»
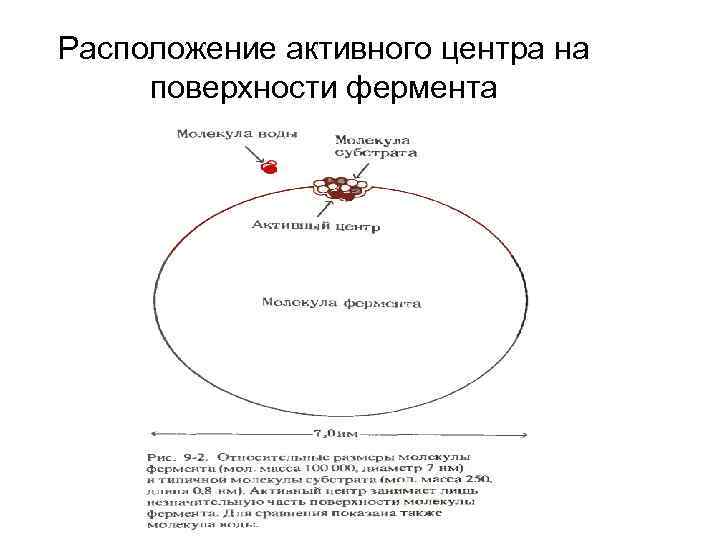 Расположение активного центра на поверхности фермента
Расположение активного центра на поверхности фермента
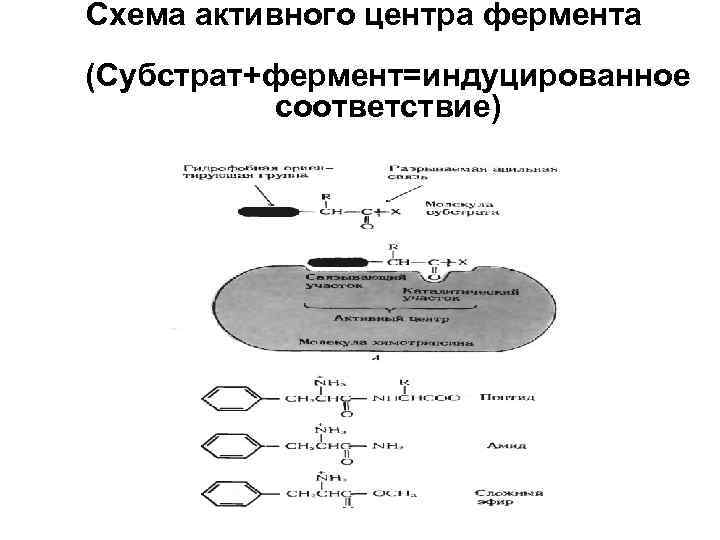 Схема активного центра фермента (Субстрат+фермент=индуцированное соответствие)
Схема активного центра фермента (Субстрат+фермент=индуцированное соответствие)
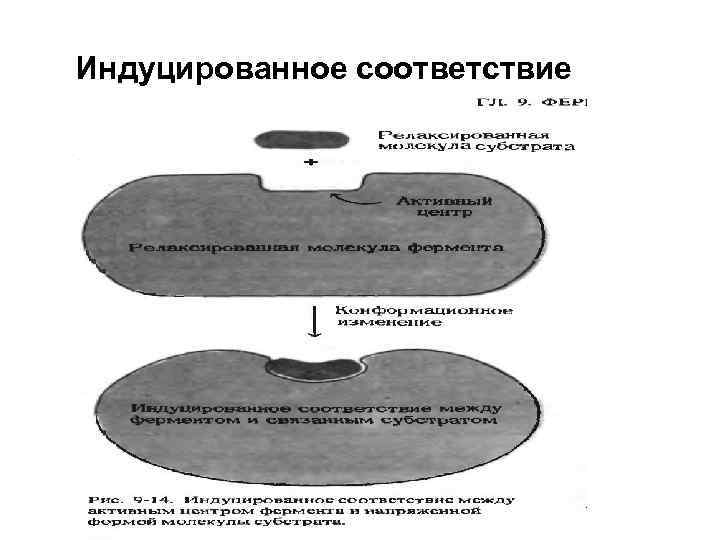 Индуцированное соответствие
Индуцированное соответствие
 Основные этапы каталитического акта: 1. Сближение и ориентация – переходное состояние 2. Напряжение и деформация – индуцированное соответствие 3. Общий кислотно-основной катализ 4. Ковалентный катализ
Основные этапы каталитического акта: 1. Сближение и ориентация – переходное состояние 2. Напряжение и деформация – индуцированное соответствие 3. Общий кислотно-основной катализ 4. Ковалентный катализ
 Соответствие субстрата и фермента Субстрат «подходит» к ферменту как ключ к замку
Соответствие субстрата и фермента Субстрат «подходит» к ферменту как ключ к замку
 Факторы внешней среды, влияющие на активность ферментов • • Доступность воды Доступность кислорода Влияние температуры Реакция среды (аргиназа – р. Н 1. 5; трипсин – р. Н 7. 7; каталаза – р. Н 7. 6) • Наличие кофакторов (металлов, коферментов, витамины) • Клеточные метаболиты – различные типы ингибирования: обратимое – аналоги субстрата, переходного состояния необратимое - «модифицирующий реагент» : связывание с ферментом или субстратом → тяжелые металлы Hg, Pb - «суицидный субстрат» → цианиды аллостерическое ингибирование – ингибирование цепи реакций конечным продуктом реакции
Факторы внешней среды, влияющие на активность ферментов • • Доступность воды Доступность кислорода Влияние температуры Реакция среды (аргиназа – р. Н 1. 5; трипсин – р. Н 7. 7; каталаза – р. Н 7. 6) • Наличие кофакторов (металлов, коферментов, витамины) • Клеточные метаболиты – различные типы ингибирования: обратимое – аналоги субстрата, переходного состояния необратимое - «модифицирующий реагент» : связывание с ферментом или субстратом → тяжелые металлы Hg, Pb - «суицидный субстрат» → цианиды аллостерическое ингибирование – ингибирование цепи реакций конечным продуктом реакции
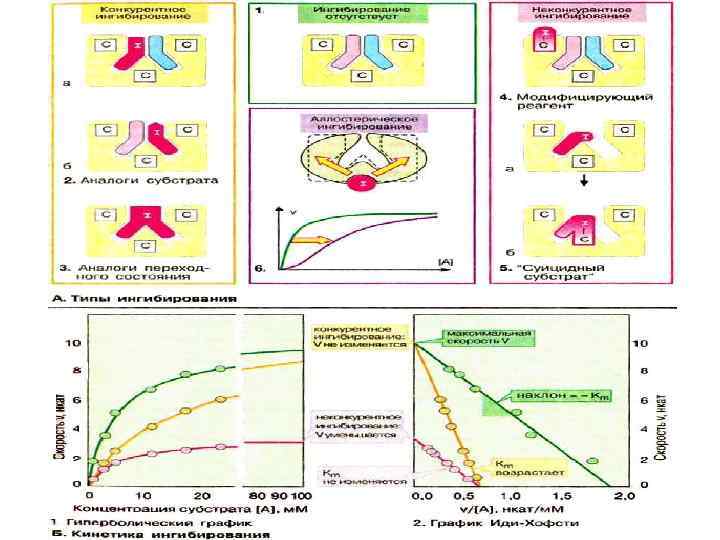
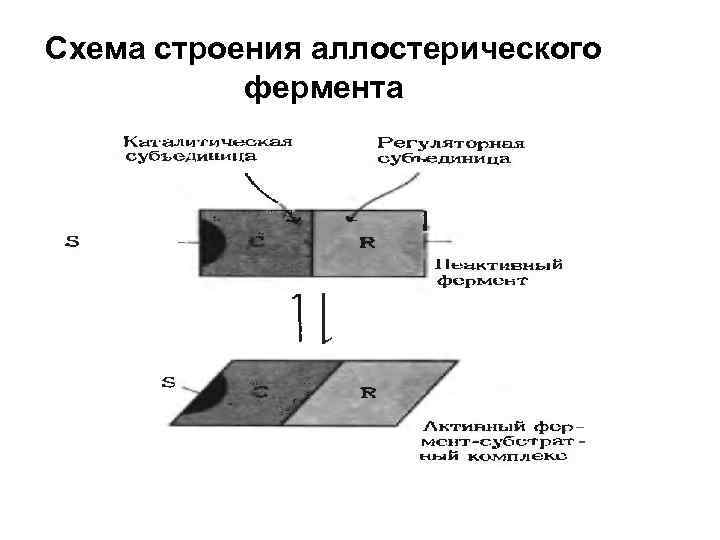 Схема строения аллостерического фермента
Схема строения аллостерического фермента
 Свойства аллостерических ферментов • Наличие помимо активного центра аллостерического (регуляторного) центра для связывания регуляторного метаболита (модулятора, эффектора) • Аллострические ферменты намного крупнее и более сложно устроены по сравнению с нерегуляторными • Кинетика реакций у аллостерических ферментов отклоняется от классического уравнения Михаэлиса. Ментен (не гипербола, а сигмоидная криавя)
Свойства аллостерических ферментов • Наличие помимо активного центра аллостерического (регуляторного) центра для связывания регуляторного метаболита (модулятора, эффектора) • Аллострические ферменты намного крупнее и более сложно устроены по сравнению с нерегуляторными • Кинетика реакций у аллостерических ферментов отклоняется от классического уравнения Михаэлиса. Ментен (не гипербола, а сигмоидная криавя)
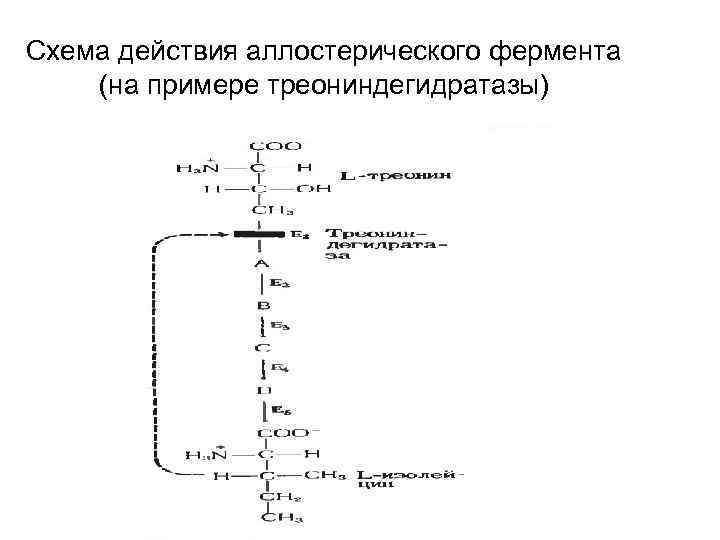 Схема действия аллостерического фермента (на примере треониндегидратазы)
Схема действия аллостерического фермента (на примере треониндегидратазы)


