ЛЕКЦИЯ 5 апоптоз и некроз.ppt
- Количество слайдов: 38
 ЛЕКЦИЯ 4 Апоптоз и некроз клетки Т. В. Метревели
ЛЕКЦИЯ 4 Апоптоз и некроз клетки Т. В. Метревели
 Содержание Введение Морфологические различия апоптоза и некроза Признаки апоптоза. Каспазы Реализация механизма апоптоза Програмируемая смерть клетки растении Т. В. Метревели
Содержание Введение Морфологические различия апоптоза и некроза Признаки апоптоза. Каспазы Реализация механизма апоптоза Програмируемая смерть клетки растении Т. В. Метревели
 Введение Некро з (от греч. Νεκρός — мёртвый) — это патологический процесс, выражающийся в местной гибели ткани в живом организме в результате какого-либо экзо- или эндогенного её повреждения. При некрозе клетка раздувается и лопается, выбрасывая своё содержимое (потенциально вредное) в межклеточное пространство. Наиболее частыми причинами некротического повреждения ткани являются: острый дефицит кислорода, воздействие токсинами бактерий или вирусов и др.
Введение Некро з (от греч. Νεκρός — мёртвый) — это патологический процесс, выражающийся в местной гибели ткани в живом организме в результате какого-либо экзо- или эндогенного её повреждения. При некрозе клетка раздувается и лопается, выбрасывая своё содержимое (потенциально вредное) в межклеточное пространство. Наиболее частыми причинами некротического повреждения ткани являются: острый дефицит кислорода, воздействие токсинами бактерий или вирусов и др.
 Апоптоз – запрограммированная смерть клетки. Механизмы апоптоза "запускаются" тогда, когда вредное воздействие недостаточно сильно, чтобы вызвать некроз. Форма клеточной гибели - по пути апоптоза или некроза - во многом определяется внутриклеточным содержанием NAD+ и ATP. Снижение уровня NADН и ATP ведет к индукции некроза. В нормальном организме апоптоз - механизм для поддержания гомеостаза. В отличие от некроза, при апоптозе клетка сжимается и часто делится на части. В результате остатки клетки могут быть поглощены (путём фагоцитоза) соседними клетками или макрофагами.
Апоптоз – запрограммированная смерть клетки. Механизмы апоптоза "запускаются" тогда, когда вредное воздействие недостаточно сильно, чтобы вызвать некроз. Форма клеточной гибели - по пути апоптоза или некроза - во многом определяется внутриклеточным содержанием NAD+ и ATP. Снижение уровня NADН и ATP ведет к индукции некроза. В нормальном организме апоптоз - механизм для поддержания гомеостаза. В отличие от некроза, при апоптозе клетка сжимается и часто делится на части. В результате остатки клетки могут быть поглощены (путём фагоцитоза) соседними клетками или макрофагами.
 Апоптоз играет важную роль в развитии эмбрионов и морфогенезе животных и растений. Так, например, 1) разделение пальцев у эмбриона требует, чтобы клетки, находящиеся между пальцами, погибли. Апоптоз во время нормального развития конечности мыши.
Апоптоз играет важную роль в развитии эмбрионов и морфогенезе животных и растений. Так, например, 1) разделение пальцев у эмбриона требует, чтобы клетки, находящиеся между пальцами, погибли. Апоптоз во время нормального развития конечности мыши.
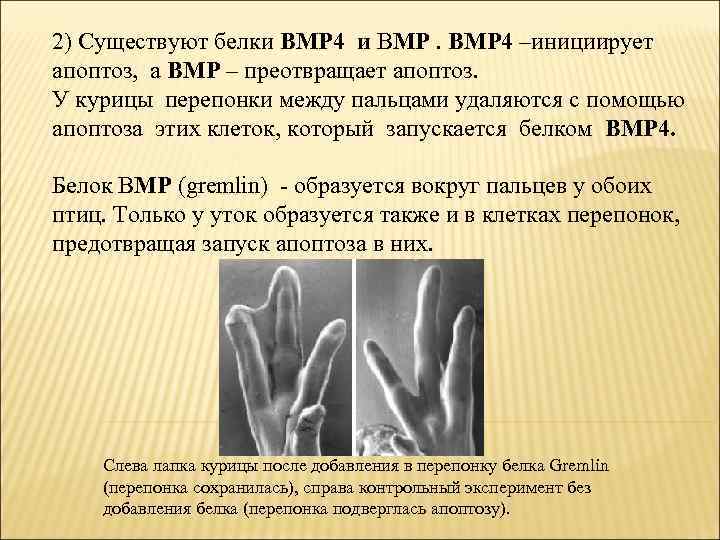 2) Существуют белки BMP 4 и BMP 4 –инициирует апоптоз, а ВМР – преотвращает апоптоз. У курицы перепонки между пальцами удаляются с помощью апоптоза этих клеток, который запускается белком BMP 4. Белок BMP (gremlin) - образуется вокруг пальцев у обоих птиц. Только у уток образуется также и в клетках перепонок, предотвращая запуск апоптоза в них. Слева лапка курицы после добавления в перепонку белка Gremlin (перепонка сохранилась), справа контрольный эксперимент без добавления белка (перепонка подверглась апоптозу).
2) Существуют белки BMP 4 и BMP 4 –инициирует апоптоз, а ВМР – преотвращает апоптоз. У курицы перепонки между пальцами удаляются с помощью апоптоза этих клеток, который запускается белком BMP 4. Белок BMP (gremlin) - образуется вокруг пальцев у обоих птиц. Только у уток образуется также и в клетках перепонок, предотвращая запуск апоптоза в них. Слева лапка курицы после добавления в перепонку белка Gremlin (перепонка сохранилась), справа контрольный эксперимент без добавления белка (перепонка подверглась апоптозу).
 3) метаморфоз головастика лягушки. Под воздействием тиреоидного гормона при метаморфозе головастика лягушки, запускается апоптоз и хвост головастика исчезает.
3) метаморфоз головастика лягушки. Под воздействием тиреоидного гормона при метаморфозе головастика лягушки, запускается апоптоз и хвост головастика исчезает.
 Морфологические различия апоптоза и некроза Эти различия сводятся к следующему (см. рис. 1): 1. Митохондрии при некрозе набухают и разрушаются, при апоптозе большинство митохондрий мало изменено по сравнению с нормой. 2. Ядра при некрозе мало изменены, при апоптозе они сначала сжимаются (конденсируются), а потом фрагментируются. 3. Клетка при некрозе набухает, а затем может произойти разрыв цитопрлазматической мембраны. 4. при апоптозе клетка сжимается, на ее поверхности образуются «бородавки» (blebbing), а на поздних стадиях клетка фрагментируется.
Морфологические различия апоптоза и некроза Эти различия сводятся к следующему (см. рис. 1): 1. Митохондрии при некрозе набухают и разрушаются, при апоптозе большинство митохондрий мало изменено по сравнению с нормой. 2. Ядра при некрозе мало изменены, при апоптозе они сначала сжимаются (конденсируются), а потом фрагментируются. 3. Клетка при некрозе набухает, а затем может произойти разрыв цитопрлазматической мембраны. 4. при апоптозе клетка сжимается, на ее поверхности образуются «бородавки» (blebbing), а на поздних стадиях клетка фрагментируется.
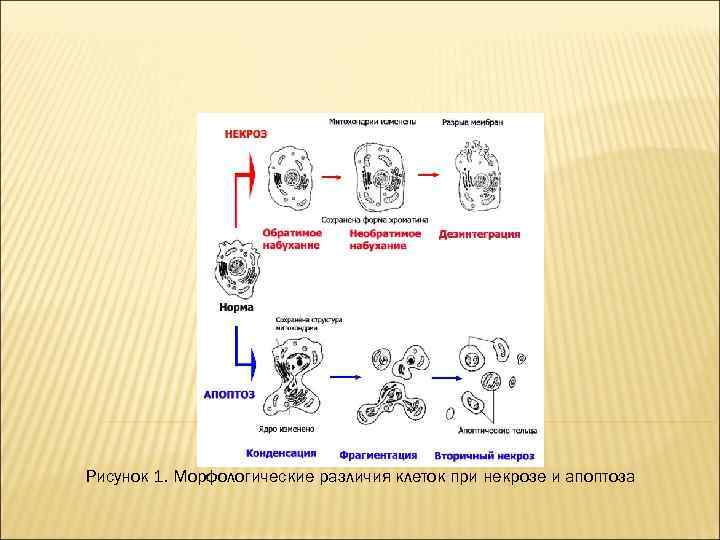 Рисунок 1. Морфологические различия клеток при некрозе и апоптоза
Рисунок 1. Морфологические различия клеток при некрозе и апоптоза
 Признаки апоптоза. Каспазы. Непосредственной причиной апоптоза служит: активация гидролитических ферментов, в основном протеиназ и эндонуклеаз, инактивация репарирующих ферментативных систем. появление на поверхности клеток фосфатидилсерина, который в норме находится на внутренней поверхности липидного бислоя цитоплазматической мембраны. Все эти изменения используются для обнаружения апоптоза. Наиболее характерным признаком апоптоза служит также появление в клетке специфических протеиназ – каспаз (cysteinyl aspartate-specific proteases).
Признаки апоптоза. Каспазы. Непосредственной причиной апоптоза служит: активация гидролитических ферментов, в основном протеиназ и эндонуклеаз, инактивация репарирующих ферментативных систем. появление на поверхности клеток фосфатидилсерина, который в норме находится на внутренней поверхности липидного бислоя цитоплазматической мембраны. Все эти изменения используются для обнаружения апоптоза. Наиболее характерным признаком апоптоза служит также появление в клетке специфических протеиназ – каспаз (cysteinyl aspartate-specific proteases).
 Каспазы - цистеиновые протеиназы, синтезируемые из про-энзимов в результате протеолиза последних. Известно 14 каспаз: Каспаза-1; альтернативное название: ICE; Каспаза-2; альтернативное название: ICH-1. Каспаза-3; альтернативное название: CPP 32, Каспаза-4; альтернативное название: ICErel-II, TX, ICH-2. Каспаза-5; альтернативное название: ICErel-III, TY. Каспаза-6; альтернативное название: Mch 2; Каспаза-7; альтернативное название: Mch 3, ICE-LAPS, CMH-1. Каспаза-8; альтернативное название: FLICE, MACH, Mch 5. Каспаза-9; альтернативное название: ICE-LAP 6, Mch 6. Каспаза-10; альтернативное название: Mch 4.
Каспазы - цистеиновые протеиназы, синтезируемые из про-энзимов в результате протеолиза последних. Известно 14 каспаз: Каспаза-1; альтернативное название: ICE; Каспаза-2; альтернативное название: ICH-1. Каспаза-3; альтернативное название: CPP 32, Каспаза-4; альтернативное название: ICErel-II, TX, ICH-2. Каспаза-5; альтернативное название: ICErel-III, TY. Каспаза-6; альтернативное название: Mch 2; Каспаза-7; альтернативное название: Mch 3, ICE-LAPS, CMH-1. Каспаза-8; альтернативное название: FLICE, MACH, Mch 5. Каспаза-9; альтернативное название: ICE-LAP 6, Mch 6. Каспаза-10; альтернативное название: Mch 4.
 Каспазы подразделяются на: инициаторы, эффекторы и стимуляторы. Инициаторы (каспаза-8 и -9) расщепляют и активируют каспазы эффекторы (каспаза-3). Эффекторы расщепляют различные белки, что ведет к гибели клетки. Инициаторные каспазы активируются автоактивацией, которая происходит при взаимодействии нескольких прокаспаз (например, прокаспаза-8 и DISC).
Каспазы подразделяются на: инициаторы, эффекторы и стимуляторы. Инициаторы (каспаза-8 и -9) расщепляют и активируют каспазы эффекторы (каспаза-3). Эффекторы расщепляют различные белки, что ведет к гибели клетки. Инициаторные каспазы активируются автоактивацией, которая происходит при взаимодействии нескольких прокаспаз (например, прокаспаза-8 и DISC).
 Каскад активации каспаз
Каскад активации каспаз
 Вещества, которые приводят к апоптозу клеток называют апоптогенами. К апоптогенам относят: Fas (антигенный домен на поверхности иммунных комплексов) TNF (фактор некроза опухоли) Церамиды Каспазы АКР Оксиданты кальций.
Вещества, которые приводят к апоптозу клеток называют апоптогенами. К апоптогенам относят: Fas (антигенный домен на поверхности иммунных комплексов) TNF (фактор некроза опухоли) Церамиды Каспазы АКР Оксиданты кальций.
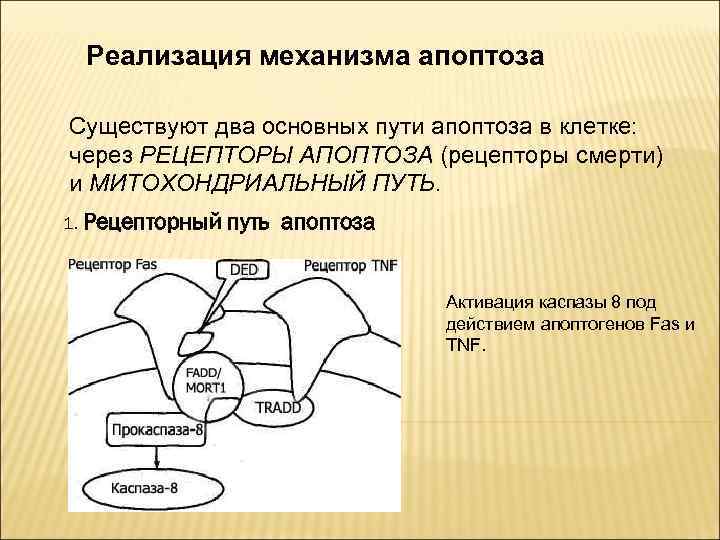 Реализация механизма апоптоза Существуют два основных пути апоптоза в клетке: через РЕЦЕПТОРЫ АПОПТОЗА (рецепторы смерти) и МИТОХОНДРИАЛЬНЫЙ ПУТЬ. 1. Рецепторный путь апоптоза Активация каспазы 8 под действием апоптогенов Fas и TNF.
Реализация механизма апоптоза Существуют два основных пути апоптоза в клетке: через РЕЦЕПТОРЫ АПОПТОЗА (рецепторы смерти) и МИТОХОНДРИАЛЬНЫЙ ПУТЬ. 1. Рецепторный путь апоптоза Активация каспазы 8 под действием апоптогенов Fas и TNF.
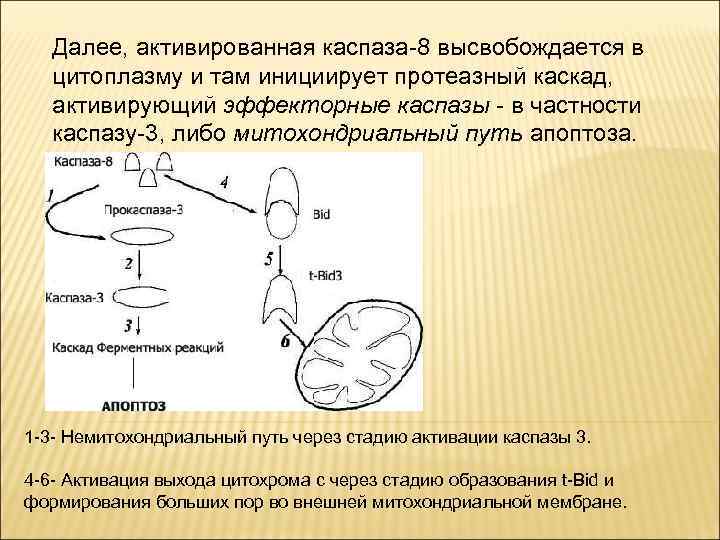 Далее, активированная каспаза-8 высвобождается в цитоплазму и там инициирует протеазный каскад, активирующий эффекторные каспазы - в частности каспазу-3, либо митохондриальный путь апоптоза. 1 -3 - Немитохондриальный путь через стадию активации каспазы 3. 4 -6 - Активация выхода цитохрома с через стадию образования t-Bid и формирования больших пор во внешней митохондриальной мембране.
Далее, активированная каспаза-8 высвобождается в цитоплазму и там инициирует протеазный каскад, активирующий эффекторные каспазы - в частности каспазу-3, либо митохондриальный путь апоптоза. 1 -3 - Немитохондриальный путь через стадию активации каспазы 3. 4 -6 - Активация выхода цитохрома с через стадию образования t-Bid и формирования больших пор во внешней митохондриальной мембране.
 Рецепторный путь апоптоза реализуется посредством специализированных рецепторов. Рецепторы апоптоза (или рецепторы смерти) – это суперсемейство трансмембранных белков, которые в цитоплазматическом домене содержат одинаковую аминокислотную последовательность из 80 аминокислот, которая обозначается как домен смерти DD (death domain). Рецепторы апоптоза: Fas - (известный как CD 95 или APO-1) TNFR — «рецептор фактора некроза опухолей» APO-3 (или CARI, DR 3 (англ. death receptor 3 — «рецептор смерти 3» ), DR 4 и DR 5. Помимо DD имеются также белковые домены DED и CARD.
Рецепторный путь апоптоза реализуется посредством специализированных рецепторов. Рецепторы апоптоза (или рецепторы смерти) – это суперсемейство трансмембранных белков, которые в цитоплазматическом домене содержат одинаковую аминокислотную последовательность из 80 аминокислот, которая обозначается как домен смерти DD (death domain). Рецепторы апоптоза: Fas - (известный как CD 95 или APO-1) TNFR — «рецептор фактора некроза опухолей» APO-3 (или CARI, DR 3 (англ. death receptor 3 — «рецептор смерти 3» ), DR 4 и DR 5. Помимо DD имеются также белковые домены DED и CARD.
 Внецитоплазматические домены содержат участки для присоединения лигандов. Путь передачи сигнала ПКС : индукторы + рецепторы + адаптеры + инициаторные каспазы + регуляторы + каспазы эфекторные. Пример - Fas –зависимый апоптоз играет решающую роль в регуляции иммунного ответа. Fas - (CD 95 или APO-1) экспрессируется в тканях : в тимусе, печени, сердце, почках. Лиганд Fas - Fas. L, преимущественно экспрессируется цитотоксическими Т-лимфоцитами (Т-киллерами) и натуральными киллерами (НК-клетками).
Внецитоплазматические домены содержат участки для присоединения лигандов. Путь передачи сигнала ПКС : индукторы + рецепторы + адаптеры + инициаторные каспазы + регуляторы + каспазы эфекторные. Пример - Fas –зависимый апоптоз играет решающую роль в регуляции иммунного ответа. Fas - (CD 95 или APO-1) экспрессируется в тканях : в тимусе, печени, сердце, почках. Лиганд Fas - Fas. L, преимущественно экспрессируется цитотоксическими Т-лимфоцитами (Т-киллерами) и натуральными киллерами (НК-клетками).
 Через механизм Fas-зависимого апоптоза цитотоксические Тлимфоциты: расправляются с клетками, инфицированными вирусами или бактериями, а натуральные киллеры – с опухолевыми клетками. вызывает гибель активированных Т-лимфоцитов – продуцентов цитокинов и В-лимфоцитов – продуцентов антител по окончании иммунного ответа, когда повержен инфекционный возбудитель, внедрившийся в организм. редотвращается распространение воспалительного процесса. Таким образом Fas –зависимый апоптоз регулируют гомеостаз (равновесие) лимфоцитов.
Через механизм Fas-зависимого апоптоза цитотоксические Тлимфоциты: расправляются с клетками, инфицированными вирусами или бактериями, а натуральные киллеры – с опухолевыми клетками. вызывает гибель активированных Т-лимфоцитов – продуцентов цитокинов и В-лимфоцитов – продуцентов антител по окончании иммунного ответа, когда повержен инфекционный возбудитель, внедрившийся в организм. редотвращается распространение воспалительного процесса. Таким образом Fas –зависимый апоптоз регулируют гомеостаз (равновесие) лимфоцитов.
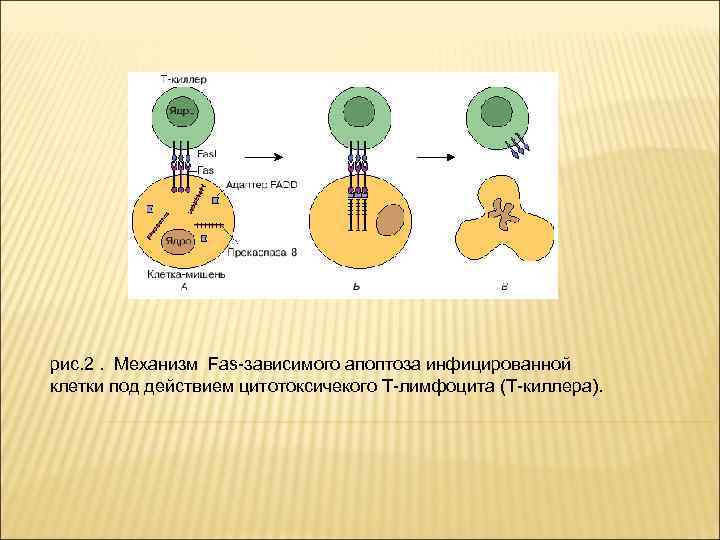 рис. 2. Механизм Fas-зависимого апоптоза инфицированной клетки под действием цитотоксичекого Т-лимфоцита (Т-киллера).
рис. 2. Механизм Fas-зависимого апоптоза инфицированной клетки под действием цитотоксичекого Т-лимфоцита (Т-киллера).
 (А) - В плазматической мембране Т-киллера молекулы Fas. L находятся в форме тримеров. (Б) - Тримеры Fas. L связываются с олекулами Fas-рецептора клеткимишени. Затем молекулы Fas связываютцитоплазматический адаптерный белок FADD ( Fas-associated death domain – связанный с Fas домен смерти). (В) - адаптер FADD содержит домен DED, который взаимодействует с DED-доменами продомена прокаспазы-8. Формируются таким образом сигнальные комплексы DISC (Death-inducing signaling complex), которые индуцируют смерть. Обычно прокаспаза-8 имеет очень низкую активность (1 -2% зрелой каспазы).
(А) - В плазматической мембране Т-киллера молекулы Fas. L находятся в форме тримеров. (Б) - Тримеры Fas. L связываются с олекулами Fas-рецептора клеткимишени. Затем молекулы Fas связываютцитоплазматический адаптерный белок FADD ( Fas-associated death domain – связанный с Fas домен смерти). (В) - адаптер FADD содержит домен DED, который взаимодействует с DED-доменами продомена прокаспазы-8. Формируются таким образом сигнальные комплексы DISC (Death-inducing signaling complex), которые индуцируют смерть. Обычно прокаспаза-8 имеет очень низкую активность (1 -2% зрелой каспазы).
 Прокаспаза-8 аутоактивируется в каспазу- 8 при повышении концентрации прокаспазы в DISC комплексе. Каспаза-8 в свою очередь активирует эффекторную каспазу-3. С этого момента процесс запущенный ПКС становится необратимым. Каспаза-3 активирует другие прокаспазы, активирует фрагментацию ДНК, к распаду ядра и образованию апоптозных везикул (по: Самуилов 2001)
Прокаспаза-8 аутоактивируется в каспазу- 8 при повышении концентрации прокаспазы в DISC комплексе. Каспаза-8 в свою очередь активирует эффекторную каспазу-3. С этого момента процесс запущенный ПКС становится необратимым. Каспаза-3 активирует другие прокаспазы, активирует фрагментацию ДНК, к распаду ядра и образованию апоптозных везикул (по: Самуилов 2001)
 2. Митохондриальный путь апоптоза. Под влиянием внешних сигналов, или рецепторов смерти происходит повышение проницаемости обеих мембран, снижение мембранного потенциала и высвобождение из межмембранного пространства специфических белков апоптоза. К итохондриальным белкам апоптоза относят: AIF (апоптоз-индуцирующего фактор) SMAC (second mitochondria-derived activator of caspases) Некоторые каспазы Цитохром с Высвобождение этих белков происходит вследствие открытия Са 2+зависимой так называемой митохондриальной поры. Открытие этой поры - ключевое событие в запуске реакций апоптоза и некроза животных клеток.
2. Митохондриальный путь апоптоза. Под влиянием внешних сигналов, или рецепторов смерти происходит повышение проницаемости обеих мембран, снижение мембранного потенциала и высвобождение из межмембранного пространства специфических белков апоптоза. К итохондриальным белкам апоптоза относят: AIF (апоптоз-индуцирующего фактор) SMAC (second mitochondria-derived activator of caspases) Некоторые каспазы Цитохром с Высвобождение этих белков происходит вследствие открытия Са 2+зависимой так называемой митохондриальной поры. Открытие этой поры - ключевое событие в запуске реакций апоптоза и некроза животных клеток.
 Факторы, вызывающие образование пор в митохондриальной мембране: истощение клеток восстановленным глутатионом, снижение концентрации NAD(P)H, ATP и ADP образование активных форм кислорода, разобщение окислительного фосфорелирования протонофорными соединениями, увеличение содержания Ca 2+ в цитоплазме. Образование пор в митохондриях можно вызвать церамиды, NO некоторые каспазы амфипатические пептиды жирные кислоты
Факторы, вызывающие образование пор в митохондриальной мембране: истощение клеток восстановленным глутатионом, снижение концентрации NAD(P)H, ATP и ADP образование активных форм кислорода, разобщение окислительного фосфорелирования протонофорными соединениями, увеличение содержания Ca 2+ в цитоплазме. Образование пор в митохондриях можно вызвать церамиды, NO некоторые каспазы амфипатические пептиды жирные кислоты
 Цитохром с как «вторичный мессенжер» апоптоза Цитохром С в присутствии кофакторов активирует каскад реакций, осуществляемых каспазами. Выход цитохрома С из митохондрий может происходить по двум причинам: из-за увеличения объема (распухание) матрикса митохондрий и разрыва наружной мембраны под действием давления со стороны внутренней мембраны открытием каналов во внешней мембране (без соответствующего распухания органелл).
Цитохром с как «вторичный мессенжер» апоптоза Цитохром С в присутствии кофакторов активирует каскад реакций, осуществляемых каспазами. Выход цитохрома С из митохондрий может происходить по двум причинам: из-за увеличения объема (распухание) матрикса митохондрий и разрыва наружной мембраны под действием давления со стороны внутренней мембраны открытием каналов во внешней мембране (без соответствующего распухания органелл).
 Причина распухания митохондрий - увеличение ионной проницаемости внутренней мембраны – гидролиз фосфолипидов эндогенной фосфолипазой A 2. – перекисное окисление липидов мембран под действием АКР
Причина распухания митохондрий - увеличение ионной проницаемости внутренней мембраны – гидролиз фосфолипидов эндогенной фосфолипазой A 2. – перекисное окисление липидов мембран под действием АКР
 Участие цитохрома С в апоптозе Цитохром c в цитоплазме клетки участвует в формировании апоптосомы вместе с белковым доменом Apaf-1(от англ. apoptosis protease activating factor-1 — «фактор активации протеаз апоптоза» ). В этом комплексе APAF-1 играет роль скелета, на котором происходит аутокаталитический процессинг каспазы-9 (рис. 3). Предполагается, что в результате зависимого от гидролиза d. ATP (или АТР) конформационного изменения APAF-1 приобретает способность связывать цитохром с. Связав цитохром с, APAF-1 претерпевает дальнейшее конформационное изменение, способствующее его олигомеризации и открывающее доступ CARD-домена APAF-1 для прокаспазы-9, которая тоже содержит CARD-домен. Так образуется конструкция, называемая тоже апоптосомой. В таком комплексе происходит автокатализ прокаспазы 9 с помледующим связыванием ее с прокаспазой 3, которая активируется каспазой 9.
Участие цитохрома С в апоптозе Цитохром c в цитоплазме клетки участвует в формировании апоптосомы вместе с белковым доменом Apaf-1(от англ. apoptosis protease activating factor-1 — «фактор активации протеаз апоптоза» ). В этом комплексе APAF-1 играет роль скелета, на котором происходит аутокаталитический процессинг каспазы-9 (рис. 3). Предполагается, что в результате зависимого от гидролиза d. ATP (или АТР) конформационного изменения APAF-1 приобретает способность связывать цитохром с. Связав цитохром с, APAF-1 претерпевает дальнейшее конформационное изменение, способствующее его олигомеризации и открывающее доступ CARD-домена APAF-1 для прокаспазы-9, которая тоже содержит CARD-домен. Так образуется конструкция, называемая тоже апоптосомой. В таком комплексе происходит автокатализ прокаспазы 9 с помледующим связыванием ее с прокаспазой 3, которая активируется каспазой 9.
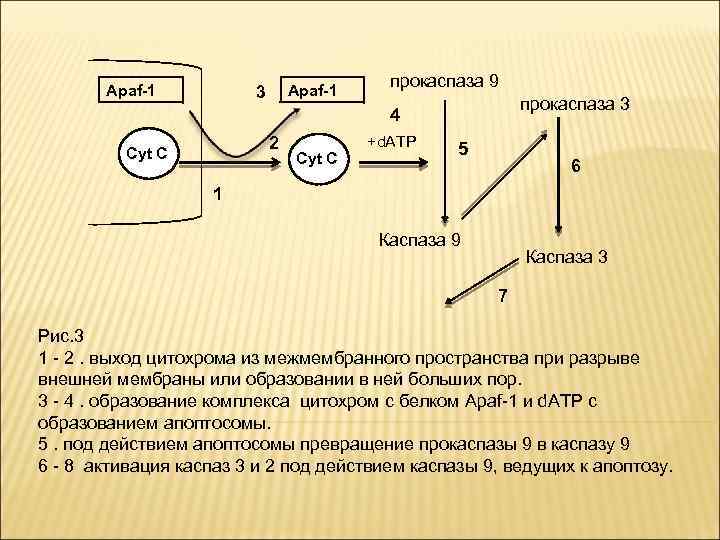 Apaf-1 3 прокаспаза 9 прокаспаза 3 4 2 Cyt С +d. ATP 5 6 1 Каспаза 9 Каспаза 3 7 Рис. 3 1 - 2. выход цитохрома из межмембранного пространства при разрыве внешней мембраны или образовании в ней больших пор. 3 - 4. образование комплекса цитохром с белком Apaf-1 и d. ATP с образованием апоптосомы. 5. под действием апоптосомы превращение прокаспазы 9 в каспазу 9 6 - 8 активация каспаз 3 и 2 под действием каспазы 9, ведущих к апоптозу.
Apaf-1 3 прокаспаза 9 прокаспаза 3 4 2 Cyt С +d. ATP 5 6 1 Каспаза 9 Каспаза 3 7 Рис. 3 1 - 2. выход цитохрома из межмембранного пространства при разрыве внешней мембраны или образовании в ней больших пор. 3 - 4. образование комплекса цитохром с белком Apaf-1 и d. ATP с образованием апоптосомы. 5. под действием апоптосомы превращение прокаспазы 9 в каспазу 9 6 - 8 активация каспаз 3 и 2 под действием каспазы 9, ведущих к апоптозу.
 Последствия высвобождения цитохрома C зависят от типа клеток В клетках, где цитохром C существует в избытке, его хватает и для активирования каспаз, и для поддержания электронного транспорта. В этом случае потребление кислорода и производство ATP может оставаться незатронутым, тогда как каспазы продолжают атаковать цитозольные и ядерные субстраты, что приводит к апоптозу
Последствия высвобождения цитохрома C зависят от типа клеток В клетках, где цитохром C существует в избытке, его хватает и для активирования каспаз, и для поддержания электронного транспорта. В этом случае потребление кислорода и производство ATP может оставаться незатронутым, тогда как каспазы продолжают атаковать цитозольные и ядерные субстраты, что приводит к апоптозу
 В клетках, которые содержат большие количества эндогенных каспазных ингибиторов, высвобождение цитохрома C может не индуцировать зависимый от каспаз апоптоз. Нарушается цепь переноса электронов. Развивается некроз.
В клетках, которые содержат большие количества эндогенных каспазных ингибиторов, высвобождение цитохрома C может не индуцировать зависимый от каспаз апоптоз. Нарушается цепь переноса электронов. Развивается некроз.
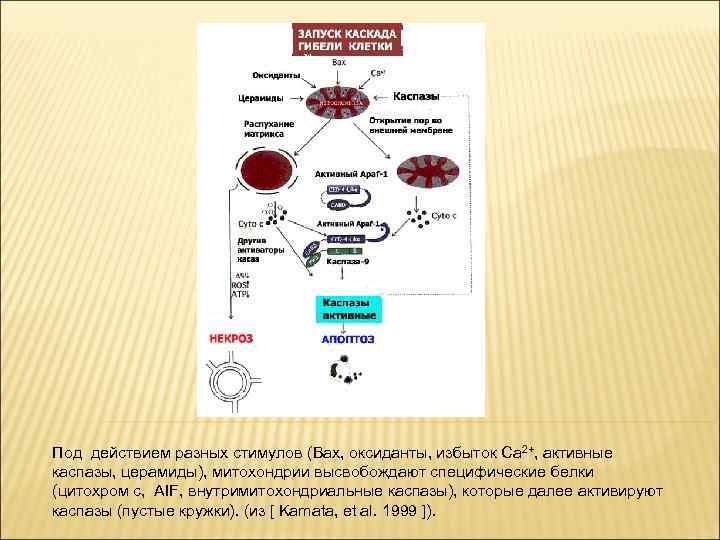 Под действием разных стимулов (Bax, оксиданты, избыток Ca 2+, активные каспазы, церамиды), митохондрии высвобождают специфические белки (цитохром c, AIF, внутримитохондриальные каспазы), которые далее активируют каспазы (пустые кружки). (из [ Kamata, et al. 1999 ]).
Под действием разных стимулов (Bax, оксиданты, избыток Ca 2+, активные каспазы, церамиды), митохондрии высвобождают специфические белки (цитохром c, AIF, внутримитохондриальные каспазы), которые далее активируют каспазы (пустые кружки). (из [ Kamata, et al. 1999 ]).
 Сокращения. DD - death domain ICE - interleicin converting enzime Белок Bcl-Х участвует в регуляции апоптоза. В результате альтернативного сплайсинга образуются две формы Bcl. X - Bcl-XL и Bcl-Xs. Первая из них останавливает апоптоз, тогда как вторая вместе с белком Вах вызывает гибель клетки.
Сокращения. DD - death domain ICE - interleicin converting enzime Белок Bcl-Х участвует в регуляции апоптоза. В результате альтернативного сплайсинга образуются две формы Bcl. X - Bcl-XL и Bcl-Xs. Первая из них останавливает апоптоз, тогда как вторая вместе с белком Вах вызывает гибель клетки.
 ПСК у растении Изменения в морфологии клеток растений, претерпевающих ПКС, сходны с таковыми при апоптозе у животных. Т. е. происходит: конденсация и дробление ядра на фрагменты, съеживание протопласта и складчатость цитоплазматической мембраны дробление протопласта на отдельные везикулы (аналогичные апоптозным тельцам животных клеток). разрушение апоптозных везикул под действием ферментов, секретируемых соседними клетками. (в отличие от везикул эукариотических клеток, которые поглощаются соседними, или специализированными клетками – макрофаги, лимфоциты и др. ) В результате, останки разрушенных клеток утилизируются другими клетками, что имеет место например, при отмирании листьев.
ПСК у растении Изменения в морфологии клеток растений, претерпевающих ПКС, сходны с таковыми при апоптозе у животных. Т. е. происходит: конденсация и дробление ядра на фрагменты, съеживание протопласта и складчатость цитоплазматической мембраны дробление протопласта на отдельные везикулы (аналогичные апоптозным тельцам животных клеток). разрушение апоптозных везикул под действием ферментов, секретируемых соседними клетками. (в отличие от везикул эукариотических клеток, которые поглощаются соседними, или специализированными клетками – макрофаги, лимфоциты и др. ) В результате, останки разрушенных клеток утилизируются другими клетками, что имеет место например, при отмирании листьев.
 С физиологической клеточной смертью в жизни растений связаны процессы формообразования в онтогенезе, иммунные реакции на внедрение патогена и др. Например: ксилогенез - разрушение отдельных клеток ксилемы для образование в них трахеидов флоэмогенез - развитие ситовидных трубок флоэмы формообразование листьев - у с. аронниковых разрушение отдельных клеток для образования в листьях места перфорации и лопастей на их ранней стадии развития аэренхимогенез - образование полостей, заполненных воздухом – как адаптивная реакция растений на дефицит кислорода, например, при затоплении опадание листьев и созревших плодов - избирательная гибель клеток отделительной зоны, расположенной между основанием черешка листа или плода и стеблем благодаря экспрессии sag-генов
С физиологической клеточной смертью в жизни растений связаны процессы формообразования в онтогенезе, иммунные реакции на внедрение патогена и др. Например: ксилогенез - разрушение отдельных клеток ксилемы для образование в них трахеидов флоэмогенез - развитие ситовидных трубок флоэмы формообразование листьев - у с. аронниковых разрушение отдельных клеток для образования в листьях места перфорации и лопастей на их ранней стадии развития аэренхимогенез - образование полостей, заполненных воздухом – как адаптивная реакция растений на дефицит кислорода, например, при затоплении опадание листьев и созревших плодов - избирательная гибель клеток отделительной зоны, расположенной между основанием черешка листа или плода и стеблем благодаря экспрессии sag-генов
 прорастание пыльцевой трубки - зависит от видовой принадлежности пыльцы и не включается при действии чужеродной пыльцы. разрушение алейроновых клеток после прорастания семян. (В процессе прорастании семян эти клетки нужны, т. к. они секретируют ферменты, катализирующие гидролиз запасных полимеров эндосперма и обеспечивающие тем самым питание проростка. Процесс гибели этих клеток похож на апоптоз клеток млекопитающих. Под действием гиббереловой кислоты активизируются нуклеазы, расщепляющие ядерную ДНК этих клеток на олигонуклеосомальные фрагменты. Под действием абсцизовой кислоты процесс блокируется. Таким образом, в расщеплении ДНК алейроновых клеток принимают участие нуклеазы, активность которых регулируется гиббереловой и абсцизовой кислотой.
прорастание пыльцевой трубки - зависит от видовой принадлежности пыльцы и не включается при действии чужеродной пыльцы. разрушение алейроновых клеток после прорастания семян. (В процессе прорастании семян эти клетки нужны, т. к. они секретируют ферменты, катализирующие гидролиз запасных полимеров эндосперма и обеспечивающие тем самым питание проростка. Процесс гибели этих клеток похож на апоптоз клеток млекопитающих. Под действием гиббереловой кислоты активизируются нуклеазы, расщепляющие ядерную ДНК этих клеток на олигонуклеосомальные фрагменты. Под действием абсцизовой кислоты процесс блокируется. Таким образом, в расщеплении ДНК алейроновых клеток принимают участие нуклеазы, активность которых регулируется гиббереловой и абсцизовой кислотой.
 иммунная реакция на патоген - включение механизма защиты от патогенов (вирусов, бактерий, грибов и нематод) у растении: индукция фитоалексинов (растительных антибиотиков) активизирование в инфицированных клетках и клетках, локализованных вблизи очага инфекции процесса ГО (гиперчувствительный ответ). в процессе ГО происходит сжатие протопласта и отделение его от клеточной стенки. в здоровых клетках окружающих зараженную клетку активизируется меристематическая активность, которая приводит к образованию перидермы - так называемая демаркационная ткань, оттораживающая очаг инфекции. происходит разрыв плазмодесм – мембранных мостиков между соседними клетками. Образуется зона мертвых обезвоженных клеток, которая служит барьером для дальнейшего распространения патогена.
иммунная реакция на патоген - включение механизма защиты от патогенов (вирусов, бактерий, грибов и нематод) у растении: индукция фитоалексинов (растительных антибиотиков) активизирование в инфицированных клетках и клетках, локализованных вблизи очага инфекции процесса ГО (гиперчувствительный ответ). в процессе ГО происходит сжатие протопласта и отделение его от клеточной стенки. в здоровых клетках окружающих зараженную клетку активизируется меристематическая активность, которая приводит к образованию перидермы - так называемая демаркационная ткань, оттораживающая очаг инфекции. происходит разрыв плазмодесм – мембранных мостиков между соседними клетками. Образуется зона мертвых обезвоженных клеток, которая служит барьером для дальнейшего распространения патогена.
 при индукция ГО на одном или нескольких листьях растения развитие иммунитета в других листьях растении, которые не имели контакта с патогеном называется системной приобретенной устойчивостью. Клеточная стенка может подвергаться укреплению или разрушению. Укрепление клеточной стенки происходит благодаря: q сшивке белков, q образованию целлюлозных утолщений q лигнификации. Укрепление клеточной стенки затрудняет проникновение патогена в клетку или, напротив, способствует замуровыванию уже проникшего микроба внутри клетки.
при индукция ГО на одном или нескольких листьях растения развитие иммунитета в других листьях растении, которые не имели контакта с патогеном называется системной приобретенной устойчивостью. Клеточная стенка может подвергаться укреплению или разрушению. Укрепление клеточной стенки происходит благодаря: q сшивке белков, q образованию целлюлозных утолщений q лигнификации. Укрепление клеточной стенки затрудняет проникновение патогена в клетку или, напротив, способствует замуровыванию уже проникшего микроба внутри клетки.
 разрушение клеточной стенки при участии активирующихся гидролитических ферментов. Тотальное разрушение клеточных стенок происходит при аэренхимогенезе. У растений, как и у животных, наряду с апоптозом, существует некроз. Так, Н 2 О 2 в малых концентрациях – индуктор апоптоза, в высоких концентрациях вызывает быструю гибель клеток, без каких-либо морфологических изменений, характерных для апоптоза.
разрушение клеточной стенки при участии активирующихся гидролитических ферментов. Тотальное разрушение клеточных стенок происходит при аэренхимогенезе. У растений, как и у животных, наряду с апоптозом, существует некроз. Так, Н 2 О 2 в малых концентрациях – индуктор апоптоза, в высоких концентрациях вызывает быструю гибель клеток, без каких-либо морфологических изменений, характерных для апоптоза.


