Химия атмосферы лекция 3 4.pptx
- Количество слайдов: 23
 Лекция № 3 Химия атмосферы Химические процессы в тропосфере
Лекция № 3 Химия атмосферы Химические процессы в тропосфере
 Свободные радикалы в тропосфере Гидроксидный радикал (OH): - при химических превращениях с участием синглетно возбужденного атома кислорода O(1 D), молекул воды, метана, водорода: O 2+ hv → O(1 D) + O(3 P), λ < 175 нм; O 3+ hv → О 2 + O(1 D), λ < 310 нм; N 2 O + hv → N 2 + O(1 D), λ < 240 нм; NO 2 + hv →NO + O(1 D), λ < 244 нм. O(1 D) + H 2 O → 2 OH; O(1 D) + CH 4 →CH 3 + OH; O(1 D) + H 2 → H + OH.
Свободные радикалы в тропосфере Гидроксидный радикал (OH): - при химических превращениях с участием синглетно возбужденного атома кислорода O(1 D), молекул воды, метана, водорода: O 2+ hv → O(1 D) + O(3 P), λ < 175 нм; O 3+ hv → О 2 + O(1 D), λ < 310 нм; N 2 O + hv → N 2 + O(1 D), λ < 240 нм; NO 2 + hv →NO + O(1 D), λ < 244 нм. O(1 D) + H 2 O → 2 OH; O(1 D) + CH 4 →CH 3 + OH; O(1 D) + H 2 → H + OH.
 Свободные радикалы в тропосфере - при протекании других реакций: HNO 2 → NO + OH, λ < 340 нм; HNO 3 → NO 2 + OH, λ < 335 нм; H 2 O 2 → 2 OH, λ < 300 нм.
Свободные радикалы в тропосфере - при протекании других реакций: HNO 2 → NO + OH, λ < 340 нм; HNO 3 → NO 2 + OH, λ < 335 нм; H 2 O 2 → 2 OH, λ < 300 нм.
 Свободные радикалы в тропосфере ОН-радикал взаимодействует с оксидом углерода, метаном и оксидом азота: CO + OH → CO 2 + H; CH 4 + OH → CH 3 + H 2 O; NO + OH + M → HNO 2 + M*.
Свободные радикалы в тропосфере ОН-радикал взаимодействует с оксидом углерода, метаном и оксидом азота: CO + OH → CO 2 + H; CH 4 + OH → CH 3 + H 2 O; NO + OH + M → HNO 2 + M*.
 Свободные радикалы в тропосфере Образующийся водород может реагировать с кислородом с образованием гидропероксидного радикала (HO 2) : H + O 2 → HO 2 - радикал образуется также взаимодействии О 3 или Н 2 О 2 с ОН-радикалом: O 3 + OH → HO 2 + O 2; H 2 O 2 + OH → HO 2 + H 2 O
Свободные радикалы в тропосфере Образующийся водород может реагировать с кислородом с образованием гидропероксидного радикала (HO 2) : H + O 2 → HO 2 - радикал образуется также взаимодействии О 3 или Н 2 О 2 с ОН-радикалом: O 3 + OH → HO 2 + O 2; H 2 O 2 + OH → HO 2 + H 2 O
 Свободные радикалы в тропосфере В результате реакции HO 2 - радикала с оксидом азота или озоном получаем OH - радикал: HO 2 + NO → NO 2 + OH; HO 2 + O 3 → 2 O 2 + OH. HO 2 - радикал может замкнуть цепочку превращений с участием свободных радикалов: HO 2 + HO 2 → H 2 O 2 + O 2.
Свободные радикалы в тропосфере В результате реакции HO 2 - радикала с оксидом азота или озоном получаем OH - радикал: HO 2 + NO → NO 2 + OH; HO 2 + O 3 → 2 O 2 + OH. HO 2 - радикал может замкнуть цепочку превращений с участием свободных радикалов: HO 2 + HO 2 → H 2 O 2 + O 2.
 Парниковый эффект Парниковые газы: - водяной пар; - углекислый газ; - метан; - фтор- и хлорсодержащие углеводороды; - монооксид азота
Парниковый эффект Парниковые газы: - водяной пар; - углекислый газ; - метан; - фтор- и хлорсодержащие углеводороды; - монооксид азота
 Превращения метана в атмосфере OH· + CH 4 → CH 3· + H 2 O CH 3· + O 2 → CH 3 O 2·+ NO → CH 3 O· +NO 2 CH 3 O·+ O 2 → CH 2 O + HO 2·+ NO → OH· + NO 2 2[NO 2 + hν = NO + O] 2[O + O 2 = O 3] CH 4 + 4 O 2 = CH 2 O + 2 O 3
Превращения метана в атмосфере OH· + CH 4 → CH 3· + H 2 O CH 3· + O 2 → CH 3 O 2·+ NO → CH 3 O· +NO 2 CH 3 O·+ O 2 → CH 2 O + HO 2·+ NO → OH· + NO 2 2[NO 2 + hν = NO + O] 2[O + O 2 = O 3] CH 4 + 4 O 2 = CH 2 O + 2 O 3
 Превращения метана в атмосфере CH 2 O + hν → H 2 + CO· (1) CH 2 O + hν → H· + HCO· (2) CH 2 O + OH· → HCO· + H 2 O (3) (2) CH 2 O + hν → H· + HCO· H· + O 2 → HO 2· HCO· + O 2 → CO + HO 2· 2 [HO 2· + NO → HO· + NO 2] 2[NO 2 + hν → NO· + O·] 2 [O 2 + O· → O 3] CH 2 O + 4 O 2 + hν → CO·+ 2 O 3 + 2 OH·
Превращения метана в атмосфере CH 2 O + hν → H 2 + CO· (1) CH 2 O + hν → H· + HCO· (2) CH 2 O + OH· → HCO· + H 2 O (3) (2) CH 2 O + hν → H· + HCO· H· + O 2 → HO 2· HCO· + O 2 → CO + HO 2· 2 [HO 2· + NO → HO· + NO 2] 2[NO 2 + hν → NO· + O·] 2 [O 2 + O· → O 3] CH 2 O + 4 O 2 + hν → CO·+ 2 O 3 + 2 OH·
 Превращения метана в атмосфере (3) CH 2 O + OH· → HCO· + H 2 O HCO· + O 2 → CO + HO 2· 2[HO 2· + NO → HO· + NO 2] 2[NO 2 + hν → NO + O·] 2[O 2 + O· → O 3] CH 2 O + 2 O 2 + hν → CO·+ O 3 + H 2 O
Превращения метана в атмосфере (3) CH 2 O + OH· → HCO· + H 2 O HCO· + O 2 → CO + HO 2· 2[HO 2· + NO → HO· + NO 2] 2[NO 2 + hν → NO + O·] 2[O 2 + O· → O 3] CH 2 O + 2 O 2 + hν → CO·+ O 3 + H 2 O
 Превращения метана в атмосфере CO + HO· → CO 2 + H· H·+ O 2 → HO 2· 2[HO 2·+ NO → HO· + NO 2] 2[NO 2 + hν → NO + O·] O 2 + O· → O 3 CO + 2 O 3 + hν → CO 2 + O 3
Превращения метана в атмосфере CO + HO· → CO 2 + H· H·+ O 2 → HO 2· 2[HO 2·+ NO → HO· + NO 2] 2[NO 2 + hν → NO + O·] O 2 + O· → O 3 CO + 2 O 3 + hν → CO 2 + O 3
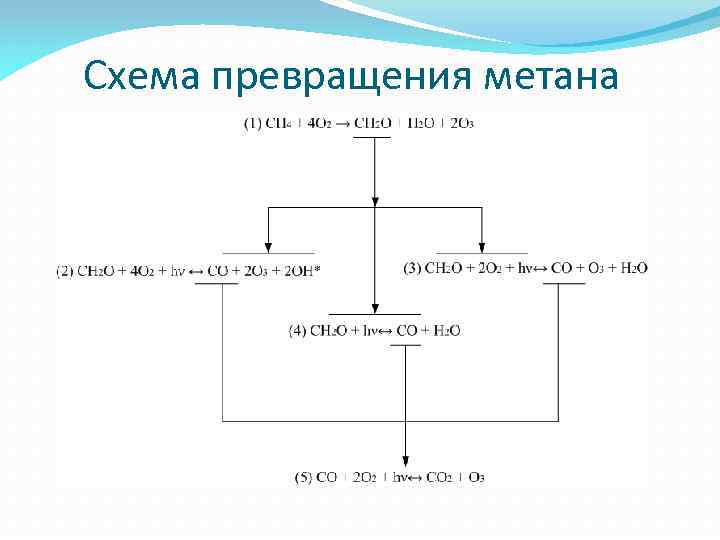 Схема превращения метана
Схема превращения метана
 Соединения серы в тропосфере Трансформация соединений серы Сероводород H 2 S + OH → H 2 O + HS HS + O 2 → SO + OH SO + HO 2 → SO 2 + OH Диоксид серы SO 2 Окисление диоксида серы Øв газовой фазе , Øв твердой фазе (окислению предшествует адсорбция) Øжидкой фазе (окислению предшествует абсорбция)
Соединения серы в тропосфере Трансформация соединений серы Сероводород H 2 S + OH → H 2 O + HS HS + O 2 → SO + OH SO + HO 2 → SO 2 + OH Диоксид серы SO 2 Окисление диоксида серы Øв газовой фазе , Øв твердой фазе (окислению предшествует адсорбция) Øжидкой фазе (окислению предшествует абсорбция)
 При газообразном окислении основную роль играют свободные радикалы SO 2 + OH + M → HSO 3 +M● HSO 3 +HO 2→ SO 3 +2 OH SO 2+HO 2→ SO 3+OH SO 2 + CH 3 O 2→SO 3+CH 2 O Окисление диоксида серы в твердой фазе – на поверхности твердых частиц SO 2 + Ca. O → Ca. SO 3 SO 2 + Mg. O → Mg. SO 3
При газообразном окислении основную роль играют свободные радикалы SO 2 + OH + M → HSO 3 +M● HSO 3 +HO 2→ SO 3 +2 OH SO 2+HO 2→ SO 3+OH SO 2 + CH 3 O 2→SO 3+CH 2 O Окисление диоксида серы в твердой фазе – на поверхности твердых частиц SO 2 + Ca. O → Ca. SO 3 SO 2 + Mg. O → Mg. SO 3
 Механизм образования кислотных дождей Механизм I: HO· + SO 2 → HSO 3· + O 2 → SO 3 + HO·2 SO 3 + H 2 O → H 2 SO 4 Механизм II: HSO 3 - + H 2 O 2 + H 3 O+ → H 2 SO 4 + H 2 O HSO 3 - + O 3 + H 3 O+ → H 2 SO 4 + H 2 O + O 2 HSO 3 - + 2 Fe. O + O 2 → H 2 SO 4 - + Fe 2 O 3
Механизм образования кислотных дождей Механизм I: HO· + SO 2 → HSO 3· + O 2 → SO 3 + HO·2 SO 3 + H 2 O → H 2 SO 4 Механизм II: HSO 3 - + H 2 O 2 + H 3 O+ → H 2 SO 4 + H 2 O HSO 3 - + O 3 + H 3 O+ → H 2 SO 4 + H 2 O + O 2 HSO 3 - + 2 Fe. O + O 2 → H 2 SO 4 - + Fe 2 O 3
 Механизм образования кислотных дождей Механизм III ( «дневной» механизм): OH+ + NO 2 → HNO 3 Механизм IV ( «ночной» механизм): NO 2 + O 3 → NO 3· + O 2 NO 3· + NO 2 → N 2 O 5 + H 2 O → 2 HNO 3
Механизм образования кислотных дождей Механизм III ( «дневной» механизм): OH+ + NO 2 → HNO 3 Механизм IV ( «ночной» механизм): NO 2 + O 3 → NO 3· + O 2 NO 3· + NO 2 → N 2 O 5 + H 2 O → 2 HNO 3
 Соединения азота в тропосфере Общая формула – NOx NO, NO 2, N 2 O, N 2 O 3. N 2 O 5 N 2 O + hν → N 2 + O N 2 O + O → N 2 + O 2 N 2 O + O → 2 NO NO + HO 2 → NO 2 + OH NO + O 3 → NO 2 + O 2 NO 2 + hν → NO + O HNO 3 + NH 3 → NH 4 NO 3
Соединения азота в тропосфере Общая формула – NOx NO, NO 2, N 2 O, N 2 O 3. N 2 O 5 N 2 O + hν → N 2 + O N 2 O + O → N 2 + O 2 N 2 O + O → 2 NO NO + HO 2 → NO 2 + OH NO + O 3 → NO 2 + O 2 NO 2 + hν → NO + O HNO 3 + NH 3 → NH 4 NO 3
 Фотохимический смог Смог – это совокупность газообразных и твердых примесей в сочетании с туманом или аэрозольной дымкой, образующихся в результате их преобразования и вызывающих интенсивное загрязнение атмосферы Два типа смога: Ø классический (лондонский) Ø фотохимический Характерные особенности фотохимического смога: • образуется в ясную солнечную погоду при низкой влажности воздуха; • сопровождается возникновением голубоватой дымки, небольшого тумана и ухудшением видимости; • вызывает сильное раздражение слизистых оболочек и губит листву растений, что является результатом сильного окислительного действия.
Фотохимический смог Смог – это совокупность газообразных и твердых примесей в сочетании с туманом или аэрозольной дымкой, образующихся в результате их преобразования и вызывающих интенсивное загрязнение атмосферы Два типа смога: Ø классический (лондонский) Ø фотохимический Характерные особенности фотохимического смога: • образуется в ясную солнечную погоду при низкой влажности воздуха; • сопровождается возникновением голубоватой дымки, небольшого тумана и ухудшением видимости; • вызывает сильное раздражение слизистых оболочек и губит листву растений, что является результатом сильного окислительного действия.
 Химизм образования фотохимического смога ультрафиолетовая радиация оксиды азота + углеводороды → пероксиацетилнитрат (ПАН) + озон (O 3)
Химизм образования фотохимического смога ультрафиолетовая радиация оксиды азота + углеводороды → пероксиацетилнитрат (ПАН) + озон (O 3)
 С присутствием органических соединений в воздухе городов связаны и процессы образования высокотоксичных пероксидных соединений: R–C(O)–O–O–NO 2 Пероксиацетилнитрат (ПАН) Пероксибензилнитрат (ПБН) CH 3–C(O)–O–O–NO 2 C 6 H 5–C(O)–O–O–NO 2
С присутствием органических соединений в воздухе городов связаны и процессы образования высокотоксичных пероксидных соединений: R–C(O)–O–O–NO 2 Пероксиацетилнитрат (ПАН) Пероксибензилнитрат (ПБН) CH 3–C(O)–O–O–NO 2 C 6 H 5–C(O)–O–O–NO 2
 Схема вероятного механизма образования фотохимического смога 1. Поглощение света: NO 2 + hν → NO + O (SO 2 и SO 3 также способны поглощать свет) 2. Цепь ароматного кислорода: а) O + R → R·+ RCHO (не уравнено) б) R·+ O 2 → RO 2· в) RO 2· + NO → RO· + NO 2 г) RO· → R· + O NO + O 2 → NO 2 + O (суммарная реакция) 3. Цепь озона: а) O + O 2 → O 3 б) О 3 + R → RСO 2· + RСHO (не уравнено) в) RСO 2· + NO → RСO· + NO 2 г) RСO· + NO 2 + O 2 → RC-O-O-NO 2 ║ O (вероятно, в две стадии) 4. Обрыв цепи: а) O + NO 2 → NO + O 2 б) O 3 + NO → NO 2 + O 2 в) RO· + NO 2 → RONO 2
Схема вероятного механизма образования фотохимического смога 1. Поглощение света: NO 2 + hν → NO + O (SO 2 и SO 3 также способны поглощать свет) 2. Цепь ароматного кислорода: а) O + R → R·+ RCHO (не уравнено) б) R·+ O 2 → RO 2· в) RO 2· + NO → RO· + NO 2 г) RO· → R· + O NO + O 2 → NO 2 + O (суммарная реакция) 3. Цепь озона: а) O + O 2 → O 3 б) О 3 + R → RСO 2· + RСHO (не уравнено) в) RСO 2· + NO → RСO· + NO 2 г) RСO· + NO 2 + O 2 → RC-O-O-NO 2 ║ O (вероятно, в две стадии) 4. Обрыв цепи: а) O + NO 2 → NO + O 2 б) O 3 + NO → NO 2 + O 2 в) RO· + NO 2 → RONO 2
 Лондонский смог Смог лондонского типа — сочетание газообразных загрязнителей (в основном сернистого газа SO 2), пылевых частиц и тумана. Впервые был отмечен в 1952 г. в Лондоне. Главным действующим компонентом смога является сернистый газ в сочетании с аэрозолем серной кислоты. Смог наблюдается обычно в осенне-зимнее время (с октября по февраль).
Лондонский смог Смог лондонского типа — сочетание газообразных загрязнителей (в основном сернистого газа SO 2), пылевых частиц и тумана. Впервые был отмечен в 1952 г. в Лондоне. Главным действующим компонентом смога является сернистый газ в сочетании с аэрозолем серной кислоты. Смог наблюдается обычно в осенне-зимнее время (с октября по февраль).
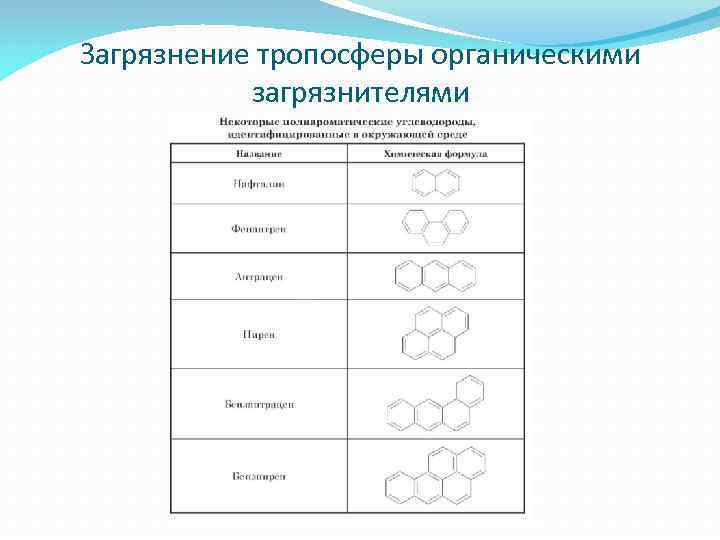 Загрязнение тропосферы органическими загрязнителями
Загрязнение тропосферы органическими загрязнителями


