Slayd_k_l_3.ppt
- Количество слайдов: 27
 Лекция № 3 XИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
Лекция № 3 XИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
 Зачем изучают химическую кинетику? Реакции гомогенные 2 Н 2 + О 2 = 2 Н 2 О Н+ +ОН- =Н 2 О гетерогенные Mo. O 3 + 3 H 2 =Mo + 3 H 2 O металл + к-та = …
Зачем изучают химическую кинетику? Реакции гомогенные 2 Н 2 + О 2 = 2 Н 2 О Н+ +ОН- =Н 2 О гетерогенные Mo. O 3 + 3 H 2 =Mo + 3 H 2 O металл + к-та = …
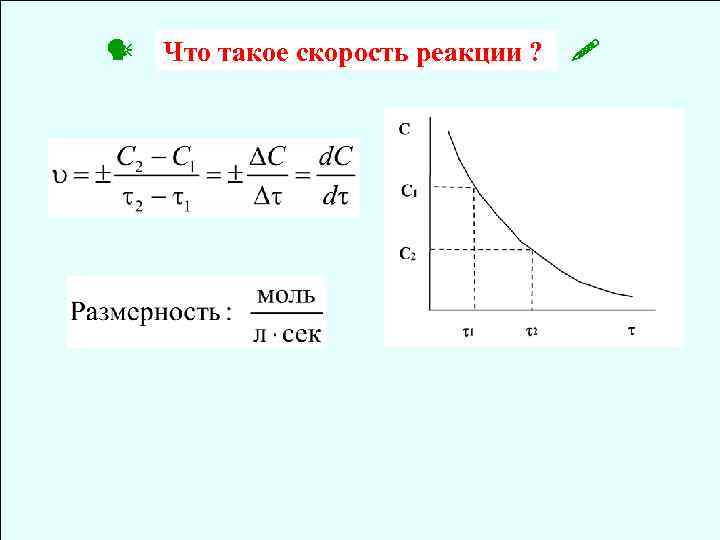 Что такое скорость реакции ?
Что такое скорость реакции ?
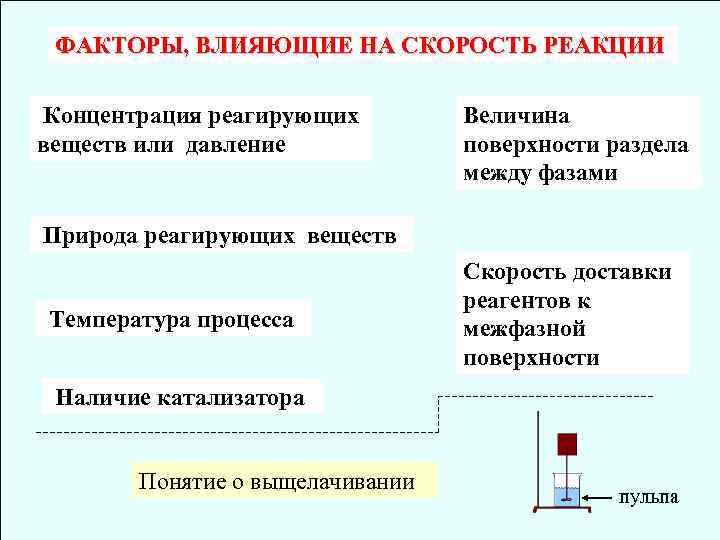 ФАКТОРЫ, ВЛИЯЮЩИЕ НА СКОРОСТЬ РЕАКЦИИ Концентрация реагирующих веществ или давление Величина поверхности раздела между фазами Природа реагирующих веществ Температура процесса Скорость доставки реагентов к межфазной поверхности Наличие катализатора Понятие о выщелачивании пульпа
ФАКТОРЫ, ВЛИЯЮЩИЕ НА СКОРОСТЬ РЕАКЦИИ Концентрация реагирующих веществ или давление Величина поверхности раздела между фазами Природа реагирующих веществ Температура процесса Скорость доставки реагентов к межфазной поверхности Наличие катализатора Понятие о выщелачивании пульпа
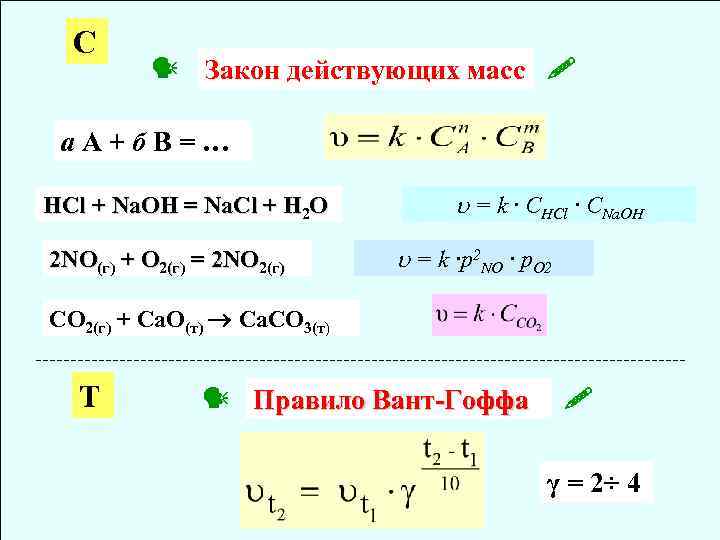 С Закон действующих масс а. А+б. В=… HCl + Na. OH = Na. Cl + H 2 O 2 NO(г) + O 2(г) = 2 NO 2(г) = k · CHCl · CNa. OH = k ·p 2 NO · p. O 2 CO 2(г) + Ca. O(т) Ca. CO 3(т) T Правило Вант-Гоффа γ = 2÷ 4
С Закон действующих масс а. А+б. В=… HCl + Na. OH = Na. Cl + H 2 O 2 NO(г) + O 2(г) = 2 NO 2(г) = k · CHCl · CNa. OH = k ·p 2 NO · p. O 2 CO 2(г) + Ca. O(т) Ca. CO 3(т) T Правило Вант-Гоффа γ = 2÷ 4
 Природа реагирующих веществ Н 2 + F 2 = 2 HF H 2 + Cl 2 = 2 HCl Н 2 + Br 2 = 2 HBr Н 2 + I 2 = 2 HI при комнатной температуре, со взрывом на свету, или нагреть, или пропустить электрический разряд начинается при температуре 200 -300 С при нагревании до 500 -700 С
Природа реагирующих веществ Н 2 + F 2 = 2 HF H 2 + Cl 2 = 2 HCl Н 2 + Br 2 = 2 HBr Н 2 + I 2 = 2 HI при комнатной температуре, со взрывом на свету, или нагреть, или пропустить электрический разряд начинается при температуре 200 -300 С при нагревании до 500 -700 С
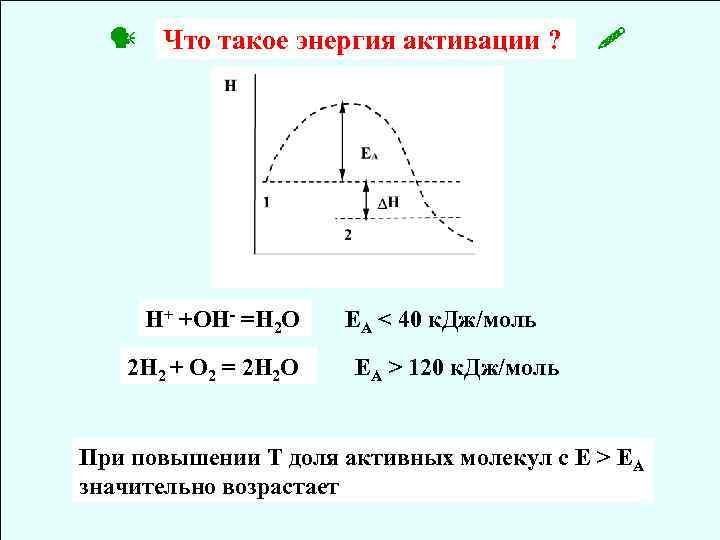 Что такое энергия активации ? Н+ +ОН- =Н 2 О 2 Н 2 + О 2 = 2 Н 2 О ЕА < 40 к. Дж/моль ЕА > 120 к. Дж/моль При повышении Т доля активных молекул с E > EA значительно возрастает
Что такое энергия активации ? Н+ +ОН- =Н 2 О 2 Н 2 + О 2 = 2 Н 2 О ЕА < 40 к. Дж/моль ЕА > 120 к. Дж/моль При повышении Т доля активных молекул с E > EA значительно возрастает
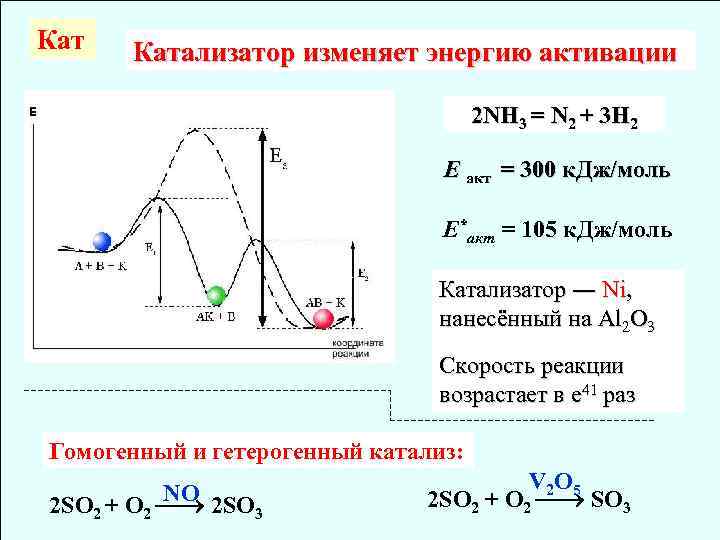 Кат Катализатор изменяет энергию активации 2 NH 3 = N 2 + 3 H 2 Е акт = 300 к. Дж/моль Е*акт = 105 к. Дж/моль Катализатор ― Ni, нанесённый на Al 2 O 3 Скорость реакции возрастает в е 41 раз Гомогенный и гетерогенный катализ: NO 2 SO 2 + O 2 2 SO 3 V 2 O 5 2 SO 2 + O 2 SO 3
Кат Катализатор изменяет энергию активации 2 NH 3 = N 2 + 3 H 2 Е акт = 300 к. Дж/моль Е*акт = 105 к. Дж/моль Катализатор ― Ni, нанесённый на Al 2 O 3 Скорость реакции возрастает в е 41 раз Гомогенный и гетерогенный катализ: NO 2 SO 2 + O 2 2 SO 3 V 2 O 5 2 SO 2 + O 2 SO 3
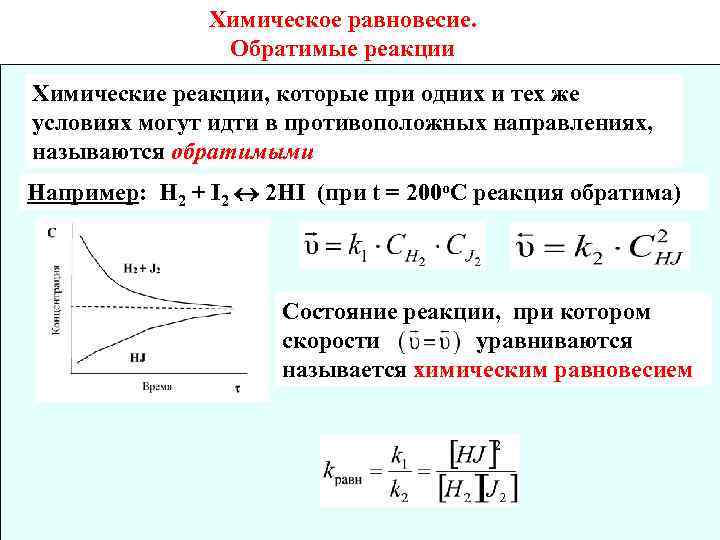 Химическое равновесие. Обратимые реакции Химические реакции, которые при одних и тех же условиях могут идти в противоположных направлениях, называются обратимыми Например: Н 2 + I 2 2 HI (при t = 200 o. C реакция обратима) Состояние реакции, при котором скорости уравниваются называется химическим равновесием
Химическое равновесие. Обратимые реакции Химические реакции, которые при одних и тех же условиях могут идти в противоположных направлениях, называются обратимыми Например: Н 2 + I 2 2 HI (при t = 200 o. C реакция обратима) Состояние реакции, при котором скорости уравниваются называется химическим равновесием
![а. А + b. В с. С + d. D [C]c [D]d K = а. А + b. В с. С + d. D [C]c [D]d K =](https://present5.com/presentation/140522884_157222824/image-10.jpg) а. А + b. В с. С + d. D [C]c [D]d K = k 1 / k 2 = ————— [A]a [B]b Математическое выражение закона действующих масс при химическом равновесии K не зависит от С, но зависит от Т
а. А + b. В с. С + d. D [C]c [D]d K = k 1 / k 2 = ————— [A]a [B]b Математическое выражение закона действующих масс при химическом равновесии K не зависит от С, но зависит от Т
 Выход реакции Если Кравн>>1, то выход реакции велик Если Кравн <<1, то выход реакции мал Cu(т) + 2 Ag+(водн) Сu 2+(водн) + 2 Ag(т) [Сu 2+] К = —— = 2 · 1015 [Ag+]2 Ag. I(т) Ag+ + I- K = [Ag+] [I-] = 1· 10 -16
Выход реакции Если Кравн>>1, то выход реакции велик Если Кравн <<1, то выход реакции мал Cu(т) + 2 Ag+(водн) Сu 2+(водн) + 2 Ag(т) [Сu 2+] К = —— = 2 · 1015 [Ag+]2 Ag. I(т) Ag+ + I- K = [Ag+] [I-] = 1· 10 -16
 Кс и Кр m Р V = — RT M Н 2(г) + I 2(г) 2 HI(г) Р 2(НI) Кр = ————— P(H 2) ·P(I 2) n P = — RT = const · C C V Fe 2 O 3(к) + 3 CO(г) 2 Fe(к) +3 CO 2(г) Р 3(СО 2) Кр = ———— Р 3(СО) В гетерогенных системах константа равновесия учитывает Р или С только летучих веществ
Кс и Кр m Р V = — RT M Н 2(г) + I 2(г) 2 HI(г) Р 2(НI) Кр = ————— P(H 2) ·P(I 2) n P = — RT = const · C C V Fe 2 O 3(к) + 3 CO(г) 2 Fe(к) +3 CO 2(г) Р 3(СО 2) Кр = ———— Р 3(СО) В гетерогенных системах константа равновесия учитывает Р или С только летучих веществ
 Смещение равновесия С Сso 3 2 SO 2 +O 2 2 SO 3 , H < 0 T T Са. СО 3 Са. О + СО 2 , Н 0 T P 2 SO 2 + O 2 2 SO 3 Сso 2 и Со 2 , Т ПРИНЦИП ЛЕ ШАТЕЛЬЕ T N 2(г) + 3 Н 2(г) 2 NН 3 (г Р Катализатор не влияет на смещение химического равновесия N 2(г) +O 2(г) = N 2 O 4(г) Р – не влияет В гетерогенных системах учитываются только летучие вещества
Смещение равновесия С Сso 3 2 SO 2 +O 2 2 SO 3 , H < 0 T T Са. СО 3 Са. О + СО 2 , Н 0 T P 2 SO 2 + O 2 2 SO 3 Сso 2 и Со 2 , Т ПРИНЦИП ЛЕ ШАТЕЛЬЕ T N 2(г) + 3 Н 2(г) 2 NН 3 (г Р Катализатор не влияет на смещение химического равновесия N 2(г) +O 2(г) = N 2 O 4(г) Р – не влияет В гетерогенных системах учитываются только летучие вещества
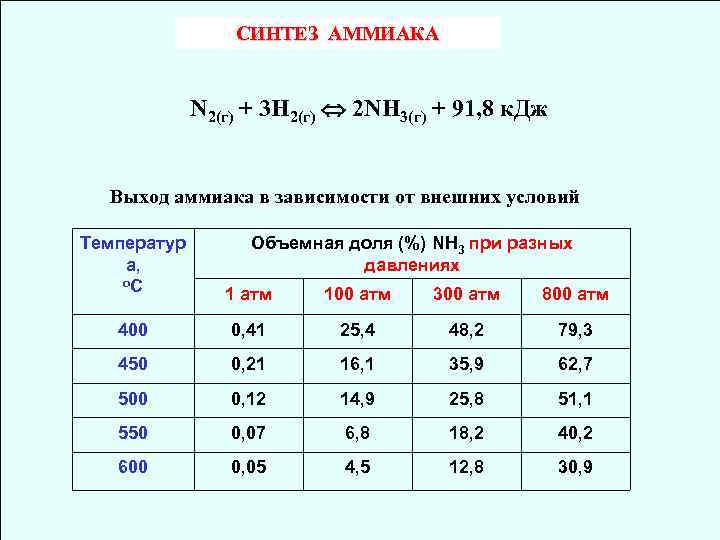 СИНТЕЗ АММИАКА N 2(г) + 3 H 2(г) 2 NH 3(г) + 91, 8 к. Дж Выход аммиака в зависимости от внешних условий Температур а, о. С Объемная доля (%) NH 3 при разных давлениях 1 атм 100 атм 300 атм 800 атм 400 0, 41 25, 4 48, 2 79, 3 450 0, 21 16, 1 35, 9 62, 7 500 0, 12 14, 9 25, 8 51, 1 550 0, 07 6, 8 18, 2 40, 2 600 0, 05 4, 5 12, 8 30, 9
СИНТЕЗ АММИАКА N 2(г) + 3 H 2(г) 2 NH 3(г) + 91, 8 к. Дж Выход аммиака в зависимости от внешних условий Температур а, о. С Объемная доля (%) NH 3 при разных давлениях 1 атм 100 атм 300 атм 800 атм 400 0, 41 25, 4 48, 2 79, 3 450 0, 21 16, 1 35, 9 62, 7 500 0, 12 14, 9 25, 8 51, 1 550 0, 07 6, 8 18, 2 40, 2 600 0, 05 4, 5 12, 8 30, 9
 Посмотрите дополнительный материал на сайте кафедры - лекция № 3 Процесс выщелачивания Промышленный синтез аммиака *
Посмотрите дополнительный материал на сайте кафедры - лекция № 3 Процесс выщелачивания Промышленный синтез аммиака *
 Лекция № 3 ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
Лекция № 3 ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
 Выщелачивание - это процесс перевода химического соединения основного металла из руд или концентратов в раствор с помощью селективного (избирательно) действующего растворителя. В качестве растворителей используют воду, водные растворы минеральных кислот (H 2 SO 4; HCl; HNO 3), щелочей (Na. OH; NH 4 OH) или солей (Na 2 CO 3 и др. ). Цель выщелачивания – подбор оптимальных условий (температура, концентрация растворов), при которых извлекаемый металл растворялся бы с максимальной полнотой и скоростью, а пустая порода и сопутствующие элементы либо вообще не растворялись, либо степень их перехода в раствор была бы невелика. Факторы, влияющие на скорость выщелачивания (или параметры процесса): температура, скорость перемешивания, поверхность твердой фазы и пр.
Выщелачивание - это процесс перевода химического соединения основного металла из руд или концентратов в раствор с помощью селективного (избирательно) действующего растворителя. В качестве растворителей используют воду, водные растворы минеральных кислот (H 2 SO 4; HCl; HNO 3), щелочей (Na. OH; NH 4 OH) или солей (Na 2 CO 3 и др. ). Цель выщелачивания – подбор оптимальных условий (температура, концентрация растворов), при которых извлекаемый металл растворялся бы с максимальной полнотой и скоростью, а пустая порода и сопутствующие элементы либо вообще не растворялись, либо степень их перехода в раствор была бы невелика. Факторы, влияющие на скорость выщелачивания (или параметры процесса): температура, скорость перемешивания, поверхность твердой фазы и пр.
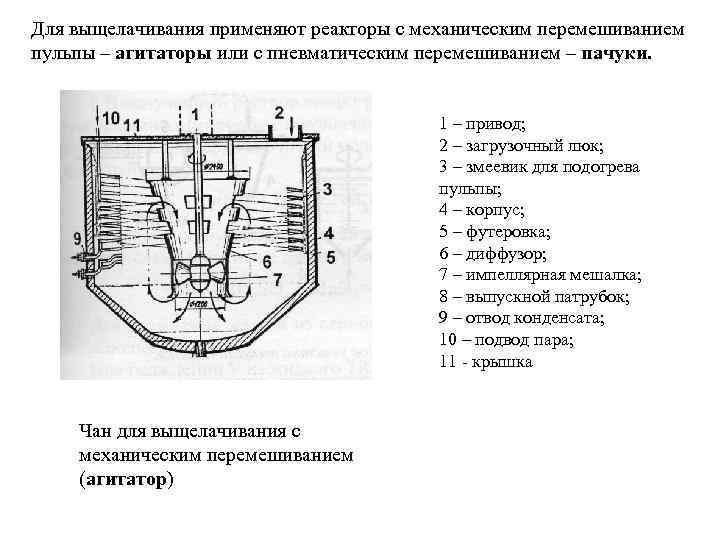 Для выщелачивания применяют реакторы с механическим перемешиванием пульпы – агитаторы или с пневматическим перемешиванием – пачуки. 1 – привод; 2 – загрузочный люк; 3 – змеевик для подогрева пульпы; 4 – корпус; 5 – футеровка; 6 – диффузор; 7 – импеллярная мешалка; 8 – выпускной патрубок; 9 – отвод конденсата; 10 – подвод пара; 11 - крышка Чан для выщелачивания с механическим перемешиванием (агитатор)
Для выщелачивания применяют реакторы с механическим перемешиванием пульпы – агитаторы или с пневматическим перемешиванием – пачуки. 1 – привод; 2 – загрузочный люк; 3 – змеевик для подогрева пульпы; 4 – корпус; 5 – футеровка; 6 – диффузор; 7 – импеллярная мешалка; 8 – выпускной патрубок; 9 – отвод конденсата; 10 – подвод пара; 11 - крышка Чан для выщелачивания с механическим перемешиванием (агитатор)
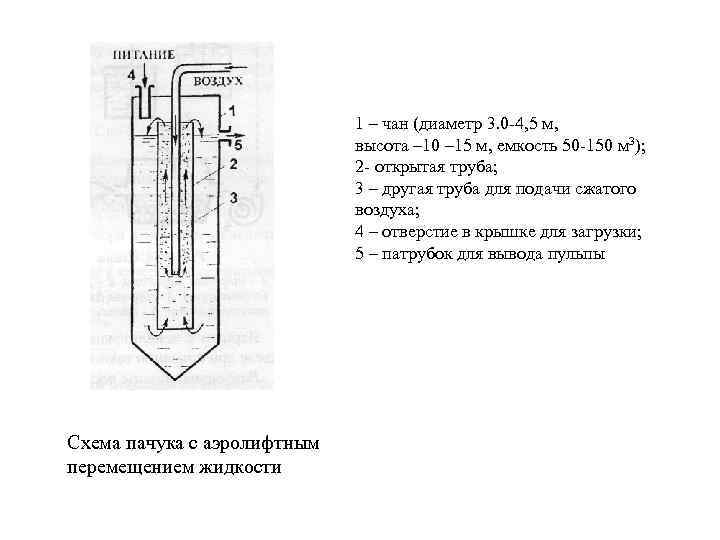 1 – чан (диаметр 3. 0 -4, 5 м, высота – 10 – 15 м, емкость 50 -150 м 3); 2 - открытая труба; 3 – другая труба для подачи сжатого воздуха; 4 – отверстие в крышке для загрузки; 5 – патрубок для вывода пульпы Схема пачука с аэролифтным перемещением жидкости
1 – чан (диаметр 3. 0 -4, 5 м, высота – 10 – 15 м, емкость 50 -150 м 3); 2 - открытая труба; 3 – другая труба для подачи сжатого воздуха; 4 – отверстие в крышке для загрузки; 5 – патрубок для вывода пульпы Схема пачука с аэролифтным перемещением жидкости
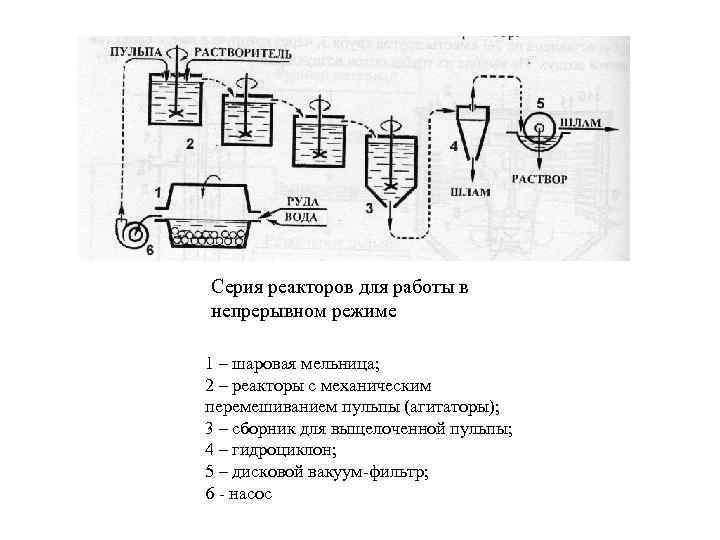 Серия реакторов для работы в непрерывном режиме 1 – шаровая мельница; 2 – реакторы с механическим перемешиванием пульпы (агитаторы); 3 – сборник для выщелоченной пульпы; 4 – гидроциклон; 5 – дисковой вакуум-фильтр; 6 - насос
Серия реакторов для работы в непрерывном режиме 1 – шаровая мельница; 2 – реакторы с механическим перемешиванием пульпы (агитаторы); 3 – сборник для выщелоченной пульпы; 4 – гидроциклон; 5 – дисковой вакуум-фильтр; 6 - насос
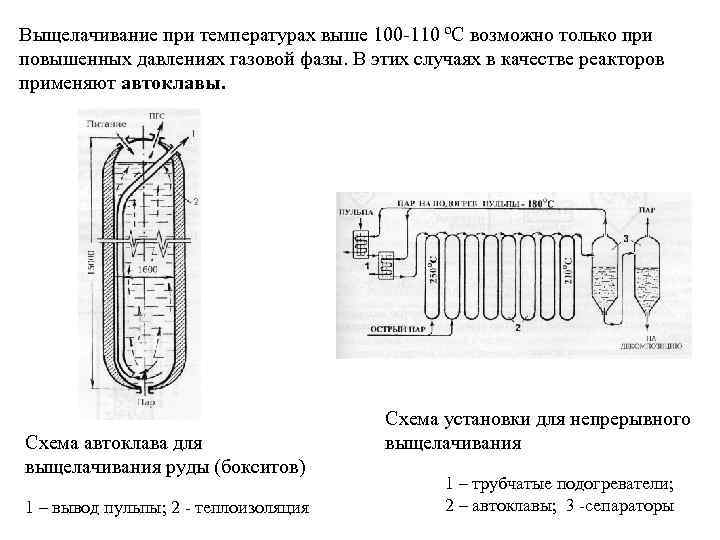 Выщелачивание при температурах выше 100 -110 ºС возможно только при повышенных давлениях газовой фазы. В этих случаях в качестве реакторов применяют автоклавы. Cхема автоклава для выщелачивания руды (бокситов) 1 – вывод пульпы; 2 - теплоизоляция Схема установки для непрерывного выщелачивания 1 – трубчатые подогреватели; 2 – автоклавы; 3 -сепараторы
Выщелачивание при температурах выше 100 -110 ºС возможно только при повышенных давлениях газовой фазы. В этих случаях в качестве реакторов применяют автоклавы. Cхема автоклава для выщелачивания руды (бокситов) 1 – вывод пульпы; 2 - теплоизоляция Схема установки для непрерывного выщелачивания 1 – трубчатые подогреватели; 2 – автоклавы; 3 -сепараторы
 Разделение пульпы после выщелачивания на раствор и твердый осадок производят с помощью различных аппаратов: отстойников-сгустителей, гидроциклонов, фильтров, а также центрифугированием. Твердую фазу – шлам – после разделения промывают и направляют либо в отвал, либо на извлечение сопутствующих элементов. Жидкую фазу – раствор – вначале подвергают очистке от нежелательных элементов, перешедших в раствор из руды, а затем направляют на извлечение из нее основного элемента. Выщелачивание – один из основных процессов в гидрометаллургических схемах переработки рудного сырья. Исследование кинетики процессов выщелачивания необходимо для определения энергии активации, установления лимитирующей стадии процесса и на основании этого определение оптимальных параметров.
Разделение пульпы после выщелачивания на раствор и твердый осадок производят с помощью различных аппаратов: отстойников-сгустителей, гидроциклонов, фильтров, а также центрифугированием. Твердую фазу – шлам – после разделения промывают и направляют либо в отвал, либо на извлечение сопутствующих элементов. Жидкую фазу – раствор – вначале подвергают очистке от нежелательных элементов, перешедших в раствор из руды, а затем направляют на извлечение из нее основного элемента. Выщелачивание – один из основных процессов в гидрометаллургических схемах переработки рудного сырья. Исследование кинетики процессов выщелачивания необходимо для определения энергии активации, установления лимитирующей стадии процесса и на основании этого определение оптимальных параметров.
 Примеры реальных технологических процессов выщелачивания. 1. Выщелачивание вольфрама из шеелита Сa. WO 4 растворами соды в автоклавах. Сa. WO 4(тв) + Na 2 CO 3(раст) = Na 2 WO 4(раств) + Ca. CO 3(тв) Оптимальные параметры процесса: температура 200 -225 С, расход соды в 2, 5 -2, 7 раза больше от стехиометрически необходимого количества, энергия активации составляет 75 -92 к. Дж/моль. Величина энергии активации указывает на лимитирующую стадию процесса. Установлено, что если энергия активации составляет 8÷ 20 к. Дж/моль, то скорость реакции лимитируется процессами диффузии. Если энергия активации составляет 40 -300 к. Дж/моль, то процесс лимитируется собственной химической реакцией 2. Выщелачивание минералов бокситовых руд растворами едкого натра. Al(OH)3 + Na. OH = Na. Al(OH)4 Температура выщелачивания: 100 -105 C, концентрация растворов Na. OH – 200 -250 г/л, давление – атмосферное. Al. OOH +Na. OH + H 2 O = Na. Al(OH)4 Температура – 200 -220 С, концентрация щелочи 290 -300 г/л, выщелачивание в автоклавах.
Примеры реальных технологических процессов выщелачивания. 1. Выщелачивание вольфрама из шеелита Сa. WO 4 растворами соды в автоклавах. Сa. WO 4(тв) + Na 2 CO 3(раст) = Na 2 WO 4(раств) + Ca. CO 3(тв) Оптимальные параметры процесса: температура 200 -225 С, расход соды в 2, 5 -2, 7 раза больше от стехиометрически необходимого количества, энергия активации составляет 75 -92 к. Дж/моль. Величина энергии активации указывает на лимитирующую стадию процесса. Установлено, что если энергия активации составляет 8÷ 20 к. Дж/моль, то скорость реакции лимитируется процессами диффузии. Если энергия активации составляет 40 -300 к. Дж/моль, то процесс лимитируется собственной химической реакцией 2. Выщелачивание минералов бокситовых руд растворами едкого натра. Al(OH)3 + Na. OH = Na. Al(OH)4 Температура выщелачивания: 100 -105 C, концентрация растворов Na. OH – 200 -250 г/л, давление – атмосферное. Al. OOH +Na. OH + H 2 O = Na. Al(OH)4 Температура – 200 -220 С, концентрация щелочи 290 -300 г/л, выщелачивание в автоклавах.
 Промышленный синтез аммиака Аммиак NH 3 – практически самое важное водородное соединение азота, так как лежит в основе получения азотных минеральных удобрений. Азот, как известно, является необходимым элементом для роста растений. Основным сырьем в производстве аммиака являются атмосферный воздух и природный газ. Азот получают путем сжижения воздуха (в состав воздуха входит 79 % азота), а водород или водородосодержащий газ получают из природного газа. Аммиак в обычных условиях представляет собой бесцветный газ с резким запахом, легко сжижается, хорошо растворим в воде c образованием гидратов. В жидком состоянии аммиак – бесцветная подвижная жидкость, не проводящая электрического тока. Промышленный синтез аммиака из элементов осуществляется по уравнению: N 2(г) + 3 H 2(г) 2 NH 3(г) + 91, 8 к. Дж ( ) Так называемый процесс Габера – по имени немецкого химика Ф. Габера, разработавшего физикохимические основы этого метода и получившего за это Нобелевскую премию по химии в 1918 г.
Промышленный синтез аммиака Аммиак NH 3 – практически самое важное водородное соединение азота, так как лежит в основе получения азотных минеральных удобрений. Азот, как известно, является необходимым элементом для роста растений. Основным сырьем в производстве аммиака являются атмосферный воздух и природный газ. Азот получают путем сжижения воздуха (в состав воздуха входит 79 % азота), а водород или водородосодержащий газ получают из природного газа. Аммиак в обычных условиях представляет собой бесцветный газ с резким запахом, легко сжижается, хорошо растворим в воде c образованием гидратов. В жидком состоянии аммиак – бесцветная подвижная жидкость, не проводящая электрического тока. Промышленный синтез аммиака из элементов осуществляется по уравнению: N 2(г) + 3 H 2(г) 2 NH 3(г) + 91, 8 к. Дж ( ) Так называемый процесс Габера – по имени немецкого химика Ф. Габера, разработавшего физикохимические основы этого метода и получившего за это Нобелевскую премию по химии в 1918 г.
 Реакция обратимая, экзотермическая. Исходя из принципа Ле Шателье ясно, что чем ниже температура, тем больше равновесие будет сдвигаться в сторону образования аммиака, т. е. вправо. Поэтому, можно предположить, что следует максимально понижать температуру. Однако, при низких температурах реакция протекает очень медленно (практически не идет). Поэтому, на практике процесс проводят при температуре 400 -450 ºС. Но даже при такой высокой температуре для достижения высокой скорости реакции требуется присутствие специального катализатора. В качестве катализатора используется губчатое железо, активированное оксидами калия и алюминия. Cогласно принципу Ле Шателье, процесс выгодно проводить, повышая давление. Однако, оборудование, рассчитанное на очень высокое давление, дорого и процесс становится экономически менее выгодным. Поэтому, на практике держат «среднее» давление 250 атм.
Реакция обратимая, экзотермическая. Исходя из принципа Ле Шателье ясно, что чем ниже температура, тем больше равновесие будет сдвигаться в сторону образования аммиака, т. е. вправо. Поэтому, можно предположить, что следует максимально понижать температуру. Однако, при низких температурах реакция протекает очень медленно (практически не идет). Поэтому, на практике процесс проводят при температуре 400 -450 ºС. Но даже при такой высокой температуре для достижения высокой скорости реакции требуется присутствие специального катализатора. В качестве катализатора используется губчатое железо, активированное оксидами калия и алюминия. Cогласно принципу Ле Шателье, процесс выгодно проводить, повышая давление. Однако, оборудование, рассчитанное на очень высокое давление, дорого и процесс становится экономически менее выгодным. Поэтому, на практике держат «среднее» давление 250 атм.
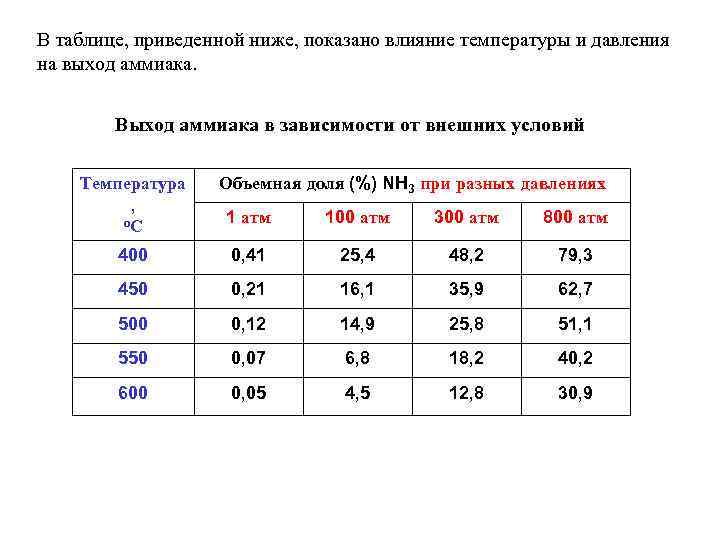 В таблице, приведенной ниже, показано влияние температуры и давления на выход аммиака. Выход аммиака в зависимости от внешних условий Температура , о. С Объемная доля (%) NH 3 при разных давлениях 1 атм 100 атм 300 атм 800 атм 400 0, 41 25, 4 48, 2 79, 3 450 0, 21 16, 1 35, 9 62, 7 500 0, 12 14, 9 25, 8 51, 1 550 0, 07 6, 8 18, 2 40, 2 600 0, 05 4, 5 12, 8 30, 9
В таблице, приведенной ниже, показано влияние температуры и давления на выход аммиака. Выход аммиака в зависимости от внешних условий Температура , о. С Объемная доля (%) NH 3 при разных давлениях 1 атм 100 атм 300 атм 800 атм 400 0, 41 25, 4 48, 2 79, 3 450 0, 21 16, 1 35, 9 62, 7 500 0, 12 14, 9 25, 8 51, 1 550 0, 07 6, 8 18, 2 40, 2 600 0, 05 4, 5 12, 8 30, 9
 Таким образом, оптимальными параметрами процесса получения аммиака в процессе Габера являются температура 450 ºС и давление 250 атм. Хотя при этих условиях только около 20 % исходных веществ превращается в аммиак, однако в результате использования циркуляционной технологической схемы (введение непрореагировавших Н 2 и N 2 вновь в реакцию) суммарная степень превращения исходных веществ в аммиак является очень высокой.
Таким образом, оптимальными параметрами процесса получения аммиака в процессе Габера являются температура 450 ºС и давление 250 атм. Хотя при этих условиях только около 20 % исходных веществ превращается в аммиак, однако в результате использования циркуляционной технологической схемы (введение непрореагировавших Н 2 и N 2 вновь в реакцию) суммарная степень превращения исходных веществ в аммиак является очень высокой.


