2010 Лекция 3. КИНЕТИКА.ppt
- Количество слайдов: 19
 ЛЕКЦИЯ 3 Химическая кинетика
ЛЕКЦИЯ 3 Химическая кинетика
 H 2 (г) + 1/2 O 2 (г) H 2 O(г) + 241, 8 к. Дж/моль H+ (воды) + ОН- (воды) Н 2 О (ж) Мгновенно протекающие реакции. Al 2 Si. O 5+Si. O 2+2 H 2 O=Al 2 Si 2 O 7+2 H 2 O = [Al 2(Si 2 O 5)][OH] силлиманит метакаолинит Реакция В. И. Вернадского KAl. Si 3 O 8+Al 2 O 3+H 2 O = K[Al 2[Al. Si 3 O 10]](OH)2 микроклин корунд мусковит H 0298= -48 к. Дж/моль Реакция В. А. Жарикова Эти реакции протекают очень медленно.
H 2 (г) + 1/2 O 2 (г) H 2 O(г) + 241, 8 к. Дж/моль H+ (воды) + ОН- (воды) Н 2 О (ж) Мгновенно протекающие реакции. Al 2 Si. O 5+Si. O 2+2 H 2 O=Al 2 Si 2 O 7+2 H 2 O = [Al 2(Si 2 O 5)][OH] силлиманит метакаолинит Реакция В. И. Вернадского KAl. Si 3 O 8+Al 2 O 3+H 2 O = K[Al 2[Al. Si 3 O 10]](OH)2 микроклин корунд мусковит H 0298= -48 к. Дж/моль Реакция В. А. Жарикова Эти реакции протекают очень медленно.
 Скорость химической реакции показывает число химических взаимодействий, приводящих к образованию продукта реакции в единице объема или на единице поверхности за единицу времени. =- = =
Скорость химической реакции показывает число химических взаимодействий, приводящих к образованию продукта реакции в единице объема или на единице поверхности за единицу времени. =- = =
 От каких факторов зависит скорость химических реакций? а) От концентрации б) От температуры в) От катализатора
От каких факторов зависит скорость химических реакций? а) От концентрации б) От температуры в) От катализатора
 Скорость реакции пропорциональна произведению концентрации реагирующих веществ в степенях некоторых чисел, определяемых опытным путем. А + В + С = X V = k. CA CB CC - кинетическое уравнение реакции , , - порядок химических реакций по компонентам, + + - общий порядок реакции k - константа скорости реакции, когда CA CB CC = 1, тогда V = k
Скорость реакции пропорциональна произведению концентрации реагирующих веществ в степенях некоторых чисел, определяемых опытным путем. А + В + С = X V = k. CA CB CC - кинетическое уравнение реакции , , - порядок химических реакций по компонентам, + + - общий порядок реакции k - константа скорости реакции, когда CA CB CC = 1, тогда V = k
 2 H 2 O = 2 H 2 + O 2 I порядок V = k. CH 2 O 2 = 2 H 2 O + O 2 I порядок V = k. CH 2 O 2 H 2(газ) + I 2(газ) 2 HI(газ) II порядок V = k. CH 2 CI 2 2 NO = N 2 O 2 II порядок V = k. C 2 NO Молекулярность реакции - число молекул, принимающих участие в акте простейшего химического взаимодействия. N 2 O 4 = 2 NO 2 - мономолекулярная 2 NO = N 2 O 2 - бимолекулярная 2 NO + Cl 2 = 2 NОCl тримолекулярная
2 H 2 O = 2 H 2 + O 2 I порядок V = k. CH 2 O 2 = 2 H 2 O + O 2 I порядок V = k. CH 2 O 2 H 2(газ) + I 2(газ) 2 HI(газ) II порядок V = k. CH 2 CI 2 2 NO = N 2 O 2 II порядок V = k. C 2 NO Молекулярность реакции - число молекул, принимающих участие в акте простейшего химического взаимодействия. N 2 O 4 = 2 NO 2 - мономолекулярная 2 NO = N 2 O 2 - бимолекулярная 2 NO + Cl 2 = 2 NОCl тримолекулярная
 Последовательные реакции- продукты одной стадии являются исходными веществами другой. Лимитирующая стадия – самая медленная из элементарных реакций. 5 H 2 SO 3 + 2 HIO 3 I 2 + 5 H 2 SO 4 + H 2 O Должна быть реакция 2 го порядка и окраска иода должна постепенно усиливаться. IO 3 - + 3 SO 32 - = I- + SO 42 - - медленная стадия, иода нет. Когда израсходуется весь сульфит-ион, быстро протекает 2 ая стадия. IO 3 - + 5 I- + 6 H+ = 3 I 2 + 3 H 2 O Первая стадия - лимитирующая и первого порядка по IO 3 -
Последовательные реакции- продукты одной стадии являются исходными веществами другой. Лимитирующая стадия – самая медленная из элементарных реакций. 5 H 2 SO 3 + 2 HIO 3 I 2 + 5 H 2 SO 4 + H 2 O Должна быть реакция 2 го порядка и окраска иода должна постепенно усиливаться. IO 3 - + 3 SO 32 - = I- + SO 42 - - медленная стадия, иода нет. Когда израсходуется весь сульфит-ион, быстро протекает 2 ая стадия. IO 3 - + 5 I- + 6 H+ = 3 I 2 + 3 H 2 O Первая стадия - лимитирующая и первого порядка по IO 3 -
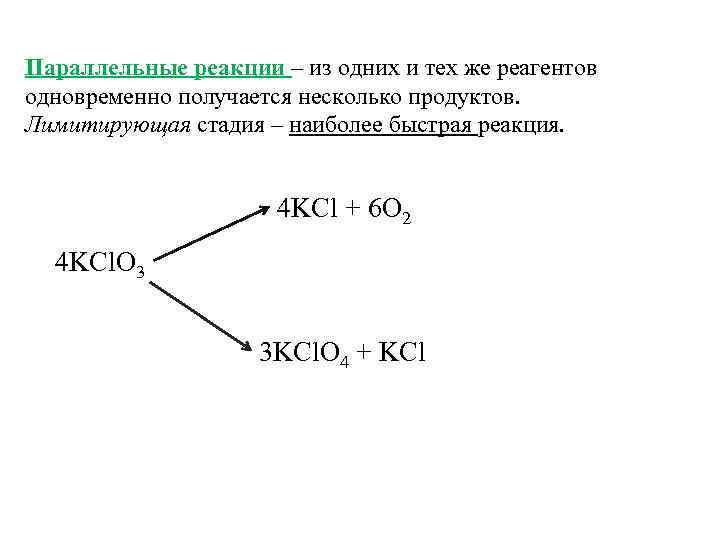 Параллельные реакции – из одних и тех же реагентов одновременно получается несколько продуктов. Лимитирующая стадия – наиболее быстрая реакция. 4 KCl + 6 O 2 4 KCl. O 3 3 KCl. O 4 + KCl
Параллельные реакции – из одних и тех же реагентов одновременно получается несколько продуктов. Лимитирующая стадия – наиболее быстрая реакция. 4 KCl + 6 O 2 4 KCl. O 3 3 KCl. O 4 + KCl
 Цепные реакции можно рассматривать, как частный случай последовательных реакций. Их особенность- многократное повторение одних и тех же стадий с участием свободных радикалов – частиц, имеющих неспаренные электроны. 2 H 2 + O 2 = 2 H 2 O H 2 = H* + H* H* + O 2 = OH* + O* H 2 + O* = OH* + H* - зарождение цепи развитие цепи O*+H*+OH* + H* = 2 OH = H 2 O + ½ O 2 - обрыв цепи.
Цепные реакции можно рассматривать, как частный случай последовательных реакций. Их особенность- многократное повторение одних и тех же стадий с участием свободных радикалов – частиц, имеющих неспаренные электроны. 2 H 2 + O 2 = 2 H 2 O H 2 = H* + H* H* + O 2 = OH* + O* H 2 + O* = OH* + H* - зарождение цепи развитие цепи O*+H*+OH* + H* = 2 OH = H 2 O + ½ O 2 - обрыв цепи.
 Для элементарных реакций – скорость реакции пропорциональна произведению концентрации реагирующих веществ в степенях их стехиометрических коэффициентов. 2 NO + O 2 = 2 NO 2 V = k. C 2 NOCO 2
Для элементарных реакций – скорость реакции пропорциональна произведению концентрации реагирующих веществ в степенях их стехиометрических коэффициентов. 2 NO + O 2 = 2 NO 2 V = k. C 2 NOCO 2
 ПРАВИЛО ИЛИ ЗАКОН ВАНТ-ГОФФА. При повышении температуры на 100 скорость химической реакции возрастает в 2 -4 раза. Скорость реакции Ландольта при увеличении температуры на 100 увеличивается в 2 раза.
ПРАВИЛО ИЛИ ЗАКОН ВАНТ-ГОФФА. При повышении температуры на 100 скорость химической реакции возрастает в 2 -4 раза. Скорость реакции Ландольта при увеличении температуры на 100 увеличивается в 2 раза.
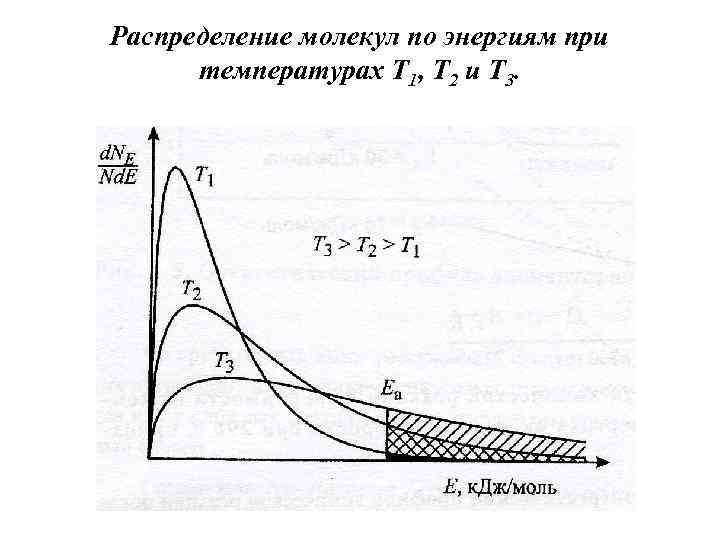 Распределение молекул по энергиям при температурах Т 1, Т 2 и Т 3.
Распределение молекул по энергиям при температурах Т 1, Т 2 и Т 3.
 УРАВНЕНИЕ АРРЕНИУСА ln. K 1 = A – B/T 1 ln. K 2 = A – B/T 2
УРАВНЕНИЕ АРРЕНИУСА ln. K 1 = A – B/T 1 ln. K 2 = A – B/T 2
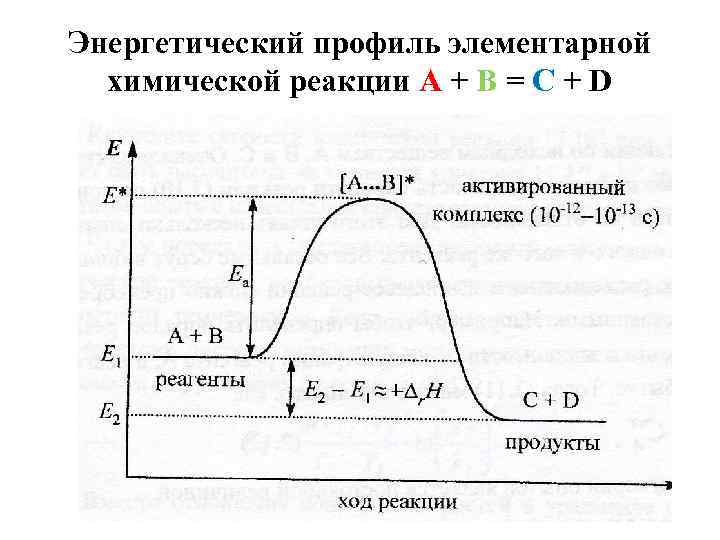 Энергетический профиль элементарной химической реакции А + В = С + D
Энергетический профиль элементарной химической реакции А + В = С + D
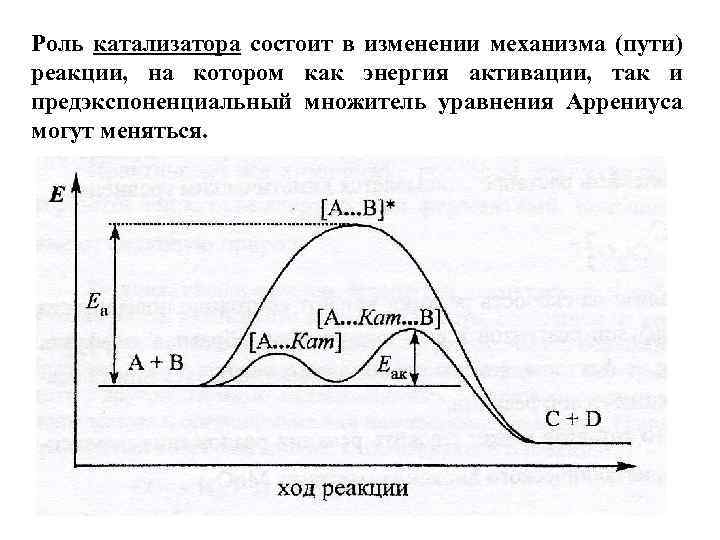 Роль катализатора состоит в изменении механизма (пути) реакции, на котором как энергия активации, так и предэкспоненциальный множитель уравнения Аррениуса могут меняться.
Роль катализатора состоит в изменении механизма (пути) реакции, на котором как энергия активации, так и предэкспоненциальный множитель уравнения Аррениуса могут меняться.
 КАТАЛИЗ может быть гомогенным (когда катализатор и взаимодействующие вещества образуют одну фазу) и гетерогенным (когда реакция происходит на границе раздела двух фаз) C 2 H 5 OC 2 H 5 = 2 CH 4 + 1/2 C 2 H 4 + CO C 2 H 5 OC 2 H 5 CH 4 + C 2 H 6 + CO Cкорость реакции с увеличилась в 10 000 раз. катализатором I 2
КАТАЛИЗ может быть гомогенным (когда катализатор и взаимодействующие вещества образуют одну фазу) и гетерогенным (когда реакция происходит на границе раздела двух фаз) C 2 H 5 OC 2 H 5 = 2 CH 4 + 1/2 C 2 H 4 + CO C 2 H 5 OC 2 H 5 CH 4 + C 2 H 6 + CO Cкорость реакции с увеличилась в 10 000 раз. катализатором I 2
 Гетерогенный катализ находит широкое применение в промышленности (получение HNO 3, H 2 SO 4, NH 3 и др. ). NH 3 + 5 O 2 2 Al + 3 I 2 6 P + 5 KCl. O 3 4 NO + 6 H 2 O 2 Al. I 3 5 KCl + 3 P 2 O 5
Гетерогенный катализ находит широкое применение в промышленности (получение HNO 3, H 2 SO 4, NH 3 и др. ). NH 3 + 5 O 2 2 Al + 3 I 2 6 P + 5 KCl. O 3 4 NO + 6 H 2 O 2 Al. I 3 5 KCl + 3 P 2 O 5
 АВТОКАТАЛИТИЧЕСКИЕ РЕАКЦИИ • 2 KMn. O 4 + 5 H 2 C 2 O 4 + 3 H 2 SO 4 = 2 Mn. SO 4 + 10 CO 2 + 8 H 2 O + K 2 SO 4 • Mn. O 4 - + Mn 2+ + 8 H+ = 2 Mn 3+ +4 H 2 O • H 2 C 2 O 4 + 2 Mn 3+ = 2 CO 2 + 2 Mn 2+ + H 2 O
АВТОКАТАЛИТИЧЕСКИЕ РЕАКЦИИ • 2 KMn. O 4 + 5 H 2 C 2 O 4 + 3 H 2 SO 4 = 2 Mn. SO 4 + 10 CO 2 + 8 H 2 O + K 2 SO 4 • Mn. O 4 - + Mn 2+ + 8 H+ = 2 Mn 3+ +4 H 2 O • H 2 C 2 O 4 + 2 Mn 3+ = 2 CO 2 + 2 Mn 2+ + H 2 O
 КАТАЛИЗАТОРЫ - ФЕРМЕНТЫ 1 моль алкогольдегидрогеназы за 1 сек при комнатной температуре превращает в уксусный альдегид 720 молей этанола. Применяя катализатор медь при 2000 С за 1 сек 0, 1 - 1 моль спирта на 1 моль катализатора.
КАТАЛИЗАТОРЫ - ФЕРМЕНТЫ 1 моль алкогольдегидрогеназы за 1 сек при комнатной температуре превращает в уксусный альдегид 720 молей этанола. Применяя катализатор медь при 2000 С за 1 сек 0, 1 - 1 моль спирта на 1 моль катализатора.


