термодинамика.ppt
- Количество слайдов: 24

ЛЕКЦИЯ № 3 ТЕРМОДИНАМИКА БИОЛОГИЧЕСКИХ СИСТЕМ
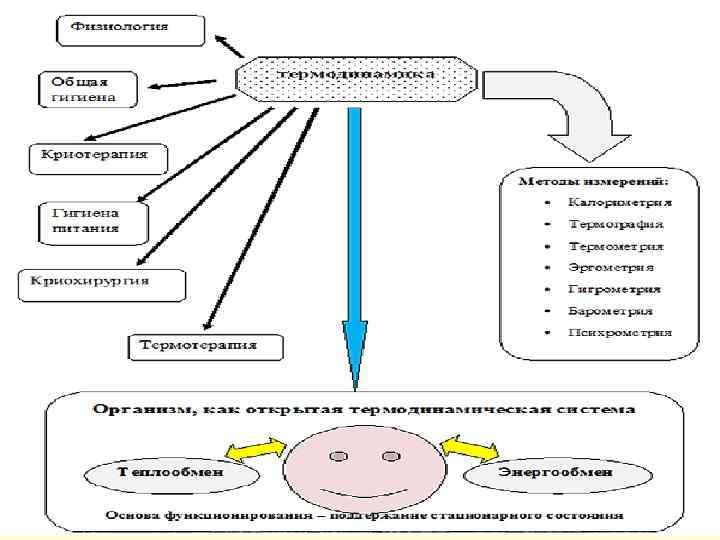
ПРЕДМЕТ ТЕРМОДИНАМИКИ Термодинамика – это наука об общих законах обмена и превращения энергии в системах. Рассматривает эти законы без учёта микроскопического строения тел, составляющих систему. Энергия – универсальная количественная мера для всех форм движения материи, способных превращаться одна в другую. ФОРМЫ ЭНЕРГИИ механическая ядерная тепловая электрическая химическая Виды энергии – потенциальная и кинетическая тепловая электрическая Энергия не может возникнуть из ничего и не может в никуда исчезнуть, она может только переходить из одной формы в другую.
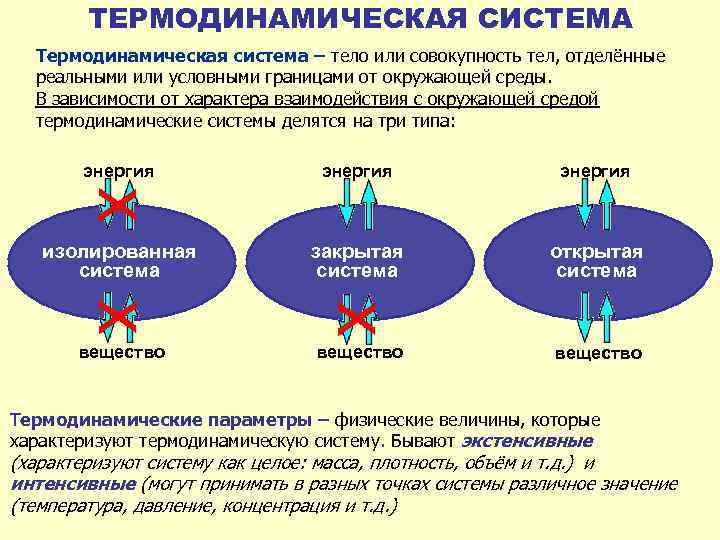
ТЕРМОДИНАМИЧЕСКАЯ СИСТЕМА Термодинамическая система – тело или совокупность тел, отделённые реальными или условными границами от окружающей среды. В зависимости от характера взаимодействия с окружающей средой термодинамические системы делятся на три типа: энергия закрытая система открытая система х энергия изолированная система х х вещество Термодинамические параметры – физические величины, которые характеризуют термодинамическую систему. Бывают экстенсивные (характеризуют систему как целое: масса, плотность, объём и т. д. ) и интенсивные (могут принимать в разных точках системы различное значение (температура, давление, концентрация и т. д. )
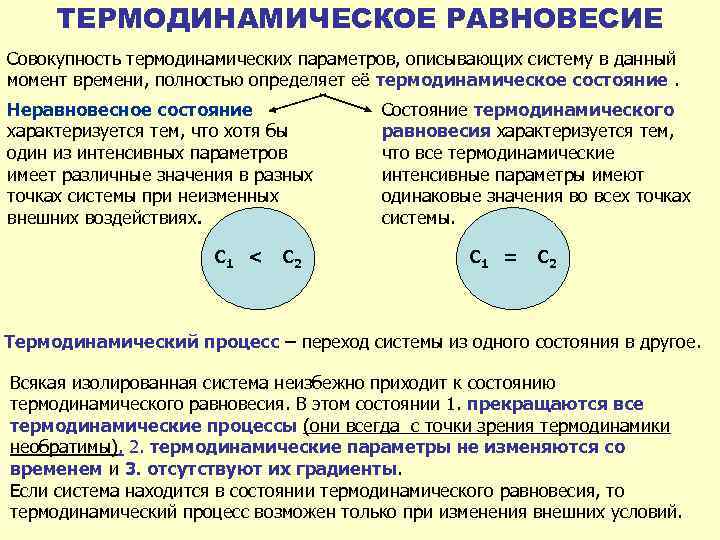
ТЕРМОДИНАМИЧЕСКОЕ РАВНОВЕСИЕ Совокупность термодинамических параметров, описывающих систему в данный момент времени, полностью определяет её термодинамическое состояние. Неравновесное состояние характеризуется тем, что хотя бы один из интенсивных параметров имеет различные значения в разных точках системы при неизменных внешних воздействиях. С 1 < С 2 Состояние термодинамического равновесия характеризуется тем, что все термодинамические интенсивные параметры имеют одинаковые значения во всех точках системы. С 1 = С 2 Термодинамический процесс – переход системы из одного состояния в другое. Всякая изолированная система неизбежно приходит к состоянию термодинамического равновесия. В этом состоянии 1. прекращаются все термодинамические процессы (они всегда с точки зрения термодинамики необратимы), 2. термодинамические параметры не изменяются со временем и 3. отсутствуют их градиенты. Если система находится в состоянии термодинамического равновесия, то термодинамический процесс возможен только при изменения внешних условий.

ВНУТРЕННЯЯ ЭНЕРГИЯ, СПОСОБЫ ЕЁ ИЗМЕНЕНИЯ Внутренняя энергия системы - это общая сумма всех видов энергии в данной системе (механической, тепловой, химической, электрической и т. д. ). Внутренняя энергия системы - суммарная кинетическая и потенциальная энергия всех частиц, составляющих систему. Изменение внутренней энергии происходит в результате взаимодействий. Существует два принципиально различных их способа: совершение работы и теплообмен. - Передача энергии в результате силового взаимодействия и макроскопически упорядоченного движения называется работой (A). - Передача энергии в результате обмена хаотическим движением микрочастиц называется теплообменом. Количество переданной при этом энергии называется теплотой Q. если системе сообщается теплота если система отдаёт теплоту если система совершает работу если над системой совершают работу
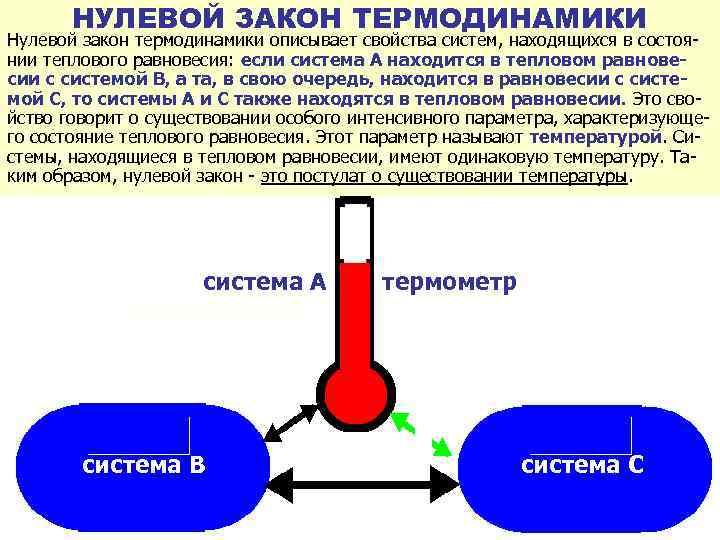
НУЛЕВОЙ ЗАКОН ТЕРМОДИНАМИКИ Нулевой закон термодинамики описывает свойства систем, находящихся в состоянии теплового равновесия: если система А находится в тепловом равновесии с системой В, а та, в свою очередь, находится в равновесии с системой С, то системы А и С также находятся в тепловом равновесии. Это свойство говорит о существовании особого интенсивного параметра, характеризующего состояние теплового равновесия. Этот параметр называют температурой. Системы, находящиеся в тепловом равновесии, имеют одинаковую температуру. Таким образом, нулевой закон - это постулат о существовании температуры. система А термометр система В система С
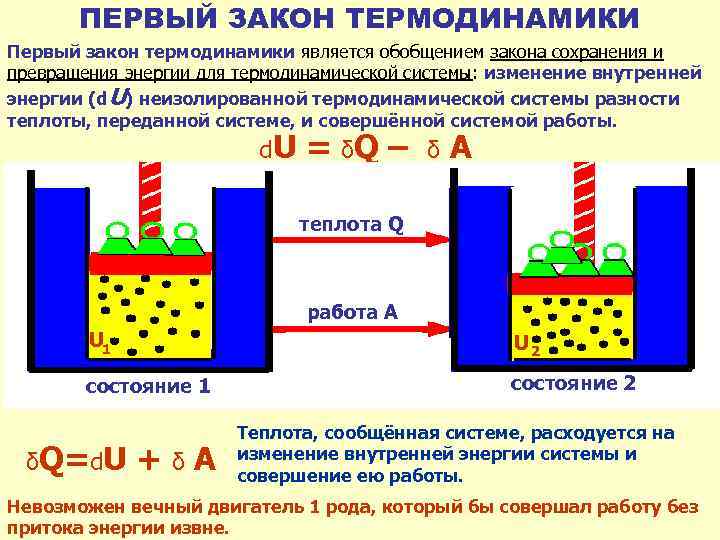
ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ Первый закон термодинамики является обобщением закона сохранения и превращения энергии для термодинамической системы: изменение внутренней энергии (d. U) неизолированной термодинамической системы разности теплоты, переданной системе, и совершённой системой работы. d. U = δQ – δ A теплота Q работа А U 1 U 2 состояние 1 состояние 2 δQ=d. U + δ A Теплота, сообщённая системе, расходуется на изменение внутренней энергии системы и совершение ею работы. Невозможен вечный двигатель 1 рода, который бы совершал работу без притока энергии извне.
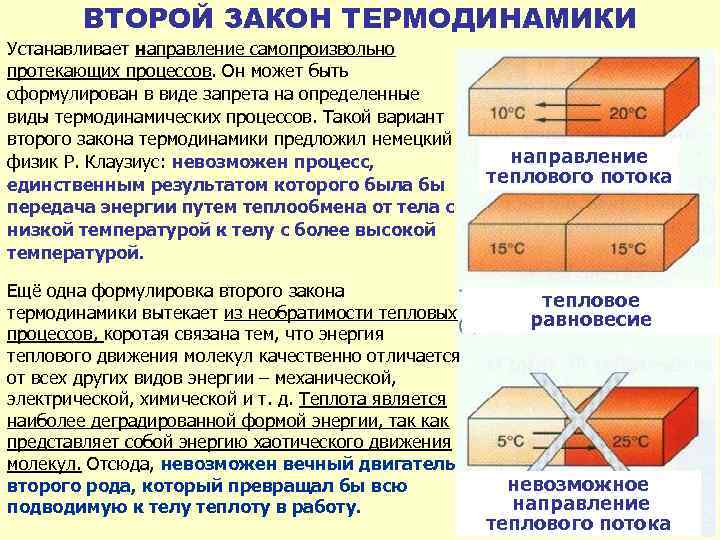
ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ Устанавливает направление самопроизвольно протекающих процессов. Он может быть сформулирован в виде запрета на определенные виды термодинамических процессов. Такой вариант второго закона термодинамики предложил немецкий физик Р. Клаузиус: невозможен процесс, единственным результатом которого была бы передача энергии путем теплообмена от тела с низкой температурой к телу с более высокой температурой. Ещё одна формулировка второго закона термодинамики вытекает из необратимости тепловых процессов, коротая связана тем, что энергия теплового движения молекул качественно отличается от всех других видов энергии – механической, электрической, химической и т. д. Теплота является наиболее деградированной формой энергии, так как представляет собой энергию хаотического движения молекул. Отсюда, невозможен вечный двигатель второго рода, который превращал бы всю подводимую к телу теплоту в работу. направление теплового потока тепловое равновесие невозможное направление теплового потока
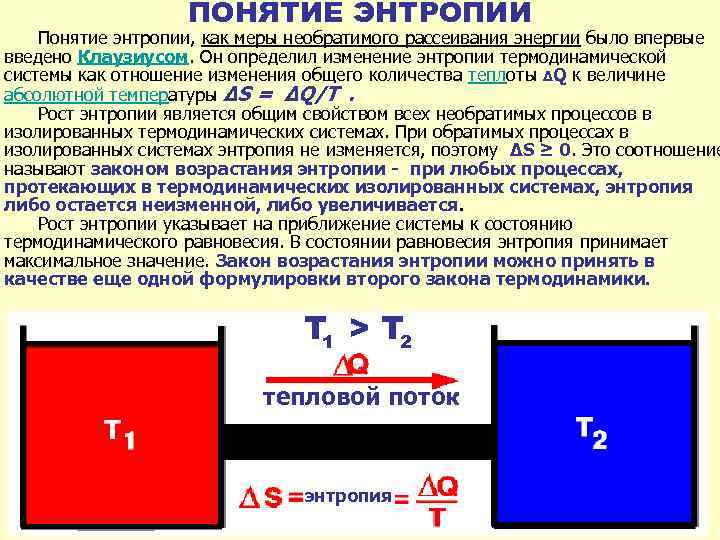
ПОНЯТИЕ ЭНТРОПИИ Понятие энтропии, как меры необратимого рассеивания энергии было впервые введено Клаузиусом. Он определил изменение энтропии термодинамической системы как отношение изменения общего количества теплоты ΔQ к величине абсолютной температуры ΔS = ΔQ/T . Рост энтропии является общим свойством всех необратимых процессов в изолированных термодинамических системах. При обратимых процессах в изолированных системах энтропия не изменяется, поэтому ΔS ≥ 0. Это соотношение называют законом возрастания энтропии - при любых процессах, протекающих в термодинамических изолированных системах, энтропия либо остается неизменной, либо увеличивается. Рост энтропии указывает на приближение системы к состоянию термодинамического равновесия. В состоянии равновесия энтропия принимает максимальное значение. Закон возрастания энтропии можно принять в качестве еще одной формулировки второго закона термодинамики. T 1 > T 2 тепловой поток энтропия
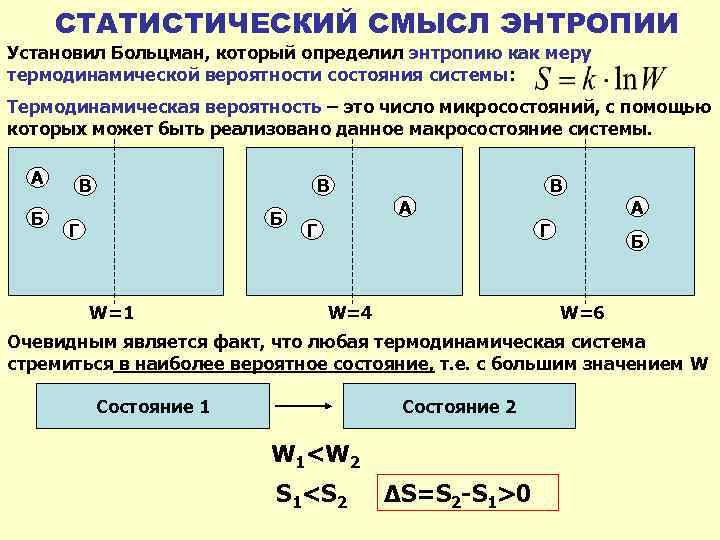
СТАТИСТИЧЕСКИЙ СМЫСЛ ЭНТРОПИИ Установил Больцман, который определил энтропию как меру термодинамической вероятности состояния системы: Термодинамическая вероятность – это число микросостояний, с помощью которых может быть реализовано данное макросостояние системы. А Б В В Б Г W=1 А Г В Г W=4 А Б W=6 Очевидным является факт, что любая термодинамическая система стремиться в наиболее вероятное состояние, т. е. с большим значением W Состояние 1 Состояние 2 W 1<W 2 S 1<S 2 ΔS=S 2 -S 1>0

КАЧЕСТВО ФОРМ ЭНЕРГИИ - Энергия высшего качества (класс А)– гравитационная, ядерная, световая, электрическая – обладают наименьшей энтропией и наиболее эффективно преобразуются в другие формы энергии и в работу. - Энергия класса Б – химическая. - Энергия класса С – тепловая – имеет наибольшую энтропию и наименее эффективно преобразуется в другие формы энергии и в работу. «В гигантской фабрике природных процессов энтропия занимает место директора, который определяет характер и способ ведения всех сделок, тогда как закон сохранения энергии – только бухгалтер, который приводит в равновесие дебет и кредит» Р. Эмден.

ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ характеризуют способность тела совершать работу в тех или иных условиях (при постоянстве определённой пары параметров) и являются вторым критерием самопроизвольного протекания процессов. V, S P, S V, T P, T Внутренняя энергия d. U Энтальпия (теплосодержание) Свободная энергия Гельмгольца Свободная энергия Гиббса d. H=d. U+pd. V d. F=d. U-Td. S d. G=d. U+pd. V-Td. S Электрохимический потенциал концентрация стандартный электрохимический потенциал универсальная газовая постоянная термодинамическая температура заряд число Фарадея электрический потенциал В самопроизвольных процессах термодинамические потенциалы уменьшаются!!!
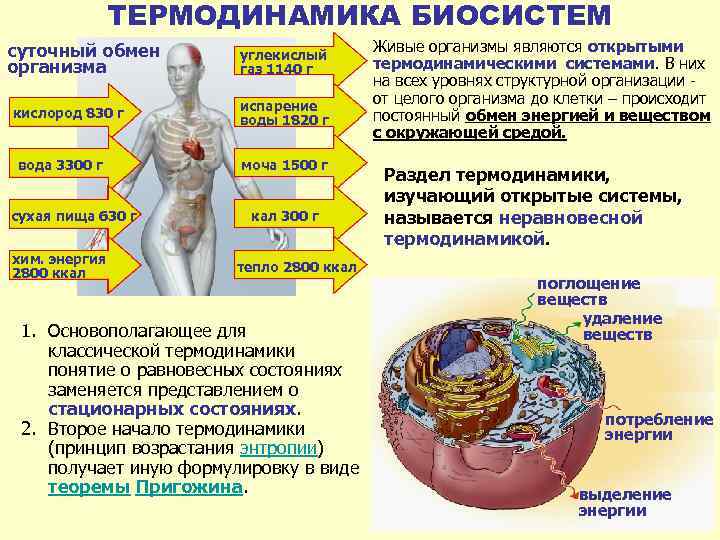
ТЕРМОДИНАМИКА БИОСИСТЕМ суточный обмен организма кислород 830 г вода 3300 г сухая пища 630 г хим. энергия 2800 ккал углекислый газ 1140 г испарение воды 1820 г моча 1500 г кал 300 г тепло 2800 ккал 1. Основополагающее для классической термодинамики понятие о равновесных состояниях заменяется представлением о стационарных состояниях. 2. Второе начало термодинамики (принцип возрастания энтропии) получает иную формулировку в виде теоремы Пригожина. Живые организмы являются открытыми термодинамическими системами. В них на всех уровнях структурной организации - от целого организма до клетки – происходит постоянный обмен энергией и веществом с окружающей средой. Раздел термодинамики, изучающий открытые системы, называется неравновесной термодинамикой. поглощение веществ удаление веществ потребление энергии выделение энергии

СТАЦИОНАРНОЕ СОСТОЯНИЕ Взрослые живые организмы, находящиеся в нормальных условиях, то есть в отсутствие резких изменений внешних (например, атмосферных) или внутренних (например, болезнь) параметров, находятся в стационарном состоянии. Общее между равновесным и стационарным состояниями – устойчивость во времени. Отличия стационарного состояния от равновесного: 1. В разных частях системы могут отличаться значения интенсивных параметров, т. е. существуют градиенты. 2. Осуществляются различные термодинамические потоки. 3. Энтропия имеет определённое, но не максимальное значение. 4. Термодинамические потенциалы поддерживаются на постоянном, но не минимальном уровне.

УРАВНЕНИЕ ПРИГОЖИНА состоит в том, что общее изменение энтропии d. S открытой системы происходит за счет процессов обмена с внешней средой (d. Se ) и за счёт внутренних необратимых процессов (d. Sі ): d. S = d. Se + d. Sі Член d. Si - всегда положителен, а член d. Se - отрицателен, сумма d. S может иметь любой знак. В стационарном состоянии d. S = 0, т. е. нарастание энтропии уравновешено её удалением. Случай d. S < 0 отвечает кажущемуся нарушению принципов термодинамики. Однако, если учесть, что в окружающей среде происходит рост энтропии за счет продуктов выделения, то общая энтропия в системе «организм – среда» повышается, что находится в полном соответствии с законами термодинамики. поглощение и аккумуляция энергии - уменьшение энтропии необратимое использование энергии увеличение энтропии выделение тепла и продуктов обмена – рост энтропии в среде открытая термодинамическая система

ТЕОРЕМА ПРИГОЖИНА Теорема Пригожина: при неизменных внешних условиях открытая термодинамическая система стремится к такому стационарному состоянию, которое характеризуется минимальным производством энтропии. Если же внешние условия меняются, то организм вынужден так модифицировать происходящие в нем процессы, чтобы перейти к новому стационарному состоянию. Неспособность организма восстанавливать свое стационарное состояние приводит к его гибели. при развитии заболеваний характеризует процессы роста и развития Благодаря стационарному состоянию за счёт непрерывного обмена энергией и веществом с внешней средой биосистемы не только находятся на удалении от термодинамического равновесия и сохраняют свою работоспособность, но и поддерживают во времени постоянство своих параметров, которое носит название гомеостаз.
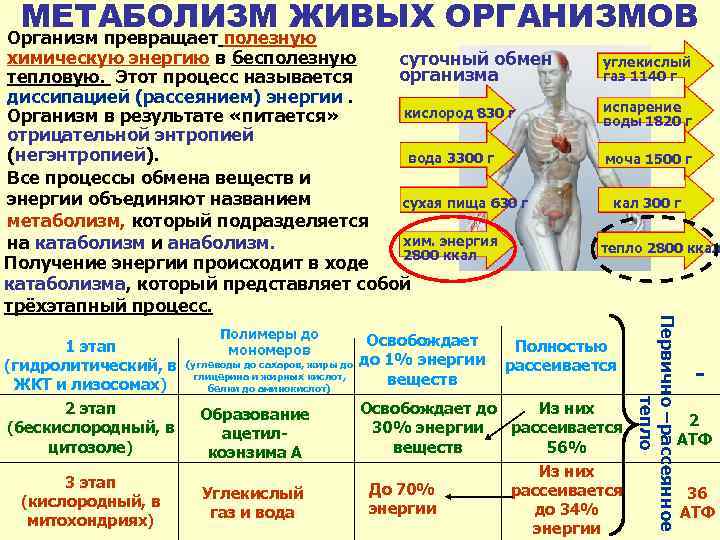
МЕТАБОЛИЗМ ЖИВЫХ ОРГАНИЗМОВ углекислый газ 1140 г испарение воды 1820 г моча 1500 г кал 300 г тепло 2800 ккал Полимеры до Освобождает 1 этап Полностью мономеров (гидролитический, в (углеводы до сахаров, жиры до до 1% энергии рассеивается глицерина и жирных кислот, веществ ЖКТ и лизосомах) белки до аминокислот) Освобождает до Из них 2 этап Образование 30% энергии рассеивается (бескислородный, в ацетилвеществ 56% цитозоле) коэнзима А Из них 3 этап До 70% рассеивается Углекислый (кислородный, в энергии до 34% газ и вода митохондриях) энергии Первично –рассеянное тепло Организм превращает полезную химическую энергию в бесполезную суточный обмен организма тепловую. Этот процесс называется диссипацией (рассеянием) энергии. кислород 830 г Организм в результате «питается» отрицательной энтропией (негэнтропией). вода 3300 г Все процессы обмена веществ и энергии объединяют названием сухая пища 630 г метаболизм, который подразделяется хим. энергия на катаболизм и анаболизм. 2800 ккал Получение энергии происходит в ходе катаболизма, который представляет собой трёхэтапный процесс. - 2 АТФ 36 АТФ

ЭНЕРГЕТИКА КЛЕТКИ МИТОХОНДРИЯ внутренняя мембрана внешняя мембрана криста матрикс Клетка получает энергию, в основном, при окислении глюкозы (мономер углеводов) и жирных кислот (мономеры жиров). Этот процесс проходит в митохондриях. Каждая клетка содержит от 50 до 5000 митохондрий и синтезирует АТФ только для себя! Часть энергии окисления запасается в форме АТФ - аденозинтрифосфорной кислоты (АТФ) - универсального, но не единственного источника энергии для всех видов биологической работы. Энерготраты человека за сутки покрываются пищей, в которой содержится примерно полкилограмма глюкозы. Из каждой молекулы глюкозы образуется 38 молекул АТФ, поэтому за сутки в теле человека образуется и вновь расщепляется более 50 кг АТФ. Более эффективным является использование жиров. Сначала они при участии ферментов гидролизуются до глицерина и жирных кислот. Окисление одной молекулы глицерина даёт в общем итоге всего 19 молекул АТФ, а окисление, к примеру, стеариновой кислоты – целых 147 молекул. Белки практически не используются для получения энергии!
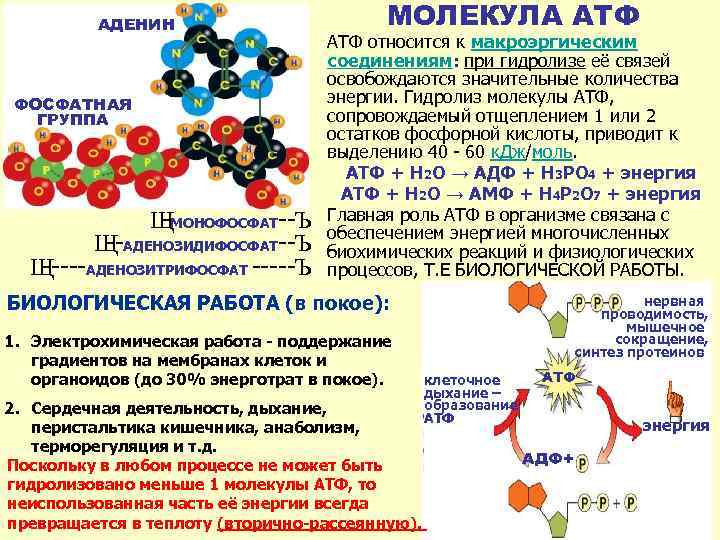
АДЕНИН ФОСФАТНАЯ ГРУППА ЩМОНОФОСФАТ--Ъ Щ АДЕНОЗИДИФОСФАТ--Ъ -Щ АДЕНОЗИТРИФОСФАТ -----Ъ ----- МОЛЕКУЛА АТФ относится к макроэргическим соединениям: при гидролизе её связей освобождаются значительные количества энергии. Гидролиз молекулы АТФ, сопровождаемый отщеплением 1 или 2 остатков фосфорной кислоты, приводит к выделению 40 - 60 к. Дж/моль. АТФ + H 2 O → AДФ + H 3 PO 4 + энергия АТФ + H 2 O → AМФ + H 4 P 2 O 7 + энергия Главная роль АТФ в организме связана с обеспечением энергией многочисленных биохимических реакций и физиологических процессов, Т. Е БИОЛОГИЧЕСКОЙ РАБОТЫ. БИОЛОГИЧЕСКАЯ РАБОТА (в покое): 1. Электрохимическая работа - поддержание градиентов на мембранах клеток и органоидов (до 30% энерготрат в покое). нервная проводимость, мышечное сокращение, синтез протеинов клеточное дыхание – образование АТФ 2. Сердечная деятельность, дыхание, перистальтика кишечника, анаболизм, терморегуляция и т. д. Поскольку в любом процессе не может быть гидролизовано меньше 1 молекулы АТФ, то неиспользованная часть её энергии всегда превращается в теплоту (вторично-рассеянную). АТФ энергия АДФ+

БИОКАЛОРИМЕТРИЯ. ОСНОВНОЙ ОБМЕН. Выделение в ходе метаболизма теплоты имеет большое значение для организма – оно служит для обогревания тела. Выделенная теплота может быть измерена для анализа энергетических трат организма и эффективности процессов жизнедеятельности. Подавляющее число заболеваний снижает КПД органов и тканей, что приводит к увеличению выделения теплоты. Биокалориметрия – методы измерения теплоты, которую выделяет организм в процессе жизнедеятельности. Основной обмен – это лабораторный показатель, который характеризует базовые энерготраты организма в определённых стандартных условиях, приближённых к наиболее экономичному режиму жизнедеятельности. Основной обмен (1785 ккал/сутки для мужчин, 1679 В других условиях (при достаточно высокой ккал/сутки для женщин) определяют: мышечной нагрузке) 1. В состоянии полного мышечного и психического дополнительно спокойствия. расходуется столько же 2. Натощак (через 12 -18 часов после принятия пищи). энергии, сколько составляет основной 3. В горизонтальном положении. обмен. Т. е. с точки 4. При температуре комфорта (18 -21 градус, если зрения термодинамики, человек одет). жить – уже значит 5. Определяют за час и экстраполируют на сутки. работать.
Эргометрия – измерение и расчёт энерготрат организма с учётом вида выполняемой нагрузки. Энерготраты должны покрываться поступлением энергии с пищей. На основе эргометрических измерений составляют правильный пищевой рацион и подбирают оптимальную физическую нагрузку. Установлено, что мозг окисляет одно и то же количества глюкозы как в покое, так и при крайнем умственном напряжении (около 5 г в час). Это происходит не потому, что он экономный при нагрузке, а потому, что он расточительный в покое. 80% энергии мозг тратит на поддержание фоновой электрической активности – «готовности действовать» .

ГОМОЙОТЕРМИЯ В теле человека за один час образуется столько тепла, сколько нужно, чтобы вскипятить 1 л ледяной воды. Если бы тело вместо кожи было покрыто непроницаемым для тепла футляром, то уже через час температура тела поднялась бы примерно на 1, 5°, а через сорок часов - достигла бы точки кипения воды. Во время тяжёлой физической конвекция работы образование тепла увеличивается еще в несколько раз. Но температура тела не меняется: у здорового человека она обычно равна 36, 5— 37°. Такое постоянство температуры тела испарение поддерживается почти исключительно я путём регуляции отдачи тепла через ци иа д кожу. В ней находятся терморецепторы, ра которые сигнализируют о температуре окружающей среды в спинной мозг и ия ц гипоталамус. Нервные структуры иа управляют диаметром сосудов в коже и ад р другими реакциями. Теплоотдача происходит путем излучения (55%), испарения (5% из теплопродыхательных путей и 20% с поверхности водность кожи), теплопроводности (15%) и конвекции (5%).

термодинамика.ppt