лекция 3 НХ ОВР,рус.ppt
- Количество слайдов: 29
 Лекция № 3 Тема: ОКИСЛИТЕЛЬНОВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
Лекция № 3 Тема: ОКИСЛИТЕЛЬНОВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
 • Степень окисления - это условный заряд атома в молекуле, вычисленный в предположении, что молекула состоит из ионов и в целом электронейтральна. • Наиболее электроотрицательные элементы в соединении имеют отрицательные степени окисления, а атомы элементов с меньшей электроотрицательностью - положительные. • Степень окисления - формальное понятие; в ряде случаев степень окисления не совпадает с валентностью. • Например: • N 2 H 4 (гидразин), степень окисления азота -2; валентность азота 3.
• Степень окисления - это условный заряд атома в молекуле, вычисленный в предположении, что молекула состоит из ионов и в целом электронейтральна. • Наиболее электроотрицательные элементы в соединении имеют отрицательные степени окисления, а атомы элементов с меньшей электроотрицательностью - положительные. • Степень окисления - формальное понятие; в ряде случаев степень окисления не совпадает с валентностью. • Например: • N 2 H 4 (гидразин), степень окисления азота -2; валентность азота 3.
 • Расчет степени окисления. Для вычисления степени окисления элемента следует учитывать следующие положения: • 1. Степени окисления атомов в простых веществах равны нулю (Na 0; H 20). • 2. Алгебраическая сумма степеней окисления всех атомов, входящих в состав молекулы, всегда равна нулю, а в сложном ионе эта сумма равна заряду иона. • 3. Постоянную степень окисления имеют атомы: щелочных металлов (+1), щелочноземельных металлов (+2), водорода (+1) (кроме гидридов Na. H, Ca. H 2 и др. , где степень окисления водорода -1), кислорода (-2) (кроме ОF 2 (+2) и пероксидов, содержащих группу –O–O–, в которой степень окисления кислорода -1). • 4. Для элементов положительная степень окисления не может превышать величину, равную номеру группы периодической системы.
• Расчет степени окисления. Для вычисления степени окисления элемента следует учитывать следующие положения: • 1. Степени окисления атомов в простых веществах равны нулю (Na 0; H 20). • 2. Алгебраическая сумма степеней окисления всех атомов, входящих в состав молекулы, всегда равна нулю, а в сложном ионе эта сумма равна заряду иона. • 3. Постоянную степень окисления имеют атомы: щелочных металлов (+1), щелочноземельных металлов (+2), водорода (+1) (кроме гидридов Na. H, Ca. H 2 и др. , где степень окисления водорода -1), кислорода (-2) (кроме ОF 2 (+2) и пероксидов, содержащих группу –O–O–, в которой степень окисления кислорода -1). • 4. Для элементов положительная степень окисления не может превышать величину, равную номеру группы периодической системы.
 • Существует два типа химических реакций: • 1. Реакции, идущие без изменения степени окисления элементов: • Реакции присоединения: SO 2 + Na 2 O = Na 2 SO 3 • Реакции разложения: Cu(OH)2 = Cu. O + H 2 O • Реакции обмена: Ag. NO 3 + KCl = Ag. Cl↓ + KNO 3 Na. OH + HNO 3 = Na. NO 3 + H 2 O
• Существует два типа химических реакций: • 1. Реакции, идущие без изменения степени окисления элементов: • Реакции присоединения: SO 2 + Na 2 O = Na 2 SO 3 • Реакции разложения: Cu(OH)2 = Cu. O + H 2 O • Реакции обмена: Ag. NO 3 + KCl = Ag. Cl↓ + KNO 3 Na. OH + HNO 3 = Na. NO 3 + H 2 O
 • 2. Реакции, идущие с изменением степеней окисления атомов элементов, входящих в состав реагирующих соединений: • 2 Mg 0 + O 20 = 2 Mg. O-2 • 2 KCl. O 3 = 2 KCl-1 + 3 O 20 • 2 KI-1 + Cl 20 = 2 KCl-1 + I 20 • Mn. O 2 + 4 HCl-1 = Mn. Cl 2 + Cl 20 + 2 H 2 O • Такие реакции называются окислительно восстановительными. • В окислительно-восстановительных реакциях электроны от одних атомов, молекул или ионов переходят к другим.
• 2. Реакции, идущие с изменением степеней окисления атомов элементов, входящих в состав реагирующих соединений: • 2 Mg 0 + O 20 = 2 Mg. O-2 • 2 KCl. O 3 = 2 KCl-1 + 3 O 20 • 2 KI-1 + Cl 20 = 2 KCl-1 + I 20 • Mn. O 2 + 4 HCl-1 = Mn. Cl 2 + Cl 20 + 2 H 2 O • Такие реакции называются окислительно восстановительными. • В окислительно-восстановительных реакциях электроны от одних атомов, молекул или ионов переходят к другим.
 Процесс отдачи электронов - окисление. При окислении степень окисления повышается : H 20 - 2ē → 2 H+ S-2 - 2ē → S 0 Al 0 – 3ē → Al+3 Процесс присоединения электронов восстановление. При восстановлении степень окисления понижается: Mn+4 + 2ē → Mn+2 S 0 + 2ē → S-2 Cr+6 +3ē → Cr+3 Атомы или ионы, которые в данной реакции присоединяют электроны являются окислителями, а которые отдают электроны - восстановителями.
Процесс отдачи электронов - окисление. При окислении степень окисления повышается : H 20 - 2ē → 2 H+ S-2 - 2ē → S 0 Al 0 – 3ē → Al+3 Процесс присоединения электронов восстановление. При восстановлении степень окисления понижается: Mn+4 + 2ē → Mn+2 S 0 + 2ē → S-2 Cr+6 +3ē → Cr+3 Атомы или ионы, которые в данной реакции присоединяют электроны являются окислителями, а которые отдают электроны - восстановителями.
 Максимальная степень окисления атома элемента равна номеру группы в периодической таблице, к которой относится данный элемент. Минимальная степень окисления у атомов металлов равна 0, для неметаллов - (n– 8) где n- номер группы в периодической системе). Соединения, содержащие атомы элементов с промежуточной степенью окисления, могут быть и окислителями и восстановителями, в зависимости от партнера, с которым взаимодействуют и от условий реакции.
Максимальная степень окисления атома элемента равна номеру группы в периодической таблице, к которой относится данный элемент. Минимальная степень окисления у атомов металлов равна 0, для неметаллов - (n– 8) где n- номер группы в периодической системе). Соединения, содержащие атомы элементов с промежуточной степенью окисления, могут быть и окислителями и восстановителями, в зависимости от партнера, с которым взаимодействуют и от условий реакции.
 Восстановители: металлы, водород, уголь. Оксид углерода (II) (CO). Сероводород (H 2 S); оксид серы (IV) (SO 2); сернистая кислота H 2 SO 3 и ее соли. Галогеноводородные кислоты и их соли. Катионы металлов в низших степенях окисления: Sn. Cl 2, Fe. Cl 2, Mn. SO 4, Cr 2(SO 4)3. Азотистая кислота HNO 2; аммиак NH 3; гидразин N 2 H 4; оксид азота(II) (NO). Катод при электролизе. Окислители: Галогены. Перманганат калия(KМn. O 4); манганат калия (K 2 Mn. O 4); оксид марганца (IV) (Mn. O 2). Дихромат калия (K 2 Cr 2 O 7); хромат калия (K 2 Cr. O 4). Азотная кислота (HNO 3). Серная кислота (H 2 SO 4) конц. Оксид меди(II) (Cu. O); оксид свинца(IV) (Pb. O 2); оксид серебра (Ag 2 O); пероксид водорода (H 2 O 2). Хлорид железа(III) (Fe. Cl 3). Бертолетова соль (KСl. O 3). Анод при электролизе.
Восстановители: металлы, водород, уголь. Оксид углерода (II) (CO). Сероводород (H 2 S); оксид серы (IV) (SO 2); сернистая кислота H 2 SO 3 и ее соли. Галогеноводородные кислоты и их соли. Катионы металлов в низших степенях окисления: Sn. Cl 2, Fe. Cl 2, Mn. SO 4, Cr 2(SO 4)3. Азотистая кислота HNO 2; аммиак NH 3; гидразин N 2 H 4; оксид азота(II) (NO). Катод при электролизе. Окислители: Галогены. Перманганат калия(KМn. O 4); манганат калия (K 2 Mn. O 4); оксид марганца (IV) (Mn. O 2). Дихромат калия (K 2 Cr 2 O 7); хромат калия (K 2 Cr. O 4). Азотная кислота (HNO 3). Серная кислота (H 2 SO 4) конц. Оксид меди(II) (Cu. O); оксид свинца(IV) (Pb. O 2); оксид серебра (Ag 2 O); пероксид водорода (H 2 O 2). Хлорид железа(III) (Fe. Cl 3). Бертолетова соль (KСl. O 3). Анод при электролизе.








 • При составлении уравнений реакций методом ионнно-электронного баланса необходимо соблюдать : • 1. Правило избытка кислорода : Избыток кислорода в левой части полуреакции связывается в кислой среде ионами водорода (Н+) в воду, а в нейтральной и щелочной средах- водой в гидроксид ионы ( ОН-)
• При составлении уравнений реакций методом ионнно-электронного баланса необходимо соблюдать : • 1. Правило избытка кислорода : Избыток кислорода в левой части полуреакции связывается в кислой среде ионами водорода (Н+) в воду, а в нейтральной и щелочной средах- водой в гидроксид ионы ( ОН-)
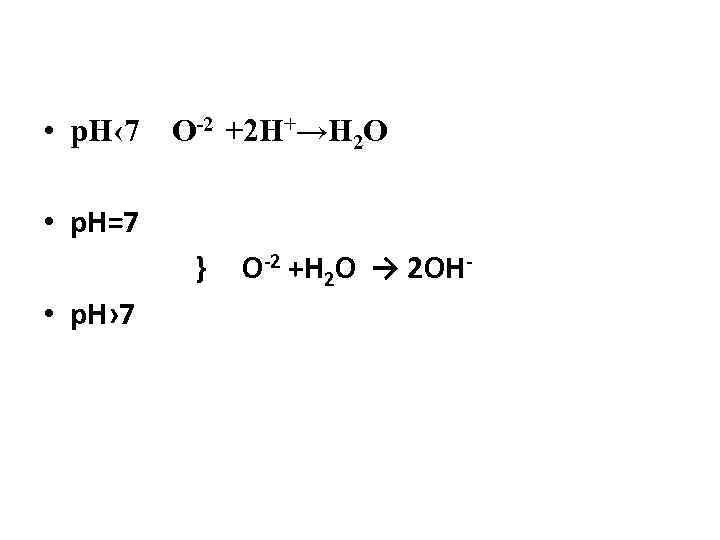 • р. Н‹ 7 О-2 +2 Н+→Н 2 О • р. Н=7 } • р. Н› 7 О-2 +Н 2 О → 2 ОН-
• р. Н‹ 7 О-2 +2 Н+→Н 2 О • р. Н=7 } • р. Н› 7 О-2 +Н 2 О → 2 ОН-
 • 2) Правило недостатка кислорода : Недостаток кислорода в левой части полуреакции восполняется в кислой и нейтральной средах водой, а в щелочной среде -гидроксид ионами ОНр. Н=7 } Н 2 О = О-2 + 2 Н+ р. Н‹ 7 р. Н› 7 2 ОН-= О-2 +Н 2 О
• 2) Правило недостатка кислорода : Недостаток кислорода в левой части полуреакции восполняется в кислой и нейтральной средах водой, а в щелочной среде -гидроксид ионами ОНр. Н=7 } Н 2 О = О-2 + 2 Н+ р. Н‹ 7 р. Н› 7 2 ОН-= О-2 +Н 2 О
 • Молярная масса эквивалента окислителя(Ох) определяется по формуле: Мэох(х) = fэох∙ M(х) где M(х)- молярная масса вещества, г/моль; fэох- фактор эквивалентости окислителя, определяется числом электронов, которое может принимать окислитель в окислительно- восстановительных реакциях
• Молярная масса эквивалента окислителя(Ох) определяется по формуле: Мэох(х) = fэох∙ M(х) где M(х)- молярная масса вещества, г/моль; fэох- фактор эквивалентости окислителя, определяется числом электронов, которое может принимать окислитель в окислительно- восстановительных реакциях
 • Молярная масса эквивалента восстановителя (Red) определяется по формуле: М э Red (х)= fэ Red∙М(х) где M(х)- молярная масса вещества, г/моль; fэ Red - фактор эквивалентости восстановителя, определяется числом электронов, которое может отдавать восстановитель в окислительновосстановительных реакции
• Молярная масса эквивалента восстановителя (Red) определяется по формуле: М э Red (х)= fэ Red∙М(х) где M(х)- молярная масса вещества, г/моль; fэ Red - фактор эквивалентости восстановителя, определяется числом электронов, которое может отдавать восстановитель в окислительновосстановительных реакции
 • Электролиз • При электролизе происходит превращение электрической энергии в химическую. Электрод, на котором идет реакция восстановления (катод), подключен к отрицательному полюсу внешнего источника тока. Электрод, на котором протекает реакция окисления (анод), подключен к положительному полюсу источника тока. • Катодная и анодная полуреакции характеризуются стандартным окислительно-восстановительным потенциалом Е 0, (размерность - вольт, В). Чем больше Е 0, тем сильнее окислительная форма как окислитель и тем слабее восстановленная форма как восстановитель, и наоборот. • За точку отсчета потенциалов принята полуреакция: 2 H+ + 2ē → H 2, для которой Е 0 = 0. • Для полуреакций Mn+ + nē → Mn 0, Е 0 называется стандартным электродным потенциалом. По величине этого потенциала металлы принято располагать в ряд стандартных электродных потенциалов (ряд напряжений металлов): • Li, K, Ba, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Co, Ni, Sn, Pb, H , Sb, Bi, Cu, Hg, Ag, Pt, Au
• Электролиз • При электролизе происходит превращение электрической энергии в химическую. Электрод, на котором идет реакция восстановления (катод), подключен к отрицательному полюсу внешнего источника тока. Электрод, на котором протекает реакция окисления (анод), подключен к положительному полюсу источника тока. • Катодная и анодная полуреакции характеризуются стандартным окислительно-восстановительным потенциалом Е 0, (размерность - вольт, В). Чем больше Е 0, тем сильнее окислительная форма как окислитель и тем слабее восстановленная форма как восстановитель, и наоборот. • За точку отсчета потенциалов принята полуреакция: 2 H+ + 2ē → H 2, для которой Е 0 = 0. • Для полуреакций Mn+ + nē → Mn 0, Е 0 называется стандартным электродным потенциалом. По величине этого потенциала металлы принято располагать в ряд стандартных электродных потенциалов (ряд напряжений металлов): • Li, K, Ba, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Co, Ni, Sn, Pb, H , Sb, Bi, Cu, Hg, Ag, Pt, Au
 Ряд напряжений характеризует химические свойства металлов: • 1. Чем левее расположен металл в ряду напряжений, тем сильнее его восстановительная способность и тем слабее окислительная способность его иона в растворе (т. е. тем легче он отдает электроны (окисляется) и тем труднее его ионы присоединяют обратно электроны). • 2. Каждый металл способен вытеснять из растворов солей те металлы, которые стоят в ряду напряжений правее его, т. е. восстанавливает ионы последующих металлов в электронейтральные атомы, отдавая электроны и сам превращаясь в ионы. • 3. Только металлы, стоящие в ряду напряжений левее водорода (Н), способны вытеснять его из растворов кислот (например, Zn, Fe, Pb, но не Сu, Hg, Ag).
Ряд напряжений характеризует химические свойства металлов: • 1. Чем левее расположен металл в ряду напряжений, тем сильнее его восстановительная способность и тем слабее окислительная способность его иона в растворе (т. е. тем легче он отдает электроны (окисляется) и тем труднее его ионы присоединяют обратно электроны). • 2. Каждый металл способен вытеснять из растворов солей те металлы, которые стоят в ряду напряжений правее его, т. е. восстанавливает ионы последующих металлов в электронейтральные атомы, отдавая электроны и сам превращаясь в ионы. • 3. Только металлы, стоящие в ряду напряжений левее водорода (Н), способны вытеснять его из растворов кислот (например, Zn, Fe, Pb, но не Сu, Hg, Ag).
 • Электролизом называется процесс разложения вещества электрическим током. Сущность электролиза заключается в том, что при пропускании тока через раствор электролита (или расплавленный электролит) положительно заряженные ионы перемещаются к катоду, а отрицательно заряженные – к аноду. • Достигнув электродов, ионы разряжаются, в результате чего у электродов выделяются составные части растворенного электролита или водород и кислород из воды. • Чем левее стоит металл в ряду напряжений, чем больше его отрицательный потенциал (или меньше положительный потенциал), тем труднее при прочих равных условиях разряжаются его ионы (легче всего разряжаются ионы Аu 3+, Ag+; труднее всего Li+, Rb+, K+).
• Электролизом называется процесс разложения вещества электрическим током. Сущность электролиза заключается в том, что при пропускании тока через раствор электролита (или расплавленный электролит) положительно заряженные ионы перемещаются к катоду, а отрицательно заряженные – к аноду. • Достигнув электродов, ионы разряжаются, в результате чего у электродов выделяются составные части растворенного электролита или водород и кислород из воды. • Чем левее стоит металл в ряду напряжений, чем больше его отрицательный потенциал (или меньше положительный потенциал), тем труднее при прочих равных условиях разряжаются его ионы (легче всего разряжаются ионы Аu 3+, Ag+; труднее всего Li+, Rb+, K+).
 • Электролиз раствора хлорида никеля Ni. Cl 2 • Раствор содержит ионы Ni 2+ и Cl-, а также в ничтожной концентрации ионы Н+ и ОН-. При пропускании тока ионы Ni 2+ перемещаются к катоду, а ионы Cl- – к аноду. Принимая от катода по два электрона, ионы Ni 2+ превращаются в нейтральные атомы, выделяющиеся из раствора. Катод постепенно покрывается никелем. Ионы хлора, достигая анода, отдают ему электроны и превращаются в атомы хлора, которые, соединяясь попарно, образуют молекулы хлора. У анода выделяется хлор. • Таким образом, у катода происходит процесс восстановления, у анода – процесс окисления. К(-): Ni 2+ + 2ē → Ni 0 A(+) : 2 Cl- - 2ē → Cl 20↑
• Электролиз раствора хлорида никеля Ni. Cl 2 • Раствор содержит ионы Ni 2+ и Cl-, а также в ничтожной концентрации ионы Н+ и ОН-. При пропускании тока ионы Ni 2+ перемещаются к катоду, а ионы Cl- – к аноду. Принимая от катода по два электрона, ионы Ni 2+ превращаются в нейтральные атомы, выделяющиеся из раствора. Катод постепенно покрывается никелем. Ионы хлора, достигая анода, отдают ему электроны и превращаются в атомы хлора, которые, соединяясь попарно, образуют молекулы хлора. У анода выделяется хлор. • Таким образом, у катода происходит процесс восстановления, у анода – процесс окисления. К(-): Ni 2+ + 2ē → Ni 0 A(+) : 2 Cl- - 2ē → Cl 20↑
 • Для количественной характеристики процессов электролиза, протекающих на электродах, применяются законы Фарадея: • 1. Весовое количество выделяемого при электролизе вещества пропорционально количеству протекшего через раствор электричества и практически не зависит от других факторов. • 2. Равные количества электричества выделяют при электролизе из различных химических соединений эквивалентные количества веществ. • 3. Для выделения из раствора электролита одного граммэквивалента любого вещества нужно пропустить через раствор 96500 кулонов электричества.
• Для количественной характеристики процессов электролиза, протекающих на электродах, применяются законы Фарадея: • 1. Весовое количество выделяемого при электролизе вещества пропорционально количеству протекшего через раствор электричества и практически не зависит от других факторов. • 2. Равные количества электричества выделяют при электролизе из различных химических соединений эквивалентные количества веществ. • 3. Для выделения из раствора электролита одного граммэквивалента любого вещества нужно пропустить через раствор 96500 кулонов электричества.
 Исходя из этой формулы, можно производить ряд расчетов, связанных с процессом электролиза, например: 1. Вычислять количества веществ, выделяемых или разлагаемых определенным количеством электричества; 2. Находить силу тока по количеству выделившегося вещества и времени, затраченному на его выделение; 3. Устанавливать, сколько времени потребуется для выделения определенного количества вещества при заданной силе тока.
Исходя из этой формулы, можно производить ряд расчетов, связанных с процессом электролиза, например: 1. Вычислять количества веществ, выделяемых или разлагаемых определенным количеством электричества; 2. Находить силу тока по количеству выделившегося вещества и времени, затраченному на его выделение; 3. Устанавливать, сколько времени потребуется для выделения определенного количества вещества при заданной силе тока.
 • Электролиз раствора йодида калия KI Йодид калия находится в растворе в виде ионов К+ и I-. При пропускании тока ионы К+ передвигаются к катоду, ионы I– к аноду. Но так калий стоит в ряду напряжений гораздо левее водорода, то у катода разряжаются не ионы калия, а водородные ионы воды. Образующиеся при этом атомы водорода соединяются в молекулы Н 2, и таким образом у катода выделяется водород. По мере разряда ионов водорода диссоциируют все новые молекулы воды, вследствие чего у катода накапливаются гидроксильные ионы (освобождающиеся из молекулы воды), а также ионы К+, непрерывно перемещающиеся к катоду. Образуется раствор КОН. У анода происходит выделение йода, т. к. ионы Iразряжаются легче, чем гидроксильные ионы воды.
• Электролиз раствора йодида калия KI Йодид калия находится в растворе в виде ионов К+ и I-. При пропускании тока ионы К+ передвигаются к катоду, ионы I– к аноду. Но так калий стоит в ряду напряжений гораздо левее водорода, то у катода разряжаются не ионы калия, а водородные ионы воды. Образующиеся при этом атомы водорода соединяются в молекулы Н 2, и таким образом у катода выделяется водород. По мере разряда ионов водорода диссоциируют все новые молекулы воды, вследствие чего у катода накапливаются гидроксильные ионы (освобождающиеся из молекулы воды), а также ионы К+, непрерывно перемещающиеся к катоду. Образуется раствор КОН. У анода происходит выделение йода, т. к. ионы Iразряжаются легче, чем гидроксильные ионы воды.
 Электролиз раствора сульфата калия K 2 SO 4 • Раствор содержит ионы K+, SO 42 - и ионы Н+ и ОН- из воды. Так как ионы K+ разряжаются труднее, чем ионы Н+, а ионы SO 42 -, чем ионы ОН-, то при пропускании электрического тока у катода будут разряжаться ионы водорода, у анода - гидроксильные группы, то есть фактически будет происходить электролиз воды. В то же время вследствие разряда водородных и гидроксильных ионов воды и непрерывного перемещения ионов K+ к катоду, а ионов SO 42 - к аноду, у катода образуется раствор щелочи (КОН), а у анода – раствор серной кислоты.
Электролиз раствора сульфата калия K 2 SO 4 • Раствор содержит ионы K+, SO 42 - и ионы Н+ и ОН- из воды. Так как ионы K+ разряжаются труднее, чем ионы Н+, а ионы SO 42 -, чем ионы ОН-, то при пропускании электрического тока у катода будут разряжаться ионы водорода, у анода - гидроксильные группы, то есть фактически будет происходить электролиз воды. В то же время вследствие разряда водородных и гидроксильных ионов воды и непрерывного перемещения ионов K+ к катоду, а ионов SO 42 - к аноду, у катода образуется раствор щелочи (КОН), а у анода – раствор серной кислоты.


