03 Лек Алкены.ppt
- Количество слайдов: 40
 Лекция № 3 Тема: «Непредельные углеводороды. Алкены. Олефины. Этиленовые углеводороды)» .
Лекция № 3 Тема: «Непредельные углеводороды. Алкены. Олефины. Этиленовые углеводороды)» .
 План: 1. Общая характеристика алкенов. 2. Гомологический ряд. 3. Номенклатура. 4. Изомерия. 5. Физические свойства. 6. Способы получения. 7. Строение двойной связи. 8. Химические свойства. 9. Применение. 10. Понятие о полимерах.
План: 1. Общая характеристика алкенов. 2. Гомологический ряд. 3. Номенклатура. 4. Изомерия. 5. Физические свойства. 6. Способы получения. 7. Строение двойной связи. 8. Химические свойства. 9. Применение. 10. Понятие о полимерах.
 1. Общая характеристика алкенов. Алкенами называются ненасыщенные углеводороды, молекулы которых содержат одну двойную связь. Общая формула гомологического ряда алкенов Сn. H 2 n. Ненасыщенными (непредельными) их называют потому, что не все валентности атомов углерода насыщены атомами водорода. Для алкенов сохранилось тривиальное название олефины, связанное с тем, что первый представитель – газообразный этилен С 2 Н 4 – при взаимодействии с хлором превращался в тяжёлую маслянистую жидкость состава С 2 Н 4 Cl 2 (1, 2 -дихлорэтан), и, поэтому получил название «маслородный газ» .
1. Общая характеристика алкенов. Алкенами называются ненасыщенные углеводороды, молекулы которых содержат одну двойную связь. Общая формула гомологического ряда алкенов Сn. H 2 n. Ненасыщенными (непредельными) их называют потому, что не все валентности атомов углерода насыщены атомами водорода. Для алкенов сохранилось тривиальное название олефины, связанное с тем, что первый представитель – газообразный этилен С 2 Н 4 – при взаимодействии с хлором превращался в тяжёлую маслянистую жидкость состава С 2 Н 4 Cl 2 (1, 2 -дихлорэтан), и, поэтому получил название «маслородный газ» .
 2. Гомологический ряд Алкены – простейший класс непредельных соединений. У них имеется одна -связь в составе одной двойной связи. Для введения одной -связи требуется удалить из молекулы алкана два атома водорода, то есть общая формула гомологического ряда алкенов должна иметь вид: Сn. H 2 n
2. Гомологический ряд Алкены – простейший класс непредельных соединений. У них имеется одна -связь в составе одной двойной связи. Для введения одной -связи требуется удалить из молекулы алкана два атома водорода, то есть общая формула гомологического ряда алкенов должна иметь вид: Сn. H 2 n
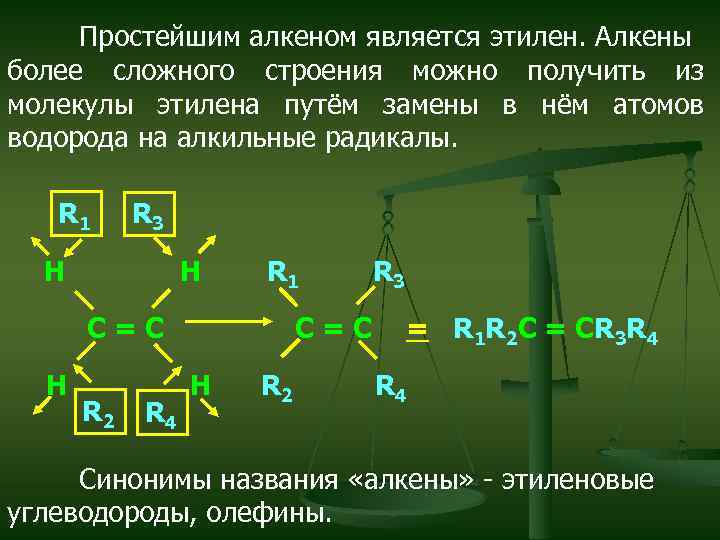 Простейшим алкеном является этилен. Алкены более сложного строения можно получить из молекулы этилена путём замены в нём атомов водорода на алкильные радикалы. R 1 R 3 Н Н R 1 С=С Н R 2 R 4 С=С Н R 2 R 3 = R 1 R 2 С = СR 3 R 4 Синонимы названия «алкены» - этиленовые углеводороды, олефины.
Простейшим алкеном является этилен. Алкены более сложного строения можно получить из молекулы этилена путём замены в нём атомов водорода на алкильные радикалы. R 1 R 3 Н Н R 1 С=С Н R 2 R 4 С=С Н R 2 R 3 = R 1 R 2 С = СR 3 R 4 Синонимы названия «алкены» - этиленовые углеводороды, олефины.
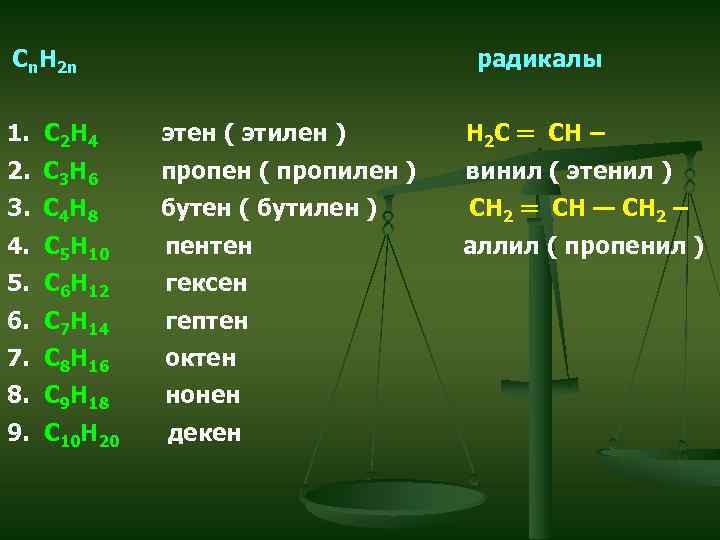 Cn. H 2 n радикалы 1. C 2 H 4 этен ( этилен ) H 2 C ═ CH – 2. C 3 H 6 пропен ( пропилен ) винил ( этенил ) 3. C 4 H 8 бутен ( бутилен ) СH 2 ═ CH — CH 2 – 4. C 5 H 10 пентен аллил ( пропенил ) 5. C 6 H 12 гексен 6. C 7 H 14 гептен 7. C 8 H 16 октен 8. C 9 H 18 нонен 9. C 10 H 20 декен
Cn. H 2 n радикалы 1. C 2 H 4 этен ( этилен ) H 2 C ═ CH – 2. C 3 H 6 пропен ( пропилен ) винил ( этенил ) 3. C 4 H 8 бутен ( бутилен ) СH 2 ═ CH — CH 2 – 4. C 5 H 10 пентен аллил ( пропенил ) 5. C 6 H 12 гексен 6. C 7 H 14 гептен 7. C 8 H 16 октен 8. C 9 H 18 нонен 9. C 10 H 20 декен
 3. Номенклатура алкенов. Названия алкенов с нормальной (неразветвлённой) цепью атомов углеводорода образуются из названий алканов с такой же длиной цепи путём заменив нём окончания –ан на –ен или – илен (только для этилена и пропилена) и с указанием после окончания индекса атома углерода, у которого находится двойная связь. В этилене и пропилене двойная связь всегда находится у первого атома углерода, поэтому индекс опускается. Например: СН 3 – СН 3 этан СН 3 – СН 2 – СН 3 пропан СН 2 = СН 2 этилен СН 2 = СН – СН 3 пропилен или пропен
3. Номенклатура алкенов. Названия алкенов с нормальной (неразветвлённой) цепью атомов углеводорода образуются из названий алканов с такой же длиной цепи путём заменив нём окончания –ан на –ен или – илен (только для этилена и пропилена) и с указанием после окончания индекса атома углерода, у которого находится двойная связь. В этилене и пропилене двойная связь всегда находится у первого атома углерода, поэтому индекс опускается. Например: СН 3 – СН 3 этан СН 3 – СН 2 – СН 3 пропан СН 2 = СН 2 этилен СН 2 = СН – СН 3 пропилен или пропен
 4 3 2 1 СН 3 – СН 2 – СН = СН 2 бутен-1 1 2 3 4 СН 3 – СН = СН – СН 3 бутен-2 Названия разветвлённых алкенов строятся в несколько этапов, аналогично названию алканов. 1. Находят в молекуле родоначальную структуру – самую длинную цепь углеродных атомов, содержащую обязательно двойную связь, и её берут за основу названия. При этом считается, что группы, не вошедшие в основную цепь, являются заместителями атомов водорода при углеродах основной цепи.
4 3 2 1 СН 3 – СН 2 – СН = СН 2 бутен-1 1 2 3 4 СН 3 – СН = СН – СН 3 бутен-2 Названия разветвлённых алкенов строятся в несколько этапов, аналогично названию алканов. 1. Находят в молекуле родоначальную структуру – самую длинную цепь углеродных атомов, содержащую обязательно двойную связь, и её берут за основу названия. При этом считается, что группы, не вошедшие в основную цепь, являются заместителями атомов водорода при углеродах основной цепи.
 2. Нумеруют основную цепь атомов углерода с того конца, чтобы первый атом углерода с двойной связью получил наименьший номер. 3. Строят само название. В префиксе (приставке), аналогично названиям разветвлённых алканов, перечисляют названия всех радикалов-заместителей с указанием перед ними цифровым индексом номера атома углерода основной цепи, к которому присоединён радикал. После префикса без разделения слов приводится в корне название неразветвлённого алкена с таким же количеством атомов углерода и положением двойной связи, как в основной цепи. Например: 5 4 3 2 1 СН 3 – СН 2 – СН = СН – СН 3 пентен-2 (но не пентен-3)
2. Нумеруют основную цепь атомов углерода с того конца, чтобы первый атом углерода с двойной связью получил наименьший номер. 3. Строят само название. В префиксе (приставке), аналогично названиям разветвлённых алканов, перечисляют названия всех радикалов-заместителей с указанием перед ними цифровым индексом номера атома углерода основной цепи, к которому присоединён радикал. После префикса без разделения слов приводится в корне название неразветвлённого алкена с таким же количеством атомов углерода и положением двойной связи, как в основной цепи. Например: 5 4 3 2 1 СН 3 – СН 2 – СН = СН – СН 3 пентен-2 (но не пентен-3)
 5 4 3 2 1 СН 3 – СН = СН – СН 3 │ СН 3 4 -метилпентен-2 (но не 2 -метилпентен-3) (наименьший номер д. б. у двойной связи!) 5 4 3 2 1 СН 2 – СН – С = СН – СН 3 │ │ │ Сl СН 3 Сl 4 -метил-3, 5 -дихлорпентен-2 (но не 2 -метил 1, 3 -дихлорпентен-3 или не 3, 5 -дихлор-4 метилпентен-2)
5 4 3 2 1 СН 3 – СН = СН – СН 3 │ СН 3 4 -метилпентен-2 (но не 2 -метилпентен-3) (наименьший номер д. б. у двойной связи!) 5 4 3 2 1 СН 2 – СН – С = СН – СН 3 │ │ │ Сl СН 3 Сl 4 -метил-3, 5 -дихлорпентен-2 (но не 2 -метил 1, 3 -дихлорпентен-3 или не 3, 5 -дихлор-4 метилпентен-2)
 4. Изомерия. Для алкенов характерны следующие виды изомерии: 1. Структурная изомерия алкенов обусловлена не только строением углеродного скелета, но и положением двойной связи в главной углеродной цепи. Первым гомологом, для которого осуществляется изомерия с учётом этих двух признаков, является алкен С 4 Н 8. а) изомерия цепи. СН 3 – СН 2 – СН = СН 2 бутен-1 и СН 3 – С = СН 2 │ СН 3 2 -метилпропен СН 3 – СН 2 – СН = СН – СН 3 и СН 3 – С = СН – СН 3 пентен-2 │ СН 3 2 -метилбутен-2
4. Изомерия. Для алкенов характерны следующие виды изомерии: 1. Структурная изомерия алкенов обусловлена не только строением углеродного скелета, но и положением двойной связи в главной углеродной цепи. Первым гомологом, для которого осуществляется изомерия с учётом этих двух признаков, является алкен С 4 Н 8. а) изомерия цепи. СН 3 – СН 2 – СН = СН 2 бутен-1 и СН 3 – С = СН 2 │ СН 3 2 -метилпропен СН 3 – СН 2 – СН = СН – СН 3 и СН 3 – С = СН – СН 3 пентен-2 │ СН 3 2 -метилбутен-2
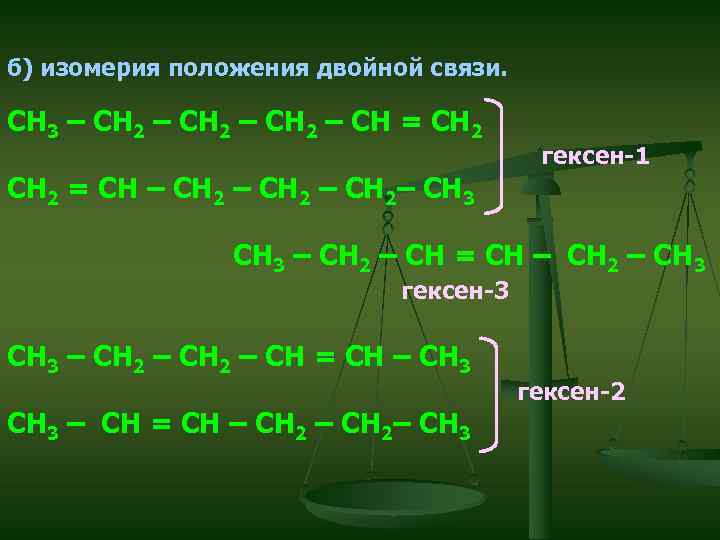 б) изомерия положения двойной связи. СН 3 – СН 2 – СН = СН 2 гексен-1 СН 2 = СН – СН 2– СН 3 – СН 2 – СН = СН – СН 2 – СН 3 гексен-3 СН 3 – СН 2 – СН = СН – СН 3 – СН = СН – СН 2– СН 3 гексен-2
б) изомерия положения двойной связи. СН 3 – СН 2 – СН = СН 2 гексен-1 СН 2 = СН – СН 2– СН 3 – СН 2 – СН = СН – СН 2 – СН 3 гексен-3 СН 3 – СН 2 – СН = СН – СН 3 – СН = СН – СН 2– СН 3 гексен-2
 2. Пространственная (стереоизомерия, цис-. трансизомерия) Обусловлена наличием в молекуле двойной связи и различным расположением заместителей относительно плоскости π-связи. Многие алкены могут существовать в виде цис- и транс-изомеров. Цис-изомер — изомер, в котором два одинаковых заместителя у двух атомов углерода, связанных двойной связью, расположены по одну сторону плоскости π-связи. Транс-изомер — изомер, в котором два одинаковых заместителя расположены по разные стороны плоскости πсвязи.
2. Пространственная (стереоизомерия, цис-. трансизомерия) Обусловлена наличием в молекуле двойной связи и различным расположением заместителей относительно плоскости π-связи. Многие алкены могут существовать в виде цис- и транс-изомеров. Цис-изомер — изомер, в котором два одинаковых заместителя у двух атомов углерода, связанных двойной связью, расположены по одну сторону плоскости π-связи. Транс-изомер — изомер, в котором два одинаковых заместителя расположены по разные стороны плоскости πсвязи.
 Цис- и транс-изомеры не являются структурными изомерами, так как они имеют одинаковую последовательность связей атомов, а различаются только расположением атомов или групп в пространстве, т. е. представляют собой пространственные изомеры, или стереоизомеры. Примером могут служить два стереоизомера бутена-2: цис-бутен-2, у которого два метильных заместителя расположены по одну и ту же сторону плоскости π-связи, и транс-бутен-2, у которого эти заместители располагаются по разные стороны плоскости π-связи.
Цис- и транс-изомеры не являются структурными изомерами, так как они имеют одинаковую последовательность связей атомов, а различаются только расположением атомов или групп в пространстве, т. е. представляют собой пространственные изомеры, или стереоизомеры. Примером могут служить два стереоизомера бутена-2: цис-бутен-2, у которого два метильных заместителя расположены по одну и ту же сторону плоскости π-связи, и транс-бутен-2, у которого эти заместители располагаются по разные стороны плоскости π-связи.
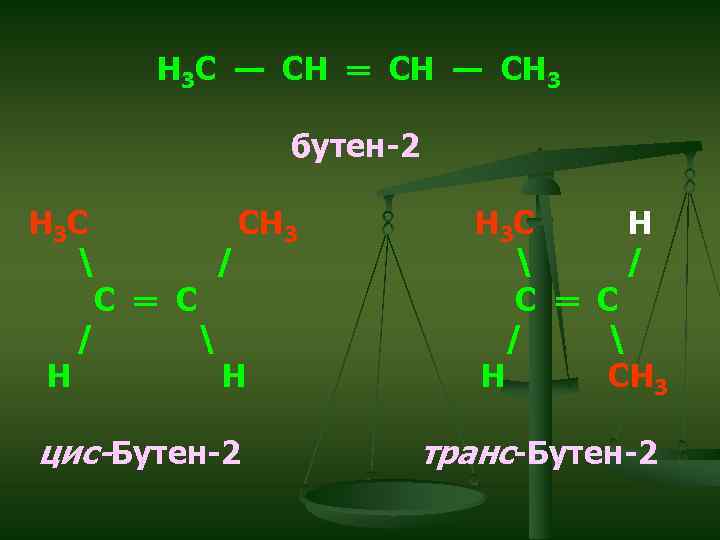 H 3 C — CH ═ CH — CH 3 бутен-2 H 3 C / H H H 3 C H / C ═ C / H CH 3 цис-Бутен-2 транс-Бутен-2 C ═ C / CH 3
H 3 C — CH ═ CH — CH 3 бутен-2 H 3 C / H H H 3 C H / C ═ C / H CH 3 цис-Бутен-2 транс-Бутен-2 C ═ C / CH 3
 Алкены, у которых атом углерода, связанный двойной связью, имеет два одинаковых заместителя, например 2 -метилпропен (СН 3)2 С + СН 2, не имеют циси транс-изомеров. Цис- и транс-изомеры различаются по энергетическому состоянию. Более устойчивыми являются транс-изомеры (заместители удалены друг от друга). Переход этих изомеров друга возможен только при условии поворота вокруг двойной связи, для чего необходимо разорвать -связь. Этот высокий энергетический барьер вращения вокруг двойной углерод-углеродной связи можно преодолеть только при температуре около 300 С. Цис- и транс-изомеры существуют в индивидуальном виде, различаются по физическим константам и самопроизвольно друг в друга не переходят.
Алкены, у которых атом углерода, связанный двойной связью, имеет два одинаковых заместителя, например 2 -метилпропен (СН 3)2 С + СН 2, не имеют циси транс-изомеров. Цис- и транс-изомеры различаются по энергетическому состоянию. Более устойчивыми являются транс-изомеры (заместители удалены друг от друга). Переход этих изомеров друга возможен только при условии поворота вокруг двойной связи, для чего необходимо разорвать -связь. Этот высокий энергетический барьер вращения вокруг двойной углерод-углеродной связи можно преодолеть только при температуре около 300 С. Цис- и транс-изомеры существуют в индивидуальном виде, различаются по физическим константам и самопроизвольно друг в друга не переходят.
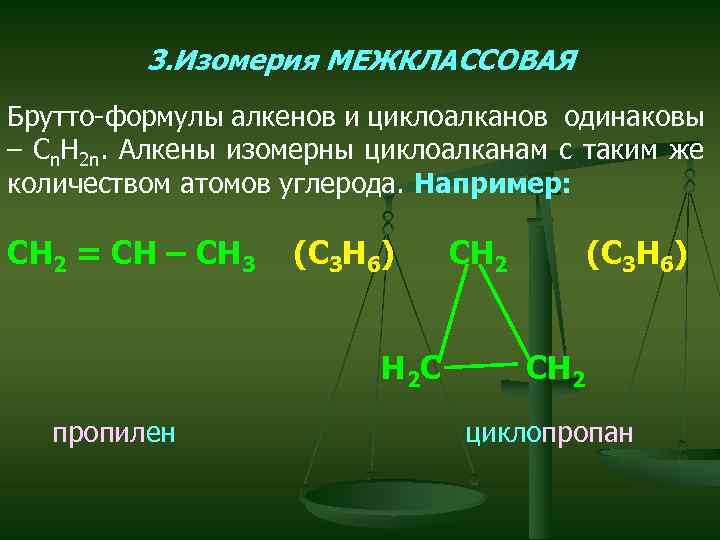 3. Изомерия МЕЖКЛАССОВАЯ Брутто-формулы алкенов и циклоалканов одинаковы – Cn. H 2 n. Алкены изомерны циклоалканам с таким же количеством атомов углерода. Например: СН 2 = СН – СН 3 (С 3 Н 6) Н 2 С пропилен СН 2 (С 3 Н 6) СН 2 циклопропан
3. Изомерия МЕЖКЛАССОВАЯ Брутто-формулы алкенов и циклоалканов одинаковы – Cn. H 2 n. Алкены изомерны циклоалканам с таким же количеством атомов углерода. Например: СН 2 = СН – СН 3 (С 3 Н 6) Н 2 С пропилен СН 2 (С 3 Н 6) СН 2 циклопропан
 СН 3 – СН 2 – СН = СН 2 (С 4 Н 8) СН 2 — СН 2 бутен-1 циклобутан 5. Физические свойства: Низшие гомологи С 2 – С 4 при нормальных условиях – газы; С 5 – С 17 – жидкости; высшие гомологи твёрдые вещества. Алкены не растворимы в воде. Хорошо растворимы в органических растворителях.
СН 3 – СН 2 – СН = СН 2 (С 4 Н 8) СН 2 — СН 2 бутен-1 циклобутан 5. Физические свойства: Низшие гомологи С 2 – С 4 при нормальных условиях – газы; С 5 – С 17 – жидкости; высшие гомологи твёрдые вещества. Алкены не растворимы в воде. Хорошо растворимы в органических растворителях.
 1. Пиролиз алканов.
1. Пиролиз алканов.
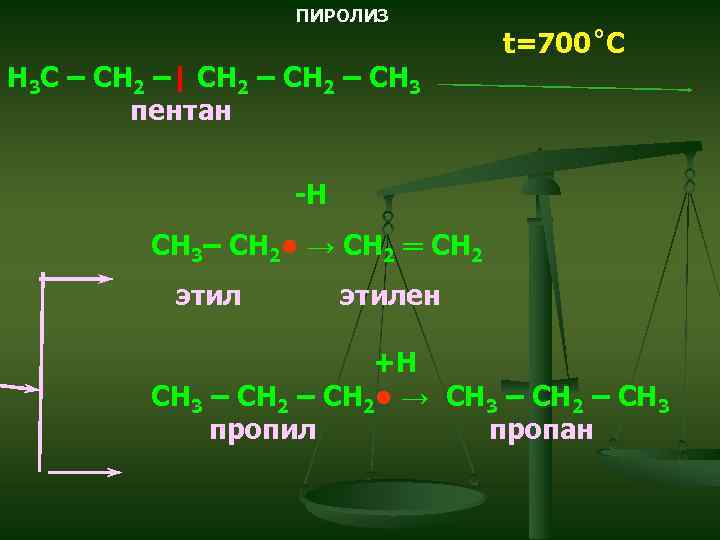 ПИРОЛИЗ H 3 C – CH 2 –| CH 2 – CH 3 пентан t=700˚C -Н СН 3– СН 2 • → CH 2 ═ CH 2 этилен +Н СH 3 – CH 2 • → СH 3 – CH 2 – CH 3 пропил пропан
ПИРОЛИЗ H 3 C – CH 2 –| CH 2 – CH 3 пентан t=700˚C -Н СН 3– СН 2 • → CH 2 ═ CH 2 этилен +Н СH 3 – CH 2 • → СH 3 – CH 2 – CH 3 пропил пропан
 2. Реакции элиминирования: Элиминирование - отщепление двух атомов или групп атомов от соседних атомов углерода с образованием между ними -– связи. а) Дегидрогалогенирование галогеноводорода) : (элиминирование t § H 2 C ― CH 3 + KOH H 3 C — CH = CH 2 + KBr + HOН | | (спирт. р-р. ) Br H 1 - бромпропан пропен – 1 НО: в водном растворе щелочи идёт гидролиз и получается спирт § H 2 C ― CH 3 + KOH H 2 C — CH 2 — CH 3 + KBr | | (водн. р-р. ) | Br H НО 1 -бромпропанол – 1
2. Реакции элиминирования: Элиминирование - отщепление двух атомов или групп атомов от соседних атомов углерода с образованием между ними -– связи. а) Дегидрогалогенирование галогеноводорода) : (элиминирование t § H 2 C ― CH 3 + KOH H 3 C — CH = CH 2 + KBr + HOН | | (спирт. р-р. ) Br H 1 - бромпропан пропен – 1 НО: в водном растворе щелочи идёт гидролиз и получается спирт § H 2 C ― CH 3 + KOH H 2 C — CH 2 — CH 3 + KBr | | (водн. р-р. ) | Br H НО 1 -бромпропанол – 1
 Правило Зайцева: атом водорода отщепляется от наименее гидрированного атома углерода, т. е. имеющего меньшее число атомов водорода. б) Дегидратация внутримолекулярная (элиминирование Н 2 О): H 2 SO 4 ( k ), t = 180˚C H 3 C ― CH ― C H 3 │ │ H OH Пропанол-1 H 3 C ― CH = CH ―CH 3 + H 2 O Пропен в) Дегалогенирование (элиминирование Hal): CH 3 │ t │ H 3 C — CH 3 +Zn пыль →H 2 C — C = CH — CH 3 + Zn. Br 2 │ │ Br Br 2–метилбутен– 2
Правило Зайцева: атом водорода отщепляется от наименее гидрированного атома углерода, т. е. имеющего меньшее число атомов водорода. б) Дегидратация внутримолекулярная (элиминирование Н 2 О): H 2 SO 4 ( k ), t = 180˚C H 3 C ― CH ― C H 3 │ │ H OH Пропанол-1 H 3 C ― CH = CH ―CH 3 + H 2 O Пропен в) Дегалогенирование (элиминирование Hal): CH 3 │ t │ H 3 C — CH 3 +Zn пыль →H 2 C — C = CH — CH 3 + Zn. Br 2 │ │ Br Br 2–метилбутен– 2
 г) дегидрирование алканов (элиминирование Н 2): t Cn. H 2 n+2 → Cn. H 2 n + H 2↑ к , t= 500˚C 2 H 3 C ─ CH 2 ─ CH 3 бутан H 3 C — CH = CH ─ CH 3 + H 2↑ бутен – 2 H 2 C = CH— CH 2 — CH 3 + H 2↑ бутен – 1
г) дегидрирование алканов (элиминирование Н 2): t Cn. H 2 n+2 → Cn. H 2 n + H 2↑ к , t= 500˚C 2 H 3 C ─ CH 2 ─ CH 3 бутан H 3 C — CH = CH ─ CH 3 + H 2↑ бутен – 2 H 2 C = CH— CH 2 — CH 3 + H 2↑ бутен – 1
 3. Разложение нефтепродуктов. 4. Гидрированием алкинов: Cn. H 2 n-2 + H 2 t; к Ni, Pt Cn. H 2 n
3. Разложение нефтепродуктов. 4. Гидрированием алкинов: Cn. H 2 n-2 + H 2 t; к Ni, Pt Cn. H 2 n
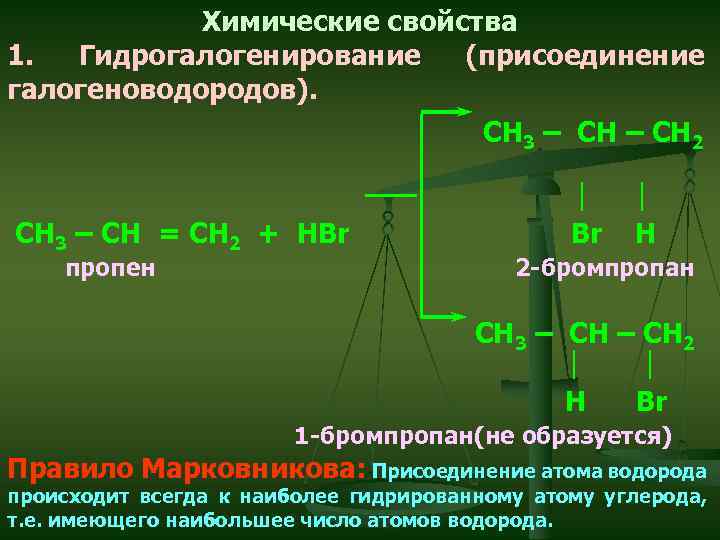 Химические свойства 1. Гидрогалогенирование (присоединение галогеноводородов). CH 3 – CН – CH 2 СH 3 – СН = CH 2 + HBr пропен Br H 2 -бромпропан CH 3 – CН – CH 2 H Br 1 -бромпропан(не образуется) Правило Марковникова: Присоединение атома водорода происходит всегда к наиболее гидрированному атому углерода, т. е. имеющего наибольшее число атомов водорода.
Химические свойства 1. Гидрогалогенирование (присоединение галогеноводородов). CH 3 – CН – CH 2 СH 3 – СН = CH 2 + HBr пропен Br H 2 -бромпропан CH 3 – CН – CH 2 H Br 1 -бромпропан(не образуется) Правило Марковникова: Присоединение атома водорода происходит всегда к наиболее гидрированному атому углерода, т. е. имеющего наибольшее число атомов водорода.
 2. Реакция гидратации (присоединение воды). При взаимодействии алкенов с водой в присутствии минеральных кислот (серной, фосфорной) образуются спирты. Минеральные кислоты выполняют роль катализаторов и являются источниками протонов. Реакция идёт по правилу Марковникова. СH 3 – СН = CH 2 + HОН Пропан H 2 SO 4 CH 3 – CН – CH 2 ОН Н Пропанол-2
2. Реакция гидратации (присоединение воды). При взаимодействии алкенов с водой в присутствии минеральных кислот (серной, фосфорной) образуются спирты. Минеральные кислоты выполняют роль катализаторов и являются источниками протонов. Реакция идёт по правилу Марковникова. СH 3 – СН = CH 2 + HОН Пропан H 2 SO 4 CH 3 – CН – CH 2 ОН Н Пропанол-2
 3. Реакция галогенирования (присоединение галогенов). При взаимодействии алкенов с галогенами (бромом, хлором) образуются галогеналканы. СH 3 + СH 3 – С = CH 2 + Br→Br 2 -метилпропен но 2 СH 3 – С – CH 2 Br Br 1, 2 -дибром-2 -метилпропан При добавлении к алкену брома (в виде бромной воды) бурая окраска брома быстро исчезает. Присоединение брома идёт легко при комнатной температуре. Эта реакция является качественной для обнаружения двойной связи.
3. Реакция галогенирования (присоединение галогенов). При взаимодействии алкенов с галогенами (бромом, хлором) образуются галогеналканы. СH 3 + СH 3 – С = CH 2 + Br→Br 2 -метилпропен но 2 СH 3 – С – CH 2 Br Br 1, 2 -дибром-2 -метилпропан При добавлении к алкену брома (в виде бромной воды) бурая окраска брома быстро исчезает. Присоединение брома идёт легко при комнатной температуре. Эта реакция является качественной для обнаружения двойной связи.
 II. Реакции окисления и восстановления. 1. Окисление. а) При окислении алкенов перманганатом калия KMn. O 4 в нейтральной или слабощелочной среде происходит разрыв -связи и присоединение гидроксильной группы к каждому атому углерода, т. е. реакция гидроксилирования. В результате получаются двухатомные спирты (гликоли). Эта реакция носит имя открывшего её русского химика Е. Е. Вагнера (1888). Она используется как качественная реакция для обнаружения двойной связи. В результате этой реакции окрашенный раствор перманганата калия быстро обесцвечивается и выпадает коричневый осадок оксида марганца (IV). СН 2 = СН 2 + [O] + HOН → 3 CH 2 – CH 2 ( + КМn. O 4) OH OH (+KOH + Mn. O 2↓) этиленгликоль
II. Реакции окисления и восстановления. 1. Окисление. а) При окислении алкенов перманганатом калия KMn. O 4 в нейтральной или слабощелочной среде происходит разрыв -связи и присоединение гидроксильной группы к каждому атому углерода, т. е. реакция гидроксилирования. В результате получаются двухатомные спирты (гликоли). Эта реакция носит имя открывшего её русского химика Е. Е. Вагнера (1888). Она используется как качественная реакция для обнаружения двойной связи. В результате этой реакции окрашенный раствор перманганата калия быстро обесцвечивается и выпадает коричневый осадок оксида марганца (IV). СН 2 = СН 2 + [O] + HOН → 3 CH 2 – CH 2 ( + КМn. O 4) OH OH (+KOH + Mn. O 2↓) этиленгликоль
 б) При окислении перманганатом калия в кислой среде или хромовой смесью происходит полный разрыв двойной связи с образованием продуктов окисления. Эту реакцию называют окислительным расщеплением двойной связи. Из молекулы бутена-2 в результате окислительного расщепления образуются две молекулы уксусной кислоты. [O] СН 3 – СН = СН – СН 3 → 2 СН 3 – С Бутен-2 O OH уксусная кислота t=300˚C, K =Ag в) 2 СH 2 = CH 2 + O 2 2 CH 2 — CH 2 O этоксиэтан (эпоксид)
б) При окислении перманганатом калия в кислой среде или хромовой смесью происходит полный разрыв двойной связи с образованием продуктов окисления. Эту реакцию называют окислительным расщеплением двойной связи. Из молекулы бутена-2 в результате окислительного расщепления образуются две молекулы уксусной кислоты. [O] СН 3 – СН = СН – СН 3 → 2 СН 3 – С Бутен-2 O OH уксусная кислота t=300˚C, K =Ag в) 2 СH 2 = CH 2 + O 2 2 CH 2 — CH 2 O этоксиэтан (эпоксид)
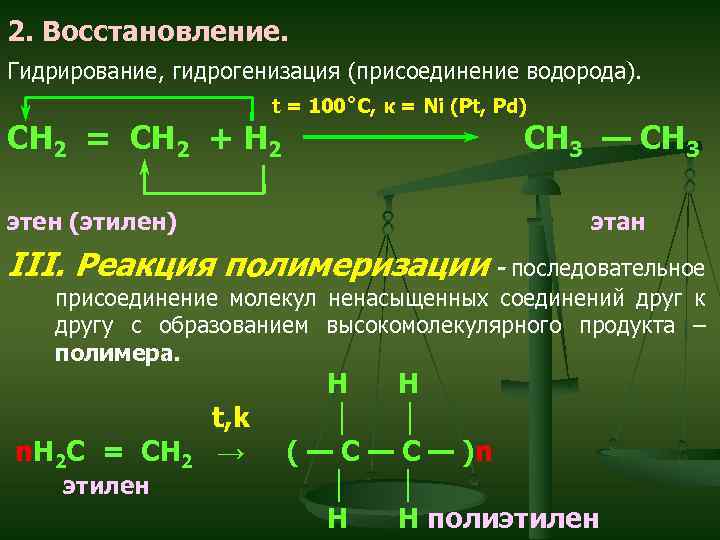 2. Восстановление. Гидрирование, гидрогенизация (присоединение водорода). t = 100˚C, к = Ni (Pt, Pd) CH 2 = CH 2 + H 2 этен (этилен) CH 3 — CH 3 этан III. Реакция полимеризации - последовательное присоединение молекул ненасыщенных соединений друг к другу с образованием высокомолекулярного продукта – полимера. n. H 2 C = CH 2 этилен t, k → H H │ │ ( — C — )n │ │ H H полиэтилен
2. Восстановление. Гидрирование, гидрогенизация (присоединение водорода). t = 100˚C, к = Ni (Pt, Pd) CH 2 = CH 2 + H 2 этен (этилен) CH 3 — CH 3 этан III. Реакция полимеризации - последовательное присоединение молекул ненасыщенных соединений друг к другу с образованием высокомолекулярного продукта – полимера. n. H 2 C = CH 2 этилен t, k → H H │ │ ( — C — )n │ │ H H полиэтилен
 IV. Горение. Этилен горит светящимся, слегка коптящим пламенем с образованием СО 2 и Н 2 О. а) С 2 Н 4 + 3 О 2 избыток t → 2 СО 2↑ + 2 Н 2 О (в струе кислорода) V. Разложение. t С 2 Н 4 → 2 С + 2 Н 2↑
IV. Горение. Этилен горит светящимся, слегка коптящим пламенем с образованием СО 2 и Н 2 О. а) С 2 Н 4 + 3 О 2 избыток t → 2 СО 2↑ + 2 Н 2 О (в струе кислорода) V. Разложение. t С 2 Н 4 → 2 С + 2 Н 2↑
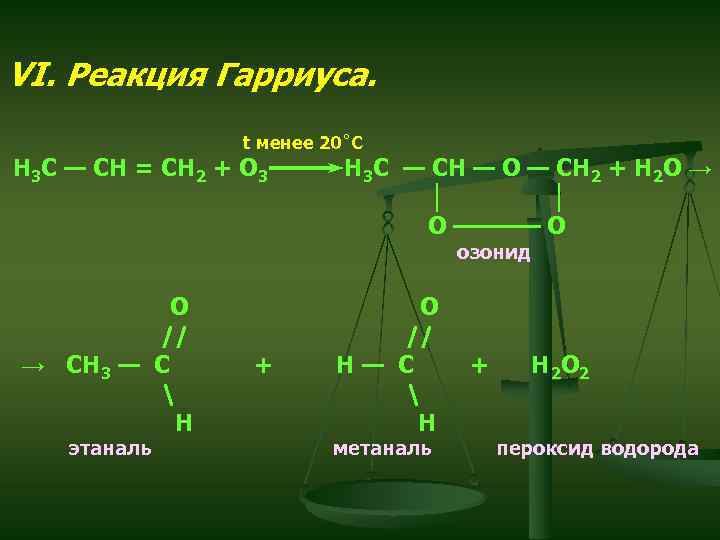 VI. Реакция Гарриуса. t менее 20˚С Н 3 С — СН = СН 2 + О 3 Н 3 С — СН — О — СН 2 + Н 2 О → │ │ О ———— О озонид О // → СН 3 — С Н этаналь + О // Н— С Н метаналь + Н 2 О 2 пероксид водорода
VI. Реакция Гарриуса. t менее 20˚С Н 3 С — СН = СН 2 + О 3 Н 3 С — СН — О — СН 2 + Н 2 О → │ │ О ———— О озонид О // → СН 3 — С Н этаналь + О // Н— С Н метаналь + Н 2 О 2 пероксид водорода
 8. Применение алкенов. 1. Этилен (этен) широко используется в промышленном органическом синтезе для получения разнообразных органических соединений, таких, как галогенопроизводные, спирты (этанол, этиленгликоль), уксусный альдегид, уксусная кислота и др. Многие вещества, получаемые на базе этилена, сами затем служат сырьём для дальнейших синтезов. В большом количестве этилен расходуется для производства полимеров. Обладает слабым наркотическим действием. В обогащенной этиленом атмосфере происходит ускоренное созревание плодов и овощей. 2. Пропилен (пропен) используют для получения спиртов, ацетона, полипропилена.
8. Применение алкенов. 1. Этилен (этен) широко используется в промышленном органическом синтезе для получения разнообразных органических соединений, таких, как галогенопроизводные, спирты (этанол, этиленгликоль), уксусный альдегид, уксусная кислота и др. Многие вещества, получаемые на базе этилена, сами затем служат сырьём для дальнейших синтезов. В большом количестве этилен расходуется для производства полимеров. Обладает слабым наркотическим действием. В обогащенной этиленом атмосфере происходит ускоренное созревание плодов и овощей. 2. Пропилен (пропен) используют для получения спиртов, ацетона, полипропилена.
 3. Озониды используют для получения альдегидов и карбоновых кислот, взрывчатых веществ. 4. В медицине используют смесь этилена и ацетилена – «нарцилен» для ингаляционного наркоза. 10. Понятие о полимерах. Молекулы алкенов могут вступать во взаимодействие друг с другом. За счёт разрыва -связи идёт реакция полимеризации с образованием молекул с большой молекулярной массой – макромолекул (от греч. macros – большой). Реакция полимеризации – это последовательное присоединение молекул ненасыщенных соединений друг к другу с образованием высокомолекулярного продукта – полимера.
3. Озониды используют для получения альдегидов и карбоновых кислот, взрывчатых веществ. 4. В медицине используют смесь этилена и ацетилена – «нарцилен» для ингаляционного наркоза. 10. Понятие о полимерах. Молекулы алкенов могут вступать во взаимодействие друг с другом. За счёт разрыва -связи идёт реакция полимеризации с образованием молекул с большой молекулярной массой – макромолекул (от греч. macros – большой). Реакция полимеризации – это последовательное присоединение молекул ненасыщенных соединений друг к другу с образованием высокомолекулярного продукта – полимера.
 Молекулы алкена, вступающие в реакцию полимеризации, называются мономерами. n C=C мономер │ │ → (– C – )n │ │ полимер cтепень полимеризации Полиэтилен получают полимеризацией этилена. Молекулярная масса макромолекулы полимера достигает 1 млн. Полиэтилен представляет собой бесцветный материал, имеющий низкую тепло- и электропроводность. Он широко применяется в быту и технике в виде посуды, плёнок, изоляции электропроводов и т. д. n. CН 2 = CН 2 → (– CН 2 – )n этилен полиэтилен
Молекулы алкена, вступающие в реакцию полимеризации, называются мономерами. n C=C мономер │ │ → (– C – )n │ │ полимер cтепень полимеризации Полиэтилен получают полимеризацией этилена. Молекулярная масса макромолекулы полимера достигает 1 млн. Полиэтилен представляет собой бесцветный материал, имеющий низкую тепло- и электропроводность. Он широко применяется в быту и технике в виде посуды, плёнок, изоляции электропроводов и т. д. n. CН 2 = CН 2 → (– CН 2 – )n этилен полиэтилен
 Полипропилен получается стереоспецифической полимеризацией пропилена (пропена). Стереоспецифическая полимеризация – это процесс получения полимера со строго упорядоченным пространственным строением. Полипропилен – твёрдый, прозрачный материал, используется при изготовлении различных изделий для химических производств – труб, деталей аппаратуры, особо прочной электроизоляции, волокон для технических целей. Химическая устойчивость полиэтилена и полипропилена объясняется прежде всего тем, что оба они являются алканами. Нерегулярная и регулярная структура пропилена
Полипропилен получается стереоспецифической полимеризацией пропилена (пропена). Стереоспецифическая полимеризация – это процесс получения полимера со строго упорядоченным пространственным строением. Полипропилен – твёрдый, прозрачный материал, используется при изготовлении различных изделий для химических производств – труб, деталей аппаратуры, особо прочной электроизоляции, волокон для технических целей. Химическая устойчивость полиэтилена и полипропилена объясняется прежде всего тем, что оба они являются алканами. Нерегулярная и регулярная структура пропилена
 Большое значение, благодаря исключительной термостойкости и химической устойчивости, имеют полимеры из фторированного этилена: n. CF 2 = CCl. F → (– CF 2 – CCl. F –)n трифторхлорэтилен фторопласт-3 n. CF 2 = CF 2 → (– CF 2 –)n тетрафторэтилен фторопласт-4 Фторопласты чрезвычайно химически инертны. Фторопласты используются для изготовления коррозионностойкой химической аппаратуры.
Большое значение, благодаря исключительной термостойкости и химической устойчивости, имеют полимеры из фторированного этилена: n. CF 2 = CCl. F → (– CF 2 – CCl. F –)n трифторхлорэтилен фторопласт-3 n. CF 2 = CF 2 → (– CF 2 –)n тетрафторэтилен фторопласт-4 Фторопласты чрезвычайно химически инертны. Фторопласты используются для изготовления коррозионностойкой химической аппаратуры.
 ПРИЛОЖЕНИЕ Строение двойной связи. Атомы углерода, связанные двойной связью, находятся в состоянии sp 2 -гибридизации. Двойная связь между ними образована их двух пар обобществленных электронов, т. е. это четырехэлектронная связь. Она является сочетанием ковалентных δ-связи и -– связи. δ-связь образована за счет осевого перекрывания sp 2 -гибридных орбиталей, а -– связь – за счет бокового перекрывания негибридизованных р-орбиталей двух атомов углерода. Энергия = 606 к. Дж/моль (энергия --связи 259 к. Дж/моль, δсвязи 347 к. Дж/ моль). При образовании – связи происходит сближение атомов углерода, потому что межъядерное пространство в двойной связи более насыщено электронами, чем в δ-связи. Это стягивает атомные ядра и поэтому длина двойной связи (0, 133 нм) меньше одинарной (0, 154 нм).
ПРИЛОЖЕНИЕ Строение двойной связи. Атомы углерода, связанные двойной связью, находятся в состоянии sp 2 -гибридизации. Двойная связь между ними образована их двух пар обобществленных электронов, т. е. это четырехэлектронная связь. Она является сочетанием ковалентных δ-связи и -– связи. δ-связь образована за счет осевого перекрывания sp 2 -гибридных орбиталей, а -– связь – за счет бокового перекрывания негибридизованных р-орбиталей двух атомов углерода. Энергия = 606 к. Дж/моль (энергия --связи 259 к. Дж/моль, δсвязи 347 к. Дж/ моль). При образовании – связи происходит сближение атомов углерода, потому что межъядерное пространство в двойной связи более насыщено электронами, чем в δ-связи. Это стягивает атомные ядра и поэтому длина двойной связи (0, 133 нм) меньше одинарной (0, 154 нм).
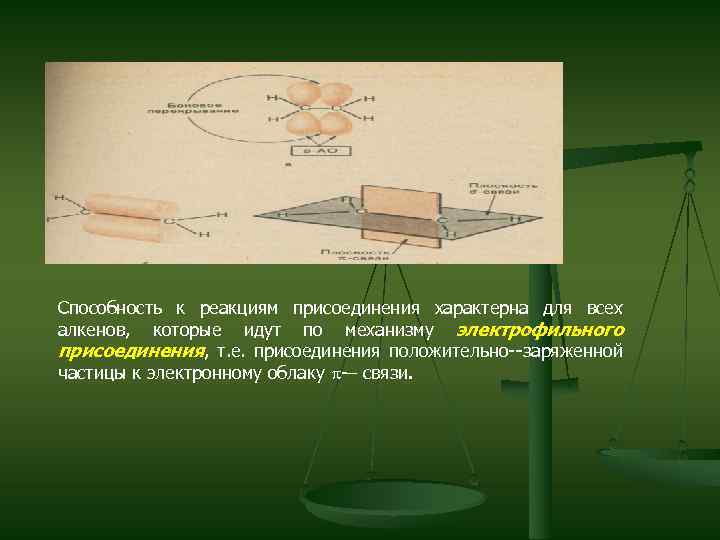 Способность к реакциям присоединения характерна для всех алкенов, которые идут по механизму электрофильного присоединения, т. е. присоединения положительно--заряженной частицы к электронному облаку -– связи.
Способность к реакциям присоединения характерна для всех алкенов, которые идут по механизму электрофильного присоединения, т. е. присоединения положительно--заряженной частицы к электронному облаку -– связи.
 Реакции электрофильного присоединения (АЕ). Механизм реакции электрофильного присоединения. Реакции присоединения идут в четыре стадии: а) Поляризуемость молекулы: δ+ δ- δ+ Сl : Cl → Cl- : Cl + Fe. Cl 3 → Cl — Fe. Cl 4 а) Образование π – комплекса: δ+ H 2 C = CH 2 + Cl — Fe. Cl 4 δ- δ- CH 2 ═ CH 2 π ↑δ+ δCl — Fe Cl 4 в) Образование карбкатиона (карбкатион — это частица с положительным зарядом на атоме углерода). + 0 СH 2 ═ CH 2 — CH 2 + Cl + Fe. Cl 3 ↑δ+ δ│ Cl — Fe. Cl 4 Cl г) Стабилизация молекул. + – СH 2 — CH 2 + Cl │ 0 CH 2 — CH 2 │ │
Реакции электрофильного присоединения (АЕ). Механизм реакции электрофильного присоединения. Реакции присоединения идут в четыре стадии: а) Поляризуемость молекулы: δ+ δ- δ+ Сl : Cl → Cl- : Cl + Fe. Cl 3 → Cl — Fe. Cl 4 а) Образование π – комплекса: δ+ H 2 C = CH 2 + Cl — Fe. Cl 4 δ- δ- CH 2 ═ CH 2 π ↑δ+ δCl — Fe Cl 4 в) Образование карбкатиона (карбкатион — это частица с положительным зарядом на атоме углерода). + 0 СH 2 ═ CH 2 — CH 2 + Cl + Fe. Cl 3 ↑δ+ δ│ Cl — Fe. Cl 4 Cl г) Стабилизация молекул. + – СH 2 — CH 2 + Cl │ 0 CH 2 — CH 2 │ │


