Лекция 3. Поверхность тел.ppt
- Количество слайдов: 14
 Лекция № 3 Тема лекции: Поверхность твердых тел. Микроскопические аспекты Поверхность твердого тела - особый мир, где проявляются не только твердотельные свойства, но также свойства жидкости и газовой фазы Свойства поверхности на микроскопическом уровне - это атомная, электронная, магнитная структура Остановимся на основных подходах и приемах, которые используются для описания структурных и электронных свойств атомов и молекул, входящих в состав поверхности или адсорбированных на ней метод молекулярных орбиталей позволяет конструировать химические связи и образовывать из атомов молекулы, нанокластеры и 1 наночастицы, а также и массивное твердое тело
Лекция № 3 Тема лекции: Поверхность твердых тел. Микроскопические аспекты Поверхность твердого тела - особый мир, где проявляются не только твердотельные свойства, но также свойства жидкости и газовой фазы Свойства поверхности на микроскопическом уровне - это атомная, электронная, магнитная структура Остановимся на основных подходах и приемах, которые используются для описания структурных и электронных свойств атомов и молекул, входящих в состав поверхности или адсорбированных на ней метод молекулярных орбиталей позволяет конструировать химические связи и образовывать из атомов молекулы, нанокластеры и 1 наночастицы, а также и массивное твердое тело
 Атомные и молекулярные орбитали Орбитали получаются при решении уравнений квантовой механики типа Hψ = Eψ, где H - оператор Гамильтона, Е энергия орбиталей, ψ - атомные или молекулярные орбитали В одноэлектронном приближении атомные орбитали ищутся в виде ψn, l, m(r, θ, φ) =Rn, l(r)Yl, m(θ, φ), где r - расстояние электрона от ядра, θ и φ - углы сферической системы координат, Rn, l(r) и Yl, m(θ, φ)) называют радиальной и сферической функциями При l = 1, 2, 3, . . . образуются s-, p-, d- и т. д. орбитали. Вид атомных орбиталей различен для s-, p- и d-электронов и характеризует распределение электронной плотности 2
Атомные и молекулярные орбитали Орбитали получаются при решении уравнений квантовой механики типа Hψ = Eψ, где H - оператор Гамильтона, Е энергия орбиталей, ψ - атомные или молекулярные орбитали В одноэлектронном приближении атомные орбитали ищутся в виде ψn, l, m(r, θ, φ) =Rn, l(r)Yl, m(θ, φ), где r - расстояние электрона от ядра, θ и φ - углы сферической системы координат, Rn, l(r) и Yl, m(θ, φ)) называют радиальной и сферической функциями При l = 1, 2, 3, . . . образуются s-, p-, d- и т. д. орбитали. Вид атомных орбиталей различен для s-, p- и d-электронов и характеризует распределение электронной плотности 2
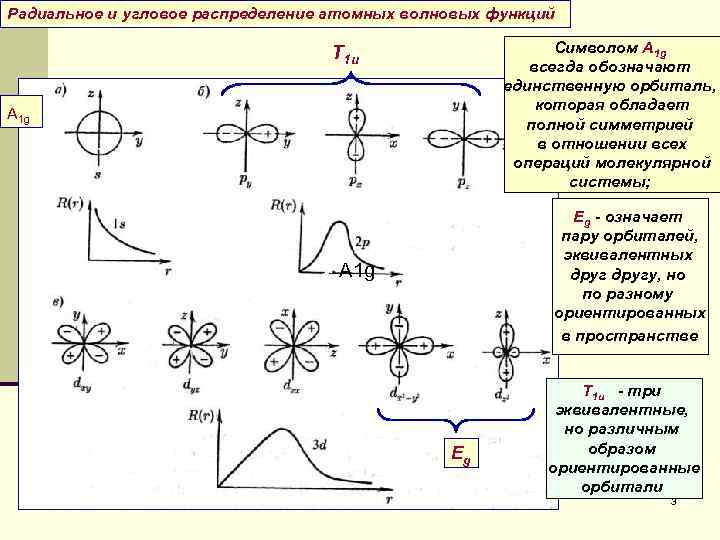 Радиальное и угловое распределение атомных волновых функций Символом A 1 g всегда обозначают единственную орбиталь, которая обладает полной симметрией в отношении всех операций молекулярной системы; Т 1 u A 1 g Eg - означает пару орбиталей, эквивалентных другу, но по разному ориентированных в пространстве A 1 g Eg Т 1 u - три эквивалентные, но различным образом ориентированные орбитали 3
Радиальное и угловое распределение атомных волновых функций Символом A 1 g всегда обозначают единственную орбиталь, которая обладает полной симметрией в отношении всех операций молекулярной системы; Т 1 u A 1 g Eg - означает пару орбиталей, эквивалентных другу, но по разному ориентированных в пространстве A 1 g Eg Т 1 u - три эквивалентные, но различным образом ориентированные орбитали 3
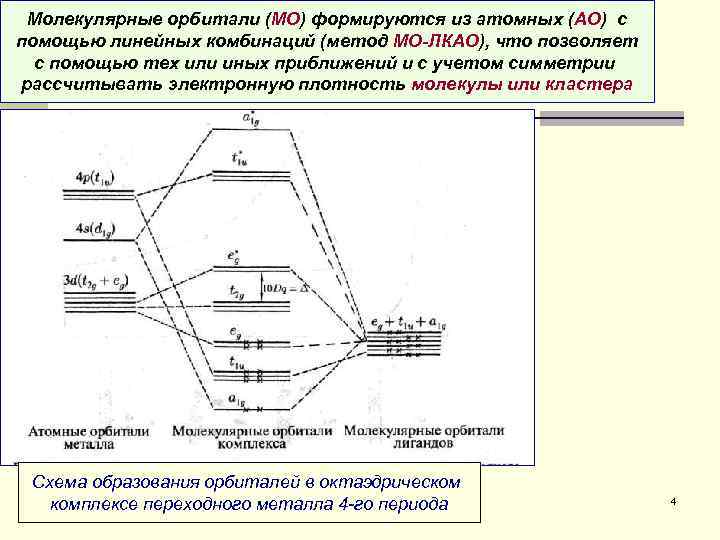 Молекулярные орбитали (МО) формируются из атомных (АО) с помощью линейных комбинаций (метод МО-ЛКАО), что позволяет с помощью тех или иных приближений и с учетом симметрии рассчитывать электронную плотность молекулы или кластера Схема образования орбиталей в октаэдрическом комплексе переходного металла 4 -го периода 4
Молекулярные орбитали (МО) формируются из атомных (АО) с помощью линейных комбинаций (метод МО-ЛКАО), что позволяет с помощью тех или иных приближений и с учетом симметрии рассчитывать электронную плотность молекулы или кластера Схема образования орбиталей в октаэдрическом комплексе переходного металла 4 -го периода 4
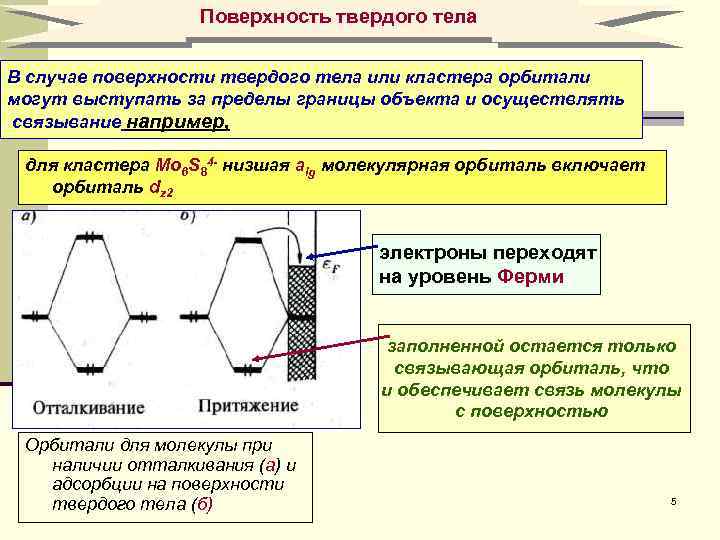 Поверхность твердого тела В случае поверхности твердого тела или кластера орбитали могут выступать за пределы границы объекта и осуществлять связывание например, ! для кластера Mo 6 S 84 - низшая аlg молекулярная орбиталь включает орбиталь dz 2 электроны переходят на уровень Ферми заполненной остается только связывающая орбиталь, что и обеспечивает связь молекулы с поверхностью Орбитали для молекулы при наличии отталкивания (а) и адсорбции на поверхности твердого тела (б) 5
Поверхность твердого тела В случае поверхности твердого тела или кластера орбитали могут выступать за пределы границы объекта и осуществлять связывание например, ! для кластера Mo 6 S 84 - низшая аlg молекулярная орбиталь включает орбиталь dz 2 электроны переходят на уровень Ферми заполненной остается только связывающая орбиталь, что и обеспечивает связь молекулы с поверхностью Орбитали для молекулы при наличии отталкивания (а) и адсорбции на поверхности твердого тела (б) 5
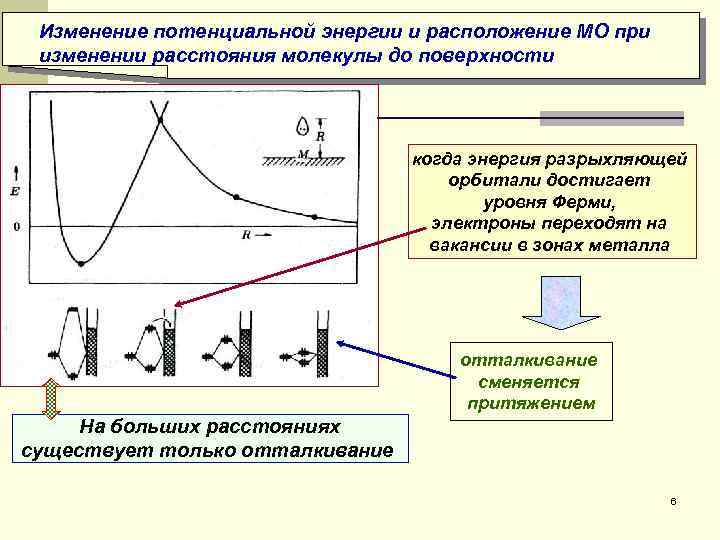 Изменение потенциальной энергии и расположение МО при изменении расстояния молекулы до поверхности когда энергия разрыхляющей орбитали достигает уровня Ферми, электроны переходят на вакансии в зонах металла отталкивание сменяется притяжением На больших расстояниях существует только отталкивание 6
Изменение потенциальной энергии и расположение МО при изменении расстояния молекулы до поверхности когда энергия разрыхляющей орбитали достигает уровня Ферми, электроны переходят на вакансии в зонах металла отталкивание сменяется притяжением На больших расстояниях существует только отталкивание 6
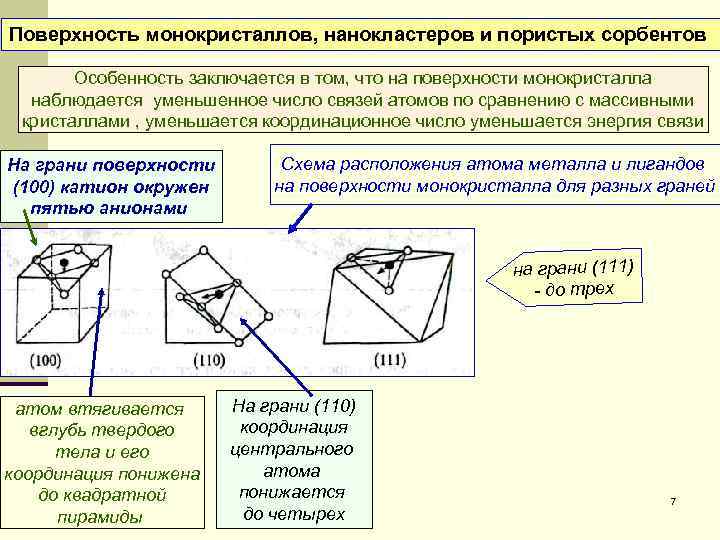 Поверхность монокристаллов, нанокластеров и пористых сорбентов Особенность заключается в том, что на поверхности монокристалла наблюдается уменьшенное число связей атомов по сравнению с массивными кристаллами , уменьшается координационное число уменьшается энергия связи На грани поверхности (100) катион окружен пятью анионами Схема расположения атома металла и лигандов на поверхности монокристалла для разных граней на грани (111) - до трех атом втягивается вглубь твердого тела и его координация понижена до квадратной пирамиды На грани (110) координация центрального атома понижается до четырех 7
Поверхность монокристаллов, нанокластеров и пористых сорбентов Особенность заключается в том, что на поверхности монокристалла наблюдается уменьшенное число связей атомов по сравнению с массивными кристаллами , уменьшается координационное число уменьшается энергия связи На грани поверхности (100) катион окружен пятью анионами Схема расположения атома металла и лигандов на поверхности монокристалла для разных граней на грани (111) - до трех атом втягивается вглубь твердого тела и его координация понижена до квадратной пирамиды На грани (110) координация центрального атома понижается до четырех 7
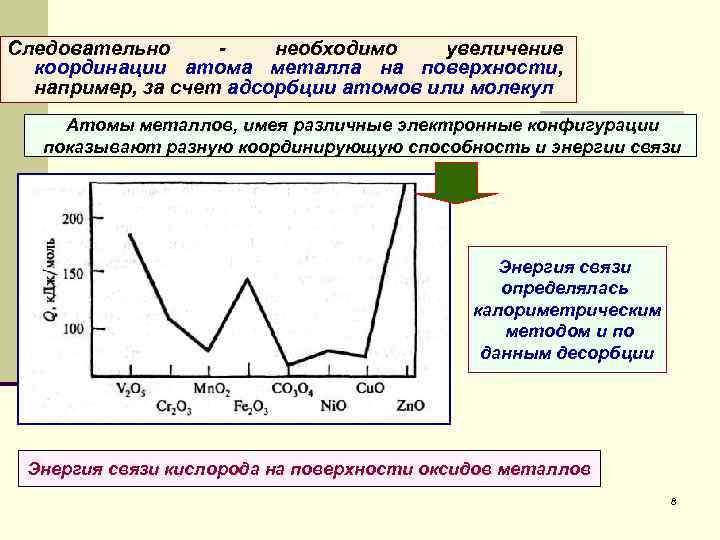 Следовательно необходимо увеличение координации атома металла на поверхности, например, за счет адсорбции атомов или молекул Атомы металлов, имея различные электронные конфигурации показывают разную координирующую способность и энергии связи Энергия связи определялась калориметрическим методом и по данным десорбции Энергия связи кислорода на поверхности оксидов металлов 8
Следовательно необходимо увеличение координации атома металла на поверхности, например, за счет адсорбции атомов или молекул Атомы металлов, имея различные электронные конфигурации показывают разную координирующую способность и энергии связи Энергия связи определялась калориметрическим методом и по данным десорбции Энергия связи кислорода на поверхности оксидов металлов 8
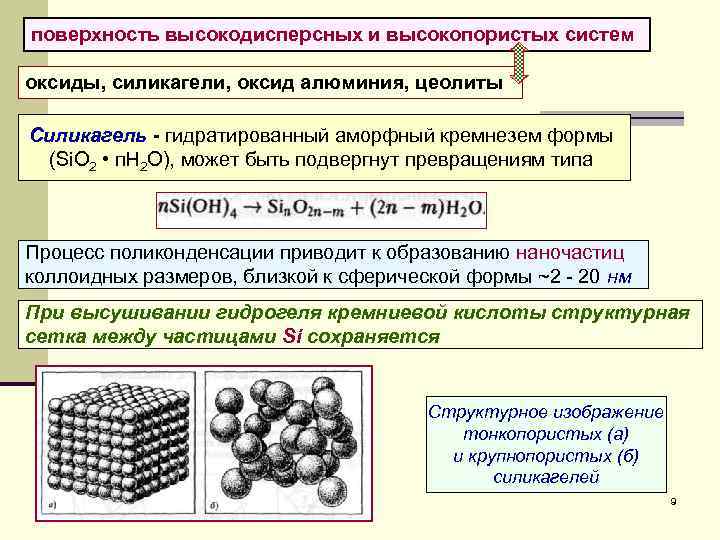 поверхность высокодисперсных и высокопористых систем оксиды, силикагели, оксид алюминия, цеолиты Силикагель - гидратированный аморфный кремнезем формы (Si. O 2 • п. Н 2 О), может быть подвергнут превращениям типа Процесс поликонденсации приводит к образованию наночастиц коллоидных размеров, близкой к сферической формы ~2 - 20 нм При высушивании гидрогеля кремниевой кислоты структурная сетка между частицами Si сохраняется Структурное изображение тонкопористых (а) и крупнопористых (б) силикагелей 9
поверхность высокодисперсных и высокопористых систем оксиды, силикагели, оксид алюминия, цеолиты Силикагель - гидратированный аморфный кремнезем формы (Si. O 2 • п. Н 2 О), может быть подвергнут превращениям типа Процесс поликонденсации приводит к образованию наночастиц коллоидных размеров, близкой к сферической формы ~2 - 20 нм При высушивании гидрогеля кремниевой кислоты структурная сетка между частицами Si сохраняется Структурное изображение тонкопористых (а) и крупнопористых (б) силикагелей 9
 Силикагели Поверхность силикагеля покрыта силанольными группами с концентрацией ОН 1, 7 12 мкмоль/м 2 или l, 0 7, 2 групп ОН на 1 нм 2. Структура поверхности может включать • изолированные силанольные группы –Si-ОН, • двойные силанольные группы -Si=(OH)2 и • соседние (вицинальные) группы -(Si-ОН)2. И еще Поверхность силикагеля модифицируется и может обладать как гидрофильными, так и гидрофобными свойствами 10
Силикагели Поверхность силикагеля покрыта силанольными группами с концентрацией ОН 1, 7 12 мкмоль/м 2 или l, 0 7, 2 групп ОН на 1 нм 2. Структура поверхности может включать • изолированные силанольные группы –Si-ОН, • двойные силанольные группы -Si=(OH)2 и • соседние (вицинальные) группы -(Si-ОН)2. И еще Поверхность силикагеля модифицируется и может обладать как гидрофильными, так и гидрофобными свойствами 10
 Оксид алюминия получают прокаливанием гидроксидов алюминия - тригидратов и моногидратов Различают следующие типы оксидов алюминия: • Низкотемпературные оксиды (Аl 2 О 3 • n. Н 2 О), в которых 0 < n < 0. 6, получаются при Т не выше 600° С в виде γ-, ρ-, χ- и -модификаций • Высокотемпературные оксиды (почти безводные) получают при 900 1000° С в виде δ-, - и θ-модификаций • Корунд ( -Al 2 O 3) получают при Т = 1000°С и выше γ-Аl 2 О 3 обладает дефектной структурой, которая стабилизирована небольшим количеством молекул воды. Первичные нанокристаллиты 3 8 нм упакованы так, что поры образуют либо щелевую, либо бутылочную форму Поверхность гидроксилирована и легко модифицируется ионами металлов, что играет важную роль в оптике, электронике, магнитных 11 свойствах, а также в таких известных процессах, как адсорбция и катализ
Оксид алюминия получают прокаливанием гидроксидов алюминия - тригидратов и моногидратов Различают следующие типы оксидов алюминия: • Низкотемпературные оксиды (Аl 2 О 3 • n. Н 2 О), в которых 0 < n < 0. 6, получаются при Т не выше 600° С в виде γ-, ρ-, χ- и -модификаций • Высокотемпературные оксиды (почти безводные) получают при 900 1000° С в виде δ-, - и θ-модификаций • Корунд ( -Al 2 O 3) получают при Т = 1000°С и выше γ-Аl 2 О 3 обладает дефектной структурой, которая стабилизирована небольшим количеством молекул воды. Первичные нанокристаллиты 3 8 нм упакованы так, что поры образуют либо щелевую, либо бутылочную форму Поверхность гидроксилирована и легко модифицируется ионами металлов, что играет важную роль в оптике, электронике, магнитных 11 свойствах, а также в таких известных процессах, как адсорбция и катализ
 Цеолиты Это регулярные пористые структуры, заполненные в обычных условиях водой При нагревании цеолитов вода выделяется, цеолиты «кипят» , что и дало им греческое название от слов цео (кипение) и литос (камень). Цеолиты представляют собой алюмосиликаты, в которых для компенсации отрицательного заряда, возникающего при замещении Si 4+ на Аl 3+ вводятся щелочные катионы или водород Общая химическая формула цеолитов: Ме 2/n. О • Аl 2 О 3 • x. Si. O 2 • 4 Н 2 О, где Me - щелочной металл или водород, n - валентность Кристаллическая структура включает тетраэдры Si. O 4 и АIO 4. Катионы должны компенсировать избыточный заряд [Аl. О 4]-. 12
Цеолиты Это регулярные пористые структуры, заполненные в обычных условиях водой При нагревании цеолитов вода выделяется, цеолиты «кипят» , что и дало им греческое название от слов цео (кипение) и литос (камень). Цеолиты представляют собой алюмосиликаты, в которых для компенсации отрицательного заряда, возникающего при замещении Si 4+ на Аl 3+ вводятся щелочные катионы или водород Общая химическая формула цеолитов: Ме 2/n. О • Аl 2 О 3 • x. Si. O 2 • 4 Н 2 О, где Me - щелочной металл или водород, n - валентность Кристаллическая структура включает тетраэдры Si. O 4 и АIO 4. Катионы должны компенсировать избыточный заряд [Аl. О 4]-. 12
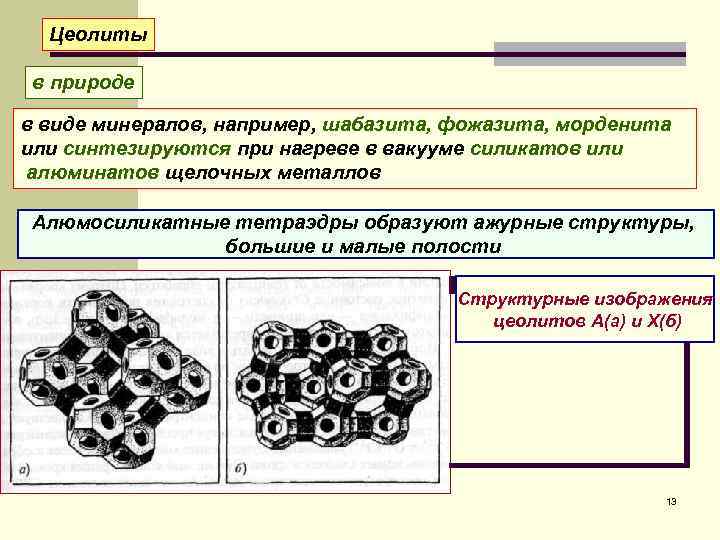 Цеолиты в природе в виде минералов, например, шабазита, фожазита, морденита или синтезируются при нагреве в вакууме силикатов или алюминатов щелочных металлов Алюмосиликатные тетраэдры образуют ажурные структуры, большие и малые полости Структурные изображения цеолитов А(а) и Х(б) 13
Цеолиты в природе в виде минералов, например, шабазита, фожазита, морденита или синтезируются при нагреве в вакууме силикатов или алюминатов щелочных металлов Алюмосиликатные тетраэдры образуют ажурные структуры, большие и малые полости Структурные изображения цеолитов А(а) и Х(б) 13
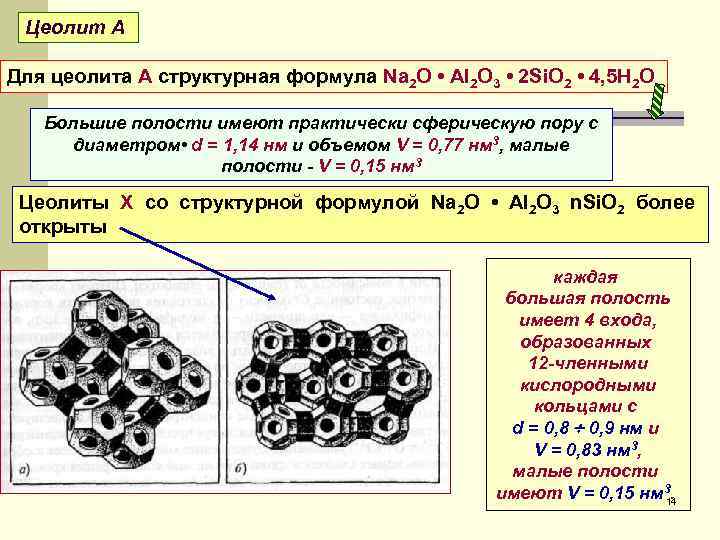 Цеолит А Для цеолита А структурная формула Na 2 O • Аl 2 О 3 • 2 Si. O 2 • 4, 5 Н 2 О Большие полости имеют практически сферическую пору с диаметром • d = 1, 14 нм и объемом V = 0, 77 нм 3, малые полости - V = 0, 15 нм 3 Цеолиты X со структурной формулой Na 2 O • Аl 2 О 3 n. Si. O 2 более открыты каждая большая полость имеет 4 входа, образованных 12 -членными кислородными кольцами с d = 0, 8 0, 9 нм и V = 0, 83 нм 3, малые полости имеют V = 0, 15 нм 3. 14
Цеолит А Для цеолита А структурная формула Na 2 O • Аl 2 О 3 • 2 Si. O 2 • 4, 5 Н 2 О Большие полости имеют практически сферическую пору с диаметром • d = 1, 14 нм и объемом V = 0, 77 нм 3, малые полости - V = 0, 15 нм 3 Цеолиты X со структурной формулой Na 2 O • Аl 2 О 3 n. Si. O 2 более открыты каждая большая полость имеет 4 входа, образованных 12 -членными кислородными кольцами с d = 0, 8 0, 9 нм и V = 0, 83 нм 3, малые полости имеют V = 0, 15 нм 3. 14


