lek_3_IBM_2013_k.ppt
- Количество слайдов: 27
 Лекция № 3 ОСНОВЫ КВАНТОВОЙ ТЕОРИИ АТОМА (окончание) (Мартинсон Л. К. , Смирнов Е. В. Квантовая физика. – М. : МГТУ им. Н. Э. Баумана, 2004)
Лекция № 3 ОСНОВЫ КВАНТОВОЙ ТЕОРИИ АТОМА (окончание) (Мартинсон Л. К. , Смирнов Е. В. Квантовая физика. – М. : МГТУ им. Н. Э. Баумана, 2004)
 Выражение в каждой скобке равно нулю, т. к. тождественное равенство нулю выполняется при всех r (3. 23) (3. 24) Подставим (3. 24) в (3. 23) (3. 25)
Выражение в каждой скобке равно нулю, т. к. тождественное равенство нулю выполняется при всех r (3. 23) (3. 24) Подставим (3. 24) в (3. 23) (3. 25)
 Формула (3. 25) полностью совпадает с формулой, полученной Бором. Первая волновая функция (3. 20) найдена: 1 – известна; A 1 определяется из условия нормировки (пространственная задача). В общем случае берем тройной интеграл, в s-состоянии: (3. 26)
Формула (3. 25) полностью совпадает с формулой, полученной Бором. Первая волновая функция (3. 20) найдена: 1 – известна; A 1 определяется из условия нормировки (пространственная задача). В общем случае берем тройной интеграл, в s-состоянии: (3. 26)
 Вероятность нахождения электрона в интервале Здесь функция плотности вероятности Из (3. 26) с учетом (3. 20)
Вероятность нахождения электрона в интервале Здесь функция плотности вероятности Из (3. 26) с учетом (3. 20)
 Обозначим = 2 1, тогда
Обозначим = 2 1, тогда
 Т. к. = 2 1, то Определим экстремум плотности вероятности
Т. к. = 2 1, то Определим экстремум плотности вероятности
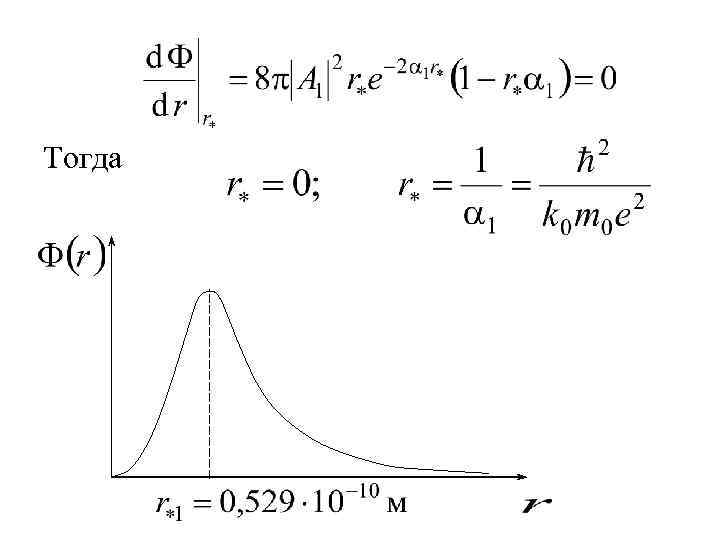 Тогда
Тогда
 Квантовая механика отказывается от понятия орбиты (траектории). Но r* совпадает с радиусом 1 -ой Боровской орбиты. Имеется определенная связь между результатами Бора и квантовой механики.
Квантовая механика отказывается от понятия орбиты (траектории). Но r* совпадает с радиусом 1 -ой Боровской орбиты. Имеется определенная связь между результатами Бора и квантовой механики.
 Волновые функции и квантовые числа Решение (3. 14) – в виде произведения двух функций с разделяющимися переменными Орбитальное квантовое число Магнитное квантовое число Вид волновой функции, определяющей квантовое состояние электрона в атоме:
Волновые функции и квантовые числа Решение (3. 14) – в виде произведения двух функций с разделяющимися переменными Орбитальное квантовое число Магнитное квантовое число Вид волновой функции, определяющей квантовое состояние электрона в атоме:
 Значение l 0 1 2 3 . . . Символ состояния s p d f . . . Cостояние с l = 0 – s-состояние, электрон в таком состоянии – s-электрон. Состояние с l = 1 – p-состояние и т. д. Электрон в квантовом состоянии с n = 2 и l = 0 обозначается символом 2 s, в состоянии с n = 4 и l = 2 – символом 4 d и т. д.
Значение l 0 1 2 3 . . . Символ состояния s p d f . . . Cостояние с l = 0 – s-состояние, электрон в таком состоянии – s-электрон. Состояние с l = 1 – p-состояние и т. д. Электрон в квантовом состоянии с n = 2 и l = 0 обозначается символом 2 s, в состоянии с n = 4 и l = 2 – символом 4 d и т. д.
 Поскольку всегда то возможны следующие состояния электрона и т. д. Все s-состояния электрона, то есть состояния с l = 0 и m = 0, – сферически симметричные. Волновая функция в них не зависит от θ и φ.
Поскольку всегда то возможны следующие состояния электрона и т. д. Все s-состояния электрона, то есть состояния с l = 0 и m = 0, – сферически симметричные. Волновая функция в них не зависит от θ и φ.
 Квантовые числа и их физический смысл Состояние электрона в атоме водорода (и квантовое состояние атома) полностью определяется заданием трех квантовых чисел. 1. Главное квантовое число определяет полную энергию электрона в любом квантовом состоянии 2. Орбитальное (азимутальное) квантовое число:
Квантовые числа и их физический смысл Состояние электрона в атоме водорода (и квантовое состояние атома) полностью определяется заданием трех квантовых чисел. 1. Главное квантовое число определяет полную энергию электрона в любом квантовом состоянии 2. Орбитальное (азимутальное) квантовое число:
 Модуль орбитального момента импульса движущегося в атоме электрона (3. 27) не совпадает с условием (3. 1) квантования момента импульса (теории Бора): В s-состояниях, в частности, в 1 sсостоянии, l = 0 и из (3. 27) получаем L = 0, что подтверждает опыт (в теории Бора L ≠ 0 ). В теории Бора: если время полного оборота электрона T, то такому движению соответствует замкнутый ток
Модуль орбитального момента импульса движущегося в атоме электрона (3. 27) не совпадает с условием (3. 1) квантования момента импульса (теории Бора): В s-состояниях, в частности, в 1 sсостоянии, l = 0 и из (3. 27) получаем L = 0, что подтверждает опыт (в теории Бора L ≠ 0 ). В теории Бора: если время полного оборота электрона T, то такому движению соответствует замкнутый ток
 магнитный момент которого Гиромагнитное отношение (3. 28) L r –e i pм где L= m 0 vr. Точный квантовомеханический расчет гиромагнитного отношения также приводит к (3. 28).
магнитный момент которого Гиромагнитное отношение (3. 28) L r –e i pм где L= m 0 vr. Точный квантовомеханический расчет гиромагнитного отношения также приводит к (3. 28).
 Модуль магнитного момента атома водорода (3. 29) где магнетон Бора Дж/Тл Правило отбора. Если атом переходит из одного квантового состояния в другое с испусканием (поглощением) фотона излучения, то возможны лишь те переходы, для которых l изменяется на единицу (для оптических переходов Δl = ± 1). n может меняться на любое целое число.
Модуль магнитного момента атома водорода (3. 29) где магнетон Бора Дж/Тл Правило отбора. Если атом переходит из одного квантового состояния в другое с испусканием (поглощением) фотона излучения, то возможны лишь те переходы, для которых l изменяется на единицу (для оптических переходов Δl = ± 1). n может меняться на любое целое число.
 Фотон уносит (вносит) не только квант энергии, но и момент импульса, изменяющий l для электрона всегда на 1. Разрешены переходы между s- и p-; p- и d-состояниями и т. д. 3. Магнитное квантовое число Проекция момента импульса электрона на выделенное в пространстве (обычно магнитным или электрическим внешним полем) направление z может иметь значения (3. 30)
Фотон уносит (вносит) не только квант энергии, но и момент импульса, изменяющий l для электрона всегда на 1. Разрешены переходы между s- и p-; p- и d-состояниями и т. д. 3. Магнитное квантовое число Проекция момента импульса электрона на выделенное в пространстве (обычно магнитным или электрическим внешним полем) направление z может иметь значения (3. 30)
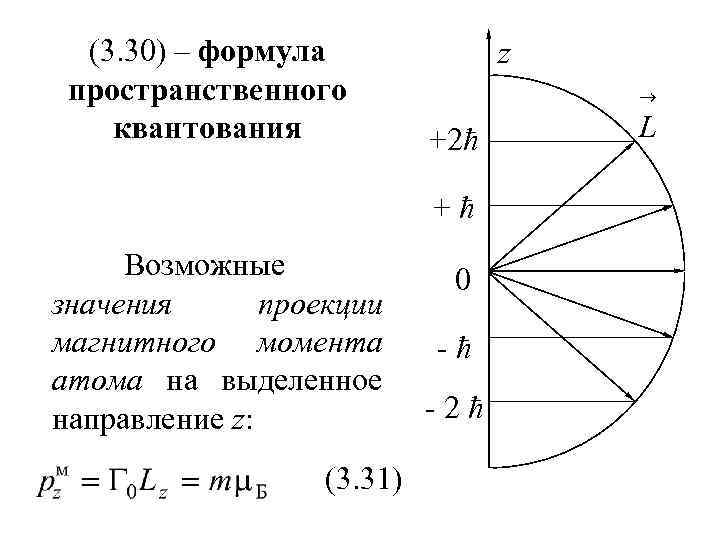 (3. 30) – формула пространственного квантования z +2ħ +ħ Возможные значения проекции магнитного момента атома на выделенное направление z: (3. 31) 0 -ħ -2ħ L
(3. 30) – формула пространственного квантования z +2ħ +ħ Возможные значения проекции магнитного момента атома на выделенное направление z: (3. 31) 0 -ħ -2ħ L
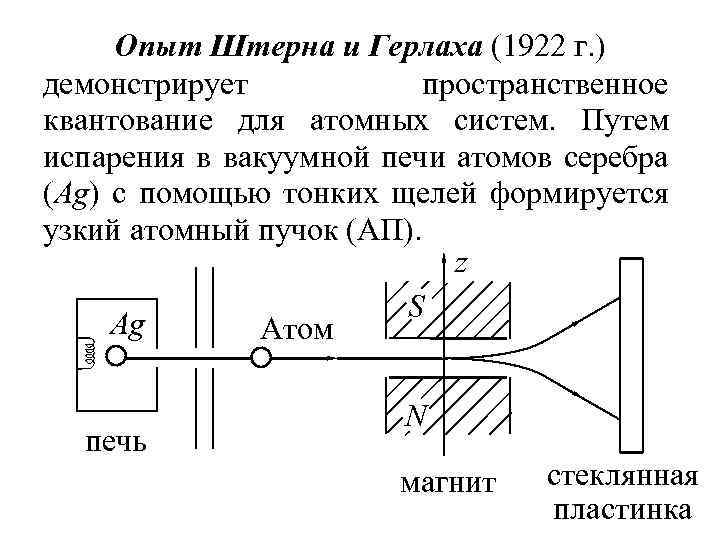 Опыт Штерна и Герлаха (1922 г. ) демонстрирует пространственное квантование для атомных систем. Путем испарения в вакуумной печи атомов серебра (Ag) с помощью тонких щелей формируется узкий атомный пучок (АП). z S Ag Атом печь N магнит стеклянная пластинка
Опыт Штерна и Герлаха (1922 г. ) демонстрирует пространственное квантование для атомных систем. Путем испарения в вакуумной печи атомов серебра (Ag) с помощью тонких щелей формируется узкий атомный пучок (АП). z S Ag Атом печь N магнит стеклянная пластинка
 АП пропускают через неоднородное магнитное поле (м. поле) с существенным градиентом магнитной индукции. Индукция м. поля в опыте велика и ↑↑ z. Поле создает магнит с ножевидным полюсным наконечником, вблизи которого проходит АП. S 0, 2 мм 1 мм АП z y N N.
АП пропускают через неоднородное магнитное поле (м. поле) с существенным градиентом магнитной индукции. Индукция м. поля в опыте велика и ↑↑ z. Поле создает магнит с ножевидным полюсным наконечником, вблизи которого проходит АП. S 0, 2 мм 1 мм АП z y N N.
 На пролетающие в зазоре магнита атомы вдоль направления м. поля действует сила (3. 32) которая отклоняет движущийся атом в направлении оси z тем больше, чем больше Fz. При этом одни атомы отклоняются вверх, а другие вниз. Согласно классической физике атомы Ag должны образовать сплошную широкую зеркальную полосу на стеклянной пластинке (из-за хаотичного теплового движения).
На пролетающие в зазоре магнита атомы вдоль направления м. поля действует сила (3. 32) которая отклоняет движущийся атом в направлении оси z тем больше, чем больше Fz. При этом одни атомы отклоняются вверх, а другие вниз. Согласно классической физике атомы Ag должны образовать сплошную широкую зеркальную полосу на стеклянной пластинке (из-за хаотичного теплового движения).
 Если имеет место пространственное принимает квантование и проекция определенные дискретные значения, то под действием силы Fz АП расщепится на дискретное число пучков, которые, оседая на стеклянной пластинке, дают серию узких дискретных зеркальных полосок из напыленных атомов. Что и наблюдалось в эксперименте. Опыт подтвердил наличие пространственного квантования магнитных моментов атомов.
Если имеет место пространственное принимает квантование и проекция определенные дискретные значения, то под действием силы Fz АП расщепится на дискретное число пучков, которые, оседая на стеклянной пластинке, дают серию узких дискретных зеркальных полосок из напыленных атомов. Что и наблюдалось в эксперименте. Опыт подтвердил наличие пространственного квантования магнитных моментов атомов.
 Спин электрона. Если в опыте Штерна - Герлаха в АП будут двигаться невозбужденные атомы (для них L = 0, pм =0), то такой АП не должен расщепляться м. полем и на стеклянной пластинке появится в центре одна узкая зеркальная полоска. Но в результате эксперимента пучок невозбужденных атомов Ag расщепился на два пучка, которые напылили на стеклянной пластинке две узкие зеркальные полоски, сдвинутые симметрично вверх и вниз.
Спин электрона. Если в опыте Штерна - Герлаха в АП будут двигаться невозбужденные атомы (для них L = 0, pм =0), то такой АП не должен расщепляться м. полем и на стеклянной пластинке появится в центре одна узкая зеркальная полоска. Но в результате эксперимента пучок невозбужденных атомов Ag расщепился на два пучка, которые напылили на стеклянной пластинке две узкие зеркальные полоски, сдвинутые симметрично вверх и вниз.
 Измерение этих сдвигов позволило определить магнитный момент невозбужденного атома Ag. Его проекция на направление магнитного поля оказалась равной +μБ или –μБ. Орбитальный, спиновый и полный угловые моменты Гипотеза о спине электрона (1925 г. , С. Гаудсмит и Дж. Уленбек): сам электрон является носителем “собственных” механического и магнитного моментов, не связанных с движением электрона в пространстве.
Измерение этих сдвигов позволило определить магнитный момент невозбужденного атома Ag. Его проекция на направление магнитного поля оказалась равной +μБ или –μБ. Орбитальный, спиновый и полный угловые моменты Гипотеза о спине электрона (1925 г. , С. Гаудсмит и Дж. Уленбек): сам электрон является носителем “собственных” механического и магнитного моментов, не связанных с движением электрона в пространстве.
 От англ. spin – кружение, верчение. Спин электрона не имеет классического аналога. Он характеризует внутреннее свойство квантовой частицы, связанное с наличием у нее дополнительной степени свободы. Количественная характеристика этой степени свободы – спин s = 1/2 является для электрона такой же величиной как, например, его масса m 0 и заряд e. Гаудсмит и Уленбек предположили, что по аналогии с орбитальными моментами, величины собственных механического Ls и моментов электрона магнитного
От англ. spin – кружение, верчение. Спин электрона не имеет классического аналога. Он характеризует внутреннее свойство квантовой частицы, связанное с наличием у нее дополнительной степени свободы. Количественная характеристика этой степени свободы – спин s = 1/2 является для электрона такой же величиной как, например, его масса m 0 и заряд e. Гаудсмит и Уленбек предположили, что по аналогии с орбитальными моментами, величины собственных механического Ls и моментов электрона магнитного
 (3. 33) (3. 34) Гиромагнитное отношение собственных механического и магнитного моментов (3. 35) в 2 раза больше гиромагнитного отношения для орбитального движения (3. 28).
(3. 33) (3. 34) Гиромагнитное отношение собственных механического и магнитного моментов (3. 35) в 2 раза больше гиромагнитного отношения для орбитального движения (3. 28).
 Проекции собственных моментов на выделенное направление z определяются спиновым квантовым числом (3. 36) (3. 37) Cостояние со спином, направленным вверх или вниз
Проекции собственных моментов на выделенное направление z определяются спиновым квантовым числом (3. 36) (3. 37) Cостояние со спином, направленным вверх или вниз
 Квантовое состояние электрона в атоме определяет набор четырех квантовых чисел Квантовое число Главное Символ n Возможные значения 1, 2, 3, . . . Орбитальное l 0, 1, 2, 3, … (n– 1) Магнитное m –l, …, – 1, 0, +1, …, +l Спиновое ms
Квантовое состояние электрона в атоме определяет набор четырех квантовых чисел Квантовое число Главное Символ n Возможные значения 1, 2, 3, . . . Орбитальное l 0, 1, 2, 3, … (n– 1) Магнитное m –l, …, – 1, 0, +1, …, +l Спиновое ms


