0d5624d75c76d2d4ec157422399749e2.ppt
- Количество слайдов: 133
 Лекция 3 Основные направления развития водородной энергетики. Водород – универсальный энергоноситель: его достоинства, недостатки, характеристики водорода как топлива. Производство водорода. Хранение и транспорт водорода. Использование водорода. Производство топливных элементов и энергоустановок на их основе. Топливный элемент: устройство и принцип его работы; виды топливных элементов; основные характеристики топливных элементов. Области применения топливных элементов. Водородная безопасность. 1
Лекция 3 Основные направления развития водородной энергетики. Водород – универсальный энергоноситель: его достоинства, недостатки, характеристики водорода как топлива. Производство водорода. Хранение и транспорт водорода. Использование водорода. Производство топливных элементов и энергоустановок на их основе. Топливный элемент: устройство и принцип его работы; виды топливных элементов; основные характеристики топливных элементов. Области применения топливных элементов. Водородная безопасность. 1
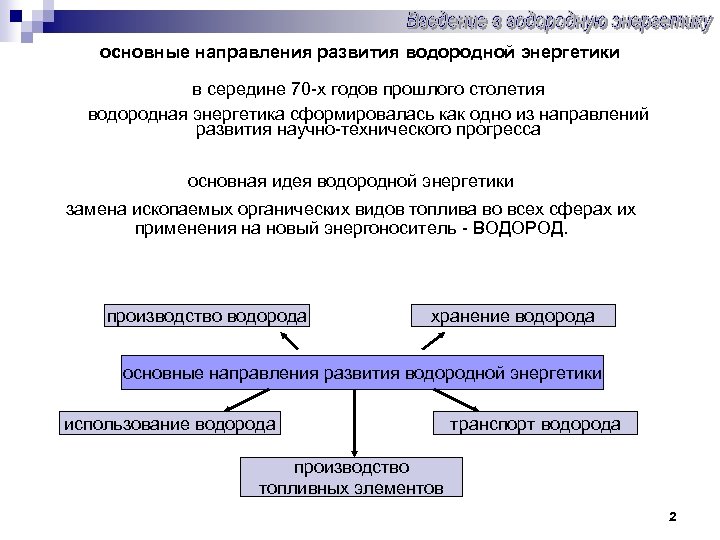 основные направления развития водородной энергетики в середине 70 -х годов прошлого столетия водородная энергетика сформировалась как одно из направлений развития научно-технического прогресса основная идея водородной энергетики замена ископаемых органических видов топлива во всех сферах их применения на новый энергоноситель - ВОДОРОД. производство водорода хранение водорода основные направления развития водородной энергетики использование водорода транспорт водорода производство топливных элементов 2
основные направления развития водородной энергетики в середине 70 -х годов прошлого столетия водородная энергетика сформировалась как одно из направлений развития научно-технического прогресса основная идея водородной энергетики замена ископаемых органических видов топлива во всех сферах их применения на новый энергоноситель - ВОДОРОД. производство водорода хранение водорода основные направления развития водородной энергетики использование водорода транспорт водорода производство топливных элементов 2
 водород история, происхождение названия Ø 1766 г. - открытие водорода английским физико-химиком Г. Кавендишом. При взаимодействии цинка с кислотами он наблюдал выделение газа, сгорающего на воздухе с образованием воды. Кавендиш исследовал этот газ и назвал его «горючим воздухом» . Ø 1783 г. - французский химик А. Лавуазье совместно с инженером Ж. Менье, используя специальные газометры, осуществили синтез воды, а затем и её анализ, они разложили водяной пар раскалённым железом. Таким образом они установил, что «горючий воздух» входит в состав воды и может быть из неё получен. Лавуазье дал водороду название hydrogène (от др. – греч. (ὕδωρ — «вода» и γενναω — «рождаю» ) - «рождающий воду» . Ø 1824 г. – химик М. Ф. Соловьев предложил русское наименование «водород» . 3
водород история, происхождение названия Ø 1766 г. - открытие водорода английским физико-химиком Г. Кавендишом. При взаимодействии цинка с кислотами он наблюдал выделение газа, сгорающего на воздухе с образованием воды. Кавендиш исследовал этот газ и назвал его «горючим воздухом» . Ø 1783 г. - французский химик А. Лавуазье совместно с инженером Ж. Менье, используя специальные газометры, осуществили синтез воды, а затем и её анализ, они разложили водяной пар раскалённым железом. Таким образом они установил, что «горючий воздух» входит в состав воды и может быть из неё получен. Лавуазье дал водороду название hydrogène (от др. – греч. (ὕδωρ — «вода» и γενναω — «рождаю» ) - «рождающий воду» . Ø 1824 г. – химик М. Ф. Соловьев предложил русское наименование «водород» . 3
 водород химический элемент Ø Водород H (Hydrogenium) - первый элемент периодической системы; Ø не имеет полной аналогии с остальными химическими элементами и не принадлежит ни к какой группе; Ø относительная атомная масса природной смеси водорода 1, 00797, атомный номер 1, валентность 1; Ø водород характеризуется наименьшими силами межмолекулярного взаимодействия по сравнению со всеми другими веществами, кроме гелия; Ø свойства водорода при обычных температурах и давлениях близки к свойствам идеального газа и хорошо подчиняются уравнению состояния идеального газа; Ø в обычных температурных условиях водород состоит из двух атомов (формула Н 2); Ø при высоких температурах (~ 2500 – 5000 К) образуется атомный водород, а при температурах ~105 К он заметно диссоциирует на протоны и электроны. 4
водород химический элемент Ø Водород H (Hydrogenium) - первый элемент периодической системы; Ø не имеет полной аналогии с остальными химическими элементами и не принадлежит ни к какой группе; Ø относительная атомная масса природной смеси водорода 1, 00797, атомный номер 1, валентность 1; Ø водород характеризуется наименьшими силами межмолекулярного взаимодействия по сравнению со всеми другими веществами, кроме гелия; Ø свойства водорода при обычных температурах и давлениях близки к свойствам идеального газа и хорошо подчиняются уравнению состояния идеального газа; Ø в обычных температурных условиях водород состоит из двух атомов (формула Н 2); Ø при высоких температурах (~ 2500 – 5000 К) образуется атомный водород, а при температурах ~105 К он заметно диссоциирует на протоны и электроны. 4
 водород химический элемент Ø в молекуле водорода атомы соединены весьма устойчивой ковалентной химической связью. Энергия разрыва одной связи Н - Н равна 4, 4776 э. В (1 э. В = 1, 60210· 10 -19 Дж), или 430, 95 к. Дж на 1 кмоль; Ø энергия ионизации молекулярного водорода составляет 1490 Дж/моль; сродство к электрону составляет 71 к. Дж/моль, межъядерное расстояние 1, 06· 10 -10 м; Ø атомы в молекуле водорода колеблются друг относительно друга с основной частотой 1, 32· 1014 Гц, причем эти колебания не вполне гармоничны; Ø в молекуле Н 2 электроны спарены, поэтому она диамагнитна. Ионы Н 2+ и Н 2 - имеют по одному неспаренному электрону, и поэтому они парамагнитны. 5
водород химический элемент Ø в молекуле водорода атомы соединены весьма устойчивой ковалентной химической связью. Энергия разрыва одной связи Н - Н равна 4, 4776 э. В (1 э. В = 1, 60210· 10 -19 Дж), или 430, 95 к. Дж на 1 кмоль; Ø энергия ионизации молекулярного водорода составляет 1490 Дж/моль; сродство к электрону составляет 71 к. Дж/моль, межъядерное расстояние 1, 06· 10 -10 м; Ø атомы в молекуле водорода колеблются друг относительно друга с основной частотой 1, 32· 1014 Гц, причем эти колебания не вполне гармоничны; Ø в молекуле Н 2 электроны спарены, поэтому она диамагнитна. Ионы Н 2+ и Н 2 - имеют по одному неспаренному электрону, и поэтому они парамагнитны. 5
 водород химический элемент Ø молекулярный водород нетоксичен; Ø он не имеет вкуса и запаха, бесцветен, легко воспламеняется и горит бледно – голубым слабосветящимся пламенем; Ø водород почти не растворим в полярных растворителях, но хорошо растворим в неполярных растворителях; Ø вследствие небольшой молярной массы водород обладает наибольшей из всех газов диффузионной и эффузионной способностями; Ø в широком диапазоне температур водород имеет наибольшую теплопроводность, которая, например, при температуре 25 ºС и атмосферном давлении примерно в 7 раз больше, чем у воздуха. Водород проводит тепло в 7 раз лучше воздуха. 6
водород химический элемент Ø молекулярный водород нетоксичен; Ø он не имеет вкуса и запаха, бесцветен, легко воспламеняется и горит бледно – голубым слабосветящимся пламенем; Ø водород почти не растворим в полярных растворителях, но хорошо растворим в неполярных растворителях; Ø вследствие небольшой молярной массы водород обладает наибольшей из всех газов диффузионной и эффузионной способностями; Ø в широком диапазоне температур водород имеет наибольшую теплопроводность, которая, например, при температуре 25 ºС и атмосферном давлении примерно в 7 раз больше, чем у воздуха. Водород проводит тепло в 7 раз лучше воздуха. 6
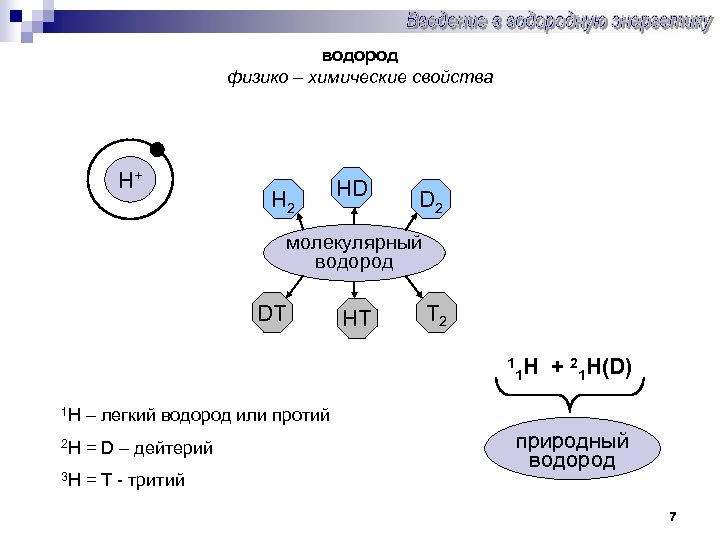 водород физико – химические свойства H+ Н 2 НD D 2 молекулярный водород DT НT T 2 1 1 H + 21 H(D) 1 Н – легкий водород или протий 2 Н = D – дейтерий 3 Н = Т - тритий природный водород 7
водород физико – химические свойства H+ Н 2 НD D 2 молекулярный водород DT НT T 2 1 1 H + 21 H(D) 1 Н – легкий водород или протий 2 Н = D – дейтерий 3 Н = Т - тритий природный водород 7
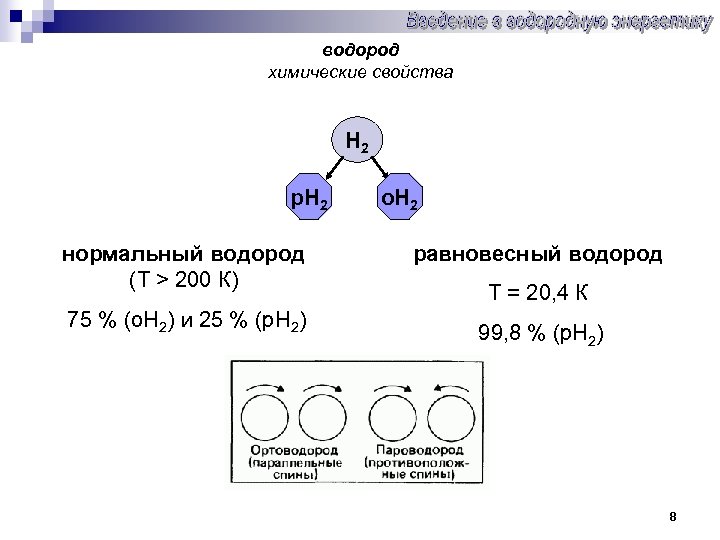 водород химические свойства Н 2 р. Н 2 нормальный водород (Т > 200 К) 75 % (о. Н 2) и 25 % (р. Н 2) о. Н 2 равновесный водород Т = 20, 4 К 99, 8 % (р. Н 2) 8
водород химические свойства Н 2 р. Н 2 нормальный водород (Т > 200 К) 75 % (о. Н 2) и 25 % (р. Н 2) о. Н 2 равновесный водород Т = 20, 4 К 99, 8 % (р. Н 2) 8
 водород самый лёгкий газ Ø водород легче воздуха в 14, 5 раз (очевидно, что чем меньше масса молекул, тем выше их скорость при одной и той же температуре); Ø как самые лёгкие, молекулы водорода движутся быстрее молекул любого другого газа и тем самым быстрее могут передавать теплоту от одного тела к другому. Отсюда следует, что водород обладает самой высокой теплопроводностью среди газообразных веществ. Его теплопроводность примерно в семь раз выше теплопроводности воздуха. 9
водород самый лёгкий газ Ø водород легче воздуха в 14, 5 раз (очевидно, что чем меньше масса молекул, тем выше их скорость при одной и той же температуре); Ø как самые лёгкие, молекулы водорода движутся быстрее молекул любого другого газа и тем самым быстрее могут передавать теплоту от одного тела к другому. Отсюда следует, что водород обладает самой высокой теплопроводностью среди газообразных веществ. Его теплопроводность примерно в семь раз выше теплопроводности воздуха. 9
 Жидкий водород Ø существует в очень узком интервале температур от − 252, 76 до − 259, 2 °C; Ø это бесцветная жидкость, очень лёгкая (плотность при − 253 °C 0, 0708 г/см 3) и текучая (вязкость при − 253 °C 13, 8 спуаз); Ø критические параметры водорода очень низкие: температура − 240, 2 °C и давление 12, 8 атм. Этим объясняются трудности при ожижении водорода; Ø в жидком состоянии равновесный водород состоит из 99, 79 % пара-Н 2, 0, 21 % орто-Н 2; Ø жидкий водород примерно в 15 раз легче воды; Ø он представляет собой прозрачную бесцветную легкоподвижную жидкость, которая не проводит электричество и обладает небольшим поверхностным натяжением. 10
Жидкий водород Ø существует в очень узком интервале температур от − 252, 76 до − 259, 2 °C; Ø это бесцветная жидкость, очень лёгкая (плотность при − 253 °C 0, 0708 г/см 3) и текучая (вязкость при − 253 °C 13, 8 спуаз); Ø критические параметры водорода очень низкие: температура − 240, 2 °C и давление 12, 8 атм. Этим объясняются трудности при ожижении водорода; Ø в жидком состоянии равновесный водород состоит из 99, 79 % пара-Н 2, 0, 21 % орто-Н 2; Ø жидкий водород примерно в 15 раз легче воды; Ø он представляет собой прозрачную бесцветную легкоподвижную жидкость, которая не проводит электричество и обладает небольшим поверхностным натяжением. 10
 Твердый водород Ø образуется при охлаждении водорода до -259 ºС; Ø твердый водород представляет собой белую пенообразную или снегоподобную массу, плотность которой в 12 раз меньше плотности воды (т. е. температура плавления − 259, 2 °C, плотность твердого водорода 0, 0807 г/см 3 (при − 262 °C). 11
Твердый водород Ø образуется при охлаждении водорода до -259 ºС; Ø твердый водород представляет собой белую пенообразную или снегоподобную массу, плотность которой в 12 раз меньше плотности воды (т. е. температура плавления − 259, 2 °C, плотность твердого водорода 0, 0807 г/см 3 (при − 262 °C). 11
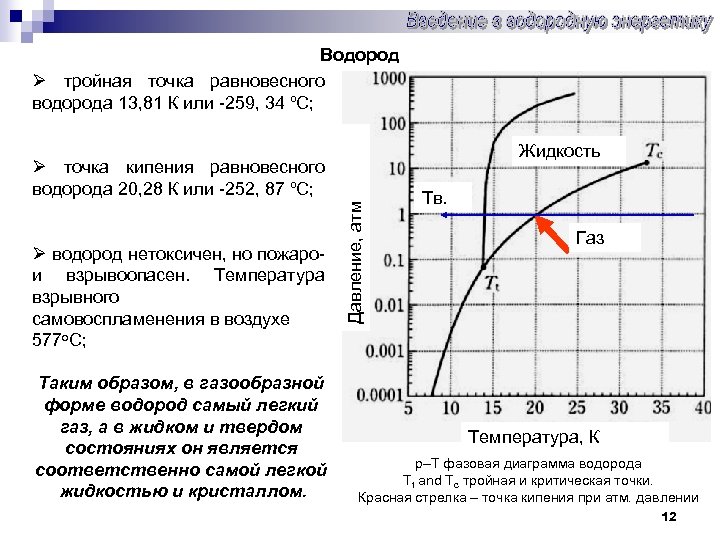 Водород Ø тройная точка равновесного водорода 13, 81 К или -259, 34 ºС; Жидкость Ø водород нетоксичен, но пожаро- и взрывоопасен. Температура взрывного самовоспламенения в воздухе 577 о. С; Таким образом, в газообразной форме водород самый легкий газ, а в жидком и твердом состояниях он является соответственно самой легкой жидкостью и кристаллом. Давление, атм Ø точка кипения равновесного водорода 20, 28 К или -252, 87 ºС; Тв. Газ Температура, К p–T фазовая диаграмма водорода Tt and Tc тройная и критическая точки. Красная стрелка – точка кипения при атм. давлении 12
Водород Ø тройная точка равновесного водорода 13, 81 К или -259, 34 ºС; Жидкость Ø водород нетоксичен, но пожаро- и взрывоопасен. Температура взрывного самовоспламенения в воздухе 577 о. С; Таким образом, в газообразной форме водород самый легкий газ, а в жидком и твердом состояниях он является соответственно самой легкой жидкостью и кристаллом. Давление, атм Ø точка кипения равновесного водорода 20, 28 К или -252, 87 ºС; Тв. Газ Температура, К p–T фазовая диаграмма водорода Tt and Tc тройная и критическая точки. Красная стрелка – точка кипения при атм. давлении 12
 водород химические свойства шугообразное состояние водорода При охлаждении водорода до температуры ниже температуры тройной точки (Т=33, 0 К) водород переходит в твердое состояние. А при температурах несколько выше температуры тройной точки возможно получение смеси твердого водорода с жидким. Именно такую смесь, которая представляет собой суспензию, и принято называть шугообразный водород. 13
водород химические свойства шугообразное состояние водорода При охлаждении водорода до температуры ниже температуры тройной точки (Т=33, 0 К) водород переходит в твердое состояние. А при температурах несколько выше температуры тройной точки возможно получение смеси твердого водорода с жидким. Именно такую смесь, которая представляет собой суспензию, и принято называть шугообразный водород. 13
 водород физико – химические свойства водород восстановитель реже как окислитель реакция диссоциации водорода Н 2 → 2 Н, ∆Но = 432, 1 к. Дж/кмоль 14
водород физико – химические свойства водород восстановитель реже как окислитель реакция диссоциации водорода Н 2 → 2 Н, ∆Но = 432, 1 к. Дж/кмоль 14
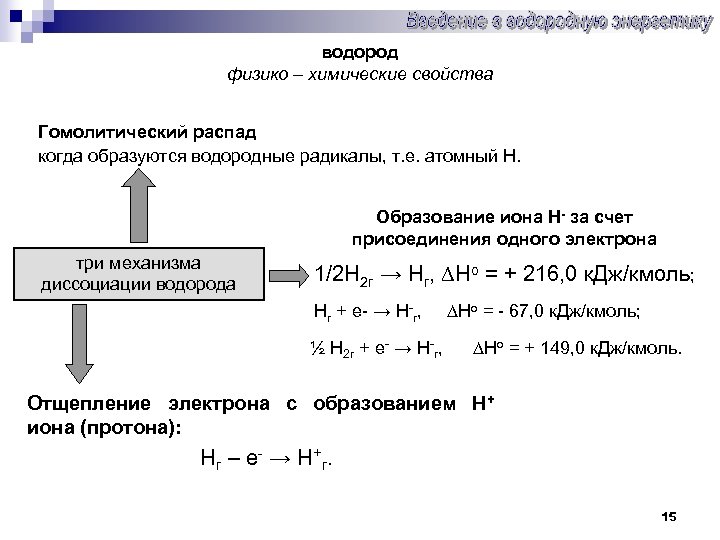 водород физико – химические свойства Гомолитический распад когда образуются водородные радикалы, т. е. атомный Н. Образование иона Н- за счет присоединения одного электрона три механизма диссоциации водорода 1/2 Н 2 г → Нг, ∆Но = + 216, 0 к. Дж/кмоль; о Нг + е- → Н г, ∆Н = - 67, 0 к. Дж/кмоль; ½ Н 2 г + е- → Н-г, ∆Но = + 149, 0 к. Дж/кмоль. Отщепление электрона с образованием Н+ иона (протона): Нг – е- → Н+г. 15
водород физико – химические свойства Гомолитический распад когда образуются водородные радикалы, т. е. атомный Н. Образование иона Н- за счет присоединения одного электрона три механизма диссоциации водорода 1/2 Н 2 г → Нг, ∆Но = + 216, 0 к. Дж/кмоль; о Нг + е- → Н г, ∆Н = - 67, 0 к. Дж/кмоль; ½ Н 2 г + е- → Н-г, ∆Но = + 149, 0 к. Дж/кмоль. Отщепление электрона с образованием Н+ иона (протона): Нг – е- → Н+г. 15
 водород химические свойства Ø водород обладает признаками, которые свойственны элементам первой и последней групп периодической системы химических элементов; Ø двойственное положение водорода в таблице элементов объясняется тем, что в химических соединениях водород обычно имеет положительную валентность, а следовательно ведет себя подобно щелочному металлу, однако в гидридах ион водорода отрицательно одновалентен; Ø многие соединения водорода с металлоидами при комнатной температуре являются газами; Ø соединения водорода с металлами в обычных условиях находятся в кристаллическом состоянии. 16
водород химические свойства Ø водород обладает признаками, которые свойственны элементам первой и последней групп периодической системы химических элементов; Ø двойственное положение водорода в таблице элементов объясняется тем, что в химических соединениях водород обычно имеет положительную валентность, а следовательно ведет себя подобно щелочному металлу, однако в гидридах ион водорода отрицательно одновалентен; Ø многие соединения водорода с металлоидами при комнатной температуре являются газами; Ø соединения водорода с металлами в обычных условиях находятся в кристаллическом состоянии. 16
 водород химические свойства Ø водород обладает сильными восстановительными свойствами, он может отнимать кислород или галогены от многих металлов и металлоидов; Øно при 25 ºС и 0, 1 МПа его химическая активность невелика, и в этих условиях он медленно реагирует даже с кислородом (а вот при Т=550 ºС эта реакция носит взрывной характер); Øбез нагрева водород способен реагировать лишь с фтором и хлором (на свету). И с металлоидами он более активен, чем с металлами; Øпри повышенных температурах водород вступает в соединения со многими элементами; 17
водород химические свойства Ø водород обладает сильными восстановительными свойствами, он может отнимать кислород или галогены от многих металлов и металлоидов; Øно при 25 ºС и 0, 1 МПа его химическая активность невелика, и в этих условиях он медленно реагирует даже с кислородом (а вот при Т=550 ºС эта реакция носит взрывной характер); Øбез нагрева водород способен реагировать лишь с фтором и хлором (на свету). И с металлоидами он более активен, чем с металлами; Øпри повышенных температурах водород вступает в соединения со многими элементами; 17
 водород химические свойства Ø реакционная способность водорода возрастает под действием света (ультрафиолетовые лучи), также под действием электрической искры и электроразряда, кроме того в присутствии катализаторов, под действием элементарных частиц атомного распада; Ø повышенная реакционная способность водорода в момент его выделения объясняется тем, что при этом реагируют не только молекулы, но и атомы водорода; Ø атомный водород уже при комнатной температуре соединяется с серой, фосфором, мышьяком, кроме того при комнатной температуре он восстанавливает оксиды ряда металлов, а также вытесняет некоторые металлы (Cu, Pb, Ag и др. ) из их солей. 18
водород химические свойства Ø реакционная способность водорода возрастает под действием света (ультрафиолетовые лучи), также под действием электрической искры и электроразряда, кроме того в присутствии катализаторов, под действием элементарных частиц атомного распада; Ø повышенная реакционная способность водорода в момент его выделения объясняется тем, что при этом реагируют не только молекулы, но и атомы водорода; Ø атомный водород уже при комнатной температуре соединяется с серой, фосфором, мышьяком, кроме того при комнатной температуре он восстанавливает оксиды ряда металлов, а также вытесняет некоторые металлы (Cu, Pb, Ag и др. ) из их солей. 18
 водород химические свойства основные реакции с водородом: 1. Цепная реакция с кислородом: 2 Н 2 + О → 2 Н 2 Ожид, Н = - 286, 4 к. Дж/кмоль; Н 2 + О → 2 ОН, Н = +46, 0 к. Дж/кмоль; ОН + Н 2 → Н 2 О+ Н, Н = - 50, 0 к. Дж/кмоль; О 2 + Н → ОН + О, Н = + 71 к. Дж/кмоль; О + Н 2 → ОН + Н, Н = + 13 к. Дж/кмоль; 19
водород химические свойства основные реакции с водородом: 1. Цепная реакция с кислородом: 2 Н 2 + О → 2 Н 2 Ожид, Н = - 286, 4 к. Дж/кмоль; Н 2 + О → 2 ОН, Н = +46, 0 к. Дж/кмоль; ОН + Н 2 → Н 2 О+ Н, Н = - 50, 0 к. Дж/кмоль; О 2 + Н → ОН + О, Н = + 71 к. Дж/кмоль; О + Н 2 → ОН + Н, Н = + 13 к. Дж/кмоль; 19
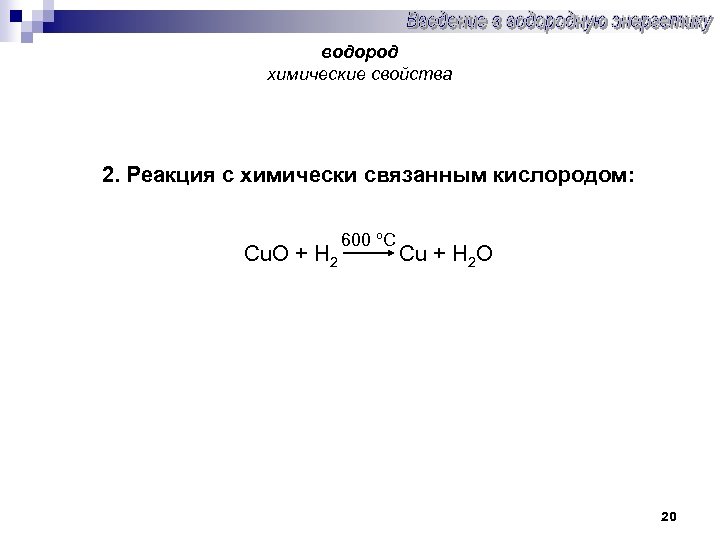 водород химические свойства 2. Реакция с химически связанным кислородом: 600 ºC Cu. O + H 2 Cu + H 2 O 20
водород химические свойства 2. Реакция с химически связанным кислородом: 600 ºC Cu. O + H 2 Cu + H 2 O 20
 водород химические свойства 3. Реакция с азотом и хлором: 3 Н 2 + N 2 ↔ 2 NH 3, H = -92, 5 к. Дж/кмоль; H 2 + Cl 2 ↔ 2 HCl, H = - 183, 4 к. Дж/кмоль. 21
водород химические свойства 3. Реакция с азотом и хлором: 3 Н 2 + N 2 ↔ 2 NH 3, H = -92, 5 к. Дж/кмоль; H 2 + Cl 2 ↔ 2 HCl, H = - 183, 4 к. Дж/кмоль. 21
 водород химические свойства 4. Реакции с бором и элементами главных подгрупп IV – VII групп периодической системы приводят к образованию легколетучих гидридов (гидриды бора, углеводороды, кремневодороды, фосфины, сероводород, аммиак, галогеноводороды). 22
водород химические свойства 4. Реакции с бором и элементами главных подгрупп IV – VII групп периодической системы приводят к образованию легколетучих гидридов (гидриды бора, углеводороды, кремневодороды, фосфины, сероводород, аммиак, галогеноводороды). 22
 водород химические свойства 5. Реакции с элементами главных подгрупп I и II групп периодической системы: приводят к образованию солеобразных гидридов (например, Li. H, Ca. H 2, Sr. H 2, Ba. H 2): Ca + H 2 → Ca. H 2, 2 Na + H 2 → 2 Na. H. В виде ионов Н- водород находится в соединениях с рядом металлов (натрий, кальций, магний и др. ), которые легко отдают ему электроны. Приведенные здесь реакции протекают в атмосфере водорода и при нагревании металлов. 23
водород химические свойства 5. Реакции с элементами главных подгрупп I и II групп периодической системы: приводят к образованию солеобразных гидридов (например, Li. H, Ca. H 2, Sr. H 2, Ba. H 2): Ca + H 2 → Ca. H 2, 2 Na + H 2 → 2 Na. H. В виде ионов Н- водород находится в соединениях с рядом металлов (натрий, кальций, магний и др. ), которые легко отдают ему электроны. Приведенные здесь реакции протекают в атмосфере водорода и при нагревании металлов. 23
 водород химические свойства 6. Реакции образования комплексных гидридов: 1) гидриды с элементами главных подгрупп: Na[BH 4], Li[Ga. H 4], U[BH 4]4, Al[BH 4]3, Na[BH(OCH 3)]3; 2) гидриды с переходными элементами: Re. Hg 2 -, [Rh(en)2 Cl. H]+, [Rh(en)2 H 2]+, Mn(CO)5 H, Fe(CO)4 H 2, Fe(CO)4 H, Co(CO)4 H, Re(C 2 H 5)2 H, W(C 2 H 5)2 H 2, Ta(C 2 H 5)2 H 2 и др. 24
водород химические свойства 6. Реакции образования комплексных гидридов: 1) гидриды с элементами главных подгрупп: Na[BH 4], Li[Ga. H 4], U[BH 4]4, Al[BH 4]3, Na[BH(OCH 3)]3; 2) гидриды с переходными элементами: Re. Hg 2 -, [Rh(en)2 Cl. H]+, [Rh(en)2 H 2]+, Mn(CO)5 H, Fe(CO)4 H 2, Fe(CO)4 H, Co(CO)4 H, Re(C 2 H 5)2 H, W(C 2 H 5)2 H 2, Ta(C 2 H 5)2 H 2 и др. 24
 водород химические свойства 7. Реакции с металлами побочных подгрупп I – VIII групп периодической системы: приводят к образованию металлоподобных гидридов – твердых веществ с металлическими свойствами, а также соединений или твердых растворов. Металлоподобные или металлообразные гидриды – это в основном твердые растворы водорода в металлах. По своим свойствам и характеру химической связи эти гидриды схожи с металлами. 25
водород химические свойства 7. Реакции с металлами побочных подгрупп I – VIII групп периодической системы: приводят к образованию металлоподобных гидридов – твердых веществ с металлическими свойствами, а также соединений или твердых растворов. Металлоподобные или металлообразные гидриды – это в основном твердые растворы водорода в металлах. По своим свойствам и характеру химической связи эти гидриды схожи с металлами. 25
 водород – как универсальный энергоноситель характеристики водорода как энергоносителя и топлива: ü водород химически активен; ü как топливо он имеет высокое содержание энергии на единицу массы: 120, 7 ГДж/т, что выше, чем у любого органического топлива; ü при соединении водорода с кислородом в электрохимическом генераторе (ЭХГ) происходит прямое преобразование химической энергии в электричество с высоким коэффициентом полезного действия; 26
водород – как универсальный энергоноситель характеристики водорода как энергоносителя и топлива: ü водород химически активен; ü как топливо он имеет высокое содержание энергии на единицу массы: 120, 7 ГДж/т, что выше, чем у любого органического топлива; ü при соединении водорода с кислородом в электрохимическом генераторе (ЭХГ) происходит прямое преобразование химической энергии в электричество с высоким коэффициентом полезного действия; 26
 водород – как универсальный энергоноситель характеристики водорода как энергоносителя и топлива: ü водород обладает широким диапазоном воспламенения, высокой температурой сгорания; ü скорость распространения ламинарного пламени для водорода в 10 раз выше, а минимальная энергия, необходимая для индуцирования воспламенения в 16 раз меньше, чем у метана; ü важным достоинством водорода как топлива является отсутствие в продуктах сгорания окиси углерода и радикалов CHx. При сжигании водорода в чистом кислороде единственными продуктами являются высокопотенциальное тепло и вода, из которой этот водород опять же можно получать. 27
водород – как универсальный энергоноситель характеристики водорода как энергоносителя и топлива: ü водород обладает широким диапазоном воспламенения, высокой температурой сгорания; ü скорость распространения ламинарного пламени для водорода в 10 раз выше, а минимальная энергия, необходимая для индуцирования воспламенения в 16 раз меньше, чем у метана; ü важным достоинством водорода как топлива является отсутствие в продуктах сгорания окиси углерода и радикалов CHx. При сжигании водорода в чистом кислороде единственными продуктами являются высокопотенциальное тепло и вода, из которой этот водород опять же можно получать. 27
 характеристика природных источников водорода Ø Водород – наиболее распространенный элемент во Вселенной; Øна долю водорода приходится около 92% всех атомов (8% составляют атомы гелия, доля всех остальных вместе взятых элементов — менее 0, 1%); Ø водород - основная составная часть звёзд и межзвёздного газа. В условиях звёздных температур (например, температура поверхности Солнца ~ 6000 °С) и межзвёздного пространства, которое пронизано космическим излучением, этот элемент существует в виде отдельных атомов; Ø в земной коре из каждых 100 атомов 15 приходится на водород. В плотной части земной коры (16 км), включая воду и атмосферу, содержится примерно 0, 88 % (масс. ) или 15, 4 % (ат. ) водорода; Øсолнце содержит 57 % (масс. ) водорода и 40% гелия. 28
характеристика природных источников водорода Ø Водород – наиболее распространенный элемент во Вселенной; Øна долю водорода приходится около 92% всех атомов (8% составляют атомы гелия, доля всех остальных вместе взятых элементов — менее 0, 1%); Ø водород - основная составная часть звёзд и межзвёздного газа. В условиях звёздных температур (например, температура поверхности Солнца ~ 6000 °С) и межзвёздного пространства, которое пронизано космическим излучением, этот элемент существует в виде отдельных атомов; Ø в земной коре из каждых 100 атомов 15 приходится на водород. В плотной части земной коры (16 км), включая воду и атмосферу, содержится примерно 0, 88 % (масс. ) или 15, 4 % (ат. ) водорода; Øсолнце содержит 57 % (масс. ) водорода и 40% гелия. 28
 характеристика природных источников водорода Ø практически весь водород на Земле находится в виде соединений; Ø в свободном состоянии водород встречается крайне редко, лишь в очень незначительном количестве (в виде простого вещества водород содержится в атмосфере в количестве 5· 10 -5 % по объёму); Ø водород выделяется в свободном состоянии при извержении вулканов, находится в газообразных продуктах выделения фумарола, а также присутствует в виде включений в калийных солях, некоторых других минералах, в изверженных горных породах (гранит, гнейсы, базальты); Ø свободный водород содержится в некоторых природных и попутных газах ряда нефтяных месторождений, однако в результате геологических процессов в атмосферу переходит гораздо меньше водорода, чем от биологических превращений; 29
характеристика природных источников водорода Ø практически весь водород на Земле находится в виде соединений; Ø в свободном состоянии водород встречается крайне редко, лишь в очень незначительном количестве (в виде простого вещества водород содержится в атмосфере в количестве 5· 10 -5 % по объёму); Ø водород выделяется в свободном состоянии при извержении вулканов, находится в газообразных продуктах выделения фумарола, а также присутствует в виде включений в калийных солях, некоторых других минералах, в изверженных горных породах (гранит, гнейсы, базальты); Ø свободный водород содержится в некоторых природных и попутных газах ряда нефтяных месторождений, однако в результате геологических процессов в атмосферу переходит гораздо меньше водорода, чем от биологических превращений; 29
 характеристика природных источников водорода Ø ежегодно в почве, водоемах разлагаются миллионы тонн растительных остатков, например целлюлозы, белковых веществ и т. д. и происходит разложение их некоторыми видами анаэробных бактерий. Эти процессы дают значительное количество свободного водорода; Ø в природе водород находится в соединении со многими элементами: кислородом, серой, азотом, хлором, реже с фосфором, йодом, бромом и др. элементами; Ø водород входит в состав пресной воды (11, 19 %), морской воды (10, 72%), различных соединений, образующих угли, нефть, природные газы, а также организмы животных и растений, т. е. входит в состав белков, нуклеиновых кислот, жиров, углеводородов и др. сложных соединений. 30
характеристика природных источников водорода Ø ежегодно в почве, водоемах разлагаются миллионы тонн растительных остатков, например целлюлозы, белковых веществ и т. д. и происходит разложение их некоторыми видами анаэробных бактерий. Эти процессы дают значительное количество свободного водорода; Ø в природе водород находится в соединении со многими элементами: кислородом, серой, азотом, хлором, реже с фосфором, йодом, бромом и др. элементами; Ø водород входит в состав пресной воды (11, 19 %), морской воды (10, 72%), различных соединений, образующих угли, нефть, природные газы, а также организмы животных и растений, т. е. входит в состав белков, нуклеиновых кислот, жиров, углеводородов и др. сложных соединений. 30
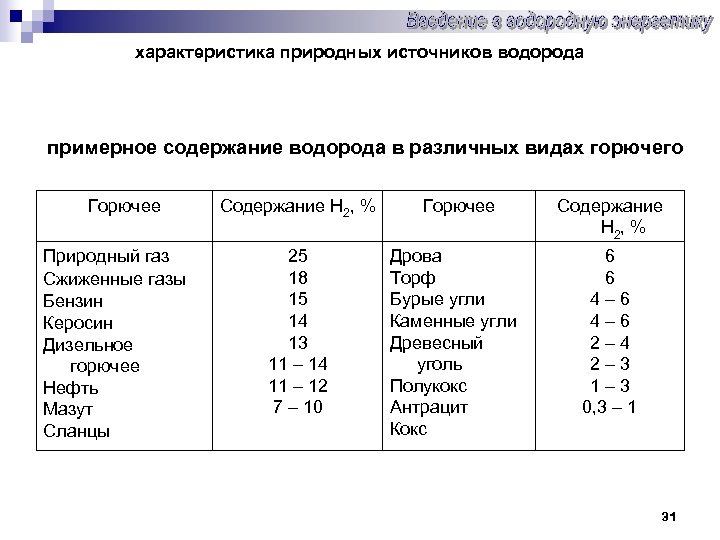 характеристика природных источников водорода примерное содержание водорода в различных видах горючего Горючее Природный газ Сжиженные газы Бензин Керосин Дизельное горючее Нефть Мазут Сланцы Содержание Н 2, % 25 18 15 14 13 11 – 14 11 – 12 7 – 10 Горючее Дрова Торф Бурые угли Каменные угли Древесный уголь Полукокс Антрацит Кокс Содержание Н 2, % 6 6 4 – 6 2 – 4 2 – 3 1 – 3 0, 3 – 1 31
характеристика природных источников водорода примерное содержание водорода в различных видах горючего Горючее Природный газ Сжиженные газы Бензин Керосин Дизельное горючее Нефть Мазут Сланцы Содержание Н 2, % 25 18 15 14 13 11 – 14 11 – 12 7 – 10 Горючее Дрова Торф Бурые угли Каменные угли Древесный уголь Полукокс Антрацит Кокс Содержание Н 2, % 6 6 4 – 6 2 – 4 2 – 3 1 – 3 0, 3 – 1 31
 преимущества и недостатки водородного топлива ü водород выступает в качестве альтернативы традиционным ископаемым топливам; ü неисчерпаемость водорода (в Мировом океане содержится 1, 2× 1013 тонн водорода, суммарная масса водорода составляет 1% от общей массы Земли); ü экологичность водорода (самое важное, пожалуй то, что водород при сгорании превращается в воду и возвращается в круговорот веществ в природе); 32
преимущества и недостатки водородного топлива ü водород выступает в качестве альтернативы традиционным ископаемым топливам; ü неисчерпаемость водорода (в Мировом океане содержится 1, 2× 1013 тонн водорода, суммарная масса водорода составляет 1% от общей массы Земли); ü экологичность водорода (самое важное, пожалуй то, что водород при сгорании превращается в воду и возвращается в круговорот веществ в природе); 32
 преимущества и недостатки водородного топлива üкроме того, если использовать водород как топливо, то не возникает парникового эффекта (при сгорании выделяется вода, а не углекислый газ); водород легко улетучивается, а значит не возникает застойных зон; ü высокая весовая теплотворная способность водорода (она составляет 28630 ккал/кг), что в 2, 8 раза выше по сравнению, например, с бензином; ü энергия воспламенения водорода в 15 раз меньше, чем для углеводородного топлива. Однако, ни один вид топлива не может не иметь недостатков или скрытых опасностей при использовании. 33
преимущества и недостатки водородного топлива üкроме того, если использовать водород как топливо, то не возникает парникового эффекта (при сгорании выделяется вода, а не углекислый газ); водород легко улетучивается, а значит не возникает застойных зон; ü высокая весовая теплотворная способность водорода (она составляет 28630 ккал/кг), что в 2, 8 раза выше по сравнению, например, с бензином; ü энергия воспламенения водорода в 15 раз меньше, чем для углеводородного топлива. Однако, ни один вид топлива не может не иметь недостатков или скрытых опасностей при использовании. 33
 недостатки водородного топлива ü водород более взрывоопасен, чем, например, метан; ü объемная теплота сгорания водорода в три раза меньше, чем у природного газа; ü относительно высокая цена при промышленном получении водорода (два основных направления получения водорода - электролиз и плазмохимия. При электролизе для получения одного кубометра водорода требуется 4 - 5 киловатт-часов электроэнергии. Это дорого. Например, производство такого же количества бензина обходится примерно втрое дешевле). И всё же преимуществ у водородного топлива гораздо больше, чем недостатков. Таким образом, водород является перспективной заменой используемым сейчас источникам энергии. 34
недостатки водородного топлива ü водород более взрывоопасен, чем, например, метан; ü объемная теплота сгорания водорода в три раза меньше, чем у природного газа; ü относительно высокая цена при промышленном получении водорода (два основных направления получения водорода - электролиз и плазмохимия. При электролизе для получения одного кубометра водорода требуется 4 - 5 киловатт-часов электроэнергии. Это дорого. Например, производство такого же количества бензина обходится примерно втрое дешевле). И всё же преимуществ у водородного топлива гораздо больше, чем недостатков. Таким образом, водород является перспективной заменой используемым сейчас источникам энергии. 34
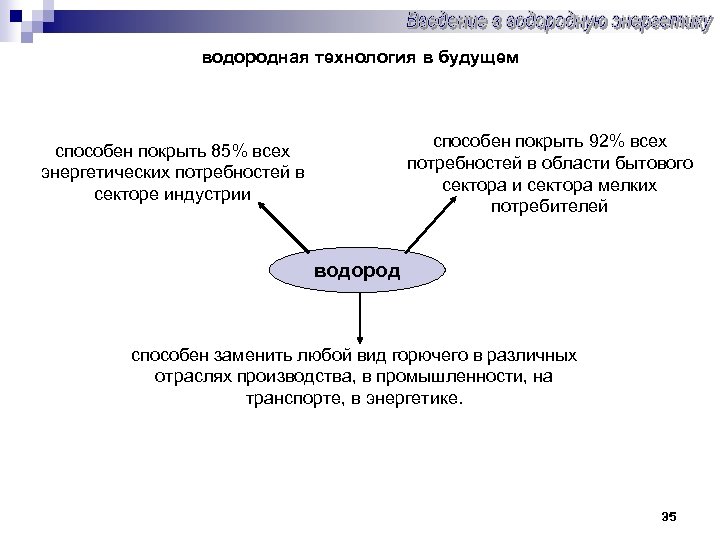 водородная технология в будущем способен покрыть 92% всех потребностей в области бытового сектора и сектора мелких потребителей способен покрыть 85% всех энергетических потребностей в секторе индустрии водород способен заменить любой вид горючего в различных отраслях производства, в промышленности, на транспорте, в энергетике. 35
водородная технология в будущем способен покрыть 92% всех потребностей в области бытового сектора и сектора мелких потребителей способен покрыть 85% всех энергетических потребностей в секторе индустрии водород способен заменить любой вид горючего в различных отраслях производства, в промышленности, на транспорте, в энергетике. 35
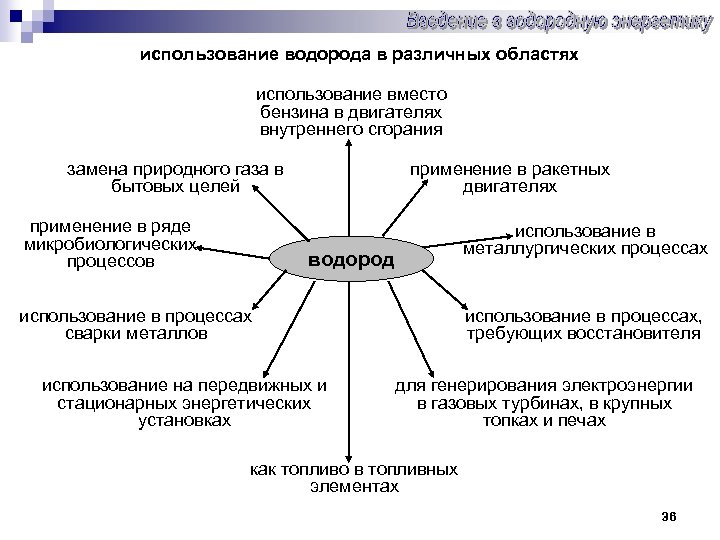 использование водорода в различных областях использование вместо бензина в двигателях внутреннего сгорания замена природного газа в бытовых целей применение в ряде микробиологических процессов применение в ракетных двигателях водород использование в металлургических процессах использование в процессах сварки металлов использование на передвижных и стационарных энергетических установках использование в процессах, требующих восстановителя для генерирования электроэнергии в газовых турбинах, в крупных топках и печах как топливо в топливных элементах 36
использование водорода в различных областях использование вместо бензина в двигателях внутреннего сгорания замена природного газа в бытовых целей применение в ряде микробиологических процессов применение в ракетных двигателях водород использование в металлургических процессах использование в процессах сварки металлов использование на передвижных и стационарных энергетических установках использование в процессах, требующих восстановителя для генерирования электроэнергии в газовых турбинах, в крупных топках и печах как топливо в топливных элементах 36
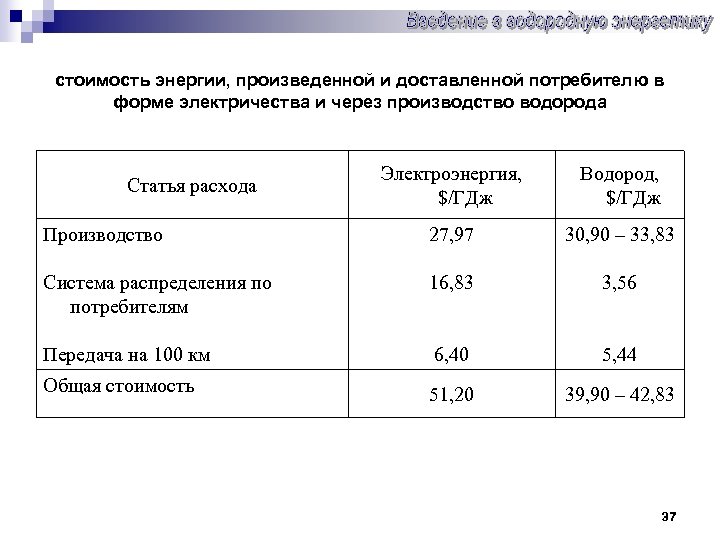 стоимость энергии, произведенной и доставленной потребителю в форме электричества и через производство водорода Электроэнергия, $/ГДж Водород, $/ГДж Производство 27, 97 30, 90 – 33, 83 Система распределения по потребителям 16, 83 3, 56 Передача на 100 км 6, 40 5, 44 Общая стоимость 51, 20 39, 90 – 42, 83 Статья расхода 37
стоимость энергии, произведенной и доставленной потребителю в форме электричества и через производство водорода Электроэнергия, $/ГДж Водород, $/ГДж Производство 27, 97 30, 90 – 33, 83 Система распределения по потребителям 16, 83 3, 56 Передача на 100 км 6, 40 5, 44 Общая стоимость 51, 20 39, 90 – 42, 83 Статья расхода 37
 рациональная энергетическая система на электричестве на водороде (использование в процессах автоматизации, механизации, освещения, передачи информации, в системах управления ) основными областями применения которого станут транспорт, быт, такие отрасли промышленности как химия и металлургия, а также энергетика 38
рациональная энергетическая система на электричестве на водороде (использование в процессах автоматизации, механизации, освещения, передачи информации, в системах управления ) основными областями применения которого станут транспорт, быт, такие отрасли промышленности как химия и металлургия, а также энергетика 38
 водородная энергетика ü переход транспорта, промышленности и бытовых потребителей на водород – это путь, который приведет к возможности решить глобальные проблемы, касающиеся охраны окружающей среды (защита окружающей среды от различных отравлений, которые вызваны выбросами оксида углерода и азота, оксидами серы, углеводородами, также от вековых накоплений в атмосфере диоксида углерода); ü назревающая научно – техническая революция XXI века диктует новые формы взаимодействия человека с природой. Создание нового универсального энергоносителя – водорода - не частная задача какой-то отдельной отрасли. Развитие водородной технологии должно происходить при тесном взаимодействии всех областей современной техники, промышленности и т. д. 39
водородная энергетика ü переход транспорта, промышленности и бытовых потребителей на водород – это путь, который приведет к возможности решить глобальные проблемы, касающиеся охраны окружающей среды (защита окружающей среды от различных отравлений, которые вызваны выбросами оксида углерода и азота, оксидами серы, углеводородами, также от вековых накоплений в атмосфере диоксида углерода); ü назревающая научно – техническая революция XXI века диктует новые формы взаимодействия человека с природой. Создание нового универсального энергоносителя – водорода - не частная задача какой-то отдельной отрасли. Развитие водородной технологии должно происходить при тесном взаимодействии всех областей современной техники, промышленности и т. д. 39
 водородная энергетика основана на применении водорода, предполагает решение целого комплекса задач: Ø разработка эффективных технологий производства водорода; Ø решение проблем, касающихся хранения, доставки и транспортировки потребителю; Ø создание условий для удобного и безопасного использования водорода; Ø разработка технологий производства дешёвого, т. е. доступного для широко применения топливного элемента. 40
водородная энергетика основана на применении водорода, предполагает решение целого комплекса задач: Ø разработка эффективных технологий производства водорода; Ø решение проблем, касающихся хранения, доставки и транспортировки потребителю; Ø создание условий для удобного и безопасного использования водорода; Ø разработка технологий производства дешёвого, т. е. доступного для широко применения топливного элемента. 40
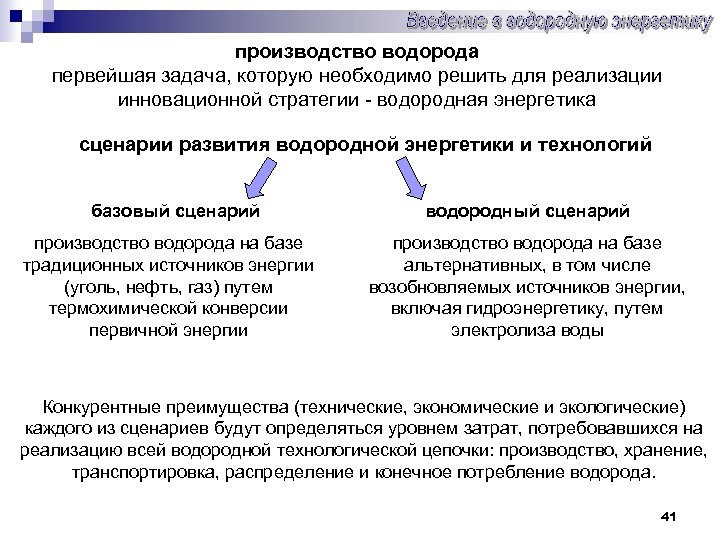 производство водорода первейшая задача, которую необходимо решить для реализации инновационной стратегии - водородная энергетика сценарии развития водородной энергетики и технологий базовый сценарий водородный сценарий производство водорода на базе традиционных источников энергии (уголь, нефть, газ) путем термохимической конверсии первичной энергии производство водорода на базе альтернативных, в том числе возобновляемых источников энергии, включая гидроэнергетику, путем электролиза воды Конкурентные преимущества (технические, экономические и экологические) каждого из сценариев будут определяться уровнем затрат, потребовавшихся на реализацию всей водородной технологической цепочки: производство, хранение, транспортировка, распределение и конечное потребление водорода. 41
производство водорода первейшая задача, которую необходимо решить для реализации инновационной стратегии - водородная энергетика сценарии развития водородной энергетики и технологий базовый сценарий водородный сценарий производство водорода на базе традиционных источников энергии (уголь, нефть, газ) путем термохимической конверсии первичной энергии производство водорода на базе альтернативных, в том числе возобновляемых источников энергии, включая гидроэнергетику, путем электролиза воды Конкурентные преимущества (технические, экономические и экологические) каждого из сценариев будут определяться уровнем затрат, потребовавшихся на реализацию всей водородной технологической цепочки: производство, хранение, транспортировка, распределение и конечное потребление водорода. 41
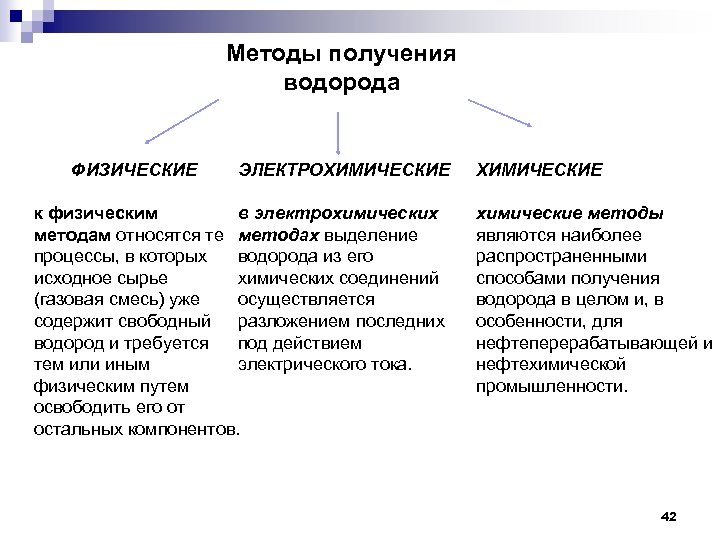 Методы получения водорода ФИЗИЧЕСКИЕ ЭЛЕКТРОХИМИЧЕСКИЕ к физическим в электрохимических методам относятся те методах выделение процессы, в которых водорода из его исходное сырье химических соединений (газовая смесь) уже осуществляется содержит свободный разложением последних водород и требуется под действием тем или иным электрического тока. физическим путем освободить его от остальных компонентов. ХИМИЧЕСКИЕ химические методы являются наиболее распространенными способами получения водорода в целом и, в особенности, для нефтеперерабатывающей и нефтехимической промышленности. 42
Методы получения водорода ФИЗИЧЕСКИЕ ЭЛЕКТРОХИМИЧЕСКИЕ к физическим в электрохимических методам относятся те методах выделение процессы, в которых водорода из его исходное сырье химических соединений (газовая смесь) уже осуществляется содержит свободный разложением последних водород и требуется под действием тем или иным электрического тока. физическим путем освободить его от остальных компонентов. ХИМИЧЕСКИЕ химические методы являются наиболее распространенными способами получения водорода в целом и, в особенности, для нефтеперерабатывающей и нефтехимической промышленности. 42
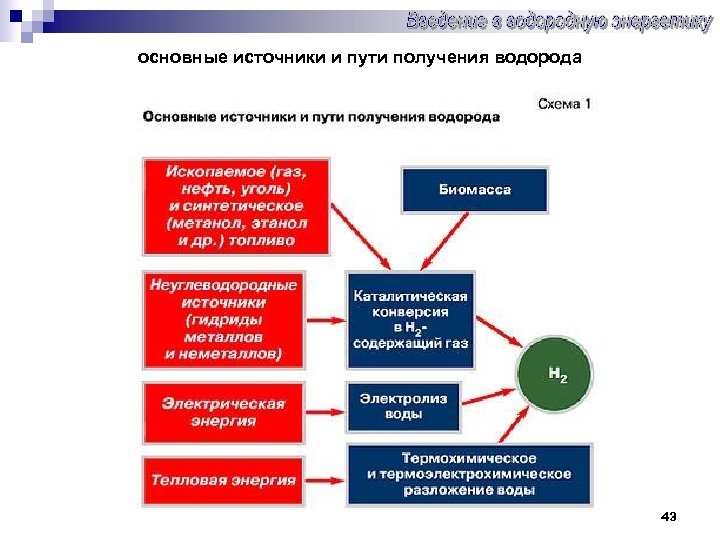 основные источники и пути получения водорода 43
основные источники и пути получения водорода 43
 паровая конверсия природного газа - метана Ø предполагается, что данный способ производства водорода будет использоваться в начальной стадии перехода к водородной экономики; Ø однако, в долгосрочной перспективе необходимо будет перейти на производство водорода из возобновляемых источников энергии, наиболее перспективными из них видятся энергия ветра или солнечная энергия; Ø сейчас с использованием метода паровой конверсии газа производится примерно половина всего водорода; Ø суть метода: водяной пар при температуре 700 – 1000 °С смешивается с метаном под давлением в присутствии катализатора. 44
паровая конверсия природного газа - метана Ø предполагается, что данный способ производства водорода будет использоваться в начальной стадии перехода к водородной экономики; Ø однако, в долгосрочной перспективе необходимо будет перейти на производство водорода из возобновляемых источников энергии, наиболее перспективными из них видятся энергия ветра или солнечная энергия; Ø сейчас с использованием метода паровой конверсии газа производится примерно половина всего водорода; Ø суть метода: водяной пар при температуре 700 – 1000 °С смешивается с метаном под давлением в присутствии катализатора. 44
 паровая конверсия природного газа - метана Наиболее критическими параметрами в этом способе производства водорода являются выбор оптимальной температуры процесса и выбор материала катализатора, т. е. его состава, а также стабильность работы такого катализатора. типы катализаторов и способов получения водорода: 1. разложение метана в присутствии массивного металлического катализатора (Fe, Co, Ni) при Т = 650 – 720 o. C; 2. разложение углеводородных газов на поверхности железосодержащего катализатора при Т = 850 – 900 o. C под давлением 1 - 35 атм; 3. разложение метана или других углеводородов на поверхности брикетированной сажи с никелем или сажи с железом при температурах ниже точки разложения этих соединений; 4. разложение метана на поверхности Ni/Al 2 O 3 или Ni/Mg. O катализаторов при Т = 500 – 550 o. C; 5. разложение метана на поверхности Ni-Cu/Al 2 O 3 или Ni-Cu/Mg. O катализаторов при Т = 560 – 650 o. C. 45
паровая конверсия природного газа - метана Наиболее критическими параметрами в этом способе производства водорода являются выбор оптимальной температуры процесса и выбор материала катализатора, т. е. его состава, а также стабильность работы такого катализатора. типы катализаторов и способов получения водорода: 1. разложение метана в присутствии массивного металлического катализатора (Fe, Co, Ni) при Т = 650 – 720 o. C; 2. разложение углеводородных газов на поверхности железосодержащего катализатора при Т = 850 – 900 o. C под давлением 1 - 35 атм; 3. разложение метана или других углеводородов на поверхности брикетированной сажи с никелем или сажи с железом при температурах ниже точки разложения этих соединений; 4. разложение метана на поверхности Ni/Al 2 O 3 или Ni/Mg. O катализаторов при Т = 500 – 550 o. C; 5. разложение метана на поверхности Ni-Cu/Al 2 O 3 или Ni-Cu/Mg. O катализаторов при Т = 560 – 650 o. C. 45
 Получение водорода с помощью угля 1. Создание Фрицем Винклером (концерн BASF) в 1926 г. газогенератора с кипящим слоем. 2. Разработка фирмой "Лурги" в 1932 г. слоевого газогенератора, работающего под давлением 3 Мпа. 3. Разработка Генрихом Копперсом и Фридрихом Тотцеком в 1944 -45 гг. пылеугольного газогенератора с жидким шлакоудалением. Удаление шлака в жидком виде реализовано в слоевом газогенераторе BGL (British Gas– Lurgy), разработанном на основе газогенератора Лурги. 4. Разработка фирмой Texaco в 1950 -е годы газификаторов для переработки тяжелых нефтяных остатков. 46
Получение водорода с помощью угля 1. Создание Фрицем Винклером (концерн BASF) в 1926 г. газогенератора с кипящим слоем. 2. Разработка фирмой "Лурги" в 1932 г. слоевого газогенератора, работающего под давлением 3 Мпа. 3. Разработка Генрихом Копперсом и Фридрихом Тотцеком в 1944 -45 гг. пылеугольного газогенератора с жидким шлакоудалением. Удаление шлака в жидком виде реализовано в слоевом газогенераторе BGL (British Gas– Lurgy), разработанном на основе газогенератора Лурги. 4. Разработка фирмой Texaco в 1950 -е годы газификаторов для переработки тяжелых нефтяных остатков. 46
 газификация угля процесс превращения твердого топлива в горючий газ суть метода: уголь проходит предварительную газификацию, затем нагревается до температуры ~ 800 – 1300 °С без доступа воздуха. Процесс газификации угля необходим для того, чтобы отфильтровать и исключить проникновение в атмосферу таких примесей как сера и др. токсичные элементы, содержащихся в угле. 47
газификация угля процесс превращения твердого топлива в горючий газ суть метода: уголь проходит предварительную газификацию, затем нагревается до температуры ~ 800 – 1300 °С без доступа воздуха. Процесс газификации угля необходим для того, чтобы отфильтровать и исключить проникновение в атмосферу таких примесей как сера и др. токсичные элементы, содержащихся в угле. 47
 газификация угля параметры определяющие активность и скорость процессов газификации: - тип газифицирующего агента; - температура и давление процесса; - способ образования минерального остатка и его удаление; - способ подачи газифицирующего агента; - способ подвода тепла в реакционную зону. 48
газификация угля параметры определяющие активность и скорость процессов газификации: - тип газифицирующего агента; - температура и давление процесса; - способ образования минерального остатка и его удаление; - способ подачи газифицирующего агента; - способ подвода тепла в реакционную зону. 48
 газификация угля типы газифицирующего агента воздух кислород водяной пар 49
газификация угля типы газифицирующего агента воздух кислород водяной пар 49
 газификация угля температура и давление процесса Т = 850 – 2000 °С р = 0. 1 – 10. 0 МПа 50
газификация угля температура и давление процесса Т = 850 – 2000 °С р = 0. 1 – 10. 0 МПа 50
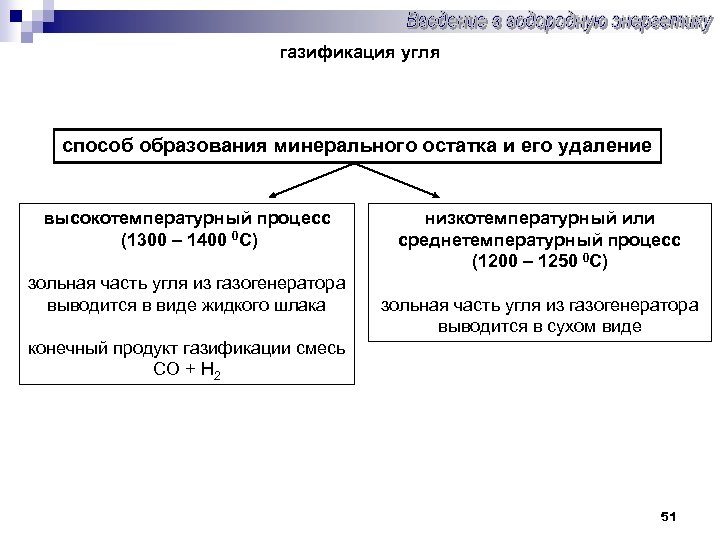 газификация угля способ образования минерального остатка и его удаление высокотемпературный процесс (1300 – 1400 0 С) зольная часть угля из газогенератора выводится в виде жидкого шлака низкотемпературный или среднетемпературный процесс (1200 – 1250 0 С) зольная часть угля из газогенератора выводится в сухом виде конечный продукт газификации смесь CO + H 2 51
газификация угля способ образования минерального остатка и его удаление высокотемпературный процесс (1300 – 1400 0 С) зольная часть угля из газогенератора выводится в виде жидкого шлака низкотемпературный или среднетемпературный процесс (1200 – 1250 0 С) зольная часть угля из газогенератора выводится в сухом виде конечный продукт газификации смесь CO + H 2 51
 газификация угля способ подачи газифицирующего агента оксогазификацию гидрогазификацию 52
газификация угля способ подачи газифицирующего агента оксогазификацию гидрогазификацию 52
 газификация угля способ подвода тепла в реакционную зону автотермические при которых тепло, необходимое для проведения эндотермических процессов, производят за счет сжигания в кислороде части газифицируемого топлива до СО 2. аллотермические сжигание и газификация разделены и тепло для происхождения процесса газификации подводятся через теплопередающую стенку внутри единого газогенераторного объема или при помощи автономно нагретого теплоносителя, который вводится в газифицируемую среду 53
газификация угля способ подвода тепла в реакционную зону автотермические при которых тепло, необходимое для проведения эндотермических процессов, производят за счет сжигания в кислороде части газифицируемого топлива до СО 2. аллотермические сжигание и газификация разделены и тепло для происхождения процесса газификации подводятся через теплопередающую стенку внутри единого газогенераторного объема или при помощи автономно нагретого теплоносителя, который вводится в газифицируемую среду 53
 роль катализатора в протекании процесса газификации угля Относительное каталитическое влияние микроэлементов углей при газификации может быть представлено следующим рядом: Mn>Ba>>B, Pb, Be>>Y, Co>Ga>Cr>Ni>V>Cu. 54
роль катализатора в протекании процесса газификации угля Относительное каталитическое влияние микроэлементов углей при газификации может быть представлено следующим рядом: Mn>Ba>>B, Pb, Be>>Y, Co>Ga>Cr>Ni>V>Cu. 54
 газификация угля процессы газификации газификация крупнокускового горючего в псевдопокоящемся слое газификация мелкозернистого горючего в псевдоожиженном слое газификация пылевидного горючего в потоке 55
газификация угля процессы газификации газификация крупнокускового горючего в псевдопокоящемся слое газификация мелкозернистого горючего в псевдоожиженном слое газификация пылевидного горючего в потоке 55
 Термодинамика процесса газификации Разложение 1 моля жидкой воды при 298 К, требует затрат работы ΔG 1 Ж=237, 4 к. Дж/моль: Н 20=Н 2+1/202 (1) Максимальная работа при полном окислении угля: ΔG 2 =394, 6 к. Дж/моль С 02 в реакции С+02 = С 02, (2) Для получения 1 кмоля водорода (2 кг водорода) нужно: 237, 4/394, 6 = 0, 6 кмоля С =7, 22 кг С, 3, 61 кг С на 1 кг Н 2. При разложении воды в виде пара (ΔG 01 п=228, 7 к. Дж/моль Н 20), расход углерода: 0, 58 моля С или 3, 48 кг С на 1 кг водорода. КПД в расчете на НТС водорода (241, 9 к. Дж/моль Н 2) - 1, 06. КПД> 1 т. к. при обратимом протекании реакции С + 2 Н 20↔ 2 Н 2 + С 02 энтропия возрастает на 78, 59 энтропийной единицы (э. е. )- возможность подвода из окружающей среды 98, 0 к. Дж/моль углерода. (1 энтропийная единица равна 1 кал * град-1) 56
Термодинамика процесса газификации Разложение 1 моля жидкой воды при 298 К, требует затрат работы ΔG 1 Ж=237, 4 к. Дж/моль: Н 20=Н 2+1/202 (1) Максимальная работа при полном окислении угля: ΔG 2 =394, 6 к. Дж/моль С 02 в реакции С+02 = С 02, (2) Для получения 1 кмоля водорода (2 кг водорода) нужно: 237, 4/394, 6 = 0, 6 кмоля С =7, 22 кг С, 3, 61 кг С на 1 кг Н 2. При разложении воды в виде пара (ΔG 01 п=228, 7 к. Дж/моль Н 20), расход углерода: 0, 58 моля С или 3, 48 кг С на 1 кг водорода. КПД в расчете на НТС водорода (241, 9 к. Дж/моль Н 2) - 1, 06. КПД> 1 т. к. при обратимом протекании реакции С + 2 Н 20↔ 2 Н 2 + С 02 энтропия возрастает на 78, 59 энтропийной единицы (э. е. )- возможность подвода из окружающей среды 98, 0 к. Дж/моль углерода. (1 энтропийная единица равна 1 кал * град-1) 56
 Реакция С + 2 Н 20↔ 2 Н 2 + С 02 - эндотермическая - к системе нужно подводить теплоту (сжечь уголь). Можно подвести аллотермически (через стенку реактора) или автотермически (добавив кислород в реактор). Аллотермический процесс. Стандартный тепловой эффект реакции (если вода подана в виде пара): ΔН° 298 = +90 к. Дж/моль С - реакция эндотермическая Если эта теплота - за счет сжигания С в О 2 по реакции: С+02=С 02 то, нужно сжечь до С 02 дополнительно 0, 23 моля. На получение 1 кг Н 2 нужно потратить 3, 69 кг С КПД, рассчитанный по НТС водорода, - 100%. Учетом затрат на разделение СО 2 и Н 2 Суммарные затраты С 3, 75 кг С на 1 кг Н 2 57
Реакция С + 2 Н 20↔ 2 Н 2 + С 02 - эндотермическая - к системе нужно подводить теплоту (сжечь уголь). Можно подвести аллотермически (через стенку реактора) или автотермически (добавив кислород в реактор). Аллотермический процесс. Стандартный тепловой эффект реакции (если вода подана в виде пара): ΔН° 298 = +90 к. Дж/моль С - реакция эндотермическая Если эта теплота - за счет сжигания С в О 2 по реакции: С+02=С 02 то, нужно сжечь до С 02 дополнительно 0, 23 моля. На получение 1 кг Н 2 нужно потратить 3, 69 кг С КПД, рассчитанный по НТС водорода, - 100%. Учетом затрат на разделение СО 2 и Н 2 Суммарные затраты С 3, 75 кг С на 1 кг Н 2 57
 плазменная парокислородная газификация угля Ø процесс плазменной парокислородной газификации угля относится к классу процессов с внутренним подводом тепла; Ø данный метод позволяет удерживать постоянную температуру процесса порядка 1500 – 2000 0 С во всем объеме газогенератора; Ø поддержание температуры возможно за счет использования в качестве источника высокотемпературного тепла электроэнергии; Ø высокая рабочая температура обеспечивает получение синтез – газа, который не содержит окислителей таких, как CO 2 и H 2 O; Ø сам процесс заключается в том, что измельченный уголь в смеси с кислородом перемешивают плазменной струей водяного пара в плазмотроне, а затем подают в газогенератор, где при температурах 1500 0 С и выше получают синтез – газ с достаточно высоким содержанием водорода и оксида углерода, и незначительным содержанием СО 2, Н 2 О и N 2; Ø КПД такого газогенератора достигает 80 – 90 %. 58
плазменная парокислородная газификация угля Ø процесс плазменной парокислородной газификации угля относится к классу процессов с внутренним подводом тепла; Ø данный метод позволяет удерживать постоянную температуру процесса порядка 1500 – 2000 0 С во всем объеме газогенератора; Ø поддержание температуры возможно за счет использования в качестве источника высокотемпературного тепла электроэнергии; Ø высокая рабочая температура обеспечивает получение синтез – газа, который не содержит окислителей таких, как CO 2 и H 2 O; Ø сам процесс заключается в том, что измельченный уголь в смеси с кислородом перемешивают плазменной струей водяного пара в плазмотроне, а затем подают в газогенератор, где при температурах 1500 0 С и выше получают синтез – газ с достаточно высоким содержанием водорода и оксида углерода, и незначительным содержанием СО 2, Н 2 О и N 2; Ø КПД такого газогенератора достигает 80 – 90 %. 58
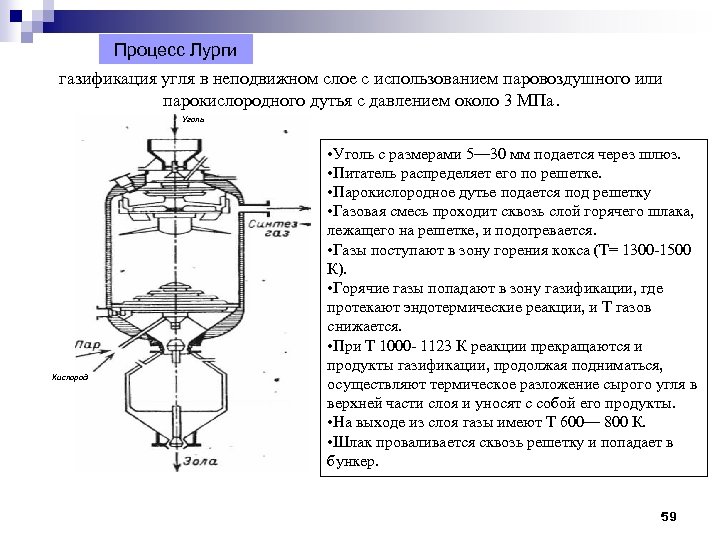 Процесс Лурги газификация угля в неподвижном слое с использованием паровоздушного или парокислородного дутья с давлением около 3 МПа. Уголь Кислород • Уголь с размерами 5— 30 мм подается через шлюз. • Питатель распределяет его по решетке. • Парокислородное дутье подается под решетку • Газовая смесь проходит сквозь слой горячего шлака, лежащего на решетке, и подогревается. • Газы поступают в зону горения кокса (Т= 1300 -1500 К). • Горячие газы попадают в зону газификации, где протекают эндотермические реакции, и Т газов снижается. • При Т 1000 - 1123 К реакции прекращаются и продукты газификации, продолжая подниматься, осуществляют термическое разложение сырого угля в верхней части слоя и уносят с собой его продукты. • На выходе из слоя газы имеют Т 600— 800 К. • Шлак проваливается сквозь решетку и попадает в бункер. 59
Процесс Лурги газификация угля в неподвижном слое с использованием паровоздушного или парокислородного дутья с давлением около 3 МПа. Уголь Кислород • Уголь с размерами 5— 30 мм подается через шлюз. • Питатель распределяет его по решетке. • Парокислородное дутье подается под решетку • Газовая смесь проходит сквозь слой горячего шлака, лежащего на решетке, и подогревается. • Газы поступают в зону горения кокса (Т= 1300 -1500 К). • Горячие газы попадают в зону газификации, где протекают эндотермические реакции, и Т газов снижается. • При Т 1000 - 1123 К реакции прекращаются и продукты газификации, продолжая подниматься, осуществляют термическое разложение сырого угля в верхней части слоя и уносят с собой его продукты. • На выходе из слоя газы имеют Т 600— 800 К. • Шлак проваливается сквозь решетку и попадает в бункер. 59
 Основные недостатки процесса Лурги: 1. необходимость использования сортированного угля — всю мелочь приходится использовать в других процессах. 2. наряду с газификацией происходит пиролиз угля, продукты которого (смола, пирогенетическая влага и другие) уносятся с газом, что требует более сложной его очистки. Состав газа(по объему), получаемого по методу Лурги 58 % СО, 6 % С 02, 26 % Н 2, 9 % СН 4, 1 % N 2 60
Основные недостатки процесса Лурги: 1. необходимость использования сортированного угля — всю мелочь приходится использовать в других процессах. 2. наряду с газификацией происходит пиролиз угля, продукты которого (смола, пирогенетическая влага и другие) уносятся с газом, что требует более сложной его очистки. Состав газа(по объему), получаемого по методу Лурги 58 % СО, 6 % С 02, 26 % Н 2, 9 % СН 4, 1 % N 2 60
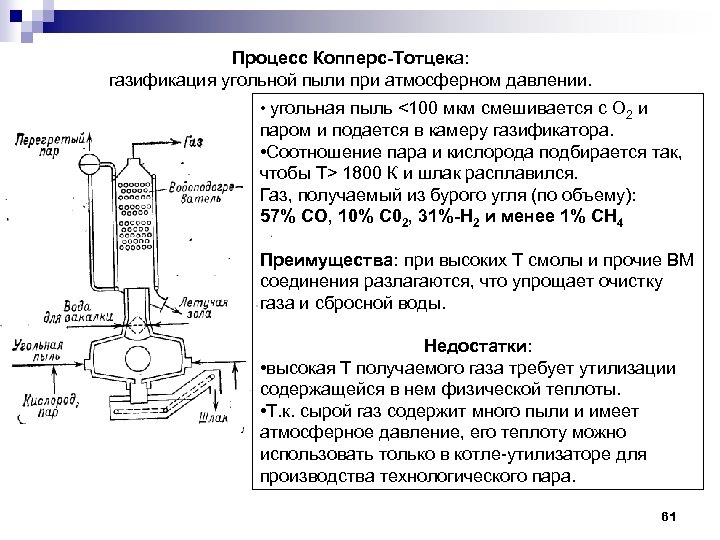 Процесс Копперс-Тотцека: газификация угольной пыли при атмосферном давлении. • угольная пыль <100 мкм смешивается с О 2 и паром и подается в камеру газификатора. • Соотношение пара и кислорода подбирается так, чтобы Т> 1800 К и шлак расплавился. Газ, получаемый из бурого угля (по объему): 57% СО, 10% С 02, 31%-Н 2 и менее 1% СН 4 Преимущества: при высоких Т смолы и прочие ВМ соединения разлагаются, что упрощает очистку газа и сбросной воды. Недостатки: • высокая Т получаемого газа требует утилизации содержащейся в нем физической теплоты. • Т. к. сырой газ содержит много пыли и имеет атмосферное давление, его теплоту можно использовать только в котле-утилизаторе для производства технологического пара. 61
Процесс Копперс-Тотцека: газификация угольной пыли при атмосферном давлении. • угольная пыль <100 мкм смешивается с О 2 и паром и подается в камеру газификатора. • Соотношение пара и кислорода подбирается так, чтобы Т> 1800 К и шлак расплавился. Газ, получаемый из бурого угля (по объему): 57% СО, 10% С 02, 31%-Н 2 и менее 1% СН 4 Преимущества: при высоких Т смолы и прочие ВМ соединения разлагаются, что упрощает очистку газа и сбросной воды. Недостатки: • высокая Т получаемого газа требует утилизации содержащейся в нем физической теплоты. • Т. к. сырой газ содержит много пыли и имеет атмосферное давление, его теплоту можно использовать только в котле-утилизаторе для производства технологического пара. 61
 Электролиз воды Принцип электролиза: H 2 O (жидкость/пар) + электрическая энергия → H 2 (г) + ½ O 2 (г) • Метод получения водорода из воды путем электролиза является полупромышленным полулабораторным методом получения водорода и кислорода; • данный метод не так широко используется в промышленности, по сравнению, например, с методами производства водорода из органических топлив (электролизный метод, требует относительно большого потребления электроэнергии, более 5 - 6 к. Вт·ч на 1 м 3 водорода, а также малыми мощностями установок этого процесса); • тем не менее, метод получения водорода электролизом воды является одним из наиболее известных и хорошо исследованных методов получения водорода; • данный метод обеспечивает получение чистого продукта в одну технологическую цепь (на выходе получают 99, 6 – 99, 9 % Н 2); • в экологическом отношении метод получения водорода электролизом воды идеален. 62
Электролиз воды Принцип электролиза: H 2 O (жидкость/пар) + электрическая энергия → H 2 (г) + ½ O 2 (г) • Метод получения водорода из воды путем электролиза является полупромышленным полулабораторным методом получения водорода и кислорода; • данный метод не так широко используется в промышленности, по сравнению, например, с методами производства водорода из органических топлив (электролизный метод, требует относительно большого потребления электроэнергии, более 5 - 6 к. Вт·ч на 1 м 3 водорода, а также малыми мощностями установок этого процесса); • тем не менее, метод получения водорода электролизом воды является одним из наиболее известных и хорошо исследованных методов получения водорода; • данный метод обеспечивает получение чистого продукта в одну технологическую цепь (на выходе получают 99, 6 – 99, 9 % Н 2); • в экологическом отношении метод получения водорода электролизом воды идеален. 62
 электролиз воды Ø данный метод производства водорода является достаточно энергозатратным, а поэтому необходимо найти такие способы получения электроэнергии, которые не приводили бы к выбросам парниковых газов и прочим видам загрязнения окружающей среды и, кроме того, чтобы стоимость этой электроэнергии, которая используется для осуществления процесса электролиза была достаточно низкой; Ø именно наличия дешевой энергии является очень важным требованием, т. к. примерно 85 % от общей суммы производственных затрат, при производстве водорода, составляет стоимость электрической энергии; Ø таким образом, данный метод производства водорода может быть успешно осуществлен в странах, обладающих значительными ресурсами дешевой энергии, к которой, например, относится гидроэнергия; Ø в настоящее время наиболее крупные электрохимические комплексы находятся в таких странах как Канада, Индия, Египет, Норвегия, также созданы и работают тысячи более мелких установок во многих странах мира. 63
электролиз воды Ø данный метод производства водорода является достаточно энергозатратным, а поэтому необходимо найти такие способы получения электроэнергии, которые не приводили бы к выбросам парниковых газов и прочим видам загрязнения окружающей среды и, кроме того, чтобы стоимость этой электроэнергии, которая используется для осуществления процесса электролиза была достаточно низкой; Ø именно наличия дешевой энергии является очень важным требованием, т. к. примерно 85 % от общей суммы производственных затрат, при производстве водорода, составляет стоимость электрической энергии; Ø таким образом, данный метод производства водорода может быть успешно осуществлен в странах, обладающих значительными ресурсами дешевой энергии, к которой, например, относится гидроэнергия; Ø в настоящее время наиболее крупные электрохимические комплексы находятся в таких странах как Канада, Индия, Египет, Норвегия, также созданы и работают тысячи более мелких установок во многих странах мира. 63
 Реакция разложения воды Н 20↔Н 2+1/202 при Т=298, 15 К и при стандартном давлении р =0, 1013 Мпа ΔH= 241, 98 к. Дж/моль ΔG=228, 78 к. Дж/моль ΔS=44, 497 Дж/моль ΔH=ΔG+TΔS H – энтальпия (внутренняя энергия) G – потенциал (энергия) Гиббса S – энтропия ΔH -Тепловой эффект реакции – полное изменение внутренней энергии системы равно сумме: ΔG -изменение «свободной» энергии, способной превращаться в работу, TΔS – изменение «связанной» энергии , которая может перейти только в теплоту. S - энтропия 64
Реакция разложения воды Н 20↔Н 2+1/202 при Т=298, 15 К и при стандартном давлении р =0, 1013 Мпа ΔH= 241, 98 к. Дж/моль ΔG=228, 78 к. Дж/моль ΔS=44, 497 Дж/моль ΔH=ΔG+TΔS H – энтальпия (внутренняя энергия) G – потенциал (энергия) Гиббса S – энтропия ΔH -Тепловой эффект реакции – полное изменение внутренней энергии системы равно сумме: ΔG -изменение «свободной» энергии, способной превращаться в работу, TΔS – изменение «связанной» энергии , которая может перейти только в теплоту. S - энтропия 64
 электролиз воды Электрохимический метод получения водорода из воды обладает следующими положительными качествами: 1) высокая чистота получаемого водорода – до 99, 99% и выше; 2) простота технологического процесса, его непрерывность, возможность наиболее полной автоматизации, отсутствие движущихся частей в электролитической ячейке; 3) возможность получения ценнейших побочных продуктов, которыми являются тяжелая вода и кислород; 4) общедоступное и неисчерпаемое сырье – вода; 5) гибкость процесса и возможность получения водорода непосредственно под давлением; 6) физическое разделение водорода и кислорода в самом процессе электролиза. 65
электролиз воды Электрохимический метод получения водорода из воды обладает следующими положительными качествами: 1) высокая чистота получаемого водорода – до 99, 99% и выше; 2) простота технологического процесса, его непрерывность, возможность наиболее полной автоматизации, отсутствие движущихся частей в электролитической ячейке; 3) возможность получения ценнейших побочных продуктов, которыми являются тяжелая вода и кислород; 4) общедоступное и неисчерпаемое сырье – вода; 5) гибкость процесса и возможность получения водорода непосредственно под давлением; 6) физическое разделение водорода и кислорода в самом процессе электролиза. 65
 процессы, происходящие в комплексе с процессом получением водорода электролизом воды: получение наряду с водородом кислорода кислород найдет свое применение, прежде всего, как ускоритель технологических процессов; кислород может стать незаменимым очистителем и оздоровителем водоемов и промышленных стоков, т. е. использование кислорода в качестве оздоровителя и очистителя может быть распространено на атмосферу, почву и воду. получение в процессе электролиза тяжелой воды D 2 O - изотопная разновидность воды, в которой лёгкий атом водорода 1 H замещен его тяжёлым изотопом 2 Н - дейтерием D; физ. свойства: D 2 O кипит при 101, 43 °С, замерзает при 3, 82 °С, имеет плотность 1, 104 г/см 3; хим. свойства D 2 O очень близки к H 2 O, хотя некоторые реакции в ней замедляются или ускоряются (иногда в 2 - 3 раза); основные промышленные методы получения D 2 O: изотопный обмен воды и сероводорода, дистилляция водорода и многоступенчатый электролиз. опреснение морской воды получение в процессе электролиза морской соли 66
процессы, происходящие в комплексе с процессом получением водорода электролизом воды: получение наряду с водородом кислорода кислород найдет свое применение, прежде всего, как ускоритель технологических процессов; кислород может стать незаменимым очистителем и оздоровителем водоемов и промышленных стоков, т. е. использование кислорода в качестве оздоровителя и очистителя может быть распространено на атмосферу, почву и воду. получение в процессе электролиза тяжелой воды D 2 O - изотопная разновидность воды, в которой лёгкий атом водорода 1 H замещен его тяжёлым изотопом 2 Н - дейтерием D; физ. свойства: D 2 O кипит при 101, 43 °С, замерзает при 3, 82 °С, имеет плотность 1, 104 г/см 3; хим. свойства D 2 O очень близки к H 2 O, хотя некоторые реакции в ней замедляются или ускоряются (иногда в 2 - 3 раза); основные промышленные методы получения D 2 O: изотопный обмен воды и сероводорода, дистилляция водорода и многоступенчатый электролиз. опреснение морской воды получение в процессе электролиза морской соли 66
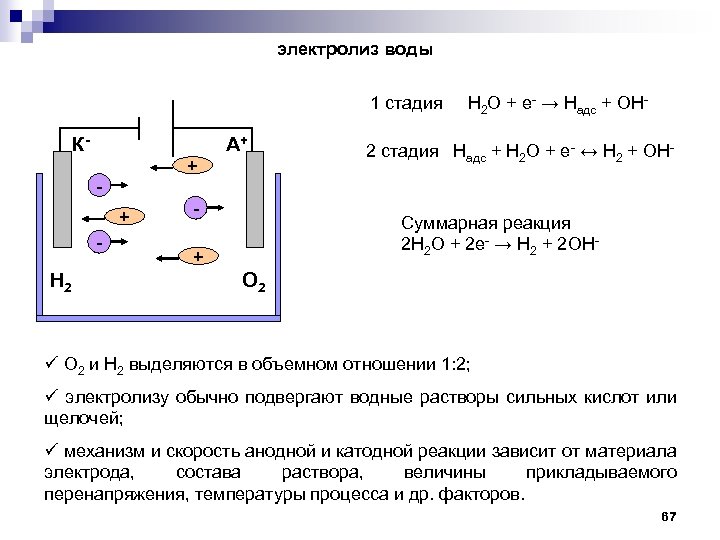 электролиз воды 1 стадия H 2 O + e- → Hадс + OH- К- + + - Н 2 А+ - 2 стадия Hадс + H 2 O + e- ↔ Н 2 + OH- Суммарная реакция 2 H 2 O + 2 e- → H 2 + 2 OH- + О 2 ü О 2 и Н 2 выделяются в объемном отношении 1: 2; ü электролизу обычно подвергают водные растворы сильных кислот или щелочей; ü механизм и скорость анодной и катодной реакции зависит от материала электрода, состава раствора, величины прикладываемого перенапряжения, температуры процесса и др. факторов. 67
электролиз воды 1 стадия H 2 O + e- → Hадс + OH- К- + + - Н 2 А+ - 2 стадия Hадс + H 2 O + e- ↔ Н 2 + OH- Суммарная реакция 2 H 2 O + 2 e- → H 2 + 2 OH- + О 2 ü О 2 и Н 2 выделяются в объемном отношении 1: 2; ü электролизу обычно подвергают водные растворы сильных кислот или щелочей; ü механизм и скорость анодной и катодной реакции зависит от материала электрода, состава раствора, величины прикладываемого перенапряжения, температуры процесса и др. факторов. 67
 получение водорода из щелочных растворов реакции на катоде: 1. H 2 O + e- → Hадс + OH- реакции на аноде: 1. 2 OH- → 2 ОH + 2 e- 2. Hадс + H 2 O + e- ↔ Н 2 + OH- 2 H 2 O + 2 e- → H 2 + 2 OH- 2. 2 ОН + 2 ОН- → 2 О- + 2 Н 2 О; 2 О- → 2 О + 2 е-; 2 О → О 2 Н 2 О → 2 Н 2 + О 2 68
получение водорода из щелочных растворов реакции на катоде: 1. H 2 O + e- → Hадс + OH- реакции на аноде: 1. 2 OH- → 2 ОH + 2 e- 2. Hадс + H 2 O + e- ↔ Н 2 + OH- 2 H 2 O + 2 e- → H 2 + 2 OH- 2. 2 ОН + 2 ОН- → 2 О- + 2 Н 2 О; 2 О- → 2 О + 2 е-; 2 О → О 2 Н 2 О → 2 Н 2 + О 2 68
 электролиз воды Ø наиболее удобным электролитом, используемым в современных промышленных электролизерах является 25 – 30 % КОН; Ø электролит также может быть и твердотельным, например, в виде твердой полимерной мембраны или твердый керамический материал; Ø в качестве материала электродов обычно используют углеродистую сталь, при этом аноды покрывают никелем, а катоды активируют путем нанесения на их поверхность либо серосодержащего никеля, либо металла платиновой группы. 69
электролиз воды Ø наиболее удобным электролитом, используемым в современных промышленных электролизерах является 25 – 30 % КОН; Ø электролит также может быть и твердотельным, например, в виде твердой полимерной мембраны или твердый керамический материал; Ø в качестве материала электродов обычно используют углеродистую сталь, при этом аноды покрывают никелем, а катоды активируют путем нанесения на их поверхность либо серосодержащего никеля, либо металла платиновой группы. 69
 типы электролизеров и их характеристики Ø электролизер это устройство, установка, в которой собственно и осуществляется процесс электролиза; Ø в настоящее время применяется и разрабатывается довольно большое число электролизеров различных типов и конструкций для электролиза воды; Ø основными структурными составляющими электролизера являются анод, катод, электролит, биполярная пластина. По конструкции и схеме включения в цепь электродов все электролизеры могут быть разделены на два типа: с монополярными электродами с биполярными электродами 70
типы электролизеров и их характеристики Ø электролизер это устройство, установка, в которой собственно и осуществляется процесс электролиза; Ø в настоящее время применяется и разрабатывается довольно большое число электролизеров различных типов и конструкций для электролиза воды; Ø основными структурными составляющими электролизера являются анод, катод, электролит, биполярная пластина. По конструкции и схеме включения в цепь электродов все электролизеры могут быть разделены на два типа: с монополярными электродами с биполярными электродами 70
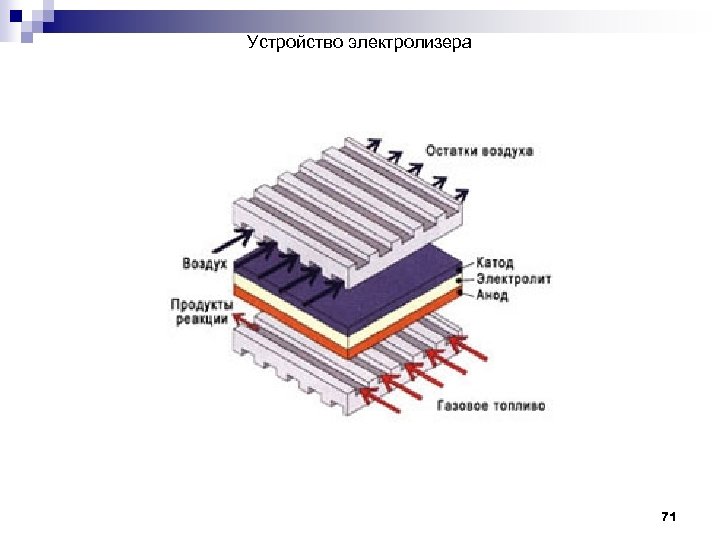 Устройство электролизера 71
Устройство электролизера 71
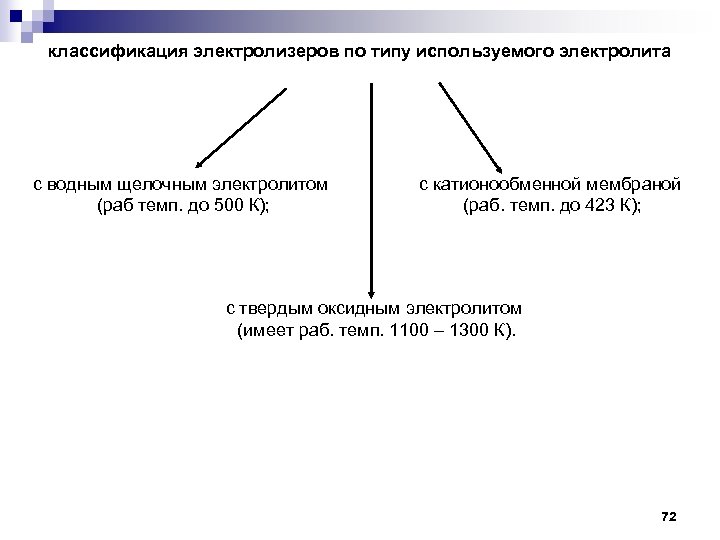 классификация электролизеров по типу используемого электролита с водным щелочным электролитом (раб темп. до 500 К); с катионообменной мембраной (раб. темп. до 423 К); с твердым оксидным электролитом (имеет раб. темп. 1100 – 1300 К). 72
классификация электролизеров по типу используемого электролита с водным щелочным электролитом (раб темп. до 500 К); с катионообменной мембраной (раб. темп. до 423 К); с твердым оксидным электролитом (имеет раб. темп. 1100 – 1300 К). 72
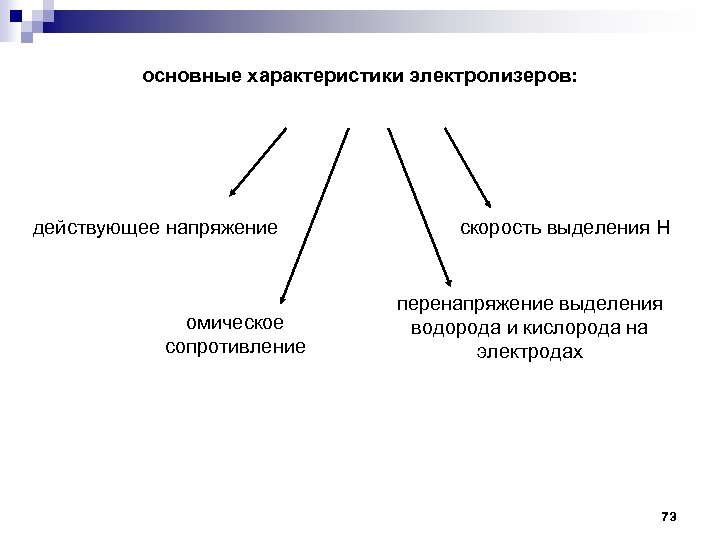 основные характеристики электролизеров: действующее напряжение омическое сопротивление скорость выделения Н перенапряжение выделения водорода и кислорода на электродах 73
основные характеристики электролизеров: действующее напряжение омическое сопротивление скорость выделения Н перенапряжение выделения водорода и кислорода на электродах 73
 снижение омических потерь осуществляется за счет - повышения температуры процесса, - за счет использования соответствующих диафрагм, - за счет использования электролитов с высокой проводимостью, - а также за счет уменьшения расстояния между электродами. 74
снижение омических потерь осуществляется за счет - повышения температуры процесса, - за счет использования соответствующих диафрагм, - за счет использования электролитов с высокой проводимостью, - а также за счет уменьшения расстояния между электродами. 74
 - падение напряжения на электродах и контактах может быть уменьшено за счет использования др. соответствующих материалов электродов, и использования электролита с малой коррозионной активностью; - от выбора материала электрода, зависит в свою очередь перенапряжение водорода на катоде, или кислорода на аноде. Так, например, перенапряжение водорода на платине стремится к нулю, в то время как на никеле оно составляет не ниже 0, 4 В. - аналогичное справедливо и для кислородного перенапряжения. 75
- падение напряжения на электродах и контактах может быть уменьшено за счет использования др. соответствующих материалов электродов, и использования электролита с малой коррозионной активностью; - от выбора материала электрода, зависит в свою очередь перенапряжение водорода на катоде, или кислорода на аноде. Так, например, перенапряжение водорода на платине стремится к нулю, в то время как на никеле оно составляет не ниже 0, 4 В. - аналогичное справедливо и для кислородного перенапряжения. 75
 для снижения перенапряжения необходимо: Ø использовать соответствующие электродные материалы, или же проводить только поверхностную обработку имеющихся электродов определенными материалами; Ø увеличивать истинную (рабочую) поверхность электродов, используя высокопористые материалы, либо если осуществить такую поверхностную обработку электрода, которая бы повышала пористость материала; Ø вводить различные каталитические добавки в электроды, что позволяет ускорить электродные реакции на самой поверхности электродов; 76
для снижения перенапряжения необходимо: Ø использовать соответствующие электродные материалы, или же проводить только поверхностную обработку имеющихся электродов определенными материалами; Ø увеличивать истинную (рабочую) поверхность электродов, используя высокопористые материалы, либо если осуществить такую поверхностную обработку электрода, которая бы повышала пористость материала; Ø вводить различные каталитические добавки в электроды, что позволяет ускорить электродные реакции на самой поверхности электродов; 76
 основные требования, предъявляемые к электродным материалам - низкое перенапряжение; - развитая рабочая поверхность; - каталитическая активность материала электрода; - коррозионная стойкость; - длительная работоспособность 77
основные требования, предъявляемые к электродным материалам - низкое перенапряжение; - развитая рабочая поверхность; - каталитическая активность материала электрода; - коррозионная стойкость; - длительная работоспособность 77
 исследования в области создания электродных материалов направлены на: - снижение перенапряжения; - создания развитой активной поверхности электродов; - нахождение оптимальных каталитических добавок; - на снижение стоимости электродов путем изготовления их не из драгоценных металлов, а из дешевых материалов (неблагородных металлов). 78
исследования в области создания электродных материалов направлены на: - снижение перенапряжения; - создания развитой активной поверхности электродов; - нахождение оптимальных каталитических добавок; - на снижение стоимости электродов путем изготовления их не из драгоценных металлов, а из дешевых материалов (неблагородных металлов). 78
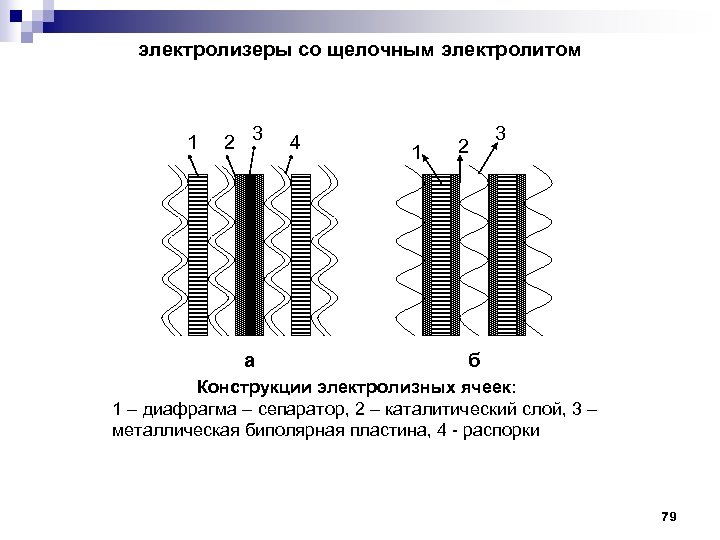 электролизеры со щелочным электролитом 1 2 3 а 4 1 2 3 б Конструкции электролизных ячеек: 1 – диафрагма – сепаратор, 2 – каталитический слой, 3 – металлическая биполярная пластина, 4 - распорки 79
электролизеры со щелочным электролитом 1 2 3 а 4 1 2 3 б Конструкции электролизных ячеек: 1 – диафрагма – сепаратор, 2 – каталитический слой, 3 – металлическая биполярная пластина, 4 - распорки 79
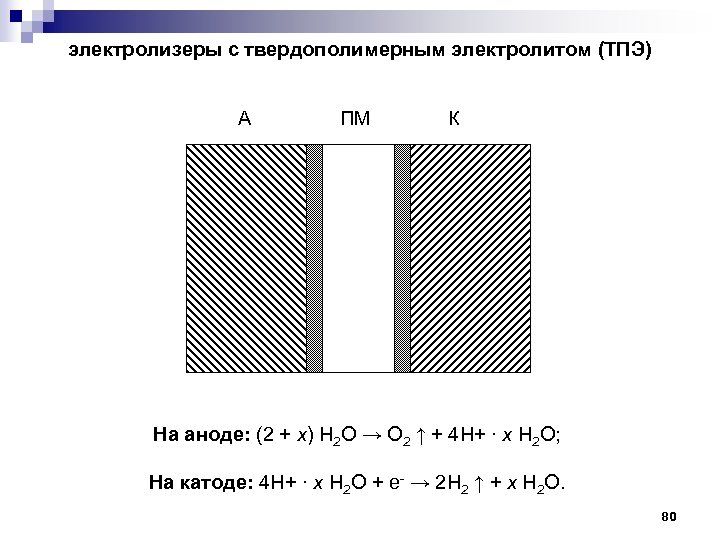 электролизеры с твердополимерным электролитом (ТПЭ) А ПМ К На аноде: (2 + x) H 2 O → O 2 ↑ + 4 H+ ∙ x H 2 O; На катоде: 4 H+ ∙ x H 2 O + e- → 2 H 2 ↑ + x H 2 O. 80
электролизеры с твердополимерным электролитом (ТПЭ) А ПМ К На аноде: (2 + x) H 2 O → O 2 ↑ + 4 H+ ∙ x H 2 O; На катоде: 4 H+ ∙ x H 2 O + e- → 2 H 2 ↑ + x H 2 O. 80
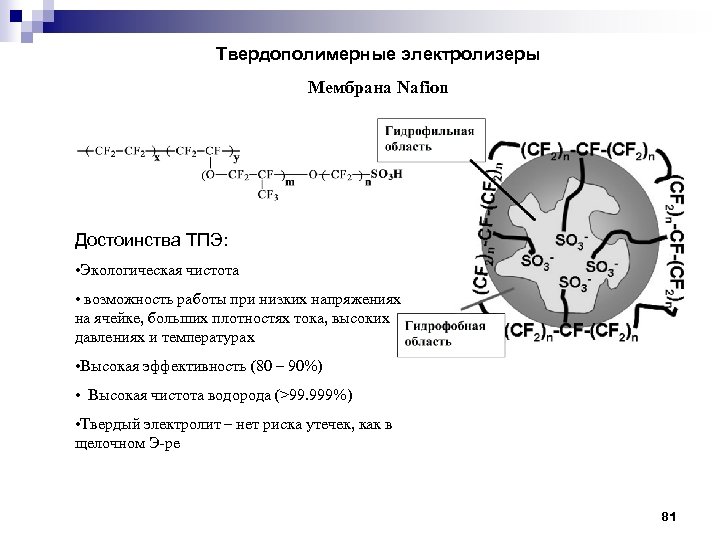 Твердополимерные электролизеры Мембрана Nafion Достоинства ТПЭ: • Экологическая чистота • возможность работы при низких напряжениях на ячейке, больших плотностях тока, высоких давлениях и температурах • Высокая эффективность (80 – 90%) • Высокая чистота водорода (>99. 999%) • Твердый электролит – нет риска утечек, как в щелочном Э-ре 81
Твердополимерные электролизеры Мембрана Nafion Достоинства ТПЭ: • Экологическая чистота • возможность работы при низких напряжениях на ячейке, больших плотностях тока, высоких давлениях и температурах • Высокая эффективность (80 – 90%) • Высокая чистота водорода (>99. 999%) • Твердый электролит – нет риска утечек, как в щелочном Э-ре 81
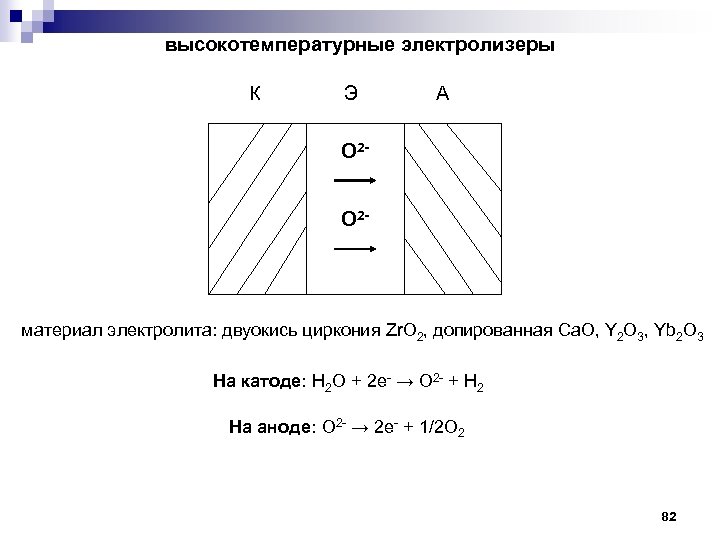 высокотемпературные электролизеры К Э А О 2 О 2 - материал электролита: двуокись циркония Zr. O 2, допированная Ca. O, Y 2 O 3, Yb 2 O 3 На катоде: Н 2 О + 2 е- → О 2 - + Н 2 На аноде: О 2 - → 2 е- + 1/2 О 2 82
высокотемпературные электролизеры К Э А О 2 О 2 - материал электролита: двуокись циркония Zr. O 2, допированная Ca. O, Y 2 O 3, Yb 2 O 3 На катоде: Н 2 О + 2 е- → О 2 - + Н 2 На аноде: О 2 - → 2 е- + 1/2 О 2 82
 высокотемпературные электролизеры требования, предъявляемые к материалам электродов: - высокая коррозионная стойкость; - механическая прочность; - термический коэффициент расширения, близкий к коэффициенту термического расширения твердого электролита, чтобы исключить коррозию, отслаивание между электродом и электролитом, их растрескивание в условиях высоких рабочих температур. 83
высокотемпературные электролизеры требования, предъявляемые к материалам электродов: - высокая коррозионная стойкость; - механическая прочность; - термический коэффициент расширения, близкий к коэффициенту термического расширения твердого электролита, чтобы исключить коррозию, отслаивание между электродом и электролитом, их растрескивание в условиях высоких рабочих температур. 83
 высокотемпературные электролизеры На катоде: Н 2 О + 2 е- → О 2 - + Н 2 , На аноде: О 2 - → 2 е- + 1/2 О 2. Ø высокотемпературный электролиз по своим термодинамическим параметрам превосходит низкотемпературные системы; Ø достигнуты успехи по созданию отдельных ячеек высокотемпературных электролизеров; Ø однако, создать промышленный аппарат до сих пор не удается; Ø проблематично создать проводящую по О 2 - керамическую беспористую диафрагму на основе диоксида циркония достаточно большого размера; Ø основным из недостатком всех приведенных типов электролизеров является высокое потребление электрической энергии. Так, например, отечественные электролизеры имеют энергопотребление 5, 0 – 5, 3 к. Вт·ч/м 3 Н 2, а лучшие зарубежные образцы 4, 1 – 4, 3 к. Вт·ч/м 3 Н 2. Ø КПД электролизеров достаточно высок и для различных типов электролизеров он составляет от 55 % до 90%. 84
высокотемпературные электролизеры На катоде: Н 2 О + 2 е- → О 2 - + Н 2 , На аноде: О 2 - → 2 е- + 1/2 О 2. Ø высокотемпературный электролиз по своим термодинамическим параметрам превосходит низкотемпературные системы; Ø достигнуты успехи по созданию отдельных ячеек высокотемпературных электролизеров; Ø однако, создать промышленный аппарат до сих пор не удается; Ø проблематично создать проводящую по О 2 - керамическую беспористую диафрагму на основе диоксида циркония достаточно большого размера; Ø основным из недостатком всех приведенных типов электролизеров является высокое потребление электрической энергии. Так, например, отечественные электролизеры имеют энергопотребление 5, 0 – 5, 3 к. Вт·ч/м 3 Н 2, а лучшие зарубежные образцы 4, 1 – 4, 3 к. Вт·ч/м 3 Н 2. Ø КПД электролизеров достаточно высок и для различных типов электролизеров он составляет от 55 % до 90%. 84
 электролиз морской воды Ø недостатком обычного электролиза является выделение низкопотенциального трудноиспользуемого тепла (температура на уровне 40 – 60 °С) и это тепло нужно постоянно отводить от электролита, на что расходуется значительное количество охлаждающей воды; Ø подобного недостатка можно избежать, если использовать для электролиза морскую воду; Ø в отличие от пресной воды ресурсы морской воды на Земле практически неограниченны (97 % всей доступной воды составляет морская вода), кроме того, она является легко доступной и уже является сложным раствором электролитов; Ø в качестве возможных источников энергии для получения водорода таким способом, могут быть использованы крупные плавучие атомные электростанции большой электрической мощности, которые располагаются в море, где к тому же в неограниченном количестве имеется морская вода для охлаждения. 85
электролиз морской воды Ø недостатком обычного электролиза является выделение низкопотенциального трудноиспользуемого тепла (температура на уровне 40 – 60 °С) и это тепло нужно постоянно отводить от электролита, на что расходуется значительное количество охлаждающей воды; Ø подобного недостатка можно избежать, если использовать для электролиза морскую воду; Ø в отличие от пресной воды ресурсы морской воды на Земле практически неограниченны (97 % всей доступной воды составляет морская вода), кроме того, она является легко доступной и уже является сложным раствором электролитов; Ø в качестве возможных источников энергии для получения водорода таким способом, могут быть использованы крупные плавучие атомные электростанции большой электрической мощности, которые располагаются в море, где к тому же в неограниченном количестве имеется морская вода для охлаждения. 85
 термический метод получения водорода 1. Разложение воды Ø Процесс термического разложения воды может быть описан следующими реакциями: Н 2 О → Н 2 + 1/2 О 2, Н 2 → 2 Н; О 2 → 2 О, О + Н → ОН. Ø Эта система представляет собой прямое термическое разложение водяного пара. Этот ряд реакций позволяет рассчитать мольные фракции шести компонентов (таких как Н 2 О, Н 2, Н, О 2, ОН) как функцию температуры при заданном давлении; Ø при температуре 3000 К диссоциирует около 35 % водяных паров; Ø где температура процесса выше 3500 К наблюдается преобладание атомных водорода и кислорода. 86
термический метод получения водорода 1. Разложение воды Ø Процесс термического разложения воды может быть описан следующими реакциями: Н 2 О → Н 2 + 1/2 О 2, Н 2 → 2 Н; О 2 → 2 О, О + Н → ОН. Ø Эта система представляет собой прямое термическое разложение водяного пара. Этот ряд реакций позволяет рассчитать мольные фракции шести компонентов (таких как Н 2 О, Н 2, Н, О 2, ОН) как функцию температуры при заданном давлении; Ø при температуре 3000 К диссоциирует около 35 % водяных паров; Ø где температура процесса выше 3500 К наблюдается преобладание атомных водорода и кислорода. 86
 основные трудности реализации процесса термического разложения воды 1. проблема отделения молекулярного водорода и молекулярного кислорода (так для предотвращения рекомбинации водорода и кислорода могут быть использованы: - селективные мембраны для удаления Н 2 и О 2, как только они образуются, - быстрая закалка. 2. подбор материалов, устойчивых при столь высоких температурах; 3. подбор источников тепла высокого потенциала; 4. использование отходов низко – и среднетемпературного тепла, которое образуется в процессе. 87
основные трудности реализации процесса термического разложения воды 1. проблема отделения молекулярного водорода и молекулярного кислорода (так для предотвращения рекомбинации водорода и кислорода могут быть использованы: - селективные мембраны для удаления Н 2 и О 2, как только они образуются, - быстрая закалка. 2. подбор материалов, устойчивых при столь высоких температурах; 3. подбор источников тепла высокого потенциала; 4. использование отходов низко – и среднетемпературного тепла, которое образуется в процессе. 87
 термический метод получения водорода 2. Разложение жидких и газообразных углеводородов. Процесс представляет собой технологическую комбинацию следующих химических реакций: СН 4 → 2 Н 2 + С, С + О 2 → СО 2, Сn. H 2 n+2 → n. C + m. H 2. или в виде двух ступенчатого процесса с образованием ацетилена: 2 СН 4 ↔ С 2 Н 2 + 3 Н 2, С 2 Н 2 ↔ 2 С + Н 2. Другой способ получения водорода из ацетилена: 2 С 2 Н 2 + 3 Н 2 О → СН 3 СОСН 3 + СО 2 + 2 Н 2 88
термический метод получения водорода 2. Разложение жидких и газообразных углеводородов. Процесс представляет собой технологическую комбинацию следующих химических реакций: СН 4 → 2 Н 2 + С, С + О 2 → СО 2, Сn. H 2 n+2 → n. C + m. H 2. или в виде двух ступенчатого процесса с образованием ацетилена: 2 СН 4 ↔ С 2 Н 2 + 3 Н 2, С 2 Н 2 ↔ 2 С + Н 2. Другой способ получения водорода из ацетилена: 2 С 2 Н 2 + 3 Н 2 О → СН 3 СОСН 3 + СО 2 + 2 Н 2 88
 термический метод получения водорода 3. Разложение метилового спирта СН 3 ОН → СО + 2 Н 2 Катализатором процесса является смешанный медно – никелевый или никелево – алюминиевый катализатор, нанесенный на огнеупорный носитель. Состав получаемого газа после первой ступени процесса: 61 % Н 2, 31 % СО, 2 % СО 2 89
термический метод получения водорода 3. Разложение метилового спирта СН 3 ОН → СО + 2 Н 2 Катализатором процесса является смешанный медно – никелевый или никелево – алюминиевый катализатор, нанесенный на огнеупорный носитель. Состав получаемого газа после первой ступени процесса: 61 % Н 2, 31 % СО, 2 % СО 2 89
 термический метод получения водорода 4. Разложение сероводорода При нагревании сероводород разлагается по реакции: 2 Н 2 S → 2 H 2 + 2 S 90
термический метод получения водорода 4. Разложение сероводорода При нагревании сероводород разлагается по реакции: 2 Н 2 S → 2 H 2 + 2 S 90
 термический метод получения водорода 5. Термическое разложение аммиака При нагреве аммиак разлагается по реакции: 2 NH 3 → N 2 + 3 H 2 91
термический метод получения водорода 5. Термическое разложение аммиака При нагреве аммиак разлагается по реакции: 2 NH 3 → N 2 + 3 H 2 91
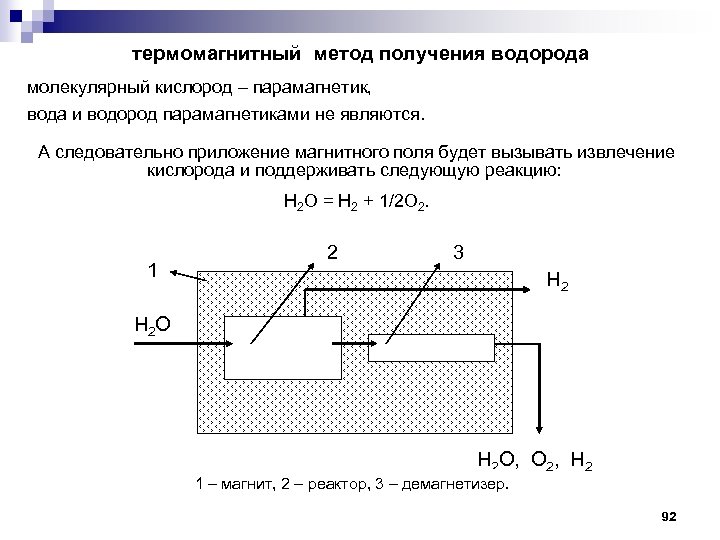 термомагнитный метод получения водорода молекулярный кислород – парамагнетик, вода и водород парамагнетиками не являются. А следовательно приложение магнитного поля будет вызывать извлечение кислорода и поддерживать следующую реакцию: Н 2 О = Н 2 + 1/2 О 2. 1 2 3 Н 2 О Н 2 О, О 2, Н 2 1 – магнит, 2 – реактор, 3 – демагнетизер. 92
термомагнитный метод получения водорода молекулярный кислород – парамагнетик, вода и водород парамагнетиками не являются. А следовательно приложение магнитного поля будет вызывать извлечение кислорода и поддерживать следующую реакцию: Н 2 О = Н 2 + 1/2 О 2. 1 2 3 Н 2 О Н 2 О, О 2, Н 2 1 – магнит, 2 – реактор, 3 – демагнетизер. 92
 Фотолиз Ø получение водорода методом фотолиза основано на способности поглощенного кванта света разрывать водородные связи в молекуле воды или др. водородосодержащих соединениях; Ø неисчерпаемым источником световой энергии является Солнце; Ø из-за рассеяния и отражения в атмосфере до поверхности Земли доходит примерно 50% от общего солнечного излучения, что составляет 20· 1020 к. Дж/год, а это в 104 раз больше годовой добычи всех органических горючих в мире (таких как уголь, нефть, газ); Ø одной из важнейших задач водородной технологии является обязательное использование этого мощного источника первичной энергии для получения водорода, т. к. этот процесс характеризуется практической неисчерпаемостью ресурсов и полной совместимостью с окружающей средой, что очень актуально в настоящее время. 93
Фотолиз Ø получение водорода методом фотолиза основано на способности поглощенного кванта света разрывать водородные связи в молекуле воды или др. водородосодержащих соединениях; Ø неисчерпаемым источником световой энергии является Солнце; Ø из-за рассеяния и отражения в атмосфере до поверхности Земли доходит примерно 50% от общего солнечного излучения, что составляет 20· 1020 к. Дж/год, а это в 104 раз больше годовой добычи всех органических горючих в мире (таких как уголь, нефть, газ); Ø одной из важнейших задач водородной технологии является обязательное использование этого мощного источника первичной энергии для получения водорода, т. к. этот процесс характеризуется практической неисчерпаемостью ресурсов и полной совместимостью с окружающей средой, что очень актуально в настоящее время. 93
 Фотолиз Ø Фотолиз воды основан на прямом распаде молекулы воды под воздействием кванта hν поглощенного света; Ø энергия кванта света, достаточная для разрыва связи молекулы воды, равна 237, 4 к. Дж/моль, что соответствует длине волны 5, 07· 10 -7 м; Ø необходимая интенсивность фотолиза достигается в области спектра излучения короче 4· 10 -7 м, что соответствует примерно 293 к. Дж/моль; Ø наиболее благоприятно процесс протекает в диапазоне волн 1, 90 – 2, 44 · 10 -7 м, в виде такой энергии до земной поверхности доходит всего около 3 % от общей суммарной солнечного излучения; Ø прямое фотолитическое разложение воды наблюдается в верхних слоях атмосферы под действием короткого ультрафиолетового излучения с энергией 3 э. В. Между тем средняя энергия фотонов, достигающих поверхность Земли, составляет 1, 14 – 1, 48 э. В, что не достаточно для протекания прямой фотолитической реакции; Ø для протекания реакции требуется энергия 2, 46 э. В. 94
Фотолиз Ø Фотолиз воды основан на прямом распаде молекулы воды под воздействием кванта hν поглощенного света; Ø энергия кванта света, достаточная для разрыва связи молекулы воды, равна 237, 4 к. Дж/моль, что соответствует длине волны 5, 07· 10 -7 м; Ø необходимая интенсивность фотолиза достигается в области спектра излучения короче 4· 10 -7 м, что соответствует примерно 293 к. Дж/моль; Ø наиболее благоприятно процесс протекает в диапазоне волн 1, 90 – 2, 44 · 10 -7 м, в виде такой энергии до земной поверхности доходит всего около 3 % от общей суммарной солнечного излучения; Ø прямое фотолитическое разложение воды наблюдается в верхних слоях атмосферы под действием короткого ультрафиолетового излучения с энергией 3 э. В. Между тем средняя энергия фотонов, достигающих поверхность Земли, составляет 1, 14 – 1, 48 э. В, что не достаточно для протекания прямой фотолитической реакции; Ø для протекания реакции требуется энергия 2, 46 э. В. 94
 Фотолиз Ø энергию для протекания процесса (2, 46 э. В) можно снизить до уровня 1, 23 э. В, если осуществлять эту реакцию как последовательность реакций переноса электронов с использованием катализатора для выделения Н 2 и О 2 ; Ø т. к. обычная вода прозрачна, для ее фотохимического разложения необходимо вводить в процесс фотокатализаторы, имеющие большой коэффициент поглощения в широкой области солнечного спектра; Ø здесь посредником в передаче энергии солнечного света будет молекула, которая будет поглощать квант видимого света и переходить при этом в возбужденное состояние, а затем буде отдавать эту энергию воде; Ø в качестве фотохимических катализаторов (сенсибилизаторы), используются соединения типа сложных неорганических солей элементов, имеющих переменную валентность, а также органические красители (метиленовый голубой C 16 H 24 Cl. N 3 O 3 S); Ø кроме (фотосенсибилизатора) в фотохимическом процессе участвуют несветочувствительное вещество, в водной среде играющее роль восстановителя по отношению к катализатору (аскорбиновая кислота, 95 аллилтиомочевина - C 4 H 8 N 2 S)
Фотолиз Ø энергию для протекания процесса (2, 46 э. В) можно снизить до уровня 1, 23 э. В, если осуществлять эту реакцию как последовательность реакций переноса электронов с использованием катализатора для выделения Н 2 и О 2 ; Ø т. к. обычная вода прозрачна, для ее фотохимического разложения необходимо вводить в процесс фотокатализаторы, имеющие большой коэффициент поглощения в широкой области солнечного спектра; Ø здесь посредником в передаче энергии солнечного света будет молекула, которая будет поглощать квант видимого света и переходить при этом в возбужденное состояние, а затем буде отдавать эту энергию воде; Ø в качестве фотохимических катализаторов (сенсибилизаторы), используются соединения типа сложных неорганических солей элементов, имеющих переменную валентность, а также органические красители (метиленовый голубой C 16 H 24 Cl. N 3 O 3 S); Ø кроме (фотосенсибилизатора) в фотохимическом процессе участвуют несветочувствительное вещество, в водной среде играющее роль восстановителя по отношению к катализатору (аскорбиновая кислота, 95 аллилтиомочевина - C 4 H 8 N 2 S)
 Фотолиз Ø в основе процесса фотохимического разложения воды лежат реакции межмолекулярного переноса электронов, т. е. электронные окислительно – восстановительные реакции; Ø суть процесса заключается в том, что молекула красителя, которая поглощает свет, переходит после поглощения света в электронно – возбужденное состояние, при этом она становится одновременно и очень хорошим донором, и очень хорошим акцептором кислорода. В результате этого энергия кванта света вначале переходит в энергию электронного возбуждения молекулы красителя, а затем уже в энергию разделенных электрических зарядов; Ø именно превращение энергии кванта света в энергию разделения зарядов обеспечивает фотосинтез и фоторазложение воды. 96
Фотолиз Ø в основе процесса фотохимического разложения воды лежат реакции межмолекулярного переноса электронов, т. е. электронные окислительно – восстановительные реакции; Ø суть процесса заключается в том, что молекула красителя, которая поглощает свет, переходит после поглощения света в электронно – возбужденное состояние, при этом она становится одновременно и очень хорошим донором, и очень хорошим акцептором кислорода. В результате этого энергия кванта света вначале переходит в энергию электронного возбуждения молекулы красителя, а затем уже в энергию разделенных электрических зарядов; Ø именно превращение энергии кванта света в энергию разделения зарядов обеспечивает фотосинтез и фоторазложение воды. 96
 электрохимический фотолиз Ø В данном методе в качестве электродов электрохимической ячейки используют полупроводниковый монокристалл, например титана, и металлическую сетку с платиновой чернью, которые в электролизере с водой разделены диафрагмой. Метод фотоэлектрохимического разложения воды это один из методов многоступенчатого процесса разложения воды. В зависимости от того, где происходит поглощение света, а следовательно идет первичный фотопроцесс фотоэлектрохимические устройства для преобразования солнечной энергии делятся на две группы: в растворе (фотогальванические элементы) на электроде (фотоэлектрохимические элементы с полупроводниковыми электродами) 97
электрохимический фотолиз Ø В данном методе в качестве электродов электрохимической ячейки используют полупроводниковый монокристалл, например титана, и металлическую сетку с платиновой чернью, которые в электролизере с водой разделены диафрагмой. Метод фотоэлектрохимического разложения воды это один из методов многоступенчатого процесса разложения воды. В зависимости от того, где происходит поглощение света, а следовательно идет первичный фотопроцесс фотоэлектрохимические устройства для преобразования солнечной энергии делятся на две группы: в растворе (фотогальванические элементы) на электроде (фотоэлектрохимические элементы с полупроводниковыми электродами) 97
 электрохимический фотолиз Ø Фотоэлектрохимический процесс разложения воды это электрохимические реакции, протекающие при облучении электрода светом. Ø Если использовать полупроводниковые соединения в качестве катализаторов фотоэлектролитического разложения воды, то появляется возможность увеличить термическую эффективность процесса. Ø Процесс в целом состоит из двух взаимно связанных частей: 1. преобразование света в электрический ток (т. е. поток электронов); 2. превращение электрического тока в химическую энергию водорода. 98
электрохимический фотолиз Ø Фотоэлектрохимический процесс разложения воды это электрохимические реакции, протекающие при облучении электрода светом. Ø Если использовать полупроводниковые соединения в качестве катализаторов фотоэлектролитического разложения воды, то появляется возможность увеличить термическую эффективность процесса. Ø Процесс в целом состоит из двух взаимно связанных частей: 1. преобразование света в электрический ток (т. е. поток электронов); 2. превращение электрического тока в химическую энергию водорода. 98
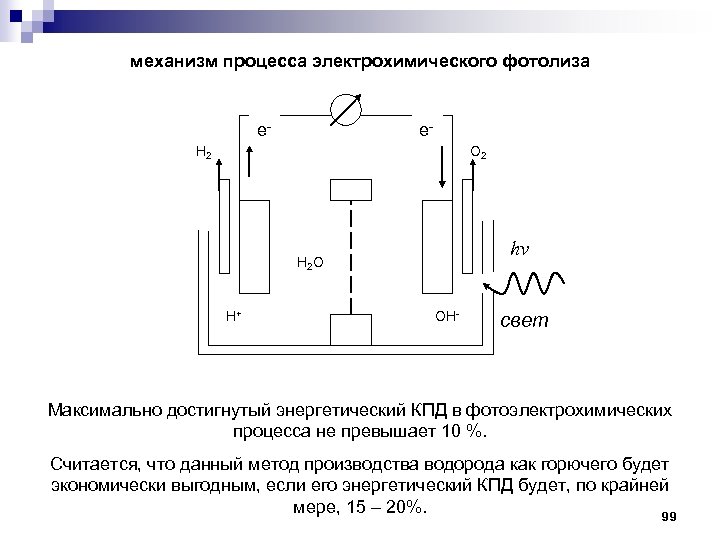 механизм процесса электрохимического фотолиза е- е- Н 2 О 2 hν Н 2 О Н+ ОН- свет Максимально достигнутый энергетический КПД в фотоэлектрохимических процесса не превышает 10 %. Считается, что данный метод производства водорода как горючего будет экономически выгодным, если его энергетический КПД будет, по крайней мере, 15 – 20%. 99
механизм процесса электрохимического фотолиза е- е- Н 2 О 2 hν Н 2 О Н+ ОН- свет Максимально достигнутый энергетический КПД в фотоэлектрохимических процесса не превышает 10 %. Считается, что данный метод производства водорода как горючего будет экономически выгодным, если его энергетический КПД будет, по крайней мере, 15 – 20%. 99
 термохимические методы получения водорода Термохимические методы получения водорода относят к промышленным методам получения водорода на базе конверсии углеводородов и газификации твердых горючих и использованием разных источников энергии, в том числе энергии атомных реакторов. Термохимические методы получения Н делятся на две большие группы: термохимические методы получения водорода с открытым циклом термохимические методы получения водорода с закрытым циклом 100
термохимические методы получения водорода Термохимические методы получения водорода относят к промышленным методам получения водорода на базе конверсии углеводородов и газификации твердых горючих и использованием разных источников энергии, в том числе энергии атомных реакторов. Термохимические методы получения Н делятся на две большие группы: термохимические методы получения водорода с открытым циклом термохимические методы получения водорода с закрытым циклом 100
 термохимические методы получения водорода с открытым циклом Ø практически все современные промышленные процессы получения водорода базируются на первой группе методов; Ø их характерная особенность заключается в том, что энергию, необходимую для разложения воды на водород и кислород, получают путем сжигания органического горючего; Ø процесс получения водорода из воды сопровождается реакцией, в которой происходит связывание кислорода углеродом горючего с образованием диоксида углерода: C + H 2 O = CO + H 2, CO + H 2 O = H 2 + CO 2 или C + H 2 O + 2 KOH = K 2 CO 3 + 2 H 2, K 2 CO 3 + H 2 O = 2 KOH + CO 2↑ 101
термохимические методы получения водорода с открытым циклом Ø практически все современные промышленные процессы получения водорода базируются на первой группе методов; Ø их характерная особенность заключается в том, что энергию, необходимую для разложения воды на водород и кислород, получают путем сжигания органического горючего; Ø процесс получения водорода из воды сопровождается реакцией, в которой происходит связывание кислорода углеродом горючего с образованием диоксида углерода: C + H 2 O = CO + H 2, CO + H 2 O = H 2 + CO 2 или C + H 2 O + 2 KOH = K 2 CO 3 + 2 H 2, K 2 CO 3 + H 2 O = 2 KOH + CO 2↑ 101
 термохимические методы получения водорода с открытым циклом Ø важнейшим недостатком открытого термохимического цикла является то, что наряду с товарным водородом, в качестве отхода в окружающее пространство выбрасывается такое вредное соединение как диоксид углерода (углекислый газ CO 2); Ø например, на 1 т водорода получается примерно 10 – 50 т СО 2 в зависимости от того, по какой технологии осуществлен процесс и что было использовано в качестве исходного сырья. 102
термохимические методы получения водорода с открытым циклом Ø важнейшим недостатком открытого термохимического цикла является то, что наряду с товарным водородом, в качестве отхода в окружающее пространство выбрасывается такое вредное соединение как диоксид углерода (углекислый газ CO 2); Ø например, на 1 т водорода получается примерно 10 – 50 т СО 2 в зависимости от того, по какой технологии осуществлен процесс и что было использовано в качестве исходного сырья. 102
 термохимические методы получения водорода с закрытым циклом термохимические циклы, которые в принципе не дают отходов, если к циклу будет подведено тепло необходимого потенциала Примеры закрытого термохимического цикла: 1. Высокотемпературный вариант: C + H 2 O → 1000 К CO + H 2, CO + 2 Fe 3 O 4 → 520 K C + 3 Fe 2 O 3; 3 Fe 2 O 3 → 1700 K 2 Fe 3 O 4 + 0, 5 O 2 H 2 O → H 2 + 0, 5 O 2 2. Низкотемпературный вариант: 3 Fe + 3 H 2 O → 820 -870 K 3 Fe. O + 3 H 2, 3 Fe. O + H 2 O → 820 -870 K Fe 3 O 4 + H 2; Fe 3 O 4 + CO → 1220 K 3 Fe. O + CO 2 , 3 Fe. O + 3 CO → 1220 K 3 Fe + 3 CO 2 ; 4 CO 2 → 590 K 4 CO + 2 O 2 2 H 2 O → 2 H 2 + O 2 103
термохимические методы получения водорода с закрытым циклом термохимические циклы, которые в принципе не дают отходов, если к циклу будет подведено тепло необходимого потенциала Примеры закрытого термохимического цикла: 1. Высокотемпературный вариант: C + H 2 O → 1000 К CO + H 2, CO + 2 Fe 3 O 4 → 520 K C + 3 Fe 2 O 3; 3 Fe 2 O 3 → 1700 K 2 Fe 3 O 4 + 0, 5 O 2 H 2 O → H 2 + 0, 5 O 2 2. Низкотемпературный вариант: 3 Fe + 3 H 2 O → 820 -870 K 3 Fe. O + 3 H 2, 3 Fe. O + H 2 O → 820 -870 K Fe 3 O 4 + H 2; Fe 3 O 4 + CO → 1220 K 3 Fe. O + CO 2 , 3 Fe. O + 3 CO → 1220 K 3 Fe + 3 CO 2 ; 4 CO 2 → 590 K 4 CO + 2 O 2 2 H 2 O → 2 H 2 + O 2 103
 термохимические методы получения водорода с закрытым циклом Ø В ходе процесса из цикла отводится водород, соответствующее количество кислорода и деградированное тепло; Ø в том случае, если необходимое тепло получать только на основе сжигания органического горючего, то понятно, что ни в экономическом, ни в экологическом отношении эти термохимические циклы не дают никаких преимуществ по сравнению с открытыми циклами; Ø если для получения теплоты использовать альтернативные, экологически чистые, да к тому же еще и возобновляемые источники, то данный процесс становится весьма привлекательным и перспективным. 104
термохимические методы получения водорода с закрытым циклом Ø В ходе процесса из цикла отводится водород, соответствующее количество кислорода и деградированное тепло; Ø в том случае, если необходимое тепло получать только на основе сжигания органического горючего, то понятно, что ни в экономическом, ни в экологическом отношении эти термохимические циклы не дают никаких преимуществ по сравнению с открытыми циклами; Ø если для получения теплоты использовать альтернативные, экологически чистые, да к тому же еще и возобновляемые источники, то данный процесс становится весьма привлекательным и перспективным. 104
 термохимические методы получения водорода с закрытым циклом Ø Источник энергии, который мог бы быть использован и, более того, давно используется является атомная энергия; Ø сущность использования тепла ядерной реакции для закрытых термохимических циклов заключается в том, что в этом случае тепло ядерной реакции непосредственно превращается в химическую энергию водорода (например, также как в энергетических циклах тепло превращается в работу); Ø считается, что наибольшим экономическим потенциалом обладает энергетическая система на основе водорода, в фундамент которой заложена ядерная станция, которая выдает тепло для термохимического разложения воды. 105
термохимические методы получения водорода с закрытым циклом Ø Источник энергии, который мог бы быть использован и, более того, давно используется является атомная энергия; Ø сущность использования тепла ядерной реакции для закрытых термохимических циклов заключается в том, что в этом случае тепло ядерной реакции непосредственно превращается в химическую энергию водорода (например, также как в энергетических циклах тепло превращается в работу); Ø считается, что наибольшим экономическим потенциалом обладает энергетическая система на основе водорода, в фундамент которой заложена ядерная станция, которая выдает тепло для термохимического разложения воды. 105
 термохимические методы получения водорода с закрытым циклом Для осуществления процесса термохимического разложения воды, могут быть построены две следующие энергетические системы: 1. тепло ядерной реакции – пар – электричество – водород; 2. тепло ядерной реакции – водород – тепло или электричество. Ø Обе эти системы удовлетворяют строгим экологическим требованиям; Ø для создания этих систем не требуется органическое горючее; Ø оба эти решения основаны на применении воды в качестве источника для получения водорода и применении тепловой энергии, которая будет производиться при помощи ядерного реактора; Ø но путь использования этого тепла в первом и во втором случаях 106 различен.
термохимические методы получения водорода с закрытым циклом Для осуществления процесса термохимического разложения воды, могут быть построены две следующие энергетические системы: 1. тепло ядерной реакции – пар – электричество – водород; 2. тепло ядерной реакции – водород – тепло или электричество. Ø Обе эти системы удовлетворяют строгим экологическим требованиям; Ø для создания этих систем не требуется органическое горючее; Ø оба эти решения основаны на применении воды в качестве источника для получения водорода и применении тепловой энергии, которая будет производиться при помощи ядерного реактора; Ø но путь использования этого тепла в первом и во втором случаях 106 различен.
 термохимические методы получения водорода с закрытым циклом система “тепло ядерной реакции – пар – электричество – водород”, Ø данная система предусматривает использование тепла ядерной реакции для получения пара с его последующим использованием в паровой турбине, которая связана с электрогенераторо; Ø произведенную таким образом электроэнергию далее используют в электролизере для электрохимического разложения воды на водород и кислород. 107
термохимические методы получения водорода с закрытым циклом система “тепло ядерной реакции – пар – электричество – водород”, Ø данная система предусматривает использование тепла ядерной реакции для получения пара с его последующим использованием в паровой турбине, которая связана с электрогенераторо; Ø произведенную таким образом электроэнергию далее используют в электролизере для электрохимического разложения воды на водород и кислород. 107
 термохимические методы получения водорода с закрытым циклом система “тепло ядерной реакции – водород – тепло или электричество” Ø данная система основана на непосредственном использовании тепла ядерной реакции, минуя стадию получения электроэнергии для термохимического разложения воды на водород и кислород. В этих обоих системах в качестве побочных продуктов выделяются вода и низкопотенциальное тепло, т. е. в отходах нет продуктов, загрязняющих окружающую среду. 108
термохимические методы получения водорода с закрытым циклом система “тепло ядерной реакции – водород – тепло или электричество” Ø данная система основана на непосредственном использовании тепла ядерной реакции, минуя стадию получения электроэнергии для термохимического разложения воды на водород и кислород. В этих обоих системах в качестве побочных продуктов выделяются вода и низкопотенциальное тепло, т. е. в отходах нет продуктов, загрязняющих окружающую среду. 108
 термохимические методы получения водорода с закрытым циклом критерии выбора термохимического цикла разложения воды 1. Максимальная температура процесса. В лучшем случае она не должна превышать 1200 – 1300 К. Такая температура обусловлена максимально достижимой на сегодняшний день температурой теплоносителя на выходе из атомного реактора. 2. Общий энергетический КПД. Он д. б. достаточно высок, и во всяком случае превышать общий КПД электролиза воды с учетом КПД получения электроэнергии. 3. Химические вещества, участвующие в круговом процессе. Так эти вещества д. б. доступны по цене и не оказывать отрицательного влияния на окружающую среду. 109
термохимические методы получения водорода с закрытым циклом критерии выбора термохимического цикла разложения воды 1. Максимальная температура процесса. В лучшем случае она не должна превышать 1200 – 1300 К. Такая температура обусловлена максимально достижимой на сегодняшний день температурой теплоносителя на выходе из атомного реактора. 2. Общий энергетический КПД. Он д. б. достаточно высок, и во всяком случае превышать общий КПД электролиза воды с учетом КПД получения электроэнергии. 3. Химические вещества, участвующие в круговом процессе. Так эти вещества д. б. доступны по цене и не оказывать отрицательного влияния на окружающую среду. 109
 достоинствах и недостатках термохимических циклов достоинства: 1. Неограниченный источник дешевого сырья вода. 2. Энергия вносится в процесс в своей наиболее дешевой форме – тепло атомного реактора. 3. Все промежуточные продукты химических процессов возвращаются в цикл, т. е. система теоретически не должна иметь отходов. 4. Реакции цикла протекают при сравнительно невысоких температурах. 5. Водород и кислород, получаемые в процессе, легко разделить в ходе кругового цикла. 110
достоинствах и недостатках термохимических циклов достоинства: 1. Неограниченный источник дешевого сырья вода. 2. Энергия вносится в процесс в своей наиболее дешевой форме – тепло атомного реактора. 3. Все промежуточные продукты химических процессов возвращаются в цикл, т. е. система теоретически не должна иметь отходов. 4. Реакции цикла протекают при сравнительно невысоких температурах. 5. Водород и кислород, получаемые в процессе, легко разделить в ходе кругового цикла. 110
 достоинствах и недостатках термохимических циклов достоинства: 6. Энергия тепла атомного реактора непосредственно превращается в химическую энергию водорода. 7. Большинство предлагаемых процессов не сопровождаются образованием побочных продуктов. 8. В качестве химических реагентов, которые участвуют в циклах, используются элементы и соединения, которые широко распространены в природе и часто используются в химической технологии. 9. Энергия для процессов получается за счет использования дешевого тепла атомного реактора. 111
достоинствах и недостатках термохимических циклов достоинства: 6. Энергия тепла атомного реактора непосредственно превращается в химическую энергию водорода. 7. Большинство предлагаемых процессов не сопровождаются образованием побочных продуктов. 8. В качестве химических реагентов, которые участвуют в циклах, используются элементы и соединения, которые широко распространены в природе и часто используются в химической технологии. 9. Энергия для процессов получается за счет использования дешевого тепла атомного реактора. 111
 достоинствах и недостатках термохимических циклов недостатки: 1. Необходимость многократного нагрева и охлаждения продуктов реакции в ряде циклов. 2. Степень превращения в отдельных реакциях не достигает достаточной полноты. Не прореагировавшие вещества могут присутствовать в продуктах, переходящих в последующие реакции цикла, что взывает необходимость в каждом отдельном случае выяснять как они влияют на последующие стадии процесса. 3. Неизбежны значительные затраты энергии на циркуляцию промежуточных продуктов. 4. Возможны потери циркулирующих продуктов с покидающими систему водородом и кислородом, в частности по механическим причинам, например в результате каких-то неплотностей. Это накладывает жесткие требования на конструкцию оборудования и 112 его эксплуатацию.
достоинствах и недостатках термохимических циклов недостатки: 1. Необходимость многократного нагрева и охлаждения продуктов реакции в ряде циклов. 2. Степень превращения в отдельных реакциях не достигает достаточной полноты. Не прореагировавшие вещества могут присутствовать в продуктах, переходящих в последующие реакции цикла, что взывает необходимость в каждом отдельном случае выяснять как они влияют на последующие стадии процесса. 3. Неизбежны значительные затраты энергии на циркуляцию промежуточных продуктов. 4. Возможны потери циркулирующих продуктов с покидающими систему водородом и кислородом, в частности по механическим причинам, например в результате каких-то неплотностей. Это накладывает жесткие требования на конструкцию оборудования и 112 его эксплуатацию.
 достоинствах и недостатках термохимических циклов недостатки: 5. При образовании побочных продуктов очень важно определить требования и условия, в которых их получение будет минимальным. 6. Высокий термический КПД термохимического цикла может быть обеспечен только при использовании наиболее высокотемпературного теплоносителя. А это означает, что развитие термохимических процессов в значительной степени зависит от успехов в строительстве соответствующих атомных реакторов. 7. Проведение большинства реакций требует использование дорогих химикатов, часто неблагоприятных в экологическом плане, что вызывает необходимость тщательной очистки водорода и кислорода перед их использованием. 113
достоинствах и недостатках термохимических циклов недостатки: 5. При образовании побочных продуктов очень важно определить требования и условия, в которых их получение будет минимальным. 6. Высокий термический КПД термохимического цикла может быть обеспечен только при использовании наиболее высокотемпературного теплоносителя. А это означает, что развитие термохимических процессов в значительной степени зависит от успехов в строительстве соответствующих атомных реакторов. 7. Проведение большинства реакций требует использование дорогих химикатов, часто неблагоприятных в экологическом плане, что вызывает необходимость тщательной очистки водорода и кислорода перед их использованием. 113
 радиолиз Ø Радиолиз это процесс химического превращения происходящие под действием ионизующих излучений; вещества, Ø известно, что атомный реактор является источником не только тепла, но и излучения, поэтому, в дополнение к использованию тепла атомного реактора для генерации электроэнергии или использования этого тепла в химической и металлургической промышленности, перспективным является использование атомного реактора также в качестве источника излучения для создания радиационно – химической технологии; Ø для процесса радиолиза наиболее просто использовать γ – излучение, нейтроны и α – частицы. Ø в случае, когда требуется наиболее эффективное использование энергии реактора, могут быть использованы осколки деления; Ø например, при использовании только γ – излучения будет потребляться лишь 0, 3 – 0, 5 % от тепловой мощности реактора, остальная мощность ядерного реактора должна быть направлена на получение чисто тепловой или электрической энергии. 114
радиолиз Ø Радиолиз это процесс химического превращения происходящие под действием ионизующих излучений; вещества, Ø известно, что атомный реактор является источником не только тепла, но и излучения, поэтому, в дополнение к использованию тепла атомного реактора для генерации электроэнергии или использования этого тепла в химической и металлургической промышленности, перспективным является использование атомного реактора также в качестве источника излучения для создания радиационно – химической технологии; Ø для процесса радиолиза наиболее просто использовать γ – излучение, нейтроны и α – частицы. Ø в случае, когда требуется наиболее эффективное использование энергии реактора, могут быть использованы осколки деления; Ø например, при использовании только γ – излучения будет потребляться лишь 0, 3 – 0, 5 % от тепловой мощности реактора, остальная мощность ядерного реактора должна быть направлена на получение чисто тепловой или электрической энергии. 114
 радиолиз 1. Радиолиз воды: H 2 O (г) → 298 К Н 2 (г) + 1/2 О 2 (г), ∆Н = + 286, 0 к. Дж/моль, тип радиации: γ – лучи. 2. Радиолиз различных углеводородов: С 2 Н 4 (г) → 298 К Н 2 (г) + С 2 Н 2 (г), ∆Н = + 393, 0 к. Дж/моль, тип излучения: γ – лучи, поток нейтронов. 3. Радиолиз диоксида углерода: СО 2 (г) → 298 К СО (г), ∆Н = + 280, 0 к. Дж/моль, тип радиации: γ – лучи. 115
радиолиз 1. Радиолиз воды: H 2 O (г) → 298 К Н 2 (г) + 1/2 О 2 (г), ∆Н = + 286, 0 к. Дж/моль, тип радиации: γ – лучи. 2. Радиолиз различных углеводородов: С 2 Н 4 (г) → 298 К Н 2 (г) + С 2 Н 2 (г), ∆Н = + 393, 0 к. Дж/моль, тип излучения: γ – лучи, поток нейтронов. 3. Радиолиз диоксида углерода: СО 2 (г) → 298 К СО (г), ∆Н = + 280, 0 к. Дж/моль, тип радиации: γ – лучи. 115
 радиолиз Ø Для сравнения эффективности химических процессов, которые возбуждаются радиацией, пользуются величиной, которая называется радиационный выход g; Ø g водорода в процессах разложения воды при использовании в качестве ионизирующих излучений нейтронов и γ – излучения достаточно мал; Ø значения g для производства водорода радиолизом чистой воды находятся в интервале 0, 45 – 0, 17 в зависимости от условий и типа радиации; Ø в основном механизмы производства водорода радиолизом воды хорошо известны и шансы значительно увеличить g(Н 2) довольно малы, и этот способ производства водорода, вероятнее всего, имеет мало перспектив. 116
радиолиз Ø Для сравнения эффективности химических процессов, которые возбуждаются радиацией, пользуются величиной, которая называется радиационный выход g; Ø g водорода в процессах разложения воды при использовании в качестве ионизирующих излучений нейтронов и γ – излучения достаточно мал; Ø значения g для производства водорода радиолизом чистой воды находятся в интервале 0, 45 – 0, 17 в зависимости от условий и типа радиации; Ø в основном механизмы производства водорода радиолизом воды хорошо известны и шансы значительно увеличить g(Н 2) довольно малы, и этот способ производства водорода, вероятнее всего, имеет мало перспектив. 116
 радиолиз Ø в то же время известен тот факт, что добавка к воде соединений некоторых типов может значительно повысить g(H 2); Ø например, результаты исследований показали, что добавление иона ВН-4 (борогидрид) позволило получить g(H 2) порядка 50 к. Дж/моль; Ø тем не менее, экспериментальные исследования показали, что радиолиз воды пока малоэффективен для получения водорода. 117
радиолиз Ø в то же время известен тот факт, что добавка к воде соединений некоторых типов может значительно повысить g(H 2); Ø например, результаты исследований показали, что добавление иона ВН-4 (борогидрид) позволило получить g(H 2) порядка 50 к. Дж/моль; Ø тем не менее, экспериментальные исследования показали, что радиолиз воды пока малоэффективен для получения водорода. 117
 водород из биомассы Биома сса это совокупная масса растительных и животных организмов. Ø биомасса занимает шестое место среди всех источников энергии по запасам доступных на настоящий момент источников энергии (после горючих сланцев, урана, угля, нефти, и природного газа); Ø приближённо полная биологическая масса земли оценивается в 2, 4× 1012 тонн; Ø кроме того, в ряде возобновляемых источников энергии биомасса находится на пятом месте по производительности, после прямой солнечной, ветровой, гидро – и геотермальной энергии; Ø биологическое производство водорода включает в себя два этапа: 1. выращивание биомассы; 2. последующее ее превращение в водород посредством микробиологического сбраживания. 118
водород из биомассы Биома сса это совокупная масса растительных и животных организмов. Ø биомасса занимает шестое место среди всех источников энергии по запасам доступных на настоящий момент источников энергии (после горючих сланцев, урана, угля, нефти, и природного газа); Ø приближённо полная биологическая масса земли оценивается в 2, 4× 1012 тонн; Ø кроме того, в ряде возобновляемых источников энергии биомасса находится на пятом месте по производительности, после прямой солнечной, ветровой, гидро – и геотермальной энергии; Ø биологическое производство водорода включает в себя два этапа: 1. выращивание биомассы; 2. последующее ее превращение в водород посредством микробиологического сбраживания. 118
 водород из биомассы Ø В биомассе водорослей, находящихся в океане, заключается огромное количество энергии; Ø предполагается использовать для переработки на топливо как прибрежные водоросли, так и фитопланктон; Ø в качестве основных способов переработки рассматриваются сбраживание углеводов водорослей в спирты и ферментация больших количеств водорослей без доступа воздуха для производства метана; Ø разрабатывается также технология переработки фитопланктона для производства жидкого топлива, эту технологию предполагается совместить с эксплуатацией океанских термальных электростанций, подогретые глубинные воды которых будут обеспечивать процесс разведения фитопланктона, т. е. будут давать тепло и питательные вещества, что будет способствовать разведению фитопланктона. 119
водород из биомассы Ø В биомассе водорослей, находящихся в океане, заключается огромное количество энергии; Ø предполагается использовать для переработки на топливо как прибрежные водоросли, так и фитопланктон; Ø в качестве основных способов переработки рассматриваются сбраживание углеводов водорослей в спирты и ферментация больших количеств водорослей без доступа воздуха для производства метана; Ø разрабатывается также технология переработки фитопланктона для производства жидкого топлива, эту технологию предполагается совместить с эксплуатацией океанских термальных электростанций, подогретые глубинные воды которых будут обеспечивать процесс разведения фитопланктона, т. е. будут давать тепло и питательные вещества, что будет способствовать разведению фитопланктона. 119
 водород из биомассы способы получения водорода из биомассы термохимический биохимический 120
водород из биомассы способы получения водорода из биомассы термохимический биохимический 120
 водород из биомассы термохимический метод: - биомассу нагревают без доступа кислорода до температуры 500 – 800 °С (для отходов древесины), что намного ниже температуры процесса, например газификации угля. - в результате процесса выделяется H 2, CO и CH 4. - современные установки производят электричество из биомассы с КПД более 30 %. 121
водород из биомассы термохимический метод: - биомассу нагревают без доступа кислорода до температуры 500 – 800 °С (для отходов древесины), что намного ниже температуры процесса, например газификации угля. - в результате процесса выделяется H 2, CO и CH 4. - современные установки производят электричество из биомассы с КПД более 30 %. 121
 водород из биомассы биохимический процесс - водород вырабатывают различные бактерии, например, Rodobacter speriodes. - возможно применение различных энзимов для ускорения производства водорода из полисахаридоа (крахмал, целлюлоза), содержащихся в биомассе. - процесс проходит при температуре 30 °С при нормальном давлении. - себестоимость водорода около $2/кг. 122
водород из биомассы биохимический процесс - водород вырабатывают различные бактерии, например, Rodobacter speriodes. - возможно применение различных энзимов для ускорения производства водорода из полисахаридоа (крахмал, целлюлоза), содержащихся в биомассе. - процесс проходит при температуре 30 °С при нормальном давлении. - себестоимость водорода около $2/кг. 122
 водород из мусора ü В октябре 2006 года Лондонское Водородное Партнёрство опубликовало исследование о возможности производства водорода из муниципального и коммерческого мусора. ü Согласно исследованию, в Лондоне можно ежедневно производить 141 тонну водорода как пиролизом, так и анаэробным сбраживанием мусора. ü Этого количества водорода достаточно для работы 13750 автобусов с двигателями внутреннего сгорания, работающими на водороде. 123
водород из мусора ü В октябре 2006 года Лондонское Водородное Партнёрство опубликовало исследование о возможности производства водорода из муниципального и коммерческого мусора. ü Согласно исследованию, в Лондоне можно ежедневно производить 141 тонну водорода как пиролизом, так и анаэробным сбраживанием мусора. ü Этого количества водорода достаточно для работы 13750 автобусов с двигателями внутреннего сгорания, работающими на водороде. 123
 химическая реакция воды с металлами ü В 2007 году Университет Purdue (США) разработал метод производства водорода из воды при помощи алюминиевого сплава. ü Сплав алюминия с галием формируется в пеллеты, которые помещают в бак с водой. В результате химической реакции производится водород. Галлий создаёт вокруг алюминия плёнку, которая предотвращает окисление алюминия. В результате реакции создаётся водород и оксид алюминия. ü Из одного фунта алюминия можно получать более 2 к. Вт/ч энергии от сжигания водорода и более 2 к. Вт·ч тепловой энергии во время реакции алюминия с водой. 124
химическая реакция воды с металлами ü В 2007 году Университет Purdue (США) разработал метод производства водорода из воды при помощи алюминиевого сплава. ü Сплав алюминия с галием формируется в пеллеты, которые помещают в бак с водой. В результате химической реакции производится водород. Галлий создаёт вокруг алюминия плёнку, которая предотвращает окисление алюминия. В результате реакции создаётся водород и оксид алюминия. ü Из одного фунта алюминия можно получать более 2 к. Вт/ч энергии от сжигания водорода и более 2 к. Вт·ч тепловой энергии во время реакции алюминия с водой. 124
 производство водорода при использовании различных источников энергии из энергии ветра ü Департамент Энергетики США (DOE) и Национальная Исследовательская Энергетическая Лаборатория (NREL) с 2006 г. проводит исследовательские работы «Водород из ветра» . ü Построена водородная заправочная станция с ветрогенератором мощностью 100 к. Вт. ü Исследования должны сравнить методы производства водорода гидролизом из энергии ветра и энергии из промышленной электрической сети. ü Ветро-гидролизная система установлена в Национальном Ветряном Технологическом Центре, принадлежащем NREL. Будут сравниваться различные технологии гидролиза воды, хранения, их стоимости. ü Согласно расчетам NREL, произведённым в 2006 году, в ближайшем будущем себестоимость производства водорода из энергии ветра составит $4, 03/кг водорода. В долгосрочной перспективе себестоимость водорода снизится до $2, 33/кг водорода. 125
производство водорода при использовании различных источников энергии из энергии ветра ü Департамент Энергетики США (DOE) и Национальная Исследовательская Энергетическая Лаборатория (NREL) с 2006 г. проводит исследовательские работы «Водород из ветра» . ü Построена водородная заправочная станция с ветрогенератором мощностью 100 к. Вт. ü Исследования должны сравнить методы производства водорода гидролизом из энергии ветра и энергии из промышленной электрической сети. ü Ветро-гидролизная система установлена в Национальном Ветряном Технологическом Центре, принадлежащем NREL. Будут сравниваться различные технологии гидролиза воды, хранения, их стоимости. ü Согласно расчетам NREL, произведённым в 2006 году, в ближайшем будущем себестоимость производства водорода из энергии ветра составит $4, 03/кг водорода. В долгосрочной перспективе себестоимость водорода снизится до $2, 33/кг водорода. 125
 из энергии солнца ü Швейцарская компания Clean Hydrogen Producers (CHP) разработала технологию производства водорода из воды при помощи параболичнских солнечных концентраторов. ü Площадь зеркал установки составляет 93 м 2 ü В фокусе концентратора температура достигает 2200°С. ü Вода начинает разделяться на водород и кислород при температуре более 1700° С. ü За световой день 6, 5 часов (6, 5 к. Вт·ч/м 2) установка CHP может разделять на водород и кислород 94, 9 литров воды. ü Предполагается, что производство водорода составит 3800 кг/год (около 10, 4 кг. в день). 126
из энергии солнца ü Швейцарская компания Clean Hydrogen Producers (CHP) разработала технологию производства водорода из воды при помощи параболичнских солнечных концентраторов. ü Площадь зеркал установки составляет 93 м 2 ü В фокусе концентратора температура достигает 2200°С. ü Вода начинает разделяться на водород и кислород при температуре более 1700° С. ü За световой день 6, 5 часов (6, 5 к. Вт·ч/м 2) установка CHP может разделять на водород и кислород 94, 9 литров воды. ü Предполагается, что производство водорода составит 3800 кг/год (около 10, 4 кг. в день). 126
 из энергии солнца ü Израильский Weizmann Institute of Science в 2005 году испытал технологию получения не окисленного цинка в солнечной башне. ü Оксид цинка в присутствии древесного угля нагревался зеркалами до температуры 1200 °С на вершине солнечной башни. ü В результате процесса получался чистый цинк. Далее цинк можно герметично упаковать и транспортировать к местам производства электроэнергии. ü Уже на месте цинк помещается в воду, в результате химической реакции получается водород и оксид цинка. ü Оксид цинка можно ещё раз поместить в солнечную башню и получить чистый цинк. ü Технология прошла испытания в солнечной башне канадского Institute for the Energies and Applied Research. 127
из энергии солнца ü Израильский Weizmann Institute of Science в 2005 году испытал технологию получения не окисленного цинка в солнечной башне. ü Оксид цинка в присутствии древесного угля нагревался зеркалами до температуры 1200 °С на вершине солнечной башни. ü В результате процесса получался чистый цинк. Далее цинк можно герметично упаковать и транспортировать к местам производства электроэнергии. ü Уже на месте цинк помещается в воду, в результате химической реакции получается водород и оксид цинка. ü Оксид цинка можно ещё раз поместить в солнечную башню и получить чистый цинк. ü Технология прошла испытания в солнечной башне канадского Institute for the Energies and Applied Research. 127
 из атомной энергии ü Правительством инициатива. США принята Атомная водородная ü Ведутся работы (совместно с Южной Кореей) по созданию атомных реакторов нового поколения, способных производить в больших количествах водород. ü INEEL (Idaho National Engineering Environmental Laboratory) прогнозирует, что один энергоблок атомной электростанции 4 -го поколения будет производить ежедневно водород, эквивалентный 750000 литров бензина. 128
из атомной энергии ü Правительством инициатива. США принята Атомная водородная ü Ведутся работы (совместно с Южной Кореей) по созданию атомных реакторов нового поколения, способных производить в больших количествах водород. ü INEEL (Idaho National Engineering Environmental Laboratory) прогнозирует, что один энергоблок атомной электростанции 4 -го поколения будет производить ежедневно водород, эквивалентный 750000 литров бензина. 128
 с использованием водорослей ü Данный способ производства водорода предложили и начали разрабатывать учёные калифорнийского университета в Беркли (UC Berkeley) 1999 году, когда обнаружили, что если водорослям не хватает кислорода и серы, то процессы фотосинтеза у них резко ослабевают, и начинается бурная выработка водорода. ü Водород может производить группа зелёных водорослей, например, Chlamydomonas reinhardtii. ü Водоросли могут производить водород из морской воды, или канализационных стоков. 129
с использованием водорослей ü Данный способ производства водорода предложили и начали разрабатывать учёные калифорнийского университета в Беркли (UC Berkeley) 1999 году, когда обнаружили, что если водорослям не хватает кислорода и серы, то процессы фотосинтеза у них резко ослабевают, и начинается бурная выработка водорода. ü Водород может производить группа зелёных водорослей, например, Chlamydomonas reinhardtii. ü Водоросли могут производить водород из морской воды, или канализационных стоков. 129
 домашние системы производства водорода ü Вместо строительства водородных заправочных станций водород можно производить в бытовых установках из природного газа, или электролизом воды. ü Honda испытывает свою бытовую установку под названием “Домашняя энергетическая станция Honda” ü Установка в бытовых условиях производит водород из природного газа. ü Часть водорода используется в топливных элементах для производства тепловой и электрической энергии для дома, а оставшаяся часть водорода используется для заправки автомобиля. 130
домашние системы производства водорода ü Вместо строительства водородных заправочных станций водород можно производить в бытовых установках из природного газа, или электролизом воды. ü Honda испытывает свою бытовую установку под названием “Домашняя энергетическая станция Honda” ü Установка в бытовых условиях производит водород из природного газа. ü Часть водорода используется в топливных элементах для производства тепловой и электрической энергии для дома, а оставшаяся часть водорода используется для заправки автомобиля. 130
 домашние системы производства водорода ü Британская компания ITM Power Plc разработала и испытала в 2007 г. бытовой электролизёр для производства водорода. ü Водород производится ночью, это позволит сгладить пики потребления электроэнергии. ü Электролизер мощностью 10 к. Вт производит из воды водород, и хранит его под давлением 75 бар. ü Произведённого водорода достаточно для 40 км. пробега биотопливного (водород/бензин) Ford Focus. ü Компания начала производство таких бытовых электролизеров в начале 2008 года. ü ITM Power уже достигла уровня себестоимости электролизеров $164 за 1 к. В. 131
домашние системы производства водорода ü Британская компания ITM Power Plc разработала и испытала в 2007 г. бытовой электролизёр для производства водорода. ü Водород производится ночью, это позволит сгладить пики потребления электроэнергии. ü Электролизер мощностью 10 к. Вт производит из воды водород, и хранит его под давлением 75 бар. ü Произведённого водорода достаточно для 40 км. пробега биотопливного (водород/бензин) Ford Focus. ü Компания начала производство таких бытовых электролизеров в начале 2008 года. ü ITM Power уже достигла уровня себестоимости электролизеров $164 за 1 к. В. 131
 методы производства водорода объем мирового производства водорода уже сейчас составляет 50 млн. тонн и эта цифра постоянно растет, примерно на 5 - 10% в год. 132
методы производства водорода объем мирового производства водорода уже сейчас составляет 50 млн. тонн и эта цифра постоянно растет, примерно на 5 - 10% в год. 132
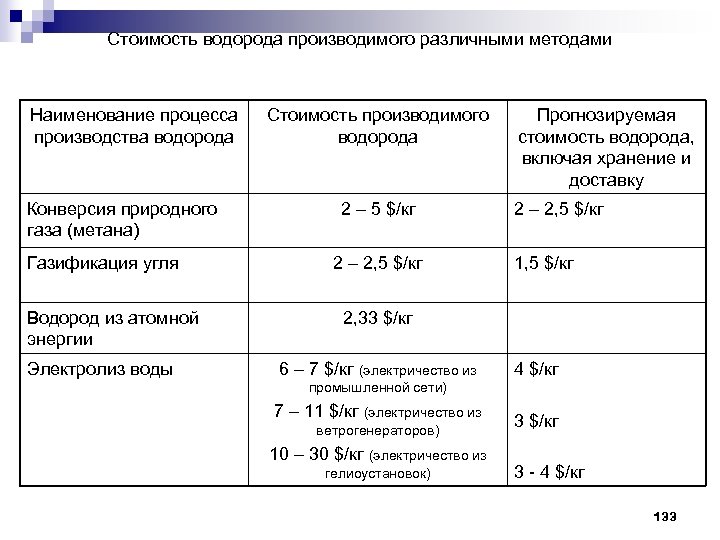 Стоимость водорода производимого различными методами Наименование процесса производства водорода Конверсия природного газа (метана) Газификация угля Водород из атомной энергии Электролиз воды Стоимость производимого водорода 2 – 5 $/кг 2 – 2, 5 $/кг Прогнозируемая стоимость водорода, включая хранение и доставку 2 – 2, 5 $/кг 1, 5 $/кг 2, 33 $/кг 6 – 7 $/кг (электричество из 4 $/кг промышленной сети) 7 – 11 $/кг (электричество из ветрогенераторов) 10 – 30 $/кг (электричество из гелиоустановок) 3 $/кг 3 - 4 $/кг 133
Стоимость водорода производимого различными методами Наименование процесса производства водорода Конверсия природного газа (метана) Газификация угля Водород из атомной энергии Электролиз воды Стоимость производимого водорода 2 – 5 $/кг 2 – 2, 5 $/кг Прогнозируемая стоимость водорода, включая хранение и доставку 2 – 2, 5 $/кг 1, 5 $/кг 2, 33 $/кг 6 – 7 $/кг (электричество из 4 $/кг промышленной сети) 7 – 11 $/кг (электричество из ветрогенераторов) 10 – 30 $/кг (электричество из гелиоустановок) 3 $/кг 3 - 4 $/кг 133


