Оксидирование сокр версия.ppt
- Количество слайдов: 26
 Лекция № 3. Оксидирование – процесс искусственного формирования на поверхности чёрных или цветных металлов оксидов – с целью защиты от коррозии, декоративной отделки, увеличения износостойкости и др. Оксидированию подвергают изделия из стали, Al и сплавов; других цветных металлов (Cu, Ti, Zn и сплавы) Различные изделия из стали, титановых сплавов, алюминиевых сплавов, с химическим покрытием (холодное чернение, анодное оксидирование) 1
Лекция № 3. Оксидирование – процесс искусственного формирования на поверхности чёрных или цветных металлов оксидов – с целью защиты от коррозии, декоративной отделки, увеличения износостойкости и др. Оксидированию подвергают изделия из стали, Al и сплавов; других цветных металлов (Cu, Ti, Zn и сплавы) Различные изделия из стали, титановых сплавов, алюминиевых сплавов, с химическим покрытием (холодное чернение, анодное оксидирование) 1
 Оксидирование стали применяется для защиты стали от коррозии и придания декоративного вида. В зависимости от режима могут быть матовые, чёрные, блестящие, с синеватым отливом, более твёрдые, с хорошими диэлектрическими свойствами и т. д. Виды оксидирования стали 1. Термическое (обработка при высоких температурах 400 -5000 С); Старейшим процессом термического оксидирования является нагревание стали и чугунных изделий до 5000 С с последующим окунанием в льняное масло. Операцию повторяют многократно. В настоящее время более распространено термооксидирование горячим воздухом или паром 2. Химическое (в щелочных или кислых растворах); 3. Электрохимическое (анодная обработка в р-ре K 2 Cr 2 O 7 и щелочах) 2
Оксидирование стали применяется для защиты стали от коррозии и придания декоративного вида. В зависимости от режима могут быть матовые, чёрные, блестящие, с синеватым отливом, более твёрдые, с хорошими диэлектрическими свойствами и т. д. Виды оксидирования стали 1. Термическое (обработка при высоких температурах 400 -5000 С); Старейшим процессом термического оксидирования является нагревание стали и чугунных изделий до 5000 С с последующим окунанием в льняное масло. Операцию повторяют многократно. В настоящее время более распространено термооксидирование горячим воздухом или паром 2. Химическое (в щелочных или кислых растворах); 3. Электрохимическое (анодная обработка в р-ре K 2 Cr 2 O 7 и щелочах) 2
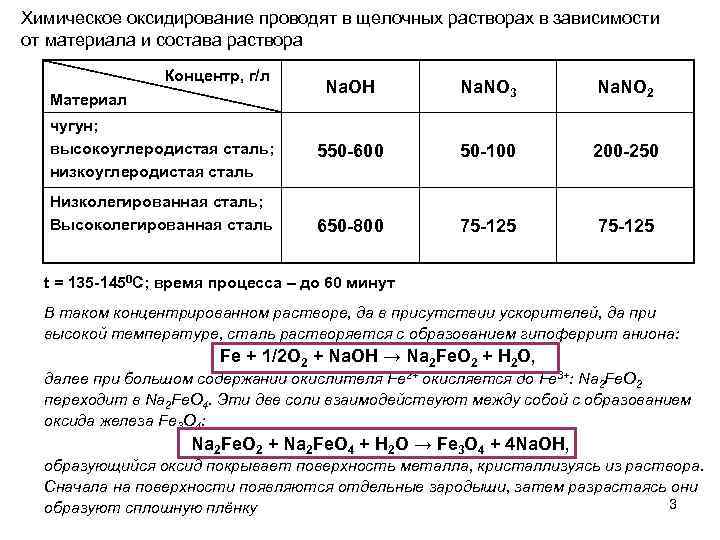 Химическое оксидирование проводят в щелочных растворах в зависимости от материала и состава раствора Концентр, г/л Материал чугун; высокоуглеродистая сталь; низкоуглеродистая сталь Низколегированная сталь; Высоколегированная сталь Na. OH Na. NO 3 Na. NO 2 550 -600 50 -100 200 -250 650 -800 75 -125 t = 135 -1450 С; время процесса – до 60 минут В таком концентрированном растворе, да в присутствии ускорителей, да при высокой температуре, сталь растворяется с образованием гипоферрит аниона: Fe + 1/2 O 2 + Na. OH → Na 2 Fe. O 2 + H 2 O, далее при большом содержании окислителя Fe 2+ окисляется до Fe 3+: Na 2 Fe. O 2 переходит в Na 2 Fe. O 4. Эти две соли взаимодействуют между собой с образованием оксида железа Fe 3 O 4: Na 2 Fe. O 2 + Na 2 Fe. O 4 + H 2 O → Fe 3 O 4 + 4 Na. OH, образующийся оксид покрывает поверхность металла, кристаллизуясь из раствора. Сначала на поверхности появляются отдельные зародыши, затем разрастаясь они 3 образуют сплошную плёнку
Химическое оксидирование проводят в щелочных растворах в зависимости от материала и состава раствора Концентр, г/л Материал чугун; высокоуглеродистая сталь; низкоуглеродистая сталь Низколегированная сталь; Высоколегированная сталь Na. OH Na. NO 3 Na. NO 2 550 -600 50 -100 200 -250 650 -800 75 -125 t = 135 -1450 С; время процесса – до 60 минут В таком концентрированном растворе, да в присутствии ускорителей, да при высокой температуре, сталь растворяется с образованием гипоферрит аниона: Fe + 1/2 O 2 + Na. OH → Na 2 Fe. O 2 + H 2 O, далее при большом содержании окислителя Fe 2+ окисляется до Fe 3+: Na 2 Fe. O 2 переходит в Na 2 Fe. O 4. Эти две соли взаимодействуют между собой с образованием оксида железа Fe 3 O 4: Na 2 Fe. O 2 + Na 2 Fe. O 4 + H 2 O → Fe 3 O 4 + 4 Na. OH, образующийся оксид покрывает поверхность металла, кристаллизуясь из раствора. Сначала на поверхности появляются отдельные зародыши, затем разрастаясь они 3 образуют сплошную плёнку
 Структура плёнки и её толщина зависят от соотношения скорости образования новых центров кристаллизации (кристаллических зародышей) и скорости роста отдельных кристаллов. При повышенной концентрации окислителей в растворе, скорость образования центров кристаллизации значительно выше скорости роста отдельных кристаллов, и на поверхности быстро образуется тонкий плотный слой оксида, в результате чего прекращается взаимодействие металла со щелочью. При увеличении концентрации Na. OH формируются более толстые, но рыхлые плёнки. Перемешивание раствора и понижение температуры приводит к уменьшению числа центров кристаллизации, в результате образуются более толстые, рыхлые покрытия Иногда при оксидировании на поверхности образуется бурый налёт гидроксида Fe(III). Для предотвращения этого оксидирование проводят в 2 х растворах: в 1 -м концентрация щелочи ниже обычной – поверхность покрывается плотной тонкой плёнкой, замедля-ющей растворение металла, а во втором – концентрированном растворе продолжается рост оксидной плёнки без образования налёта гидроксидов Fe(III). 4
Структура плёнки и её толщина зависят от соотношения скорости образования новых центров кристаллизации (кристаллических зародышей) и скорости роста отдельных кристаллов. При повышенной концентрации окислителей в растворе, скорость образования центров кристаллизации значительно выше скорости роста отдельных кристаллов, и на поверхности быстро образуется тонкий плотный слой оксида, в результате чего прекращается взаимодействие металла со щелочью. При увеличении концентрации Na. OH формируются более толстые, но рыхлые плёнки. Перемешивание раствора и понижение температуры приводит к уменьшению числа центров кристаллизации, в результате образуются более толстые, рыхлые покрытия Иногда при оксидировании на поверхности образуется бурый налёт гидроксида Fe(III). Для предотвращения этого оксидирование проводят в 2 х растворах: в 1 -м концентрация щелочи ниже обычной – поверхность покрывается плотной тонкой плёнкой, замедля-ющей растворение металла, а во втором – концентрированном растворе продолжается рост оксидной плёнки без образования налёта гидроксидов Fe(III). 4
 Цвет плёнки Оксидные покрытия черного цвета (глубокого) образуются только после накопления в растворе некоторого количества солей железа, поэтому после приготовления в раствор опускают стальные полосы и прорабатывают в течение нескольких часов. Нитраты и нитриты по разному окрашивают оксидную плёнку: В присутствии NO 3 - - матовые плёнки черного цвета, NO 2 - - блестящие с синеватым оттенком. В первом случае плёнки более коррозионностойкие, чем во втором. Кроме того цвет зависит от состава стали: Углеродистые и низколегированные – плёнки черные с синеватым оттенком; Высоколегированные стали – от тёмно-серого до тёмно-коричневого с вишнёвым; Чугун сталь, легированная кремнием – от золотистого до тёмно-коричневого 5
Цвет плёнки Оксидные покрытия черного цвета (глубокого) образуются только после накопления в растворе некоторого количества солей железа, поэтому после приготовления в раствор опускают стальные полосы и прорабатывают в течение нескольких часов. Нитраты и нитриты по разному окрашивают оксидную плёнку: В присутствии NO 3 - - матовые плёнки черного цвета, NO 2 - - блестящие с синеватым оттенком. В первом случае плёнки более коррозионностойкие, чем во втором. Кроме того цвет зависит от состава стали: Углеродистые и низколегированные – плёнки черные с синеватым оттенком; Высоколегированные стали – от тёмно-серого до тёмно-коричневого с вишнёвым; Чугун сталь, легированная кремнием – от золотистого до тёмно-коричневого 5
 Электрохимическое оксидирование Формирующиеся оксидные плёнки более коррозионностойкие, чем химические, более толстые и менее пористые. Из-за более сложной реализации и трудоёмкости не находят широкого применения. Формируют в 2 стадии: 1. Анодная обработка K 2 Cr 2 O 7 - 5% раствор, t 45 -550 С, ia 3 -5 А/дм 2; в течение 10 -15 минут затем после промывки 2. Na. OH (350 -650 г/л); t 60 -800 С; ia 3 -5 А/дм 2; в течение 10 -30 минут. Формирующиеся пленки имеют черный цвет. 6
Электрохимическое оксидирование Формирующиеся оксидные плёнки более коррозионностойкие, чем химические, более толстые и менее пористые. Из-за более сложной реализации и трудоёмкости не находят широкого применения. Формируют в 2 стадии: 1. Анодная обработка K 2 Cr 2 O 7 - 5% раствор, t 45 -550 С, ia 3 -5 А/дм 2; в течение 10 -15 минут затем после промывки 2. Na. OH (350 -650 г/л); t 60 -800 С; ia 3 -5 А/дм 2; в течение 10 -30 минут. Формирующиеся пленки имеют черный цвет. 6
 Последующая обработка После тщательной промывки от щелочи оксидированные детали - погружают в нагретый до 900 С раствор мыла в течение 2 минут, затем после сушки - погружают в минеральное масло (машинное, веретенное, авиационное) при температуре 100 -1100 С или протирают промасленными салфетками. Коррозионная стойкость оксидных плёнок не высока, они способны защищать стальные изделия лишь в легких условиях эксплуатации. 7
Последующая обработка После тщательной промывки от щелочи оксидированные детали - погружают в нагретый до 900 С раствор мыла в течение 2 минут, затем после сушки - погружают в минеральное масло (машинное, веретенное, авиационное) при температуре 100 -1100 С или протирают промасленными салфетками. Коррозионная стойкость оксидных плёнок не высока, они способны защищать стальные изделия лишь в легких условиях эксплуатации. 7
 Оксидирование алюминия и его сплавов Анодное оксидирование (анодирование) алюминия и его cплавов; цветное: золотисто-желтое, и оливково-бронзовое (шампань); естественного оттенка: от бесцветного до светло-серого 8
Оксидирование алюминия и его сплавов Анодное оксидирование (анодирование) алюминия и его cплавов; цветное: золотисто-желтое, и оливково-бронзовое (шампань); естественного оттенка: от бесцветного до светло-серого 8
 Механизм анодного оксидирования алюминия В большинстве кислых и нейтральных электролитах поверхность Al сразу покрывается тонким барьерным плотным слоем оксидов. Предполагается, что оксидный слой растет в результате взаимодействия ионов Al 3+ и O 22 - при их встречной миграции в барьерном слое. Ионы Al 3+ образуются по реакции Al → Al 3+ + 3 e и мигрируют вследствие большой напряженности электрического поля в ионной решетке оксида к внешней поверхности барьерного слоя, а ионы кислорода, O 22 - образующиеся на поверхности барьерного слоя по реакции: 2 H 2 O → 4 H+ + 4 e + O 2 2 H 2 O → 4 H+ + 2 e + O 22 - мигрируют в направлении металла навстречу ионам Al 3+. В общем виде процесс анодного окисления может быть представлен: 2 Al + 3 H 2 O → Al 2 O 3 +6 H+ +6 e 9 Схема образования барьерного слоя
Механизм анодного оксидирования алюминия В большинстве кислых и нейтральных электролитах поверхность Al сразу покрывается тонким барьерным плотным слоем оксидов. Предполагается, что оксидный слой растет в результате взаимодействия ионов Al 3+ и O 22 - при их встречной миграции в барьерном слое. Ионы Al 3+ образуются по реакции Al → Al 3+ + 3 e и мигрируют вследствие большой напряженности электрического поля в ионной решетке оксида к внешней поверхности барьерного слоя, а ионы кислорода, O 22 - образующиеся на поверхности барьерного слоя по реакции: 2 H 2 O → 4 H+ + 4 e + O 2 2 H 2 O → 4 H+ + 2 e + O 22 - мигрируют в направлении металла навстречу ионам Al 3+. В общем виде процесс анодного окисления может быть представлен: 2 Al + 3 H 2 O → Al 2 O 3 +6 H+ +6 e 9 Схема образования барьерного слоя
 Дальнейший ход событий зависит от способности электролита растворять оксидную плёнку. Существует 2 типа электролитов оксидирования: • Электролиты I типа – оксид алюминия в них практически нерастворим в электролитах • Электролиты II типа – оксид алюминия в них хорошо растворим В электролитах I типа формирование плотного практически беспористого слоя оксида из γ – модификации Al 2 O 3, прекратится, когда толщина достигнет предела, отвечающего данному напряжению. Если напряжение не увеличивать, рост толщины плотного барьерного слоя прекратится, когда толщина будет равна предельной толщине для данного напряжения. Толщина этих плёнок может достигать 1 -2 мкм, они вследствие очень малой пористости отличаются высоким электрическим сопротивлением 1014 -15 Ом∙м и используются в производстве электролитических конденсаторов. 10
Дальнейший ход событий зависит от способности электролита растворять оксидную плёнку. Существует 2 типа электролитов оксидирования: • Электролиты I типа – оксид алюминия в них практически нерастворим в электролитах • Электролиты II типа – оксид алюминия в них хорошо растворим В электролитах I типа формирование плотного практически беспористого слоя оксида из γ – модификации Al 2 O 3, прекратится, когда толщина достигнет предела, отвечающего данному напряжению. Если напряжение не увеличивать, рост толщины плотного барьерного слоя прекратится, когда толщина будет равна предельной толщине для данного напряжения. Толщина этих плёнок может достигать 1 -2 мкм, они вследствие очень малой пористости отличаются высоким электрическим сопротивлением 1014 -15 Ом∙м и используются в производстве электролитических конденсаторов. 10
 Если оксидирование проводится в электролитах II типа, способных растворять оксид алюминия, то рост оксидной пленки зависит от двух параллельных процессов, протекающих на аноде: 1. Химическое растворение плёнки; 2. Образование плёнки в основе пор, за счет окисления Al и взаимодействия с проникающим кислородом. Рост плёнки зависит от соотношения скоростей этих процессов. Рост её возможен тогда, когда ν 2>ν 1. В начале процесса ν 2>ν 1, иначе плёнка не могла бы образоваться. Затем ν 1 увеличивается, т. к. со стороны электролита плёнка становится всё более пористой и рыхлой, увеличивается площадь контакта с электролитом. В какой-то момент времени ν 2=ν 1, т. е. рост плёнки прекращается, хотя окисление Al продолжается с той же скоростью. Таким образом, толщина оксидных плёнок для каждого условия проведения имеет свой предел, до которого возможен рост. Оксидная плёнка растет за счет образования пористого слоя, продвигаясь в глубь металла. 11
Если оксидирование проводится в электролитах II типа, способных растворять оксид алюминия, то рост оксидной пленки зависит от двух параллельных процессов, протекающих на аноде: 1. Химическое растворение плёнки; 2. Образование плёнки в основе пор, за счет окисления Al и взаимодействия с проникающим кислородом. Рост плёнки зависит от соотношения скоростей этих процессов. Рост её возможен тогда, когда ν 2>ν 1. В начале процесса ν 2>ν 1, иначе плёнка не могла бы образоваться. Затем ν 1 увеличивается, т. к. со стороны электролита плёнка становится всё более пористой и рыхлой, увеличивается площадь контакта с электролитом. В какой-то момент времени ν 2=ν 1, т. е. рост плёнки прекращается, хотя окисление Al продолжается с той же скоростью. Таким образом, толщина оксидных плёнок для каждого условия проведения имеет свой предел, до которого возможен рост. Оксидная плёнка растет за счет образования пористого слоя, продвигаясь в глубь металла. 11
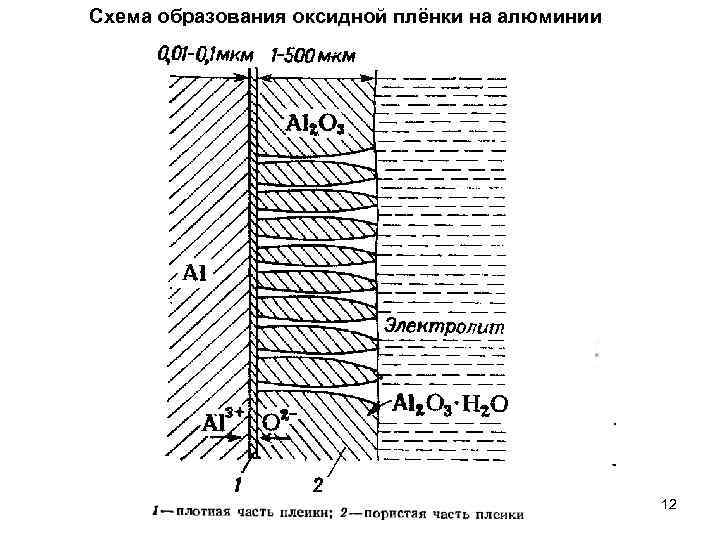 Схема образования оксидной плёнки на алюминии 12
Схема образования оксидной плёнки на алюминии 12
 Чем выше растворяющая способность электролита, тем тоньше получаемая плёнка. v 1 зависит от природы и концентрации электролита, температуры. С увеличением концентрации и температуры увеличивается скорость растворения. v 2 зависит от плотности тока; с ростом плотности тока, тем быстрее идёт образование плёнки. Например, повышение температуры сернокислого электролита от 20 до 500 С, толщина оксидной плёнки уменьшается более чем в 10 раз. - - Поэтому при наращивании толстых плёнок процесс ведут, как правило, при низких температурах. Однако при росте плотности тока выше допустимого предела в данных условиях скорость формирования плёнки может уменьшиться из-за роста температуры в зоне роста плёнки. Толщина существенно зависит от химического состава оксидируемого металла. Чистый Al легче оксидируется, чем сплавы. Чем больше содержание легирующих добавок, тем труднее образуются толстые плёнки. Сплавы, которые содержат большое количество Si, не поддается декоративному оксидированию, т. к. Si не окисляется, не растворяется, а остается в плёнке в виде черно-серого порошка. Mg, Fe, Mn, Cu – находятся в виде интерметаллидов, поэтому растворяется быстрее Al, поэтому образуются шероховатые покрытия. 13
Чем выше растворяющая способность электролита, тем тоньше получаемая плёнка. v 1 зависит от природы и концентрации электролита, температуры. С увеличением концентрации и температуры увеличивается скорость растворения. v 2 зависит от плотности тока; с ростом плотности тока, тем быстрее идёт образование плёнки. Например, повышение температуры сернокислого электролита от 20 до 500 С, толщина оксидной плёнки уменьшается более чем в 10 раз. - - Поэтому при наращивании толстых плёнок процесс ведут, как правило, при низких температурах. Однако при росте плотности тока выше допустимого предела в данных условиях скорость формирования плёнки может уменьшиться из-за роста температуры в зоне роста плёнки. Толщина существенно зависит от химического состава оксидируемого металла. Чистый Al легче оксидируется, чем сплавы. Чем больше содержание легирующих добавок, тем труднее образуются толстые плёнки. Сплавы, которые содержат большое количество Si, не поддается декоративному оксидированию, т. к. Si не окисляется, не растворяется, а остается в плёнке в виде черно-серого порошка. Mg, Fe, Mn, Cu – находятся в виде интерметаллидов, поэтому растворяется быстрее Al, поэтому образуются шероховатые покрытия. 13
 Во всех случаях плёнки состоят из двух слоёв: беспористого барьерного толщиной 0, 01÷ 0, 1 мкм и пористого толщиной от нескольких микрометров до нескольких сотен микрометров. Рост плёнки происходит на внешней, пористой ее части, при этом барьерный слой постепенно обновляется и как бы перемещается в глубь металла. Барьерный слой представляет собой γ-модификацию оксида алюминия Al 2 O 3. Внешний пористый слой состоит из более или менее гидратированного оксида алюминия. Степень гидратации зависит от электролита, в котором производили оксидирование. Для плёнок, полученных в серой и щавелевой кислотах, он соответствует формуле Al 2 O 3∙H 2 O. Плёнки, полученные в хромовой кислоте, практически безводны. Анодные плёнки из хромовокислых электролитов содержат помимо Al 2 O 3 до 0, 5% Cr. 14
Во всех случаях плёнки состоят из двух слоёв: беспористого барьерного толщиной 0, 01÷ 0, 1 мкм и пористого толщиной от нескольких микрометров до нескольких сотен микрометров. Рост плёнки происходит на внешней, пористой ее части, при этом барьерный слой постепенно обновляется и как бы перемещается в глубь металла. Барьерный слой представляет собой γ-модификацию оксида алюминия Al 2 O 3. Внешний пористый слой состоит из более или менее гидратированного оксида алюминия. Степень гидратации зависит от электролита, в котором производили оксидирование. Для плёнок, полученных в серой и щавелевой кислотах, он соответствует формуле Al 2 O 3∙H 2 O. Плёнки, полученные в хромовой кислоте, практически безводны. Анодные плёнки из хромовокислых электролитов содержат помимо Al 2 O 3 до 0, 5% Cr. 14
 Краткая характеристика электролитов, применяемых для оксидирования алюминия и сплавов Электролиты I типа. Осаждаются тонкослойные анодно-оксидные покрытия U = 500 -600 В; t 900 С; 20÷ 30 мин, δ = 0, 1 -0, 2 мкм; р. Н 5 ÷ 6 1. Лимонная кислота 0, 5 -0, 8 г/л U = 250 -300 В; t 90 -950 С 2. Борная кислота 90 -150 г/л Натрия тетраборат 1, 5 -2, 5 г/л или Na 2 CO 3 2, 5 г/л U = 25 -80 В; t 20 -300 С; i = 1, 3 -2, 0 А/дм 2 В электролитах I типа получают плотные тонкие плёнки с высокими диэлектрическим свойствами. Это обусловливается малой растворимостью оксида алюминия в этих кислотах 15
Краткая характеристика электролитов, применяемых для оксидирования алюминия и сплавов Электролиты I типа. Осаждаются тонкослойные анодно-оксидные покрытия U = 500 -600 В; t 900 С; 20÷ 30 мин, δ = 0, 1 -0, 2 мкм; р. Н 5 ÷ 6 1. Лимонная кислота 0, 5 -0, 8 г/л U = 250 -300 В; t 90 -950 С 2. Борная кислота 90 -150 г/л Натрия тетраборат 1, 5 -2, 5 г/л или Na 2 CO 3 2, 5 г/л U = 25 -80 В; t 20 -300 С; i = 1, 3 -2, 0 А/дм 2 В электролитах I типа получают плотные тонкие плёнки с высокими диэлектрическим свойствами. Это обусловливается малой растворимостью оксида алюминия в этих кислотах 15
 Защитные и защитно-декоративные анодно-оксидные покрытия 10 -15 мкм: t 18 -250 С; iа 1 -2 А/дм 2; U 12 -28 V, 20 -40 мин 1. Сернокислый электролит: 180 -250 г/л H 2 SO 4 Твердое анодирование 50 -100 мкм: t 00 С; iа 2 -10 А/дм 2; U 80 -120 V, 90 мин >150 -500 мкм: двустороннее охлаждение -290 С - +50 С; 0, 5 -0, 7 А/дм 2, Vн = 25 В↑ 80 В; ia = 0, 5 -0, 7 А/дм 2 Охлаждение электролита осуществляют с помощью холодильной установки. При анодировании необходимо поддерживать постоянную плотность тока с помощью реостатов, включенных в цепь питания ванны. Оптимальное качество покрытий при глубоком анодировании обеспечивается на деталях, изготовленных из Al и его сплавов, содержащих Mg и Mn. Покрытия прозрачные, полупрозрачные, снежно- белого цвета; v Имеют наибольшую твердость, равную твердости корунда; v Жаростойкость (до 20000 С); v Не отслаиваются от металла; v Хорошо окрашиваются органическими красителями и эл/лит способом в р-х солей металлов Преимущества: + Можно анодировать почти все сплавы; + требует на 30÷ 35% меньше затрат э/энергии + Меньше длительность обработки; + Серная к-та наиболее дешевая из электролитов и доступная Недостатки: Необходимость охлаждения электролита при работе; Необходимость последующей обработки в растворах бихромата для увеличения коррозионной стойкости; Необходимость применения специальной кислотоупорной футеровки; Невозможность длительного пребывания деталей в электролите при случайных перерывах тока; Не рекомендуется обрабатывать детали сложные и клепанные (имеющие узкие щели, зазоры, в которых трудно отмыть кислоту). 16
Защитные и защитно-декоративные анодно-оксидные покрытия 10 -15 мкм: t 18 -250 С; iа 1 -2 А/дм 2; U 12 -28 V, 20 -40 мин 1. Сернокислый электролит: 180 -250 г/л H 2 SO 4 Твердое анодирование 50 -100 мкм: t 00 С; iа 2 -10 А/дм 2; U 80 -120 V, 90 мин >150 -500 мкм: двустороннее охлаждение -290 С - +50 С; 0, 5 -0, 7 А/дм 2, Vн = 25 В↑ 80 В; ia = 0, 5 -0, 7 А/дм 2 Охлаждение электролита осуществляют с помощью холодильной установки. При анодировании необходимо поддерживать постоянную плотность тока с помощью реостатов, включенных в цепь питания ванны. Оптимальное качество покрытий при глубоком анодировании обеспечивается на деталях, изготовленных из Al и его сплавов, содержащих Mg и Mn. Покрытия прозрачные, полупрозрачные, снежно- белого цвета; v Имеют наибольшую твердость, равную твердости корунда; v Жаростойкость (до 20000 С); v Не отслаиваются от металла; v Хорошо окрашиваются органическими красителями и эл/лит способом в р-х солей металлов Преимущества: + Можно анодировать почти все сплавы; + требует на 30÷ 35% меньше затрат э/энергии + Меньше длительность обработки; + Серная к-та наиболее дешевая из электролитов и доступная Недостатки: Необходимость охлаждения электролита при работе; Необходимость последующей обработки в растворах бихромата для увеличения коррозионной стойкости; Необходимость применения специальной кислотоупорной футеровки; Невозможность длительного пребывания деталей в электролите при случайных перерывах тока; Не рекомендуется обрабатывать детали сложные и клепанные (имеющие узкие щели, зазоры, в которых трудно отмыть кислоту). 16
 2. Хромовокислый электролит: электролит 30 -55 г/л Cr. O 3 100 -150 г/л Cr. O 3 t 400 С; iа 0, 2 -0, 3 А/дм 2; U 12 -28 V, 1 час; Uн = 40 В↑ 50 В t 34 -380 С; iа 0, 3 -0, 5 А/дм 2; U 40 V, 1 час; Uн = 40 В↑ 50 В Катоды должны быть в 5 раз больше (чтобы предотвратить реакцию Cr 6+ →Cr 3+ +3 e). Бесцветные стекловидные покрытия; Имеют малую пористость; Более высокие защитные св-ва, чем в сульфатном электролите; Более высокая эластичность; Трудно окрашиваются органическими красителями, э/лит в р-х солей Ni, Cu, Sn, Co, Cd Преимущества: + + + Повышенная коррозионная стойкость плёнок, не требуется дополнительная обработка в хромпике; Высокая эластичность и пластичность плёнок; В нем выявляются дефекты поверхности металла (трещины, участки с различной микротвердостью, дефекты подготовки Пв) – используются в дефектоскопии. Недостатки: - Высокая стоимость электролита; Сложность контроля; Необходимость подогрева электролита; Длительность выдержки деталей в ванне и использование постоянного тока довольно высокого напряжения. 17
2. Хромовокислый электролит: электролит 30 -55 г/л Cr. O 3 100 -150 г/л Cr. O 3 t 400 С; iа 0, 2 -0, 3 А/дм 2; U 12 -28 V, 1 час; Uн = 40 В↑ 50 В t 34 -380 С; iа 0, 3 -0, 5 А/дм 2; U 40 V, 1 час; Uн = 40 В↑ 50 В Катоды должны быть в 5 раз больше (чтобы предотвратить реакцию Cr 6+ →Cr 3+ +3 e). Бесцветные стекловидные покрытия; Имеют малую пористость; Более высокие защитные св-ва, чем в сульфатном электролите; Более высокая эластичность; Трудно окрашиваются органическими красителями, э/лит в р-х солей Ni, Cu, Sn, Co, Cd Преимущества: + + + Повышенная коррозионная стойкость плёнок, не требуется дополнительная обработка в хромпике; Высокая эластичность и пластичность плёнок; В нем выявляются дефекты поверхности металла (трещины, участки с различной микротвердостью, дефекты подготовки Пв) – используются в дефектоскопии. Недостатки: - Высокая стоимость электролита; Сложность контроля; Необходимость подогрева электролита; Длительность выдержки деталей в ванне и использование постоянного тока довольно высокого напряжения. 17
 3. Щавелевокислый электролит: 40 -60 г/л H 2 C 2 O 4 t 18 -250 С; iа 2, 5 -3, 5 А/дм 2; 90 -120 мин; Uн = ↑ 120 В Толстые, эластичные, малопористые; От светлых до темно-бронзовых; Более высокие защитные свойства и эластичность, чем в сульфатном электролите Преимущества: + + Просты по составу; Не требуют охлаждения; Можно получать покрытия на большем числе сплавов, в том числе содержащих Cu (до 5%) и Si (до 4%); Можно получать окрашенные в разные цвета Пк (в зависимости от режима) Недостатки: - Высокие напряжения и продолжительность (увеличение затрат на э/энергию); Дороже, чем сульфатный Вредные примеси: Cl- (до 0, 04 г/л) и Al (до 30 г/л) 18
3. Щавелевокислый электролит: 40 -60 г/л H 2 C 2 O 4 t 18 -250 С; iа 2, 5 -3, 5 А/дм 2; 90 -120 мин; Uн = ↑ 120 В Толстые, эластичные, малопористые; От светлых до темно-бронзовых; Более высокие защитные свойства и эластичность, чем в сульфатном электролите Преимущества: + + Просты по составу; Не требуют охлаждения; Можно получать покрытия на большем числе сплавов, в том числе содержащих Cu (до 5%) и Si (до 4%); Можно получать окрашенные в разные цвета Пк (в зависимости от режима) Недостатки: - Высокие напряжения и продолжительность (увеличение затрат на э/энергию); Дороже, чем сульфатный Вредные примеси: Cl- (до 0, 04 г/л) и Al (до 30 г/л) 18
 Электролиты на основе сульфосалициловой кислоты Преимущества: + Покрытия получаются на большинстве алюминиевых сплавов; + Покрытия отличаются хорошими защитными свойствами; + Хорошая износостойкость; + Твердость Покрытия окрашены в светостойкие серо-черные и коричнево-бронзовые цвета Недостатки: - Самый дорогой из применяемых электролитов Оксид алюминия плохо растворим в сульфосалициловой кислоте, поэтому в этих электролитах формируются плотные тонкие плёнки. Эти плёнки эластичны и обладают хорошими электроизоляционными свойствами. Для получения более толстого слоя оксида к электролиту добавляют небольшое количество серной или щавелевой кислоты, в которой растворимость алюминия увеличивается. C 7 H 6 O 6∙ 2 H 2 O H 2 C 2 O 4 80 -100 г/л 30 -40 г/л t 5 -150 С; iа 1, 5 А/дм 2; 100 мин; Uн = 70↑ 85 В; δ = 20 мкм C 7 H 6 O 6∙ 2 H 2 O H 2 C 2 O 4 H 2 SO 4 90 -100 г/л 27 -33 г/л 2 -4 г/л t 10 -280 С; iа 1, 5÷ 3 А/дм 2; 20 -120 мин; Uн = 100 В 19
Электролиты на основе сульфосалициловой кислоты Преимущества: + Покрытия получаются на большинстве алюминиевых сплавов; + Покрытия отличаются хорошими защитными свойствами; + Хорошая износостойкость; + Твердость Покрытия окрашены в светостойкие серо-черные и коричнево-бронзовые цвета Недостатки: - Самый дорогой из применяемых электролитов Оксид алюминия плохо растворим в сульфосалициловой кислоте, поэтому в этих электролитах формируются плотные тонкие плёнки. Эти плёнки эластичны и обладают хорошими электроизоляционными свойствами. Для получения более толстого слоя оксида к электролиту добавляют небольшое количество серной или щавелевой кислоты, в которой растворимость алюминия увеличивается. C 7 H 6 O 6∙ 2 H 2 O H 2 C 2 O 4 80 -100 г/л 30 -40 г/л t 5 -150 С; iа 1, 5 А/дм 2; 100 мин; Uн = 70↑ 85 В; δ = 20 мкм C 7 H 6 O 6∙ 2 H 2 O H 2 C 2 O 4 H 2 SO 4 90 -100 г/л 27 -33 г/л 2 -4 г/л t 10 -280 С; iа 1, 5÷ 3 А/дм 2; 20 -120 мин; Uн = 100 В 19
 Анодные оксидные плёнки – подслой под нанесение гальванических покрытий Вследствие большого диаметра пор оксидные покрытия, получаемые на поверхности алюминия и его сплавов в электролите с ортофосфорной кислотой, применяют для последующего нанесения на них гальванопокрытий. H 3 PO 4 180 -190 г/л t 15 -250 С; iа 10÷ 50 А/дм 2; 10 мин; Катод: свинец; сталь Анодно-оксидная плёнка имеет темно-серый оттенок и не является электроизоляционной. Толщина ее равна 1 мкм. 20
Анодные оксидные плёнки – подслой под нанесение гальванических покрытий Вследствие большого диаметра пор оксидные покрытия, получаемые на поверхности алюминия и его сплавов в электролите с ортофосфорной кислотой, применяют для последующего нанесения на них гальванопокрытий. H 3 PO 4 180 -190 г/л t 15 -250 С; iа 10÷ 50 А/дм 2; 10 мин; Катод: свинец; сталь Анодно-оксидная плёнка имеет темно-серый оттенок и не является электроизоляционной. Толщина ее равна 1 мкм. 20
 Эматалирование – процесс формирования на Al и сплавах непрозрачных пленок, напоминающих по внешнему виду эмаль. Непрозрачность покрытий достигается при использовании в качестве электролита двойных солей щавелевой кислоты, содержащих титан, цирконий или торий, продукты гидролиза которых во время роста покрытия внедряются в поры и создают эматаль – эффект. H 3 BO 3 8 г/л К-та лимонная 1 г/л H 2 C 2 O 4 1, 2 г/л Калий-титан щавелевокислый 40 г/л 40 -500 С iа 2, 5 -3, 0 А/дм 2 120 -130 В 30 -40 мин Катоды из Al марки А 7 21
Эматалирование – процесс формирования на Al и сплавах непрозрачных пленок, напоминающих по внешнему виду эмаль. Непрозрачность покрытий достигается при использовании в качестве электролита двойных солей щавелевой кислоты, содержащих титан, цирконий или торий, продукты гидролиза которых во время роста покрытия внедряются в поры и создают эматаль – эффект. H 3 BO 3 8 г/л К-та лимонная 1 г/л H 2 C 2 O 4 1, 2 г/л Калий-титан щавелевокислый 40 г/л 40 -500 С iа 2, 5 -3, 0 А/дм 2 120 -130 В 30 -40 мин Катоды из Al марки А 7 21
 Последующая обработка оксидных покрытий Окрашивание Микропористая структура, высокая адсорбционная способность оксидных плёнок являются той базой, на которой основываются все способы их окрашивания. Известно три таких способа: осаждение в порах оксидного слоя минерального красящего пигмента; адсорбционное окрашивание органическими красителями; электрохимическое окрашивание путем обработки оксидного покрытия переменным током в разбавленных растворах минеральных солей. 22
Последующая обработка оксидных покрытий Окрашивание Микропористая структура, высокая адсорбционная способность оксидных плёнок являются той базой, на которой основываются все способы их окрашивания. Известно три таких способа: осаждение в порах оксидного слоя минерального красящего пигмента; адсорбционное окрашивание органическими красителями; электрохимическое окрашивание путем обработки оксидного покрытия переменным током в разбавленных растворах минеральных солей. 22
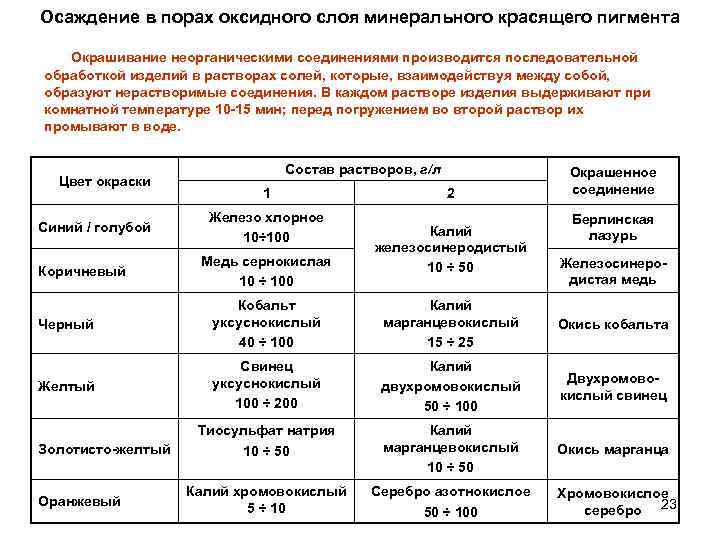 Осаждение в порах оксидного слоя минерального красящего пигмента Окрашивание неорганическими соединениями производится последовательной обработкой изделий в растворах солей, которые, взаимодействуя между собой, образуют нерастворимые соединения. В каждом растворе изделия выдерживают при комнатной температуре 10 -15 мин; перед погружением во второй раствор их промывают в воде. Цвет окраски Синий / голубой Коричневый Состав растворов, г/л 1 Железо хлорное 10÷ 100 Медь сернокислая 10 ÷ 100 2 Калий железосинеродистый 10 ÷ 50 Окрашенное соединение Берлинская лазурь Железосинеродистая медь Черный Кобальт уксуснокислый 40 ÷ 100 Калий марганцевокислый 15 ÷ 25 Окись кобальта Желтый Свинец уксуснокислый 100 ÷ 200 Калий двухромовокислый 50 ÷ 100 Двухромовокислый свинец Тиосульфат натрия 10 ÷ 50 Калий марганцевокислый 10 ÷ 50 Окись марганца Калий хромовокислый 5 ÷ 10 Серебро азотнокислое 50 ÷ 100 Хромовокислое серебро 23 Золотисто-желтый Оранжевый
Осаждение в порах оксидного слоя минерального красящего пигмента Окрашивание неорганическими соединениями производится последовательной обработкой изделий в растворах солей, которые, взаимодействуя между собой, образуют нерастворимые соединения. В каждом растворе изделия выдерживают при комнатной температуре 10 -15 мин; перед погружением во второй раствор их промывают в воде. Цвет окраски Синий / голубой Коричневый Состав растворов, г/л 1 Железо хлорное 10÷ 100 Медь сернокислая 10 ÷ 100 2 Калий железосинеродистый 10 ÷ 50 Окрашенное соединение Берлинская лазурь Железосинеродистая медь Черный Кобальт уксуснокислый 40 ÷ 100 Калий марганцевокислый 15 ÷ 25 Окись кобальта Желтый Свинец уксуснокислый 100 ÷ 200 Калий двухромовокислый 50 ÷ 100 Двухромовокислый свинец Тиосульфат натрия 10 ÷ 50 Калий марганцевокислый 10 ÷ 50 Окись марганца Калий хромовокислый 5 ÷ 10 Серебро азотнокислое 50 ÷ 100 Хромовокислое серебро 23 Золотисто-желтый Оранжевый
 Для окрашивания оксидных пленок под цвет латуни может быть использован раствор следующего состава: Железоаммонийные квасцы (NH 4)2 S 04∙Fe 2(S 04)3∙ 24 Н 20 28 г/л Щавелевая кислота С 2 Н 204 22 г/л Аммиак NH 4 OH (25%) 25 -30 мл (до р. Н 5 -6) Окрашивание оксидированных силуминовых изделий в черный цвет можно производить в растворе, содержащем: Сг 03 30 -50 г/л и КМп 04 20 -25 г/л t 80÷ 90°С; 20 -30 мин Неорганические окрашенные соединения устойчивы к воздействию солнечных лучей, но с их помощью нельзя получить такого разнообразия цветов и оттенков, как применении органических красителей. 24
Для окрашивания оксидных пленок под цвет латуни может быть использован раствор следующего состава: Железоаммонийные квасцы (NH 4)2 S 04∙Fe 2(S 04)3∙ 24 Н 20 28 г/л Щавелевая кислота С 2 Н 204 22 г/л Аммиак NH 4 OH (25%) 25 -30 мл (до р. Н 5 -6) Окрашивание оксидированных силуминовых изделий в черный цвет можно производить в растворе, содержащем: Сг 03 30 -50 г/л и КМп 04 20 -25 г/л t 80÷ 90°С; 20 -30 мин Неорганические окрашенные соединения устойчивы к воздействию солнечных лучей, но с их помощью нельзя получить такого разнообразия цветов и оттенков, как применении органических красителей. 24
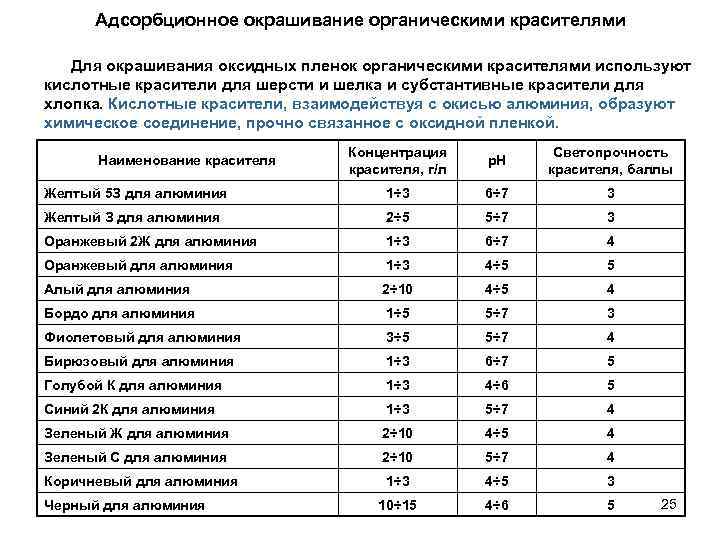 Адсорбционное окрашивание органическими красителями Для окрашивания оксидных пленок органическими красителями используют кислотные красители для шерсти и шелка и субстантивные красители для хлопка. Кислотные красители, взаимодействуя с окисью алюминия, образуют химическое соединение, прочно связанное с оксидной пленкой. Концентрация красителя, г/л р. Н Светопрочность красителя, баллы Желтый 5 З для алюминия 1÷ 3 6÷ 7 3 Желтый З для алюминия 2÷ 5 5÷ 7 3 Оранжевый 2 Ж для алюминия 1÷ 3 6÷ 7 4 Оранжевый для алюминия 1÷ 3 4÷ 5 5 Алый для алюминия 2÷ 10 4÷ 5 4 Бордо для алюминия 1÷ 5 5÷ 7 3 Фиолетовый для алюминия 3÷ 5 5÷ 7 4 Бирюзовый для алюминия 1÷ 3 6÷ 7 5 Голубой К для алюминия 1÷ 3 4÷ 6 5 Синий 2 К для алюминия 1÷ 3 5÷ 7 4 Зеленый Ж для алюминия 2÷ 10 4÷ 5 4 Зеленый С для алюминия 2÷ 10 5÷ 7 4 Коричневый для алюминия 1÷ 3 4÷ 5 3 10÷ 15 4÷ 6 5 Наименование красителя Черный для алюминия 25
Адсорбционное окрашивание органическими красителями Для окрашивания оксидных пленок органическими красителями используют кислотные красители для шерсти и шелка и субстантивные красители для хлопка. Кислотные красители, взаимодействуя с окисью алюминия, образуют химическое соединение, прочно связанное с оксидной пленкой. Концентрация красителя, г/л р. Н Светопрочность красителя, баллы Желтый 5 З для алюминия 1÷ 3 6÷ 7 3 Желтый З для алюминия 2÷ 5 5÷ 7 3 Оранжевый 2 Ж для алюминия 1÷ 3 6÷ 7 4 Оранжевый для алюминия 1÷ 3 4÷ 5 5 Алый для алюминия 2÷ 10 4÷ 5 4 Бордо для алюминия 1÷ 5 5÷ 7 3 Фиолетовый для алюминия 3÷ 5 5÷ 7 4 Бирюзовый для алюминия 1÷ 3 6÷ 7 5 Голубой К для алюминия 1÷ 3 4÷ 6 5 Синий 2 К для алюминия 1÷ 3 5÷ 7 4 Зеленый Ж для алюминия 2÷ 10 4÷ 5 4 Зеленый С для алюминия 2÷ 10 5÷ 7 4 Коричневый для алюминия 1÷ 3 4÷ 5 3 10÷ 15 4÷ 6 5 Наименование красителя Черный для алюминия 25
 Уплотнение оксидных покрытий Для повышения защитной способности, светостойкости, повышения диэлектрических свойств все оксидные покрытия на алюминиевых сплавах (окрашенные и неокрашенные) после формирования подвергают т. н. уплотнению обработкой горячим водяным паром или погружением в горячую воду. При этом оксид алюминия гидролизуется, превращаясь в гидроксид алюминия, имеющий больший объем, чем оксид, вследствие чего запечатываются поры покрытия, и его защитная способность повышается. Для уплотнения применяют дистиллированную, деионизированную или конденсатную воду при р. Н 5, 6 -6, 2. Содержание в ней примесей Fe 2+, Ca 2+, Mg 2+, Cl-, SO 42 - не должно превышать 1 мг/л каждого. Оптимальный температурный режим 96÷ 99 °С. Продолжительность обработки 30÷ 40 мин при толщине покрытия 8÷ 15 мкм и 50÷ 60 мин при 20÷ 25 мкм. В промышленности также широко используют уплотнение оксидных пленок в растворах хроматов. В этом случае образуются соединения (Al. O)2 Cr. O 4. При этом покрытия приобретают лимонно-желтую окраску, что делает такую обработку неприемлемой для цветных покрытий. Уплотняющий раствор содержит 40÷ 50 г/л дихромата калия или натрия, р. Н 4, 5÷ 5, 5. Обработку ведут при 90÷ 95 °С в течение 20÷ 30 мин. Еще варианты уплотнения: В качестве основы для солевых уплотнительных растворов предложены ацетаты никеля при концентрации 8÷ 10 г/л при 75÷ 80 °С, р. Н 5, 6÷ 5, 8. Применение солей никеля в большей концентрации при 95÷ 100°С м. б. одним из эффективных способов повышения защитной способности оксидных покрытий. Уплотняющий раствор содержит 350÷ 400 г/л Ni. S 04∙ 7 H 20, р. Н 4, 0÷ 4, 2, продолжительность обработки 80÷ 90 мин. 26
Уплотнение оксидных покрытий Для повышения защитной способности, светостойкости, повышения диэлектрических свойств все оксидные покрытия на алюминиевых сплавах (окрашенные и неокрашенные) после формирования подвергают т. н. уплотнению обработкой горячим водяным паром или погружением в горячую воду. При этом оксид алюминия гидролизуется, превращаясь в гидроксид алюминия, имеющий больший объем, чем оксид, вследствие чего запечатываются поры покрытия, и его защитная способность повышается. Для уплотнения применяют дистиллированную, деионизированную или конденсатную воду при р. Н 5, 6 -6, 2. Содержание в ней примесей Fe 2+, Ca 2+, Mg 2+, Cl-, SO 42 - не должно превышать 1 мг/л каждого. Оптимальный температурный режим 96÷ 99 °С. Продолжительность обработки 30÷ 40 мин при толщине покрытия 8÷ 15 мкм и 50÷ 60 мин при 20÷ 25 мкм. В промышленности также широко используют уплотнение оксидных пленок в растворах хроматов. В этом случае образуются соединения (Al. O)2 Cr. O 4. При этом покрытия приобретают лимонно-желтую окраску, что делает такую обработку неприемлемой для цветных покрытий. Уплотняющий раствор содержит 40÷ 50 г/л дихромата калия или натрия, р. Н 4, 5÷ 5, 5. Обработку ведут при 90÷ 95 °С в течение 20÷ 30 мин. Еще варианты уплотнения: В качестве основы для солевых уплотнительных растворов предложены ацетаты никеля при концентрации 8÷ 10 г/л при 75÷ 80 °С, р. Н 5, 6÷ 5, 8. Применение солей никеля в большей концентрации при 95÷ 100°С м. б. одним из эффективных способов повышения защитной способности оксидных покрытий. Уплотняющий раствор содержит 350÷ 400 г/л Ni. S 04∙ 7 H 20, р. Н 4, 0÷ 4, 2, продолжительность обработки 80÷ 90 мин. 26


